文档内容
专练 42 滴定曲线的综合应用
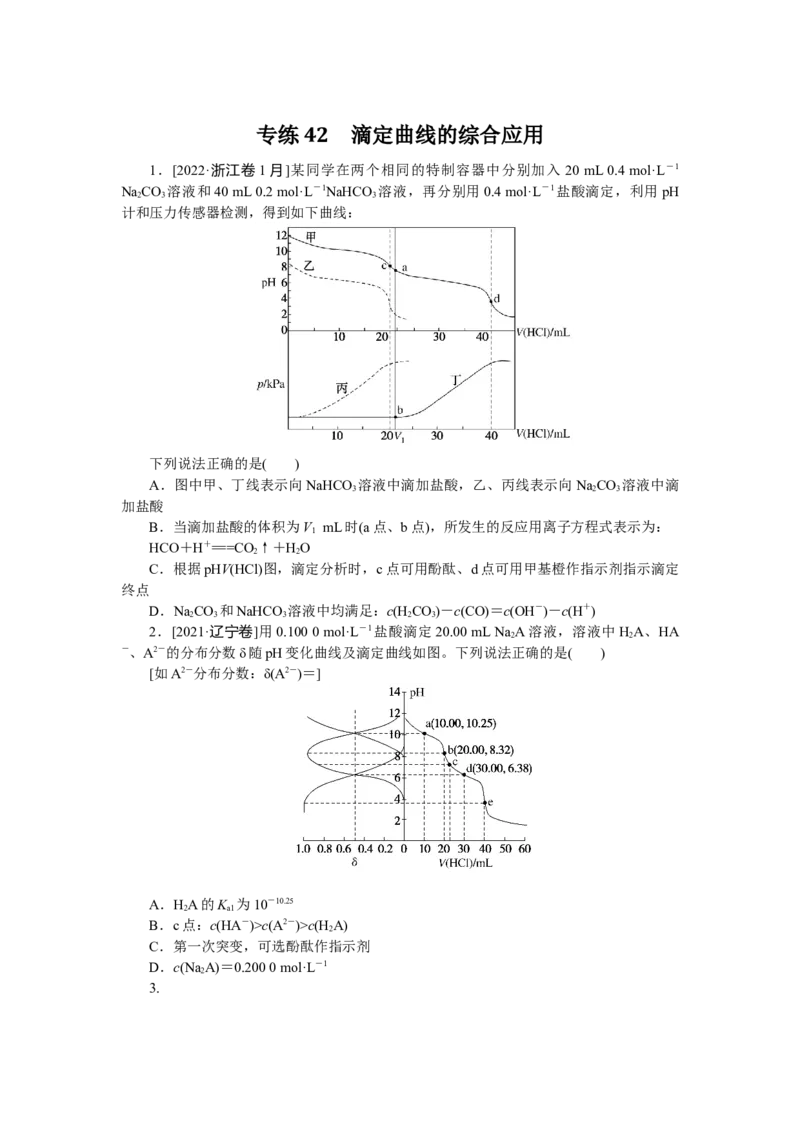
1.[2022·浙江卷1月]某同学在两个相同的特制容器中分别加入 20 mL 0.4 mol·L-1
NaCO 溶液和40 mL 0.2 mol·L-1NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,利用pH
2 3 3
计和压力传感器检测,得到如下曲线:
下列说法正确的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴
3 2 3
加盐酸
B.当滴加盐酸的体积为V mL时(a点、b点),所发生的反应用离子方程式表示为:
1
HCO+H+===CO ↑+HO
2 2
C.根据pHV(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定
终点
D.NaCO 和NaHCO 溶液中均满足:c(H CO)-c(CO)=c(OH-)-c(H+)
2 3 3 2 3
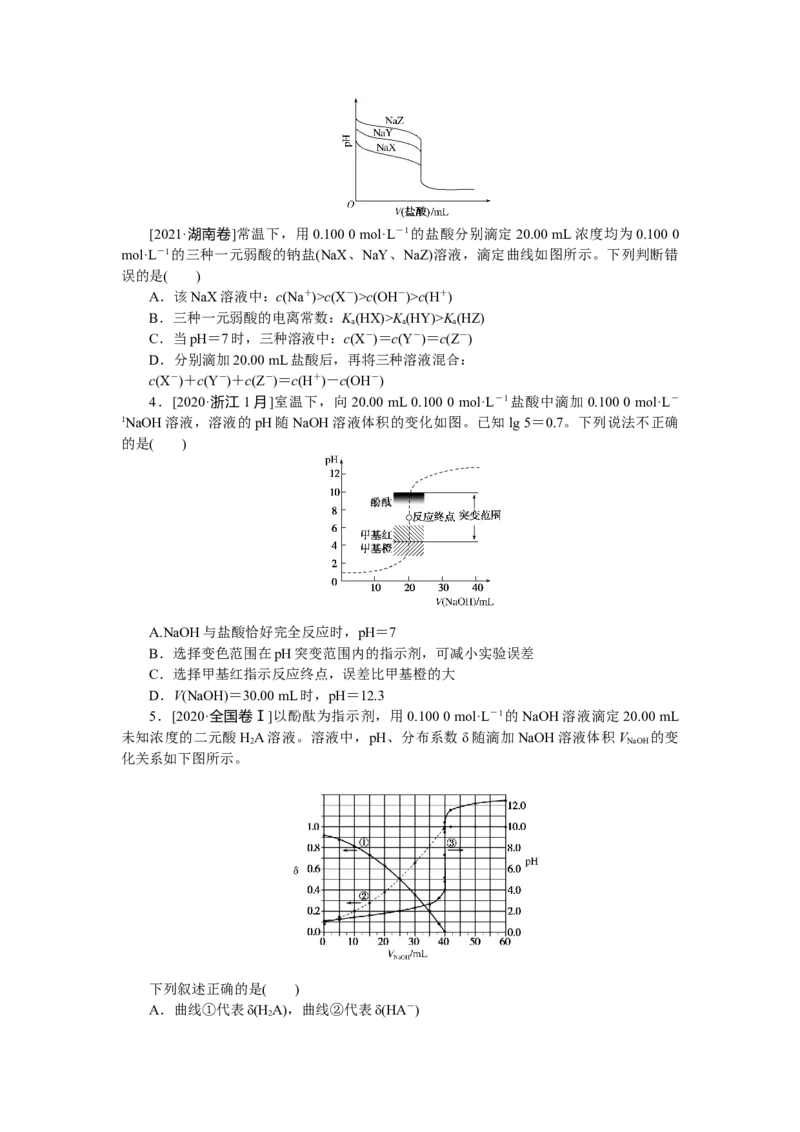
2.[2021·辽宁卷]用0.100 0 mol·L-1盐酸滴定20.00 mL Na A溶液,溶液中HA、HA
2 2
-、A2-的分布分数δ随pH变化曲线及滴定曲线如图。下列说法正确的是( )
[如A2-分布分数:δ(A2-)=]
A.HA的K 为10-10.25
2 a1
B.c点:c(HA-)>c(A2-)>c(H A)
2
C.第一次突变,可选酚酞作指示剂
D.c(Na A)=0.200 0 mol·L-1
2
3.[2021·湖南卷]常温下,用0.100 0 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.100 0
mol·L-1的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错
误的是( )
A.该NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D.分别滴加20.00 mL盐酸后,再将三种溶液混合:
c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
4.[2020·浙江1月]室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100 0 mol·L-
1NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。已知lg 5=0.7。下列说法不正确
的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
5.[2020·全国卷Ⅰ]以酚酞为指示剂,用0.100 0 mol·L-1的NaOH溶液滴定20.00 mL
未知浓度的二元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变
2 NaOH
化关系如下图所示。
下列叙述正确的是( )
A.曲线①代表δ(H A),曲线②代表δ(HA-)
2B.HA溶液的浓度为0.200 0 mol·L-1
2
C.HA-的电离常数K=1.0×10-2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
6.[2022·福建莆田二十四中高三调研]室温下,用相同物质的量浓度的HCl 溶液,分
别滴定物质的量浓度均为 0.1 mol·L-1的三种碱溶液,滴定曲线如图所示。下列判断正确的
是( )
A.滴定前,三种碱溶液中水电离出的c(H+)大小关系: DOH>BOH>AOH
B.pH=7 时,c(A+)=c(B+)=c(D+)
C.滴定至 P 点时,溶液中:
c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+)
D.当中和百分数达100%时,将三种溶液混合后:
c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-)
7.[2022·成都七中阶段性检测]常温下,向某浓度的HC O 溶液中逐滴加入已知浓度
2 2 4
的 NaOH 溶液,若定义 pC 是溶液中溶质物质的量浓度的负对数,则所得溶液中
pC(HC O)、pC(HC O)、pC(C O)与溶液的 pH 关系如图所示。则下列说法正确的是( )
2 2 4 2 2
A.pH=4时,c(HC O)<c(C O)
2 2
B.pH从3增大到5.3的过程中,水的电离程度增大
C.常温下,K =10-0.7
a1
D.常温下, 随pH的升高先增大后减小
8.[角度创新]常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10
mol·L-1的CHCOOH溶液和HCN溶液,所得滴定曲线如图
3
[K(CHCOOH)>K(HCN)]。下列说法正确的是( )
a 3 aA.点①和点②所示溶液中:
c(CHCOO-)c(NH)
B.N点所示溶液中可能存在
c(NH)+c(NH ·H O)=c(Cl-)
3 2
C.Q点盐酸与氨水恰好中和
D.M点到Q点所示溶液中水的电离程度先变大后减小