文档内容
专练 44 化学反应原理综合题
1.[2022·湖南卷]2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。
回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1mol HO(g),起始压强
2
为0.2 MPa时,发生下列反应生成水煤气:
Ⅰ.C(s)+H
2
O(g)⇌CO(g)+H
2
(g)ΔH
1
=+131.4 kJ·mol-1
Ⅱ.CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)ΔH
2
=-41.1 kJ·mol-1
①下列说法正确的是________;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时H 的体积分数可能大于
2
D.将炭块粉碎,可加快反应速率
②反应平衡时,HO(g)的转化率为50%,CO的物质的量为0.1 mol。此时,整个体系
2
________(填“吸收”或“放出”)热量________kJ,反应Ⅰ的平衡常数K =________(以分
p
压表示,分压=总压×物质的量分数)。
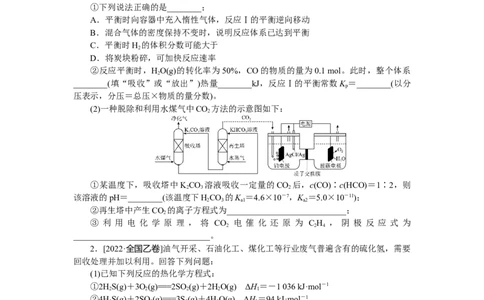
(2)一种脱除和利用水煤气中CO 方法的示意图如下:
2
①某温度下,吸收塔中KCO 溶液吸收一定量的CO 后,c(CO)∶c(HCO)=1∶2,则
2 3 2
该溶液的pH=________(该温度下HCO 的K =4.6×10-7,K =5.0×10-11);
2 3 a1 a2
②再生塔中产生CO 的离子方程式为____________________________;
2
③ 利 用 电 化 学 原 理 , 将 CO 电 催 化 还 原 为 C H , 阴 极 反 应 式 为
2 2 4
________________________________。
2.[2022·全国乙卷]油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要
回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①2HS(g)+3O(g)===2SO(g)+2HO(g) ΔH=-1 036 kJ·mol-1
2 2 2 2 1
②4HS(g)+2SO (g)===3S (g)+4HO(g) ΔH=94 kJ·mol-1
2 2 2 2 2
③2H(g)+O(g)===2H O(g) ΔH=-484 kJ·mol-1
2 2 2 3
计算HS热分解反应④2HS(g)===S (g)+2H(g)的ΔH=________ kJ·mol-1。
2 2 2 2 4
(2)较普遍采用的HS处理方法是克劳斯工艺,即利用反应①和②生成单质硫。另一种
2
方法是,利用反应④高温热分解 HS。相比克劳斯工艺,高温热分解方法的优点是
2
______________________,缺点是____________。
(3)在1 470 K、100 kPa反应条件下,将n(H S)∶n(Ar)=1∶4的混合气进行HS热分解
2 2
反应。平衡时混合气中HS与H 的分压相等,HS平衡转化率为________,平衡常数K =
2 2 2 p
________ kPa。
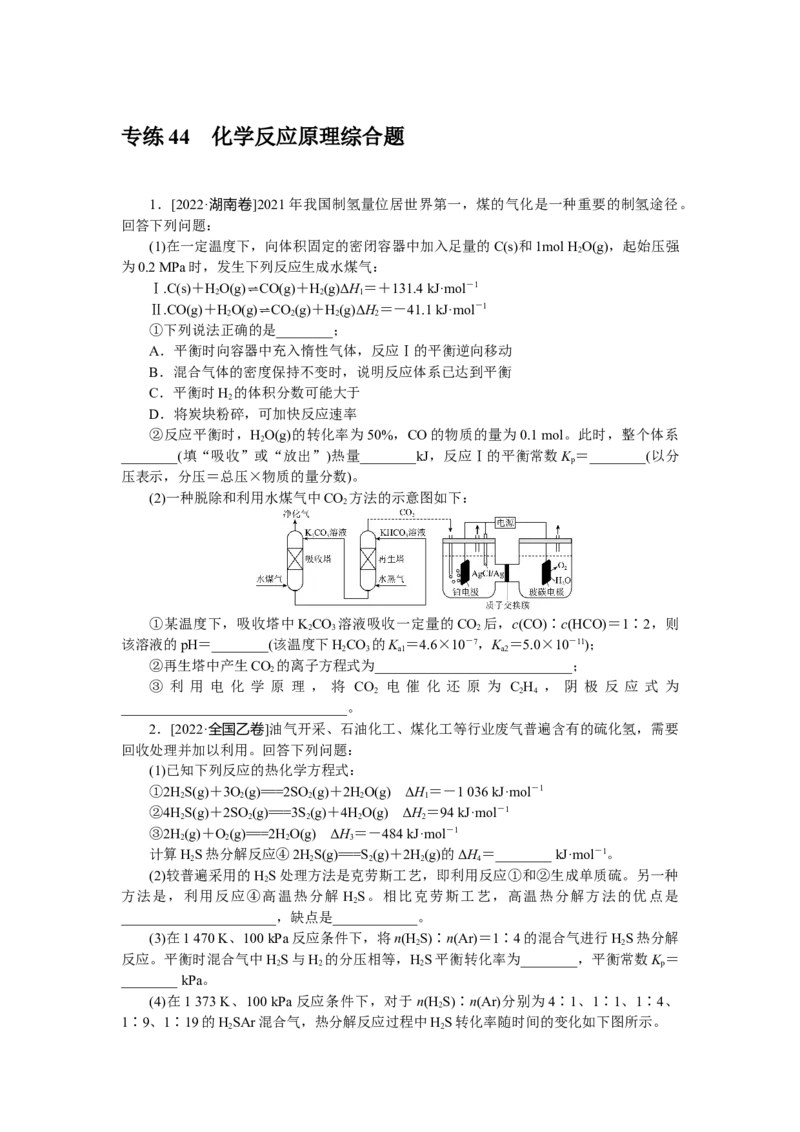
(4)在1 373 K、100 kPa反应条件下,对于n(H S)∶n(Ar)分别为4∶1、1∶1、1∶4、
2
1∶9、1∶19的HSAr混合气,热分解反应过程中HS转化率随时间的变化如下图所示。
2 2①n(H S)∶n(Ar) 越 小 , HS 平 衡 转 化 率 ________ , 理 由 是
2 2
______________________________。
②n(H S)∶n(Ar)=1∶9对应图中曲线________,计算其在0~0.1 s之间,HS分压的
2 2
平均变化率为________ kPa·s-1。
3.[2021·广东卷]我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与
4
CO 重整是CO 利用的研究热点之一。该重整反应体系主要涉及以下反应:
2 2
a)CH
4
(g)+CO
2
(g)⇌2CO(g)+2H
2
(g) ΔH
1
b)CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ΔH
2
c)CH
4
(g)⇌C(s)+2H
2
(g) ΔH
3
d)2CO(g)⇌CO
2
(g)+C(s) ΔH
4
e)CO(g)+H
2
(g)⇌H
2
O(g)+C(s) ΔH
5
(1)根据盖斯定律,反应a的ΔH=________(写出一个代数式即可)。
1
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有________。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
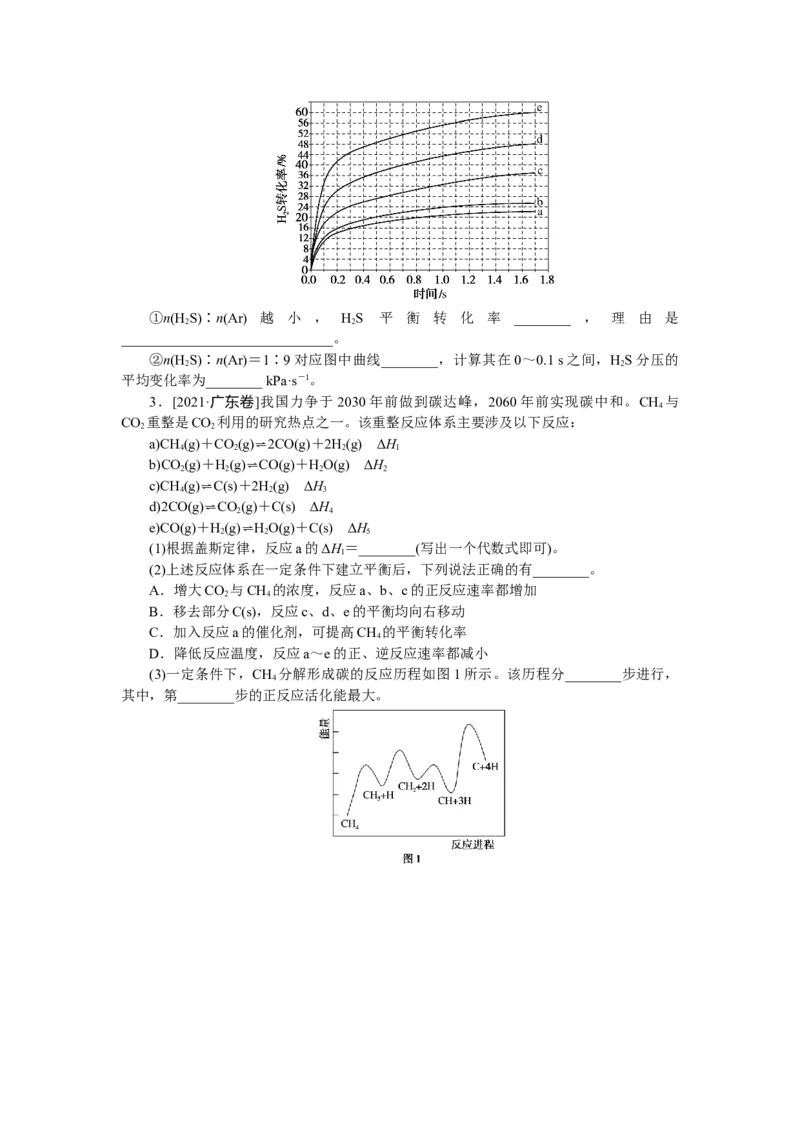
(3)一定条件下,CH 分解形成碳的反应历程如图1所示。该历程分________步进行,
4
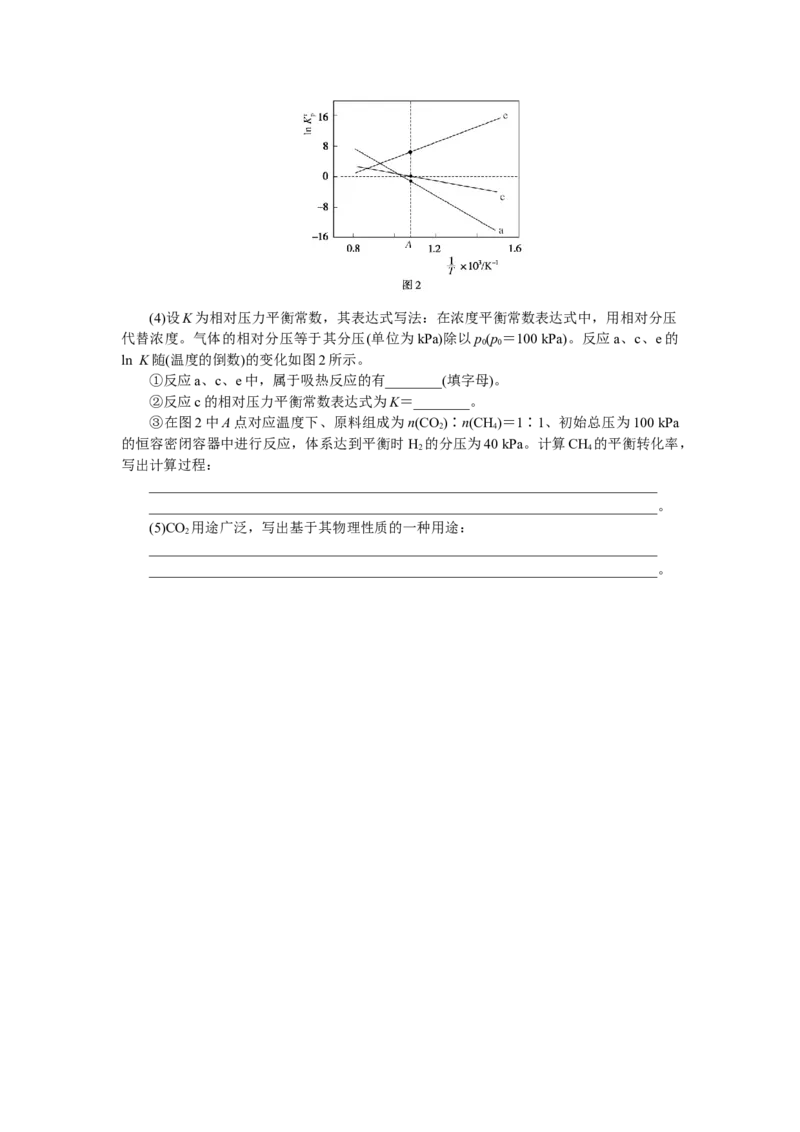
其中,第________步的正反应活化能最大。(4)设K为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压
代替浓度。气体的相对分压等于其分压(单位为kPa)除以p(p =100 kPa)。反应a、c、e的
0 0
ln K随(温度的倒数)的变化如图2所示。
①反应a、c、e中,属于吸热反应的有________(填字母)。
②反应c的相对压力平衡常数表达式为K=________。
③在图2中A点对应温度下、原料组成为n(CO)∶n(CH)=1∶1、初始总压为100 kPa
2 4
的恒容密闭容器中进行反应,体系达到平衡时H 的分压为40 kPa。计算CH 的平衡转化率,
2 4
写出计算过程:
________________________________________________________________________
________________________________________________________________________。
(5)CO 用途广泛,写出基于其物理性质的一种用途:
2
________________________________________________________________________
________________________________________________________________________。