文档内容
第四篇 化学反应速率与化学平衡
专项 27 K
P
近年来,有关压强平衡常数考查频频出现于化学反应原理综合题,已成为考查“证据推理与模型认
知”的化学学科核心素养重要题型。
一定条件下,若平衡体系中有气体物质,也可用其分压代替浓度,所求得的平衡常数为压强平衡常数,
以K 表示。
p
pc ·pd
C D
(1)对于反应aA(g)+bB(g) cC(g)+dD(g),其压强平衡常数表达式为K = 。浓度平衡常
p pa ·pb
A B
cc(C)·cd(D) n
数与压强平衡常数的关系:K= ,又p= RT=cRT,则K =K·(RT)Δn[Δn=(c+d)-(a+b)]。
c ca(A)·cb(B) V p c
(2)气体分压=气体总压×该气体的物质的量分数或体积分数。混合气体的总压等于相同温度下各组分气
体的分压之和。
1.(2022•全国甲卷)金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之
一是将金红石(TiO)转化为TiCl ,再进一步还原得到钛。回答下列问题:
2 4
(1) TiO 转化为TiCl 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
2 4
(ⅰ)直接氯化:TiO(s)+2Cl(g)= TiCl (g)+O(g) ΔH =172kJ·mol−1 Kp =1.0×10-2
2 2 4 2 1 1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)=TiCl (g)+2CO(g) ΔH =-51kJ·mol−1 Kp =1.2×1012Pa
2 2 4 2 2
①反应2C(s)+O(g)=2CO(g)的ΔH为_______ kJ·mol−1,Kp=_______Pa。
2
②碳氯化的反应趋势远大于直接氯化,其原因是_______。③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平衡转
化率_______(填“变大”“变小”或“不变”)。
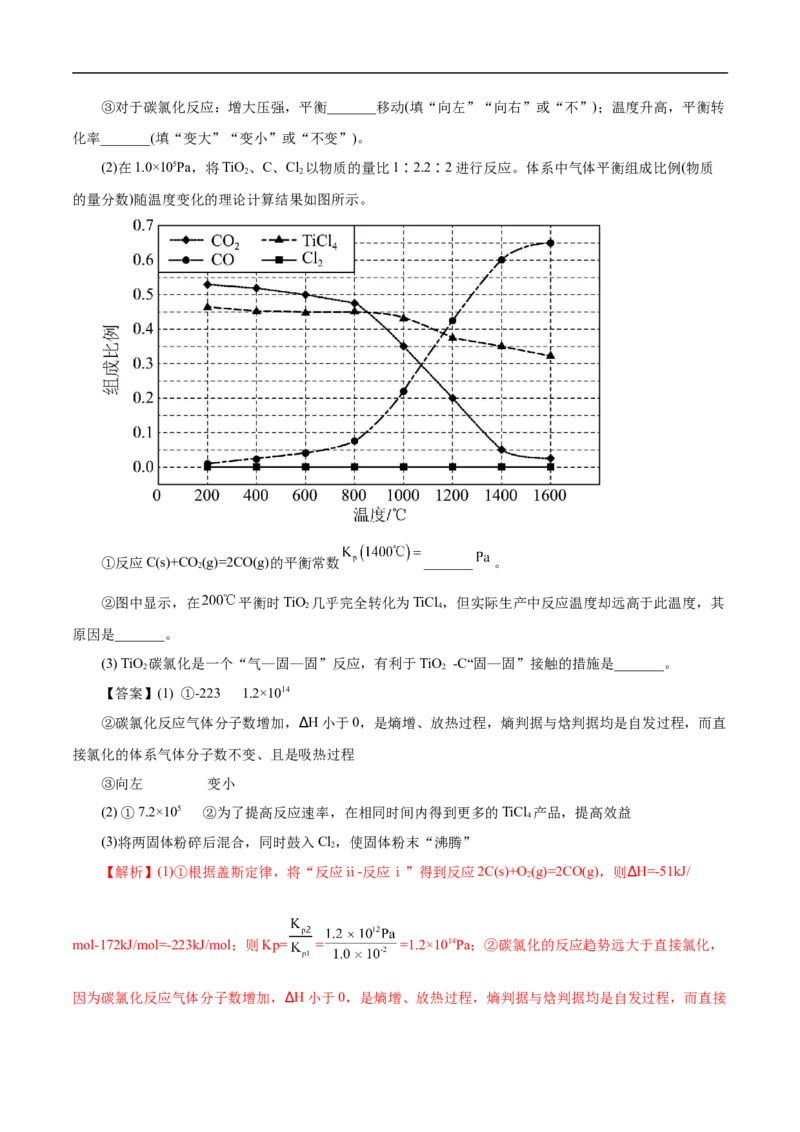
(2)在1.0×105Pa,将TiO、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质
2 2
的量分数)随温度变化的理论计算结果如图所示。
①反应C(s)+CO(g)=2CO(g)的平衡常数 _______ 。
2
②图中显示,在 平衡时TiO 几乎完全转化为TiCl ,但实际生产中反应温度却远高于此温度,其
2 4
原因是_______。
(3) TiO 碳氯化是一个“气—固—固”反应,有利于TiO -C“固—固”接触的措施是_______。
2 2
【答案】(1) ①-223 1.2×1014
②碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直
接氯化的体系气体分子数不变、且是吸热过程
③向左 变小
(2) ①7.2×105 ②为了提高反应速率,在相同时间内得到更多的TiCl 产品,提高效益
4
(3)将两固体粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”
2
【解析】(1)①根据盖斯定律,将“反应ⅱ-反应ⅰ”得到反应2C(s)+O(g)=2CO(g),则∆H=-51kJ/
2
mol-172kJ/mol=-223kJ/mol;则Kp= = =1.2×1014Pa;②碳氯化的反应趋势远大于直接氯化,
因为碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直接氯化的体系气体分子数不变、且是吸热过程;③对应碳氯化反应,气体分子数增大,依据勒夏特列原理,
增大压强,平衡往气体分子数减少的方向移动,即平衡向左移动;该反应是放热反应,温度升高,平衡往
吸热方向移动,即向左移动,则平衡转化率变小。(2)①从图中可知,1400℃,体系中气体平衡组成比例
CO 是0.05,TiCl 是0.35,CO是0.6,反应C(s)+CO(g)=2CO(g)的平衡常数Kp(1400℃)= =
2 4 2
Pa=7.2×105Pa;②实际生产中需要综合考虑反应的速率、产率等,以达到最佳效益,实际
反应温度远高于200℃,就是为了提高反应速率,在相同时间内得到更多的TiCl 产品。(3)固体颗粒越小,
4
比表面积越大,反应接触面积越大。有利于TiO – C“固-固”接触,可将两者粉碎后混合,同时鼓入Cl,
2 2
使固体粉末“沸腾”,增大接触面积。
2. (2022•湖南选择性考试节选)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和
1molH O(g),起始压强为 时,发生下列反应生成水煤气:
2
Ⅰ. C(s)+ H O(g) CO(g)+H(g) ΔH =+131.4kJ·mol−1
2 2 1
Ⅱ. CO(g)+ H O(g) CO(g)+H(g) ΔH =-41.1kJ·mol−1
2 2 2 2
①下列说法正确的是_______;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时H 的体积分数可能大于2/3
2
D.将炭块粉碎,可加快反应速率
②反应平衡时,HO(g)的转化率为 ,CO的物质的量为0.1mol。此时,整个体系_______(填“吸
2
收”或“放出”)热量_______kJ,反应Ⅰ的平衡常数K =_______(以分压表示,分压=总压×物质的量分数)。
p
【答案】BD 吸收 13.14 0.02MPa
【解析】①A项,在恒温恒容条件下,平衡时向容器中充入情性气体不能改变反应混合物的浓度,因
此反应Ⅰ的平衡不移动,A说法不正确;B项,在反应中有固体C转化为气体,气体的质量增加,而容器
的体积不变,因此气体的密度在反应过程中不断增大,当混合气体的密度保持不变时,说明反应体系已达
到平衡,B说法正确;C项,若C(s)和HO(g)完全反应全部转化为CO(g)和H(g),由C(s)+ 2H O(g) =
2 2 2 2
CO(g)+ 2H (g)可知,H 的体积分数的极值为 ,由于可逆反应只有一定的限度,反应物不可能全部转化为
2 2 2生成物,因此,平衡时H 的体积分数不可能大于 ,C说法不正确;D项,将炭块粉碎可以增大其与
2
HO(g)的接触面积,因此可加快反应速率,D说法正确;故选BD。②反应平衡时,HO(g)的转化率为
2 2
50%,则水的变化量为0.5mol,水的平衡量也是0.5mol,由于CO的物质的量为0.1mol,则根据O原子守
恒可知CO 的物质的量为0.2mol,根据相关反应的热化学方程式可知,生成0.1mol CO要吸收热量13.14kJ
2
,生成0.2mol CO 要放出热量8.22kJ此时,因此整个体系吸收热量13.14kJ-8.22kJ=4.92kJ;由H原子守恒
2
可知,平衡时H 的物质的量为0.5mol,CO的物质的量为0.1mol,CO 的物质的量为0.2mol,水的物质的
2 2
量为0.5mol,则平衡时气体的总物质的量为0.5mol+0.1mol+0.2mol+0.5mol=1.3mol,在同温同体积条件下,
气体的总压之比等于气体的总物质的量之比,则平衡体系的总压为0.2MPa 1.3=0.26MPa,反应I(C(s)
+H O(g) CO(g)+H(g))的平衡常数K = 。
2 2 p
3.(2021·全国乙卷节选)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用
作有机合成中的碘化剂。McMorris测定和计算了在136~180 ℃范围内下列反应的平衡常数K 。
p
2NO(g)+2ICl(g) 2NOCl(g)+I(g) K
2 p1
2NOCl(g) 2NO(g)+Cl (g) K
2 p2
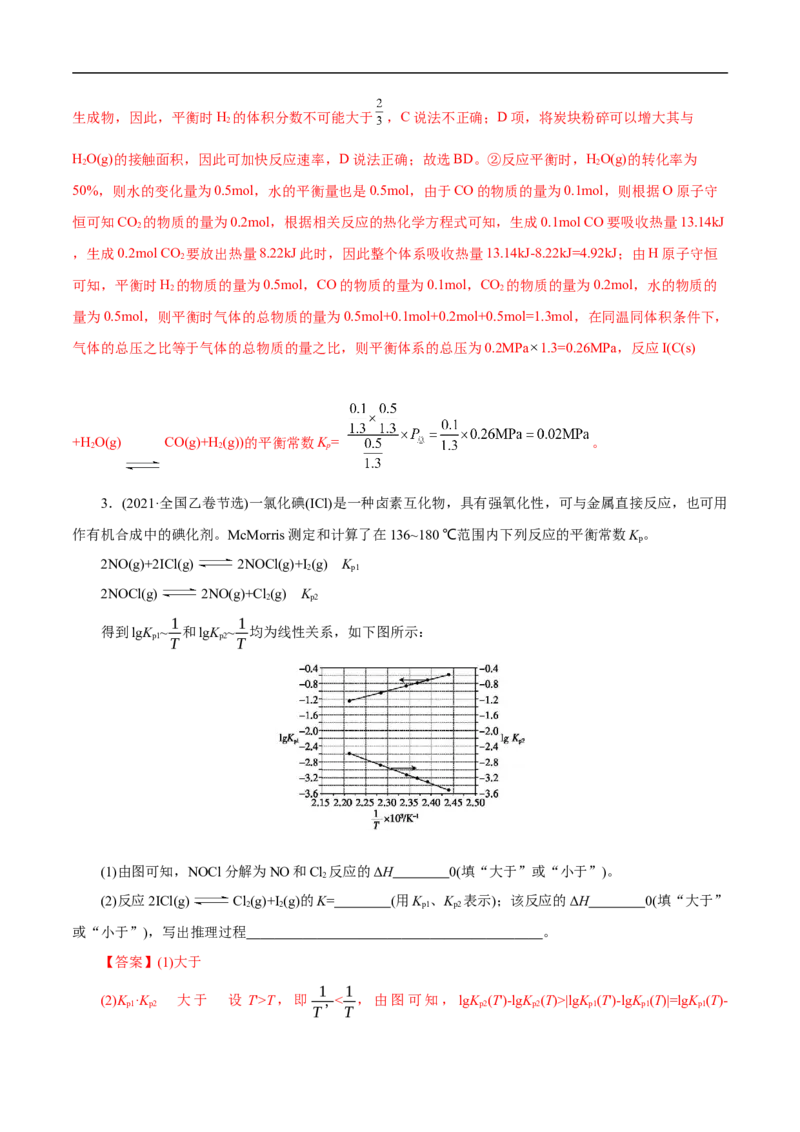
1 1
得到lgK ~ 和lgK ~ 均为线性关系,如下图所示:
p1 p2
T T
(1)由图可知,NOCl分解为NO和Cl 反应的ΔH 0(填“大于”或“小于”)。
2
(2)反应2ICl(g) Cl(g)+I (g)的K= (用K 、K 表示);该反应的ΔH 0(填“大于”
2 2 p1 p2
或“小于”),写出推理过程 。
【答案】(1)大于
1 1
(2)K ·K 大于 设 T'>T,即 < ,由图可知,lgK (T')-lgK (T)>|lgK (T')-lgK (T)|=lgK (T)-
p1 p2 T' T p2 p2 p1 p1 p1lgK (T'),则lg[K (T')·K (T')]>lg[K (T)·K (T)],即K(T')>K(T),因此该反应的正反应为吸热反应,即ΔH大
p1 p2 p1 p2 p1
于0
1
【解析】(1)结合图可知,温度越高, 越小,lgK 越大,即K 越大,说明升高温度平衡2NOCl(g)
p2 p2
T
2NO(g)+Cl (g)正向移动,则NOCl分解为NO和Cl 反应的ΔH大于0。(2)现将已知的两个热化学方
2 2
程式命名为Ⅰ、Ⅱ,根据盖斯定律,Ⅰ+Ⅱ得2ICl(g) Cl(g)+I (g),则2ICl(g) Cl(g)+I (g)的
2 2 2 2
K=K ·K 。
p1 p2
第一步 根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度
第二步 计算各气体组分的物质的量分数或体积分数
根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压
第三步
强×该气体的体积分数(或物质的量分数)
根据平衡常数计算公式代入计算。例如,N(g)+3H(g) 2NH (g),
2 2 3
第四步
压强平衡常数表达式为K= 。
p
1.氨基甲酸铵发生分解的化学方程式为NH COONH(s) 2NH (g)+CO (g)。利用如下装置测定不
2 4 3 2
同温度下该反应以分压表示的化学平衡常数K 。
p
步骤Ⅰ:关闭K,打开K 和K,开启真空泵抽气至测压仪数值稳定后关闭K;
3 1 2 1
步骤Ⅱ:关闭K,缓慢开启K 至U形管两边液面相平并保持不变,读取压强数值。
2 3
记录25 ℃、30 ℃下压强分别为12.0 kPa、17.1 kPa。下列说法错误的是( )。
A.氨基甲酸铵分解反应的ΔH>0
B.该反应25 ℃时的化学平衡常数K =2.56×1011 Pa3
p
C.步骤Ⅰ中测压仪数值未稳定即关闭K,K 测量值偏小
1 pD.步骤Ⅱ中读数时U形管左侧液面偏高,K 测量值偏大
p
2.T℃时,向容积为2L的刚性容器中充入1 mol CO 和一定量的H 发生反应:CO(g)+2H(g)
2 2 2 2
HCHO(g) +H O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始 的关系如图所
2
示。已知:初始加入2molH 时,容器内气体的总压强为1.2p kPa。下列说法错误的是
2
A.5 min时反应到达c点, (H )=0.1 mol·L-1·min-1
2
B.随 增大, HCHO的平衡压强不断增大
C.b点时反应的平衡常数K =
p
D.c点时,再加入CO(g)和HO(g) ,使二者分压均增大0.2p kPa,平衡不向移动
2 2
3.在容积固定的密闭容器中,起始时充入0.2molSO ,0.1molO ,反应体系起始总压强0.1MPa,反应
2 2
在一定温度下达到平衡时,SO 的转化率为90%,该反应的压强平衡常数K =_________(用平衡分压代替
2 p
平衡浓度计算;分压=总压×物质的量分数)。
4.二氧化硫的催化氧化是工业上生产硫酸的主要反应O(g)+2SO(g) 2SO (g)。
2 2 3
已知:标准平衡常数Kθ= ,其中pθ为标准压强(1×105Pa),p(SO )、p(O )和p(SO )为各组分
3 2 2
的平衡分压,如p(SO )=x(SO)p,p为平衡总压,x(SO )为平衡系统中SO 的物质的量分数。SO 和O 起始
3 3 3 3 2 2
物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO 的平衡产率为ω,则Kθ= (用含
3
ω的最简式表示)。
5.气体分压p=p ×x(物质的量分数)。恒温50℃、恒压101kPa,将足量的CuSO ·5H O、NaHCO 置
i 总 i 4 2 3
于一个密闭容器中,再充入已除去CO 的干燥空气。假设只发生以下反应,达平衡时两者分解的物质的量
2
比为2:1。
CuSO ·5H O(s) CuSO ·3H O(s)+2H O(g) K =36(kPa)2
4 2 4 2 2 p12NaHCO (s) NaCO(s)+HO(g)+CO(g) K
3 2 3 2 2 p2
①平衡时 =____________,K =_______________。
p2
②平衡后,用总压为101kPa的潮湿空气[其中p(H O)=8kPa、p(CO)=0.4kPa]替换容器中的气体,50℃
2 2
下达到新平衡。容器内CuSO ·5H O的质量将______(填“增加”“减少”或“不变”,下同),NaHCO 质
4 2 3
量将_________。
6.500 ℃时,向容积为2 L的密闭容器中通入1 mol N 和3 mol H ,模拟合成氨的反应,容器内的压
2 2
强随时间的变化如下表所示:
时间/min 0 10 20 30 40 +∞
压强/MPa 20 17 15 13.2 11 11
①达到平衡时N 的转化率为________。
2
②用压强表示该反应的平衡常数K =________(K 等于平衡时生成物分压幂的乘积与反应物分压幂的
p p
乘积的比值,某物质的分压等于总压×该物质的物质的量分数)。
7.乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
热裂解反应:CHCOOH(g)===2CO(g)+2H(g) ΔH=213.7kJ·mol-1
3 2
脱酸基反应 CHCOOH(g)===CH (g)+CO(g) ΔH=-33.5kJ·mol-1
3 4 2
若利用合适的催化剂控制其他的副反应,温度为 TK时达到平衡,总压强为pkPa,热裂解反应消耗乙
酸20%,脱酸基反应消耗乙酸60%,乙酸体积分数为_______(计算结果保留1位小数);脱酸基反应的平衡
常数K 为____________kPa(K 为以分压表示的平衡常数,计算结果保留1位小数)。
p p
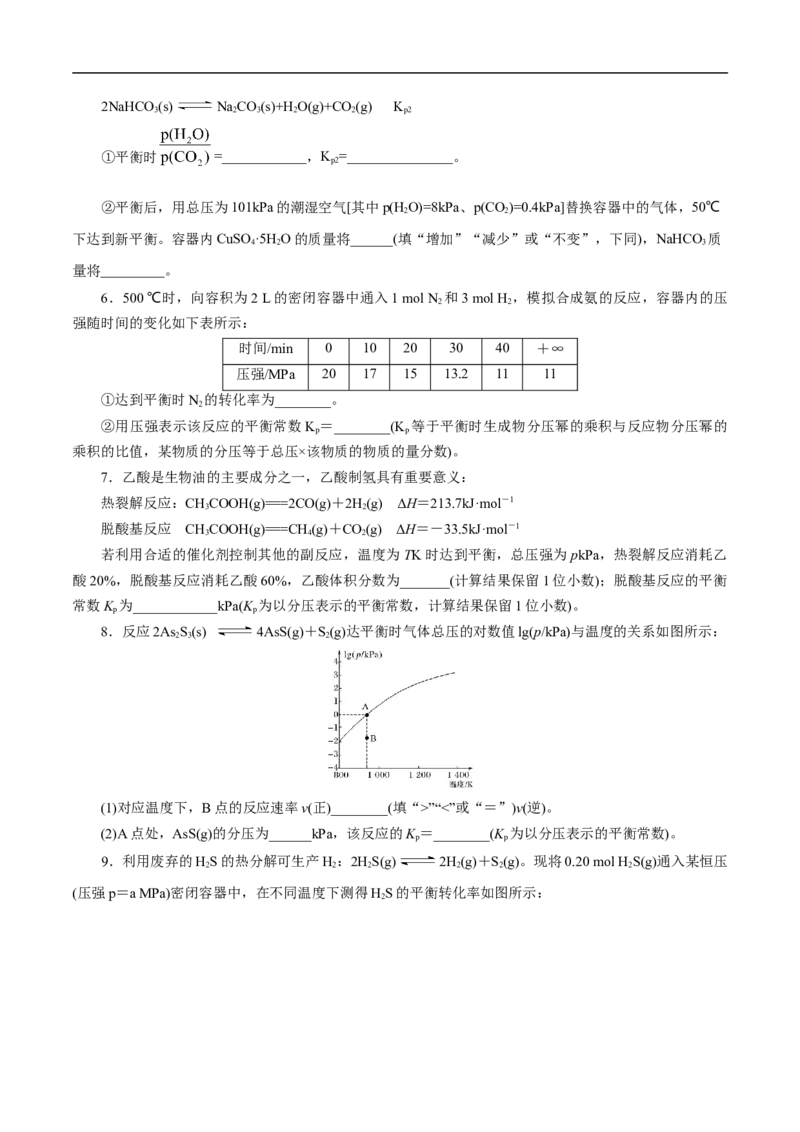
8.反应2As S(s) 4AsS(g)+S(g)达平衡时气体总压的对数值lg(p/kPa)与温度的关系如图所示:
2 3 2
(1)对应温度下,B点的反应速率v(正)________(填“>”“<”或“=”)v(逆)。
(2)A点处,AsS(g)的分压为______kPa,该反应的K =________(K 为以分压表示的平衡常数)。
p p
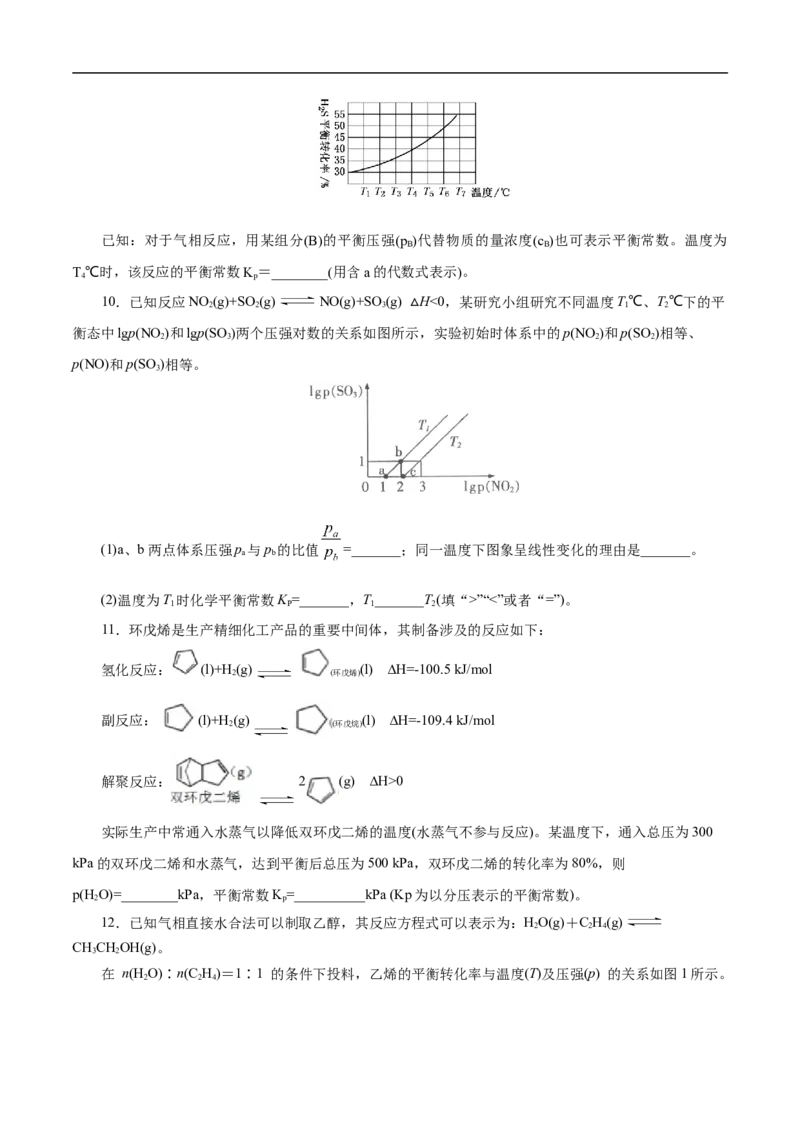
9.利用废弃的HS的热分解可生产H:2HS(g) 2H(g)+S(g)。现将0.20 mol H S(g)通入某恒压
2 2 2 2 2 2
(压强p=a MPa)密闭容器中,在不同温度下测得HS的平衡转化率如图所示:
2已知:对于气相反应,用某组分(B)的平衡压强(p )代替物质的量浓度(c )也可表示平衡常数。温度为
B B
T℃时,该反应的平衡常数K=________(用含a的代数式表示)。
4 p
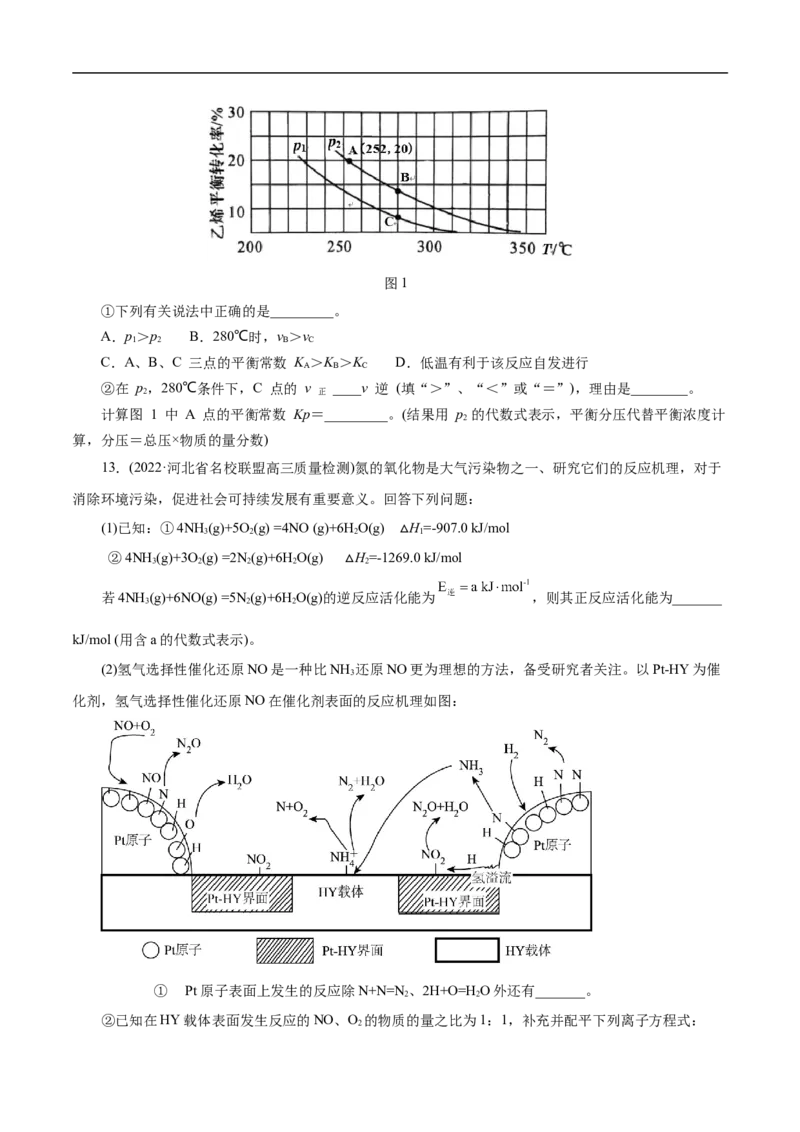
10.已知反应NO (g)+SO(g) NO(g)+SO (g) H<0,某研究小组研究不同温度T℃、T℃下的平
2 2 3 1 2
衡态中lgp(NO )和lgp(SO )两个压强对数的关系如图所示△,实验初始时体系中的p(NO )和p(SO )相等、
2 3 2 2
p(NO)和p(SO )相等。
3
(1)a、b两点体系压强p 与p 的比值 =_______;同一温度下图象呈线性变化的理由是_______。
a b
(2)温度为T 时化学平衡常数K =_______,T_______T(填“>”“<”或者“=”)。
1 P 1 2
11.环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:
氢化反应: (l)+H (g) (l) ∆H=-100.5 kJ/mol
2 (环戊烯)
副反应: (l)+H (g) (l) ∆H=-109.4 kJ/mol
2 (环戊烷)
解聚反应: 2 (g) ∆H>0
实际生产中常通入水蒸气以降低双环戊二烯的温度(水蒸气不参与反应)。某温度下,通入总压为300
kPa的双环戊二烯和水蒸气,达到平衡后总压为500 kPa,双环戊二烯的转化率为80%,则
p(H O)=________kPa,平衡常数K=__________kPa (Kp为以分压表示的平衡常数)。
2 p
12.已知气相直接水合法可以制取乙醇,其反应方程式可以表示为:HO(g)+C H(g)
2 2 4
CHCHOH(g)。
3 2
在 n(H O)∶n(C H)=1∶1 的条件下投料,乙烯的平衡转化率与温度(T)及压强(p) 的关系如图1所示。
2 2 4图1
①下列有关说法中正确的是_________。
A.p>p B.280℃时,v >v
1 2 B C
C.A、B、C 三点的平衡常数 K >K >K D.低温有利于该反应自发进行
A B C
②在 p,280℃条件下,C 点的 v ____v 逆 (填“>”、“<”或“=”),理由是________。
2 正
计算图 1 中 A 点的平衡常数 Kp=_________。(结果用 p 的代数式表示,平衡分压代替平衡浓度计
2
算,分压=总压×物质的量分数)
13.(2022·河北省名校联盟高三质量检测)氮的氧化物是大气污染物之一、研究它们的反应机理,对于
消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)已知:①4NH (g)+5O(g) =4NO (g)+6H O(g) H=-907.0 kJ/mol
3 2 2 1
②4NH
3
(g)+3O
2
(g) =2N
2
(g)+6H
2
O(g) H
2
=-126△9.0 kJ/mol
△
若4NH (g)+6NO(g) =5N (g)+6HO(g)的逆反应活化能为 ,则其正反应活化能为_______
3 2 2
kJ/mol (用含a的代数式表示)。
(2)氢气选择性催化还原NO是一种比NH 还原NO更为理想的方法,备受研究者关注。以Pt-HY为催
3
化剂,氢气选择性催化还原NO在催化剂表面的反应机理如图:
① Pt原子表面上发生的反应除N+N=N、2H+O=HO外还有_______。
2 2
②已知在HY载体表面发生反应的NO、O 的物质的量之比为1:1,补充并配平下列离子方程式:
2NH ++NO+O N+H O+__________。
4 2 2 2
(3)在密闭容器中充入4mol NO和5mol H,发生反应:2NO(g)+2H (g) =N (g)+2HO(g) ΔH<0。平
2 2 2 2
衡时NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中d点大于b点的是_______(填字母)。
A.正反应速率 B.逆反应速率
C.N(g)的浓度 D.对应温度的平衡常数
2
②c点NO的平衡转化率为_______。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中
a、b、c、d中的点。_______
(4)T℃时,向容积为2L的恒容容器中充入0.4mol NO、0.8mol H ,发生反应:2NO(g)+2H (g) =N (g)
2 2 2
+2H O(g),体系的总压强p随时间t的变化如下表所示:
2
t/min 0 10 20 30 40
p/kPa 240 226 216 210 210
①0~20min内该反应的平均反应速率v(NO)= _______ 。
②该温度下反应的平衡常数K =_______ (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分
P
数,列出计算式即可)。