文档内容
专项训练 无机物的分离提纯
1.NH Al(SO )·12H O俗称铵明矾,其性质稳定,是化学实验中常用的基准试剂,借
4 4 2 2
助碳酸氢铵与硫酸钠可以制备纯净的铵明矾,制备过程如图所示。下列相关说法错误
的是
A.为加快操作Ⅰ的速率,实验时采用抽滤,常用玻璃纤维替代滤纸
B.操作Ⅱ的基本过程为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.滤液a中加稀硫酸调节pH=2的目的是抑制NH 的水解
D.将气体a通入饱和纯碱溶液中会有晶体析出,该晶体与固体a成分相同
2.用海水得到的粗盐中含有较多杂质(如不溶性的泥沙,可溶性的CaCl 、MgCl 以及
2 2
一些硫酸盐等),粗盐提纯的流程如图所示。下列说法错误的是
A.步骤①⑤⑦均会使用的仪器是玻璃棒
B.步骤②所加X溶液和步骤④所加Y溶液的顺序可以调换
C.步骤⑥加入盐酸的目的是除去过量的NaOH和NaCO
2 3
D.该提纯过程未涉及氧化还原反应
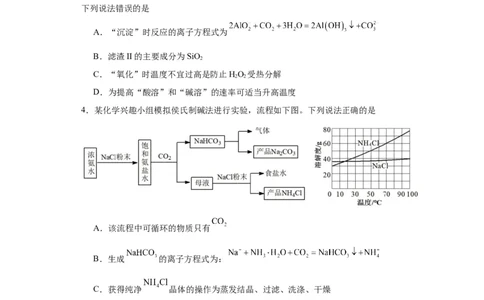
3.聚合硫酸铝铁(PFAS)是一种新型高效水处理剂。以粉煤灰(主要成分为Al O、
2 3
Fe O、FeO等)为铝源,利用硫铁矿烧渣(主要成分为Fe O、FeO、SiO 等)为铁源,制
2 3 3 4 2
备PFAS 的工艺流程如下:
资料收集整理【淘宝店铺:向阳百分百】下列说法错误的是
A.“沉淀”时反应的离子方程式为
B.滤渣II的主要成分为SiO
2
C.“氧化”时温度不宜过高是防止HO 受热分解
2 2
D.为提高“酸溶”和“碱溶”的速率可适当升高温度
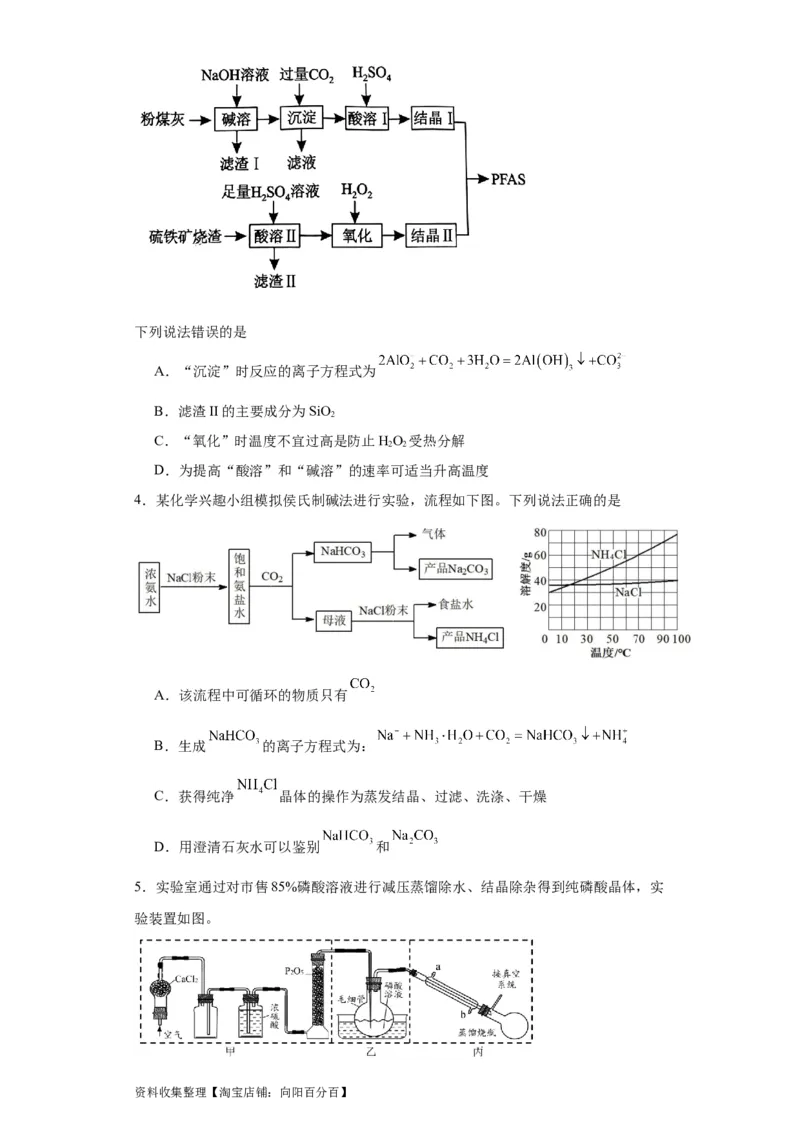
4.某化学兴趣小组模拟侯氏制碱法进行实验,流程如下图。下列说法正确的是
A.该流程中可循环的物质只有
B.生成 的离子方程式为:
C.获得纯净 晶体的操作为蒸发结晶、过滤、洗涤、干燥
D.用澄清石灰水可以鉴别 和
5.实验室通过对市售85%磷酸溶液进行减压蒸馏除水、结晶除杂得到纯磷酸晶体,实
验装置如图。
资料收集整理【淘宝店铺:向阳百分百】已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成 (熔点为
30℃),高于100℃则发生分子间脱水生成焦磷酸。
下列实验装置和操作不能达到实验目的的是
A.图甲中使用的 、浓硫酸、 的目的均为干燥气体
B.向图乙得到的过饱和磷酸溶液中加入磷酸晶体,可以促进其结晶
C.图丙中冷凝管的进水口是b,具支烧瓶中得到磷酸溶液
D.磷酸中少量的水极难除去的原因是磷酸可与水分子间形成氢键
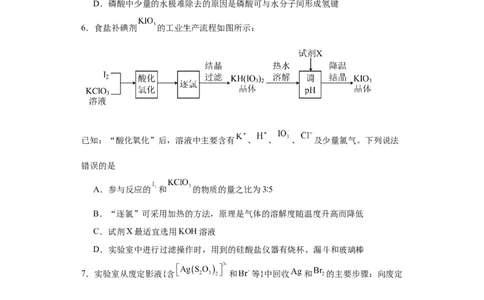
6.食盐补碘剂 的工业生产流程如图所示:
已知:“酸化氧化”后,溶液中主要含有 、 、 、 及少量氯气。下列说法
错误的是
A.参与反应的 和 的物质的量之比为3∶5
B.“逐氯”可采用加热的方法,原理是气体的溶解度随温度升高而降低
C.试剂X最适宜选用KOH溶液
D.实验室中进行过滤操作时,用到的硅酸盐仪器有烧杯、漏斗和玻璃棒
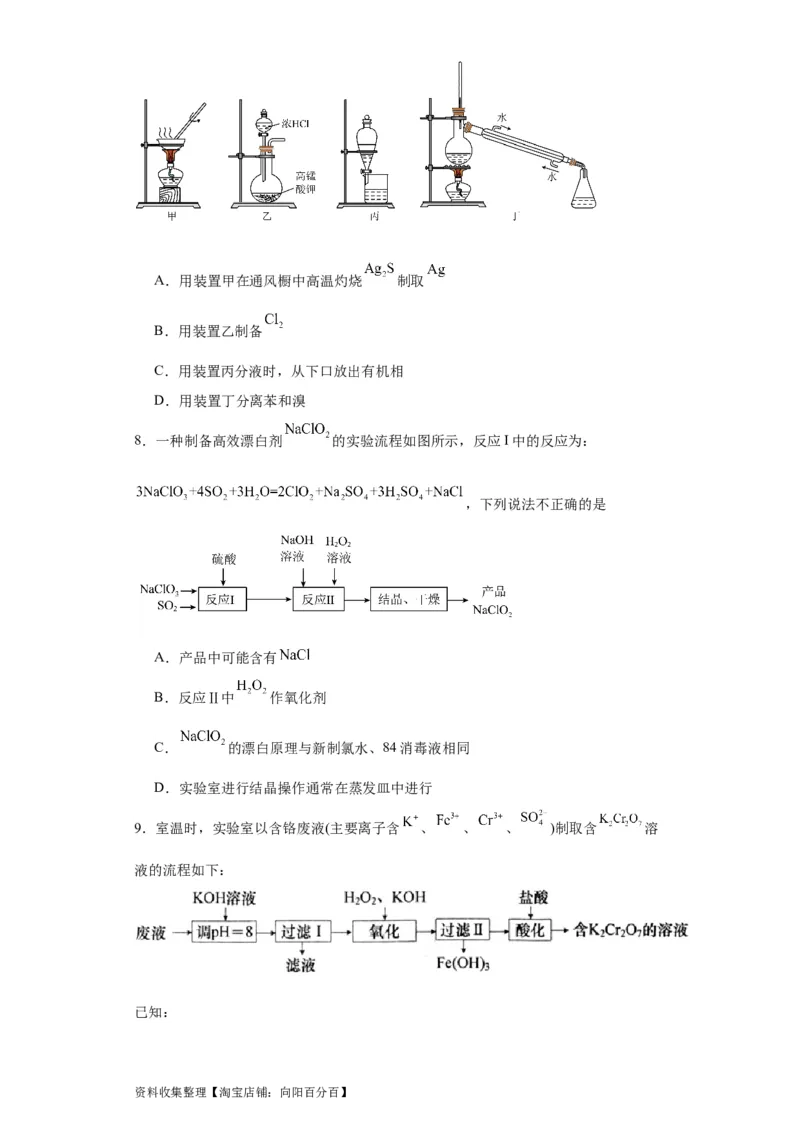
7.实验室从废定影液{含 和 等}中回收 和 的主要步骤:向废定
影液中加入 溶液沉银,过滤、洗涤及干燥,灼烧 制 ;制取 并通入滤
液氧化 ,用苯萃取分液,最后蒸馏分离苯和溴。部分操作的装置如图,下列叙述正
确的是
资料收集整理【淘宝店铺:向阳百分百】A.用装置甲在通风橱中高温灼烧 制取
B.用装置乙制备
C.用装置丙分液时,从下口放出有机相
D.用装置丁分离苯和溴
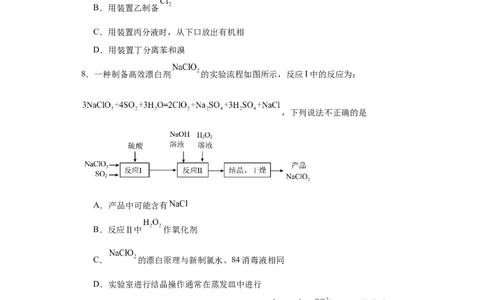
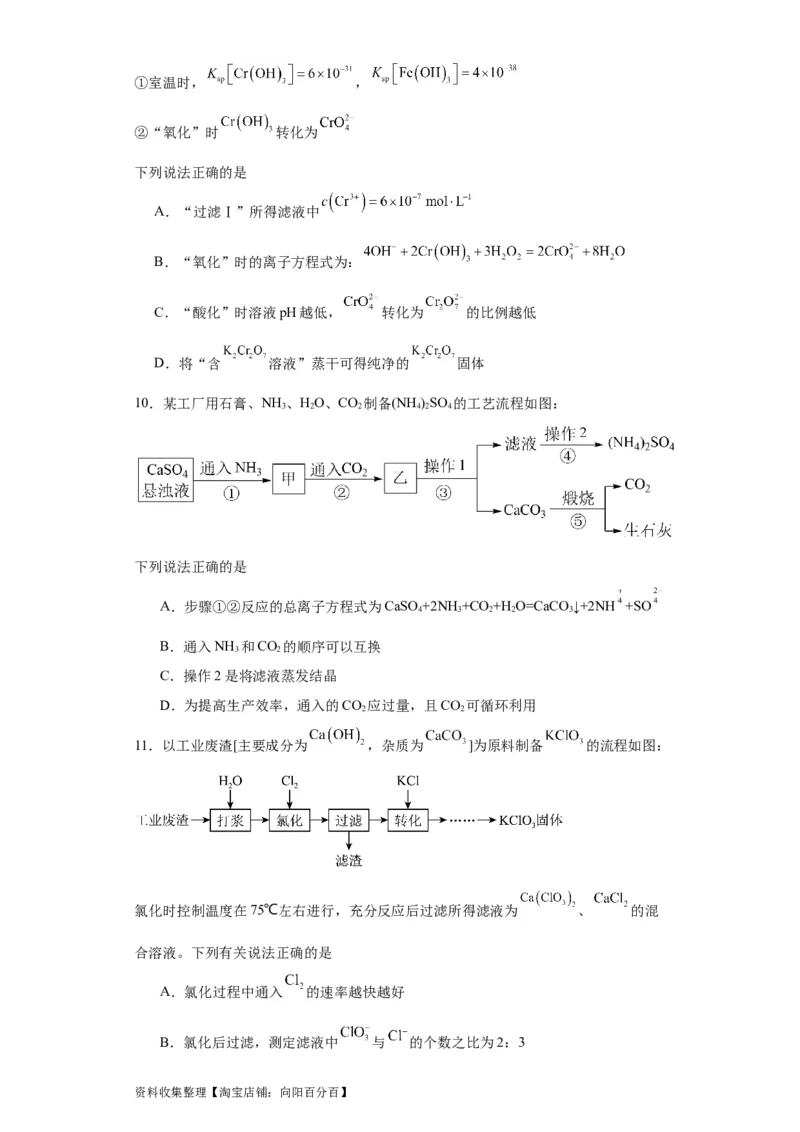
8.一种制备高效漂白剂 的实验流程如图所示,反应I中的反应为:
,下列说法不正确的是
A.产品中可能含有
B.反应Ⅱ中 作氧化剂
C. 的漂白原理与新制氯水、84消毒液相同
D.实验室进行结晶操作通常在蒸发皿中进行
9.室温时,实验室以含铬废液(主要离子含 、 、 、 )制取含 溶
液的流程如下:
已知:
资料收集整理【淘宝店铺:向阳百分百】①室温时, ,
②“氧化”时 转化为
下列说法正确的是
A.“过滤Ⅰ”所得滤液中
B.“氧化”时的离子方程式为:
C.“酸化”时溶液pH越低, 转化为 的比例越低
D.将“含 溶液”蒸干可得纯净的 固体
10.某工厂用石膏、NH 、HO、CO 制备(NH )SO 的工艺流程如图:
3 2 2 4 2 4
下列说法正确的是
A.步骤①②反应的总离子方程式为CaSO+2NH+CO +H O=CaCO ↓+2NH +SO
4 3 2 2 3
B.通入NH 和CO 的顺序可以互换
3 2
C.操作2是将滤液蒸发结晶
D.为提高生产效率,通入的CO 应过量,且CO 可循环利用
2 2
11.以工业废渣[主要成分为 ,杂质为 ]为原料制备 的流程如图:
氯化时控制温度在75℃左右进行,充分反应后过滤所得滤液为 、 的混
合溶液。下列有关说法正确的是
A.氯化过程中通入 的速率越快越好
B.氯化后过滤,测定滤液中 与 的个数之比为2:3
资料收集整理【淘宝店铺:向阳百分百】C.滤渣的主要成分为
D.转化过程可能发生反应的化学方程式为
12.绿矾(FeSO •7H O)是治疗缺铁性贫血药品的重要成分。下面是市售铁屑(少量锡、
4 2
氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
已知:室温时,饱和HS溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开
2
始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5;FeSO •7H O不溶于乙醇。
4 2
A.将浓硫酸稀释为25%稀硫酸,所需玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管
B.操作Ⅰ、Ⅲ中均需用到玻璃棒,为了加快反应速率,可用玻璃棒进行搅拌
C.操作Ⅱ中,通入HS至饱和的目的是使Sn2+转化为SnS沉淀并防止Fe2+被氧化
2
D.操作Ⅳ中所得的晶体可用乙醇洗去晶体表面附着的水
13. 是一种重要的无机化合物,能溶于水、稀硫酸,不溶于乙醇,受热易分解。
利用“ 氧化法”制备 的工艺流程如下:
“酸化反应”所得产物有 、 和KCl。
下列说法错误的是
A.“升温回流”的目的是使氯气逸出
B.“结晶过滤”所得滤液的主要成分是KCl
C.“系列操作”为蒸发结晶、过滤、乙醇洗涤
D. 还可以通过电解KI溶液制备,电解前后溶液的pH不变
14.氯化磷酸三钠 具有良好的灭菌、消毒、漂白作用,亦
资料收集整理【淘宝店铺:向阳百分百】能除去墨迹、血迹、油迹和茶迹等多种污垢,广泛地用于医院、餐馆、食品加工行业。
氯化磷酸三钠的熔点为67℃,常温下较稳定,受热易分解。在水溶液中可直接与钙、
镁及重金属离子形成不溶性磷酸盐。某小组设计如图流程制备氯化磷酸三钠。下列叙
述错误的是
A.理论上制得的氯化磷酸三钠不超过
B.“反应池1”中最少应加入 磷酸溶液
C.“系列操作”包括蒸发浓缩、降温结晶、过滤、洗涤和高温烘干
D.氯化磷酸三钠因含 而具有漂白、杀菌和消毒作用
15.用含少量 的废铁屑制备三草酸合铁酸钾晶体 ,流程如图。
已知:① 为蓝绿色晶体, 为黄色晶体,
为翠绿色晶体。
② 时,
下列说法错误的是
A.试剂 和 分别为稀硫酸、氨水
B.“反应I”的离子方程式为:
C.“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤(乙醇)、干燥
D.可以用KSCN溶液检测所得晶体中铁元素的价态
16.醋酸亚铬[(CH COO) Cr·H O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分
3 2 2
析中常用作氧气吸收剂。一般制备方法:先在封闭体系中利用金属锌作还原剂,将铬
(Ⅲ)还原为铬(Ⅱ);铬(Ⅱ)再与醋酸钠溶液作用可制得醋酸亚铬。实验装置如图所示,
资料收集整理【淘宝店铺:向阳百分百】则下列说法不正确的是
A.实验中所用蒸馏水均需经煮沸后迅速冷却,目的是去除溶解氧,防止铬(Ⅱ)被
氧化
B.将过量锌粒和氯化铬固体置于c装置中,加入少量蒸馏水,按图连接好装置,
关闭K,打开K、K,可以利用产生的H 排净体c装置内的空气
3 1 2 2
C.当b装置中导管末端产生稳定持续的气流后,打开K,关闭K、K,利用压
3 2 1
强差可以将c装置中溶液压入d装置
D.d装置中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是:蒸发
浓缩、趁热过滤、洗涤、干燥,从而在d装置中得到纯净的(CHCOO) Cr·H O
3 2 2
17.正高碘酸 是白色结晶性粉末,溶于水,主要用作氧化剂和分析试剂。由
制取 的实验流程如图所示:
下列说法错误的是
A.“反应1”是为了将 转化为
B.“反应2”中发生的反应是
C.“反应3”的滤液中含有大量的 等
D.“反应4”得到的无色气体可能是氧气
18.草酸亚铁晶体是生产感光材料的原料 ,制
备流程如下:
资料收集整理【淘宝店铺:向阳百分百】下列说法错误的是
A.可用 溶液检验 是否变质
B.步骤①酸化的目的是抑制 的水解
C.步骤②反应为
D.步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
19.工业中制取高铁酸钾( ),是先制取高铁酸钠,然后在低温下,往高铁酸钠
溶液中加入 至饱和就可以析出高铁酸钾。
湿法制备 ,的主要反应为: ;
干法制备 ,的主要反应为:
。
下列有关说法不正确的是
A.湿法和干法制备中,生成质量相同的 转移电子数目相同
B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小
C.干法制备的主要反应中 既是氧化剂又是还原剂
D. 处理水时,既能杀菌消毒,生成的 胶体还能吸附水中的悬浮杂
质
20.混合物的分离提纯在生产、生活中有着重要的意义。已知某工业废水中含有大量
的FeSO ,还可能含有较多的Fe3+、OH-、Ba2+、Cu2+,以及部分污泥,通过下列流程
4
可从该废水中回收FeSO ·7H O晶体及固体单质。已知氧化性:Fe3+>Cu2+。下列说法
4 2
不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.步骤1采用了过滤操作
B.根据步骤2中得到固体混合物可以确定Cu2+一定存在
C.步骤3中加入的试剂X为稀盐酸
D.步骤4中涉及的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥
资料收集整理【淘宝店铺:向阳百分百】