文档内容
专项训练 氢键与物质的性质
一、单选题
1.下列说法正确的是
I I I I I I I
1 2 3 4 5 6 7
57 1483
1817 2745 11575 18376 23293
8 0
A.杂化轨道全部参与形成化学键
B.元素周期表中19~36号元素,有2个单电子的元素有4种
C.氢键X-H•••Y的3个原子一定在一条直线上
D.某主族元素的电离能I~I 数据如表所示(单位:kJ•mol-1),可推测该元素位于元
1 7
素周期表第VA族
2.下列说法正确的是
A.甲醇、甲醛都存在分子之间氢键
B.第一电离能在Al和P之间的元素有2种
C.分子空间构型V形,中心原子可能发生sp2杂化或sp3杂化
D.气体单质中,一定有σ键,可能有π键
3.下列说法正确的是
A.干冰熔化时破坏了共价键
B.液态HI受热分解过程中,只破坏分子间作用力
C.水在液态时,除了单个水分子,还有几个水分子通过氢键结合而形成的缔合水
分子(HO)n的存在
2
D.NaHSO 溶于水时,离子键被破坏,共价键不受影响
4
4.下列关于物质性质的解释合理的是
选
物质性质 解释
项
A 氨水中存在 是离子化合物
石墨的导电性只能沿石 相邻碳原子平面之间相隔较远,电子不能从一个平
B
墨平面的方向 面跳跃到另一个平面
C 氯化银能溶于氨水 接受 的孤对电子形成配位键
沸点:对羟基苯甲酸> 前者主要形成分子内氢键,后者主要形成分子间氢
D
邻羟基苯甲酸 键,前者分子间作用力较大
A.A B.B C.C D.D
5.下列有关有机物的叙述正确的是
A.能与新制氢氧化铜共热产生砖红色沉淀的物质一定是醛类
资料收集整理【淘宝店铺:向阳百分百】B.淀粉、纤维素都是天然高分子化合物,也是人类必需的营养物质
C.甲醇、乙酸、葡萄糖都能与水形成氢键
D.聚乙烯、聚乙炔都不能使溴水褪色
6. 是微电子工业中常用的等离子刻蚀气体,遇水发生反应:
。下列有关说法错误的是
A.第一电离能:N>F>H B.电负性:F>N>H
C.基态N原子的电子排布式为 D. 、HF分子间均能形成氢键
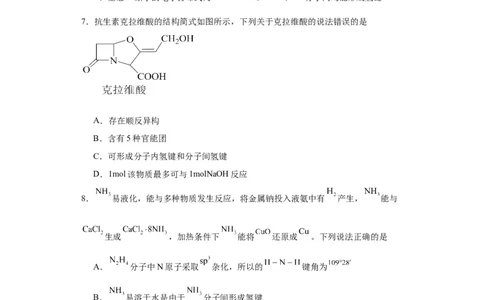
7.抗生素克拉维酸的结构简式如图所示,下列关于克拉维酸的说法错误的是
A.存在顺反异构
B.含有5种官能团
C.可形成分子内氢键和分子间氢键
D.1mol该物质最多可与1molNaOH反应
8. 易液化,能与多种物质发生反应,将金属钠投入液氨中有 产生, 能与
生成 ,加热条件下 能将 还原成 。下列说法正确的是
A. 分子中N原子采取 杂化,所以的 键角为
B. 易溶于水是由于 分子间形成氢键
C. 与 反应生成的白烟成分为
D.金属钢与液氮反应体现了 的还原性
9.我国建成全球首套千吨级液态太阳能燃料合成示范装置,其原理如图所示。下列说
法正确的是
资料收集整理【淘宝店铺:向阳百分百】A. 中 键和 键个数比是
B.反应Ⅰ和Ⅱ中均存在极性键的断裂和形成
C. 和 中碳原子的杂化方式不同
D. 沸点比水低,说明 分子间不存在氢键
10.下列说法不正确的是
A.食品中添加适量的 可起到漂白、防腐和抗氧化等作用
B. 具有强氧化性,可用作消毒剂
C.钛的合金与人体“相容性”好,可用于制造人造骨骼
D. 分子间存在较多的氢键,液氨常用作制冷剂
11.胆矾( )是一种重要的盐,在电镀、印染、颜料、农药等领域都有着
广泛的应用,可写作 ,其结构如图1,胆矾溶于水可得 溶
液,如图2所示,向 溶液中逐滴加入浓氨水至过量,得到透明的深蓝色溶液,
其溶质为 ,再向其中加入乙醇,可析出深蓝色的晶体,其组成为
,下列有关说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.由图1知胆矾中的水在不同温度下会分步失去
B.胆矾晶体中存在离子键、共价键、氢键及范德华力
C.该实验证明配离子 比 稳定
D.加入乙醇能使 在水中的溶解度减小
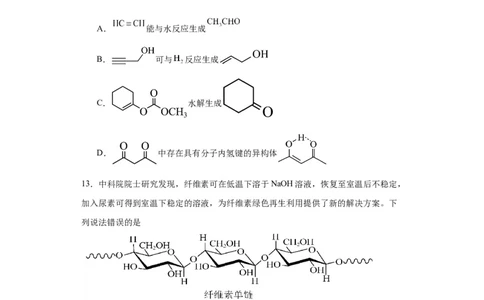
12.下列事实不涉及烯醇式与酮式互变异构原理的是
A. 能与水反应生成
B. 可与 反应生成
C. 水解生成
D. 中存在具有分子内氢键的异构体
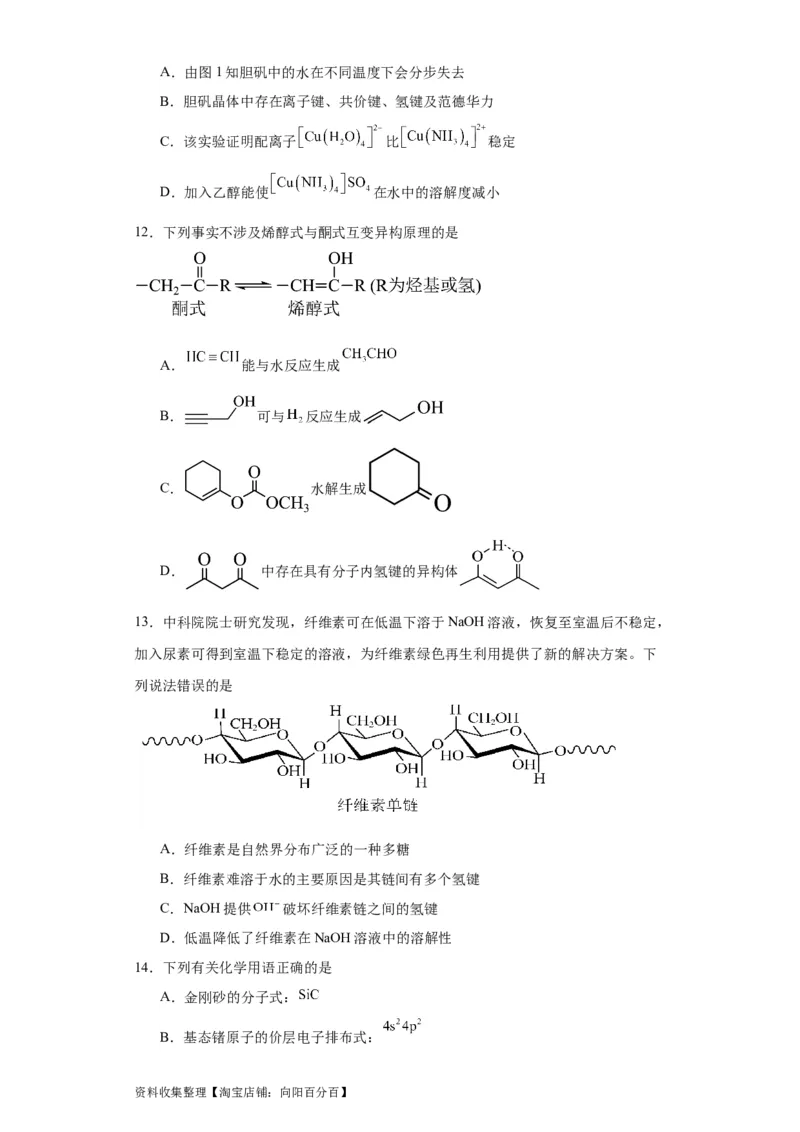
13.中科院院士研究发现,纤维素可在低温下溶于NaOH溶液,恢复至室温后不稳定,
加入尿素可得到室温下稳定的溶液,为纤维素绿色再生利用提供了新的解决方案。下
列说法错误的是
A.纤维素是自然界分布广泛的一种多糖
B.纤维素难溶于水的主要原因是其链间有多个氢键
C.NaOH提供 破坏纤维素链之间的氢键
D.低温降低了纤维素在NaOH溶液中的溶解性
14.下列有关化学用语正确的是
A.金刚砂的分子式:
B.基态锗原子的价层电子排布式:
资料收集整理【淘宝店铺:向阳百分百】C.邻羟基苯甲醛分子内氢键示意图:
D. 分子的球棍模型:
15.一种可吸附甲醇的材料,其化学式为 ,部分晶体结构
如下图所示,其中 为平面结构。
下列说法正确的是
A.该晶体中存在N-H…O氢键 B.基态原子的第一电离能:
C.基态原子未成对电子数: D.晶体中B、N和O原子轨道的杂化类
型相同
16.化合物M是一种新型超分子晶体材料,由X、18-冠-6、HClO 以CHCOCH 为
4 3 3
溶剂反应制得(如图)。下列叙述正确的是
A.组成M的元素均位于元素周期表p区
B.M中碳、氮、氯原子的轨道杂化类型均为sp3
C.M由X的高氯酸盐与18-冠-6通过氢键结合生成
D.M的阴离子的空间结构为正方形
17.周期表中ⅢA族单质及其化合物应用广泛。 极易水解生成 ( 在水中
完全电离为 和 )和硼酸( ),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓
资料收集整理【淘宝店铺:向阳百分百】硫酸存在下生成挥发性的硼酸甲酯[ ],硼酸甲酯主要用作热稳定剂、木材防
腐剂等。高温下 和焦炭在氯气的氛围中获得 。GaN的结构与晶体硅类似,
是第三代半导体研究的热点。铊(Tl)位于元素周期表中第6周期,于1861年发现。下
列说法正确的是
A.硼酸电离方程式:
B. 分子间能形成氢键
C.Tl原子基态外围电子排布式为
D.GaN属于分子晶体
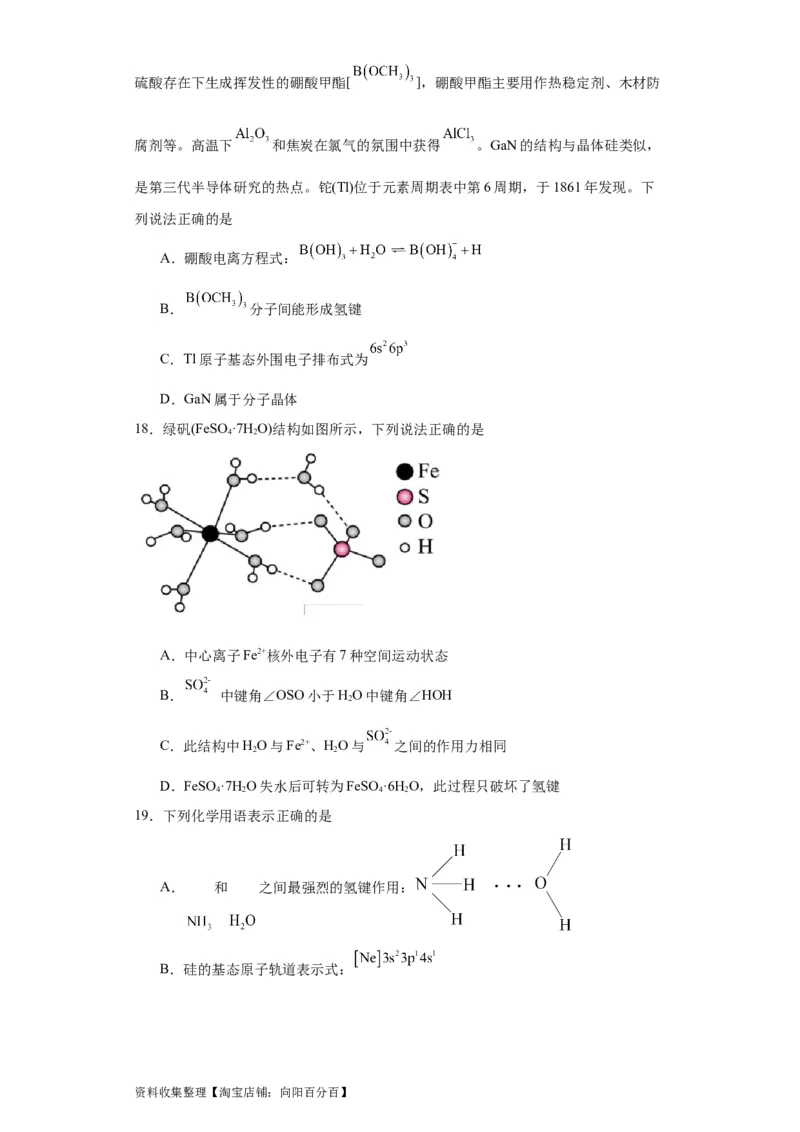
18.绿矾(FeSO ·7H O)结构如图所示,下列说法正确的是
4 2
A.中心离子Fe2+核外电子有7种空间运动状态
B. 中键角∠OSO小于HO中键角∠HOH
2
C.此结构中HO与Fe2+、HO与 之间的作用力相同
2 2
D.FeSO ·7H O失水后可转为FeSO ·6H O,此过程只破坏了氢键
4 2 4 2
19.下列化学用语表示正确的是
A. 和 之间最强烈的氢键作用:
B.硅的基态原子轨道表示式:
资料收集整理【淘宝店铺:向阳百分百】C. 中 的化合价: 价
D. 的电子式:
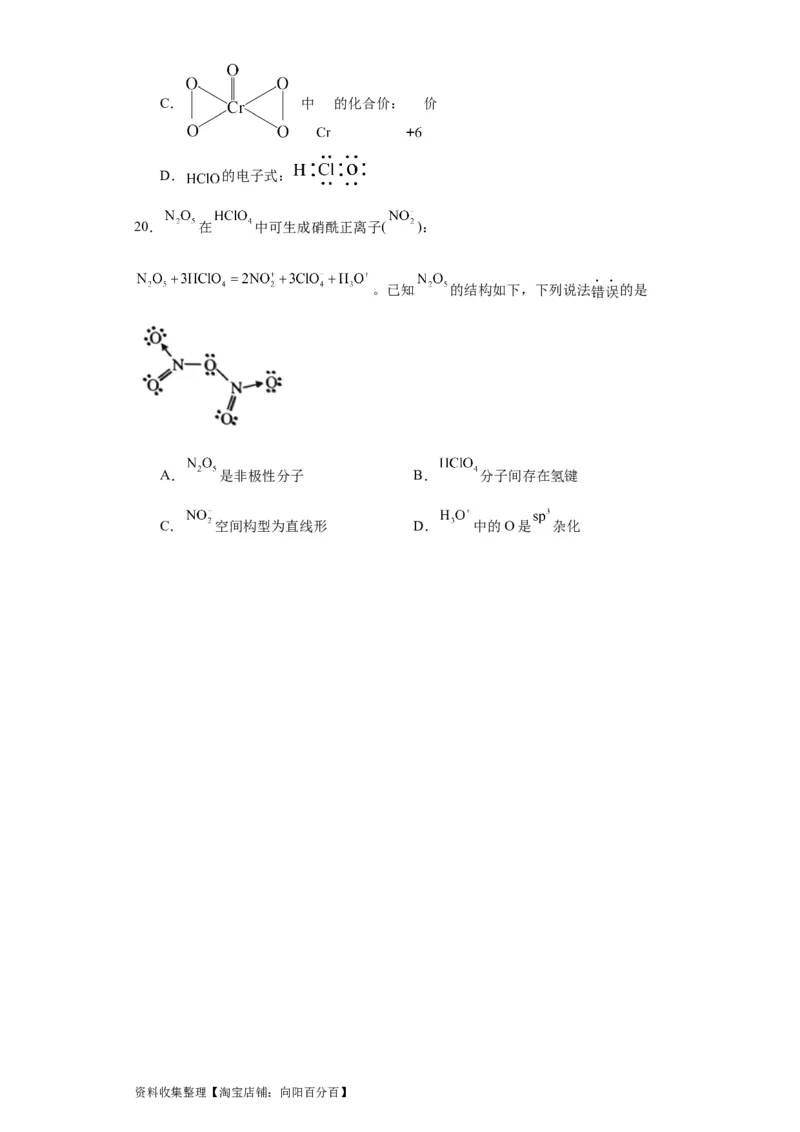
20. 在 中可生成硝酰正离子( ):
。已知 的结构如下,下列说法错误的是
A. 是非极性分子 B. 分子间存在氢键
C. 空间构型为直线形 D. 中的O是 杂化
资料收集整理【淘宝店铺:向阳百分百】