文档内容
专项训练 氧族元素及其化合物(解析版)
一、单选题
1.硫酸是当今世界上最重要的化工产品之一、目前工业制备硫酸主要采用接触法,常
见的有硫铁矿制酸、硫磺制酸等。以硫铁矿 ( )为原料制备硫酸的主要设备有:沸
腾炉、接触室、吸收塔。硫酸工业、金属冶炼产生的尾气中含有 ,需经回收利用
处理才能排放到空气中。下列有关化学反应表示不正确的是
A.煅烧硫铁矿获得 :
B.接触室中 被氧化:
C.用少量氨水吸收尾气中的 :
D. 与 溶液反应的离子方程式:
2.根据实验操作和和现象得出的结论正确的是
选
实验操作和和现象 结论
项
在试管中加入10mL溴水和5mL正己烷。将试管在光照下振 正己烷与溴在
A 荡后静置,溶液分层,上、下两层液体几乎均是无色的,用 光照下发生取
玻璃棒蘸取浓氨水伸入试管内液面上方,有白烟出现 代反应
铜与浓硫酸反
B 铜与浓硫酸反应后的试管中加蒸馏水稀释,溶液变蓝色 应有CuSO 生
4
成
该溶液中一定
C 用铂丝蘸取某溶液在酒精灯外焰上灼烧,火焰呈黄色 含有Na+,不含
K+
某溶液中加入AgNO 溶液有白色沉淀生成,加盐酸沉淀不 该溶液中一定
D 3
溶解 有Cl-
A.A B.B C.C D.D
3.实验室常利用难挥发性酸制备易挥发性酸的原理,用浓硫酸与硝石(NaNO )反应制
3
备HNO 反应装置如图,下列说法不正确的是
3
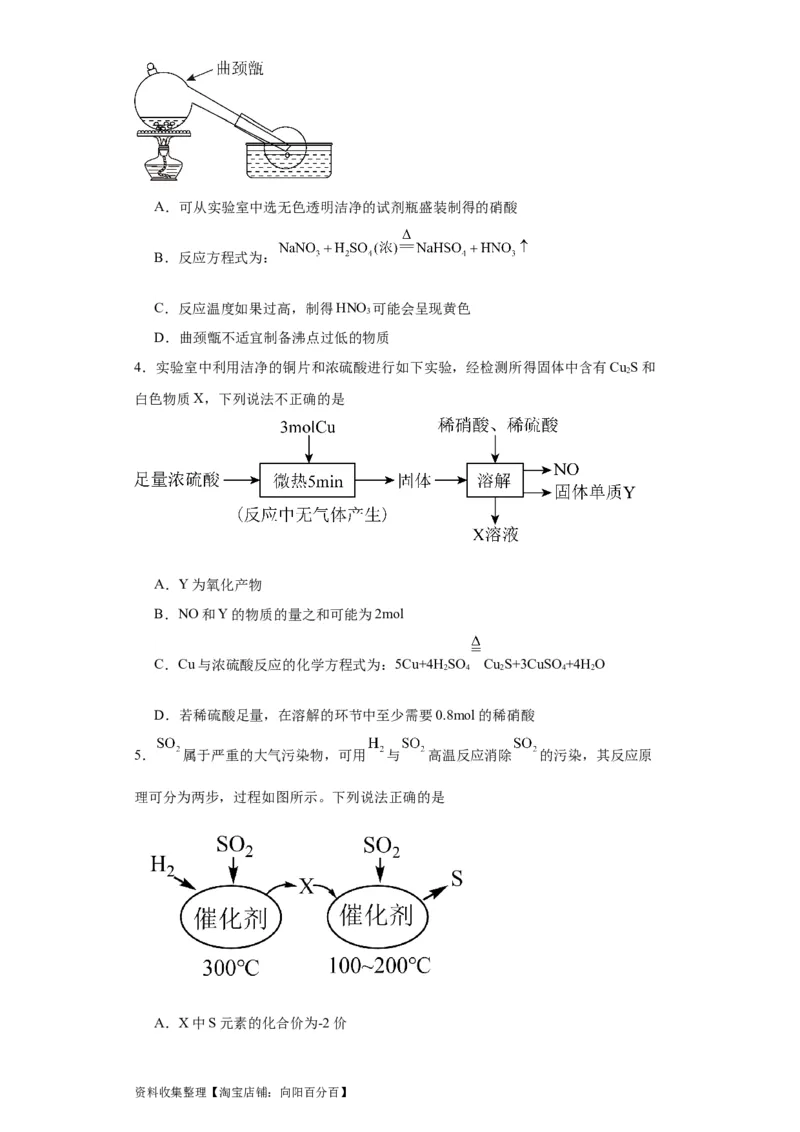
资料收集整理【淘宝店铺:向阳百分百】A.可从实验室中选无色透明洁净的试剂瓶盛装制得的硝酸
B.反应方程式为:
C.反应温度如果过高,制得HNO 可能会呈现黄色
3
D.曲颈甑不适宜制备沸点过低的物质
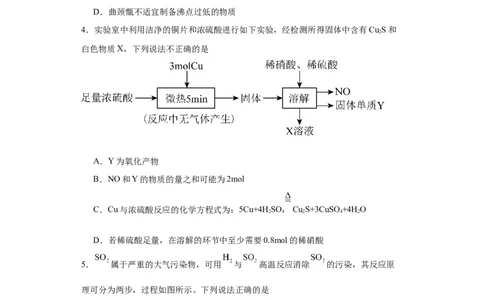
4.实验室中利用洁净的铜片和浓硫酸进行如下实验,经检测所得固体中含有Cu S和
2
白色物质X,下列说法不正确的是
A.Y为氧化产物
B.NO和Y的物质的量之和可能为2mol
C.Cu与浓硫酸反应的化学方程式为:5Cu+4H SO Cu S+3CuSO+4H O
2 4 2 4 2
D.若稀硫酸足量,在溶解的环节中至少需要0.8mol的稀硝酸
5. 属于严重的大气污染物,可用 与 高温反应消除 的污染,其反应原
理可分为两步,过程如图所示。下列说法正确的是
A.X中S元素的化合价为-2价
资料收集整理【淘宝店铺:向阳百分百】B.大气中的 必须氧化成 才能形成酸雨
C.在100~200℃温度时发生的是置换反应
D.工业上可用浓硝酸处理工业尾气中的
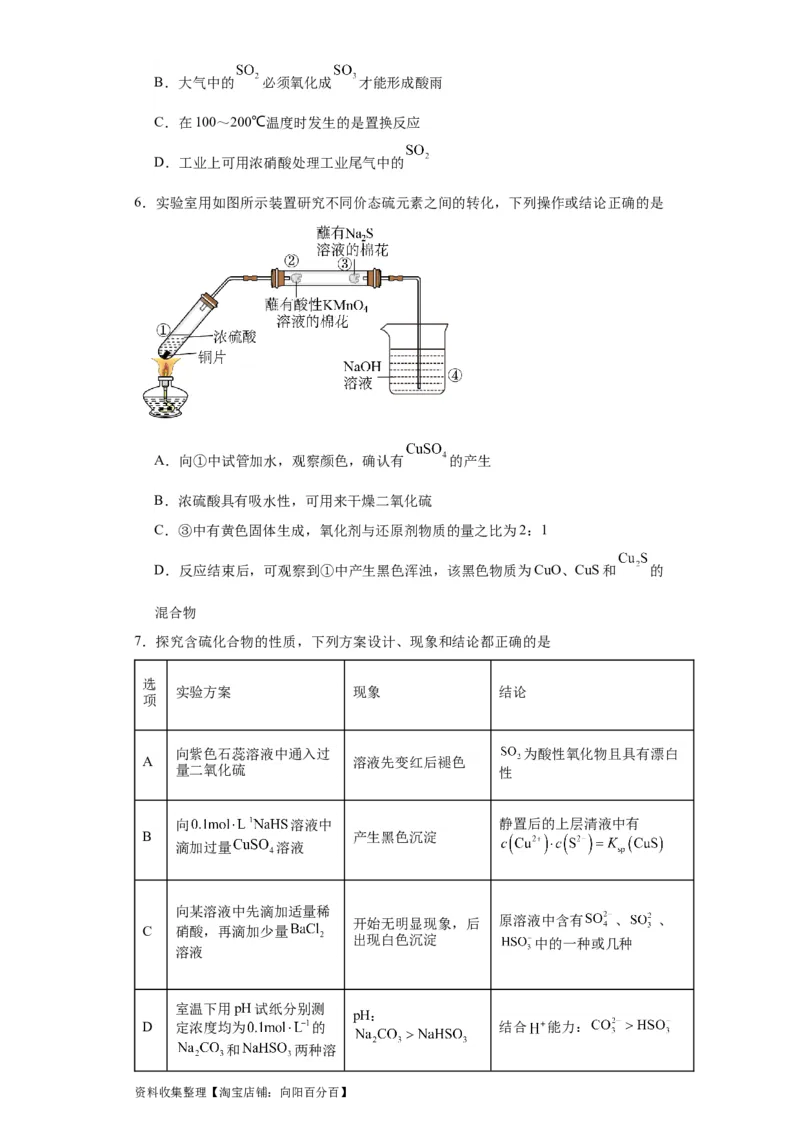
6.实验室用如图所示装置研究不同价态硫元素之间的转化,下列操作或结论正确的是
A.向①中试管加水,观察颜色,确认有 的产生
B.浓硫酸具有吸水性,可用来干燥二氧化硫
C.③中有黄色固体生成,氧化剂与还原剂物质的量之比为2:1
D.反应结束后,可观察到①中产生黑色浑浊,该黑色物质为CuO、CuS和 的
混合物
7.探究含硫化合物的性质,下列方案设计、现象和结论都正确的是
选
实验方案 现象 结论
项
向紫色石蕊溶液中通入过 为酸性氧化物且具有漂白
A 溶液先变红后褪色
量二氧化硫 性
向 溶液中 静置后的上层清液中有
B 产生黑色沉淀
滴加过量 溶液
向某溶液中先滴加适量稀
开始无明显现象,后 原溶液中含有 、 、
C 硝酸,再滴加少量
出现白色沉淀 中的一种或几种
溶液
室温下用pH试纸分别测
pH:
D 定浓度均为 的 结合 能力:
和 两种溶
资料收集整理【淘宝店铺:向阳百分百】液的pH
A.A B.B C.C D.D
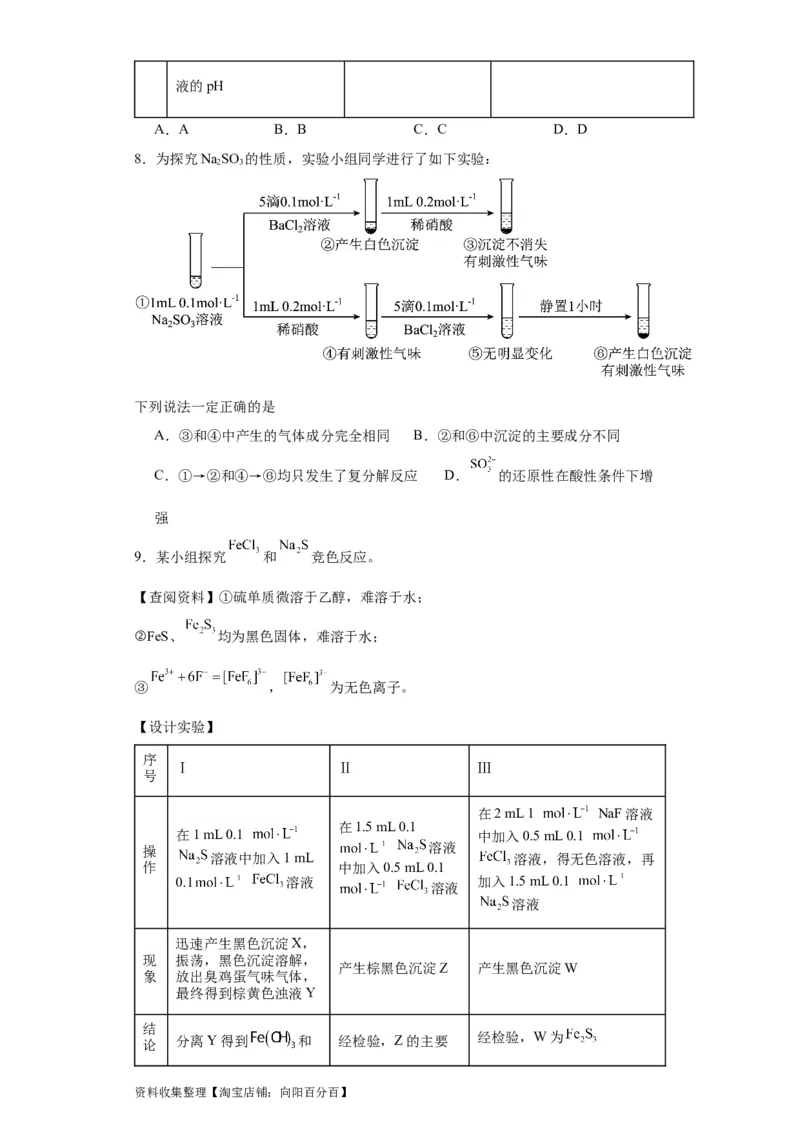
8.为探究NaSO 的性质,实验小组同学进行了如下实验:
2 3
下列说法一定正确的是
A.③和④中产生的气体成分完全相同 B.②和⑥中沉淀的主要成分不同
C.①→②和④→⑥均只发生了复分解反应 D. 的还原性在酸性条件下增
强
9.某小组探究 和 竞色反应。
【查阅资料】①硫单质微溶于乙醇,难溶于水;
②FeS、 均为黑色固体,难溶于水;
③ , 为无色离子。
【设计实验】
序
Ⅰ Ⅱ Ⅲ
号
在2 mL 1 NaF溶液
在1.5 mL 0.1
在1 mL 0.1 中加入0.5 mL 0.1
操 溶液
溶液中加入1 mL 溶液,得无色溶液,再
作 中加入0.5 mL 0.1
0.1 溶液 加入1.5 mL 0.1
溶液
溶液
迅速产生黑色沉淀X,
现 振荡,黑色沉淀溶解,
产生棕黑色沉淀Z 产生黑色沉淀W
象 放出臭鸡蛋气味气体,
最终得到棕黄色浊液Y
结
分离Y得到 和 经检验,Z的主要 经检验,W为
论
资料收集整理【淘宝店铺:向阳百分百】成分是 ,含少
S
量
下列推断正确的是
A.黑色沉淀X溶解只发生复分解反应
B.实验Ⅱ不生成S可能是氧化还原速率较大
C.生成黑色沉淀W的反应为
D.实验Ⅲ得到 的原因是NaF降低了 的浓度,使氧化还原反应的趋势减
小
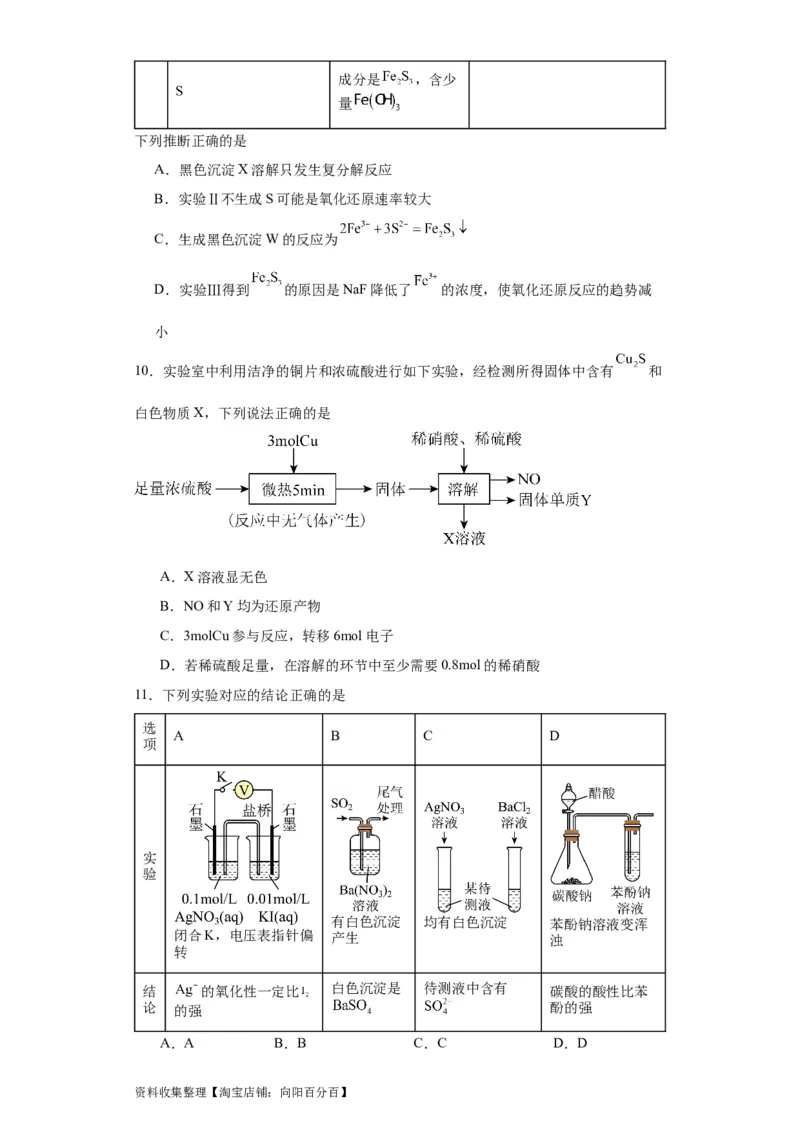
10.实验室中利用洁净的铜片和浓硫酸进行如下实验,经检测所得固体中含有 和
白色物质X,下列说法正确的是
A.X溶液显无色
B.NO和Y均为还原产物
C.3molCu参与反应,转移6mol电子
D.若稀硫酸足量,在溶解的环节中至少需要0.8mol的稀硝酸
11.下列实验对应的结论正确的是
选
A B C D
项
实
验
有白色沉淀 均有白色沉淀 苯酚钠溶液变浑
闭合K,电压表指针偏 产生 浊
转
结 的氧化性一定比 白色沉淀是 待测液中含有 碳酸的酸性比苯
论 的强 酚的强
A.A B.B C.C D.D
资料收集整理【淘宝店铺:向阳百分百】12. 俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品
工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目
的、实验操作或现象得到的相关离子方程式正确的是
选
实验目的 实验操作或现象 相关离子方程式
项
实验室用 通入
和 的
A 制备
混合溶液中来制备
取少量样品溶于
检验硫代硫酸
水,先加入过量稀
钠氧化变质可
B 盐酸,再滴加
能混有的
溶液,有沉
淀生成
分别将两种反应溶
探究温度对硫
液先混合,再水浴
代硫酸钠与硫
C 加热至反应要求温
酸反应速率的
度,测得该温度下
影响
的反应速率
用过量硫代硫
D 酸钠除去水中 黄绿色褪去
溶解的氯气
A.A B.B C.C D.D
13.煤燃烧排放的烟气含有SO 和NO ,是大气的重要污染源之一、用Ca(ClO) 溶液
2 x 2
对模拟烟气[n(NO):n(SO )=2:3]同时进行脱硝脱硫,分别生成NO 、SO 。NO、SO
2 2
脱除率与时间关系如图所示,下列说法不正确的是
A.脱除NO的反应:2NO+3ClO-+H O=2H++2NO +3Cl-
2
B.依图信息,在80min时,吸收液中n(SO ):n(Cl-)=1:1
资料收集整理【淘宝店铺:向阳百分百】C.SO 脱除率高于NO的原因可能是SO 在水中的溶解度大于NO
2 2
D.随着脱除反应的进行,吸收剂溶液的H+浓度增大
14.连二亚硫酸钠(Na SO)俗称保险粉,有强还原性,在空气中极易被氧化。用
2 2 4
NaHSO 还原法制备保险粉的流程如图所示。下列说法正确的是
3
A.反应1的离子方程式为
B.反应1结束后,可用盐酸酸化的BaCl 溶液检验NaHSO 是否被氧化
2 3
C.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2
D.反应2以及结晶脱水均可在空气中进行
15.科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意
图如图。下列说法错误的是
A.氧化性:NO >SO ,还原性:SO >HNO
2 2
B.第II、III阶段总的化学方程式为:SO +H O+NO =HNO +HSO
2 2 2
C.NO 在所有过程中都是被还原
2
D.上述反应过程中,S的成键数目保持不变
16.硫元素的含氧酸根离子,有如下转化关系。
①
②
③
资料收集整理【淘宝店铺:向阳百分百】④
下列说法正确的是
A.反应③中每消耗4.5gH O同时生成40.5g
2
B.反应④中表现了+2价硫元素的强氧化性
C.上述反应中 都只表现了还原性
D.反应②中每消耗2.8g SO 转移电子数为0.05N
2 A
17.烟气脱硫能有效减少 的排放。实验室用粉煤灰(主要含 、 等)制备碱
式硫酸铝 溶液,并用于烟气脱硫。下列说法不正确的是
A.上述过程中,所得滤渣Ⅰ和滤渣II的主要成分分别为 、
B.调pH时,若pH偏高,则所得碱式硫酸铝中x将偏小
C.碱式硫酸铝溶液吸收 后再热分解放出 ,所得溶液中 将减小
D.碱式硫酸铝溶液经多次循环吸收 后,可加入 粉末再生
二、多选题
18.二氯化二硫 是一种黄红色液体,常用作橡胶的低温硫化剂和粘结剂。
分子中各原子最层均有8个电子。 遇水反应会产生淡黄色沉淀和刺激性气
味气体。下列说法不正确的是
A. 可能使品红溶液褪色
B. 的结构式为Cl-S-S-Cl
C. 与水反应时,氧化产物与还原产物的物质的量之比为1:2
资料收集整理【淘宝店铺:向阳百分百】D.将 气体通入 溶液中,若有白色沉淀产生,则 气体中有HCl
19.某同学按图示装置进行实验,向抽滤瓶溶液中通入足量a气体获得a的饱和溶液,
再通入足量的b气体,抽滤瓶中最终一定得到沉淀。下列物质组合符合要求的是
a b c
A 饱和食盐水
B 溶液
C 溶液
D 溶液
A.A B.B C.C D.D
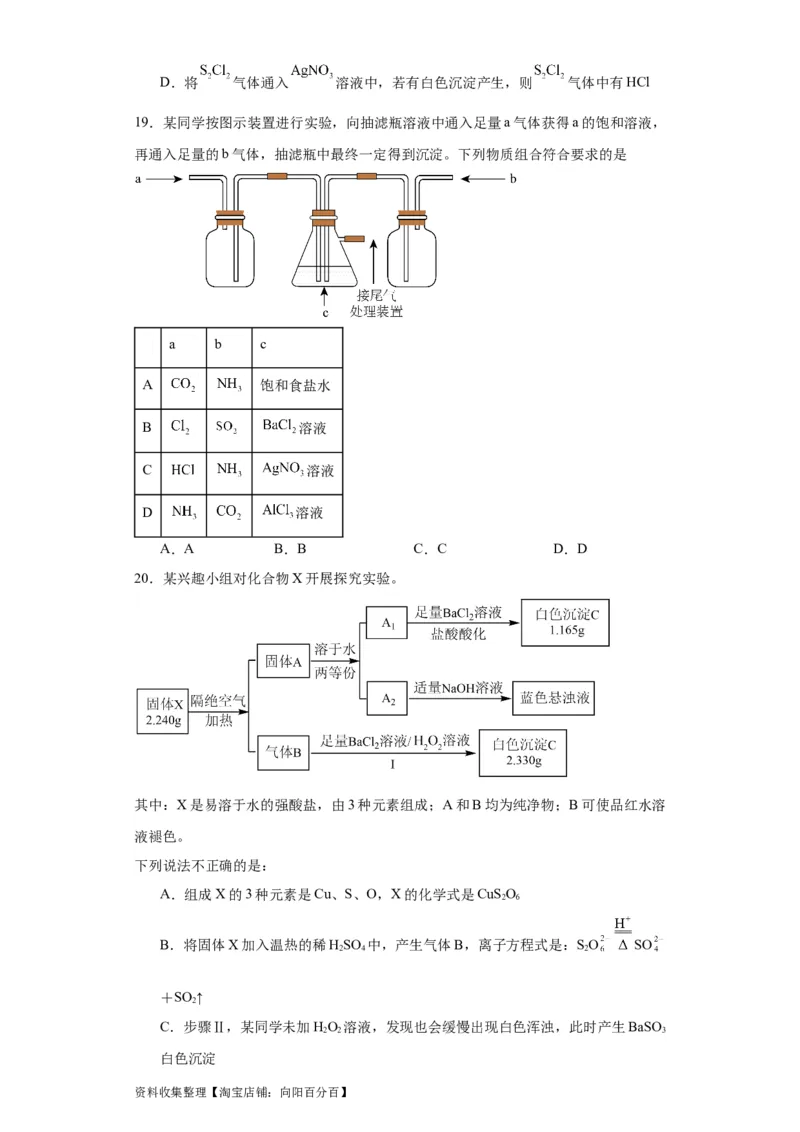
20.某兴趣小组对化合物X开展探究实验。
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶
液褪色。
下列说法不正确的是:
A.组成X的3种元素是Cu、S、O,X的化学式是CuSO
2 6
B.将固体X加入温热的稀HSO 中,产生气体B,离子方程式是:SO SO
2 4 2
+SO ↑
2
C.步骤Ⅱ,某同学未加HO 溶液,发现也会缓慢出现白色浑浊,此时产生BaSO
2 2 3
白色沉淀
资料收集整理【淘宝店铺:向阳百分百】D.气体B通入石蕊试液,溶液先变红后褪色,体现了B的水溶液具有酸性和漂白
性
资料收集整理【淘宝店铺:向阳百分百】