文档内容
专项训练 速率方程的有关计算
一、填空题
1. 是一种常用的还原剂。一定条件下,反应
的速率方程为 (k为速率常数,只与温度、催化剂有关。与浓度无
关)。某温度下,该反应在不同浓度下反应速率如下表所示:
反应速率
① 0.10 0.10
② 0.20 0.10 2
③ 0.20 0.20 4
(1)根据表中测定结果,推断出a= 、b= 。
(2)改变下列反应条件,反应速率增大的是___________(填字母)。
A.降温 B.缩小体积 C.加入催化剂 D.减压
2.我国力争于2030年前做到碳达峰,2060年前实现碳中和,因此,研发二氧碳利用
技术,降低空气中二氧化碳含量成为研究热点。在一定催化剂催化作用下CO 加氢合
2
成甲酸发生反应如下:CO(g)+H(g) HCOOH(g) ΔH =-30.9kJ/mol
2 2 1
(1)温度为T℃时,该反应平衡常数K=2,将等物质的量的CO 和H 充入体积为1L的
1 2 2
密闭容器中,实验测得:v =k ·c(CO)·c(H),v =k ·c(HCOOH),k 、k 为速率常
正 正 2 2 逆 逆 正 逆
数。T℃时,k = k 。
1 逆 正
(2)当温度改变为T℃时,k =1.9 k ,则T℃时平衡压强 (填“>”“<”或
2 正 逆 2
“=”) T ℃时平衡压强。
1
(3)该反应的 Arrhenius经验公式的实验数据如图中的曲线d所示,已知 Arrhenius经验
公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数),则该反应的活化能
Ea= kJ/mol。改变外界条件,实验数据如图中的曲e所示,则实验可能改变
的外界条件是 。
资料收集整理【淘宝店铺:向阳百分百】3.碘蒸气存在能大幅度提高NO的分解速率,反应历程为:
2
第一步:I(g)→2I(g)(快反应)
2
第二步:I(g)+NO(g)→N (g)+IO(g)(慢反应)
2 2
第三步:IO(g)+NO(g)→N (g)+O(g)+I(g)(快反应)
2 2 2 2
(1)实验表明,含碘时NO分解速率方程v=k·c(N O)·[c(I )]0.5(k为速率常数)。下列表
2 2 2
述正确的是_______。
A.NO分解反应中,k值与碘蒸气浓度大小有关
2
B.v(第二步的逆反应)<v(第三步反应)
C.IO为反应的催化剂
D.第二步活化能比第三步大
(2)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净
化装置中CO和NO发生反应2NO(g)+2CO(g) N(g)+2CO(g) ΔH=-746.8kJ-mol-1.实
2 2
验测得:v =k ·p2(NO)·p2(CO),v =k ·p(N )·p2(CO)。其中k 、k 分别为正、逆反
正 正 逆 逆 2 2 正 逆
应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
①达到平衡后,仅升高温度,k 增大的倍数 (填“大于”“小于”或“等
正
于”)k 增大的倍数。
逆
②一定温度下在刚性密闭容器中充入CO、NO和N 物质的量之比为2:2:1,压强为
2
PkPa。达平衡时压强为0.9P kPa,则平衡时CO的转化率为 , 。
0 0
4. 一定温度下,固定容积的密闭容器中发生反应: 。
其中,正、逆反应速率分别满足以下关系: ( 、
表示速率常数,与温度有关)
资料收集整理【淘宝店铺:向阳百分百】①若该温度下平衡常数K=10,则 ,升高温度, 增大的倍数
(填“大于”“小于”或“等于”) 增大的倍数。
②在该条件下反应达平衡后,再充入一定量的 ,则 (填“变
大”、“变小”或“不变”)。
5.氮气转化为氮的化合物对于工业制备硝酸有着重要的意义。回答下列问题。
(1)
某反应(假设只涉及气体)的平衡常数表达式为 ,则该反应
的热化学方程式为 。
(2)已知反应 的速率方程为 ,
,其中 、 是正、逆反应的速率常数,只与温度有关,且
随温度升高而增大。 温度下,在2L恒容密闭容器中充入一定量 气体发生上述
反应,测得容器中不同时刻 如表所示:
时间/s 0 1 2 3 4 5
2.00 1.60 1.32 1.14 1.00 1.00
①1~4s内该反应的平均反应速率 。
② 温度下达到化学平衡时, 。
③若将容器的温度改为 ,其他条件不变, ,则 (填“<”“>”或
“=”)。
6.温度为T 时,在一个容积均为1L的密闭容器中仅发生反应:
1
资料收集整理【淘宝店铺:向阳百分百】。实验测得: = (NO) =2 (O ) =k
正 消耗 2 消耗 正
c2(NO)·c(O ), = (NO ) =k c2(NO ),k 、k 为速率常数,受温度影响。
2 逆 2 消耗 逆 2 正 逆
物质的起始浓度/mol/L 物质的平衡浓度/mol/L
c(NO) c(O ) c(NO ) c(O )
2 2 2
0.6 0.3 0 0.2
温度为T 时, (填数据);当温度升高为T 时,k 、k 分别增大m倍和n
1 2 正 逆
倍,则m n(填“>”、“<”或“=”)
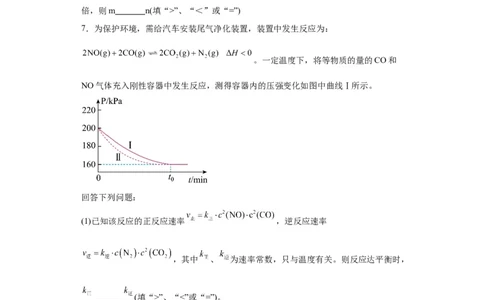
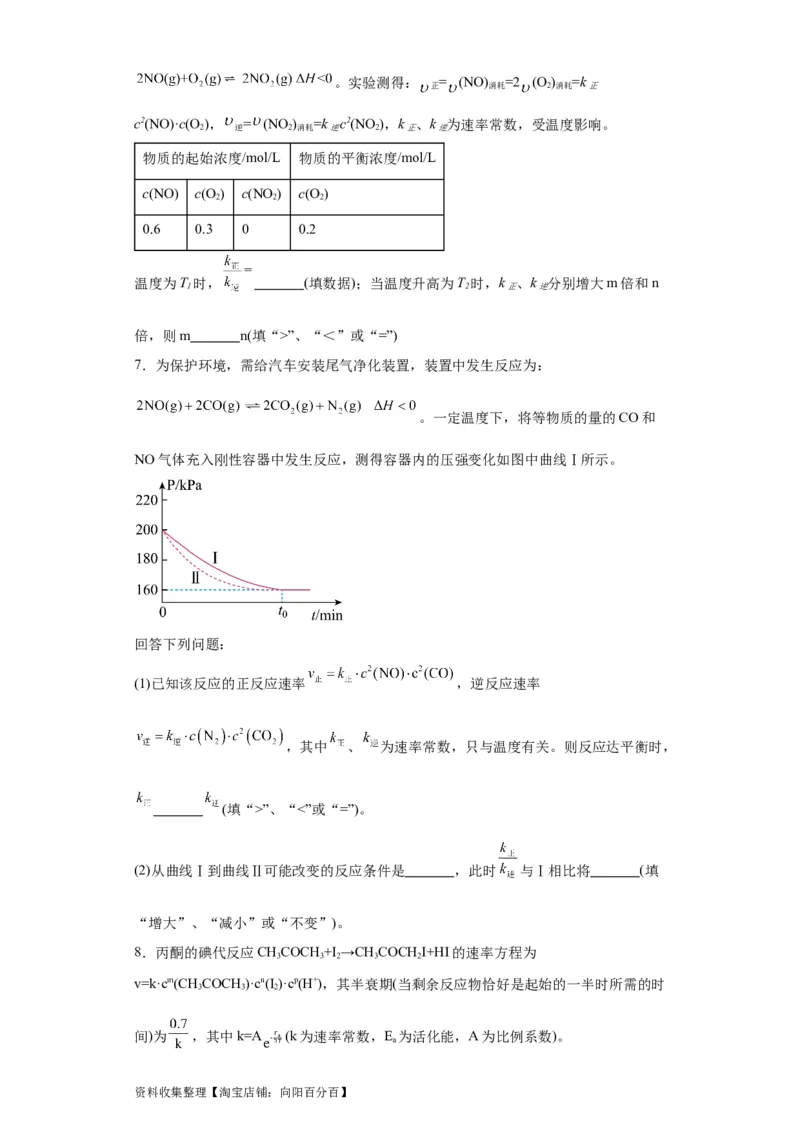
7.为保护环境,需给汽车安装尾气净化装置,装置中发生反应为:
。一定温度下,将等物质的量的CO和
NO气体充入刚性容器中发生反应,测得容器内的压强变化如图中曲线Ⅰ所示。
回答下列问题:
(1)已知该反应的正反应速率 ,逆反应速率
,其中 、 为速率常数,只与温度有关。则反应达平衡时,
(填“>”、“<”或“=”)。
(2)从曲线Ⅰ到曲线Ⅱ可能改变的反应条件是 ,此时 与Ⅰ相比将 (填
“增大”、“减小”或“不变”)。
8.丙酮的碘代反应CHCOCH +I →CHCOCH I+HI的速率方程为
3 3 2 3 2
v=k·cm(CHCOCH )·cn(I)·cp(H+),其半衰期(当剩余反应物恰好是起始的一半时所需的时
3 3 2
间)为 ,其中k=A (k为速率常数,E 为活化能,A为比例系数)。
a
资料收集整理【淘宝店铺:向阳百分百】(1)在保持酸性不变的条件下,改变下列条件时,反应的瞬时速率如表所示。
序
温度 c(CHCOCH )/(mol•L-1) c(I )/(mol•L-1) v/(10-3mol•L-1•min-1)
号 3 3 2
1 T 0.25 0.050 1.4
1
2 T 0.50 0.050 2.8
1
3 T 1.00 0.050 5.6
1
4 T 0.50 0.100 2.8
1
5 T 0.50 0.100
2
①下列关于速率常数k的说法中正确的是 (填标号)。
A.速率常数k只受温度影响
B.加入催化剂,可使k增大
C.可逆反应中的正逆反应速率常数k 和k 相等
正 逆
②当T>T 时,v 2.8mol•L-1•min-1(填:“大于”、“小于”或“等于”)。
2 1 x
③速率方程中:m= ;n= ;k= 。
(2)若T℃时,v=k·cm(CHCOCH )·cn(I)·cp(H+),c(I )、c(CHCOCH )、c(H+)的起始浓度
1 3 3 2 2 3 3
依次是0.01mol•L-1、0.1mol•L-1、0.01mol•L-1。当c(I )的浓度降低为原来一半时,反应
2
速率将 (填:“变大”、“变小”或“不变”)。
(3)在过量的I 存在,c(H+)=1mol•L-1时。反应掉75%的CHCOCH 所需的时间是
2 3 3
min。
9. 一定温度下,向一恒容密闭容器中一入定量CH(g)和HO(g),发生CH(g)+HO(g)
4 2 4 2
CO(g)+3H(g)吸热反应。实验测得速率方程:v =k c(CH)c(HO),v =k
2 正 正 4 2 逆 逆
(CO)c3(H )(k 、k 为正、逆反应速率常数,只与温度、催化剂、固体表面积有关,与
2 正 逆
浓度无关)。
①他条件不变,升高温度.k (填“增大”、“减小”或“不变”,下同);加入催
正
化剂,v 。
逆
②达到平衡时, = (用含k 、k 的代数式表示)。
正 逆
10.乙烯、环氧乙烷是重要的化工原料,用途广泛。
实验测得 2CH=CH (g)+O(g) 2 (g) △H﹤0中,v =k ·c2( ),v =k
2 2 2 逆 逆 正 正
资料收集整理【淘宝店铺:向阳百分百】c2(CH=CH )·c(O)( 为速率常数,只与温度有关)。
2 2 2
(1)反应达到平衡后,仅降低温度,下列说法正确的是_______(填字母)。
A. 均增大,且 增大的倍数更多 B. 均减小,且 减小的倍
数更少
C. 增大、 减小,平衡正向移动 D. 均减小,且 减小的倍数更
少
(2)若在 的密闭容器中充入 和 ,在一定温度下只发生上
述反应,经过 反应达到平衡,体系的压强变为原来的0.875倍,则 内
, 。
11.已知基元反应mA+nB→pC+qD的速率方程为v=kcm(A)cn(B)(k为只与温度有关的速
率常数),一般反应的速率由基元反应中的慢反应决定,反应3ClO-(aq) (aq)
+2Cl-(aq)可能的机理有如下几种:
I、3C1O-→ +2Cl-
II、ClO-→Cl-+O(慢)、O+ClO-→Cl-+O (快)、C1O-+O → (快)
2 2
III、ClO-+ClO-→ +Cl-(慢)、ClO-+ → +Cl-(快)
则机理II的中间体是 。若反应3ClO-(aq) (aq)+2Cl-(aq)的速率方程
为v=kc2(ClO-),则该反应的历程可能是 (填标号)。
12.羰基硫(COS),用于合成除草剂、杀虫剂等,还能作为粮食熏蒸剂。CO、CO 分
2
别与HS反应均能制得COS,反应如下:
2
反应Ⅰ:
反应Ⅱ:
已知:在相同条件下,向两个容积相同且不变的密闭容器中按下表投料(N 不参与反
2
应),分别发生上述反应。温度相同时,反应Ⅰ的平衡常数大于反应Ⅱ的平衡常数。实
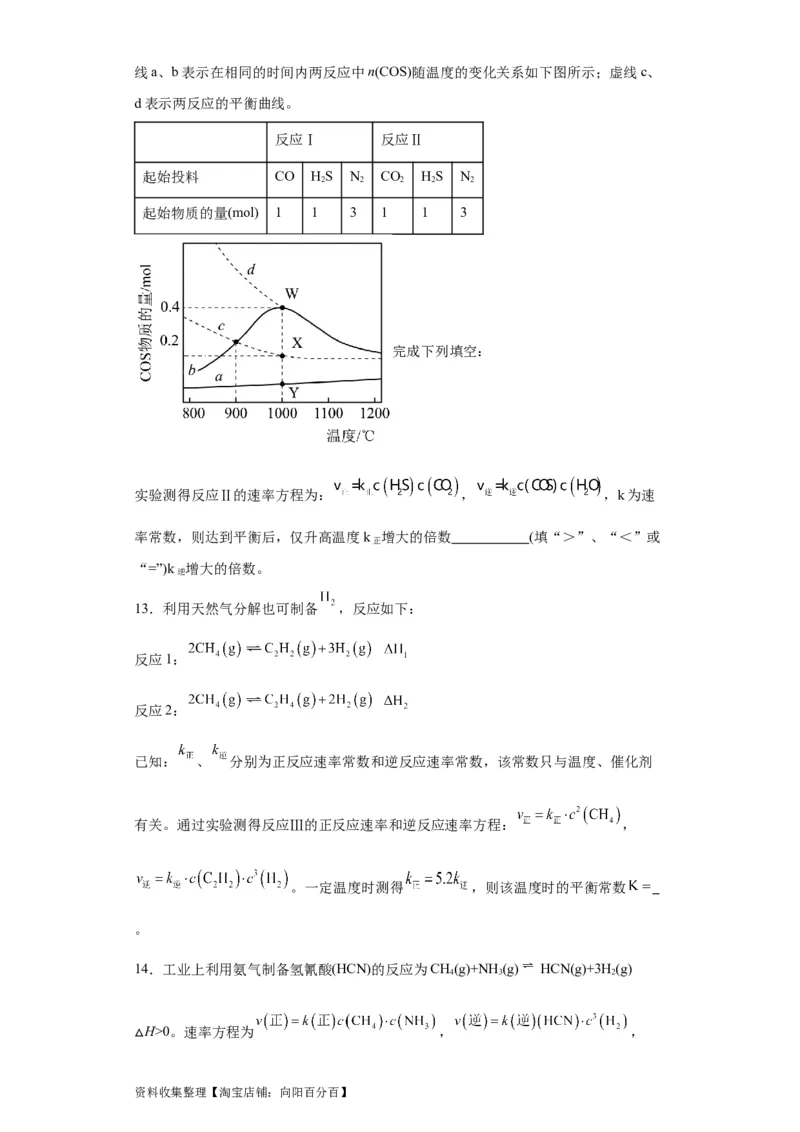
资料收集整理【淘宝店铺:向阳百分百】线a、b表示在相同的时间内两反应中n(COS)随温度的变化关系如下图所示;虚线c、
d表示两反应的平衡曲线。
反应Ⅰ 反应Ⅱ
起始投料 CO HS N CO HS N
2 2 2 2 2
起始物质的量(mol) 1 1 3 1 1 3
完成下列填空:
实验测得反应Ⅱ的速率方程为: , ,k为速
率常数,则达到平衡后,仅升高温度k 增大的倍数 (填“>”、“<”或
正
“=”)k 增大的倍数。
逆
13.利用天然气分解也可制备 ,反应如下:
反应1:
反应2:
已知: 、 分别为正反应速率常数和逆反应速率常数,该常数只与温度、催化剂
有关。通过实验测得反应Ⅲ的正反应速率和逆反应速率方程: ,
。一定温度时测得 ,则该温度时的平衡常数
。
14.工业上利用氨气制备氢氰酸(HCN)的反应为CH(g)+NH (g) HCN(g)+3H (g)
4 3 2
H>0。速率方程为 , ,
△
资料收集整理【淘宝店铺:向阳百分百】k(正)、k(逆)分别为正、逆反应速率常数,只与温度、催化剂有关。
①其他条件不变,反应达到平衡后,NH 转化率随着条件X的增大而减小,则X可能
3
是 (答一种即可)。
②当平衡常数K=20,k(逆)=2时,k(正)= 。
15.甲醇气相脱水制甲醚(CHOCH )的反应可表示为: 2 CH OH(g) CHOCH (g) +
3 3 3 3 3
HO(g) ΔH=-25 kJ/mol。若其正、逆反应速率分别可表示为v =k c2(CHOH)、v =k
2 正 正 3 逆 逆
c (CHOCH )·c (H O),k 、k 分别为正、逆反应速率常数,只与温度有关。则如图
3 3 2 正 逆
(pk=-lgk)所示①、②、③、④四条斜线中,能表示pk 随温度T变化关系的是斜线
正
。
16.甲烷水蒸气催化重整是制备高纯氢的方法之一。反应如下:
反应ⅰ. ;
反应ⅱ. ;
某科研小组研究了反应ⅱ的动力学,获得其速率方程 ,k为
速率常数(只受温度影响),m为 的反应级数。在某温度下进行实验,测得各组分
初浓度和反应初速率如下:
实验序号
1 0.100 0.100
2 0.100 0.200
的反应级数 ,当实验2进行到某时刻,测得 ,
资料收集整理【淘宝店铺:向阳百分百】则此时的反应速率 (保留3位有效数字,已知 )。
17.机动车尾气的主要污染物是氮的氧化物,采用合适的催化剂可分解NO,反应为
2NO(g) N(g)+O(g) ΔH,在T℃和T℃时,分别在容积均为1 L的密闭容器中通入
2 2 1 2
1 mol N⇌O,并发生上述反应,NO的转化率随时间的变化曲线如下图所示:
(1)T ℃ (填“>”或“<”,下同)T ℃,ΔH 0。
1 2
(2)温度为T℃时该反应的平衡常数K= (结果保留3位小数)。已知反应速
1
率v =k c2(NO),v =k c(N)·c(O),k 、k 分别为正反应速率常数和逆反应速率常
正 正 逆 逆 2 2 正 逆
数,则a点处 = 。
18.工业上用二氧化碳催化加氢可合成乙醇,其反应原理为: 2CO(g)+
2
6H(g) C HOH(g)+3H O(g) △H。
2 2 5 2
①该反⇌应的△H (填“>”“<”或“=”) 0;其正反应在 (填“高温”、“低
温”或“任何温度”)下能自发进行。
②该反应的反应速率表达式为v =k ·c2 (CO)· c6(H ),v =k
正 正 2 2 逆 逆
·c(C HOH)·c3(H O),其中k 、k 为速率常数。则该反应的平衡常数K = (用含
2 5 2 正 逆
k 、k 的代数式表示),若其他条件不变,降低温度,则下列推断合理的是
正 逆
(填标号)。
A.k 增大,k 减小 B.k 减小,k 增大
正 逆 正 逆
C. k 减小的倍数大于k D.k 减小的倍数小于k
正 逆 正 逆
19.以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.
Ⅱ.
回答下列问题:
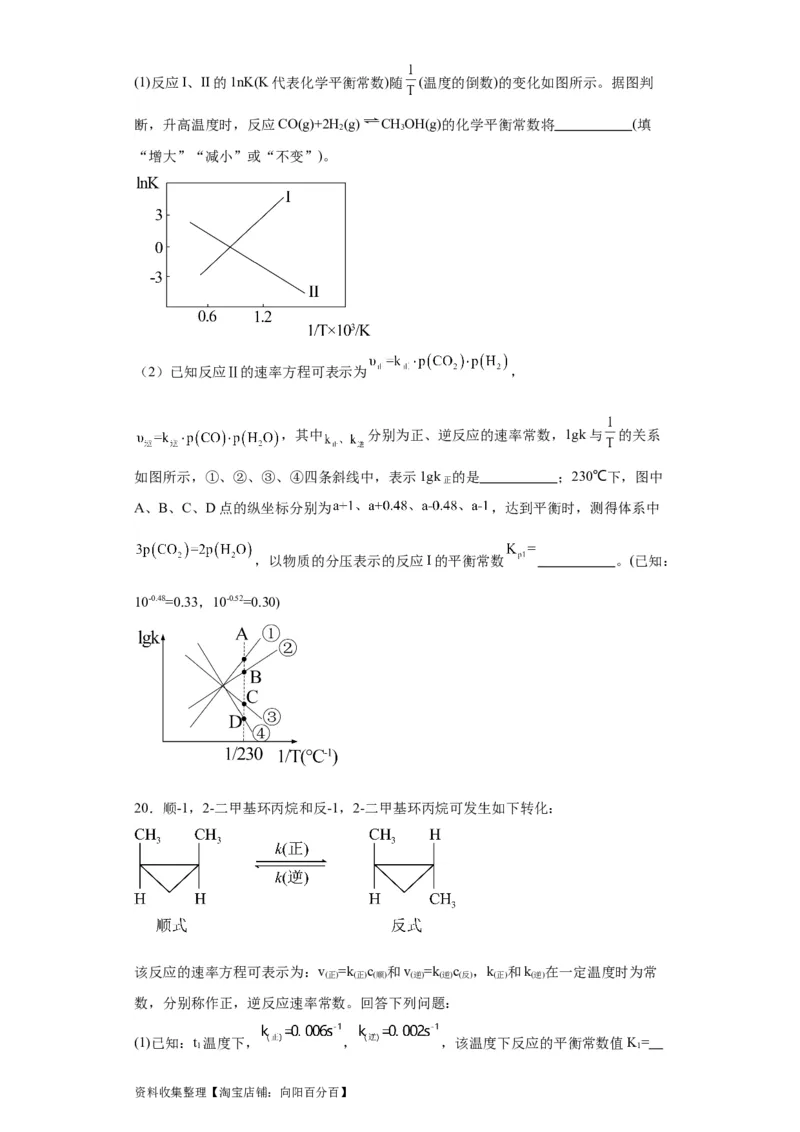
资料收集整理【淘宝店铺:向阳百分百】(1)反应I、II的1nK(K代表化学平衡常数)随 (温度的倒数)的变化如图所示。据图判
断,升高温度时,反应CO(g)+2H(g) CHOH(g)的化学平衡常数将 (填
2 3
“增大”“减小”或“不变”)。
(2)已知反应Ⅱ的速率方程可表示为 ,
,其中 分别为正、逆反应的速率常数,1gk与 的关系
如图所示,①、②、③、④四条斜线中,表示1gk 的是 ;230℃下,图中
正
A、B、C、D点的纵坐标分别为 ,达到平衡时,测得体系中
,以物质的分压表示的反应I的平衡常数 。(已知:
10-0.48=0.33,10-0.52=0.30)
20.顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化:
该反应的速率方程可表示为:v =k c 和v =k c ,k 和k 在一定温度时为常
(正) (正) (顺) (逆) (逆) (反) (正) (逆)
数,分别称作正,逆反应速率常数。回答下列问题:
(1)已知:t 温度下, , ,该温度下反应的平衡常数值K=
1 1
资料收集整理【淘宝店铺:向阳百分百】。
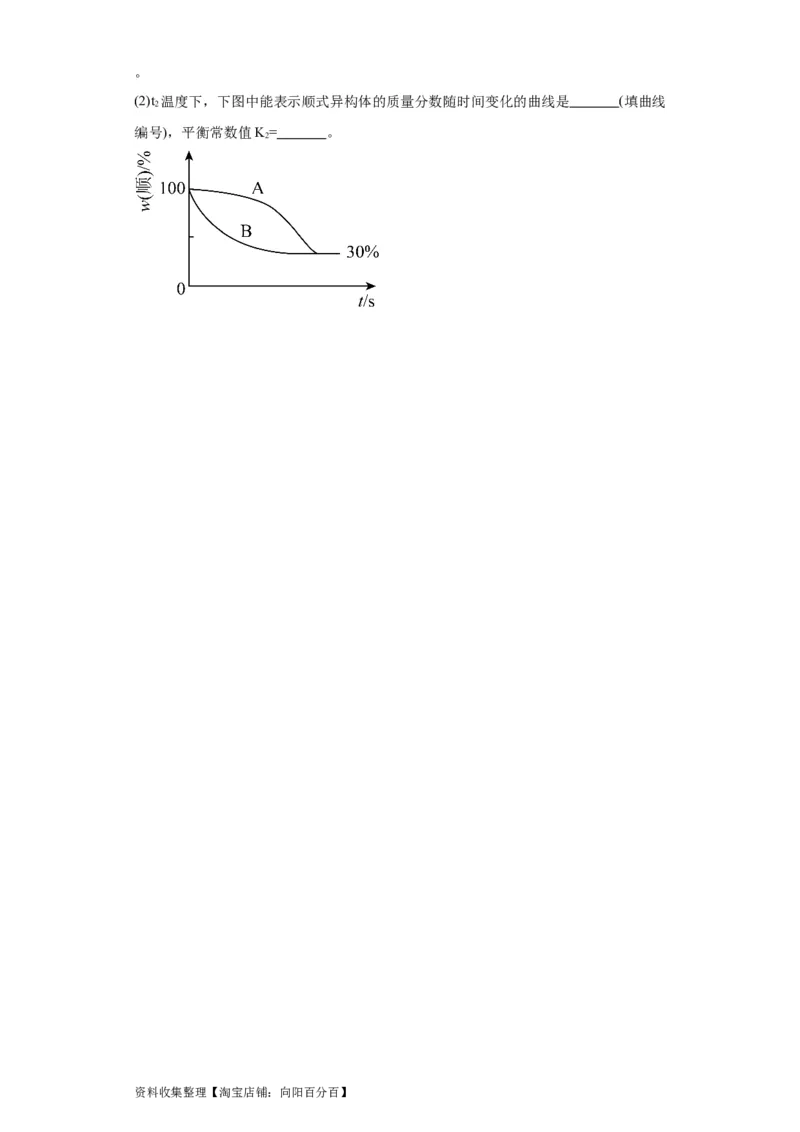
(2)t 温度下,下图中能表示顺式异构体的质量分数随时间变化的曲线是 (填曲线
2
编号),平衡常数值K= 。
2
资料收集整理【淘宝店铺:向阳百分百】