文档内容
专题04 氧化还原反应及其应用
(本卷共18小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.下列实验中物质的颜色变化与氧化还原反应无关的是
A.将NaO 粉末露置在空气中,固体由淡黄色变为白色
2 2
B.向Mg(OH) 悬浊液中滴加FeCl 溶液,固体由白色变为红褐色
2 3
C.向KCr O 酸性溶液中加入乙醇,溶液由橙色变为绿色
2 2 7
D.向KI溶液中通入少量氯气,溶液由无色变为棕黄色
【答案】B
【解析】过氧化钠在空气中与二氧化碳反应生成碳酸钠,由淡黄色变为白色,发生反应:2NaO+2CO
2 2 2
=2Na CO+O ,属于氧化还原反应,与氧化还原反应有关,故A不选;向Mg(OH) 悬浊液中滴加FeCl 溶液,
2 3 2 2 3
白色沉淀氢氧化镁转化为红褐色沉淀氢氧化铁,无化合价的变化,与氧化还原无关,故B选;向KCr O 酸性
2 2 7
溶液中加入乙醇,溶液由橙色变为绿色,可知Cr、C元素的化合价变化,属于氧化还原反应,与氧化还原反
应有关,故C不选;向KI溶液中通入少量氯气,KI被氯气氧化为碘单质,溶液由无色变为棕黄色,属于氧化
还原反应,与氧化还原反应有关,故D不选;故选B。
2.国家药监局网站公布2026年起将全面禁止生产含汞体温计。《本草纲目》记载:“水银乃至阴之毒
物,因火煅丹砂而出,加以盐、(明)矾而为轻粉,加以硫磺升而为银朱”。下列说法错误的是( )
A.短时间内吸入大量汞蒸气,会汞中毒
B.“火煅丹砂”是氧化还原反应
C.明矾的化学式是KAl(SO )·12H O,是混合物
4 2 2
D.水银温度计打碎后,洒出的汞可以用硫磺处理
【答案】C
【解析】汞蒸气被吸入人体内都会富积在体内,不易排出,人如果吸入或累积了足量的汞,就会造成慢性
中毒,A正确;丹砂主要是HgS,汞单质是由火煅丹砂而出,说明Hg元素化合价有变化,属于氧化还原反
应,B正确;明矾的化学式是KAl(SO )·12H O,是化合物,属于纯净物,C错误;汞有毒且易挥发,且汞易
4 2 2
于S单质发生化合反应生成稳定的HgS,所以水银温度计打碎后,洒出的汞可以用硫磺处理,D正确;故选
C。3.等物质的量的 与 溶液混合,反应过程中有沉淀和气体生成,恰好完全反应时,生成气体
22.4L(换算成标准状况),对该反应分析正确的是
A.氧化剂是 ,还原剂是 B.反应过程中转移电子4mol
C.被 还原的 为2mol D.反应后溶液的pH减小
【答案】C
【分析】等物质的量 与 溶液混合后一部分过氧化钠将亚铁转化为铁离子、一部分和水生成氧
气和氢氧化钠,氢氧化钠和铁离子生成氢氧化铁,过氧化钠中氧元素有化合价降低到-2价,也有化合价升高到
0价的,过氧化钠既是氧化剂又是还原剂,硫酸亚铁是还原剂,离子方程式为
据此分析。
【解析】氧化剂是过氧化钠,还原剂是硫酸亚铁和过氧化钠,A错误;4 ~O,生成1mol O 时,
2 2
有4mol 失4mol电子被氧化为+3价,1mol 失2mol电子被氧化生成氧气,有3mol 得6mol
电子被还原为-2价,可知生成1mol O,转移6mol电子,B错误;4mol 失4mol电子可还原2mol
2
,C正确;反应后Fe2+浓度减小,溶液pH增大,D错误;故选C。
4.下列实验中,实验操作、对应的现象及结论都正确的是
选项 实验操作 现象 结论
A 向乙醇中加入绿豆大小的钠块 有气泡产生 乙醇中含有水
通入X气体后产 通入的X气体一定具有强
B 向 溶液中依次通入 和X气体
生沉淀 氧化性
C 向含有淀粉的足量 溶液中滴加2滴氯水 溶液变蓝 还原性:
将用稀硫酸酸化的 溶液滴入
D 溶液变黄
氧化性:
溶液中
【答案】C【解析】乙醇也会和钠反应产生气体,A错误;X气体可能具有氧化性,生成硫酸钡沉淀;也可能具有碱
性,生成亚硫酸钡沉淀,B错误;向含有淀粉的足量FeI 溶液中滴加2滴氯水,溶液变蓝,说明I-先于Fe2+与
2
氯气反应,证明还原性I-强于Fe2+,C正确;高锰酸钾、硝酸都有强氧化性,用稀硫酸酸化后的高锰酸钾溶液
滴入硝酸亚铁溶液中,溶液变黄,不能证明氧化性KMnO >Fe3+,D错误;故选C。
4
5.我国古人曾用反应 制铜,并最早发明了青铜器的铸造技术。下列说法不正确的是
A. 只作还原剂
B.青铜的硬度比纯铜大
C. 和 是氧元素的同素异形体
D. 参与反应时,该反应中电子转移的总数约为
【答案】A
【解析】反应中Cu元素的化合价由Cu S中的+1价降至0价,S元素的化合价由Cu S中的-2价升至SO
2 2 2
中的+4价,Cu S既作氧化剂、又作还原剂,A项错误;青铜是铜合金,其硬度比纯铜大,B项正确;O 和O
2 2 3
是O元素形成的不同单质,互为同素异形体,C项正确;反应中Cu元素的化合价由Cu S中的+1价降至0
2
价,S元素的化合价由Cu S中的-2价升至SO 中的+4价,O元素的化合价由0价降至-2价,反应中每消耗
2 2
1molO 转移6mol电子,3.2gO 物质的量为0.1mol,则3.2gO 参与反应时,反应中转移电子物质的量为
2 2 2
0.6mol,转移电子数为6×6.02×1022,D项正确;答案选A。
6.黄铁矿(主要成分为FeS)在酸性条件和催化剂作用下,可发生如图所示的转化。下列说法错误的是
2
A.反应I、II、III均属于氧化还原反应
B.反应I的离子方程式为FeS+14Fe3++8H O=15Fe2++2SO 2-+16H+
2 2 4
C.反应III中氧化剂与还原剂的物质的量比为1:4D.该过程中Fe3+是催化剂,NO是中间产物
【答案】A
【解析】反应I的离子方程式为FeS+14Fe3++8H O=15Fe2++2SO 2-+16H+,反应III的离子方程式为
2 2 4
4Fe(NO) ++O +4H+=4Fe3++4NO+2HO,反应I、III是氧化还原反应;反应II的离子方程式为Fe2+
2 2 2
+NO=Fe(NO)2+,无元素化合价变化,为非氧化还原反应,A错误;根据流程中信息可知,反应I的离子方程式
为FeS+14Fe3++8H O=15Fe2++2SO 2-+16H+,B正确;反应III为4Fe(NO)2++O +4H+=4Fe3++4NO+2HO,只有
2 2 4 2 2
Fe、O元素化合价发生变化,O 为氧化剂,Fe(NO)2+为还原剂,故氧化剂与还原剂的物质的量比为1:4,C正
2
确;反应中Fe3+是催化剂,Fe2+、NO是中间产物,选项D正确;
故选A。
7.关于反应:2KClO+H C O=CO ↑+2ClO ↑+K CO+H O,下列说法正确的是
3 2 2 4 2 2 2 3 2
A.KClO 中的Cl被氧化
3
B.HC O 是氧化剂
2 2 4
C.氧化产物和还原产物的物质的量之比为1∶1
D.生成1molCO 时,反应共转移1mol电子
2
【答案】C
【分析】由方程式可知,反应中氯元素化合价降低被还原,氯酸钾是反应的氧化剂、二氧化氯是还原产
物,碳元素的化合价升高被氧化,草酸是还原剂、二氧化碳和碳酸钾是氧化产物。
【解析】由分析可知,反应中氯酸钾中氯元素化合价降低被还原,故A错误;由分析可知,反应中碳元
素的化合价升高被氧化,草酸是还原剂,故B错误;由分析可知,二氧化氯是还原产物,二氧化碳和碳酸钾
是氧化产物,由方程式可知,氧化产物和还原产物的物质的量之比为1∶1,故C正确;由分析可知,反应中生
成1mol二氧化碳,共转移2mol电子,故D错误;故选C。
8.下列过程所用的物质中,利用了其氧化性的是
A.用SO 的水溶液吸收Br B.用锌块防止钢铁船体腐蚀
2 2
C.用FeCl 溶液腐蚀铜板 D.用铁粉防止FeSO 溶液氧化
3 4
【答案】C
【解析】用SO 的水溶液吸收Br ,S元素的化合价升高,被氧化,利用其还原性,选项A错误;用Zn块
2 2
防止钢铁船体腐蚀,是利用其还原性, B错误;用FeCl 溶液腐蚀铜板发生的反应为2Fe3+ + Cu= 2Fe2+ +
3
Cu2+,铁元素的化合价降低,被还原,利用其氧化性,选项C正确;用Fe粉防止FeSO 溶液氧化,利用其还
4
原性,选项D错误;故选C。
9.CuCl为白色固体,难溶于水和乙醇,潮湿时易被氧化,常用作媒染剂。以废铜渣(主要成分为Cu,含
少量Ni、Al O 等)为原料制备CuCl的工艺流程如下:
2 3下列说法不正确的是
A.“除镍”与“碱溶”过程发生的主要反应均为非氧化还原反应
B.“酸溶”时可用热的氧气替换HO 作氧化剂
2 2
C.“还原”时发生反应离子方程式为:SO +Cu2++Cl−+H O=CuCl↓+SO +2H+
2
D.“洗涤”时采用乙醇与用蒸馏水相比较,制得CuCl纯度更高
【答案】C
【分析】废铜渣在CO作用下除去Ni,剩余Cu和Al O,加入氢氧化钠溶液经过碱溶使氧化铝转化为可溶
2 3
性盐除去氧化铝,过滤得到Cu,而后将Cu在HO、稀硫酸中氧化形成Cu2+,再加入亚硫酸钠、NaCl再还原
2 2
成CuCl,过滤、洗涤得到CuCl。
【解析】除镍时,Ni单质与CO形成配合物,不属于氧化还原反应,碱溶时,氧化铝与NaOH溶液反应生
成偏铝酸钠和水,也不属于氧化还原反应,A正确;HO 的作用是酸性环境中将铜单质氧化,热的氧气也可以
2 2
在酸性环境中将铜单质氧化,且不引入新的杂质,B正确;还原”时,在氯化钠溶液中,硫酸铜溶液被亚硫酸
钠还原为+1价铜离子生成CuCl沉淀,离子方程式为SO 2-+2Cu2++2Cl−+H O=2CuCl↓+SO 2-+2H+,C错误;有水
3 2 4
时CuCl更容易被氧化,使用乙醇能隔绝空气,防止CuCl被氧化,D正确;综上所述答案为C。
10.白磷在过量氢氧化钾溶液中可以发生反应: ,(已知
为正盐),下列说法错误的是
A.白磷P 既是氧化剂又是还原剂
4
B. 溶液中存在4种离子
C.氧化产物和还原产物的物质的量之比为3∶1
D.33.6 g KOH参加反应可得 气体11.2 L(标况)
【答案】D
【解析】A. 反应,P 中P元素化合价既有升高又有降低,所以P 既是氧化
4 4剂又是还原剂,故A正确; 为正盐, 溶液中存在K+、 、H+、OH-,共4种离子,故
B正确; 反应,P 中P元素化合价由0降低为-3,PH 是还原产物,P
4 3 4
中P元素化合价由0升高为+1, 是氧化产物,氧化产物和还原产物的物质的量之比为3∶1,故C正
确;33.6 g KOH的物质的量为0.6mol,根据反应方程式可知生成PH 的物质的量为0.2mol,生成PH 气体
3 3
4.48L(标况),故D错误;故选D。
二、选择题:本题共8个小题,每小题4分,共32分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
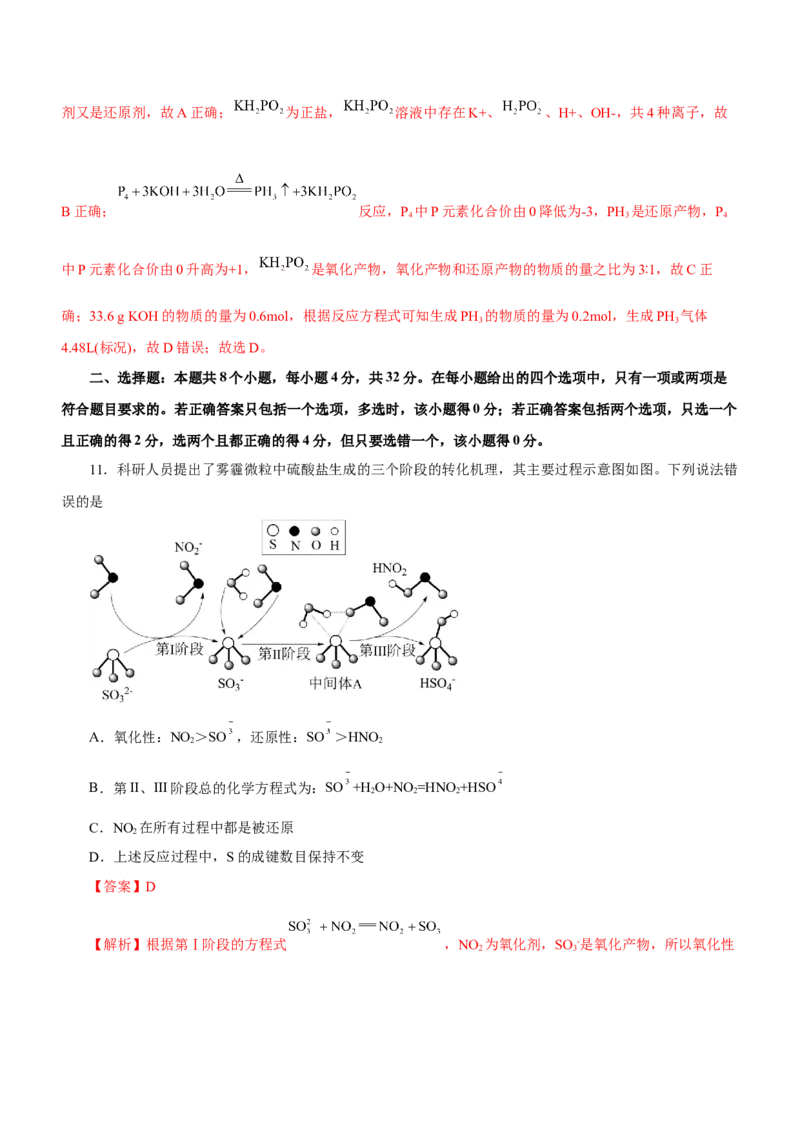
11.科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如图。下列说法错
误的是
A.氧化性:NO >SO ,还原性:SO >HNO
2 2
B.第II、III阶段总的化学方程式为:SO +H O+NO =HNO +HSO
2 2 2
C.NO 在所有过程中都是被还原
2
D.上述反应过程中,S的成键数目保持不变
【答案】D
【解析】根据第Ⅰ阶段的方程式 ,NO 为氧化剂,SO -是氧化产物,所以氧化性
2 3;第Ⅱ、Ш阶段总的方程式 可得还原性: ,A正
确;根据图示可知:在第Ⅱ阶段, 在 存在条件反应产生中间体A。在第Ⅲ阶段,中间体A转化
为 和 ,故第Ⅱ、Ⅲ阶段总的化学方程式为: ,B正确;根据图
示的转化过程知该过程中 , , 化合价均降低被还原C正确;由题图可知由,
最终生成 ,S的成健数目由3变为4,D错误。故选D。
12.铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:①T13++2Ag=Tl+
+2Ag+②Ag++Fe2+=Ag+Fe3+③Fe+2Fe3+=3Fe2+。下列离子氧化性比较顺序正确的是
A.T13+>Fe3+>Ag+ B.Fe3+>Ag+>T13+
C.T13+>Ag+>Fe2+ D.T13+>Ag+>Fe3+
【答案】CD
【解析】根据氧化还原反应方程式中氧化剂的氧化性强于氧化产物可知,氧化性①中Ti3+>Ag+,②中Ag
+>Fe3+,③中Fe3+>Fe2+,综上所述,氧化性是TI3+>Ag+>Fe3+>Fe2+,答案选CD。
13.关于反应3SiO+6C+2N Si N+6CO,下列说法正确的是
2 2 3 4
A.C在反应过程中被还原 B.Si N 既是氧化产物又是还原产物
3 4
C.氧化剂和还原剂质量之比为1:3 D.每生成14.0g Si N 共转移1.2mol电子
3 4
【答案】D
【解析】该反应中C元素化合价由0价升高为+2价,失电子被氧化,A错误;该反应中Si元素化合价没
有改变,N元素由0价变为-3价被还原,所以Si N 只是还原产物,B错误;该反应中C为还原剂,N 为氧化
3 4 2
剂,根据化学方程式可知氧化剂和还原剂物质的量之比为1:3,质量之比为28:(12×3)=7∶9,C错误;14.0g
Si N 的物质的量为 =0.1mol,所以有0.2molN 被还原,转移1.2mol电子,D正确;故选D。
3 4 2
14.已知下述三个实验均能发生化学反应
将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液中滴入几滴浓硝酸将铜丝放入氯化铁溶液中
下列判断正确的是
A.实验 中铁钉只作还原剂
B.实验 中 只体现还原性
C.实验 中发生的是置换反应
D.上述三个实验能说明氧化性:
【答案】AB
【解析】 中发生 ,铁元素化合价只升高,铁只作还原剂作,A正确; 中发生
, 只体现还原性,B正确; 中发生 ,
该反应不是置换反应,C错误;由发生的三个反应,利用氧化剂的氧化性大于氧化产物的氧化性,则上述实验
证明氧化性为 ,D错误;答案选AB。
15.酸性KMnO 溶液和CuS混合时,发生的反应如下:MnO-+CuS+H+→Cu2++SO↑+Mn2++H O,下列有关
4 4 2 2
该反应的说法中正确的是( )
A.被氧化的元素是Cu和S
B.Mn2+的还原性强于CuS的还原性
C.氧化剂与还原剂的物质的量之比为6:5
D.若生成2.24L(标况下)SO ,转移电子的物质的量是0.8mol
2
【答案】C
【解析】反应中,铜元素的化合价没变,硫元素的化合价由−2升到+4价,只有硫元素被氧化,A错误;
还原剂的还原性大于还原产物的还原性,则还原性CuS> Mn2+,B错误;氧化剂为KMnO ,还原剂为
4
CuS,设KMnO 为xmol,CuS为ymol,根据电子守恒:x×(7-2)=y×(4-(-2)),x:y=6:5,所以氧化剂
4
与还原剂的物质的量之比为6:5,C正确;二氧化硫物质的量为0.1mol,由方程式可知消耗KMnO 的量为
4
0.1×6/5=0.12 mol,反应中Mn元素化合价由+7价降低为+2价,故转移电子为0.12mol×(7−2)=0.6 mol,D
错误;答案选C。
16.KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
3。下列说法错误的是
A.产生22.4 L(标准状况)Cl 时,反应中转移10 mole-
2
B.反应中氧化剂和还原剂的物质的量之比为6:11
C.可用石灰乳吸收反应产生的Cl 制备漂白粉
2
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在
【答案】AB
【解析】根据反应方程式可知:反应消耗6 mol I 时,转移60 mol电子,反应产生3 molCl ,则产生标准
2 2
状况22.4 LCl 时,其物质的量是1 mol,则反应中转移20 mol e-,A错误;在该反应中,氧化剂是KClO,还
2 3
原剂是I,则氧化剂和还原剂的物质的量之比为11:6,B错误;Cl 与石灰乳反应产生CaCl 、Ca(ClO) 的混
2 2 2 2
合物就是漂白粉,故可用石灰乳吸收反应产生的Cl 制备漂白粉,C正确;若食盐中含有 ,在酸性条件
2
下, 、I-发生氧化还原反应产生I,I 遇淀粉溶液变为蓝色,故可用酸化的淀粉碘化钾溶液检验食盐中
2 2
的存在,D正确;故选AB。
17.已知N-Cl键中,N元素显负价,Cl元素显正价。NCl 易与水反:NCl +3H O=NH ↑+3HClO。若N 代
3 3 2 3 A
表阿伏加德罗常数的值,下列说法正确的是( )
A.该反应中,NCl 既是氧化剂,又是还原剂
3
B.标准状况下,1.7gNH 体积约为2.24L
3
C.0.1molNCl 中阴阳离子总数为0.4N
3 A
D.100mL1mol/LHClO溶液中H+总数为0.1N
A
【答案】B
【解析】该反应前后元素的化合价均没有发生变化,不是氧化还原反应,A错误;标准状况下,1.7gNH
3
的物质的量是1.7g÷17g/mol=0.1mol,体积约为2.24L,B正确;NCl 是共价化合物,不存在阴阳离子,C错
3
误;次氯酸是弱酸,部分电离,则100mL1mol/LHClO溶液中H+总数小于0.1N ,D错误;答案选B。
A
18.工业上将氯气通入到石灰乳中制备漂白粉,制备流程如下。下列有关说法正确的是
A.漂白粉是混合物B.“反应”中 是氧化剂,石灰乳是还原剂
C.将 通入到烧碱溶液中也可以制得具有漂白性的物质
D.工业制备漂白粉的离子方程式为
【答案】AC
【解析】石灰乳中通入氯气发生反应: ,蒸发后过滤得到漂白粉,主
要成分为氯化钙和次氯酸钙。漂白粉主要成分是氯化钙和次氯酸钙,是混合物,A正确;从制备方程式可知,
氯气既是氧化剂又是还原剂,B错误;将氯气通入烧碱溶液中: ,次氯酸钠具
有漂白性,C正确;石灰乳不可拆,根据漂白粉制备的化学方程式可知离子方程式为:
,D错误;故选AC。
第II卷 (非选择题共38分)
三、非选择题:本题共3个小题,共38分。
16.(8分)从某废催化剂(含ZnO、CuO、Fe O、石墨及MnO 等)中回收金属并制取活性氧化锌的工艺流
2 3 2
程如下(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):
“氧化”时Mn2+被氧化的离子方程式为____________________________________。
“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):
_____________________________________________________________________________________。
【解析】由工艺流程图可知反应物为Mn2+、(NH )SO,生成物为MnO(OH) 、(NH )SO 故反应的离子方
4 2 2 8 2 4 2 4
程式为Mn2++SO―→MnO(OH) +2SO,由环境知滤液呈酸性,故应在右侧补H+,左侧补水,Mn2++SO+
2 2 2
3HO===MnO(OH) +2SO+4H+。
2 2
【答案】Mn2++SO+3HO=MnO(OH) ↓+2SO+4H+(4分)Zn(OH) +2OH-=ZnO+2HO(4分)
2 2 2 2 2
17.(15分) 三氯化六氨合钴[Co(NH )]Cl 是橙黄色、微溶于水的配合物,是合成其他一些含钴配合物
3 6 3的原料。下图是某科研小组以含钴废料(含少量Fe、Al等杂质)制取[Co(NH )]Cl 的工艺流程:
3 6 3
回答下列问题:
(1)写出加“适量NaClO”发生反应的离子方程式:__________________________________________。
3
(2)“加NaCO 调pH至a”会生成两种沉淀,分别为__________________(填化学式)。
2 3
(3)操作Ⅰ的步骤包括________________________、冷却结晶、减压过滤。
(4)流程中NH Cl除作反应物外,还可防止加氨水时c(OH-)过大,其原理是
4
_____________________________________________________________________________。
(5)“氧化”步骤,甲同学认为应先加入氨水再加入HO,乙同学认为试剂添加顺序对产物无影响。你认为
2 2
______(填“甲”或“乙”)同学观点正确,理由是___________________________________________。
写出该步骤的化学方程式:______________________________________________________。
【解析】 (1)加适量NaClO 的目的是将亚铁离子氧化为铁离子。
3
(2)加入碳酸钠调节pH,使铝离子和铁离子转化为Fe(OH) 和Al(OH) 两种沉淀。
3 3
(3)为了防止产品水解,故应在HCl氛围下蒸发浓缩。
(4)流程中氯化铵除作为反应物外,NH Cl溶于水电离出NH会抑制后期加入的NH ·H O的电离,可防止
4 3 2
加氨水时氢氧根离子浓度过大。
(5)若先加入过氧化氢,将钴元素氧化为Co3+,后加入氨水,会生成氢氧化钴,不利于产品的生成,故甲
同学正确,先加入氨水再加入过氧化氢,可防止Co(OH) 的生成。
3
【答案】(1)6Fe2++ClO+6H+===6Fe3++Cl-+3HO(3分)(2)Fe(OH) 和Al(OH) (2分)
2 3 3
(3)HCl氛围下蒸发浓缩(2分)(4)NH Cl溶于水电离出NH会抑制后期加入的NH ·H O的电离(2分)
4 3 2
(5)甲(2分)防止Co(OH) 的生成(2分)HO+2CoCl +2NH Cl+10NH ·H O=2[Co(NH )]Cl ↓+12HO(2
3 2 2 2 4 3 2 3 6 3 2
分)
18.(15分)在南北朝刘宋·雷敩所著的《雷公炮炙论》中收录了一种矿物类药材石髓铅,又称自然铜,具
有活血化瘀止痛的效果。今用现代分析技术检测一份石髓铅样品,发现其含铜极少,含有铁元素的质量分数为
44.8%,硫元素的质量分数为51.2%。回答下列问题:
(1)石髓铅的主要成分是一种化合物(质量分数为96%),化学式为______________;石髓铅粉末几乎能完全
溶于硫酸酸化的高锰酸钾溶液中,形成多种硫酸盐的混合液,写出主要反应的离子方程式:
______________________。
(2)利用石髓铅、焦炭和氧气在高温下反应可制造硫黄,副产品为Fe O 和CO。Fe O 是________色晶体,
3 4 3 4可用于制作复印机的墨粉,CO可用于合成在纺织工业中广泛使用的保险粉(Na SO),其流程如下:
2 2 4
合成塔 Ⅰ 中得到的HCOONa溶液溶质质量分数约为5%,从中分离出HCOONa·2H O的主要步骤是
2
________、________、过滤、洗涤、干燥;合成塔Ⅱ中发生主要反应的化学方程式为___________________。
保险粉暴露在空气中易吸收氧气和水蒸气而变质,当吸收自身物质的量一半的氧气和一定量水蒸气时,变
质形成___________(填化学式)。
【答案】(1)FeS (2分) FeS+ 3MnO+8H+==Fe3++2SO+3Mn2++4HO(3分)
2 2 2
(2)黑(1分) (加热)蒸发(浓缩) (2分)(冷却)结晶 (2分)HCOONa·2H O+NaOH+
2
2SO ===Na SO+CO+3HO (3分)NaHSO (2分)
2 2 2 4 2 2 3
【解析】(1)由于石髓铅样品中Fe、S两种元素含量的和为96%,恰好等于石髓铅的含量,所以该物质是
Fe、S的化合物,根据质量比可得n(Fe)∶n(S)=∶=1∶2,所以该物质的化学式为FeS;石髓铅粉末完全溶于硫
2
酸酸化的高锰酸钾溶液中,FeS 被氧化为Fe3+和SO,高锰酸钾被还原为Mn2+,根据电子守恒、电荷守恒及原
2
子守恒,可得主要反应的离子方程式:FeS+ 3MnO+8H+===Fe3++2SO+3Mn2++4HO。(2) Fe O 是黑色晶
2 2 3 4
体,HCOONa的溶解度受温度的影响变化较大,所以从HCOONa溶液中获得HCOONa·2H O的方法是将该物
2
质的稀溶液蒸发浓缩,然后冷却、结晶、过滤、洗涤、干燥,就得到HCOONa·2H O;在合成塔Ⅱ中,
2
HCOONa·2H O、NaOH、SO 发生反应,产生CO、NaSO、HO,发生的主要反应的化学方程式为
2 2 2 2 2 4 2
HCOONa·2H O+NaOH+2SO ===Na SO+CO+3HO;保险粉NaSO 暴露于空气中易被氧气氧化,氧化剂
2 2 2 2 4 2 2 2 2 4
为氧气,还原剂为NaSO,又氧化剂和还原剂的物质的量之比为1∶2,设NaSO 被氧化后硫的化合价为+x
2 2 4 2 2 4
价,则根据得失电子守恒,1×4=2×2×(x-3),解得x=4,又有水蒸气参与反应,所以产物为NaHSO。
3