文档内容
专题 06 金属及其化合物
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
1.(2023·江苏省南通市如东县高三期中学情检测)下列生活应用或生产活动中物质的性质与用途具有对应
关系的是( )
A.CaO易与水反应,可用作食品干燥剂
B.CuSO 能使蛋白质变性,可用于制作颜料
4
C.Na有导电性,可用作快中子反应堆的热交换剂
D.SO 具有氧化性,可用于漂白纸张
2
2.(2023·黑龙江省哈师大附中高三模拟)下列关于物质用途的说法中不正确的是( )
A.铁粉与氧化铝发生的铝热反应可用于焊接铁轨
B.氧化铝熔点高,常用于制造耐高温材料
C.熟石膏与水混合成糊状后能很快凝固,常用于制作模型和医疗石膏绷带
D.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
3.(2022·浙江省温州十校联合体高一期中)下列各组中的物质,不能发生化合反应的是( )
A.Na与Cl B.NaO与HO C.Al O 与HCl D.FeO与O
2 2 2 2 3 2
4.(2022·广东佛山市佛山一中)铁和铁合金是生活中常见的材料,下列说法正确的是( )
A.铁与盐酸反应,铁合金不与盐酸反应 B.一定条件下,铁粉可与水蒸气反应
C.不锈钢是铁合金,只含金属元素 D.纯铁的硬度和强度均高于铁合金
5.(2022·浙江省绿谷高中联盟高一期中联考)下列关于NaO和NaO 的说法中,不正确的是( )
2 2 2
A.NaO与NaO 中的阴阳离子比均为1:2
2 2 2
B.NaO 可在呼吸面具或潜水艇中作为氧气的来源
2 2
C.钠放置在空气中,会迅速被氧化而生成白色的氧化钠
D.NaO 与NaO都能与水反应生成碱,都属于碱性氧化物
2 2 2
6.(2022·江苏省海门市高三模拟预测)关于铁及其化合物的性质与用途具有对应关系的是( )
A.Fe具有还原性,可用作抗氧化剂 B.Fe O 具有磁性,可用于炼铁
3 4
C.Fe(OH) 胶体呈红褐色,可用于净水 D.FeCl 溶液呈酸性,可用于刻蚀铜板
3 3
7.(2023·江苏省苏锡常镇四市高三教学情况调研)在给定的条件下,下列选项所示的物质间转化均能一步
实现的是
A.B.
C.
D.
8.(2023·浙江省普通高校招生高三选考模拟)下列“类比”结果正确的是( )
A.植物油不溶于水,则甘油也不溶于水
B.甲酸能与银氨溶液发生银镜反应,则乙酸也可与银氨溶液发生银镜反应
C.S和Fe加热条件下生成FeS,则S和Cu加热条件下生成Cu S
2
D.向含Ag+的溶液中滴加过量氨水不会产生沉淀,则向含Al3+的溶液滴加过量的氨水也不会产生沉淀
9.(2022·浙江省杭州地区及周边重点中学高一期中联考)下列“类比”、“推理”合理的是( )
A.Fe与Cl 反应生成FeCl ,则Fe与I 反应生成FeI
2 3 2 3
B.CaO与CO 反应生成CaCO ,CuO与CO 反应生成CuCO
2 3 2 3
C.在NaO 与水反应后的溶液中加入MnO 粉末,会产生大量气体,该气体能使带火星的木条复燃,则
2 2 2
可推测NaO 与水反应有中间产物HO 生成
2 2 2 2
D.Na与水反应生成NaOH和H,则Fe与水蒸气反应生成Fe(OH) 和H
2 3 2
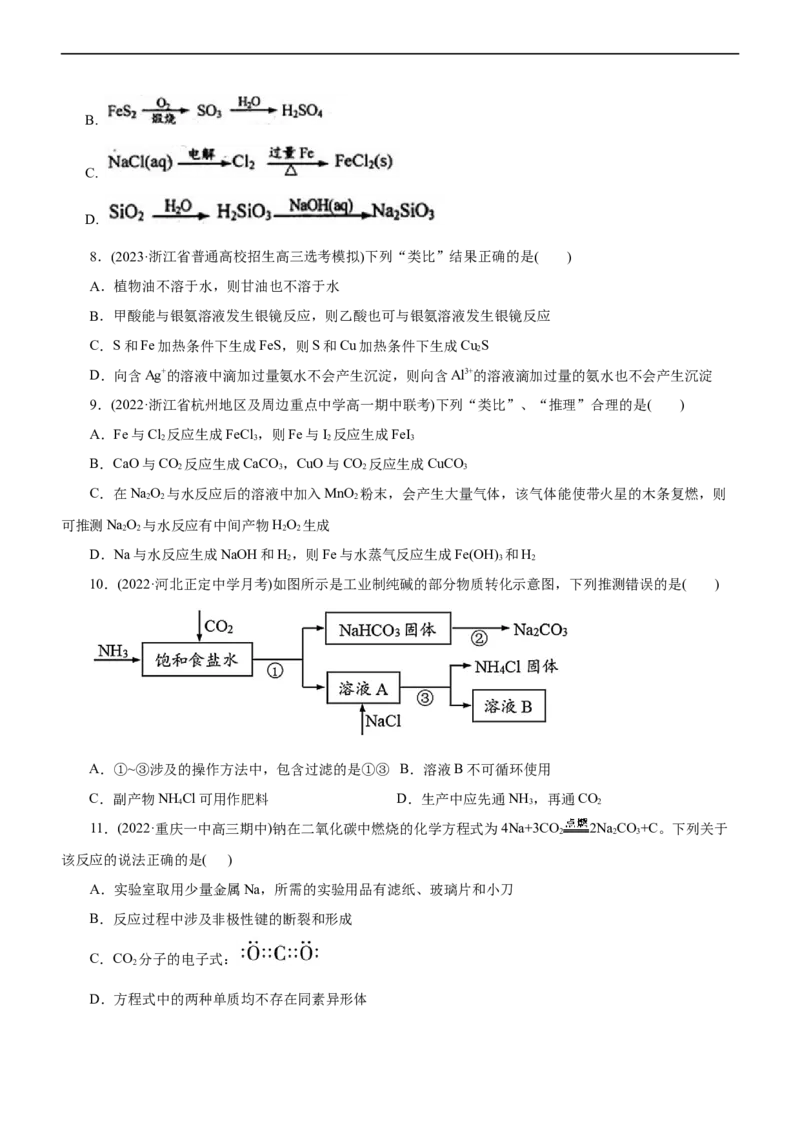
10.(2022·河北正定中学月考)如图所示是工业制纯碱的部分物质转化示意图,下列推测错误的是( )
A.①~③涉及的操作方法中,包含过滤的是①③ B.溶液B不可循环使用
C.副产物NH Cl可用作肥料 D.生产中应先通NH ,再通CO
4 3 2
11.(2022·重庆一中高三期中)钠在二氧化碳中燃烧的化学方程式为4Na+3CO 2NaCO+C。下列关于
2 2 3
该反应的说法正确的是( )
A.实验室取用少量金属Na,所需的实验用品有滤纸、玻璃片和小刀
B.反应过程中涉及非极性键的断裂和形成
C.CO 分子的电子式:
2
D.方程式中的两种单质均不存在同素异形体12.(2022·河北高三模拟预测)三星堆考古新发现了大型青铜立人神兽,青铜是金属冶铸史上最早被使用的
合金,是在纯铜(紫铜)中加入锡或铅制成的。下列关于青铜的叙述不正确的是
A.可通过热还原法利用铜矿石冶炼铜片
B.把铜和锡按一定的比例冶炼成铜锡合金,所得的合金熔点比纯铜低
C.青铜具有硬度大、可塑性强、耐磨等特点,可用于铸造多种器具
D.随着时间推移,青铜器逐渐被铁制品取代是由于铁制品的耐腐蚀性能更好
13.(2022·安徽省定远县育才学校高三月考)下列关于Fe、Cu、Mg、Al四种金属元素的说法中不正确的是
( )
A.四种元素的单质只有三种能和盐酸反应,生成相应的盐和氢气
B.制备AlCl 、FeCl 、CuCl 均不能采用将溶液直接蒸干的方法
3 3 2
C.将Mg棒和Al棒作为原电池的两个电极插入NaOH溶液中,Mg棒上发生氧化反应
D.铁锈的主要成分是氧化铁,铜锈的主要成分是碱式碳酸铜
14.(2022·陕西省安康市高三期中)实验室常用KSCN溶液检验Fe3+,可用K[Fe(CN) ]溶液检验Fe2+,现象
3 6
为产生深蓝色沉淀。下列说法正确的是( )
A.KSCN与K[Fe(CN) ]中C的化合价均为+4
3 6
B.上述元素中,金属性最强和非金属性最强的分别是K、N
C.若溶液中含有Fe3+,滴加KSCN溶液后会产生血红色沉淀
D.HS的相对分子质量大于HO的,因此熔沸点:HS>HO
2 2 2 2
15.(2022·河南省重点中学高三模拟调研)将23g钠、9g铝粉、28g铁粉分别投入盛有质量相等且过量的
CuSO 溶液的X、Y、Z三个烧杯中并使它们充分反应,下列说法中正确的是( )
4
A.都会析出红色固体 B.Y中不可能有气体放出
C.反应后氧化剂得到的电子数目相等 D.X、Y中溶液可能变成无色
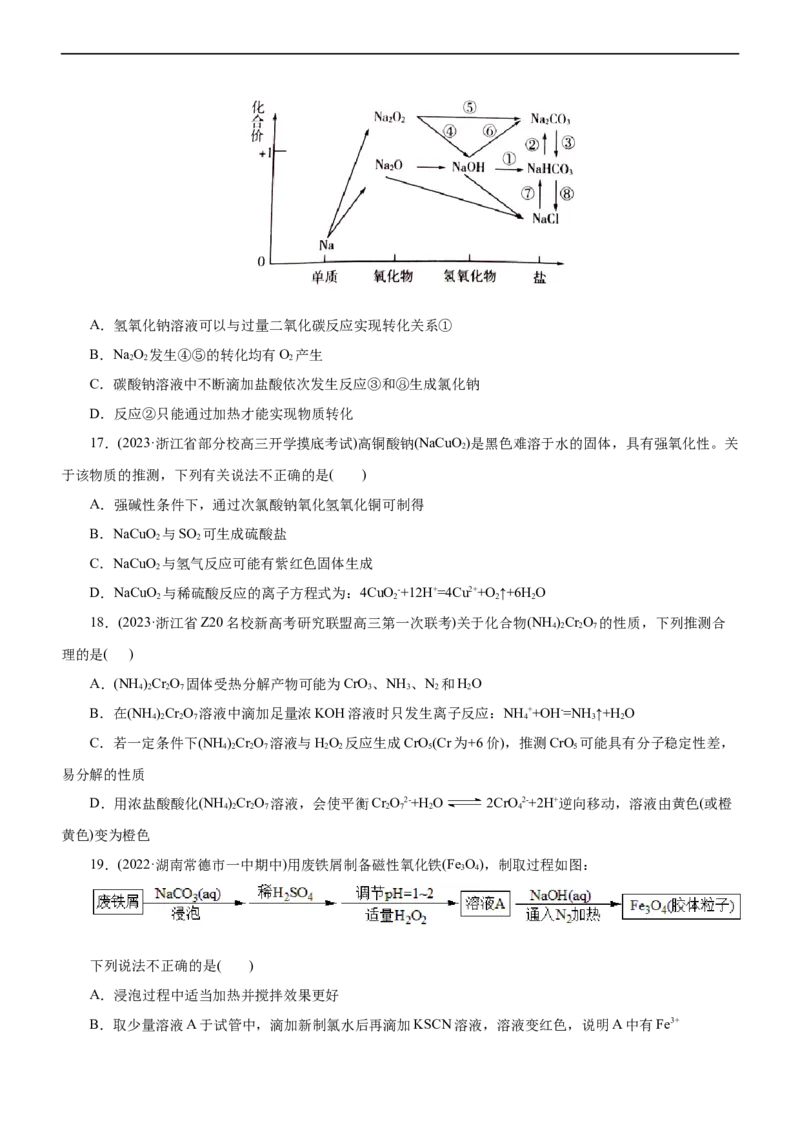
16.(2022·山东省平邑市高一期中)元素的价类二维图指的是以元素的化合价为纵坐标,以物质的类别为横
坐标所绘制的二维平面图像。下图为钠元素的价类二维图,其中的箭头表示部分物质间的转化关系,下列说法
不正确的是( )A.氢氧化钠溶液可以与过量二氧化碳反应实现转化关系①
B.NaO 发生④⑤的转化均有O 产生
2 2 2
C.碳酸钠溶液中不断滴加盐酸依次发生反应③和⑧生成氯化钠
D.反应②只能通过加热才能实现物质转化
17.(2023·浙江省部分校高三开学摸底考试)高铜酸钠(NaCuO )是黑色难溶于水的固体,具有强氧化性。关
2
于该物质的推测,下列有关说法不正确的是( )
A.强碱性条件下,通过次氯酸钠氧化氢氧化铜可制得
B.NaCuO 与SO 可生成硫酸盐
2 2
C.NaCuO 与氢气反应可能有紫红色固体生成
2
D.NaCuO 与稀硫酸反应的离子方程式为:4CuO-+12H+=4Cu2++O ↑+6H O
2 2 2 2
18.(2023·浙江省Z20名校新高考研究联盟高三第一次联考)关于化合物(NH )Cr O 的性质,下列推测合
4 2 2 7
理的是( )
A.(NH )Cr O 固体受热分解产物可能为CrO、NH 、N 和HO
4 2 2 7 3 3 2 2
B.在(NH )Cr O 溶液中滴加足量浓KOH溶液时只发生离子反应:NH ++OH-=NH↑+H O
4 2 2 7 4 3 2
C.若一定条件下(NH )Cr O 溶液与HO 反应生成CrO(Cr为+6价),推测CrO 可能具有分子稳定性差,
4 2 2 7 2 2 5 5
易分解的性质
D.用浓盐酸酸化(NH )Cr O 溶液,会使平衡Cr O2-+H O 2CrO2-+2H+逆向移动,溶液由黄色(或橙
4 2 2 7 2 7 2 4
黄色)变为橙色
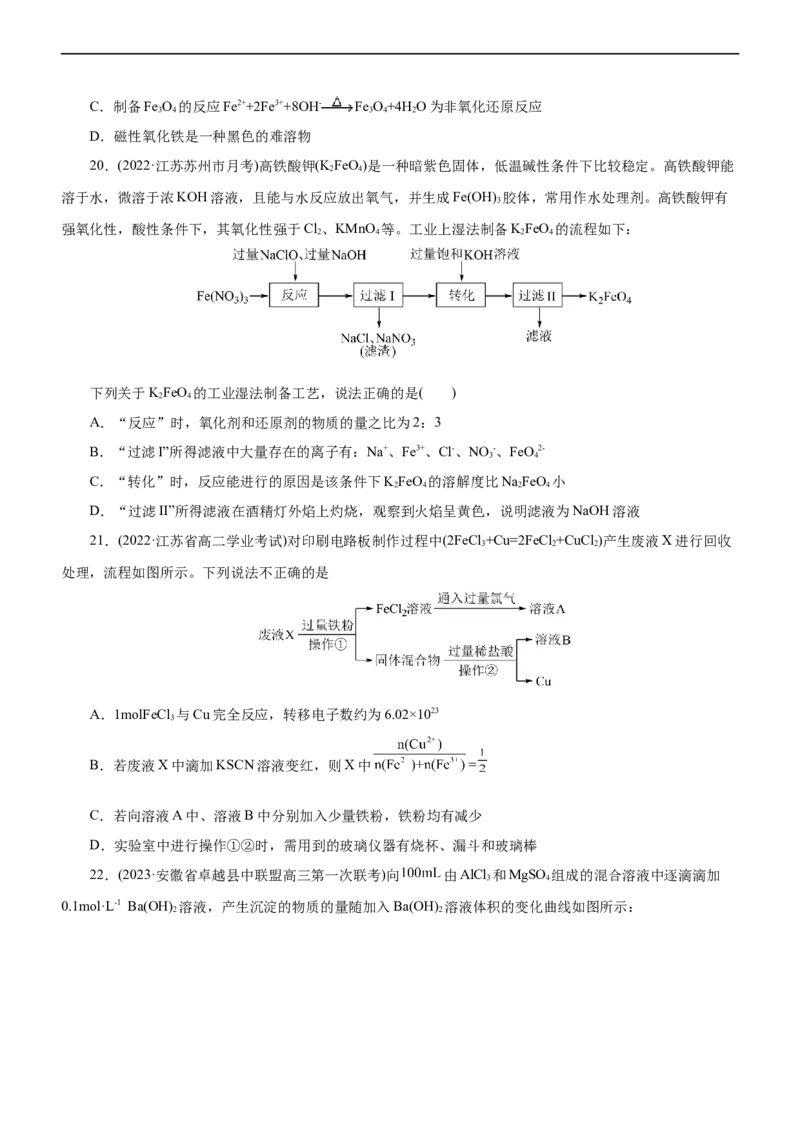
19.(2022·湖南常德市一中期中)用废铁屑制备磁性氧化铁(Fe O),制取过程如图:
3 4
下列说法不正确的是( )
A.浸泡过程中适当加热并搅拌效果更好
B.取少量溶液A于试管中,滴加新制氯水后再滴加KSCN溶液,溶液变红色,说明A中有Fe3+C.制备Fe O 的反应Fe2++2Fe3++8OH- Fe O+4H O为非氧化还原反应
3 4 3 4 2
D.磁性氧化铁是一种黑色的难溶物
20.(2022·江苏苏州市月考)高铁酸钾(K FeO)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能
2 4
溶于水,微溶于浓KOH溶液,且能与水反应放出氧气,并生成Fe(OH) 胶体,常用作水处理剂。高铁酸钾有
3
强氧化性,酸性条件下,其氧化性强于Cl、KMnO 等。工业上湿法制备KFeO 的流程如下:
2 4 2 4
下列关于KFeO 的工业湿法制备工艺,说法正确的是( )
2 4
A.“反应”时,氧化剂和还原剂的物质的量之比为2:3
B.“过滤I”所得滤液中大量存在的离子有:Na+、Fe3+、Cl-、NO -、FeO2-
3 4
C.“转化”时,反应能进行的原因是该条件下KFeO 的溶解度比NaFeO 小
2 4 2 4
D.“过滤II”所得滤液在酒精灯外焰上灼烧,观察到火焰呈黄色,说明滤液为NaOH溶液
21.(2022·江苏省高二学业考试)对印刷电路板制作过程中(2FeCl +Cu=2FeCl +CuCl )产生废液X进行回收
3 2 2
处理,流程如图所示。下列说法不正确的是
A.1molFeCl 与Cu完全反应,转移电子数约为6.02×1023
3
B.若废液X中滴加KSCN溶液变红,则X中 =
C.若向溶液A中、溶液B中分别加入少量铁粉,铁粉均有减少
D.实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和玻璃棒
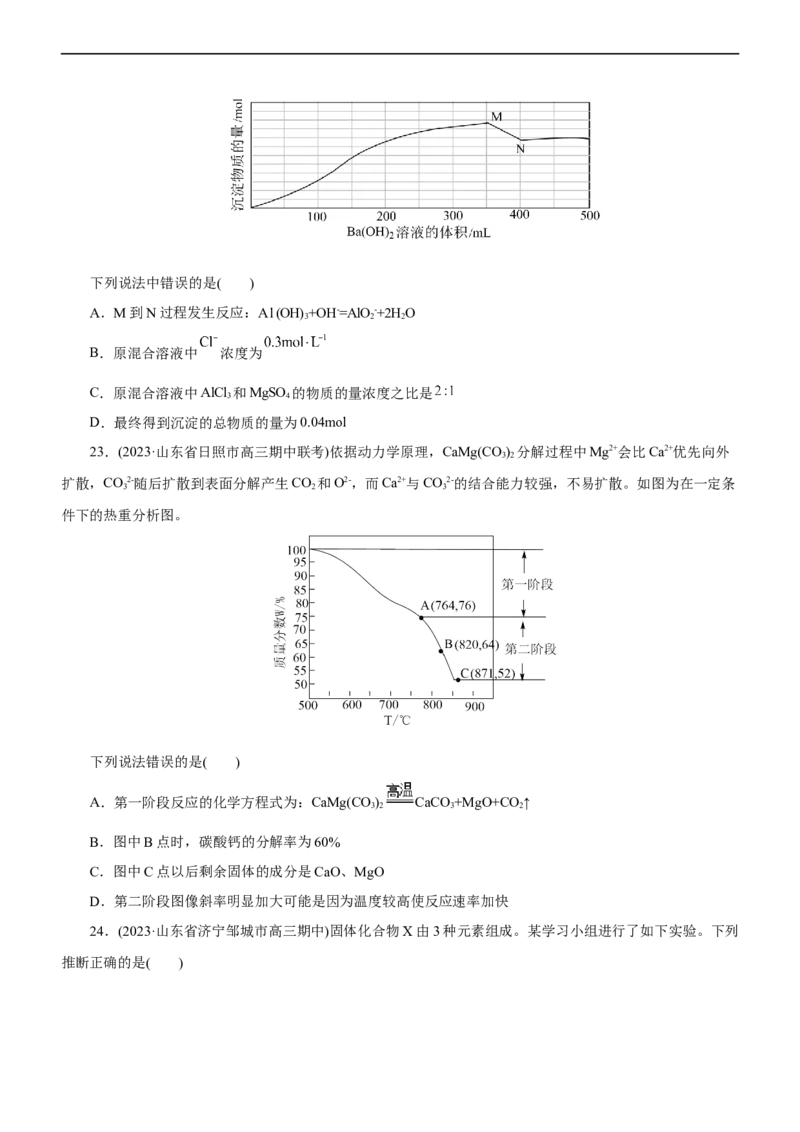
22.(2023·安徽省卓越县中联盟高三第一次联考)向 由AlCl 和MgSO 组成的混合溶液中逐滴滴加
3 4
0.1mol·L-1 Ba(OH) 溶液,产生沉淀的物质的量随加入Ba(OH) 溶液体积的变化曲线如图所示:
2 2下列说法中错误的是( )
A.M到N过程发生反应:A l (OH)+OH-=AlO-+2H O
3 2 2
B.原混合溶液中 浓度为
C.原混合溶液中AlCl 和MgSO 的物质的量浓度之比是
3 4
D.最终得到沉淀的总物质的量为0.04mol
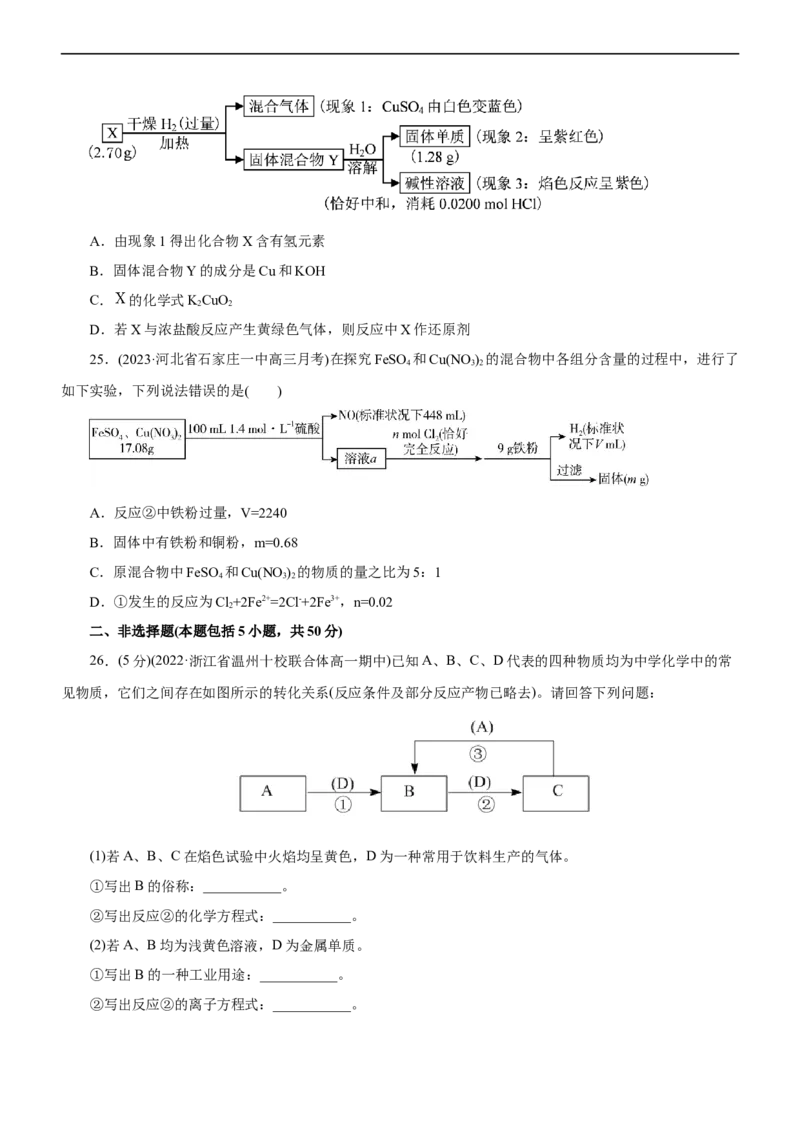
23.(2023·山东省日照市高三期中联考)依据动力学原理,CaMg(CO ) 分解过程中Mg2+会比Ca2+优先向外
3 2
扩散,CO2-随后扩散到表面分解产生CO 和O2-,而Ca2+与CO2-的结合能力较强,不易扩散。如图为在一定条
3 2 3
件下的热重分析图。
下列说法错误的是( )
A.第一阶段反应的化学方程式为:CaMg(CO ) CaCO +MgO+CO↑
3 2 3 2
B.图中B点时,碳酸钙的分解率为60%
C.图中C点以后剩余固体的成分是CaO、MgO
D.第二阶段图像斜率明显加大可能是因为温度较高使反应速率加快
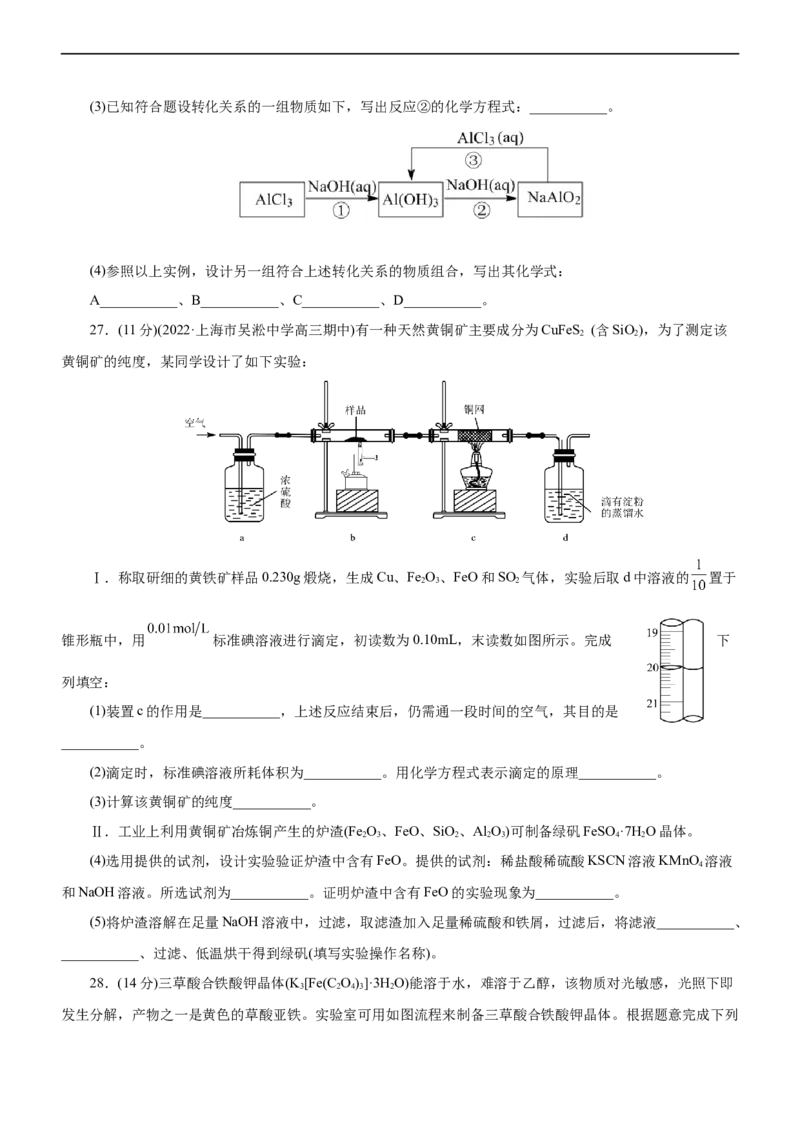
24.(2023·山东省济宁邹城市高三期中)固体化合物X由3种元素组成。某学习小组进行了如下实验。下列
推断正确的是( )A.由现象1得出化合物X含有氢元素
B.固体混合物Y的成分是Cu和KOH
C. 的化学式KCuO
2 2
D.若X与浓盐酸反应产生黄绿色气体,则反应中X作还原剂
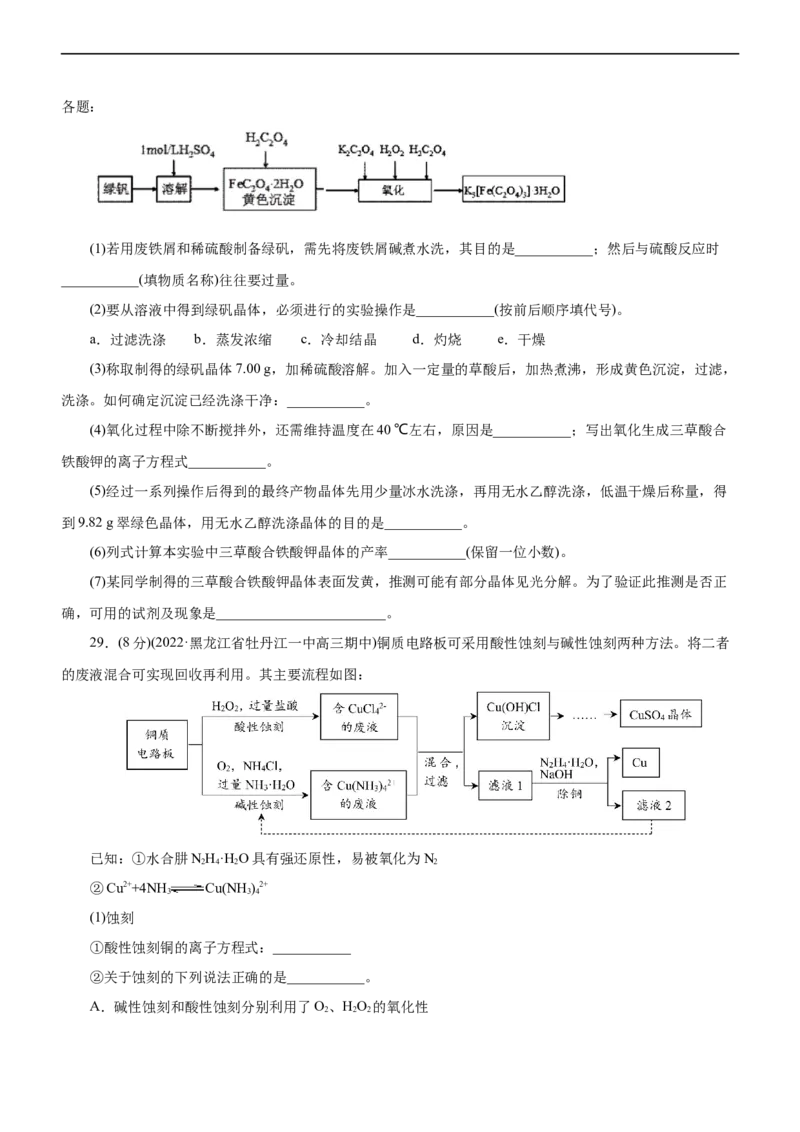
25.(2023·河北省石家庄一中高三月考)在探究FeSO 和Cu(NO ) 的混合物中各组分含量的过程中,进行了
4 3 2
如下实验,下列说法错误的是( )
A.反应②中铁粉过量,V=2240
B.固体中有铁粉和铜粉,m=0.68
C.原混合物中FeSO 和Cu(NO ) 的物质的量之比为5:1
4 3 2
D.①发生的反应为Cl+2Fe2+=2Cl-+2Fe3+,n=0.02
2
二、非选择题(本题包括5小题,共50分)
26.(5分)(2022·浙江省温州十校联合体高一期中)已知A、B、C、D代表的四种物质均为中学化学中的常
见物质,它们之间存在如图所示的转化关系(反应条件及部分反应产物已略去)。请回答下列问题:
(1)若A、B、C在焰色试验中火焰均呈黄色,D为一种常用于饮料生产的气体。
①写出B的俗称:___________。
②写出反应②的化学方程式:___________。
(2)若A、B均为浅黄色溶液,D为金属单质。
①写出B的一种工业用途:___________。
②写出反应②的离子方程式:___________。(3)已知符合题设转化关系的一组物质如下,写出反应②的化学方程式:___________。
(4)参照以上实例,设计另一组符合上述转化关系的物质组合,写出其化学式:
A___________、B___________、C___________、D___________。
27.(11分)(2022·上海市吴淞中学高三期中)有一种天然黄铜矿主要成分为CuFeS (含SiO),为了测定该
2 2
黄铜矿的纯度,某同学设计了如下实验:
Ⅰ.称取研细的黄铁矿样品0.230g煅烧,生成Cu、Fe O、FeO和SO 气体,实验后取d中溶液的 置于
2 3 2
锥形瓶中,用 标准碘溶液进行滴定,初读数为0.10mL,末读数如图所示。完成 下
列填空:
(1)装置c的作用是___________,上述反应结束后,仍需通一段时间的空气,其目的是
___________。
(2)滴定时,标准碘溶液所耗体积为___________。用化学方程式表示滴定的原理___________。
(3)计算该黄铜矿的纯度___________。
Ⅱ.工业上利用黄铜矿冶炼铜产生的炉渣(Fe O、FeO、SiO、Al O)可制备绿矾FeSO ·7H O晶体。
2 3 2 2 3 4 2
(4)选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂:稀盐酸稀硫酸KSCN溶液KMnO 溶液
4
和NaOH溶液。所选试剂为___________。证明炉渣中含有FeO的实验现象为___________。
(5)将炉渣溶解在足量NaOH溶液中,过滤,取滤渣加入足量稀硫酸和铁屑,过滤后,将滤液___________、
___________、过滤、低温烘干得到绿矾(填写实验操作名称)。
28.(14分)三草酸合铁酸钾晶体(K [Fe(C O)]·3H O)能溶于水,难溶于乙醇,该物质对光敏感,光照下即
3 2 4 3 2
发生分解,产物之一是黄色的草酸亚铁。实验室可用如图流程来制备三草酸合铁酸钾晶体。根据题意完成下列各题:
(1)若用废铁屑和稀硫酸制备绿矾,需先将废铁屑碱煮水洗,其目的是___________;然后与硫酸反应时
___________(填物质名称)往往要过量。
(2)要从溶液中得到绿矾晶体,必须进行的实验操作是___________(按前后顺序填代号)。
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)称取制得的绿矾晶体7.00 g,加稀硫酸溶解。加入一定量的草酸后,加热煮沸,形成黄色沉淀,过滤,
洗涤。如何确定沉淀已经洗涤干净:___________。
(4)氧化过程中除不断搅拌外,还需维持温度在40 ℃左右,原因是___________;写出氧化生成三草酸合
铁酸钾的离子方程式___________。
(5)经过一系列操作后得到的最终产物晶体先用少量冰水洗涤,再用无水乙醇洗涤,低温干燥后称量,得
到9.82 g翠绿色晶体,用无水乙醇洗涤晶体的目的是___________。
(6)列式计算本实验中三草酸合铁酸钾晶体的产率___________(保留一位小数)。
(7)某同学制得的三草酸合铁酸钾晶体表面发黄,推测可能有部分晶体见光分解。为了验证此推测是否正
确,可用的试剂及现象是________________________。
29.(8分)(2022·黑龙江省牡丹江一中高三期中)铜质电路板可采用酸性蚀刻与碱性蚀刻两种方法。将二者
的废液混合可实现回收再利用。其主要流程如图:
已知:①水合肼NH·H O具有强还原性,易被氧化为N
2 4 2 2
②Cu2++4NH Cu(NH )2+
3 3 4
(1)蚀刻
①酸性蚀刻铜的离子方程式:___________
②关于蚀刻的下列说法正确的是___________。
A.碱性蚀刻和酸性蚀刻分别利用了O、HO 的氧化性
2 2 2B.酸性蚀刻时盐酸的主要作用是增强溶液的酸性
C.用HO、HSO 、NaCl也可以使Cu溶解
2 2 2 4
(2)滤液1的pH约为5,其中除少量Cu2+外,还大量存在的离子是___________。
(3)除铜
①利用水合肼NH·H O还原Cu2+的离子方程式是___________。
2 4 2
②已知该反应瞬间完成。滤渣成分只有Cu。测得铜去除率、水合肼还原能力随溶液pH的变化情况如图所
示。由图可知。随溶液pH增大,铜去除率先增加后减小,结合图给值息和己知信息分析其原因:
___________。
30.(12分)黄铜矿(CuFeS)是一种铜铁硫化物矿物,常含微量的金、银等。黄铜矿是冶炼铜及制备铁氧化
2
物的重要矿藏。以黄铜矿为主要原料生产铜、铁红(氧化铁)的工艺流程如下所示:
已知:CuFeS 中Cu为+2价。
2
请回答下列问题:
(1)CuFeS 中 Fe 的 化 合 价 为 ____________ ; 写 出 反 应 Ⅰ 的 离 子 方 程 式 :
2
_______________________________,该反应的氧化剂是________。
(2)CuCl 难溶于水,但可与过量的 Cl-反应生成可溶于水的[CuCl ]-。该反应的离子方程式为
2
______________。
(3)反应Ⅰ~Ⅳ 4个反应中属于非氧化还原反应的是反应________(选填“Ⅰ~Ⅳ”)。
(4)过滤后得到的FeCO 固体应进行洗涤,检验沉淀洗涤干净的方法是___________。
3
(5)反应Ⅲ在高温下进行,该反应的化学方程式为___________。
(6)反应Ⅴ中Na[CuCl ]既是氧化剂,又是还原剂,由此可推知“溶液A”中的溶质为________(写出化学式)。
2
(7)硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的主要反应为:CuFeS+4Fe3+=Cu2++5Fe2+
2
+2S。则下列说法正确的是___________(填序号)。a.从物质分类的角度看,黄铜矿属于合金
b.当转移1mol电子时,有46 g CuFeS 参加反应
2
c.反应中,CuFeS 既作氧化剂又作还原剂
2