文档内容
专题 07 化学反应中的能量变化及机理
2020年高考真题
1.(2020年浙江卷)下列说法不正确的是( )
A.天然气是不可再生能源
B.用水煤气可合成液态碳氢化合物和含氧有机物
C.煤的液化属于物理变化
D.火棉是含氮量高的硝化纤维
2.(2020年浙江卷)关于下列ΔH的判断正确的是( )
CO2− (aq)+H+ (aq)=HCO− (aq) ΔH
3 3 1
CO
3
2- (aq)+H
2
O(l)⇌ HCO−
3
(aq)+OH− (aq) ΔH
2
OH− (aq)+H+ (aq)=H O(l) ΔH
2 3
OH− (aq)+CH COOH(aq)=CH COO− (aq)+H O(l) ΔH
3 3 2 4
A.ΔH <0 ΔH <0 B.ΔH <ΔH C.ΔH <0 ΔH >0D.
1 2 1 2 3 4
ΔH >ΔH
3 4
3.(2020年新课标Ⅰ)铑的配合物离子[Rh(CO) I]-可催化甲醇羰基化,反应过程如图所示。
2 2
下列叙述错误的是
A.CHCOI是反应中间体
3
B.甲醇羰基化反应为CHOH+CO=CH COH
3 3 2C.反应过程中Rh的成键数目保持不变
D.存在反应CHOH+HI=CH I+H O
3 3 2
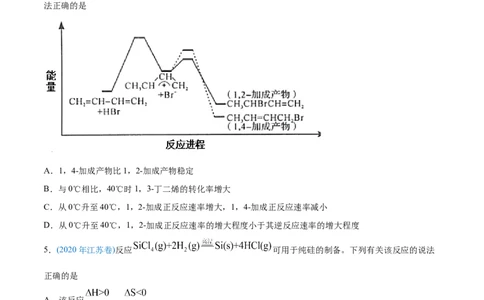
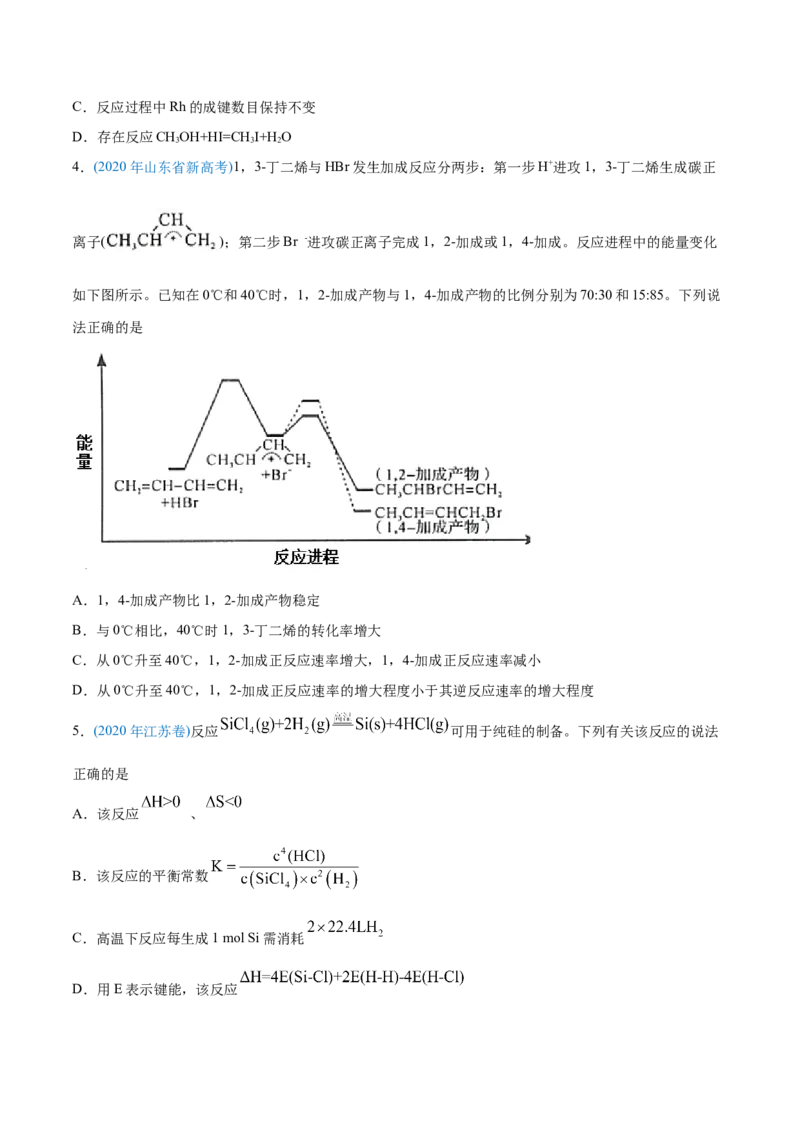
4.(2020年山东省新高考)1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正
离子( );第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化
如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说
法正确的是
A.1,4-加成产物比1,2-加成产物稳定
B.与0℃相比,40℃时1,3-丁二烯的转化率增大
C.从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小
D.从0℃升至40℃,1,2-加成正反应速率的增大程度小于其逆反应速率的增大程度
5.(2020年江苏卷)反应 可用于纯硅的制备。下列有关该反应的说法
正确的是
A.该反应 、
B.该反应的平衡常数
C.高温下反应每生成1 mol Si需消耗
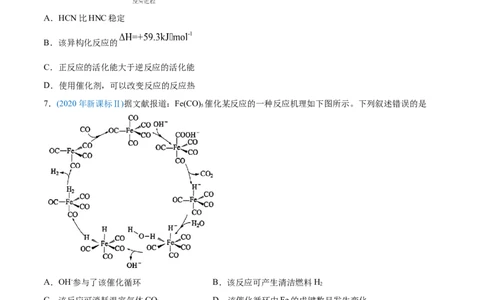
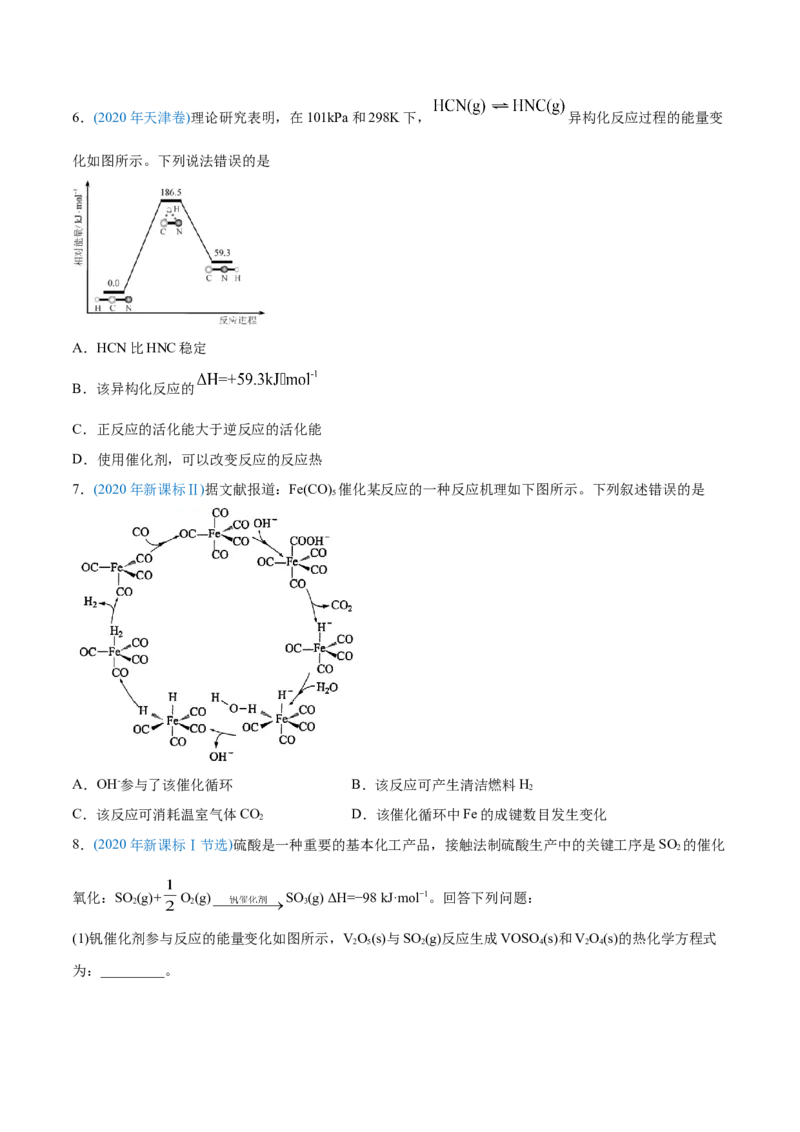
D.用E表示键能,该反应6.(2020年天津卷)理论研究表明,在101kPa和298K下, 异构化反应过程的能量变
化如图所示。下列说法错误的是
A.HCN比HNC稳定
B.该异构化反应的
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
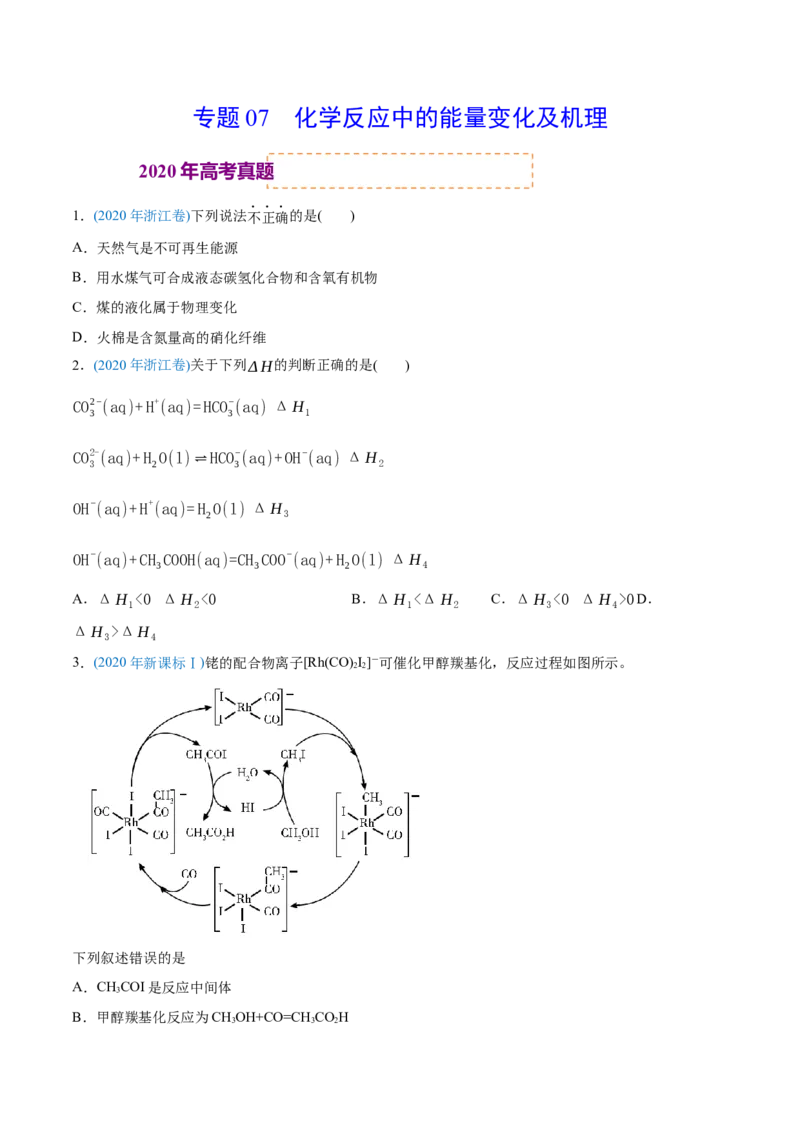
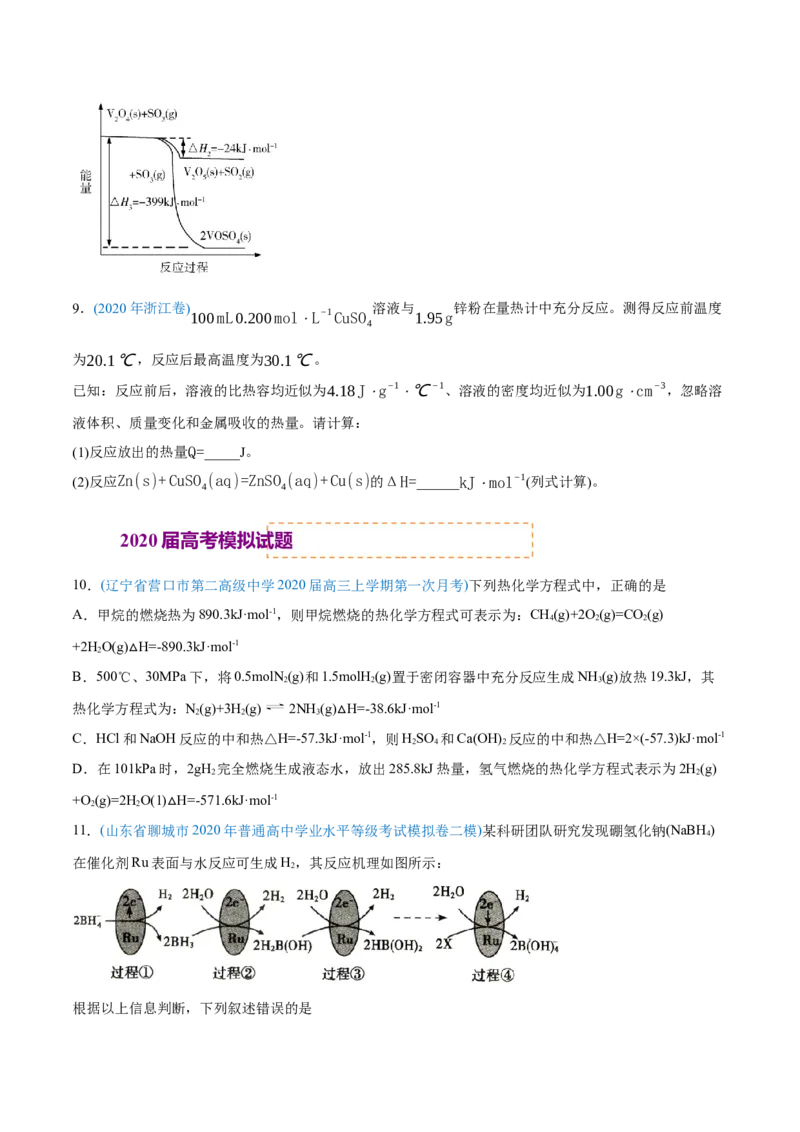
7.(2020年新课标Ⅱ)据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述错误的是
5
A.OH-参与了该催化循环 B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO D.该催化循环中Fe的成键数目发生变化
2
8.(2020年新课标Ⅰ节选)硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO 的催化
2
氧化:SO (g)+ O(g) SO (g) ΔH=−98 kJ·mol−1。回答下列问题:
2 2 3
(1)钒催化剂参与反应的能量变化如图所示,VO(s)与SO (g)反应生成VOSO(s)和VO(s)的热化学方程式
2 5 2 4 2 4
为:_________。9.(2020年浙江卷) 溶液与 锌粉在量热计中充分反应。测得反应前温度
100mL0.200mol⋅L−1CuSO 1.95g
4
为20.1℃,反应后最高温度为30.1℃。
已知:反应前后,溶液的比热容均近似为4.18J⋅g−1 ⋅℃−1、溶液的密度均近似为1.00g⋅cm−3,忽略溶
液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_____J。
(2)反应Zn(s)+CuSO (aq)=ZnSO (aq)+Cu(s)的ΔH=______kJ⋅mol−1(列式计算)。
4 4
2020届高考模拟试题
10.(辽宁省营口市第二高级中学2020届高三上学期第一次月考)下列热化学方程式中,正确的是
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH(g)+2O(g)=CO (g)
4 2 2
+2H O(g) H=-890.3kJ·mol-1
2
B.500℃△、30MPa下,将0.5molN
2
(g)和1.5molH
2
(g)置于密闭容器中充分反应生成NH
3
(g)放热19.3kJ,其
热化学方程式为:N(g)+3H(g) 2NH (g) H=-38.6kJ·mol-1
2 2 3
C.HCl和NaOH反应的中和热△H=-57.3kJ△·mol-1,则HSO 和Ca(OH) 反应的中和热△H=2×(-57.3)kJ·mol-1
2 4 2
D.在101kPa时,2gH 完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H(g)
2 2
+O (g)=2HO(1) H=-571.6kJ·mol-1
2 2
11.(山东省聊城△市2020年普通高中学业水平等级考试模拟卷二模)某科研团队研究发现硼氢化钠(NaBH
4
)
在催化剂Ru表面与水反应可生成H,其反应机理如图所示:
2
根据以上信息判断,下列叙述错误的是A.过程①至过程④中硼元素的化合价不变
B.X是HBO,HBO 和BH 两分子中H的化合价相等
3 3 3 3 3
C.过程③和过程④各产生1molH 时转移的电子数不相等
2
D.0.25molNaBH 的还原能力与标准状况下22.4LH 的还原能力相当(还原能力即生成H+失去电子的量)
4 2
12.(天津市南开区2020届高三年级第二次模拟)硝酸厂的烟气中含有大量的氮氧化物(NO),将烟气与H
x 2
的混合气体通入Ce(SO) 与Ce (SO )[Ce中文名“铈”]的混合溶液中实现无害化处理,其转化过程如图所
4 2 2 4 3
示。下列说法正确的是
A.该转化过程的实质为NO 被H 还原
x 2
B.x=l时,过程II中氧化剂与还原剂的物质的量之比为2:1
C.处理过程中,混合溶液中Ce3+和Ce4+总数减少
D.过程I发生反应的离子方程式:H+Ce4+=2H++Ce3+
2
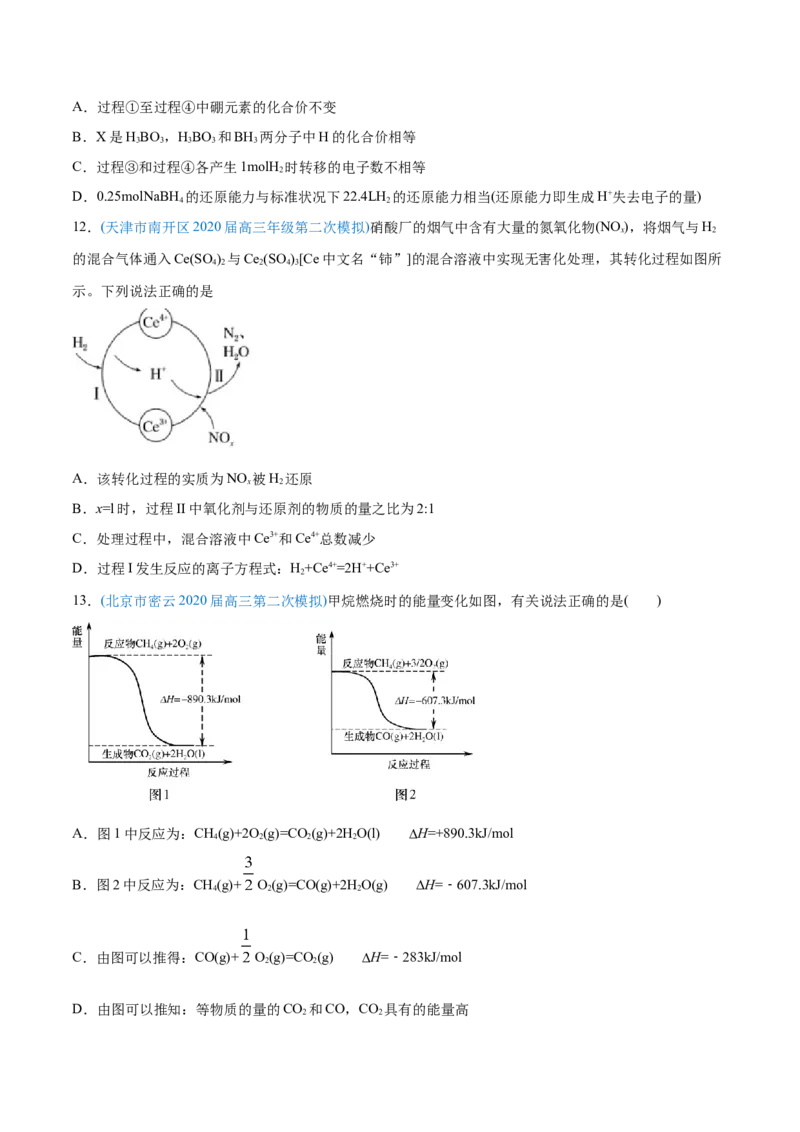
13.(北京市密云2020届高三第二次模拟)甲烷燃烧时的能量变化如图,有关说法正确的是( )
A.图1中反应为:CH(g)+2O(g)=CO (g)+2HO(l) H=+890.3kJ/mol
4 2 2 2
B.图2中反应为:CH(g)+ O(g)=CO(g)+2HO(g) H=﹣607.3kJ/mol
4 2 2
C.由图可以推得:CO(g)+ O(g)=CO (g) H=﹣283kJ/mol
2 2
D.由图可以推知:等物质的量的CO 和CO,CO 具有的能量高
2 214.(上海市松江区2020届高三高考一模)如图是某反应的能量关系图,下列叙述错误的是( )
A.反应物总能量高于生成物的总能量
B.曲线b是使用了催化剂的能量变化曲线
C.反应的热化学方程式为:4HCl(g)+O (g) 2Cl(g)+2HO(g)+115.6kJ
2 2 2
D.若反应生成2mol液态水,放出的热量低于115.6kJ
15.(北大附中2020届高三化学阶段性测试)一氧化碳甲烷化反应为:CO(g) + 3H (g) = CH (g) + HO(g)。
2 4 2
下图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。
下列说法不正确的是
A.步骤①只有非极性键断裂
B.步骤②的原子利用率为 100%
C.过渡态Ⅱ能量最高,因此其对应的步骤③反应速率最慢
D.该方法可以清除剧毒气体CO,从而保护环境
16.(陕西省榆林市2020届高三第三次模拟)中科院兰州化学物理研究所用Fe (CO) /ZSM-5催化CO 加氢
3 12 2合成低碳烯烃反应,所得产物含CH、C H、C H 等副产物,反应过程如图
4 3 6 4 8
下列说法正确的是
A.第i步反应为CO+H=CO+HO
2 2 2
B.第i步反应的活化能低于第ii步
C.Fe (CO) /ZSM-5使CO 加氢合成低碳烯的△H减小
3 12 2
D.添加不同助剂后,反应的平衡常数各不相同
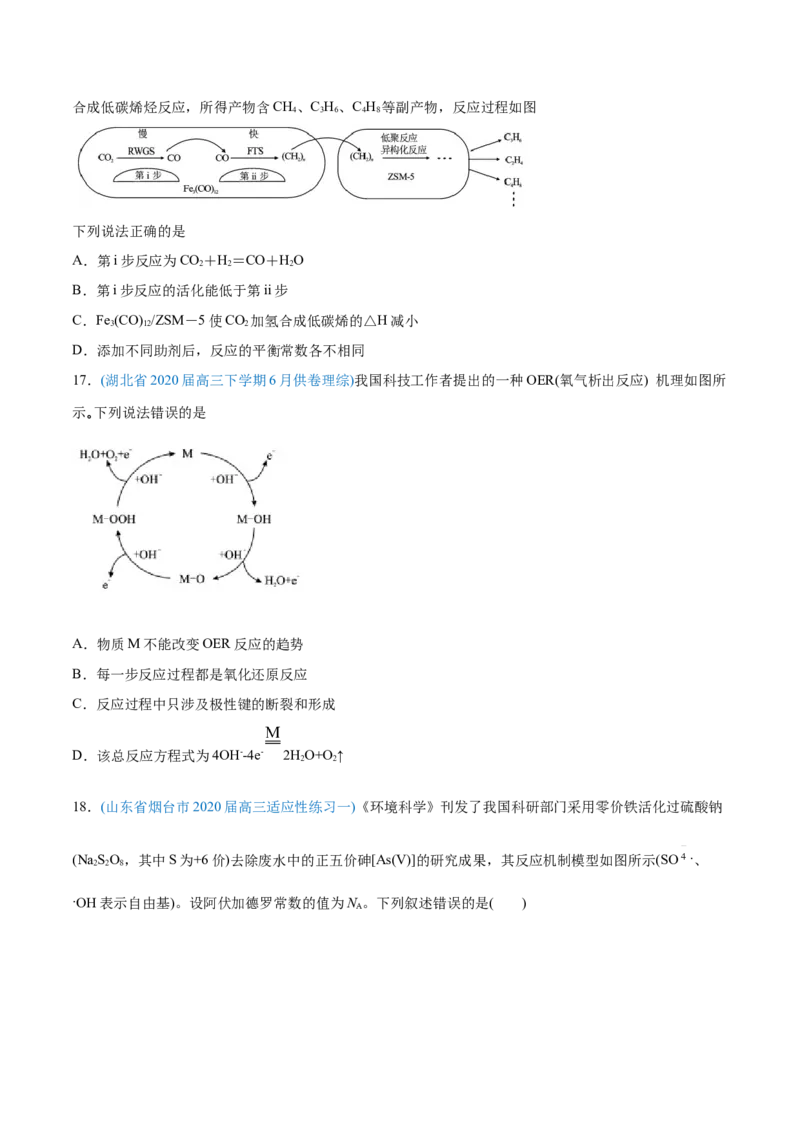
17.(湖北省2020届高三下学期6月供卷理综)我国科技工作者提出的一种OER(氧气析出反应) 机理如图所
示。下列说法错误的是
A.物质M不能改变OER反应的趋势
B.每一步反应过程都是氧化还原反应
C.反应过程中只涉及极性键的断裂和形成
D.该总反应方程式为4OH--4e- 2HO+O↑
2 2
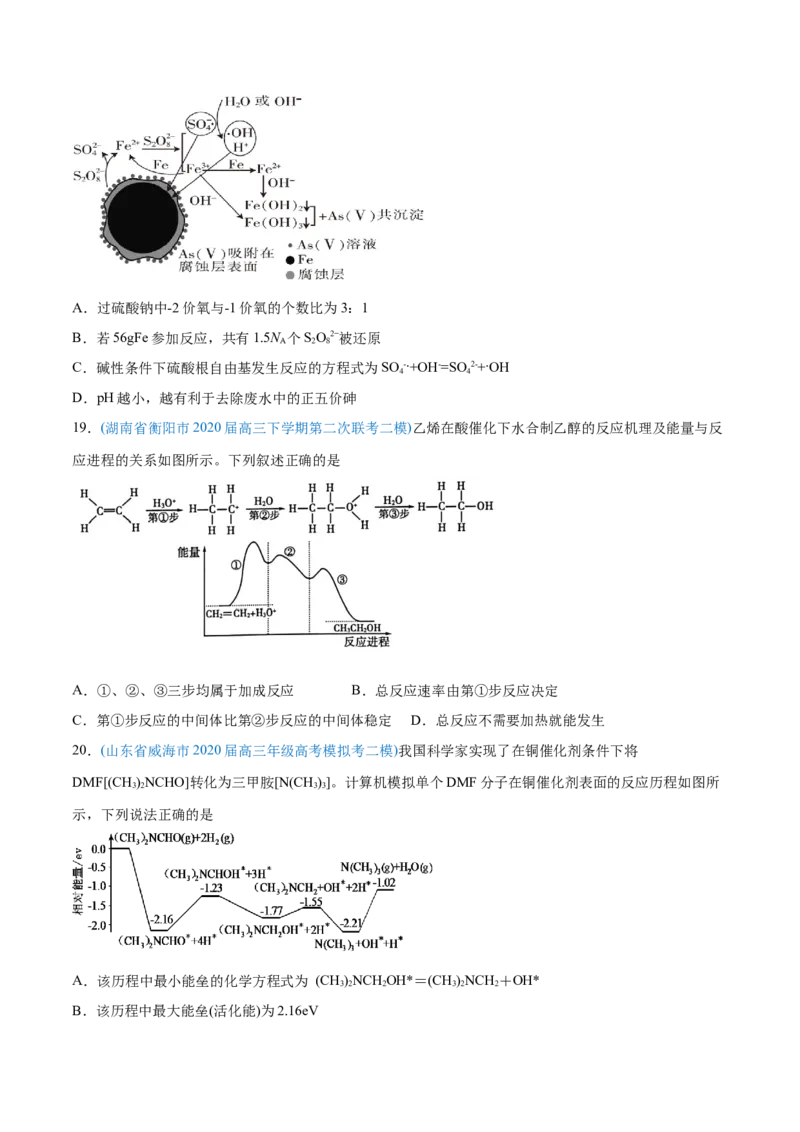
18.(山东省烟台市2020届高三适应性练习一)《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠
(Na SO,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示(SO ·、
2 2 8
·OH表示自由基)。设阿伏加德罗常数的值为N 。下列叙述错误的是( )
AA.过硫酸钠中-2价氧与-1价氧的个数比为3:1
B.若56gFe参加反应,共有1.5N 个SO2−被还原
A 2 8
C.碱性条件下硫酸根自由基发生反应的方程式为SO -·+OH-=SO2-+·OH
4 4
D.pH越小,越有利于去除废水中的正五价砷
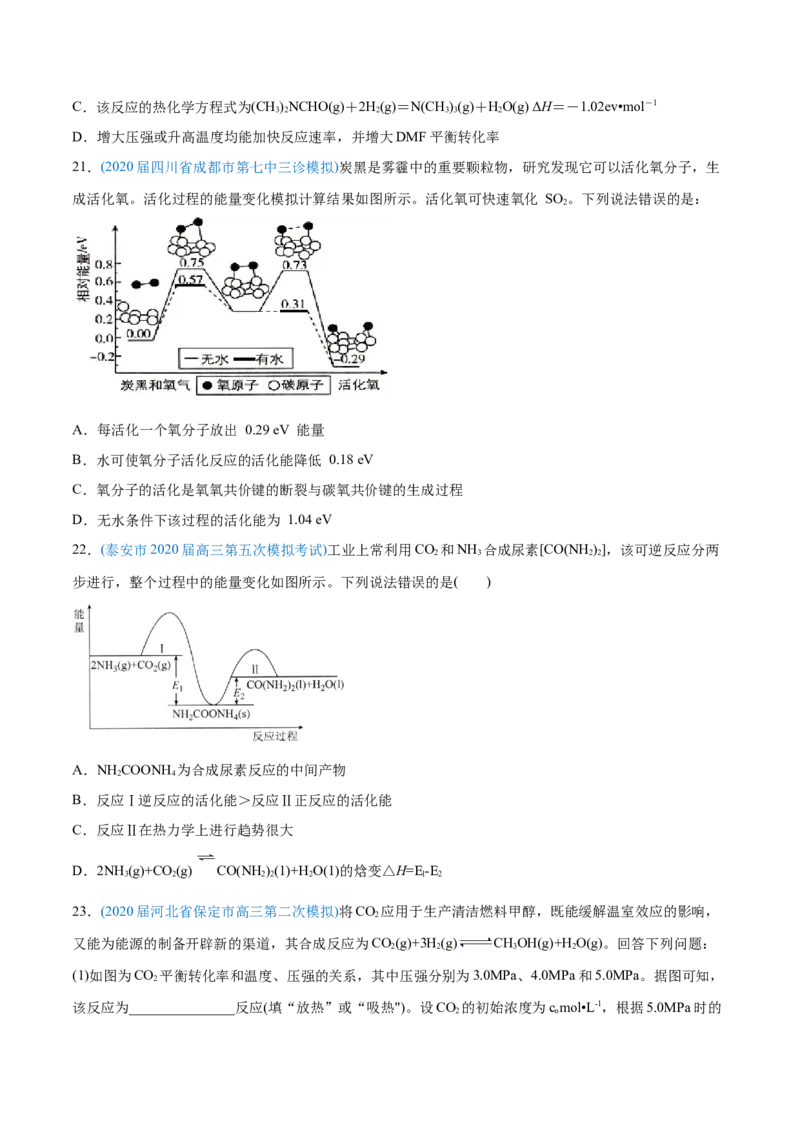
19.(湖南省衡阳市2020届高三下学期第二次联考二模)乙烯在酸催化下水合制乙醇的反应机理及能量与反
应进程的关系如图所示。下列叙述正确的是
A.①、②、③三步均属于加成反应 B.总反应速率由第①步反应决定
C.第①步反应的中间体比第②步反应的中间体稳定 D.总反应不需要加热就能发生
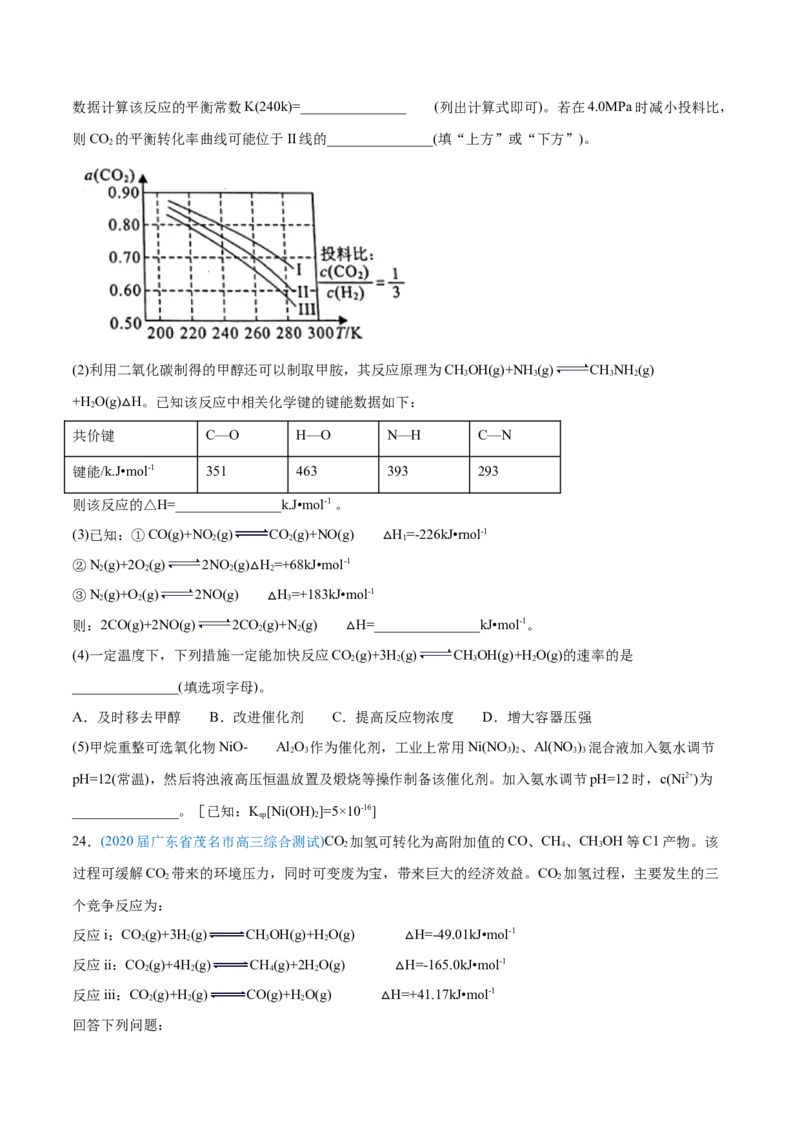
20.(山东省威海市2020届高三年级高考模拟考二模)我国科学家实现了在铜催化剂条件下将
DMF[(CH )NCHO]转化为三甲胺[N(CH )]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所
3 2 3 3
示,下列说法正确的是
A.该历程中最小能垒的化学方程式为 (CH)NCH OH*=(CH)NCH +OH*
3 2 2 3 2 2
B.该历程中最大能垒(活化能)为2.16eVC.该反应的热化学方程式为(CH)NCHO(g)+2H(g)=N(CH )(g)+HO(g) ΔH=-1.02ev•mol-1
3 2 2 3 3 2
D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率
21.(2020届四川省成都市第七中三诊模拟)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生
成活化氧。活化过程的能量变化模拟计算结果如图所示。活化氧可快速氧化 SO 。下列说法错误的是:
2
A.每活化一个氧分子放出 0.29 eV 能量
B.水可使氧分子活化反应的活化能降低 0.18 eV
C.氧分子的活化是氧氧共价键的断裂与碳氧共价键的生成过程
D.无水条件下该过程的活化能为 1.04 eV
22.(泰安市2020届高三第五次模拟考试)工业上常利用CO 和NH 合成尿素[CO(NH)],该可逆反应分两
2 3 2 2
步进行,整个过程中的能量变化如图所示。下列说法错误的是( )
A.NH COONH 为合成尿素反应的中间产物
2 4
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势很大
D.2NH (g)+CO (g) CO(NH)(1)+HO(1)的焓变△H=E-E
3 2 2 2 2 l 2
23.(2020届河北省保定市高三第二次模拟)将CO 应用于生产清洁燃料甲醇,既能缓解温室效应的影响,
2
又能为能源的制备开辟新的渠道,其合成反应为CO(g)+3H(g) CHOH(g)+H O(g)。回答下列问题:
2 2 3 2
(1)如图为CO 平衡转化率和温度、压强的关系,其中压强分别为3.0MPa、4.0MPa和5.0MPa。据图可知,
2
该反应为_______________反应(填“放热”或“吸热")。设CO 的初始浓度为cmol•L-1,根据5.0MPa时的
2 o数据计算该反应的平衡常数K(240k)=_______________ (列出计算式即可)。若在4.0MPa时减小投料比,
则CO 的平衡转化率曲线可能位于II线的_______________(填“上方”或“下方”)。
2
(2)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CHOH(g)+NH(g) CHNH (g)
3 3 3 2
+H O(g) H。已知该反应中相关化学键的键能数据如下:
2
共价键 △ C—O H—O N—H C—N
键能/k.J•mol-1 351 463 393 293
则该反应的△H=_______________k.J•mol-1 。
(3)已知:①CO(g)+NO (g) CO(g)+NO(g) H=-226kJ•rnol-1
2 2 1
②N(g)+2O(g) 2NO (g) H=+68kJ•mol-1 △
2 2 2 2
③N(g)+O(g) 2NO(g) △ H=+183kJ•mol-1
2 2 3
则:2CO(g)+2NO(g) 2CO(△g)+N(g) H=_______________kJ•mol-1。
2 2
(4)一定温度下,下列措施一定能加快反应CO△(g)+3H(g) CHOH(g)+H O(g)的速率的是
2 2 3 2
_______________(填选项字母)。
A.及时移去甲醇 B.改进催化剂 C.提高反应物浓度 D.增大容器压强
(5)甲烷重整可选氧化物NiO- Al O 作为催化剂,工业上常用Ni(NO )、Al(NO ) 混合液加入氨水调节
2 3 3 2 3 3
pH=12(常温),然后将浊液高压恒温放置及煅烧等操作制备该催化剂。加入氨水调节pH=12时,c(Ni2+)为
_______________。[已知:K [Ni(OH) ]=5×10-16]
sp 2
24.(2020届广东省茂名市高三综合测试)CO 加氢可转化为高附加值的CO、CH、CHOH等C1产物。该
2 4 3
过程可缓解CO 带来的环境压力,同时可变废为宝,带来巨大的经济效益。CO 加氢过程,主要发生的三
2 2
个竞争反应为:
反应i:CO(g)+3H(g) CHOH(g)+H O(g) H=-49.01kJ•mol-1
2 2 3 2
反应ii:CO(g)+4H(g) CH(g)+2HO(g) △H=-165.0kJ•mol-1
2 2 4 2
反应iii:CO(g)+H(g) CO(g)+HO(g) H△=+41.17kJ•mol-1
2 2 2
回答下列问题: △(1)由CO、H 合成甲醇的热化学方程式为_____。
2
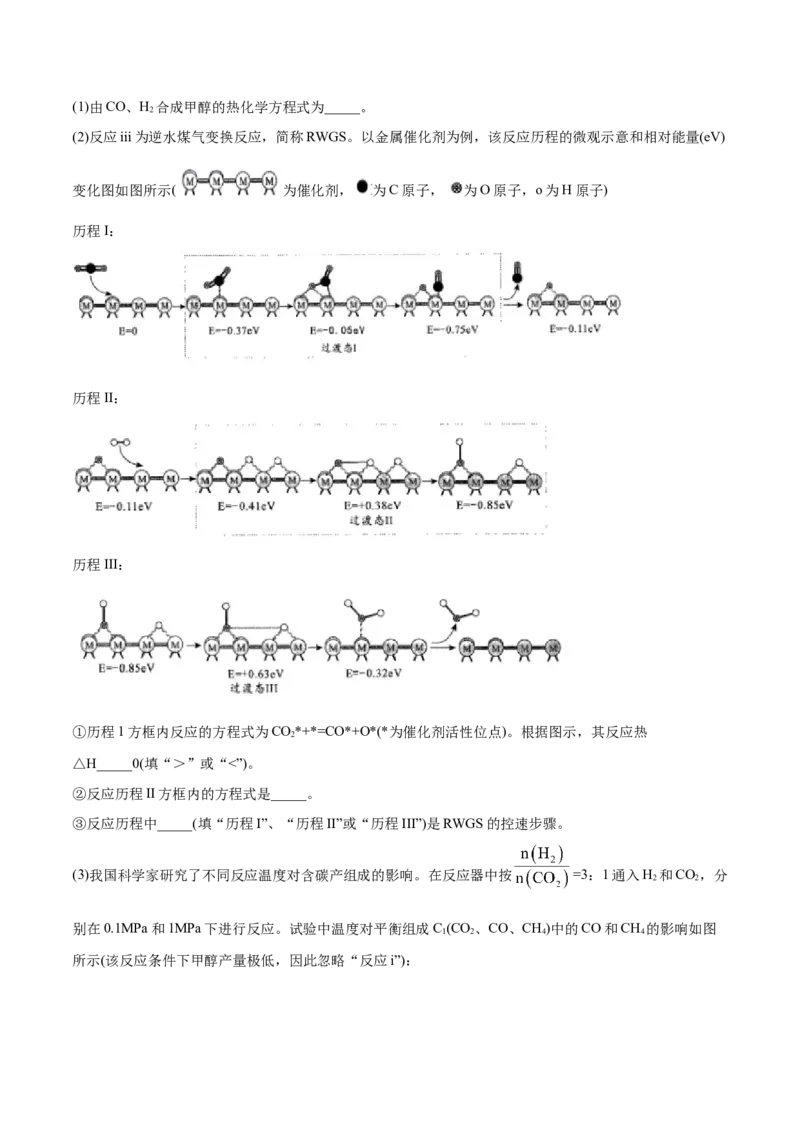
(2)反应iii为逆水煤气变换反应,简称RWGS。以金属催化剂为例,该反应历程的微观示意和相对能量(eV)
变化图如图所示( 为催化剂, 为C原子, 为O原子,o为H原子)
历程I:
历程II:
历程III:
①历程1方框内反应的方程式为CO*+*=CO*+O*(*为催化剂活性位点)。根据图示,其反应热
2
△H_____0(填“>”或“<”)。
②反应历程II方框内的方程式是_____。
③反应历程中_____(填“历程I”、“历程II”或“历程III”)是RWGS的控速步骤。
(3)我国科学家研究了不同反应温度对含碳产组成的影响。在反应器中按 =3:1通入H 和CO,分
2 2
别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C (CO、CO、CH)中的CO和CH 的影响如图
1 2 4 4
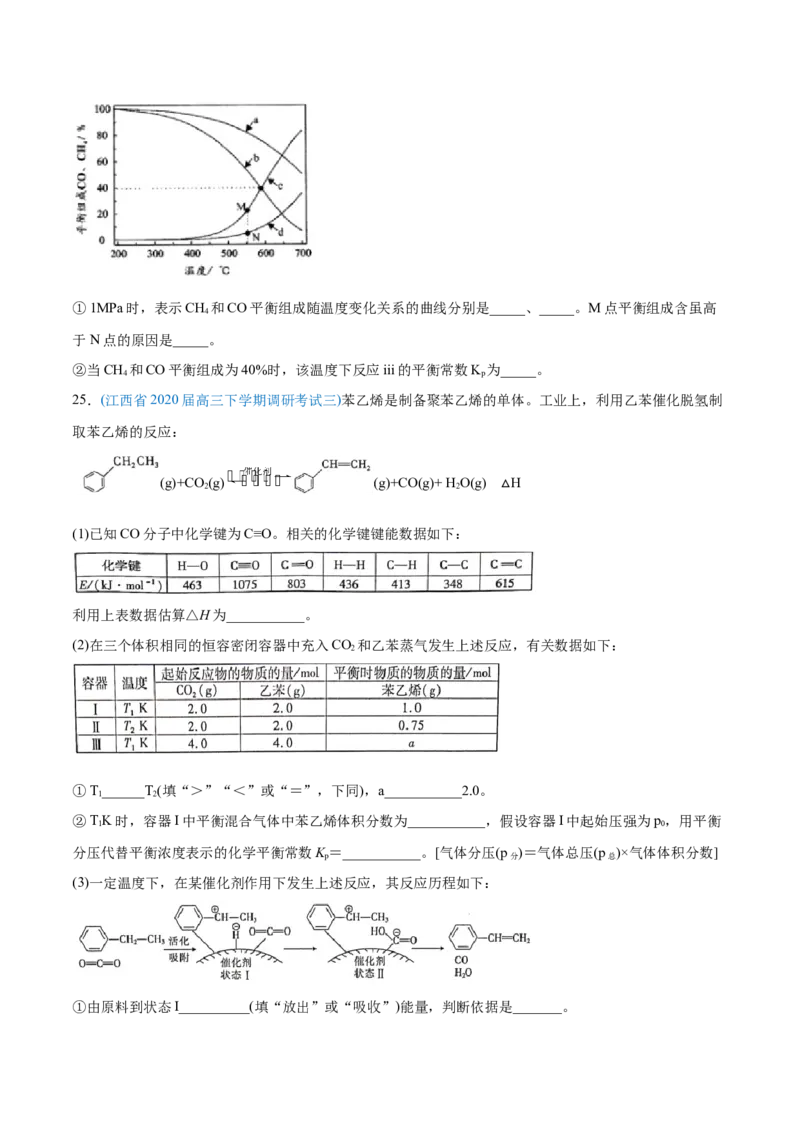
所示(该反应条件下甲醇产量极低,因此忽略“反应i”):①1MPa时,表示CH 和CO平衡组成随温度变化关系的曲线分别是_____、_____。M点平衡组成含虽高
4
于N点的原因是_____。
②当CH 和CO平衡组成为40%时,该温度下反应iii的平衡常数K 为_____。
4 p
25.(江西省2020届高三下学期调研考试三)苯乙烯是制备聚苯乙烯的单体。工业上,利用乙苯催化脱氢制
取苯乙烯的反应:
(g)+CO (g) (g)+CO(g)+ H O(g) H
2 2
△
(1)已知CO分子中化学键为C≡O。相关的化学键键能数据如下:
利用上表数据估算△H为___________。
(2)在三个体积相同的恒容密闭容器中充入CO 和乙苯蒸气发生上述反应,有关数据如下:
2
①T______T(填“>”“<”或“=”,下同),a___________2.0。
1 2
②TK时,容器I中平衡混合气体中苯乙烯体积分数为___________,假设容器I中起始压强为p,用平衡
1 0
分压代替平衡浓度表示的化学平衡常数K =___________。[气体分压(p )=气体总压(p )×气体体积分数]
p 分 总
(3)一定温度下,在某催化剂作用下发生上述反应,其反应历程如下:
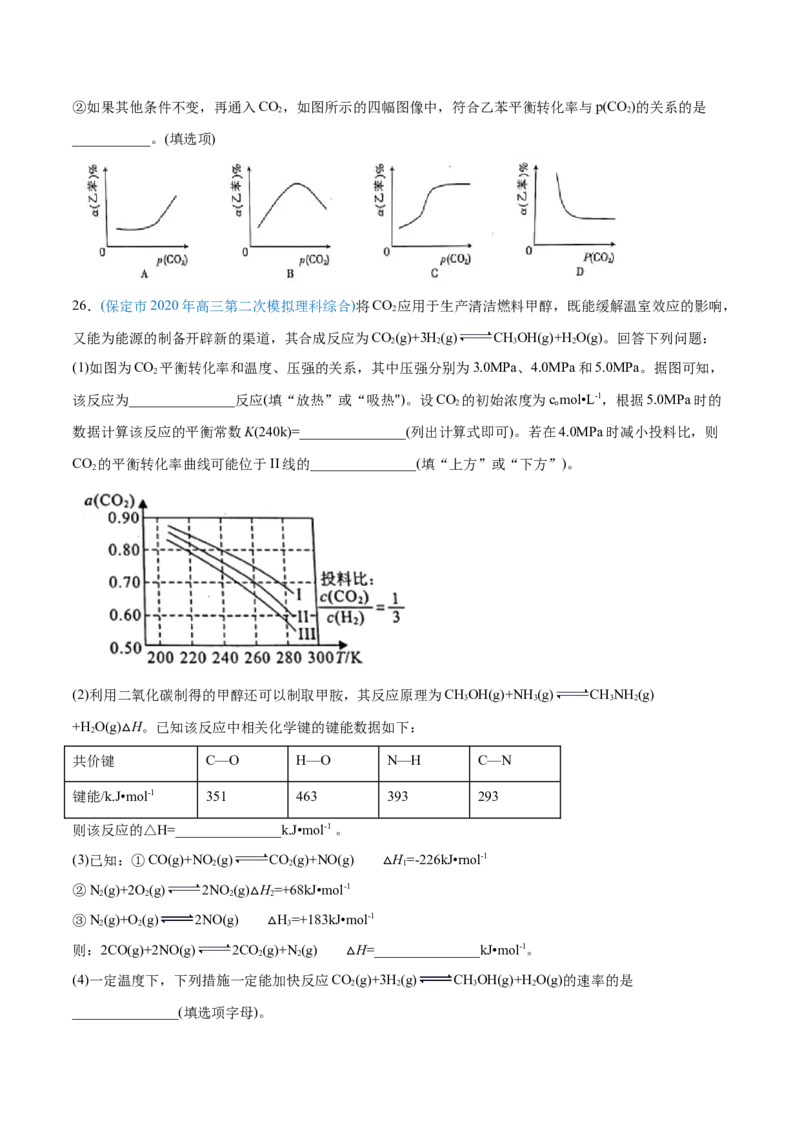
①由原料到状态I__________(填“放出”或“吸收”)能量,判断依据是_______。②如果其他条件不变,再通入CO,如图所示的四幅图像中,符合乙苯平衡转化率与p(CO)的关系的是
2 2
___________。(填选项)
26.(保定市2020年高三第二次模拟理科综合)将CO 应用于生产清洁燃料甲醇,既能缓解温室效应的影响,
2
又能为能源的制备开辟新的渠道,其合成反应为CO(g)+3H(g) CHOH(g)+H O(g)。回答下列问题:
2 2 3 2
(1)如图为CO 平衡转化率和温度、压强的关系,其中压强分别为3.0MPa、4.0MPa和5.0MPa。据图可知,
2
该反应为_______________反应(填“放热”或“吸热")。设CO 的初始浓度为cmol•L-1,根据5.0MPa时的
2 o
数据计算该反应的平衡常数K(240k)=_______________(列出计算式即可)。若在4.0MPa时减小投料比,则
CO 的平衡转化率曲线可能位于II线的_______________(填“上方”或“下方”)。
2
(2)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CHOH(g)+NH(g) CHNH (g)
3 3 3 2
+H O(g) H。已知该反应中相关化学键的键能数据如下:
2
共价键 △ C—O H—O N—H C—N
键能/k.J•mol-1 351 463 393 293
则该反应的△H=_______________k.J•mol-1 。
(3)已知:①CO(g)+NO (g) CO(g)+NO(g) H=-226kJ•rnol-1
2 2 1
②N(g)+2O(g) 2NO (g) H=+68kJ•mol-1 △
2 2 2 2
③N(g)+O(g) 2NO(g) △ H=+183kJ•mol-1
2 2 3
则:2CO(g)+2NO(g) 2CO(△g)+N(g) H=_______________kJ•mol-1。
2 2
(4)一定温度下,下列措施一定能加快反应CO△(g)+3H(g) CHOH(g)+H O(g)的速率的是
2 2 3 2
_______________(填选项字母)。A.及时移去甲醇 B.改进催化剂 C.提高反应物浓度 D.增大容器压强
(5)甲烷重整可选氧化物NiO- Al O 作为催化剂,工业上常用Ni(NO )、Al(NO ) 混合液加入氨水调节
2 3 3 2 3 3
pH=12(常温),然后将浊液高压恒温放置及煅烧等操作制备该催化剂。加入氨水调节pH=12时,c(Ni2+)为
_______________。[已知:K [Ni(OH) ]=5×10-16]
sp 2