文档内容
4.2 元素周期律
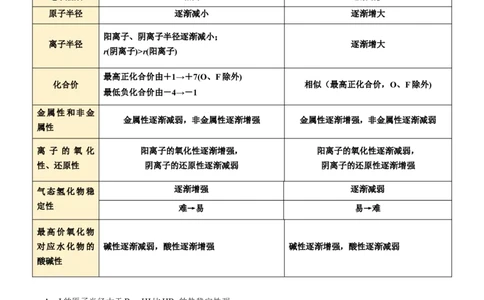
知识点一 同周期、同主族的递变规律
【例1】.(2020·西安市高陵区第一中学月考)下列说法正确的是
同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子半径 逐渐减小 逐渐增大
阳离子、阴离子半径逐渐减小;
离子半径 逐渐增大
r(阴离子)>r(阳离子)
最高正化合价由+1→+7(O、F除外)
化合价 相似(最高正化合价,O、F除外)
最低负化合价由-4→-1
金属性和非金
金属性逐渐减弱,非金属性逐渐增强 金属性逐渐增强,非金属性逐渐减弱
属性
离 子 的 氧 化 阳离子的氧化性逐渐增强, 阳离子的氧化性逐渐减弱,
性、还原性 阴离子的还原性逐渐减弱 阴离子的还原性逐渐增强
气态氢化物稳 逐渐增强 逐渐减弱
定性 难→易 易→难
最高价氧化物
对应水化物的 碱性逐渐减弱,酸性逐渐增强 碱性逐渐增强,酸性逐渐减弱
酸碱性
A.I的原子半径大于Br,HI比HBr的热稳定性强
B.P的非金属性强于Si,HPO 比HSiO 的酸性强
3 4 2 3
C.Al O 和MgO均可与NaOH溶液反应
2 3
D.SO 和SO 混合气体通入Ba(NO ) 溶液可得到BaSO 和BaSO
2 3 3 2 3 4
【答案】B
【解析】A. 非金属性Br>I,则HBr比HI的热稳定性强,A错误;
B. 非金属性P>Si,则HPO 比HSiO 的酸性强,B正确;
3 4 2 3
C. Al O 属于两性氧化物,能与氢氧化钠溶液反应,MgO属于碱性氧化物,与NaOH溶液不反应,C错误;
2 3D. SO 在酸性环境中能被Ba(NO ) 氧化成硫酸钡,则SO 和SO 混合气体通入Ba(NO ) 溶液只得到BaSO
2 3 2 2 3 3 2 4
白色沉淀,D错误;
答案选B。
【一隅三反】
1.(2020·吉林农安·期末)下列各组性质比较错误的是
A.氢化物的热稳定性:HS>HCl B.酸性:HClO >HSO
2 4 2 4
C.碱性: Mg(OH) >Al(OH) D.原子半径Cl>F
2 3
【答案】A
【解析】A.氯元素的非金属性强于硫,所以氢化物的热稳定性是:HS<HCl,A不正确;
2
B.氯元素的非金属性强于硫,故其最高价氧化物的水化物的酸性:HClO 大于HSO ,B正确;
4 2 4
C.镁的金属性强于铝,故其最高价的氧化物的水化物的碱性:Mg(OH) 大于Al(OH) ,C正确;
2 3
D.氯与氟处于同一主族,氯的原子序数较大,同一周期元素的原子半径从上到下依次增大,所以原子半
径:Cl>F,D正确;
本题选A。
2.(2020·全国课时练习)下列叙述正确的是( )
A.Na、K、Ca的电子层数依次增大
B.F、Cl、Br的最外层电子数依次增多
C.Mg、Si、P的原子半径依次增大
D.B、C、N的最高正化合价依次升高
【答案】D
【解析】A. 、 的电子层数相等,A错误;
B. 、 、 的最外层电子数相等,B错误;
C. 同周期,从左到右,原子半径减小, 、 、 的原子半径依次减小,C错误;
D. B、C、N的最高正化合价分别为 、 、 ,D正确;故答案为:D。
3.(2020·全国课时练习)下列关于元素金属性和非金属性强弱比较的说法不正确的是( )
A.根据气态氢化物的热稳定性: ,可得非金属性:
B.Si与 化合所需的温度远高于S与 化合所需的温度,说明S的非金属性强于SiC.Na与冷水反应剧烈,而Mg与冷水反应缓慢,说明Na的金属性强于Mg
D.铁投入 溶液中能置换出铜,钠投入 溶液中不能置换出铜,不能由此判断钠与铁的金属
性强弱
【答案】A
【解析】A.气态氢化物的热稳定性越强,元素非金属性越强,气态氢化物的热稳定性:
,可得非金属性: ,故A错误;
B.Si与 化合所需的温度远高于S与 化合所需的温度,即Si与 化合的难度大于S与 化合的难
度,说明非金属性: ,故B正确;
C.Na与水反应比Mg与水反应剧烈,说明金属性; ,故C正确;
D.钠投入硫酸铜溶液中,钠先和水反应生成NaOH,NaOH再和硫酸铜发生复分解反应,铁能置换出硫酸
铜中的铜,说明Cu的金属性比Fe弱,两个实验不能判断Fe、Na的金属性强弱,故D正确。
故答案:A。
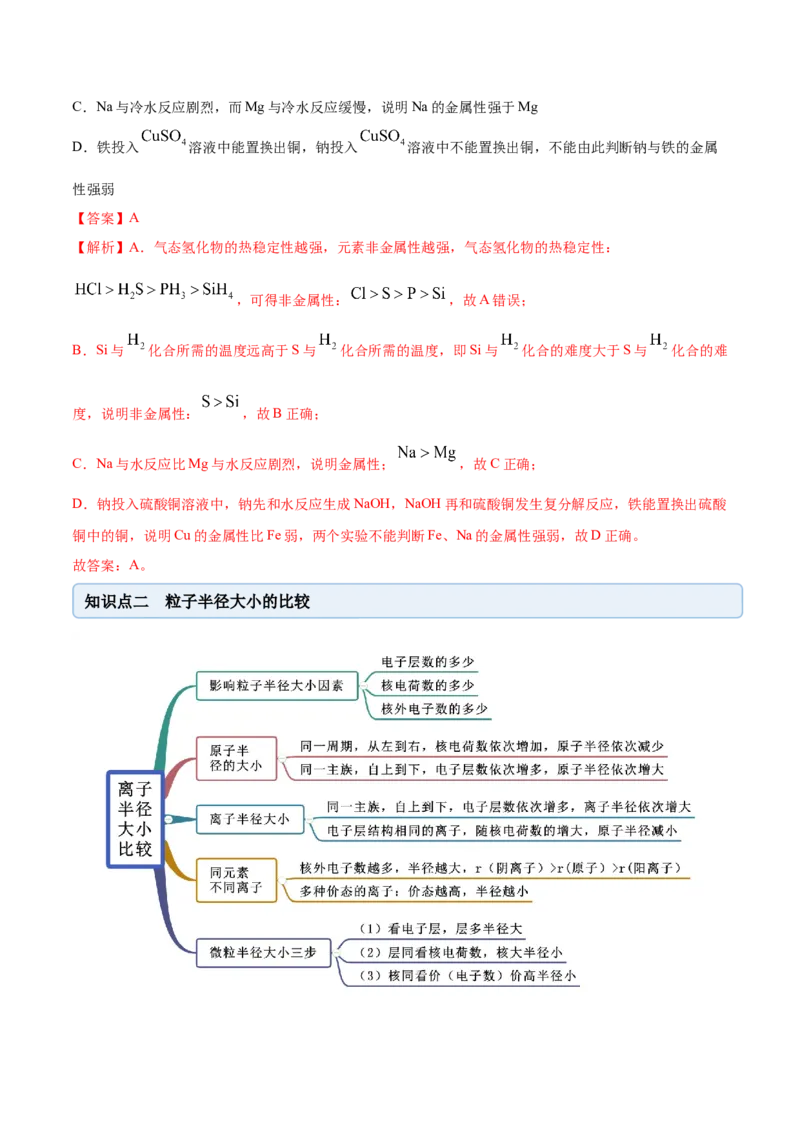
知识点二 粒子半径大小的比较【例2】(2020·上海交大附中高一期末)离子半径由小到大的次序是( )
A.Al3+、Mg2+、O2- B.K+、Na+、Li+
C.K+、C1-、F- D.I-、Br-、Cl-
【答案】A
【解析】A.Al3+、Mg2+、O2-三种离子具有相同的核外电子排布,故比较核电荷数,核电荷数越大,半径
越小,故Al3+、Mg2+、O2-离子半径依次增大,A符合题意;
B.K+、Na+、Li+属于同一主族元素的离子半径,从上往下依次增大,故K+、Na+、Li+依次较小,B不合题
意;
C.K+和C1-具有相同的核外电子排布,故半径K+比C1-小,根据电子层数越多,一般半径越大,故F-半径
最小,故C1-、K+、F-的半径依次减小,C不合题意;
D.I-、Br-、Cl-属于同一主族元素的离子半径,从上往下依次增大,故I-、Br-、Cl-依次减小,D不合题意;
故答案为:A。
【一隅三反】
1.(2020·吉林农安·期末)下列粒子中,半径最小的是( )
A.Na+ B.Na C.Mg2+ D.Cl-
【答案】C
【解析】同一元素的不同离子,核外电子数越多,半径越大,所以半径:Na>Na+;核外电子排布相同的
微粒,核电荷数越大,半径越小,所以半径:Na+>Mg2+;电子层越多,半径越大,所以半径:Cl>Na+,
综上分析,半径最小的是Mg2+,答案选C。
2.(2020·全国高一课时练习)下列各微粒半径依次减小的是( )
A. 、 、 、 B. 、 、 、
C.F、 、 、 D.Al、Mg、Na、K
【答案】B
【解析】A.电子层结构相同,核电荷数越大离子半径越小,故离子半径 > > > ,选项A错
误;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径 >K+>
Mg2+>Al3+,选项B正确;
C.电子层越多离子半径越大,原子半径小于相应的阴离子半径,故离子半径F<F-<Cl-<Br-,选项C错误;
D.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故微粒半径K>Na>Mg>Al,选项D
错误;答案选B。
3.(2020·湖北武汉·期中)X、Y、Z 均为元素周期表中前三周期元素,Xb+、Yb−、Z(b+1)−三种简单离
子的电子层结构相同,下列说法正确的是( )
A.原子半径的大小顺序为:Z > Y > X
B.离子半径的大小顺序为:Yb− > Z(b+1)− > Xb+
C.原子序数的大小顺序为:X>Y>Z
D.气态氢化物的稳定性:H Z > H Y
(b+1) b
【答案】C
【解析】A.X处于Y、Z的下一周期,核电荷数X>Y>Z,X比Y和Z多一个电子层,同一周期核电荷
数越大,原子半径越小,故原子半径大小关系X>Z>Y,故A错误;
B.核电荷数X>Y>Z,电子层结构相同核电荷数越大离子半径越小,故离子半径Z(b+1)->Yb->Xa+,故B
错误;
C.核电荷数X>Y>Z,故原子序数X>Y>Z,故C正确;
D.非金属性Z<Y,非金属性越强,氢化物越稳定,故稳定性H Z<HY,故D错误,
b+1 b
故选C。
4.(2020·全国课时练习)下列微粒半径比值大于1的是( )
A. B. C. D.
【答案】B
【解析】A.同主族元素从上到下原子半径依次增大,即 ,故 ,A不合题意;
B.因 、 具有相同的电子层结构,故离子半径随核电荷数的增大而减小,即 ,
故 ,B符合题意;
C.同周期主族元素从左到右原子半径依次减小,即 ,故 ,C不合题意;D.同种元素的阴离子半径>原子半径,即 ,故 ,D不合题意;
故答案为:B 。
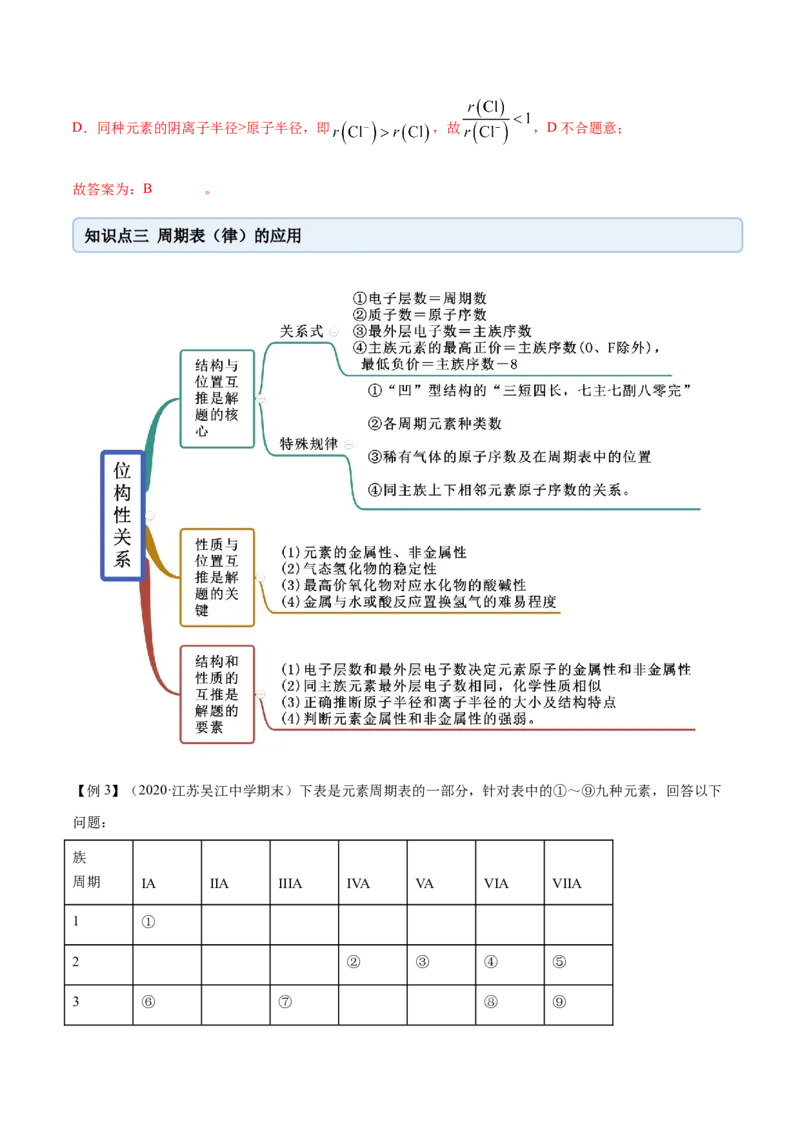
知识点三 周期表(律)的应用
【例3】(2020·江苏吴江中学期末)下表是元素周期表的一部分,针对表中的①~⑨九种元素,回答以下
问题:
族
周期 IA IIA IIIA IVA VA VIA VIIA
1 ①
2 ② ③ ④ ⑤
3 ⑥ ⑦ ⑧ ⑨(1)①⑥形成的简单化合物的电子式为______________。
(2)②与④形成的某种气体能产生温室效应,其结构式为______________。
(3)③⑤⑦元素原子形成简单离子的离子半径由大到小的顺序为________________(填离子符号)。
(4)在这些元素形成的氧化物中,不溶于水,但既能与强酸反应又能与强碱溶液反应的是________(填化学
式)。
(5)元素⑥与元素⑦相比,金属性较强的是________(填元素符号),下列表述中能证明这一事实的是
________(填字母)。
a.⑥单质的熔点比⑦单质低
b.⑥单质与水反应比⑦单质剧烈
c.⑥最高价氧化物对应的水化物的碱性比⑦强
d.⑥的化合价比⑦低
(6)⑧的低价氧化物通入⑨单质的水溶液中,发生反应的化学方程式为
_________________________________________________________________。
(7)比较⑧、⑨气态氢化物的稳定性:________>________(填化学式),除了可以通过比较⑧、⑨气态氢化物
的稳定性来验证⑧、⑨的非金属性外,请你再设计一个简单的实验,来验证元素⑧与⑨的非金属性强弱:
___________________________。
【答案】(1)Na+ [H:]-
(2) O=C=O
(3) N3-> F-> Al3+
(4) Al O
2 3
(5) Na bc
(6) SO +Cl+2HO=HSO +2HCl
2 2 2 2 4
(7) HCl H S
2
(8) 在NaS的溶液中通入Cl,若溶液变浑浊,证明Cl的非金属性强于S,反应的化学方程式为NaS+
2 2 2
Cl=S↓+2NaCl(其他合理答案亦可)
2
【解析】(1)①⑥形成的简单化合物为NaH,NaH是离子化合物,电子式是Na+ [H:]-;
(2) ②与④形成的能产生温室效应的气体为CO,其结构式为O=C=O;
2
(3)电子层结构相同的离子随着核电荷数的增多,离子半径逐渐减小,离子半径由大到小的顺序是N3-> F->
Al3+;(4)在这些元素形成的氧化物中,Al O 是两性氧化物,不溶于水,既与强酸反应,又与强碱溶液反应;
2 3
(5)同周期元素从左到右金属性减弱,元素Na与元素Al相比,金属性较强的是Na;
a.单质的熔点与金属性无关,故不选a;
b.金属性越强,单质越易与水反应,Na与水反应比Al剧烈,说明金属性Na大于Al,故选b;
c.金属性越强,最高价氧化物对应的水化物的碱性越强,Na最高价氧化物对应的水化物的碱性比Al强,
说明金属性Na大于Al,故选c;
d.只根据Na的化合价比Al低,不能说明金属性Na大于Al,故不选d;
(6) S的低价氧化物是SO ,SO 通入氯水中, SO 与Cl 反应生成盐酸和硫酸,化学方程式为SO +Cl+
2 2 2 2 2 2
2HO===H SO +2HCl;
2 2 4
(7)非金属性越强气态氢化物越稳定,由于Cl的非金属性强于S,所以HCl的稳定性大于HS;
2
(8)可以通过非金属单质间的置换反应来证明元素非金属性的强弱。在NaS的水溶液中通入Cl,若溶液变
2 2
浑浊,证明Cl的非金属性强于S,反应的化学方程式为NaS+Cl===S↓+2NaCl。
2 2
【一隅三反】
1.(2020·全国课时练习)如图是部分短周期元素的常见化合价与原子序数的关系:
(1)元素 在元素周期表中的位置是__________________。
(2)其中金属性最强的元素是______(用元素符号表示,下同),非金属性最强的元素是______。
(3) 、 、 的半径由大到小的顺序是__________(用离子符号表示)。
(4)最简单氢化物的稳定性: ______ (填“ ”或“ ”)。
(5) 、 、 元素最高价氧化物对应水化物的酸性:_____(用化学式表示,下同) ______ ______。
(6) 与 形成的具有强氧化性的化合物为______(填化学式),该化合物与 反应的化学方程式为
________________________,其中氧化剂与还原剂的物质的量之比为____________。【答案】(1)第2周期第ⅣA族
(2)
(3)
(4)<
(5)
(6)
【解析】(1)A为碳元素,原子有2个电子层,最外层电子数为4,处于周期表中第二周期ⅣA族;
(2)金属性最强的元素为Na,非金属性最强的为O;
(3)电子层教越多,离子半径越大;电子层结构相同的离子,核电荷数越小,离子半径越大,故离子半径:
。
(4)元素的非金属性: ,则最简单氢化物的稳定性: 。
(5)由于元素的非金属性: ,则最高价氧化物对应水化物的酸性:
。
(6) 和 元素形成的具有强氧化性的化合物是 , 是 ,二者发生反应的化学方程式为
,其中 既是氧化剂又是还原剂,氧化剂与还原剂的物质的量之比
为 。
2.(2020·全国课时练习)根据短周期元素的信息回答问题。
元素信息
A 第3周期第ⅥA族
B 族序数是周期数的3倍C 原子序数是11
D D3+与Ne电子数相同
(1)写出A、B的元素符号____________、_________,C、D的元素的名称__________、_____________。
(2)写出B、C单质在加热时反应的方程式____________________________________
(3)从原子结构角度分析A与B的______________相同,C与D的_______________相同。
【答案】(1)S O 钠 铝
(2) 、
(3) 最外层电子数 电子层数
【解析】(1)由上述分析可知,A为S;B为O;C为钠;D为铝;
(2)钠与氧气在加热时生成过氧化钠,反应方程式为: ;铝单质与氧气在加热时反应
生成氧化铝,其反应方程式为: ;
(3)A为S,B为O,二者同主族,C为Na、D为Al,二者同周期,从原子结构的角度分析,A原子与B
原子的最外层电子数相同;C原子与D原子的电子层数相同。
3..(2020·全国课时练习)已知铷( )是37号元素,其相对原子质量是85.5,与钠同主族,回答下列问
题:
(1)铷位于第_________周期,其原子半径比钠元素的原子半径_________(填“大”或“小”)。
(2)铷单质性质活泼,写出它在氯气中燃烧的化学方程式:__________。铷单质易与水反应,反应的离子方
程式为_______,实验表明,铷与水反应比钠与水反应_________(填“剧烈”或“缓慢”)。
(3)同主族元素的同类化合物的化学性质相似,写出过氧化铷与 反应的化学方程式:_______。
(4)现有铷和另一种碱金属形成的合金 ,当该合金与足量水反应时,可得到 (标准状况下)氢气,
则另一种碱金属可能是________(填序号)。
a. b. c. d.
【答案】(1)五 大
(2) 剧烈(3)
(4)ab
【解析】(1) 据元素周期表的结构知,第4周期0族元素的原子序数为36,故37号元素铷( )位于第五周
期ⅠA;
(2) 元素位于同主族时,从上到下,随着核电荷数增大,电子层数增多,原子半径递增,故铷原子半径大,
同一主族元素,化学性质相似,则铷与氯气反应生成氯化铷,化学方程式为: 、铷
单质与水反应生成氢氧化铷和氢气,离子方程式为: ,同一主族,从上
到下,金属性递增,则铷的还原性比钠强,与水反应比钠剧烈;
(3) 同主族元素的同类化合物的化学性质相似,则过氧化铷与 反应,可根据过氧化钠和二氧化碳的反
应类推,过氧化钠和二氧化碳反应生成碳酸钠和氧气,则过氧化铷和二氧化碳反应生成碳酸铷和氧气,化
学方程式为: ;
(4)由生成氢气的量可知, 合金共失去 电子, 纯铷失去的电子少于 ,故 的另一种
碱金属与水反应失去的电子应多于 ,结合各碱金属元素的相对原子质量可知 、 符合要求,故
选ab。