文档内容
第四章 物质结构 元素周期律
第三节 化学键 课时作业
第一课时 离子键
基础达标
1.下列说法中正确的是( )
A.熔化状态下能导电的物质一定是离子化合物
B.离子化合物不可能只含非金属元素
C.离子化合物均能溶于水
D.离子化合物在一定条件下可以转化成分子
2.下列物质中含有离子键的是( )
A.HO B.HCl
2
C.N D.MgCl
2 2
3.与氖原子的核外电子排布相同的离子跟与氩的核外电子排布相同的离子所形成的化
合物是( )
A.MgBr B.NaS
2 2
C.KCl D.KS
2
4.以下叙述中,错误的是 ( )
A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强
B.在氯化钠中,除氯离子和钠离子的静电吸引作用外,还存在电子与电子,原子核
与原子核之间的排斥作用
C.任何离子键在形成的过程中必定有电子的得与失
D.钠与氯反应生成氯化钠后,体系能量降低
5.下列离子化合物的电子式不正确的是 ( )
A.氯化钙: B.硫化钠:
C.氟化钾: D.过氧化钠:
6.下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合
形成稳定化合物的是 ( )
A.10与19 B.6与16
C.11与17 D.14与8
7.下列关于离子键的说法中,正确的是( )
A.阴、阳离子间的相互吸引即离子键B.非金属元素所组成的化合物中不可能有离子键
C.ⅠA族元素与VIA族元素之间形成的化合物一定含离子键
D.某化合物在熔融状态下能导电,该化合物一定含离子键
8.下列说法正确的是 ( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl 中,两个氯离子之间也存在离子键
2
D.含有离子键的化合物一定是离子化合物
9.下列有关离子键和离子化合物的说法中正确的是( )
A.凡含离子键的化合物,一定含金属元素
B.强碱、盐、活泼金属氧化物不属于离子化合物
C.离子化合物一定能电离
D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键
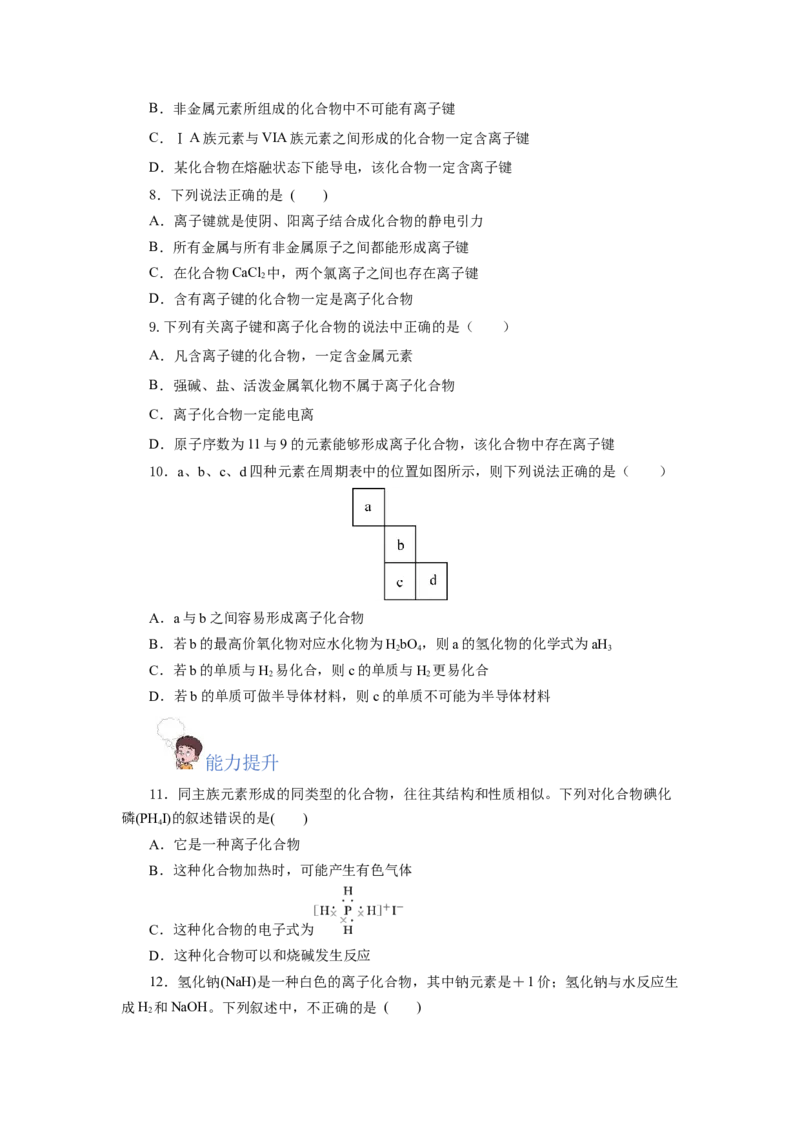
10.a、b、c、d四种元素在周期表中的位置如图所示,则下列说法正确的是( )
A.a与b之间容易形成离子化合物
B.若b的最高价氧化物对应水化物为HbO,则a的氢化物的化学式为aH
2 4 3
C.若b的单质与H 易化合,则c的单质与H 更易化合
2 2
D.若b的单质可做半导体材料,则c的单质不可能为半导体材料
能力提升
11.同主族元素形成的同类型的化合物,往往其结构和性质相似。下列对化合物碘化
磷(PH I)的叙述错误的是( )
4
A.它是一种离子化合物
B.这种化合物加热时,可能产生有色气体
C.这种化合物的电子式为
D.这种化合物可以和烧碱发生反应
12.氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应生
成H 和NaOH。下列叙述中,不正确的是 ( )
2A.NaH的电子式为Na+[H]-
B.NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同
C.微粒半径H-<Li+
D.NaH与HO反应时,水作氧化剂
2
13.X、Y、Z、W 是原子序数依次增大的不同主族的短周期元素,X、Y 的简单离子
的核外电子数相同,Y 的原子半径是短周期主族元素原子中最大的,Z原子最外层电子数
是K 层的3 倍。下列说法正确的是 ( )
A.简单离子半径:Y>Z B.X 只能形成HXO 型的酸
3
C.气态氢化物的热稳定性:W