文档内容
专题 08 元素周期律与元素周期表
1.2022年IUPAC命名117号元素为Ts(中文名“ ”,tián),Ts的原子核外最外层电子数是7,下列说法
不正确的是( )
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是Ts
答案:D
解析:中子数为176的Ts核素,其质量数为176+117=293,核素符号是Ts,D错误。
2.已知X、Y、Z、T、W是短周期中原子序数依次增大的5种主族元素,其中X、T同主族,X与Y形成
的气态化合物能使湿润的红色石蕊试纸变蓝,Z原子的最外层电子数是电子层数的3倍,W是一种重要的
半导体材料。下列说法正确的是( )
A.原子半径:XO,A项错误。N的含氧酸有硝酸和
亚硝酸等,其中亚硝酸为弱酸,B项错误。Z、T和W三种元素形成的化合物为硅酸钠,水解后溶液呈碱
性,C项正确。元素Z、T组成的化合物为氧化钠或过氧化钠,其阴、阳离子个数之比均为 1:2,D项错
误。
3.X、Y、Z、W是原子序数依次增大的短周期主族元素,经常在食品包装袋中充入 Y的单质气体延缓食
品的腐败,由X、W形成的一种化合物与Z、W形成的一种化合物反应,生成淡黄色固体。下列说法正确
的是( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.上述四种元素可以形成阴、阳离子数之比为1:1的离子化合物
C.气态氢化物的稳定性:Y>Z
D.单质沸点:X>Y>Z
答案:B
解析:经常在食品包装袋中充入Y的单质气体(氮气)延缓食品的腐败,则Y是N。由X、W形成的一种化
合物与Z、W形成的一种化合物反应,生成淡黄色固体,该淡黄色固体只能是单质 S,所以两种化合物分别是HS和SO ,反应得到单质S。所以X为H,Y为N,Z为O,W为S。O与S位于同主族,从上到
2 2
下,原子半径依次增大,则r(S)>r(O),A项错误。上述四种元素可以形成阴、阳离子数之比为 1:1的离
子化合物 NH HSO ,B 项正确。同周期主族元素从左向右,气态氢化物的稳定性增强,所以稳定性
4 3
HO>NH ,C项错误。O 、N 和H 的相对分子质量逐渐减小,所以分子间作用力减小,所以单质沸点为
2 3 2 2 2
HY>Z>W
B.最高价氧化物对应水化物的碱性:XO2->Na+> Al3+,A项错误。元素金属性越强,其最高价氧化物对应的水化物碱性越强,钠比铝的金属性
强,故最高价氧化物对应水化物的碱性NaOH>Al(OH) ,B项错误。工业电解饱和氯化钠溶液可得氯气,C
3
项正确。向NaO 中加入过量AlCl 溶液能产生氢氧化铝沉淀,D项错误。
2 2 3
5.四种短周期元素在周期表中的位置如图,其中 Y元素原子电子层数等于最外层电子数。下列说法不正
确的是( )
A.Z位于元素周期表中第三周期第ⅣA族
B.Y的最高价氧化物不能和X的气态氢化物反应
C.M的非金属性比Z的弱
D.原子半径:XO,D项正
确。
6.[2022·福建毕业班质检]X、Y、Z、W为原子序数递增的四种短周期元素,其中Y、Z为金属元素。X、
Y、Z、W的最高价氧化物对应水化物甲、乙、丙、丁之间存在如下图所示反应关系(图中“—”相连的两
种物质能发生反应)。下列判断一定正确的是( )A.X是元素周期表中非金属性最强的元素
B.Z位于元素周期表第三周期ⅠA族
C.4种原子中,Y原子半径最大
D.W的最高化合价为+7
答案:C
解析:Y、Z是金属,且其最高价氧化物对应水化物之间可以发生反应,则 Y是Na,Z是Al,乙是
NaOH,丙是Al(OH) ;X、W为非金属,它们的最高价氧化物对应水化物甲和丁都可以和 Al(OH) 反应,
3 3
故甲和丁都是强酸,第二周期最高价氧化物对应水化物是强酸的只有N,故X为N,第三周期最高价氧化
物对应水化物是强酸的有S和Cl,故W为S或Cl。元素周期表中非金属性最强的元素是F,A错误;铝位
于第三周期ⅢA族,B错误;原子半径Na>Al>S(Cl)>N,C正确;S的最高化合价为+6价,Cl的最高化合
价为+7价,D错误。
1.(2022·上海市复旦附中高三期中)科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短
周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是( )
A.WZ的水溶液呈碱性
B.元素非金属性强弱的顺序为
C.Y的最高价氧化物的水化物是弱电解质
D.该新化合物中Y不满足8电子稳定结构
【答案】C
【解析】W、X、Y、Z为同一短周期元素,则不可能为第一周期元素,由化合物结构可知Z形成1个共价
单键,最外层电子数为7,X形成4个共价单键,最外层电子数为4,Z的核外最外层电子数是X核外电子
数的一半可知,Z为Cl、X为Si,则W为Na,由结构可知Y原子最外层电子数为8-2-1=5,为P。A项,
WZ即NaCl,NaCl为强酸强碱正盐,水溶液呈中性,故A错误;B项,X为Si,Y为P,Z为Cl,同周期
元素从左到右,非金属性依次增强,则非金属性的强弱顺序为Z(Cl)>Y(P)>X(Si),故B错误;C项,Y为
P,P元素的最高价氧化物对应水化物为磷酸,磷酸是三元中强酸,只能部分电离,属于弱电解质,故C正
确;D项,新化合物中P元素最外层电子数为5+2+1=8,满足8电子稳定结构,故D错误;故选C。
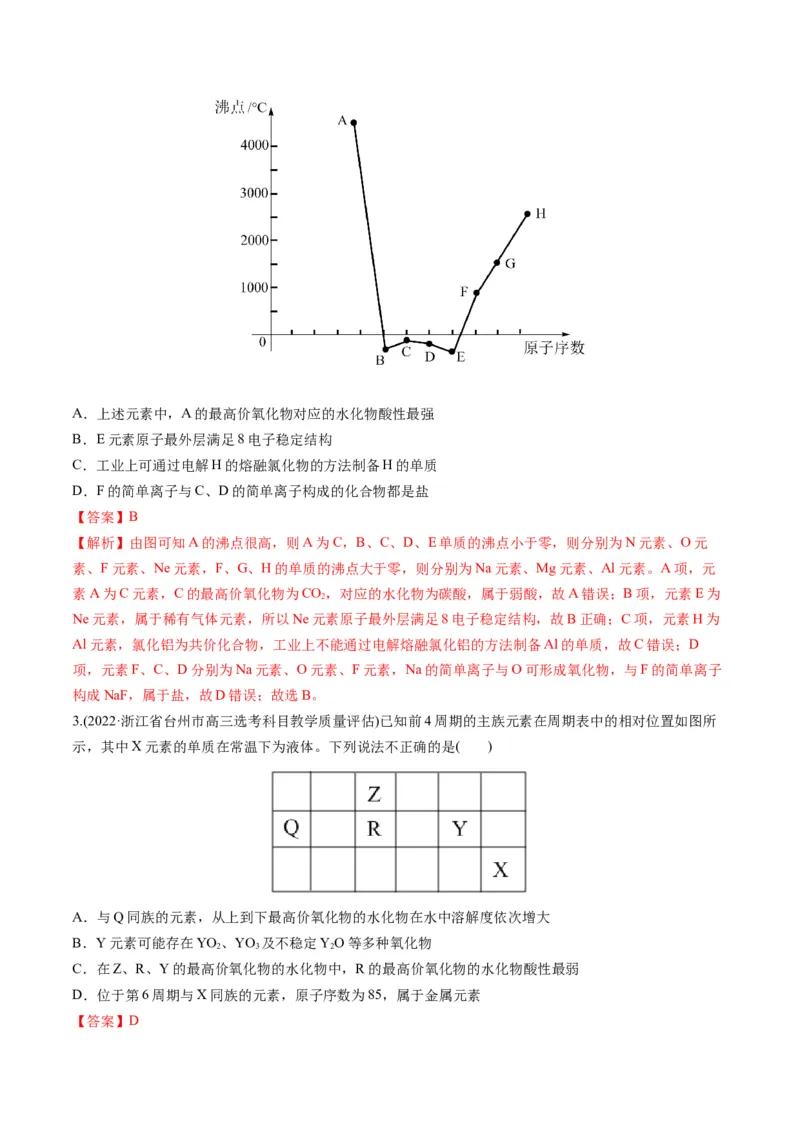
2.(2022·天津市部分区高三期中)短周期内连续八种元素单质的沸点与原子序数的关系如图,下列说法正确
的是( )A.上述元素中,A的最高价氧化物对应的水化物酸性最强
B.E元素原子最外层满足8电子稳定结构
C.工业上可通过电解H的熔融氯化物的方法制备H的单质
D.F的简单离子与C、D的简单离子构成的化合物都是盐
【答案】B
【解析】由图可知A的沸点很高,则A为C,B、C、D、E单质的沸点小于零,则分别为N元素、O元
素、F元素、Ne元素,F、G、H的单质的沸点大于零,则分别为Na元素、Mg元素、Al元素。A项,元
素A为C元素,C的最高价氧化物为CO,对应的水化物为碳酸,属于弱酸,故A错误;B项,元素E为
2
Ne元素,属于稀有气体元素,所以Ne元素原子最外层满足8电子稳定结构,故B正确;C项,元素H为
Al元素,氯化铝为共价化合物,工业上不能通过电解熔融氯化铝的方法制备Al的单质,故C错误;D
项,元素F、C、D分别为Na元素、O元素、F元素,Na的简单离子与O可形成氧化物,与F的简单离子
构成NaF,属于盐,故D错误;故选B。
3.(2022·浙江省台州市高三选考科目教学质量评估)已知前4周期的主族元素在周期表中的相对位置如图所
示,其中X元素的单质在常温下为液体。下列说法不正确的是( )
A.与Q同族的元素,从上到下最高价氧化物的水化物在水中溶解度依次增大
B.Y元素可能存在YO 、YO 及不稳定YO等多种氧化物
2 3 2
C.在Z、R、Y的最高价氧化物的水化物中,R的最高价氧化物的水化物酸性最弱
D.位于第6周期与X同族的元素,原子序数为85,属于金属元素
【答案】D【解析】X元素的单质在常温下为液体,X是Br元素;根据在元素周期表中的相对位置,可知Y是S元
素、Z是C元素、R是Si元素、Q是Mg元素。A项,Mg是ⅡA族元素,ⅡA族元素从上到下最高价氧化
物的水化物在水中溶解度依次增大,故A正确;B项,根据化合价规律,S元素可能存在SO 、SO 及不稳
2 3
定SO等多种氧化物,故B正确;C项,非金属性越强,最高价含氧酸的酸性越强,非金属性S>C>Si,所
2
以最高价氧化物的水化物中,HSiO 的酸性最弱,故C正确;D项,位于第6周期与Br同族的元素是
2 3
At,原子序数为85,属于非金属元素,故D错误;故选D。
4.(2022·湖南省长郡中学高三月考)短周期主族元素X、Y、A、D、Z的离子半径与原子序数的关系如图所
示。X的简单气态氢化物能与X的最高价氧化物的水化物反应;Y与X相邻,Y的最外层电子数是A和X
最外层电子数之和;D的简单离子半径是同周期最小;Z的某种单质是一种易自燃的物质。下列说法正确
的是( )
A.可用D单质还原 制备 单质 B.A与氢元素形成的化合物含有共价键
C.X形成的氧化物为酸性氧化物 D.Y、Z两种元素形成的一种化合物可用于干燥氨气
【答案】A
【解析】由题干信息可知,A、D、X、Y、Z是五种常见短周期元素,X的简单气态氢化物能与X的最高
价氧化物对应水化物反应,发生反应为NH +HNO =NHNO ,则X为N,Y与X相邻,原子序数Y大于X
3 3 4 3
且离子半径X大于Y,说明Y和X属于同一周期,则Y为O,D的离子半径是同周期元素的简单离子中最
小的,则D为Al;Y的最外层电子数是A和X最外层电子数之和,且A的原子序数大于Y小于D,则A
为Na;白磷是一种易自燃的单质,Z的某种单质是一种易自燃的物质,则Z为P。A项,可用Al单质还原
Fe O 制备Fe单质即铝热反应制备铁,A正确;B项,Na与氢元素形成的化合物为离子化合物,只含有离
2 3
子键,B错误;C项,氮的氧化物有很多种,如NO、NO 均不是酸性氧化物,C错误;D项,PO 为酸性
2 2 5
氧化物,会与氨气反应,不可用于干燥氨气,D错误;故选A。
5.(2022·广东省化州市高三质量调研)已知X、Y、Z、W四种短周期主族元素的原子序数依次增大,X原子
的最外层电子数与电子层数相等,Y与X同主族,且最高价化物对应的水化物是一种强碱,Z的一种氧化
物溶在雨水中,可形成酸雨。下列说法正确的是( )
A.原子半径大小:
B.X与Y、Z、W三种元素都可形成共价化合物
C.非金属性D.W的单质常用于自来水的杀菌消毒
【答案】D
【解析】X原子的最外层电子数与电子层数相等,Y与X同主族,且最高价化物对应的水化物是一种强
碱,则X是H元素、Y是Na元素;Z的一种氧化物溶在雨水中,可形成酸雨,Z是S元素,X、Y、Z、W
四种短周期主族元素的原子序数依次增大,W是Cl元素。A项,电子层数越多半径越大,电子层数相同,
质子数越多半径越小,原子半径大小: ,故A错误;B项,H与Na形成离子化合物
NaH,故B错误;C项,同周期元素从左到右,非金属性增强,非金属性Cl>S,故C错误;D项,Cl 常
2
用于自来水的杀菌消毒,故D正确;故选D。
6.(2022·河南省南阳市高三期中)短周期元素W、X、Y、Z的原子序数依次增大,浙江大学研究团队以
aYX·bZX (固态物质,a、b为系数)为载体,利用 纳米颗粒催化气态单质W、X 合成WX,其
2 3 2 2 2 2 2
原理如下图所示。下列说法错误的是( )
A.元素主要化合价(最高正价):Z>Y
B.地壳中元素含量:X>Z>Y
C.YX、ZX 均具有较高熔点
2 3 2
D.W与X形成的化合物只含极性键
【答案】D
【解析】根据四种元素形成的化合物结构aYX·bZX 的特点,该物质是盐,表示成氧化物形式,应该为硅
2 3 2
酸盐。结合元素原子序数大小关系及气态单质W、X 合成WX,可知:W是H,X是O,Y是Al,Z是
2 2 2 2
Si元素。A项,Z是Si元素,最高是+4价,Y是Al元素,最高是+3价,所以元素主要化合价(最高正
价):Z>Y,A正确;B项,在地壳中各种元素的含量由多到少的顺序为:O、Si、Al、Fe、Ca、Na等,X
是O,Y是Al,Z是Si,可见地壳中元素含量:X>Z>Y,B正确;C项,YX 是Al O,该物质是离子化
2 3 2 3
合物,离子之间以极强的离子键结合,其熔点较高;ZX 是SiO,该物质属于共价晶体原子之间以强烈共
2 2
价键结合,具有较高的熔点,C正确;D项,W是H,X是O,二者形成的化合物HO中只含有极性键H-
2
O键;在化合物HO 中既含有极性键H-O键,也含有非极性键O-O键,D错误;故选D。
2 2
7.(2022·天津市五校联考高三期中)X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间
的关系如图,下列不正确的是( )A.R的氧化物都含有离子键 B.气态氢化物的稳定性:Z>Y
C.Y形成的化合物种类最多 D.含氧酸酸性Z>M
【答案】D
【解析】X、Y、Z、M、R为五种短周期元素,X、R最外层只有一个电子,为第IA族元素;Y最外层有
4个电子,位于第IVA族,Z原子最外层有5个电子,位于第VA族,M最外层有6个电子,位于第VIA
族;R原子半径最大,为Na元素,X原子半径最小,为H元素;Y原子和Z原子半径接近、M原子半径
大于Y而最外层电子数大于Y,所以Y是C、Z是N、M为S元素。A项,Na的氧化物由氧化钠和过氧化
钠两种,但不论是氧化钠还是过氧化钠,结构中均含离子键,故A正确;B项,元素的非金属性越强,其
气态氢化物的稳定性越强,非金属性Z>Y,所以其稳定性Z>Y,故B正确;C项,Y为碳元素,而C元
素形成的有机物种类繁多,远多于无机物的种类,故C正确;D项,没有指明最高价含氧酸,无法比较酸
性,故D错误;故选D。
8.(2022·湘豫名校高三联考)已知X、Y、Z、W四种元素是原子序数依次增大的短周期元素。四种元素形
成的单质能按如图反应生成甲、乙、丙、丁四种化合物。W的质子数等于Z质子数的两倍再加上X的质子
数;Y元素是植物生长所需要的一种营养元素。四种元素不在同一主族。下列说法正确的是( )
A.Y的氧化物形成的水化物是强酸
B.化合物甲可以与化合物乙反应
C.化合物丙的比例模型:
D.化合物甲的沸点高于化合物丁
【答案】D
【解析】X、Y、Z、W四种元素是原子序数依次增大的短周期元素,Y元素是植物生长所需要的一种营养
元素,则Y为N,W的质子数等于Z质子数的两倍再加上X的质子数;则Z只能是O,W为Cl,X为H,
则甲为HO,乙为NO,丙为NCl ,丁为NH 。A项,Y的氧化物形成的水化物不一定是强酸,比如亚硝
2 3 3酸,故A错误;B项,化合物甲(H O)可以与化合物乙(NO)不反应,故B错误;C项, 不是化
2
合物丙的比例模型,氮原子比Cl原子半径小,故C错误;D项,化合物甲(H O)的沸点高于化合物丁
2
(NH ),故D正确。故选D。
3
9.(2022·重庆八中高三期中)短周期元素A、B、C、D、E在周期表中相对位置如图所示。已知:D原子的
原子序数等于其最外层电子数的3倍。
请回答下列问题:
(1)B在周期表中位于第___________周期___________族。
(2)E B分子的电子式为___________,该分子所含化学键类型是___________。
2
(3)在B、D、E的气态氢化物中,热稳定性最弱的是___________(填化学式)。
(4)工业上,制备C单质的化学方程式为___________。
(5)在A的氢化物中,能与溴水、酸性KMnO 溶液发生化学反应的有___________(填一种物质的结构简
4
式)。
(6)D的单质在氯气中燃烧生成两种产物X和Y,其中X分子中每个原子最外层都达到8电子结构。Y与足
量的NaOH溶液反应生成两种盐和水,写出该反应的化学方程式:___________。
【答案】(1) 二 ⅥA (2) 共价键(或极性共价键)
(3)PH (4)2AlO(熔融) 4Al+3O ↑
3 2 3 2
(5)CH =CH (6)PCl +8NaOH=Na PO +5NaCl+4HO
2 2 5 3 4 2
【解析】D应处于第三周期,且D原子的原子序数等于其最外层电子数的3倍,则D为P,由元素在周期
表中的位置,则A为C、B为O、C为Al、E为Cl。(1)B为O,在周期表中位于第二周期第VIA族;
(2)E B是ClO,由O和2个Cl原子各共用1对电子对,电子式为 ,化学键类型是共价键;(3)在
2 2
B、D、E分别为O、P、S,非金属性越强,其气态氢化物越稳定,由非金属性:O>S>P,则热稳定性最弱
的是PH ;(4)工业上,制备Al单质是电解熔融的氧化铝,反应的化学方程式为2Al O(熔融)
3 2 3
4Al+3O ↑;(5)A是C,能与溴水、酸性KMnO 溶液发生化学反应的有乙烯,结构简式是CH=CH ;(6)D
2 4 2 2
的单质P在氯气中燃烧生成两种产物X和Y,其中X分子中每个原子最外层都达到8电子结构说明X为
PCl ,则Y为PCl ,PCl 与足量的NaOH溶液反应生成两种盐为NaPO 、NaCl和水,该反应的化学方程
3 5 5 3 4
式:PCl +8NaOH=Na PO +5NaCl+4HO。
5 3 4 2
10.(2022·湖北黄冈高三模拟)短周期主族元素 、 、 、 的原子序数依次增大,其中 、 同主族, 、 不同周期, 与 可形成淡黄色固体 。下列说法正确的是( )
A.只有 元素存在同素异形体 B. 的氧化物溶于水,溶液呈碱性
C.简单氢化物的沸点: D.简单离子的半径:
【答案】B
【解析】 、 同主族, 、 不同周期,可知X在第一周期,Y在第三周期,W在第四周期, 与
可形成淡黄色固体 ,该物质为 ,Z为Na,Y为O, 、 同主族,则W为S,X的原子
序数最小且在第一周期,X为H,据此分析。S也存在多种同素异形体,故A错误; 为Na、其氢化物为
NaH,与水发生反应:NaH+H O=NaOH+H ↑,产生氢氧化钠使溶液呈碱性,故B正确;HO分子间存在氢
2 2 2
键,HO的沸点高于HS,故C错误;简单离子的半径: ,故D错误;故选B。
2 2
11.短周期元素W、X、Y和Z的原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年
代,X2-和Y2+具有相同的电子层结构,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是(
)
A.W与氢形成的原子个数比为1:1的化合物有多种
B.X的氢化物只含有极性共价键
C Y单质可通过电解Y的氯化物获得
D.W与Z形成化合物WZ 中各原子均满足8电子稳定结构
2
答案:B
解析:由题意可推知,W是C元素,X是O元素,Y是Mg元素,Z是S元素。W是C元素,与氢形成的
原子个数比为1:1的化合物有C H 、C H 、C H 等多种,故A正确;X是O元素,氢化物可以是HO或
2 2 6 6 8 8 2
HO,HO 中含有极性键和非极性键,故B错误;可通过电解熔融MgCl 获得金属Mg,故C正确;CS 中
2 2 2 2 2 2
C是+4价、S是-2价,各原子均满足8电子稳定结构,故D正确。
12.W、X、Y、Z均为短周期主族元素,且原子序数依次增大。已知W元素的原子形成的离子是一个质
子;X、Y在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;Z为同周期中原子半径
最大的元素。下列有关说法正确的是( )
A.四种元素均为非金属元素
B.W与X、Y形成的最简单分子的沸点:X>Y
C.Y、Z形成的化合物中只含离子键
D.W、Y、Z形成的化合物的电子式为 Z+[:Y:W]-
答案:D
解析:由题意可知,W、X、Y、Z分别为H、N、O、Na。Z为Na,属于金属元素,A错误;HO的沸点
2
高于NH ,B错误;NaO只含离子键,NaO 含有离子键和非极性共价键,C错误;NaOH的电子式为Na+
3 2 2 2
[:O:H]-,D正确。
13.X、Y、Z是三种短周期元素,原子半径的大小为Y>X>Z,三种元素的原子序数之和为15;X、Y、Z三
种元素的常见单质在适当条件下可发生右图转化关系,其中 R为10电子分子,是一种常见的无机溶剂。
下列说法不正确的是( )A.X元素位于周期表中第16列
B.X、Y、Z元素两两之间均能形成原子个数比为1:1的化合物
C.X、Y、Z元素形成的单质均具有强还原性
D.R的沸点高于M的沸点
答案:C
解析:R为10电子分子,是一种常见的无机溶剂,则R为HO,根据原子半径X>Z,Z为H,X为O,根
2
据三种元素的原子序数之和为15,推知Y为C。O元素在ⅥA族,位于周期表的第16列,A正确;碳、
氢、氧元素两两之间均能形成原子个数比为 11的化合物C H(或C H 等)、HO 、CO,B正确;碳和氢
2 2 6 6 2 2
气具有强还原性,但氧气具有强氧化性,C错误;HO为液体,M为CO或CO ,是气体,液体的沸点高
2 2
于气体,D正确。
14.短周期主族元素W、X、Y、Z原子序数依次增大,其中W元素原子的最外层电子数是内层电子数的
两倍。X与Z同主族,两原子的核外电子数之和为24。Y的原子半径是所有短周期主族元素中最大的。下
列说法正确的是( )
A.简单离子半径:Z>Y>X
B.Y分别与X、Z形成的二元化合物中不可能存在共价键
C.W、Y、Z的单质分别与X 反应时,条件不同产物均不同
2
D.如图所示实验可证明非金属性:Cl>Z
答案:D
解析:W原子最外层电子数是内层电子数的两倍,W为C。X与Z同主族,且核外电子总数为24,X为
O、Z为S。Y的原子半径是短周期主族元素中最大的,Y为Na。A项离子半径S2->O2->Na+,错误;B项
Na与O、S形成的二元化合物分别为NaO、NaO、NaS,其中NaO 中含非极性共价键,错误;C项C、
2 2 2 2 2 2
Na、S与O 反应时,生成产物分别可能为CO与CO 、NaO与NaO 、SO ,错误;D项生成的Cl 通入
2 2 2 2 2 2 2
HS溶液中发生反应HS+Cl===S↓+2HCl,生成黄色沉淀,为置换反应,故可证明非金属性Cl>S,正
2 2 2
确。
15.短周期主族元素a、b、c、d的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;x、y、z
是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;25 ℃时,0.01 mol·L-1w溶液中,=
1.0×10-10。上述物质的转化关系如图所示。下列说法正确的是( )A.原子半径的大小:ad
C.x的电子式为O::C::O
D.y、w含有的化学键类型完全相同
答案:B
解析:z是形成酸雨的主要成分之一,结合物质的转化关系图可知,z是SO ,n是O ,q是S单质;25 ℃
2 2
时,0.01 mol/L的w溶液中c(H+)/c(OH-)=1.0×10-10,说明溶液的pH=12,w是一元强碱NaOH,x是
HO,y是NaO ,m是H ,p是Na。A项,原子半径:HHS,正确;C项HO的电子式为H:O:H,错误;D项NaO 中含有离子
2 2 2 2 2 2
键和非极性键,NaOH中含有离子键和极性键,错误。
16.短周期元素A、B、C、D的原子序数依次增大,①、②、③、④、⑤、⑥是由上述元素构成的常见化合
物,且④为含有非极性键的离子化合物;⑦为元素C的单质,通常为无色无味的气体;各物质间的转化关
系如图所示。下列说法正确的是( )
A.原子半径:AA
C.物质④参与的上述反应中,④均既作氧化剂又作还原剂
D.①一定由A、B两种元素组成,且含A的质量分数为25%
答案:C
解析:④为含非极性键的离子化合物,故为NaO ,⑦为元素C的单质,故为O ,由此可知②、③分别为
2 2 2
CO 、HO,故①为 C、H 化合物。综上分析 A 为 H、B 为 C、C 为 O、D 为 Na。A 项原子半径
2 2
HNa+,错误,C项NaO 无论与HO还是与CO 反应,均发生
2 2 2 2
自身的氧化还原反应,既作氧化剂又作还原剂,正确;D项①可由C、H或者C、H、O组成,且只有为
CH 时含H量为25%,其余均小于25%,错误。
4