文档内容
专题 09 钠及其重要化合物
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 钠及其氧化物
考点二 碳酸钠、碳酸氢钠
考点三 碱金属 焰色试验
考点一 钠及其氧化物
1.(2023·上海金山·统考二模)下列物质在空气中久置会变质,变质过程不涉及氧化还原反应的物质是
A.Na B.NaO C.NaO D.NaSO
2 2 2 2 3
【答案】B
【解析】A.Na与空气中氧气反应生成氧化钠,是氧化还原反应,故A不符合题意;B.NaO与空气中二
2
氧化碳、水反应生成碳酸钠、氢氧化钠,是非氧化还原反应,故B符合题意;C.NaO 与空气中二氧化碳、
2 2
水反应生成碳酸钠和氧气、氢氧化钠和氧气,是氧化还原反应,故C不符合题意;D.NaSO 与空气中氧
2 3
气反应生成硫酸钠,是氧化还原反应,故D不符合题意。综上所述,答案为B。
2.(2023·海南海口·统考模拟预测) 代表阿伏加德罗常数。 完全溶解于 盐
酸。下列说法正确的是
A. 所含的阴离子数为 B.反应转移电子为
C.标准状况下生成气体 D.溶液中 数为
【答案】A
【解析】A.15.6gNa O 的物质的量 ,过氧化钠是钠离子和过氧根离子构成,所含
2 2
的阴离子数为0.2N ,故A正确;B.过氧化钠和盐酸反应的化学方程式:
A
2NaO+4HCl=4NaCl+O ↑+2H O,过氧化钠和水反应的化学方程式为:2NaO+2H O=4NaOH+O ↑,2mol
2 2 2 2 2 2 2 2
过氧化钠反应电子转移2mol,15.6gNa O 的物质的量为0.2mol,电子转移总数为0.2N ,故B错误;C.
2 2 A
2NaO+4HCl=4NaCl+O ↑+2H O,2NaO+2H O=4NaOH+O ↑,反应中2mol过氧化钠反应生成1mol氧气,
2 2 2 2 2 2 2 2
0.2mol过氧化钠反应生成0.1mol气体,标准状况下体积=0.1mol×22.4L/mol=2.24L,故C错误;D.钠元素
守恒得到0.2molNa O 中含钠离子0.4mol,溶液中Na+数为0.4N ,故D错误;故选:A。
2 2 A
3.(2023·广东江门·校联考模拟预测)氢化钠是一种重要的储氢试剂、缩合剂、还原剂、烷基化试剂,在
有机合成中具有重要作用,某学习小组利用如图装置制备少量氢化钠,下列说法错误的是
1
原创精品资源学科网独家享有版权,侵权必究!A.装置丙中将Na分散到NaCl晶体中可以增大接触面积,使反应更充分
B.装置乙和装置丁内盛放的试剂可以分别为无水氯化钙和碱石灰
C.实验过程中应先打开K,一段时间后,尾端验纯后再点燃酒精灯
1
D.m gH 储存到NaH中,与足量水反应也释放m gH ,遵从质量守恒定律
2 2
【答案】D
【解析】A.装置丙中将Na分散到NaCl晶体中可以增大接触面积,使反应更充分,A项正确;B.装置乙
和装置丁起干燥作用,盛放的试剂可以分别为无水氯化钙和碱石灰,B项正确;C.实验过程中应先打开
K,用生成的氢气排除装置中的空气,一段时间后,尾端验纯后,说明空气已经排尽,再点燃酒精灯,C
1
项正确;D.1 molNa吸收0.5molH 生成1molNaH,NaH与水的反应为归中反应,1mol氢化钠与足量水完
2
全反应,生成1mol氢气,D项错误;故选D。
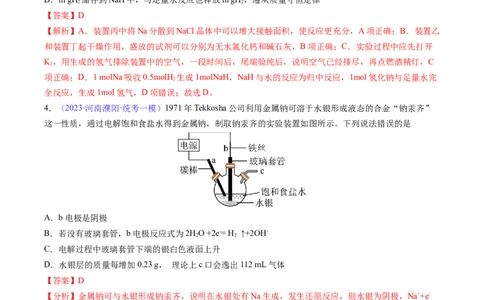
4.(2023·河南濮阳·统考一模)1971年Tekkosha公司利用金属钠可溶于水银形成液态的合金“钠汞齐”
这一性质,通过电解饱和食盐水得到金属钠,制取钠汞齐的实验装置如图所示。下列说法错误的是
A.b电极是阴极
B.若没有玻璃套管,b电极反应式为2HO +2e-= H ↑+2OH-
2 2
C.电解过程中玻璃套管下端的银白色液面上升
D.水银层的质量每增加0.23 g, 理论上c口会逸出112 mL气体
【答案】D
【分析】金属钠可与水银形成钠汞齐,说明在水银处有Na生成,发生还原反应,则水银为阴极,Na++e-
+nHg=Na·nHg,石墨为阳极,2Cl--2e-=Cl↑;
2
【解析】A.b电极处与水银相连,为阴极,选项A正确;B.若没有玻璃套管,b电极反应式为2HO +2e-
2
= H ↑+2OH-,选项B正确;C.因形成钠汞齐,故电解过程中玻璃套管下端的银白色液面上升,选项C正
2
确;D.没有注明标准状况下,故无法计算气体体积,选项D错误;答案选D。
5.(2023·北京丰台·统考二模)已知 。下列说法不正确的是
A.钠在空气中燃烧,产生黄色火焰,生成淡黄色固体
B. 中含有离子键和非极性共价键C. 中阴阳离子个数比为
D. 可作供氧制,与 反应过程中每生成 转移
【答案】C
【解析】A.钠在空气中燃烧生成过氧化钠,观察到产生黄色火焰,生成淡黄色固体物质,选项A正确;
B.NaO 中钠离子和过氧根离子之间存在离子键,过氧根离子内氧原子和氧原子之间存在非极性共价键,
2 2
选项B正确;C.NaO 由钠离子与过氧根离子构成,则NaO 中阴、阳离子个数比为1 : 2,选项C错误;
2 2 2 2
D.过氧化钠和二氧化碳反应时得到的氧气是由-1价的氧元素生成的,故生成1mol氧气时转移电子为
2mol,选项D正确;答案选C。
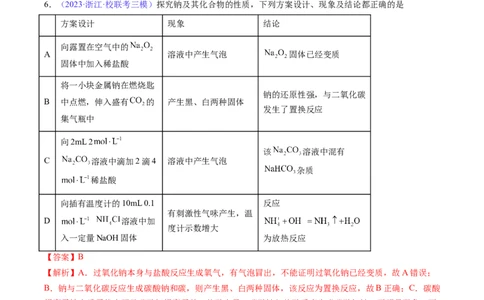
6.(2023·浙江·校联考三模)探究钠及其化合物的性质,下列方案设计、现象及结论都正确的是
方案设计 现象 结论
向露置在空气中的
A 溶液中产生气泡 固体已经变质
固体中加入稀盐酸
将一小块金属钠在燃烧匙
钠的还原性强,与二氧化碳
B 中点燃,伸入盛有 的 产生黑、白两种固体
发生了置换反应
集气瓶中
向2mL 2
该 溶液中混有
C 溶液中滴加2滴4 溶液中产生气泡
杂质
稀盐酸
向插有温度计的10mL 0.1 反应
有刺激性气味产生,温
D 溶液中加
度计示数增大
入一定量NaOH固体 为放热反应
【答案】B
【解析】A.过氧化钠本身与盐酸反应生成氧气,有气泡冒出,不能证明过氧化钠已经变质,故A错误;
B.钠与二氧化碳反应生成碳酸钠和碳,则产生黑、白两种固体,该反应为置换反应,故B正确;C.碳酸
根离子结合质子能力强于碳酸氢根离子的,盐酸少量,碳酸钠与盐酸反应生成碳酸氢钠,无明显现象,不
会产生气泡,故C错误;D.NH Cl溶液中加入一定量NaOH固体中时,由于氢氧化钠固体溶于水本身放
4
热,所以不能据此说明该反应是放热反应,故D错误;故选:B。
7.(2023·北京东城·统考二模)实验:将一小粒钠放在石棉网上,微热,待钠熔成球状时,将盛有氯气的
集气瓶迅速倒扣在钠的上方,钠剧烈燃烧,有白烟生成。下列分析不正确的是A.钠熔化后体积增大,说明钠原子间的平均距离增大
B.反应过程中, 的 键断裂
C. 的形成过程可表示为
D.该实验说明 的氧化性比 的强
【答案】D
【解析】A.钠熔化后体积增大,说明钠原子间的平均距离增大,故A正确;B.反应过程中, 的3p
上的 键断裂,故B正确;C. 的形成过程钠原子失去电子,氯原子得到电子,可表示为
,故C正确;D.该实验没有对比无法说明 的氧化性比 的强,故D错
误;故选:D。
8.(2023·江西抚州·江西省宜黄县第一中学校考一模)某小组研究钠与不同浓度盐酸的反应。
【实验操作】
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。
【实验现象与数据】
编号 ① ② ③ ④ ⑤
c(HCl)/
0.5 1.0 1.5 3.0 6.0
(mol·L-1)
钠浮在液面上,四处游动
钠燃 钠短时燃 钠的表面有 钠的表面。有 钠的周围出现白色
主要现象
烧。溶 烧。溶液 火花。溶液 少量火花。溶 浑浊,一段时间后
液澄清 澄清 澄清 液澄清 变澄清
11 21 37 65 114
钠完全消失所用的
时间/s
经检验,⑤中出现的白色浑浊中的固体为NaCl。
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式: :
(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是 。
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间 。
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的
氯化钠改变了盐酸与钠的 ,该因素影响了化学反应速率,进而影响了钠完全消失所用的时间。
【答案】(1) (2)钠浮在液面上(3)越长(4)接触面积
【分析】钠与盐酸反应生成氯化钠和氢气,盐酸浓度越大,氯化钠溶解度越小,生成的氯化钠使钠与盐酸
接触面积越小,反应速率越慢,钠完全消失所用的时间越长。
【解析】(1)钠与盐酸反应生成氯化钠和氢气,反应的化学方程式为 ;
(2)钠浮在液面上,说明钠的密度小于盐酸的密度;
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间越长;
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生
成的氯化钠改变了盐酸与钠的接触面积,盐酸浓度越大,氯化钠溶解度越小,生成的氯化钠使钠与盐酸接
触面积越小,反应速率越慢,钠完全消失所用的时间越长。
考点二 碳酸钠、碳酸氢钠
1.(2023·江苏南通·统考一模)下列物质性质与用途具有对应关系的是
A. 呈淡黄色,可用作供氧剂
B.NaCl熔点较高,可用于制取NaOH
C. 溶液呈碱性,可用于除油污
D. 易分解,可用于治疗胃酸过多
【答案】C
【解析】A. 能与水和二氧化碳反应生成氧气,因此可做供氧剂,与颜色无关,故A错误;B.电
解饱和NaCl溶液生成NaOH,与NaCl熔点无关,故B错误;C. 溶液呈碱性,可使油污水解呈溶
水物质除去,故C正确;D. 能与胃酸中HCl反应生成二氧化碳,因此可以用于治疗胃酸过多,
与其不稳定性无关,故D错误;故选:C。
2.(2023·天津南开·统考一模)下列实验方案中,不能测定出 和 的混合物中 质量
分数的是
A.取ag混合物充分加热,质量减少bg
B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体C.取ag混合物与足量 溶液充分反应,过滤、洗涤、烘干、得到bg固体
D.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
【答案】D
【解析】A.只有碳酸氢钠加热分解,由差量法可计算碳酸氢钠的质量,然后再计算碳酸钠的质量分数,
能够测出混合物中碳酸钠的质量分数,故A不选;B.加热后bg固体为氯化钠的质量,设碳酸钠的物质的
量为x、碳酸氢钠的物质的量为y,则106x+84y=a,2x+y= ,解方程计算出a、b,然后可计算出混合
物中碳酸钠的质量分数,故B不选;C.碳酸钠和碳酸氢钠均能与 反应生成碳酸钡沉淀,结合B
项分析,也可以计算出混合物中碳酸钠的质量分数,故C不选;D.ag混合物与足量稀硫酸充分反应,逸
出气体主要是二氧化碳和水,所以质量增加bg两种气体的质量,故无法求出混合物中碳酸钠的质量分数,
故D选;故选:D。
3.(2023·上海浦东新·统考二模)为除去 溶液中的下列杂质,所选用的试剂正确的是
选项 杂质 试剂
A 适量的NaOH溶液
B NaOH 适量的 溶液
C NaCl 适量的盐酸
D 适量的 溶液
【答案】A
【解析】A. 和NaOH溶液反应生成 和水,可以用适量的NaOH溶液除 溶液中的
,故A正确;B.NaOH和 不能反应,不能用 溶液除 溶液中的NaOH,故B
错误;C. 和盐酸反应生成NaCl、二氧化碳、水,不能用盐酸除 溶液中的NaCl,故C错
误;D. 、 都能与 反应,分别生成硫酸钡、碳酸钡沉淀,不能用 溶液除
溶液中的 ,故D错误;选A。
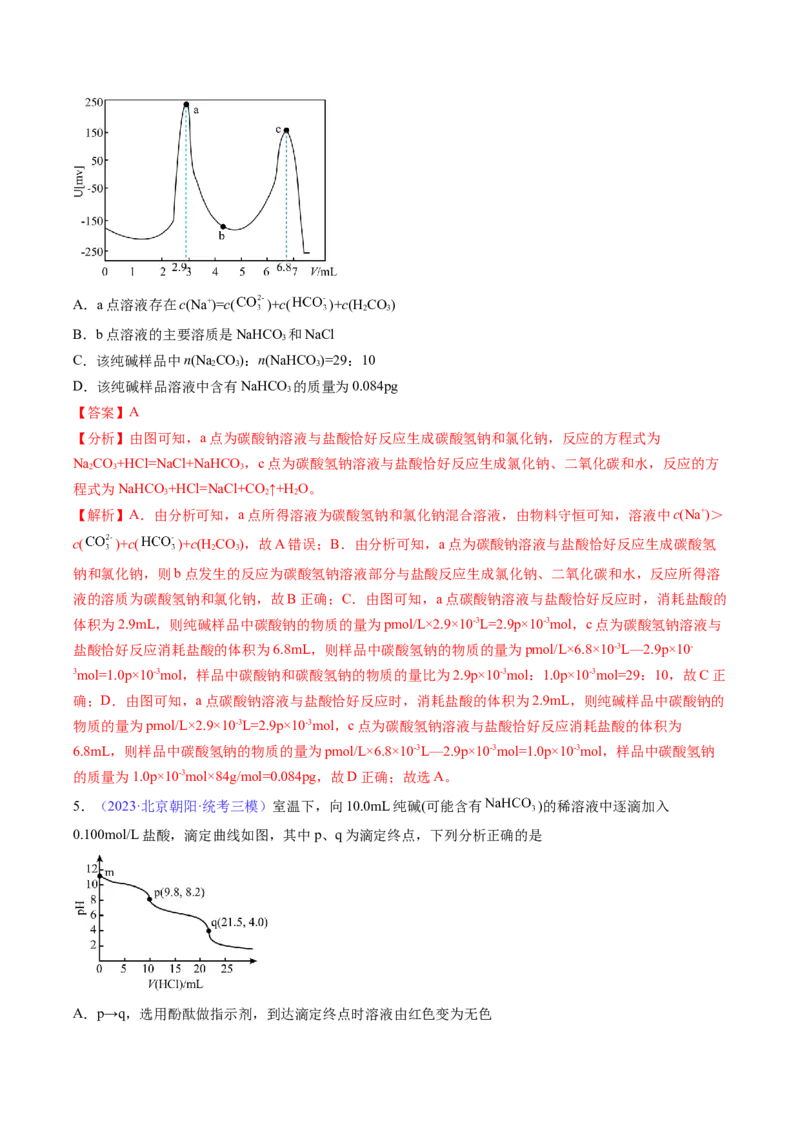
4.(2023·河南郑州·统考三模)电位滴定法是利用滴定过程中溶液电位(U)突变指示终点的滴定方法。常
温下,用pmol·L-1的盐酸测定VmL某纯碱样品溶液中NaHCO 的含量,电位滴定曲线如图所示,下列说法
3
错误的是A.a点溶液存在c(Na+)=c( )+c( )+c(H CO)
2 3
B.b点溶液的主要溶质是NaHCO 和NaCl
3
C.该纯碱样品中n(Na CO):n(NaHCO )=29:10
2 3 3
D.该纯碱样品溶液中含有NaHCO 的质量为0.084pg
3
【答案】A
【分析】由图可知,a点为碳酸钠溶液与盐酸恰好反应生成碳酸氢钠和氯化钠,反应的方程式为
NaCO+HCl=NaCl+NaHCO ,c点为碳酸氢钠溶液与盐酸恰好反应生成氯化钠、二氧化碳和水,反应的方
2 3 3
程式为NaHCO +HCl=NaCl+CO ↑+H O。
3 2 2
【解析】A.由分析可知,a点所得溶液为碳酸氢钠和氯化钠混合溶液,由物料守恒可知,溶液中c(Na+)>
c( )+c( )+c(H CO),故A错误;B.由分析可知,a点为碳酸钠溶液与盐酸恰好反应生成碳酸氢
2 3
钠和氯化钠,则b点发生的反应为碳酸氢钠溶液部分与盐酸反应生成氯化钠、二氧化碳和水,反应所得溶
液的溶质为碳酸氢钠和氯化钠,故B正确;C.由图可知,a点碳酸钠溶液与盐酸恰好反应时,消耗盐酸的
体积为2.9mL,则纯碱样品中碳酸钠的物质的量为pmol/L×2.9×10-3L=2.9p×10-3mol,c点为碳酸氢钠溶液与
盐酸恰好反应消耗盐酸的体积为6.8mL,则样品中碳酸氢钠的物质的量为pmol/L×6.8×10-3L—2.9p×10-
3mol=1.0p×10-3mol,样品中碳酸钠和碳酸氢钠的物质的量比为2.9p×10-3mol:1.0p×10-3mol=29:10,故C正
确;D.由图可知,a点碳酸钠溶液与盐酸恰好反应时,消耗盐酸的体积为2.9mL,则纯碱样品中碳酸钠的
物质的量为pmol/L×2.9×10-3L=2.9p×10-3mol,c点为碳酸氢钠溶液与盐酸恰好反应消耗盐酸的体积为
6.8mL,则样品中碳酸氢钠的物质的量为pmol/L×6.8×10-3L—2.9p×10-3mol=1.0p×10-3mol,样品中碳酸氢钠
的质量为1.0p×10-3mol×84g/mol=0.084pg,故D正确;故选A。
5.(2023·北京朝阳·统考三模)室温下,向10.0mL纯碱(可能含有 )的稀溶液中逐滴加入
0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
A.p→q,选用酚酞做指示剂,到达滴定终点时溶液由红色变为无色B.由滴定数据可知,原纯碱中
C.p点 的主要原因:
D.q点溶液中:
【答案】B
【分析】由图可知,p点溶液中的碳酸钠与盐酸恰好反应生成碳酸氢钠,反应得到氯化钠和碳酸氢钠的混
合溶液,反应方程式为NaCO+HCl=NaHCO +NaCl,q点溶液中的碳酸氢钠与盐酸恰好反应生成氯化钠、
2 3 3
二氧化碳和水,反应得到氯化钠和碳酸的混合溶液,反应方程式为NaHCO +HCl=NaCl+CO ↑+H O,由反
3 2 2
应消耗盐酸的体积可知,纯碱稀溶液中碳酸钠的物质的量为0.100mol/L×9.8×10—3L=9.8×10—4mol,碳酸氢
钠的物质的量为0.100mol/L×21.5×10—3L—9.8×10—4mol×2=1.9×10—4mol。
【解析】A.由分析可知,p→q发生的反应为溶液中的碳酸氢钠与盐酸反应生成氯化钠、二氧化碳和水,
则滴定时应选用甲基橙做指示剂,不能选用酚酞做指示剂,故A错误;B.由分析可知,原纯碱中碳酸钠
的物质的量为9.8×10—4mol,碳酸氢钠的物质的量为1.9×10—4mol,则 ,故B
正确;C.由分析可知,p点所得溶液为氯化钠和碳酸氢钠的混合溶液,溶液pH大于7是因为碳酸氢根离
子在溶液中的水解程度大于电离程度,水解的离子方程式为 ,故C错误;D.
由分析可知,原纯碱中碳酸钠的物质的量为9.8×10—4mol,碳酸氢钠的物质的量为1.9×10—4mol,则由原子
个数守恒可知,q点溶液中钠离子的浓度为 ≈0.068mol/L,故D错误;故选
B。
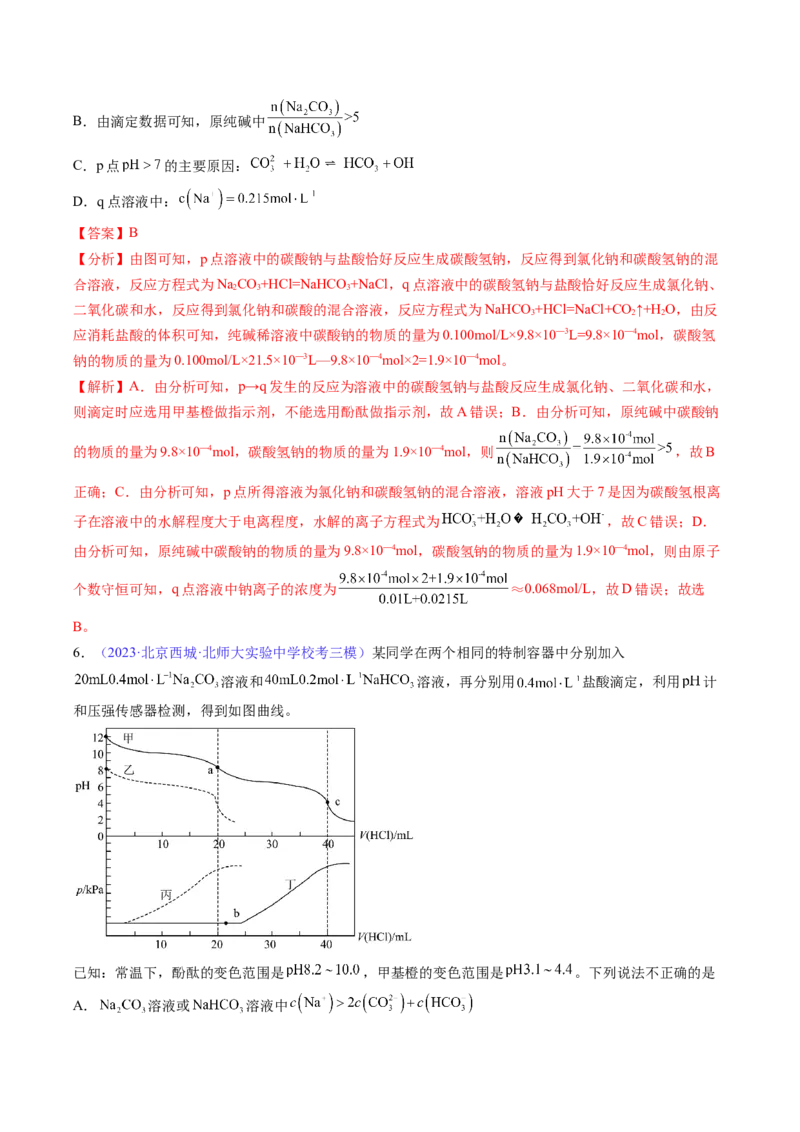
6.(2023·北京西城·北师大实验中学校考三模)某同学在两个相同的特制容器中分别加入
溶液和 溶液,再分别用 盐酸滴定,利用 计
和压强传感器检测,得到如图曲线。
已知:常温下,酚酞的变色范围是 ,甲基橙的变色范围是 。下列说法不正确的是
A. 溶液或 溶液中B.图中曲线甲和曲线丁表示向 溶液中滴加 盐酸
C.在 点发生反应的离子方程式为
D.滴定分析时, 点可用酚酞、 点可用甲基橙作指示剂指示滴定终点
【答案】C
【解析】A.根据电荷守恒, 溶液或 溶液中
,溶液呈碱性,所以 ,故A
正确;B.碳酸钠溶液的pH大于碳酸氢钠溶液,碳酸钠溶液与盐酸反应分步进行
,碳酸钠与盐酸反应开始不放二氧化碳,所以图中曲线甲和曲
线丁表示向 溶液中滴加 盐酸,故B正确;C. 点加入盐酸的体积大于20mL,
反应结束,在 点发生反应的离子方程式为 ,故C错误;D.酚酞的
变色范围是 ,甲基橙的变色范围是 ,滴定分析时, 点可用酚酞、 点可用甲基橙
作指示剂指示滴定终点,故D正确;选C。
7.(2023·上海·统考模拟预测)为探究 与一元酸HA( mol·L )的化学反应热效应,进行了如
下四组实验。已知 ℃。
实验序号 试剂I 试剂Ⅱ 反应前温度 反应后温度
① 40 mL 2.12 g 25℃
② 20 mL HCl+20 mL 2.12 g 25℃
20 mL +20
③ 2.12 g 25℃
mL
2.12 g 与20
④ 20 mL HCl 25℃
mL 形成的溶液
下列说法错误的是
A. 溶于水放热 B. 与HCl反应放热
C. D.
【答案】D
【解析】A.由实验①可知, 溶于水后,温度 ℃,则该过程放热,A正确;B.由实验①②
对比可知,温度 ,则 与HCl反应放热,B正确;C.由实验②③对比可知,将盐酸换成醋酸,
醋酸是弱酸,其电离过程是吸热的,则温度 ,C正确;D.实验②④对比可知,实验④中减少了碳酸钠溶解的过程,则放出的热量会少一些,故 ,D错误;故选D。
8.(2023·天津和平·统考三模)下图是为测定过氧化钠样品(只含NaCO 杂质)纯度而设计的装置,气球Q
2 3
弹性良好。
下列说法正确的是
A.Q中反应的离子方程式为 +2H+=H O+CO↑,2 +4H+=2H O+O↑
2 2 2 2
B.测量气体体积时应先关闭K、K,打开K,反应完毕后再缓缓打开K
1 2 3 1
C.没有导管a稀硫酸不易滴下来,而且会导致测量气体的体积偏大
D.若操作正确,量筒I、Ⅱ分别收集xmL、ymL水,则NaO 的质量分数为
2 2
【答案】C
【分析】实验开始时先打开恒压滴液漏斗的活塞使稀硫酸与样品发生反应:
, ,此时关闭K、K,打开K,利
1 2 3
用排液法测得所有气体的体积即量筒I中水的体积xmL,反应完毕后先打开K,关闭K 保证Q灵活伸缩
2 3
后打开K,碱石灰吸收 后量筒Ⅱ收集ymL水即氧气的体积,据此进一步分析。
1
【解析】A.过氧化钠不能拆,其离子方程式为: ,故A错误;B.为保
证Q灵活伸缩,量筒I测量后,需与大气相通,打开K 前,应先打开K,关闭K,故B错误;C.若没有
1 2 3
导管a,由于气压不相通,稀硫酸不易滴落,而且滴落的稀硫酸也计为气体体积,导致测量气体的体积偏
大,故C正确;D.题中计算既未考虑气体与物质的比例关系,也未考虑物质的摩尔质量,NaO 的质量分
2 2
数为: ,故D错误;故选C。
9.(2023·江西抚州·江西省乐安县第二中学校考一模)小组同学探究 的性质及工业制法。
(1)用 固体配制 溶液。
①用到的仪器有:托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和 。
②计算:需用托盘天平称量 固体 g。③下列情况中,会使所配溶液浓度偏高的是 (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.定容摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究 与 的性质。
实验装置
及操作
盛有 (填化 盛有 的试管中固体 盛有 溶液的试管中立
实验现象 学式)的试管中温度 完全溶解;盛有 即有气泡产生;盛有
计示数升高
的试管中固体有剩余 溶液的试管中
相同温度下,溶解度:
实验结论
略 略
或解释
(填“>”、“<”或“=”)
(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。下图为联合制碱法的主要过
程(部分物质已略去)。
已知:i. 溶于水生成碱,与酸反应生成盐,如 。
ii.有关物质的溶解度( )
物质
溶解度/g 36.0 21.7 9.6 37.2
①沉淀池中所发生的反应属于四种基本反应类型中的 反应。
②加热炉中发生反应的化学方程式为 。
【答案】(1) 容量瓶 5.7 b(2) > 开始无气泡产生,一段时间后产生气泡
(3)复分解
【解析】(1)①用 固体配制 溶液,还需要用到100mL容量瓶;②需要
固体质量为: ,托盘天平称量5.7g固体;③a.转移时,没有
洗涤烧杯和玻璃棒,溶质偏少,浓度偏低,a不符合题意;b.定容时,眼睛俯视刻度线,溶液的总体积偏小,
浓度偏大,b符合题意;c.定容摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切,导致溶液的
体积偏大,浓度偏低,c不符合题意;故选b;
(2)① 溶解时放热,试管温度升高;②相同温度下,碳酸钠的溶解度大于碳酸氢钠的溶解度,故
选“>”;③碳酸钠先与盐酸反应生成碳酸氢钠,无气泡产生,碳酸轻氢钠与盐酸反应生成二氧化碳,有气
泡产生,故现象是:开始无气泡产生,一段时间后产生气泡;
(3)沉淀池中的反应为: ,反应类型为复分解反应;联合制减
法制备的是碳酸钠,为碳酸氢钠受热分解产生,故加热炉中的反应为:
。
10.(2023春·陕西安康·高三开学考试)某干燥白色固体可能含有 , 、 中的几种,
取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加 的盐酸,得到 体积(换算
成标准状况下)与盐酸体积的关系如图所示。请回答下列问题:
(1)产生的 的物质的量为 ,AB段发生反应的化学方程式为 。
(2)若白色固体由 和 组成,则x= , 。
(3)若白色固体由 和 组成, ,则 与 溶于水后发生反应的离子方程式为
, 。
(4)若白色固体只由 和 组成,且 , ,则 。
【答案】(1)0.03
(2)0.01 100
(3)(4)0.02
【分析】若三种固体均含有,固体中加水溶解中发生NaOH+NaHCO =Na CO+H O,向溶液中加入盐酸可
3 2 3 2
能发生反应的先后顺序是NaOH+HCl=NaCl+H O、NaCO+HCl=NaHCO +NaCl、
2 2 3 3
NaHCO +HCl=NaCl+CO ↑+H O,根据图像可知,OA之间发生NaOH+HCl=NaCl+H O、
3 2 2 2
NaCO+HCl=NaHCO +NaCl,AB之间发生NaHCO +HCl=NaCl+CO ↑+H O,据此分析;【解析】(1)产
2 3 3 3 2 2
生的V(CO )=0.672L,则n(CO)=0.03mol;根据上述分析AB段发生反应NaHCO +HCl=NaCl+CO ↑+H O;
2 2 3 2 2
答案为:0.03;NaHCO +HCl=NaCl+CO ↑+H O;(2)CO 来自碳酸钠和碳酸氢钠,根据碳原子守恒,碳
3 2 2 2
酸氢钠的物质的量为0.03mol-0.02mol=0.01mol;OA段发生的反应为NaCO+HCl=NaHCO +NaCl,根据
2 3 3
化学计量数之比等于物质的量之比,0.02molNa CO 与0.02mol盐酸反应,V(盐酸) ,
2 3 1
即 ;A点时碳酸氢钠的物质的量为0.03mol,消耗0.03mol盐酸, ,因此
;答案为:0.01;100;(3) 与 溶于水后发生反应的离子方程式为
; ,说明白色固体溶于水后的溶质只有 ,
;答案为: ;1∶1;(4)因为白色固体只由 、
组成,OA段为 、 与盐酸反应 ,即两物质共消耗0.05mol盐酸,由碳原子
守恒知 , 消耗0.03mol盐酸,则NaOH消耗0.02mol盐酸,
;故答案为:0.02。
考点三 碱金属 焰色试验
1.(2023秋·江苏南通·高三如皋市第一中学开学考试)化学与生活、科技、社会发展息息相关。下列有关
说法正确的是
A.节日燃放烟花过程中的焰色试验是化学反应
B.铁磁流体液态机器人中驱动机器人运动的磁铁的主要成分是
C.“天问一号”火星车使用热控保温材料——纳米气凝胶,可产生丁达尔效应
D.“天和”核心舱电推进系统中使用的氮化硼陶瓷基复合材料属于新型有机高分子材料
【答案】C
【解析】A.焰色试验是物理反应,故A错误;B.Fe O 具有磁性,铁磁流体液态机器人中驱动机器人运
3 4
动的磁铁的主要成分是Fe O,故B错误;C.纳米气凝胶属于胶体,可产生丁达尔效应,故C正确;D.
3 4
氮化硼陶瓷基复合材料属于新型无机非金属材料,故D错误;故选C。
2.(2023·湖北武汉·华中师大一附中校考模拟预测)Li和Mg是两种重要的金属元素。下列说法正确的是
A.金属镁一般保存在石蜡油中 B.单质Li和冷水不反应
C.单质Li可与 反应生成 D.Li、Mg的焰色试验现象相同
【答案】C
【解析】A.金属镁表面易形成较致密氧化膜,不需要保存在石蜡油中,A错误;B.单质Li和冷水可以反应生成LiOH和氢气,B错误;C.单质Li可与 反应生成 ,C正确;D.Li的焰色为紫红色,与
Mg不同,D错误;故选C。
3.(2023·海南省直辖县级单位·嘉积中学校考一模)春节是中国最盛大、最热闹、最重要的一个古老传统
节日。下列说法不正确的是
A.春节期间应把“爆竹声中一岁除……总把新桃换旧符”的传统发扬光大
B.春节的民间习俗贴对联,所用纸的主要成分是纤维素
C.春节期间燃放烟花的焰火颜色是某些金属元素焰色试验所呈现出来的
D.春节前酿酒,淀粉先水解成葡萄糖,然后葡萄糖在酒化酶的作用下转化为乙醇
【答案】A
【解析】A.爆竹爆炸会产生污染空气的气体并产生纸屑,污染环境,A项错误;B.纸的主要成分是纤维
素,B项正确;C.一些金属元素灼烧产生不同的焰色,春节期间燃放烟花的焰火颜色是某些金属元素焰
色试验所呈现出来的,C项正确;D.用淀粉酿酒的过程为淀粉先水解成葡萄糖,然后葡萄糖在酒化酶的
作用下转化为乙醇和二氧化碳,D项正确;故选A。
4.(2023秋·全国·高三开学考试)关注“实验室化学”并加以实践能有效提高学生的实验素养,用如图所
示装置(夹持装置均已省略)进行实验,能达到实验目的的是
A.甲装置可用于验证NaO 与水反应的能量变化
2 2
B.乙装置可用于观察氯化钠的焰色试验
C.丙装置可用于制取并收集干燥、纯净的NO
D.丁装置可用于准确量取一定体积的KCr O 溶液
2 2 7
【答案】A
【解析】A.2NaO+2H O=4NaOH+O ↑,虽然反应生成气体,但是气体不进入集气瓶中,可以用液面变化
2 2 2 2
来说明反应能量变化,A符合题意;B.Cu的焰色反应为绿色,不能用铜丝代替铂丝,B不符合题意;
C.NO与氧气反应,不能选排空气法收集NO,C不符合题意;D.重铬酸钾溶液属于氧化性滴定液,因
此应装在酸性滴定管中,丁装置为碱性滴定管,D不符合题意;故选A。
5.(2023春·上海宝山·高三上海交大附中校考开学考试)陈述I和II均正确且具有因果关系的是
选项 陈述I 陈述II
A 用铁槽盛放浓硝酸 铁不与浓硝酸反应
B 用氢氟酸刻蚀玻璃 HF能与玻璃中的 反应
C 用钾盐作紫色烟花原料 K单质可燃Na高温还原KCl制备
D 金属性:Na<K
金属K
【答案】B
【解析】A.铁与浓硝酸常温下发生钝化,因此用铁槽盛放浓硝酸,故A不符合题意;B.HF能与玻璃中
的 反应,所以常用氢氟酸刻蚀玻璃,故B符合题意;C.用钾盐作紫色烟花原料,是因为电子从激发
态跃迁到基态释放能量,产生紫色光,故C不符合题意;D.Na高温还原KCl制备金属K,是因为K的熔
点低,易挥发出钾蒸汽,与金属性无关,故D不符合题意;故答案选B。