文档内容
专题 10 电化学
2021年化学高考题
一、单选题
1.(2021·山东高考真题)以KOH溶液为离子导体,分别组成CHOH—O、NH—O、
3 2 2 4 2
(CH)NNH—O 清洁燃料电池,下列说法正确的是
3 2 2 2
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1molO 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2L
2 2 4 2
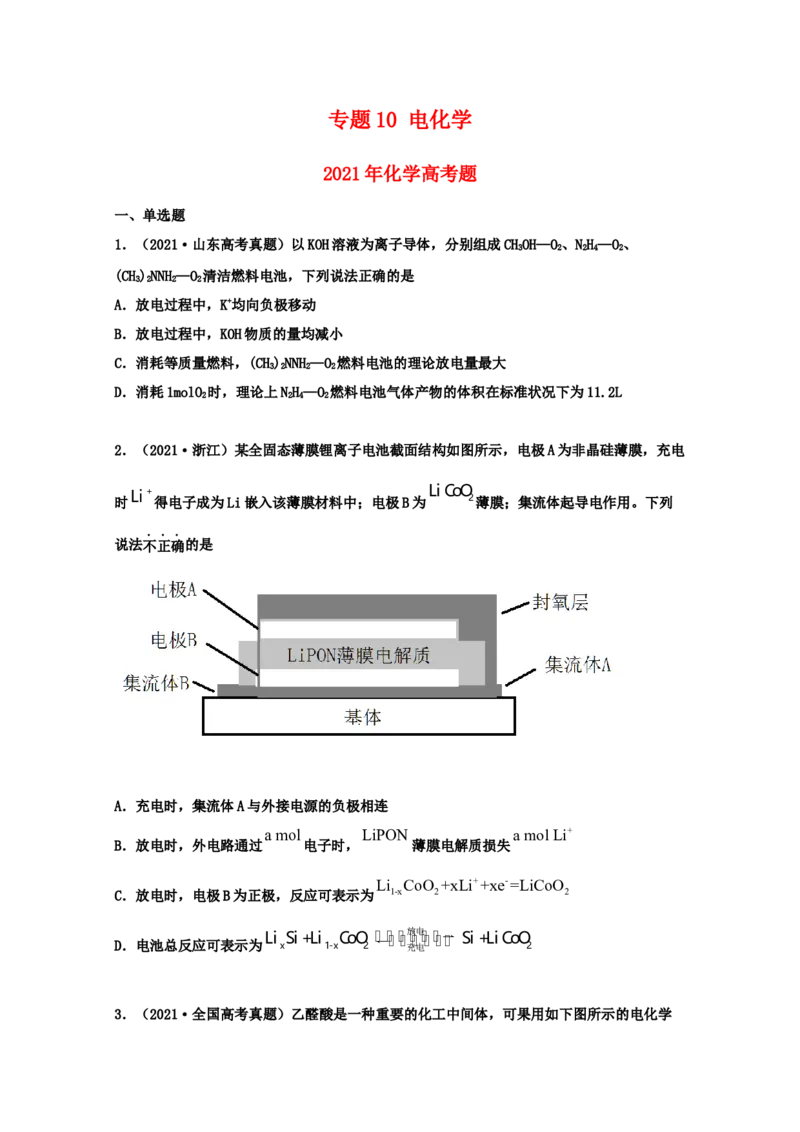
2.(2021·浙江)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电
时
Li+
得电子成为Li嵌入该薄膜材料中;电极B为
LiCoO
2薄膜;集流体起导电作用。下列
说法不正确的是
A.充电时,集流体A与外接电源的负极相连
a mol LiPON a mol Li+
B.放电时,外电路通过 电子时, 薄膜电解质损失
Li CoO +xLi++xe-=LiCoO
C.放电时,电极B为正极,反应可表示为 1-x 2 2
D.电池总反应可表示为 Li x Si+Li 1-x CoO 2 放 充 电 电 Si+LiCoO 2
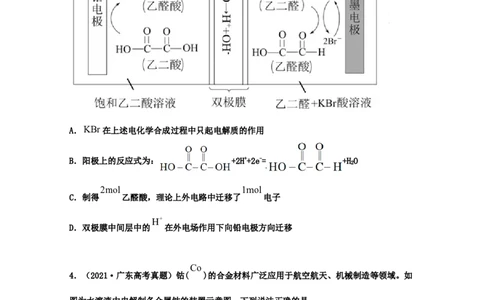
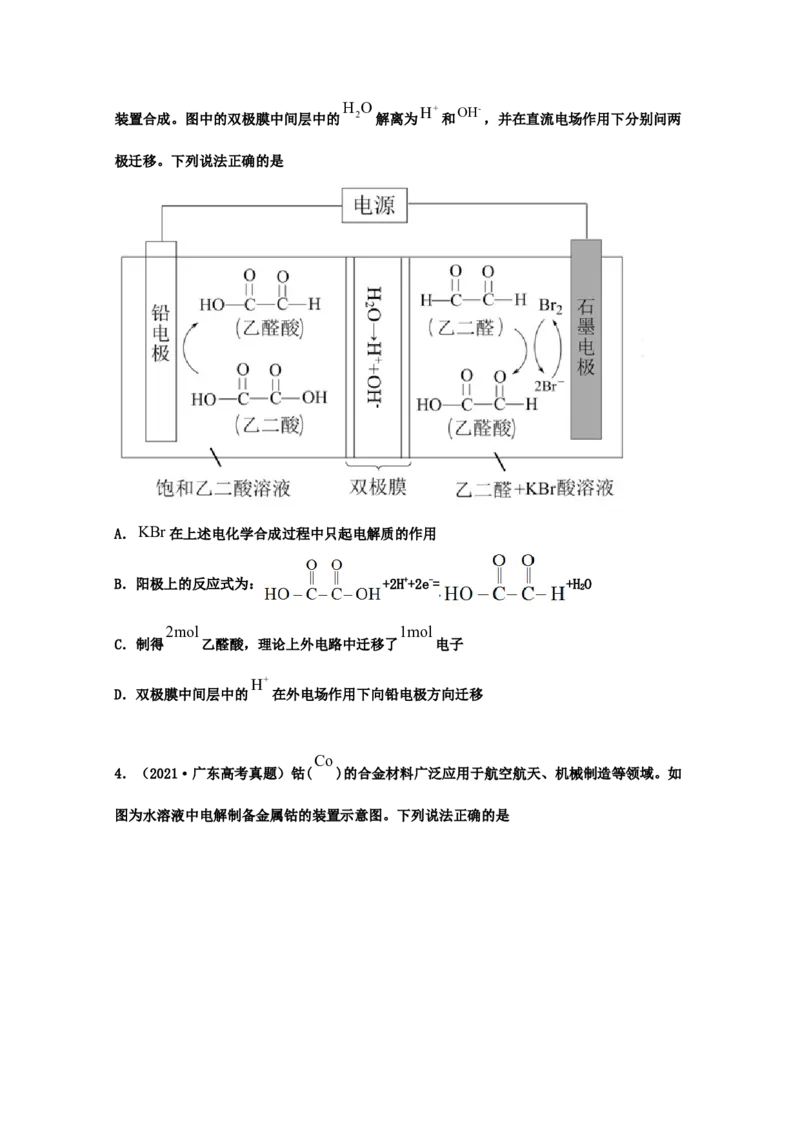
3.(2021·全国高考真题)乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。图中的双极膜中间层中的
H
2
O
解离为
H+
和
OH-
,并在直流电场作用下分别问两
极迁移。下列说法正确的是
A.KBr在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +HO
2
2mol 1mol
C.制得 乙醛酸,理论上外电路中迁移了 电子
H+
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
Co
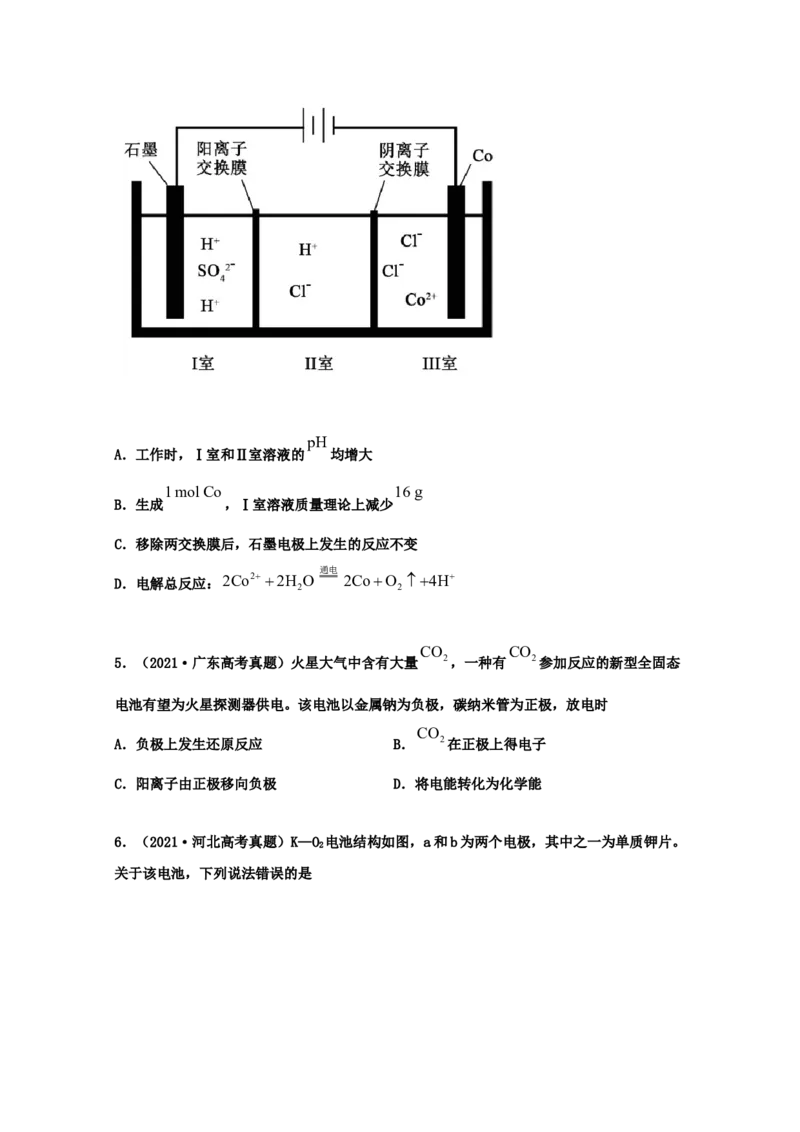
4.(2021·广东高考真题)钴( )的合金材料广泛应用于航空航天、机械制造等领域。如
图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是pH
A.工作时,Ⅰ室和Ⅱ室溶液的 均增大
1molCo 16g
B.生成 ,Ⅰ室溶液质量理论上减少
C.移除两交换膜后,石墨电极上发生的反应不变
通电
D.电解总反应:2Co2 2H O 2CoO 4H
2 2
CO CO
5.(2021·广东高考真题)火星大气中含有大量 2,一种有 2参加反应的新型全固态
电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
CO
A.负极上发生还原反应 B. 2在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能
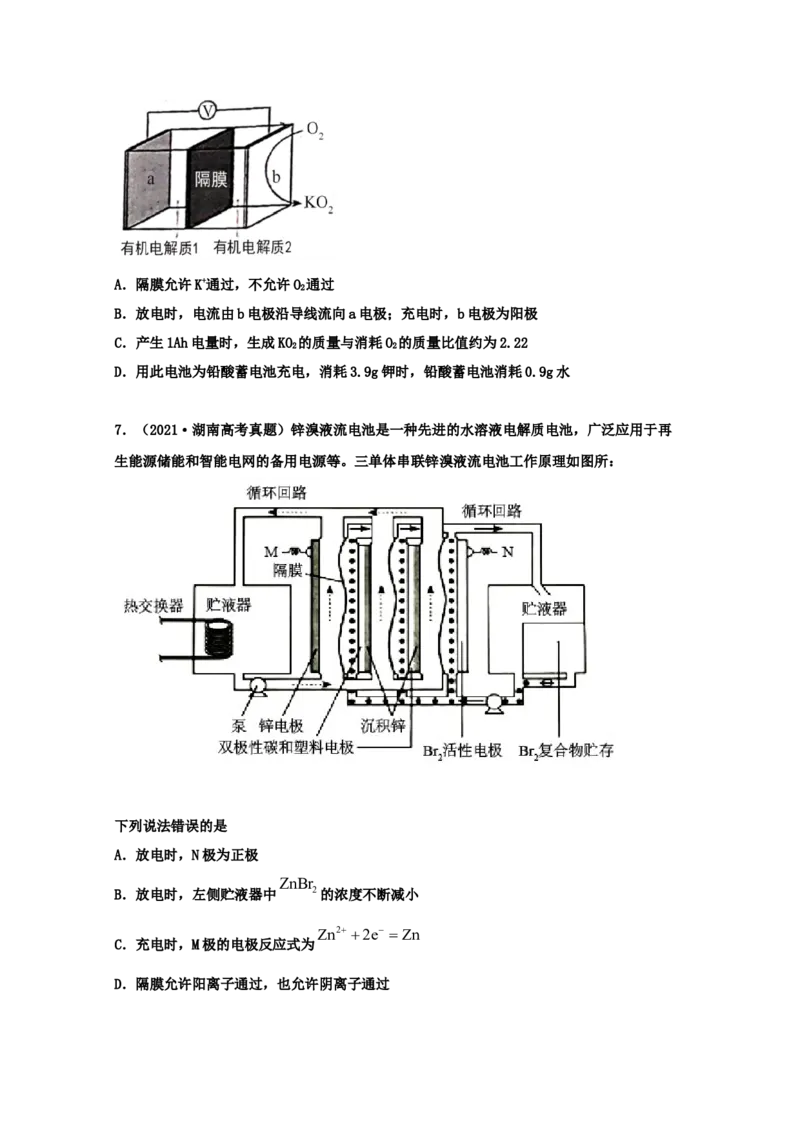
6.(2021·河北高考真题)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。
2
关于该电池,下列说法错误的是A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
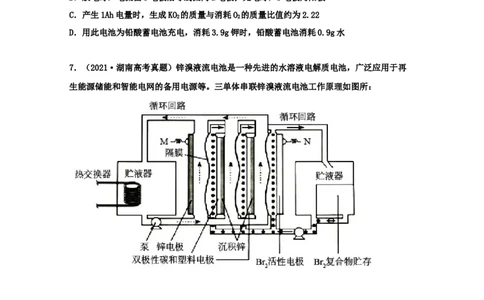
7.(2021·湖南高考真题)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再
生能源储能和智能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
ZnBr
B.放电时,左侧贮液器中 2的浓度不断减小
Zn2 2e Zn
C.充电时,M极的电极反应式为
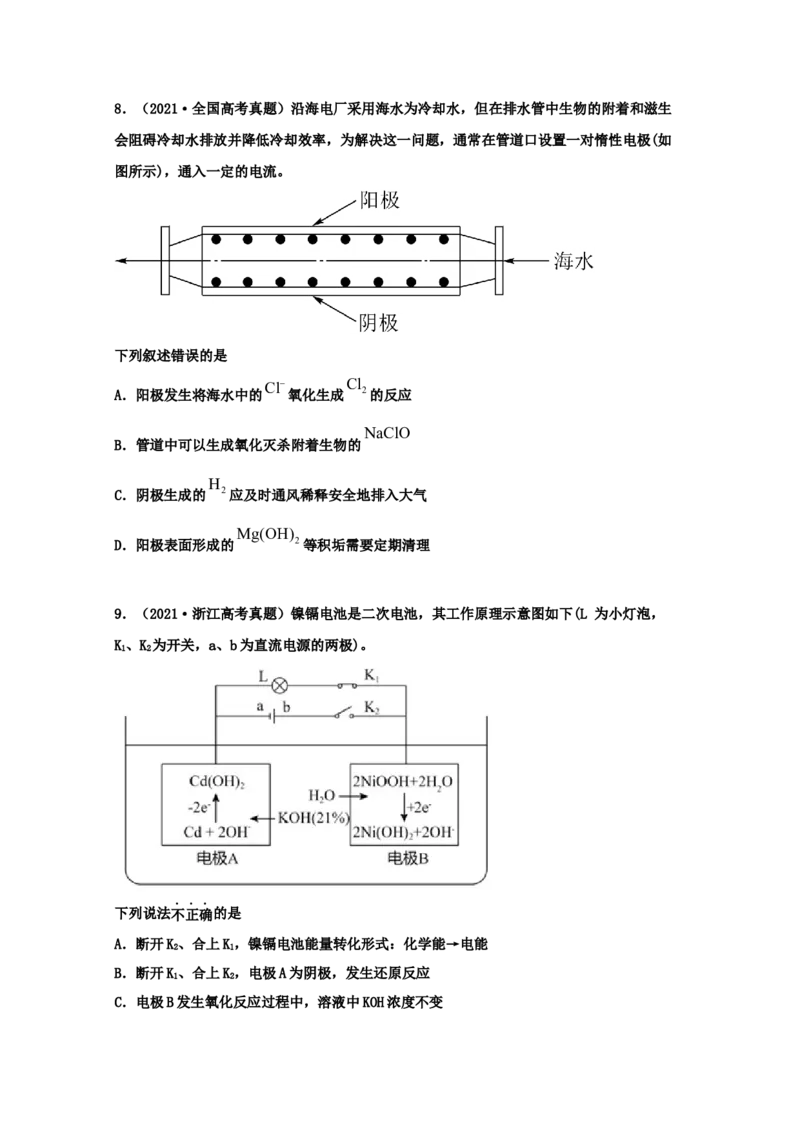
D.隔膜允许阳离子通过,也允许阴离子通过8.(2021·全国高考真题)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生
会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如
图所示),通入一定的电流。
下列叙述错误的是
Cl Cl
A.阳极发生将海水中的 氧化生成 2的反应
NaClO
B.管道中可以生成氧化灭杀附着生物的
H
C.阴极生成的 2应及时通风稀释安全地排入大气
Mg(OH)
D.阳极表面形成的 2等积垢需要定期清理
9.(2021·浙江高考真题)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,
K、K 为开关,a、b为直流电源的两极)。
1 2
下列说法不正确的是
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变放电
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2HO Cd(OH)+2Ni(OH)
2 充电 2 2
二、工业流程题
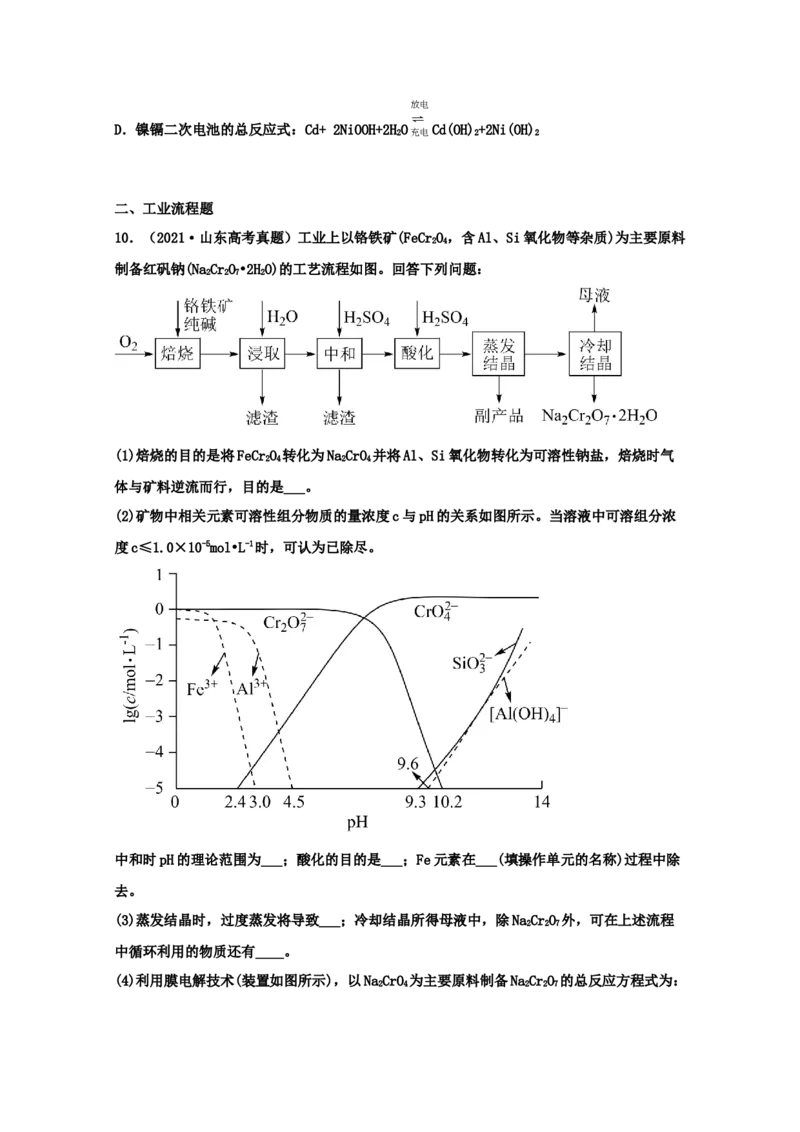
10.(2021·山东高考真题)工业上以铬铁矿(FeCrO,含Al、Si氧化物等杂质)为主要原料
2 4
制备红矾钠(NaCrO•2HO)的工艺流程如图。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCrO 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气
2 4 2 4
体与矿料逆流而行,目的是___。
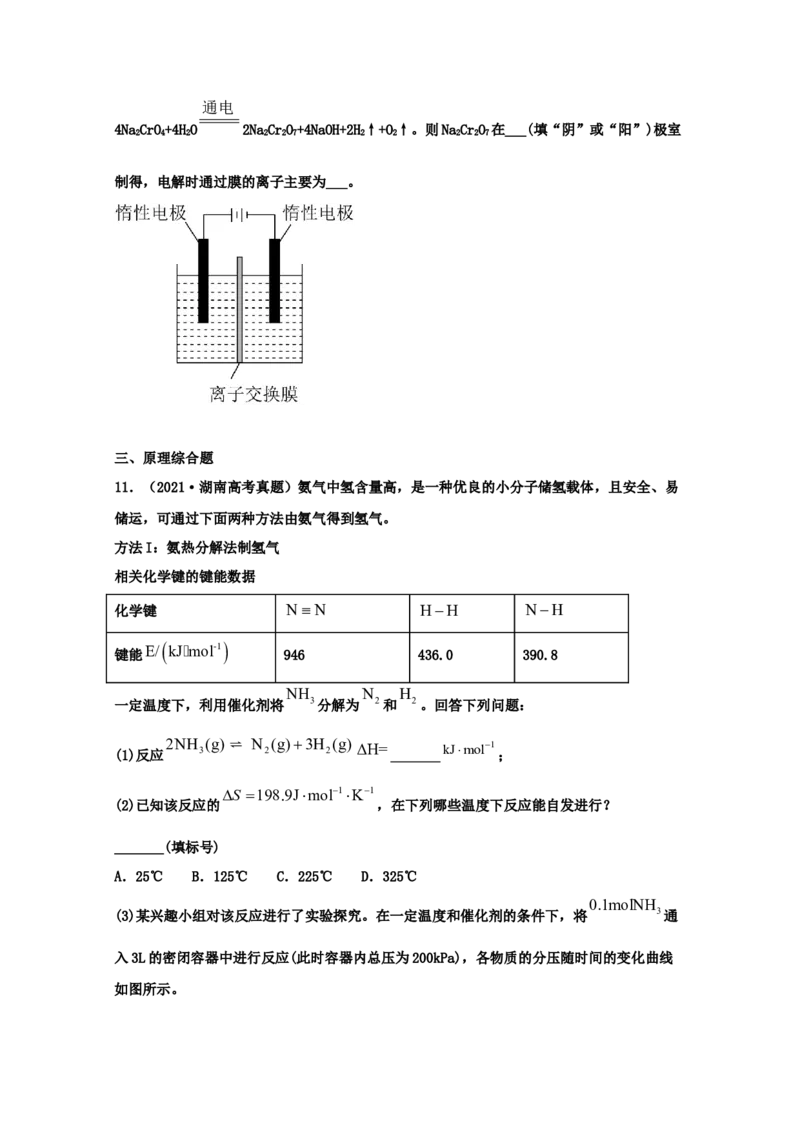
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓
度c≤1.0×10-5mol•L-1时,可认为已除尽。
中和时pH的理论范围为___;酸化的目的是___;Fe元素在___(填操作单元的名称)过程中除
去。
(3)蒸发结晶时,过度蒸发将导致___;冷却结晶所得母液中,除NaCrO 外,可在上述流程
2 2 7
中循环利用的物质还有____。
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCrO 的总反应方程式为:
2 4 2 2 7通电
4NaCrO+4HO 2NaCrO+4NaOH+2H↑+O↑。则NaCrO 在___(填“阴”或“阳”)极室
2 4 2 2 2 7 2 2 2 2 7
制得,电解时通过膜的离子主要为___。
三、原理综合题
11.(2021·湖南高考真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易
储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键 N N HH NH
键能E/
kJmol-1
946 436.0 390.8
NH N H
一定温度下,利用催化剂将 3分解为 2和 2。回答下列问题:
(1)反应
2NH
3
(g) N
2
(g)3H
2
(g)
ΔH= _______ kJmol1 ;
S 198.9Jmol1K1
(2)已知该反应的 ,在下列哪些温度下反应能自发进行?
_______(填标号)
A.25℃ B.125℃ C.225℃ D.325℃
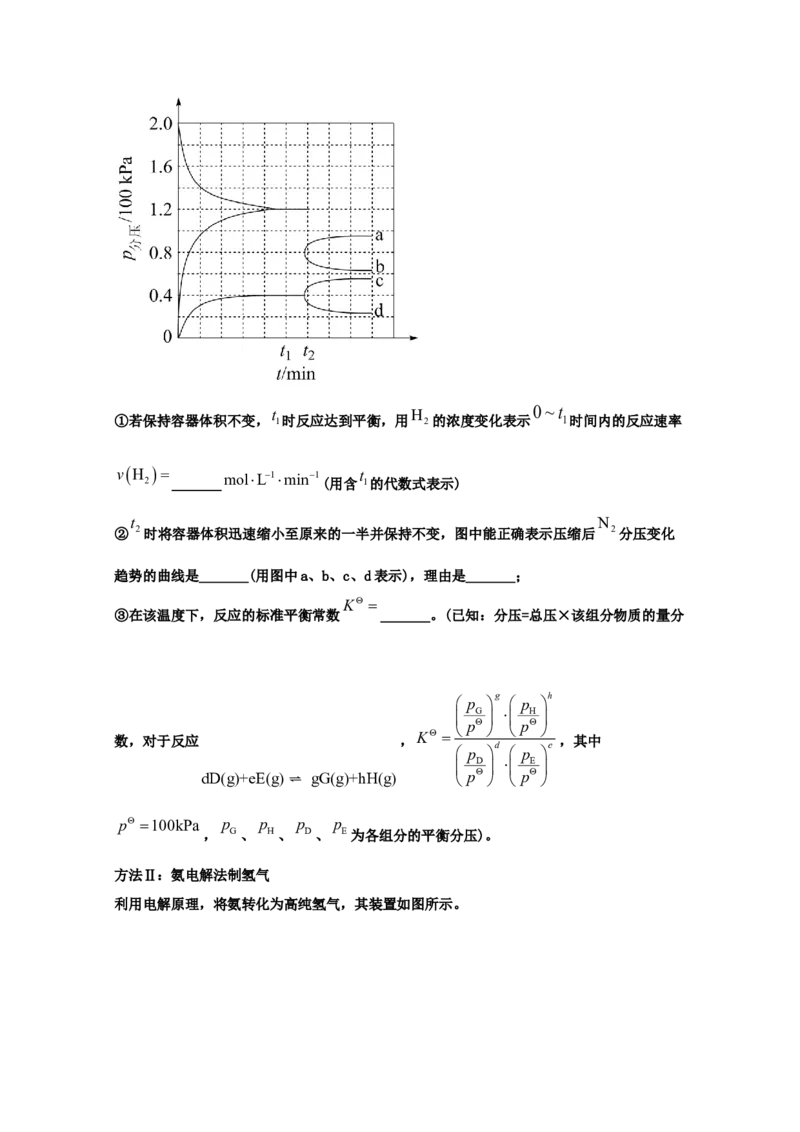
0.1molNH
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将 3通
入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线
如图所示。0~t
t H
①若保持容器体积不变, 1时反应达到平衡,用 2的浓度变化表示 1时间内的反应速率
vH
2
_______
molL1min1
(用含
t
1的代数式表示)
t N
② 2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 2分压变化
趋势的曲线是_______(用图中a、b、c、d表示),理由是_______;
K
③在该温度下,反应的标准平衡常数 _______。(已知:分压=总压×该组分物质的量分
g h
p p
G H
p
p
数,对于反应 ,K ,其中
d e
p p
D E
dD(g)+eE(g) gG(g)+hH(g) p p
p 100kPa p p p p
, G 、 H、 D、 E为各组分的平衡分压)。
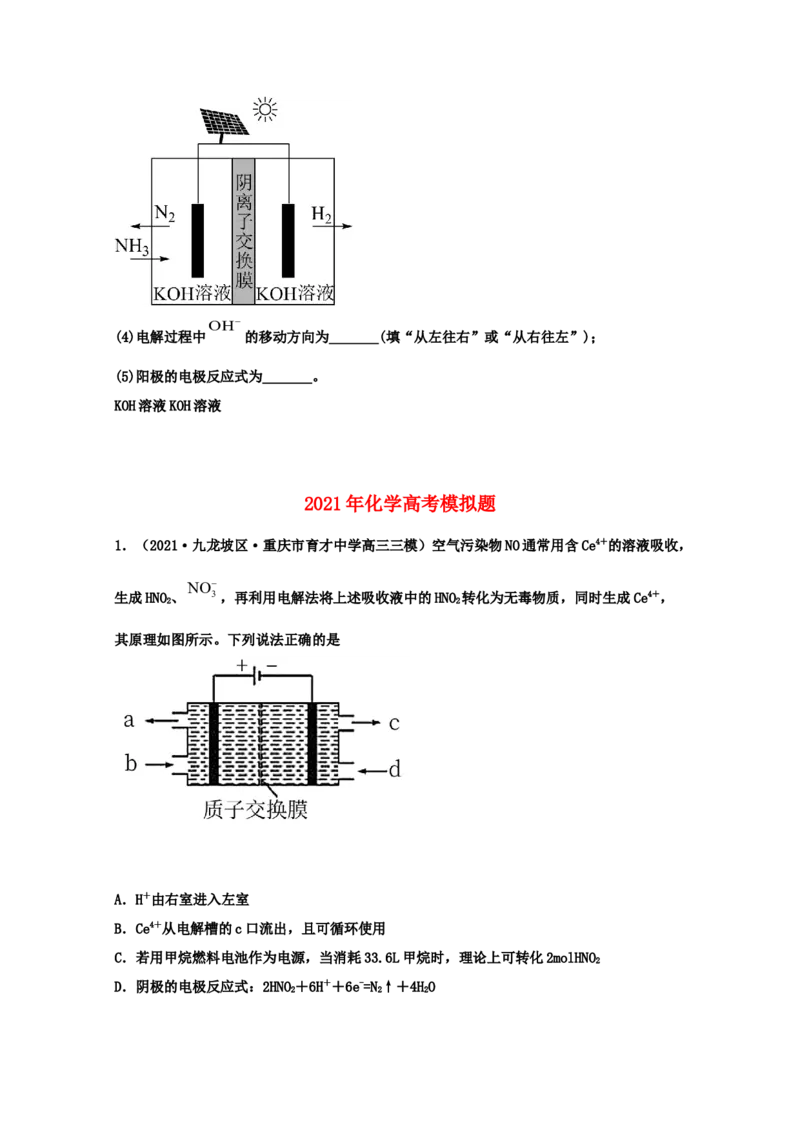
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。OH
(4)电解过程中 的移动方向为_______(填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______。
KOH溶液KOH溶液
2021年化学高考模拟题
1.(2021·九龙坡区·重庆市育才中学高三三模)空气污染物NO通常用含Ce4+的溶液吸收,
NO
生成HNO、 3,再利用电解法将上述吸收液中的HNO 转化为无毒物质,同时生成Ce4+,
2 2
其原理如图所示。下列说法正确的是
A.H+由右室进入左室
B.Ce4+从电解槽的c口流出,且可循环使用
C.若用甲烷燃料电池作为电源,当消耗33.6L甲烷时,理论上可转化2molHNO
2
D.阴极的电极反应式:2HNO+6H++6e-=N↑+4HO
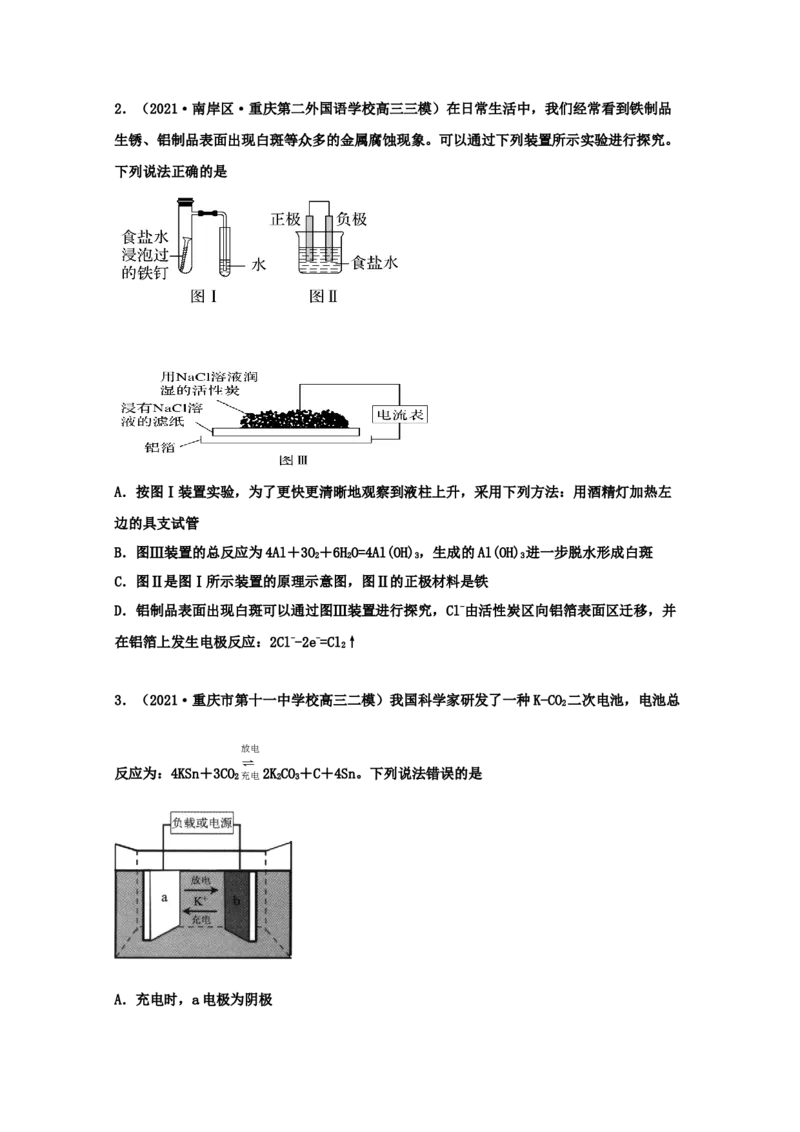
2 2 22.(2021·南岸区·重庆第二外国语学校高三三模)在日常生活中,我们经常看到铁制品
生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。
下列说法正确的是
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,采用下列方法:用酒精灯加热左
边的具支试管
B.图Ⅲ装置的总反应为4Al+3O+6HO=4Al(OH),生成的Al(OH) 进一步脱水形成白斑
2 2 3 3
C.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
D.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并
在铝箔上发生电极反应:2Cl--2e-=Cl↑
2
3.(2021·重庆市第十一中学校高三二模)我国科学家研发了一种K-CO 二次电池,电池总
2
放电
反应为:4KSn+3CO 2KCO+C+4Sn。下列说法错误的是
2充电 2 3
A.充电时,a电极为阴极B.充电时,电路中每转移1 mol e-,b电极质量减少12 g
C.放电时,电子由a极经过外电路流向b极
D.放电时,a电极发生的电极反应为:KSn-e-=K++Sn
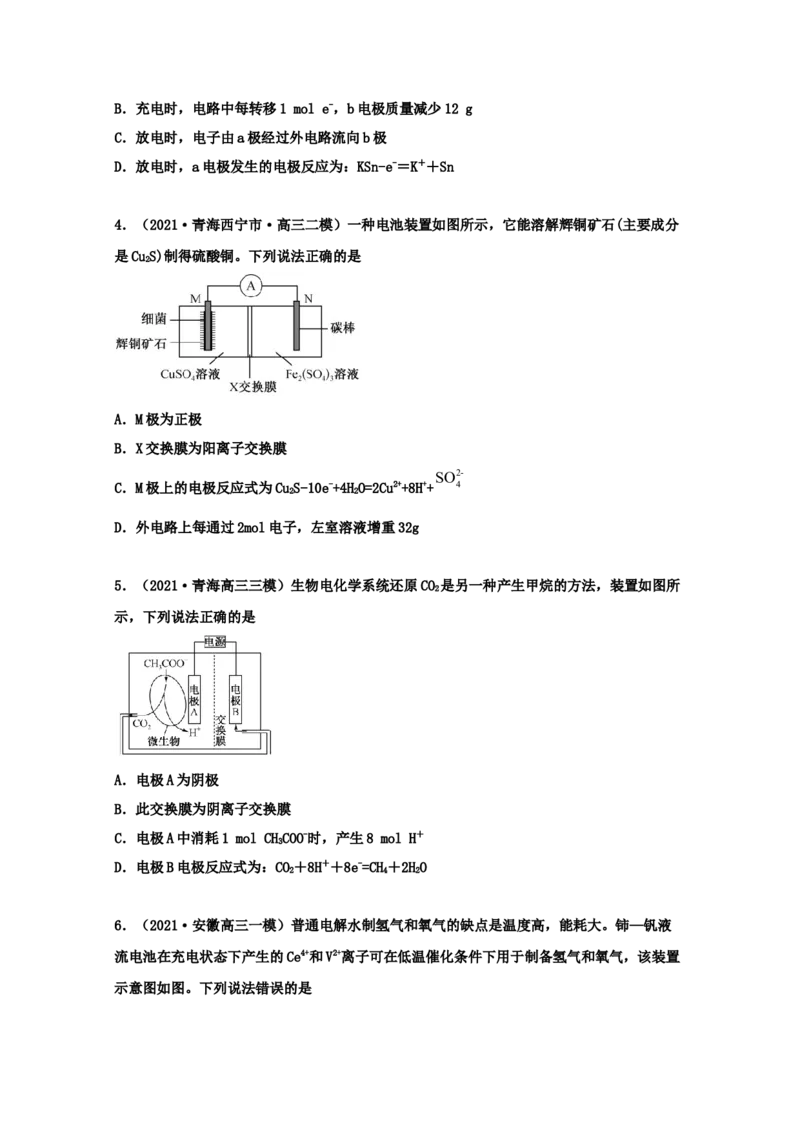
4.(2021·青海西宁市·高三二模)一种电池装置如图所示,它能溶解辉铜矿石(主要成分
是CuS)制得硫酸铜。下列说法正确的是
2
A.M极为正极
B.X交换膜为阳离子交换膜
SO2-
C.M极上的电极反应式为CuS-10e-+4HO=2Cu2++8H++ 4
2 2
D.外电路上每通过2mol电子,左室溶液增重32g
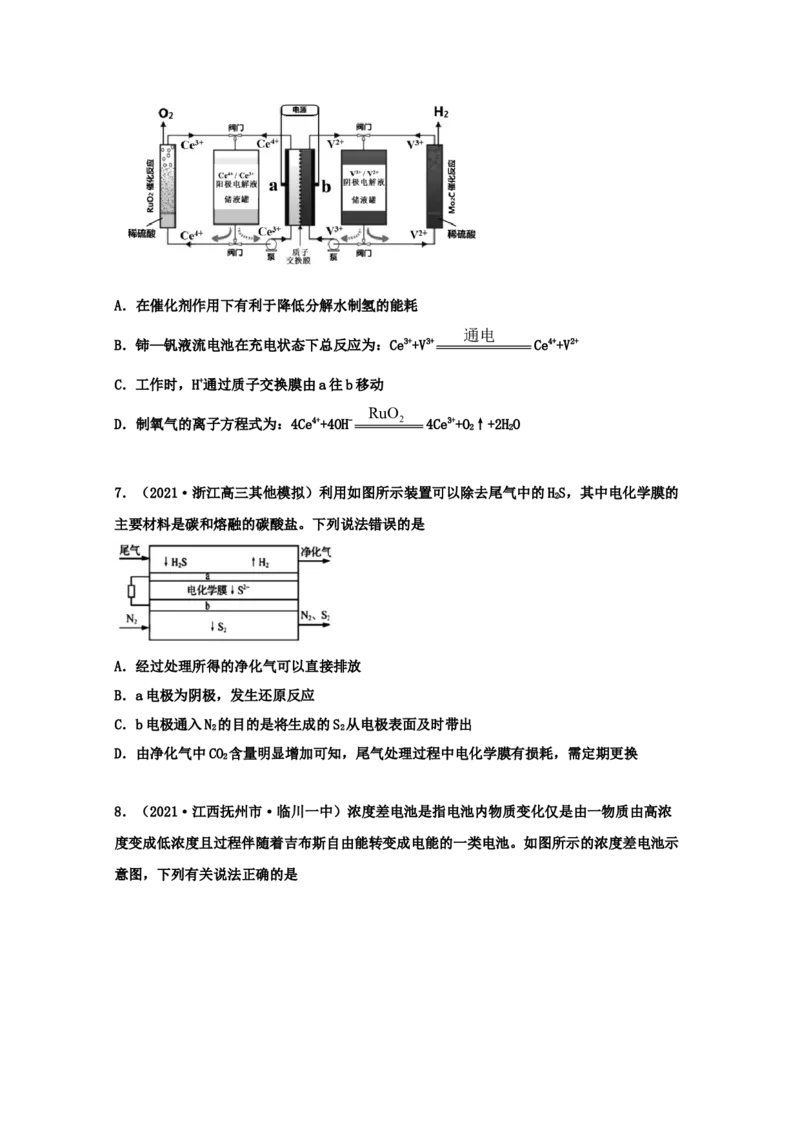
5.(2021·青海高三三模)生物电化学系统还原CO 是另一种产生甲烷的方法,装置如图所
2
示,下列说法正确的是
A.电极A为阴极
B.此交换膜为阴离子交换膜
C.电极A中消耗1 mol CHCOO-时,产生8 mol H+
3
D.电极B电极反应式为:CO+8H++8e-=CH+2HO
2 4 2
6.(2021·安徽高三一模)普通电解水制氢气和氧气的缺点是温度高,能耗大。铈—钒液
流电池在充电状态下产生的Ce4+和V2+离子可在低温催化条件下用于制备氢气和氧气,该装置
示意图如图。下列说法错误的是A.在催化剂作用下有利于降低分解水制氢的能耗
通电
B.铈—钒液流电池在充电状态下总反应为:Ce3++V3+ Ce4++V2+
C.工作时,H+通过质子交换膜由a往b移动
RuO
D.制氧气的离子方程式为:4Ce4++4OH- 2 4Ce3++O↑+2HO
2 2
7.(2021·浙江高三其他模拟)利用如图所示装置可以除去尾气中的HS,其中电化学膜的
2
主要材料是碳和熔融的碳酸盐。下列说法错误的是
A.经过处理所得的净化气可以直接排放
B.a电极为阴极,发生还原反应
C.b电极通入N 的目的是将生成的S 从电极表面及时带出
2 2
D.由净化气中CO 含量明显增加可知,尾气处理过程中电化学膜有损耗,需定期更换
2
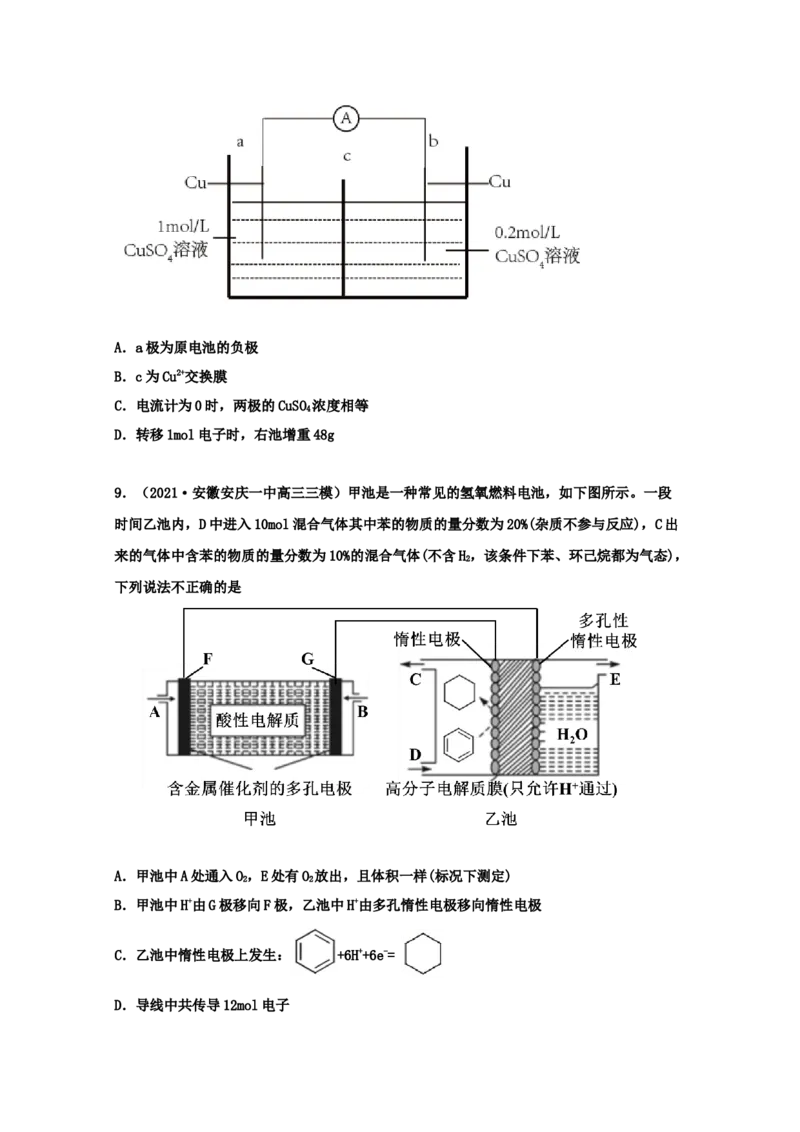
8.(2021·江西抚州市·临川一中)浓度差电池是指电池内物质变化仅是由一物质由高浓
度变成低浓度且过程伴随着吉布斯自由能转变成电能的一类电池。如图所示的浓度差电池示
意图,下列有关说法正确的是A.a极为原电池的负极
B.c为Cu2+交换膜
C.电流计为0时,两极的CuSO 浓度相等
4
D.转移1mol电子时,右池增重48g
9.(2021·安徽安庆一中高三三模)甲池是一种常见的氢氧燃料电池,如下图所示。一段
时间乙池内,D中进入10mol混合气体其中苯的物质的量分数为20%(杂质不参与反应),C出
来的气体中含苯的物质的量分数为10%的混合气体(不含H,该条件下苯、环己烷都为气态),
2
下列说法不正确的是
A.甲池中A处通入O,E处有O 放出,且体积一样(标况下测定)
2 2
B.甲池中H+由G极移向F极,乙池中H+由多孔惰性电极移向惰性电极
C.乙池中惰性电极上发生: +6H++6e-=
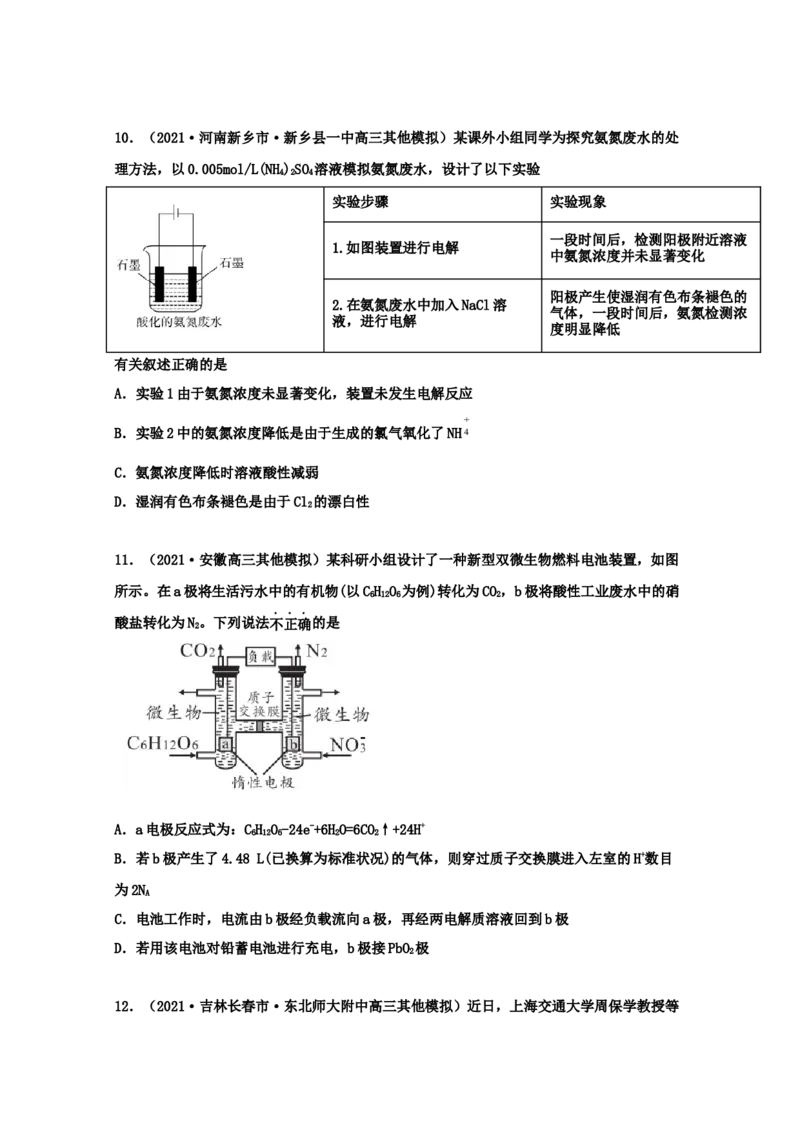
D.导线中共传导12mol电子10.(2021·河南新乡市·新乡县一中高三其他模拟)某课外小组同学为探究氨氮废水的处
理方法,以0.005mol/L(NH)SO 溶液模拟氨氮废水,设计了以下实验
4 2 4
实验步骤 实验现象
一段时间后,检测阳极附近溶液
1.如图装置进行电解
中氨氮浓度并未显著变化
阳极产生使湿润有色布条褪色的
2.在氨氮废水中加入NaCl溶
气体,一段时间后,氨氮检测浓
液,进行电解
度明显降低
有关叙述正确的是
A.实验1由于氨氮浓度未显著变化,装置未发生电解反应
+
B.实验2中的氨氮浓度降低是由于生成的氯气氧化了NH4
C.氨氮浓度降低时溶液酸性减弱
D.湿润有色布条褪色是由于Cl 的漂白性
2
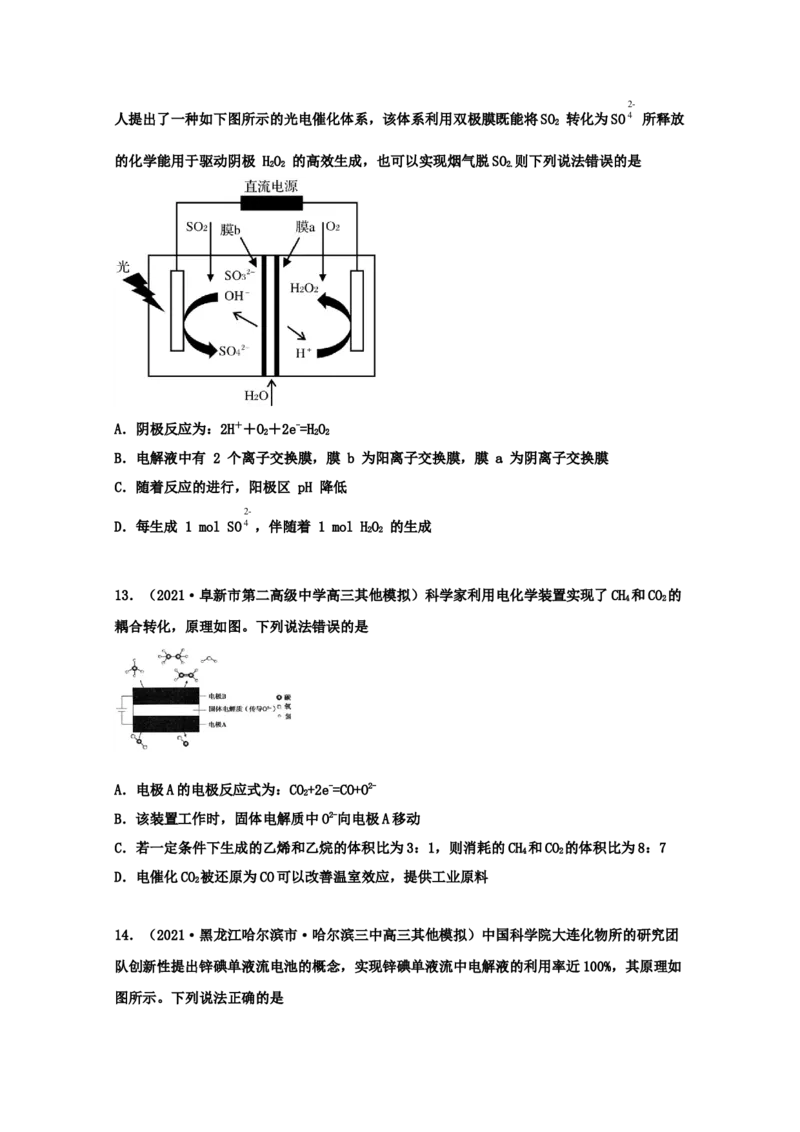
11.(2021·安徽高三其他模拟)某科研小组设计了一种新型双微生物燃料电池装置,如图
所示。在a极将生活污水中的有机物(以CH O 为例)转化为CO,b极将酸性工业废水中的硝
6 12 6 2
酸盐转化为N。下列说法不正确的是
2
A.a电极反应式为:CH O-24e-+6HO=6CO↑+24H+
6 12 6 2 2
B.若b极产生了4.48 L(已换算为标准状况)的气体,则穿过质子交换膜进入左室的H+数目
为2N
A
C.电池工作时,电流由b极经负载流向a极,再经两电解质溶液回到b极
D.若用该电池对铅蓄电池进行充电,b极接PbO 极
2
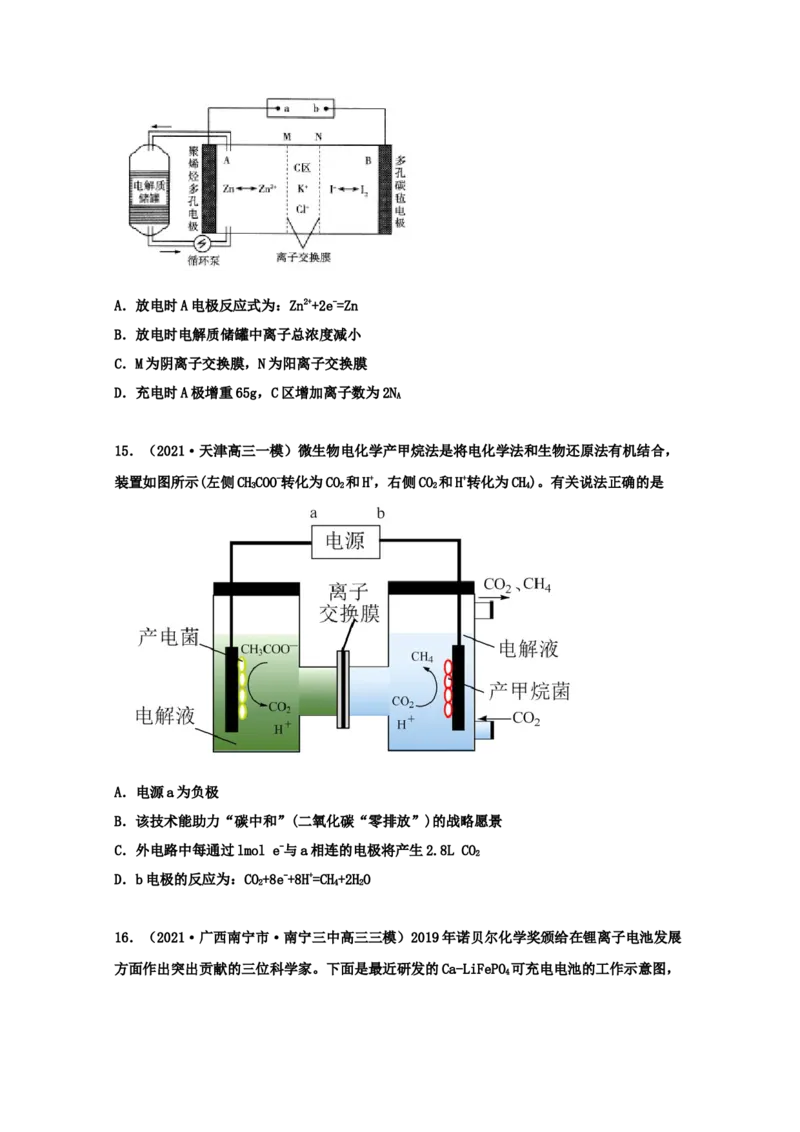
12.(2021·吉林长春市·东北师大附中高三其他模拟)近日,上海交通大学周保学教授等2-
人提出了一种如下图所示的光电催化体系,该体系利用双极膜既能将SO 转化为SO4 所释放
2
的化学能用于驱动阴极 HO 的高效生成,也可以实现烟气脱SO 则下列说法错误的是
2 2 2.
A.阴极反应为:2H++O+2e-=HO
2 2 2
B.电解液中有 2 个离子交换膜,膜 b 为阳离子交换膜,膜 a 为阴离子交换膜
C.随着反应的进行,阳极区 pH 降低
2-
D.每生成 1 mol SO4 ,伴随着 1 mol HO 的生成
2 2
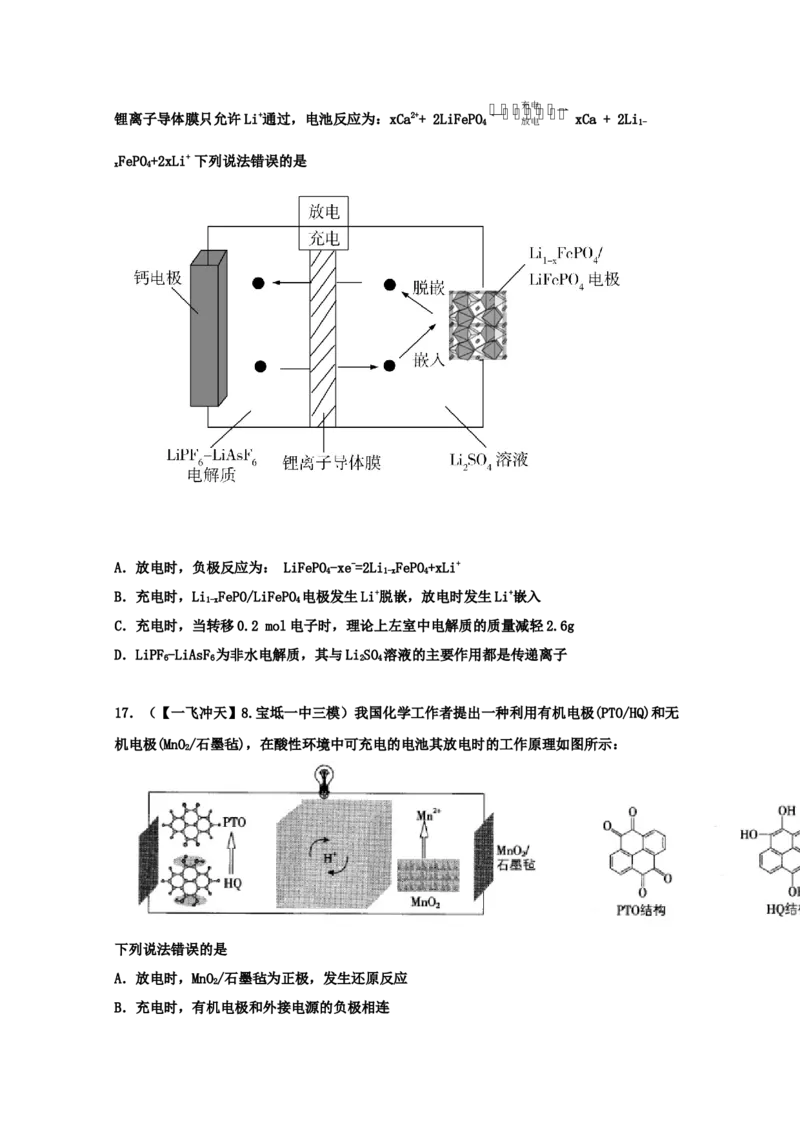
13.(2021·阜新市第二高级中学高三其他模拟)科学家利用电化学装置实现了CH 和CO 的
4 2
耦合转化,原理如图。下列说法错误的是
A.电极A的电极反应式为:CO+2e-=CO+O2-
2
B.该装置工作时,固体电解质中O2-向电极A移动
C.若一定条件下生成的乙烯和乙烷的体积比为3:1,则消耗的CH 和CO 的体积比为8:7
4 2
D.电催化CO 被还原为CO可以改善温室效应,提供工业原料
2
14.(2021·黑龙江哈尔滨市·哈尔滨三中高三其他模拟)中国科学院大连化物所的研究团
队创新性提出锌碘单液流电池的概念,实现锌碘单液流中电解液的利用率近100%,其原理如
图所示。下列说法正确的是A.放电时A电极反应式为:Zn2++2e-=Zn
B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜
D.充电时A极增重65g,C区增加离子数为2N
A
15.(2021·天津高三一模)微生物电化学产甲烷法是将电化学法和生物还原法有机结合,
装置如图所示(左侧CHCOO-转化为CO 和H+,右侧CO 和H+转化为CH)。有关说法正确的是
3 2 2 4
A.电源a为负极
B.该技术能助力“碳中和”(二氧化碳“零排放”)的战略愿景
C.外电路中每通过lmol e-与a相连的电极将产生2.8L CO
2
D.b电极的反应为:CO+8e-+8H+=CH+2HO
2 4 2
16.(2021·广西南宁市·南宁三中高三三模)2019年诺贝尔化学奖颁给在锂离子电池发展
方面作出突出贡献的三位科学家。下面是最近研发的Ca-LiFePO 可充电电池的工作示意图,
4锂离子导体膜只允许Li+通过,电池反应为:xCa2++ 2LiFePO 充 电 xCa + 2Li
4 放电 1-
FePO+2xLi+下列说法错误的是
x 4
A.放电时,负极反应为: LiFePO-xe-=2Li FePO+xLi+
4 1-x 4
B.充电时,Li FePO/LiFePO 电极发生Li+脱嵌,放电时发生Li+嵌入
1-x 4
C.充电时,当转移0.2 mol电子时,理论上左室中电解质的质量减轻2.6g
D.LiPF-LiAsF 为非水电解质,其与LiSO 溶液的主要作用都是传递离子
6 6 2 4
17.(【一飞冲天】8.宝坻一中三模)我国化学工作者提出一种利用有机电极(PTO/HQ)和无
机电极(MnO/石墨毡),在酸性环境中可充电的电池其放电时的工作原理如图所示:
2
下列说法错误的是
A.放电时,MnO/石墨毡为正极,发生还原反应
2
B.充电时,有机电极和外接电源的负极相连C.放电时,MnO/石墨毡电极的电极反应式为MnO+2e-+4H+=Mn2++2HO
2 2 2
D.充电时,有机电极的电极反应式为PTO+4e-+4HO=HQ+4OH-
2
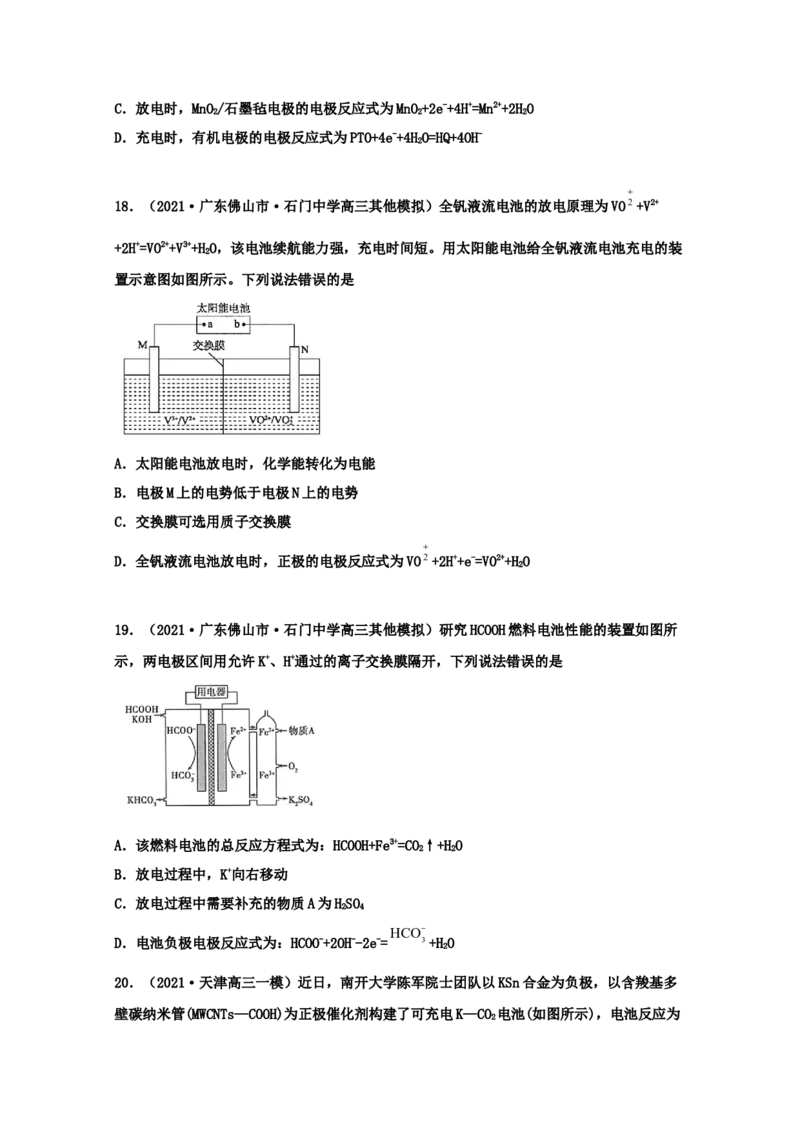
18.(2021·广东佛山市·石门中学高三其他模拟)全钒液流电池的放电原理为VO2+V2+
+2H+=VO2++V3++HO,该电池续航能力强,充电时间短。用太阳能电池给全钒液流电池充电的装
2
置示意图如图所示。下列说法错误的是
A.太阳能电池放电时,化学能转化为电能
B.电极M上的电势低于电极N上的电势
C.交换膜可选用质子交换膜
D.全钒液流电池放电时,正极的电极反应式为VO2+2H++e-=VO2++HO
2
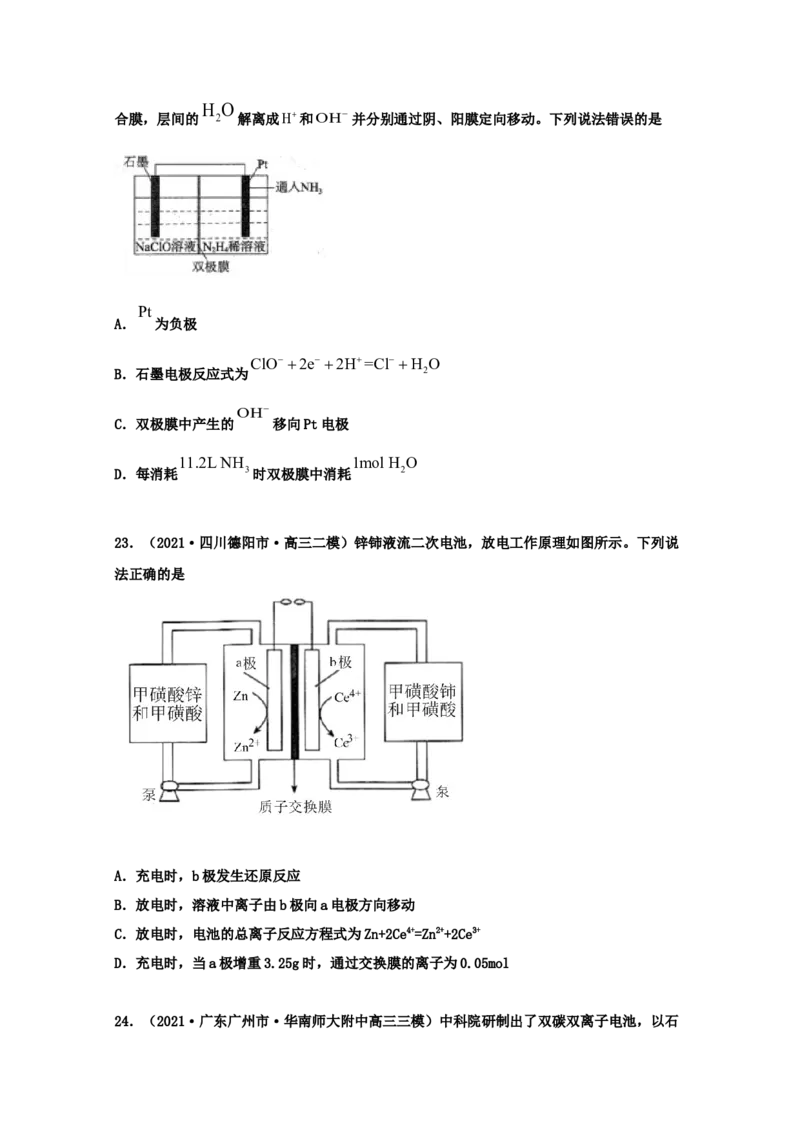
19.(2021·广东佛山市·石门中学高三其他模拟)研究HCOOH燃料电池性能的装置如图所
示,两电极区间用允许K+、H+通过的离子交换膜隔开,下列说法错误的是
A.该燃料电池的总反应方程式为:HCOOH+Fe3+=CO↑+HO
2 2
B.放电过程中,K+向右移动
C.放电过程中需要补充的物质A为HSO
2 4
HCO
D.电池负极电极反应式为:HCOO-+2OH--2e-= 3+HO
2
20.(2021·天津高三一模)近日,南开大学陈军院士团队以KSn合金为负极,以含羧基多
壁碳纳米管(MWCNTs—COOH)为正极催化剂构建了可充电K—CO 电池(如图所示),电池反应为
24KSn+3CO 2
充
放
电
电
2K 2 CO 3 +C+4Sn,其中生成的K 2 CO 3 附着在正极上。该成果对改善环境和缓解
能源问题具有巨大潜力。下列说法正确的是
A.放电时,电子由KSn合金经酯基电解质流向MWCNTs—COOH
B.电池每吸收22.4LCO,电路中转移4mole-
2
C.充电时,阳极电极反应式为:C-4e-+2KCO=3CO↑+4K+
2 3 2
D.为了更好的吸收温室气体CO,可用适当浓度的KOH溶液代替酯基电解质
2
21.(2021·天津高三一模)锌电池具有价格便宜、比能量大、可充电等优点。一种新型锌
电池的工作原理如图所示(凝胶中允许离子生成或迁移)。下列说法正确的是
SO2-
A.放电过程中, 4 向a极迁移
B.充电过程中,b电极反应为:Zn2++2e-=Zn
C.充电时,a电极与电源正极相连
D.放电过程中,转移0.4mole-时,a电极消耗0.4molH+
N H
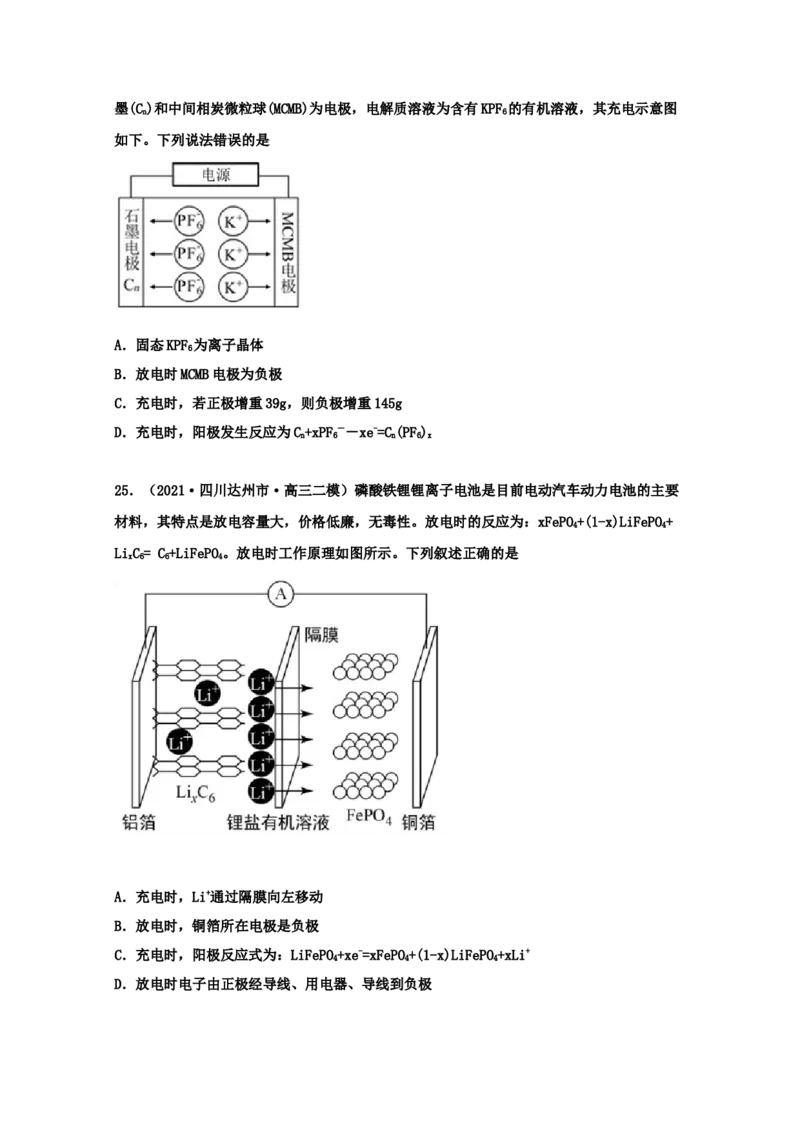
22.(2021·辽宁高三其他模拟)某实验室设计了如图装置制备 2 4。双极膜是阴、阳复H O
合膜,层间的 2 解离成H和OH 并分别通过阴、阳膜定向移动。下列说法错误的是
Pt
A. 为负极
ClO 2e 2H=Cl H O
B.石墨电极反应式为 2
OH
C.双极膜中产生的 移向Pt电极
11.2L NH 1mol H O
D.每消耗 3时双极膜中消耗 2
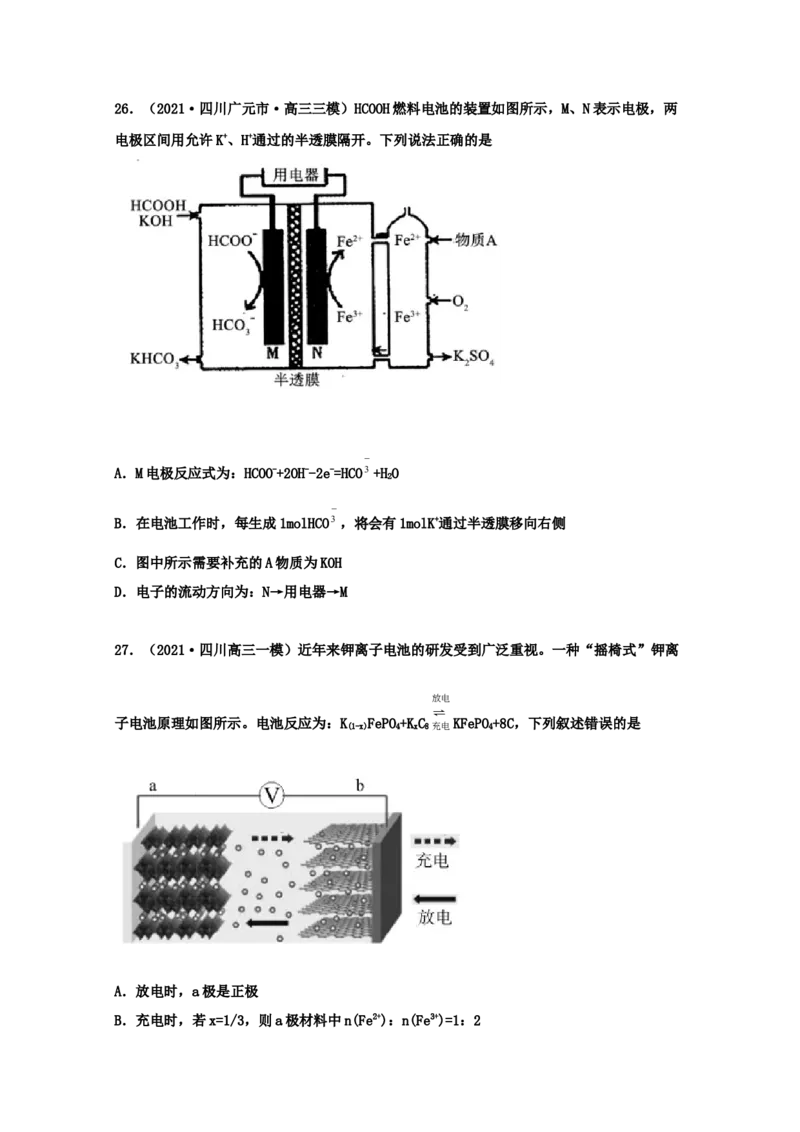
23.(2021·四川德阳市·高三二模)锌铈液流二次电池,放电工作原理如图所示。下列说
法正确的是
A.充电时,b极发生还原反应
B.放电时,溶液中离子由b极向a电极方向移动
C.放电时,电池的总离子反应方程式为Zn+2Ce4+=Zn2++2Ce3+
D.充电时,当a极增重3.25g时,通过交换膜的离子为0.05mol
24.(2021·广东广州市·华南师大附中高三三模)中科院研制出了双碳双离子电池,以石墨(C)和中间相炭微粒球(MCMB)为电极,电解质溶液为含有KPF 的有机溶液,其充电示意图
n 6
如下。下列说法错误的是
A.固态KPF 为离子晶体
6
B.放电时MCMB电极为负极
C.充电时,若正极增重39g,则负极增重145g
D.充电时,阳极发生反应为C+xPF--xe-=C(PF)
n 6 n 6 x
25.(2021·四川达州市·高三二模)磷酸铁锂锂离子电池是目前电动汽车动力电池的主要
材料,其特点是放电容量大,价格低廉,无毒性。放电时的反应为:xFePO+(1-x)LiFePO+
4 4
LiC= C+LiFePO。放电时工作原理如图所示。下列叙述正确的是
x 6 6 4
A.充电时,Li+通过隔膜向左移动
B.放电时,铜箔所在电极是负极
C.充电时,阳极反应式为:LiFePO+xe-=xFePO+(1-x)LiFePO+xLi+
4 4 4
D.放电时电子由正极经导线、用电器、导线到负极26.(2021·四川广元市·高三三模)HCOOH燃料电池的装置如图所示,M、N表示电极,两
电极区间用允许K+、H+通过的半透膜隔开。下列说法正确的是
A.M电极反应式为:HCOO-+2OH--2e-=HCO3 +HO
2
B.在电池工作时,每生成1molHCO3 ,将会有1molK+通过半透膜移向右侧
C.图中所示需要补充的A物质为KOH
D.电子的流动方向为:N→用电器→M
27.(2021·四川高三一模)近年来钾离子电池的研发受到广泛重视。一种“摇椅式”钾离
放电
子电池原理如图所示。电池反应为:K FePO+KC KFePO+8C,下列叙述错误的是
(1-x) 4 x 8充电 4
A.放电时,a极是正极
B.充电时,若x=1/3,则a极材料中n(Fe2+):n(Fe3+)=1:2C.充电时,b极反应式:xK++xe-+8C=KC
x 8
D.放、充电时,图中箭头所示为K+的移动方向,形同“摇椅”
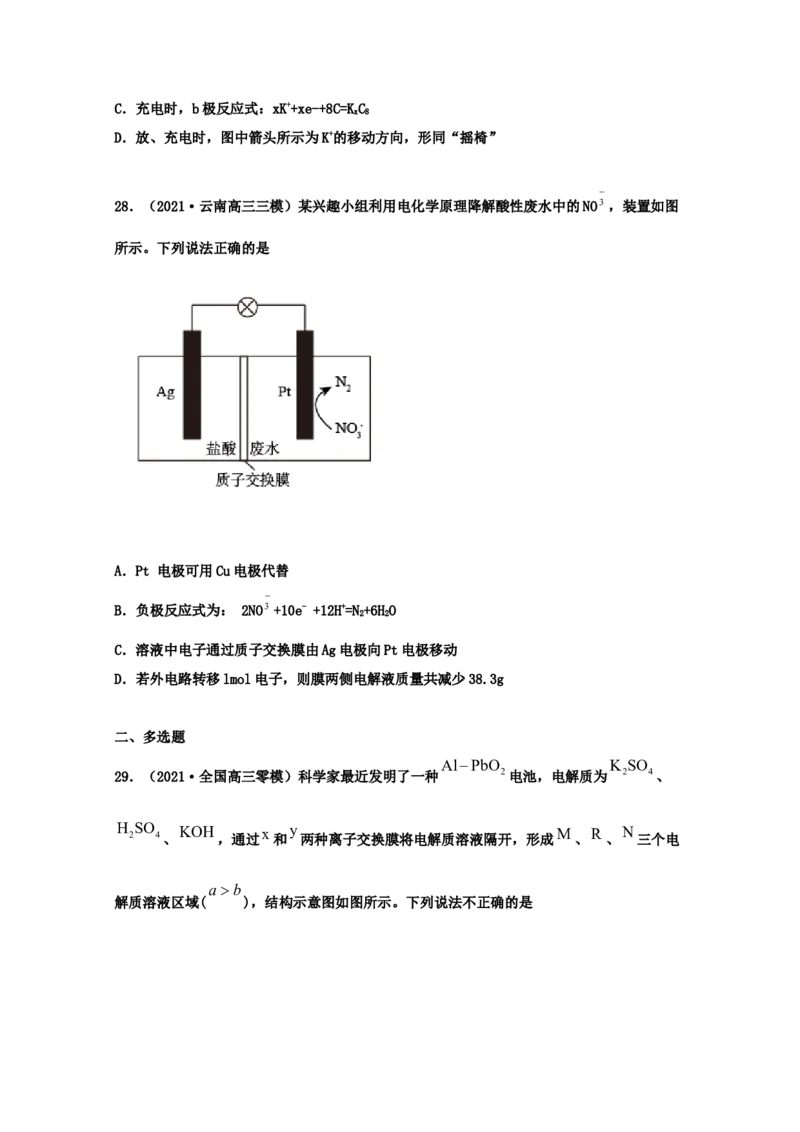
28.(2021·云南高三三模)某兴趣小组利用电化学原理降解酸性废水中的NO3 ,装置如图
所示。下列说法正确的是
A.Pt 电极可用Cu电极代替
B.负极反应式为: 2NO3 +10e- +12H+=N+6HO
2 2
C.溶液中电子通过质子交换膜由Ag电极向Pt电极移动
D.若外电路转移lmol电子,则膜两侧电解液质量共减少38.3g
二、多选题
AlPbO K SO
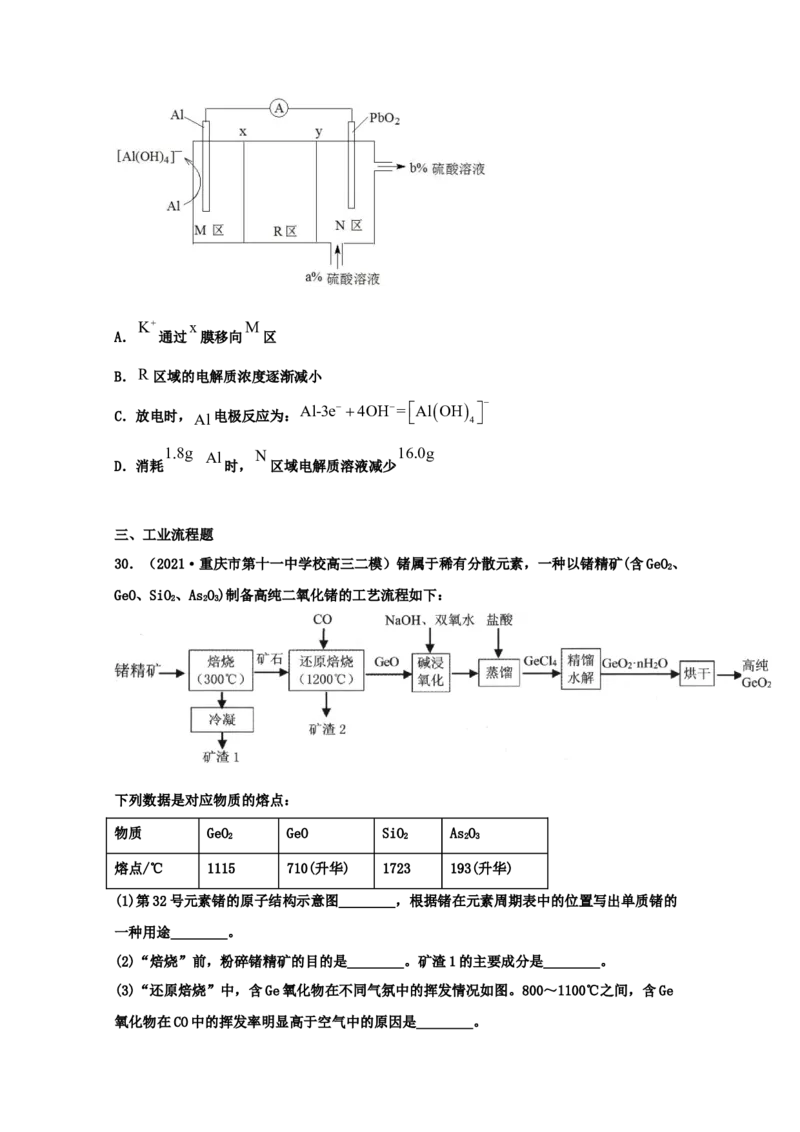
29.(2021·全国高三零模)科学家最近发明了一种 2电池,电解质为 2 4、
H 2 SO 4、 KOH ,通过 x 和 y 两种离子交换膜将电解质溶液隔开,形成 M 、 R 、 N 三个电
a b
解质溶液区域( ),结构示意图如图所示。下列说法不正确的是K x M
A. 通过 膜移向 区
B.R 区域的电解质浓度逐渐减小
Al-3e 4OH=AlOH
C.放电时,Al电极反应为:
4
1.8g Al N 16.0g
D.消耗 时, 区域电解质溶液减少
三、工业流程题
30.(2021·重庆市第十一中学校高三二模)锗属于稀有分散元素,一种以锗精矿(含GeO、
2
GeO、SiO、AsO)制备高纯二氧化锗的工艺流程如下:
2 2 3
下列数据是对应物质的熔点:
物质 GeO GeO SiO AsO
2 2 2 3
熔点/℃ 1115 710(升华) 1723 193(升华)
(1)第32号元素锗的原子结构示意图________,根据锗在元素周期表中的位置写出单质锗的
一种用途________。
(2)“焙烧”前,粉碎锗精矿的目的是________。矿渣1的主要成分是________。
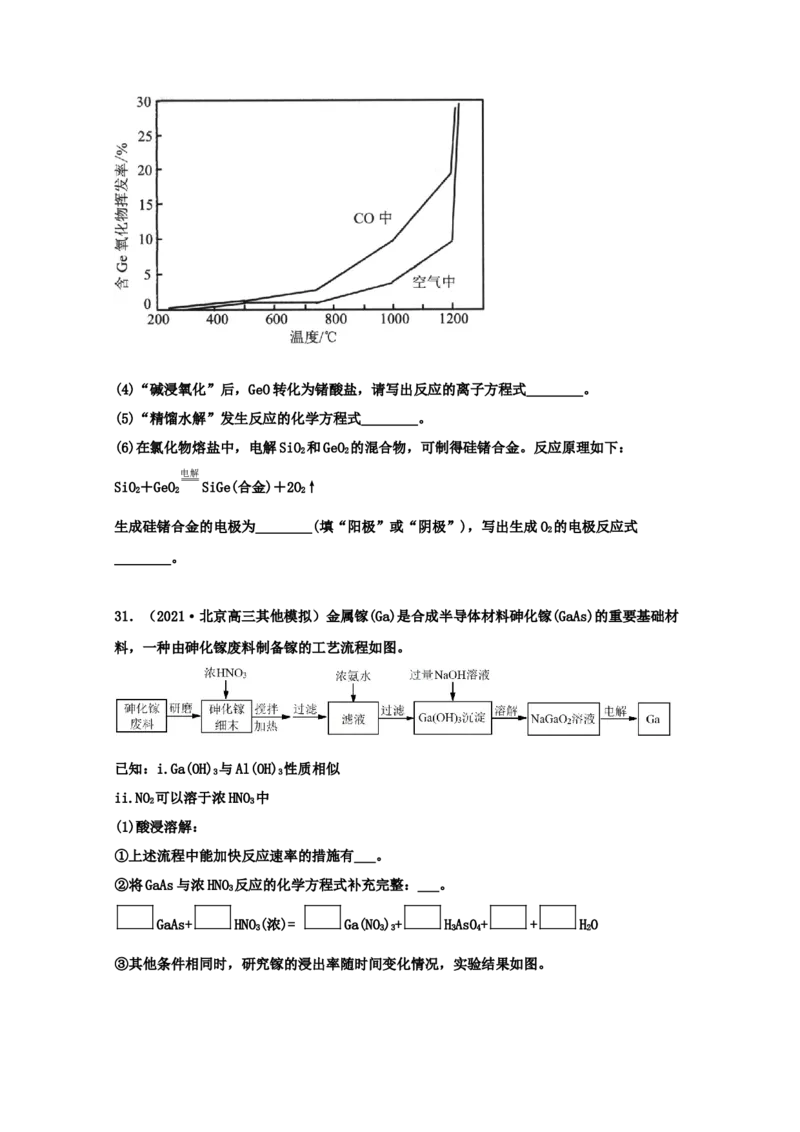
(3)“还原焙烧”中,含Ge氧化物在不同气氛中的挥发情况如图。800~1100℃之间,含Ge
氧化物在CO中的挥发率明显高于空气中的原因是________。(4)“碱浸氧化”后,GeO转化为锗酸盐,请写出反应的离子方程式________。
(5)“精馏水解”发生反应的化学方程式________。
(6)在氯化物熔盐中,电解SiO 和GeO 的混合物,可制得硅锗合金。反应原理如下:
2 2
电解
SiO+GeO SiGe(合金)+2O↑
2 2 2
生成硅锗合金的电极为________(填“阳极”或“阴极”),写出生成O 的电极反应式
2
________。
31.(2021·北京高三其他模拟)金属镓(Ga)是合成半导体材料砷化镓(GaAs)的重要基础材
料,一种由砷化镓废料制备镓的工艺流程如图。
已知:i.Ga(OH) 与Al(OH) 性质相似
3 3
ii.NO 可以溶于浓HNO 中
2 3
(1)酸浸溶解:
①上述流程中能加快反应速率的措施有___。
②将GaAs与浓HNO 反应的化学方程式补充完整:___。
3
GaAs+ HNO(浓)= Ga(NO)+ HAsO+ + HO
3 3 3 3 4 2
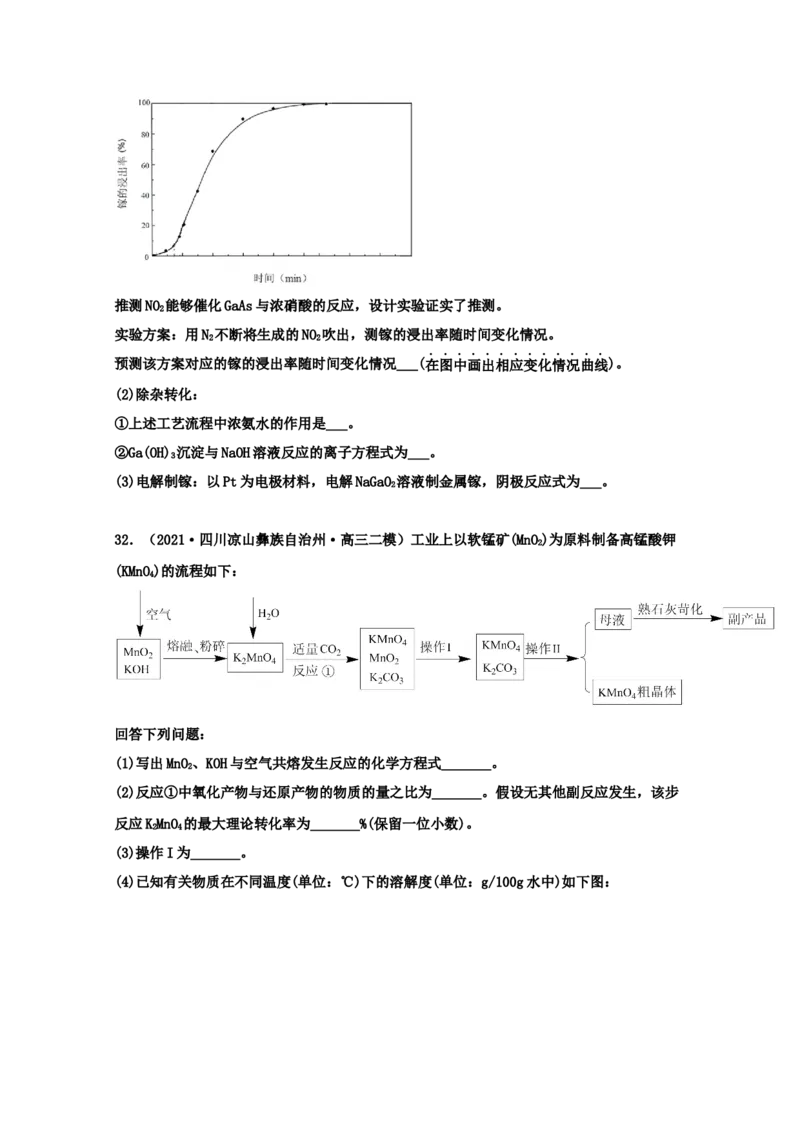
③其他条件相同时,研究镓的浸出率随时间变化情况,实验结果如图。推测NO 能够催化GaAs与浓硝酸的反应,设计实验证实了推测。
2
实验方案:用N 不断将生成的NO 吹出,测镓的浸出率随时间变化情况。
2 2
预测该方案对应的镓的浸出率随时间变化情况___(在图中画出相应变化情况曲线)。
(2)除杂转化:
①上述工艺流程中浓氨水的作用是___。
②Ga(OH) 沉淀与NaOH溶液反应的离子方程式为___。
3
(3)电解制镓:以Pt为电极材料,电解NaGaO 溶液制金属镓,阴极反应式为___。
2
32.(2021·四川凉山彝族自治州·高三二模)工业上以软锰矿(MnO)为原料制备高锰酸钾
2
(KMnO)的流程如下:
4
回答下列问题:
(1)写出MnO、KOH与空气共熔发生反应的化学方程式_______。
2
(2)反应①中氧化产物与还原产物的物质的量之比为_______。假设无其他副反应发生,该步
反应KMnO 的最大理论转化率为_______%(保留一位小数)。
2 4
(3)操作I为_______。
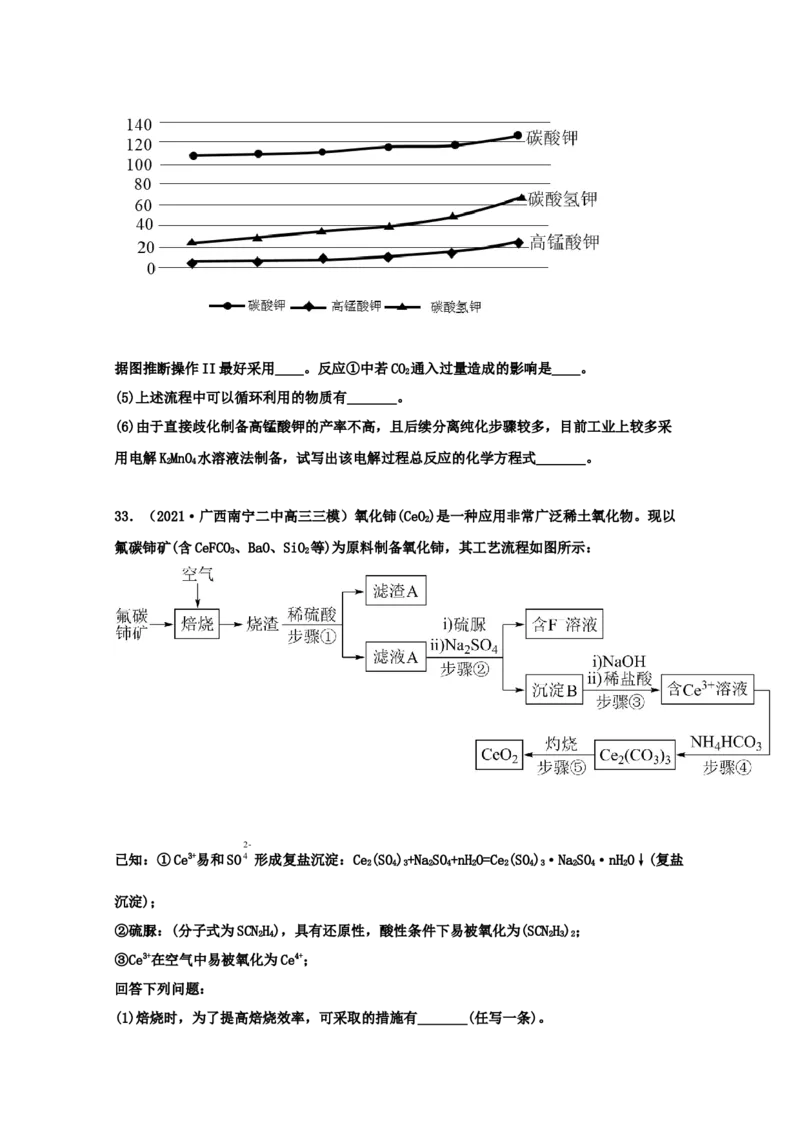
(4)已知有关物质在不同温度(单位:℃)下的溶解度(单位:g/100g水中)如下图:据图推断操作II最好采用____。反应①中若CO 通入过量造成的影响是____。
2
(5)上述流程中可以循环利用的物质有_______。
(6)由于直接歧化制备高锰酸钾的产率不高,且后续分离纯化步骤较多,目前工业上较多采
用电解KMnO 水溶液法制备,试写出该电解过程总反应的化学方程式_______。
2 4
33.(2021·广西南宁二中高三三模)氧化铈(CeO)是一种应用非常广泛稀土氧化物。现以
2
氟碳铈矿(含CeFCO、BaO、SiO 等)为原料制备氧化铈,其工艺流程如图所示:
3 2
2-
已知:①Ce3+易和SO4 形成复盐沉淀:Ce(SO)+NaSO+nHO=Ce(SO)·NaSO·nHO↓(复盐
2 4 3 2 4 2 2 4 3 2 4 2
沉淀);
②硫脲:(分子式为SCNH),具有还原性,酸性条件下易被氧化为(SCNH);
2 4 2 3 2
③Ce3+在空气中易被氧化为Ce4+;
回答下列问题:
(1)焙烧时,为了提高焙烧效率,可采取的措施有_______(任写一条)。(2)滤渣A的主要成分是_______、_______。
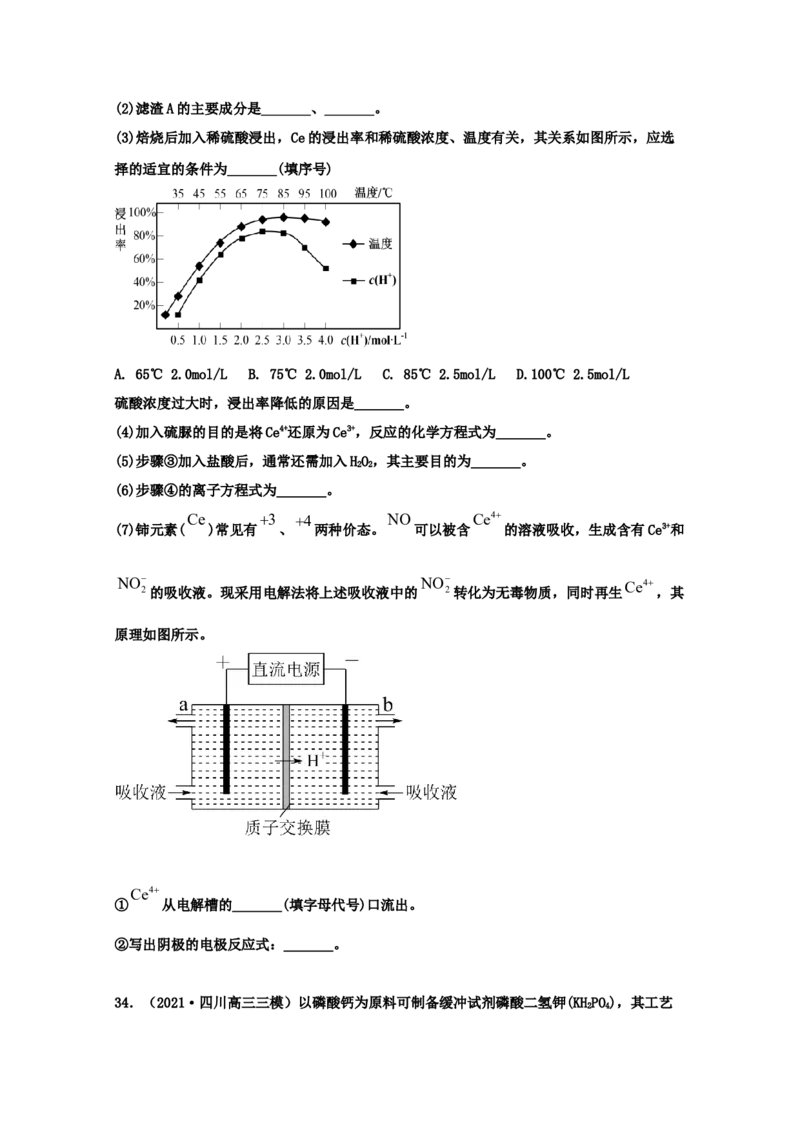
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,应选
择的适宜的条件为_______(填序号)
A. 65℃ 2.0mol/L B. 75℃ 2.0mol/L C. 85℃ 2.5mol/L D.100℃ 2.5mol/L
硫酸浓度过大时,浸出率降低的原因是_______。
(4)加入硫脲的目的是将Ce4+还原为Ce3+,反应的化学方程式为_______。
(5)步骤③加入盐酸后,通常还需加入HO,其主要目的为_______。
2 2
(6)步骤④的离子方程式为_______。
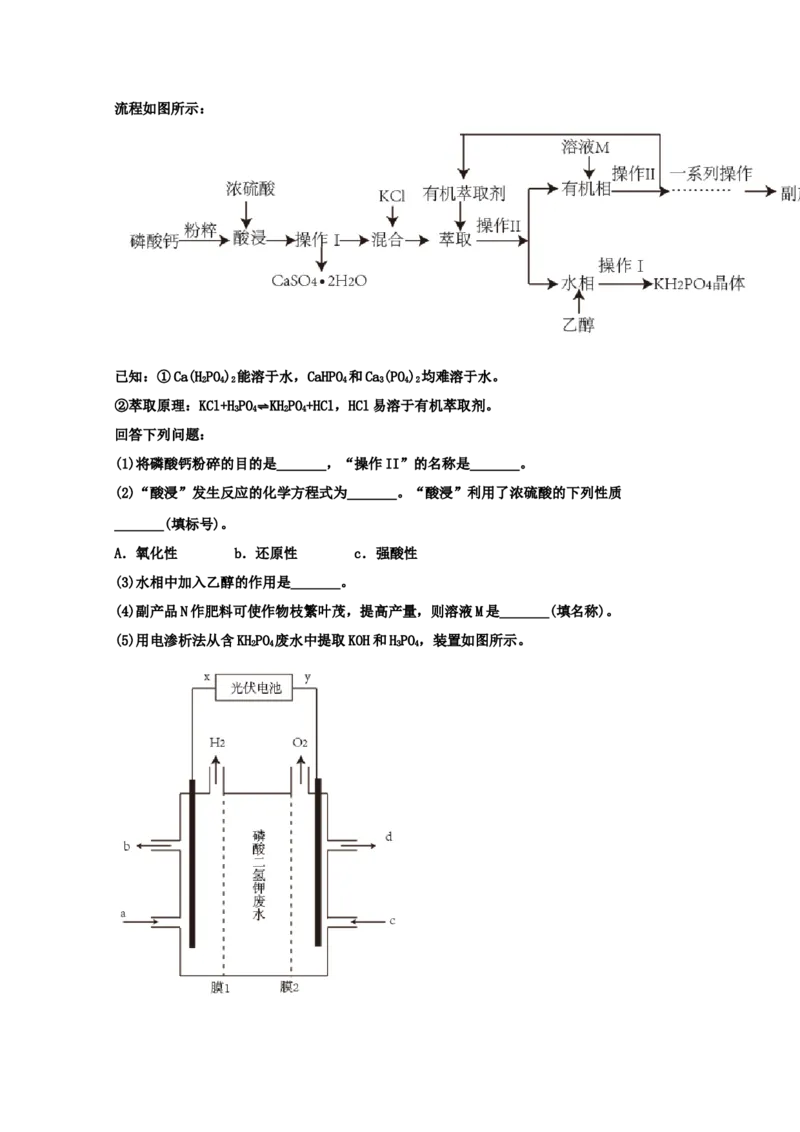
Ce 3 4 NO Ce4
(7)铈元素( )常见有 、 两种价态。 可以被含 的溶液吸收,生成含有Ce3+和
NO NO
Ce4
2的吸收液。现采用电解法将上述吸收液中的 2转化为无毒物质,同时再生 ,其
原理如图所示。
Ce4
① 从电解槽的_______(填字母代号)口流出。
②写出阴极的电极反应式:_______。
34.(2021·四川高三三模)以磷酸钙为原料可制备缓冲试剂磷酸二氢钾(KHPO),其工艺
2 4流程如图所示:
已知:①Ca(HPO) 能溶于水,CaHPO 和Ca(PO) 均难溶于水。
2 4 2 4 3 4 2
②萃取原理:KCl+HPO KHPO+HCl,HCl易溶于有机萃取剂。
3 4 2 4
回答下列问题:
(1)将磷酸钙粉碎的目的是_______,“操作II”的名称是_______。
(2)“酸浸”发生反应的化学方程式为_______。“酸浸”利用了浓硫酸的下列性质
_______(填标号)。
A.氧化性 b.还原性 c.强酸性
(3)水相中加入乙醇的作用是_______。
(4)副产品N作肥料可使作物枝繁叶茂,提高产量,则溶液M是_______(填名称)。
(5)用电渗析法从含KHPO 废水中提取KOH和HPO,装置如图所示。
2 4 3 4①b物质为_______。
②阳极反应式为_______。
四、原理综合题
35.(2021·广东广州市·华南师大附中高三三模)(1)NH 合成技术的迅速发展解决了维持
3
过去100年人口增长所需食物摄入的紧迫性。科学家一直致力研究常温、常压下“人工固
氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N 在催化剂(掺有少量FeO 的
2 2 3
TiO)表面与水发生反应,生成的主要产物为NH,进一步研究NH 生成量与温度的关系,部分
2 3 3
实验数据见下表(光照、N 压力1.0×105Pa、反应时间3h):
2
T/K 303 313 323 353
NH 生成量/(10-
3 4.8 5.9 6.0 2.0
6mol)
相应的热化学方程式如下:2N(g)+6HO(1)
4NH(g)+3O(g) ΔH=+1530.4kJ·mol-1
2 2 3 2
①实验中323K时,该反应的平均反应速率为v(N)=___________mol/h。
2
②与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应
速率且增大NH 生成量的建议:___________。
3
③353K比323K,NH 的生成量少的原因可能是___________。
3
④设在恒压为P恒温为T的条件下,密闭容器中充入0.60molN 和1.80molH,高温高压合成
2 2
3
氨,平衡时NH 的物质的量分数为7 ,计算该条件下反应2NH(g)
N(g)+3H(g)的平衡
3 3 2 2
常数Kp___________。(以分压代替浓度表示,分压=总压×物质的量分数)
=
(2)NH 还是重要的化工原料,用于生产多种化工产品如NH 等
3 2 4
①写出2种以NH 为原料制备的常见化工产品的化学式___________(除NH、铵盐外)。
3 2 4
②NH 的电子式为___________,NH 的水溶液呈弱碱性,室温下其电离常数K=1.0×10-6,则
2 4 2 4 1
0.01mol·L-1NH 水溶液的pH=___________(忽略NH 的二级电离和HO的电离)。
2 4 2 4 2
③NH 是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________。
2 4