文档内容
专题 10 铝及其重要化合物
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 铝及其化合物的结构、性质及其应用
考点二 铝及其化合物制备的工艺流程
考点三 铝及其化合物与强酸、强碱反应有关计算
考点一 铝及其化合物的结构、性质及其应用
1.(2023·江苏·统考二模)下列物质的性质和用途具有对应关系的是
A. 熔点高,可用作电解制铝 B. 不稳定,可用于治疗胃酸过多
C.明矾水解生成胶体,可用做絮凝剂 D.铝具有导热性,可用于制备铝热剂
2.(2023·广东·广州市第二中学校联考三模)下图为铝的生产原理示意图,下列相关说法不正确的是
A.冰晶石做助熔剂
B.氧化铝属于过渡晶体
C.金属铁、铜的冶炼方法与铝类似
D.铝在工业上是一种很好的还原剂
3.(2023·上海黄浦·一模)去了膜的铝条放入硫酸铜溶液中,不可能观察到的现象
A.金属表面有气泡 B.银白色金属转变为紫红色
C.出现蓝色沉淀 D.溶液蓝色变浅
4.(2023·上海宝山·统考一模)下列关于铝及其化合物反应的离子方程式书写正确的是
A.铝与NaOH溶液反应:
B. 与NaOH溶液反应:
C.明矾净水原理:
D. 与过量氨水反应:
5.(2023·广东汕头·统考二模)家庭的厨卫管道内常因留有油脂、毛发、菜渣等而造成堵塞,此时可用一
种固体疏通剂疏通。疏通剂主要成分有生物酶、铝粉和 固体。下列有关说法错误的是
1
原创精品资源学科网独家享有版权,侵权必究!A.大多数生物酶的主要成分为蛋白质
B.疏通剂使用时会产生大量可燃性气体,应避免接触明火
C.疏通剂可用于疏通陶瓷、铁制、铝制、塑料管道
D.使用过程中产生的热量和碱性环境可以加速油脂的水解
6.(2023·上海杨浦·统考二模)室温下,能完全溶解 和 反应后的固体混合物的试剂是
A.稀 B.浓 C. 溶液 D.浓
7.(2023·北京海淀·北京市十一学校校考三模)为探究温度、浓度对铝和碳酸钠溶液反应的影响,某兴趣
小组查询了相关资料,并进行了实验探究。以下三组实验均采用了相同形状且等质量的打磨后的铝片。
【文献资料】
(I)铝和碱液的反应实质是铝先和水反应生成 和 ,生成的 和 反应生成 -而
溶解。
(II)碳酸氢钠溶液常温下就能缓慢分解,温度越高分解速率越大。
实 温度/
实验现象
验 溶液
① 25 0.5 5 有细小的气泡
有较多气泡,气体不能使澄清石灰水变浑
② 25 a 5
浊;用试管收集的气体靠近火焰有爆鸣声
有大量白色絮状沉淀和气泡,气体可使澄
③ 80 2.0 5 清石灰水变浑浊;气体通过 溶液除
杂后用试管收集,靠近火焰有爆鸣声
下列说法不正确的是
A.
B.实验③的反应速率比实验②更大的原因之一是实验③中 浓度更大
C.实验③中的气体为 混合气体,白色沉淀的产生可能是由于 往溶液上方移动时与
反应生成
D.将实验②中的 溶液换成相同浓度的 溶液,无白色沉淀生成
8.(2023·湖北·校联考二模)化学焊接技术的原理之一是利用焊剂(主要成分为Al与CaO)在高温下反应制得液态金属(或合金),凝固后,除去焊接点表面的焊渣,实现焊件金属的焊接。下列说法错误的是
A.Al与Fe O 也能发生类似反应
2 3
B.焊渣的主要成分是Al(OH)
3
C.焊接前可用还原性气体在加热条件下除去焊件金属表面的氧化膜
D.若在反应体系中加入低熔点金属,则可形成低熔点液态合金便于焊接
9.(2023·上海黄浦·统考二模)将去掉氧化膜的铝片放入足量NaCO 溶液中,铝片表面产生气泡,充分
2 3
反应后得到无色溶液M。下列分析错误的是
A.产生的气体中有H B.反应与 水解有关
2
C.Al(OH) 向酸式电离方向移动 D.M中含大量:Na+、Al3+、
3
10.(2023·重庆九龙坡·高三重庆市育才中学校考开学考试)氮化铝(AlN)是一种性能优异的新型材料,在
许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝并检验其纯度。
查阅资料:
①实验室用饱和NaNO 溶液与NH C1溶液共热制N:
2 4 2
NaNO +NHC1 NaCl+N ↑+2H O
2 4 2 2
②工业制氮化铝:Al O+3C+N 2AlN+3CO,氮化铝在高温下能水解。
2 3 2
③AlN与NaOH饱和溶液反应:AlN+NaOH+H O=NaAlO +NH↑。
2 2 3
Ⅰ.氮化铝的制备
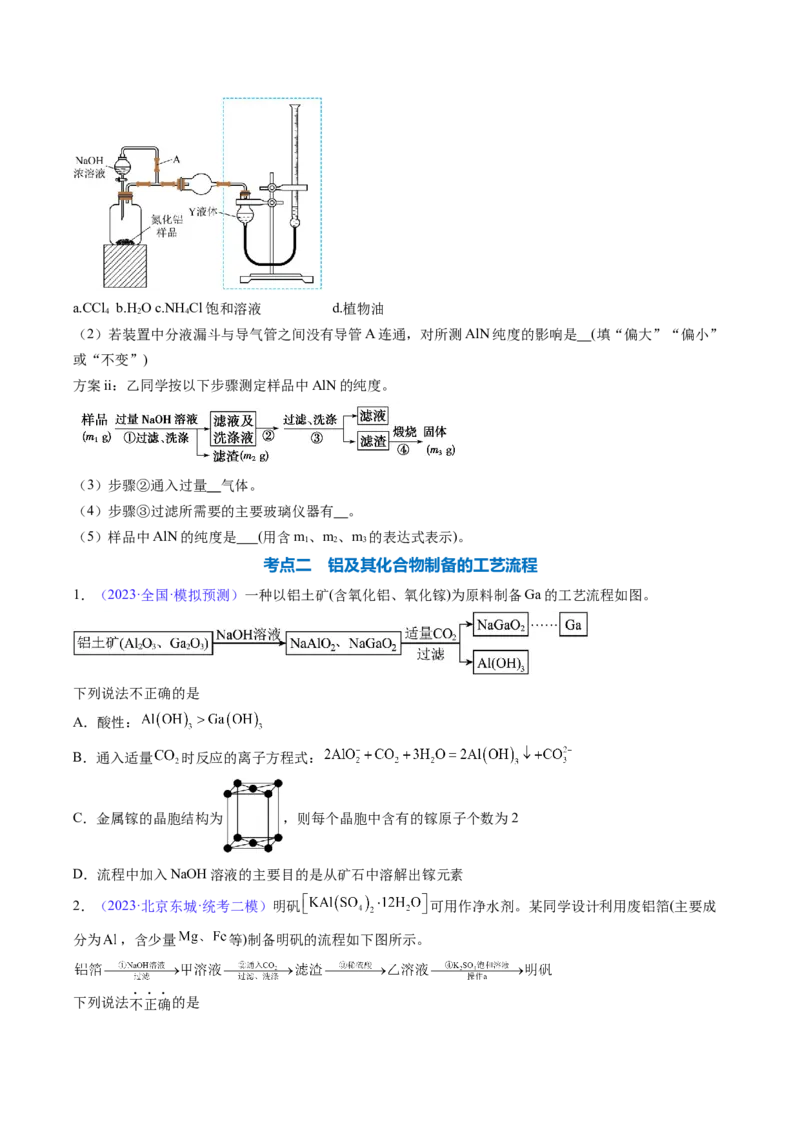
(1)实验中使用的装置如图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→a→b→ (根据实验
需要,上述装置可使用多次)。
(2)B装置内的X液体可能是 ,E装置内氯化钯溶液的作用可能是 。
Ⅱ.氮化铝纯度的测定
方案i:甲同学用如图装置测定AlN的纯度(部分夹持装置已略去)。
(1)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是 。a.CCl b.H O c.NH Cl饱和溶液 d.植物油
4 2 4
(2)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是 (填“偏大”“偏小”
或“不变”)
方案ii:乙同学按以下步骤测定样品中AlN的纯度。
(3)步骤②通入过量 气体。
(4)步骤③过滤所需要的主要玻璃仪器有 。
(5)样品中AlN的纯度是 (用含m、m、m 的表达式表示)。
1 2 3
考点二 铝及其化合物制备的工艺流程
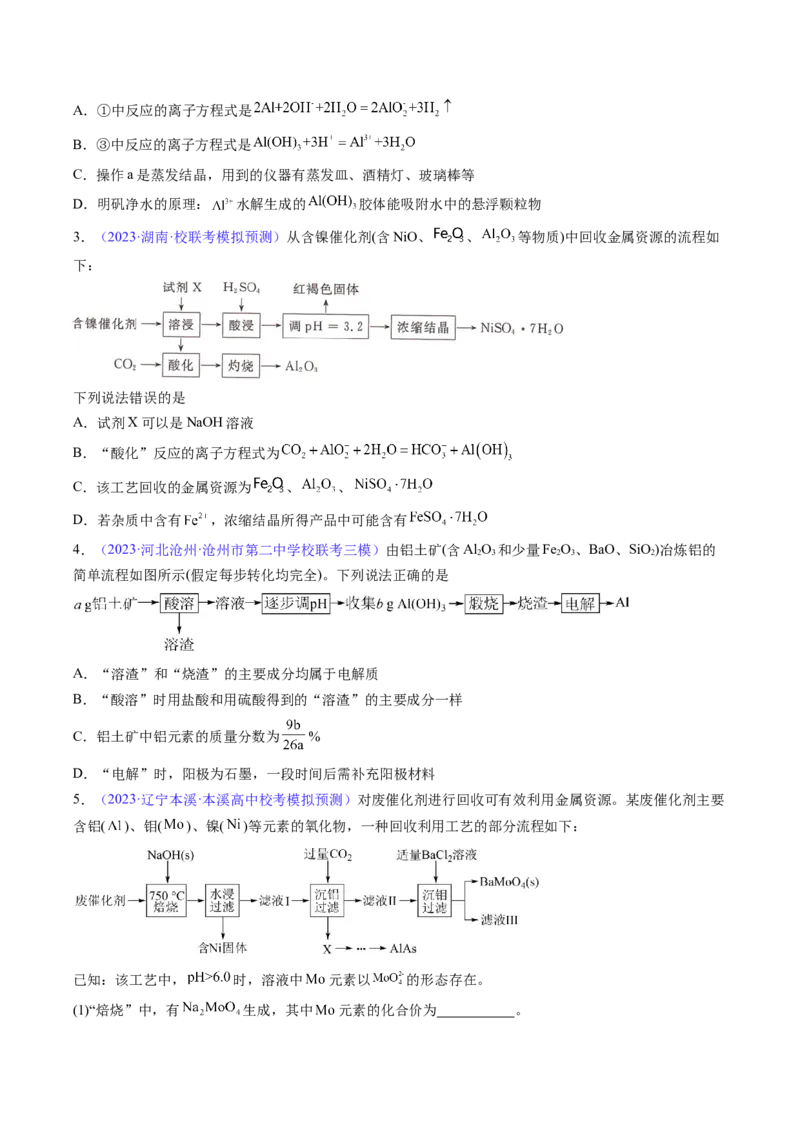
1.(2023·全国·模拟预测)一种以铝土矿(含氧化铝、氧化镓)为原料制备Ga的工艺流程如图。
下列说法不正确的是
A.酸性:
B.通入适量 时反应的离子方程式:
C.金属镓的晶胞结构为 ,则每个晶胞中含有的镓原子个数为2
D.流程中加入NaOH溶液的主要目的是从矿石中溶解出镓元素
2.(2023·北京东城·统考二模)明矾 可用作净水剂。某同学设计利用废铝箔(主要成
分为 ,含少量 等)制备明矾的流程如下图所示。
下列说法不正确的是A.①中反应的离子方程式是
B.③中反应的离子方程式是
C.操作a是蒸发结晶,用到的仪器有蒸发皿、酒精灯、玻璃棒等
D.明矾净水的原理: 水解生成的 胶体能吸附水中的悬浮颗粒物
3.(2023·湖南·校联考模拟预测)从含镍催化剂(含NiO、 、 等物质)中回收金属资源的流程如
下:
下列说法错误的是
A.试剂X可以是NaOH溶液
B.“酸化”反应的离子方程式为
C.该工艺回收的金属资源为 、 、
D.若杂质中含有 ,浓缩结晶所得产品中可能含有
4.(2023·河北沧州·沧州市第二中学校联考三模)由铝土矿(含Al O 和少量Fe O、BaO、SiO)冶炼铝的
2 3 2 3 2
简单流程如图所示(假定每步转化均完全)。下列说法正确的是
A.“溶渣”和“烧渣”的主要成分均属于电解质
B.“酸溶”时用盐酸和用硫酸得到的“溶渣”的主要成分一样
C.铝土矿中铝元素的质量分数为 %
D.“电解”时,阳极为石墨,一段时间后需补充阳极材料
5.(2023·辽宁本溪·本溪高中校考模拟预测)对废催化剂进行回收可有效利用金属资源。某废催化剂主要
含铝( )、钼( )、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为 。(2)“沉铝”中,生成的沉淀X的离子方程式 。
(3)“沉钼”中, 为7.0。生成 的离子方程式为 。
(4)①滤液Ⅲ中,主要存在的钠盐有 和Y,Y为 (填化学式)。
②往滤液Ⅲ中添加适量 固体后,通入足量 (填化学式)气体,再通入足量 ,可析出
Y。
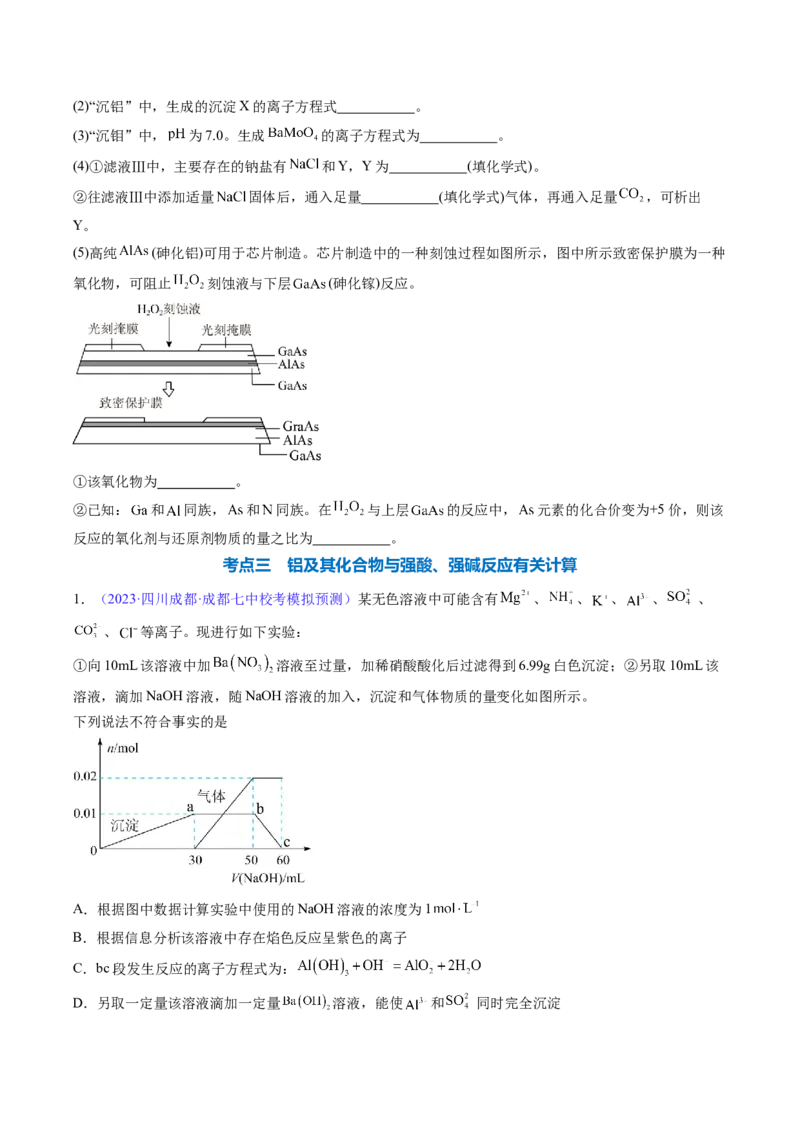
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种
氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。
①该氧化物为 。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价变为+5价,则该
反应的氧化剂与还原剂物质的量之比为 。
考点三 铝及其化合物与强酸、强碱反应有关计算
1.(2023·四川成都·成都七中校考模拟预测)某无色溶液中可能含有 、 、 、 、 、
、 等离子。现进行如下实验:
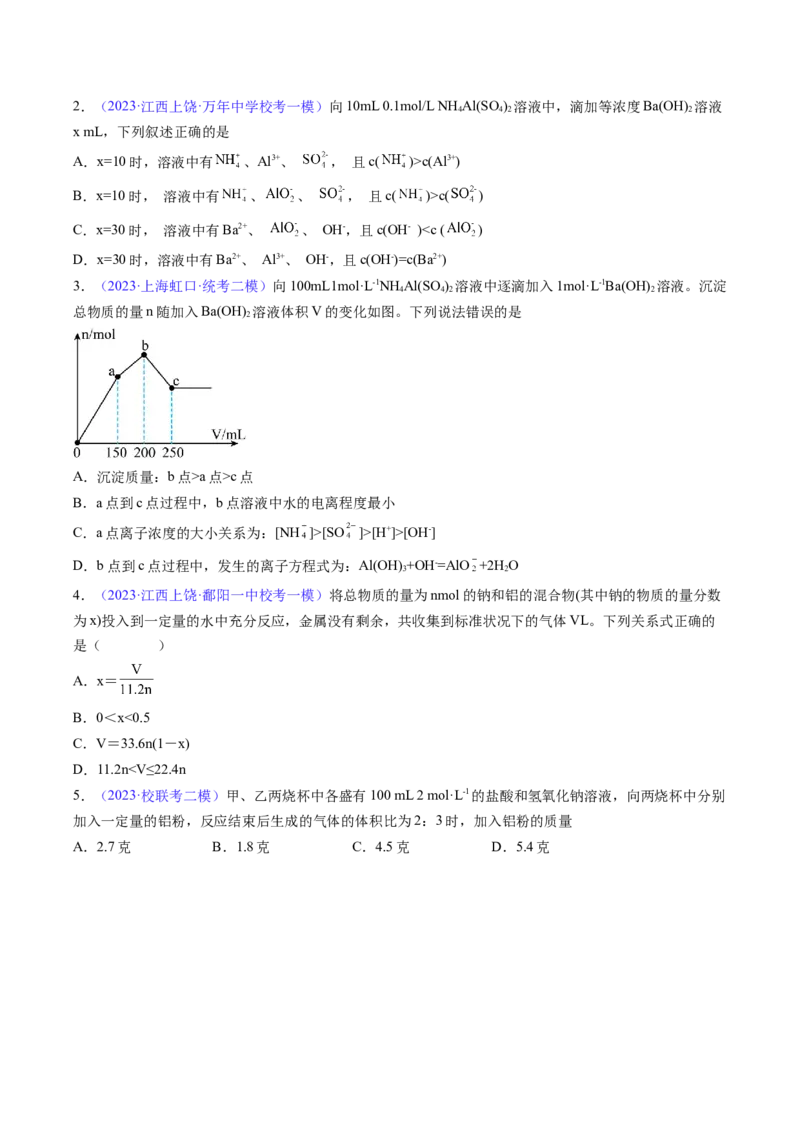
①向10mL该溶液中加 溶液至过量,加稀硝酸酸化后过滤得到6.99g白色沉淀;②另取10mL该
溶液,滴加NaOH溶液,随NaOH溶液的加入,沉淀和气体物质的量变化如图所示。
下列说法不符合事实的是
A.根据图中数据计算实验中使用的NaOH溶液的浓度为1
B.根据信息分析该溶液中存在焰色反应呈紫色的离子
C.bc段发生反应的离子方程式为:
D.另取一定量该溶液滴加一定量 溶液,能使 和 同时完全沉淀2.(2023·江西上饶·万年中学校考一模)向10mL 0.1mol/L NH Al(SO ) 溶液中,滴加等浓度Ba(OH) 溶液
4 4 2 2
x mL,下列叙述正确的是
A.x=10时,溶液中有 、Al3+、 , 且c( )>c(Al3+)
B.x=10时, 溶液中有 、 、 , 且c( )>c( )
C.x=30时, 溶液中有Ba2+、 、 OH-,且c(OH- )a点>c点
B.a点到c点过程中,b点溶液中水的电离程度最小
C.a点离子浓度的大小关系为:[NH ]>[SO ]>[H+]>[OH-]
D.b点到c点过程中,发生的离子方程式为:Al(OH) +OH-=AlO +2H O
3 2
4.(2023·江西上饶·鄱阳一中校考一模)将总物质的量为nmol的钠和铝的混合物(其中钠的物质的量分数
为x)投入到一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体VL。下列关系式正确的
是( )
A.x=
B.0<x<0.5
C.V=33.6n(1-x)
D.11.2n