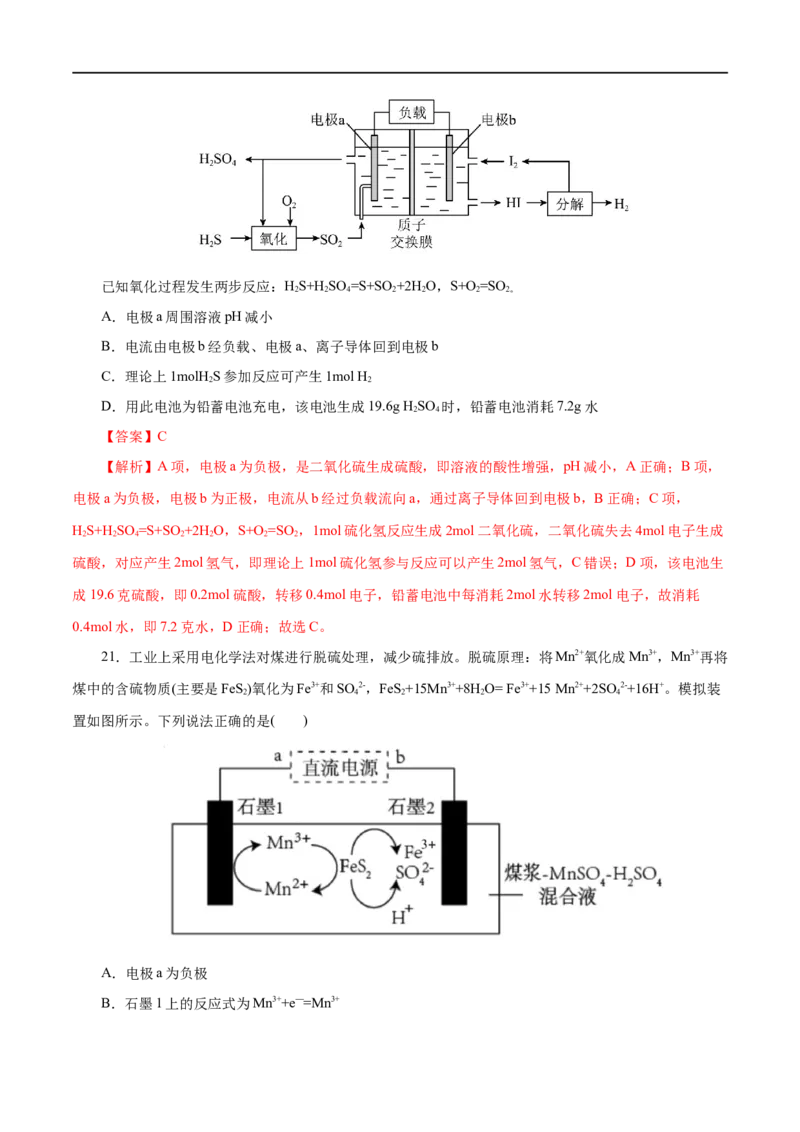
文档内容
专题 12 化学反应与电能
1.有关原电池的下列说法中正确的是( )
A.在外电路中电子由正极流向负极 B.在原电池中,只有金属锌作为负极
C.原电池工作时,阳离子向正极方向移动 D.原电池工作时,阳离子向负极方向移动
【答案】C
【解析】在原电池中,电子从负极流向正极;原电池中活泼的金属作负极,而不一定是 Zn;随着反应
的进行,阳离子在正极被还原,所以电解质溶液中的阳离子向正极移动,而阴离子向负极移动。答案为
C。
2.下列有关叙述正确的是( )
A.在空气中金属铝发生原电池反应表面迅速氧化形成保护层
B.原电池电解质溶液中阳离子向负极移动
C.最早使用的锌锰干电池的寿命和性能都不如改进后的碱性锌锰电池
D.“嫦娥五号”使用的太阳能电池阵和锂离子电池组,均可将化学能转变成电能
【答案】C
【解析】A项,Al和氧气直接反应生成致密的氧化铝薄膜,不涉及原电池反应,A错误;B项,原电
池工作时,电解质溶液中阳离子移向正极、阴离子移向负极,B错误;C项,最早使用的锌锰干电池电解
质溶液显酸性容易腐蚀锌皮,寿命和性能都不如改进后的碱性锌锰电池,C正确;D项,太阳能电池阵是
将光能转化为电能,描述错误,D错误;故选C。
3.下列有关电化学的说法正确的是( )
A.原电池的金属负极质量一定减小 B.待充电电池的负极应与电源正极相连
C.电解池的电解质溶液质量一定减小 D.原电池工作时在溶液中电流由负极到正极
【答案】D
【解析】A项,原电池放电时,负极质量可能增大、可能不变也可能减小,如铅蓄电池中负极电极反
应式为Pb-2e-+SO2-=PbSO↓,负极质量增加,燃料电池中负极材料质量不变,故A错误;B项,蓄电池充
4 4
电时,其负极应与电源的负极相连,正极与电源的正极相连,故B错误;C项,电解池的电解质溶液质量
可能不变,如精炼铜,电解质溶液CuSO 的质量不变,故C错误;D项,原电池工作时,外电路中电流是
4
从正极经过导线到负极,电池内部电流从负极经溶液到正极,故D正确;故选D。
4.下列说法正确的是( )
A.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
B.用HS作沉淀剂,可除去废水中的Fe2+和Cu2+
2
C.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属D.将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO 溶液,AgCl沉淀少于AgBr
3
【答案】A
【解析】A项,海轮外壳连接锌块时,锌和外壳构成了原电池,锌做负极,外壳受到了保护不被腐蚀,
采用了牺牲阳极的阴极保护法,A正确;B项,若用HS作沉淀剂除去废水中的Fe2+和Cu2+后溶液呈酸性,
2
应选择NaS做沉淀剂,B错误;C项,电解精炼铜时,阳极泥中含有比铜稳定的金属,如Ag、Au等金属,
2
没有Zn、Fe,C错误;D项,因为K (AgCl)>K (AgBr),所以将AgCl和AgBr的饱和溶液等体积混合后,
sp sp
c (Cl-) >c (Br-),再加入足量的浓AgNO 溶液,AgCl沉淀多于AgBr,D错误;故选 A。
3
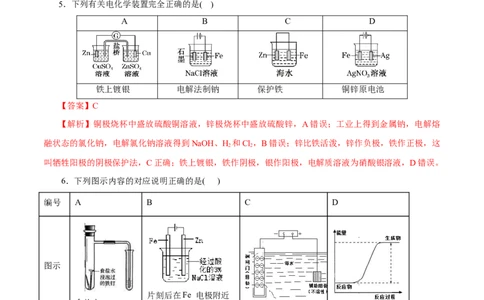
5.下列有关电化学装置完全正确的是( )
A B C D
铁上镀银 电解法制钠 保护铁 铜锌原电池
【答案】C
【解析】铜极烧杯中盛放硫酸铜溶液,锌极烧杯中盛放硫酸锌,A错误;工业上得到金属钠,电解熔
融状态的氯化钠,电解氯化钠溶液得到NaOH、H 和Cl ,B错误;锌比铁活泼,锌作负极,铁作正极,这
2 2
叫牺牲阳极的阴极保护法,C正确;铁上镀银,铁作阴极,银作阳极,电解质溶液为硝酸银溶液,D错误。
6.下列图示内容的对应说明正确的是( )
编号 A B C D
图示
片刻后在Fe 电极附近
食盐水
滴入K[Fe(CN) ]溶液
3 6
验证铁钉发生 该装置是牺牲阳极的 该化学反应为放热
说明 验证 Fe 电极被保护
吸氧腐蚀 阴极保护法 反应
【答案】A
【解析】A项,食盐水浸泡过的铁钉,会发生吸氧腐蚀,、装置内的O 得到电子,方程式为O+4e-
2 2
+2HO=4OH-,装置内O 减小,压强减小,右侧试管内导管中的液面上升,A正确;B项,Fe电极被保
2 2
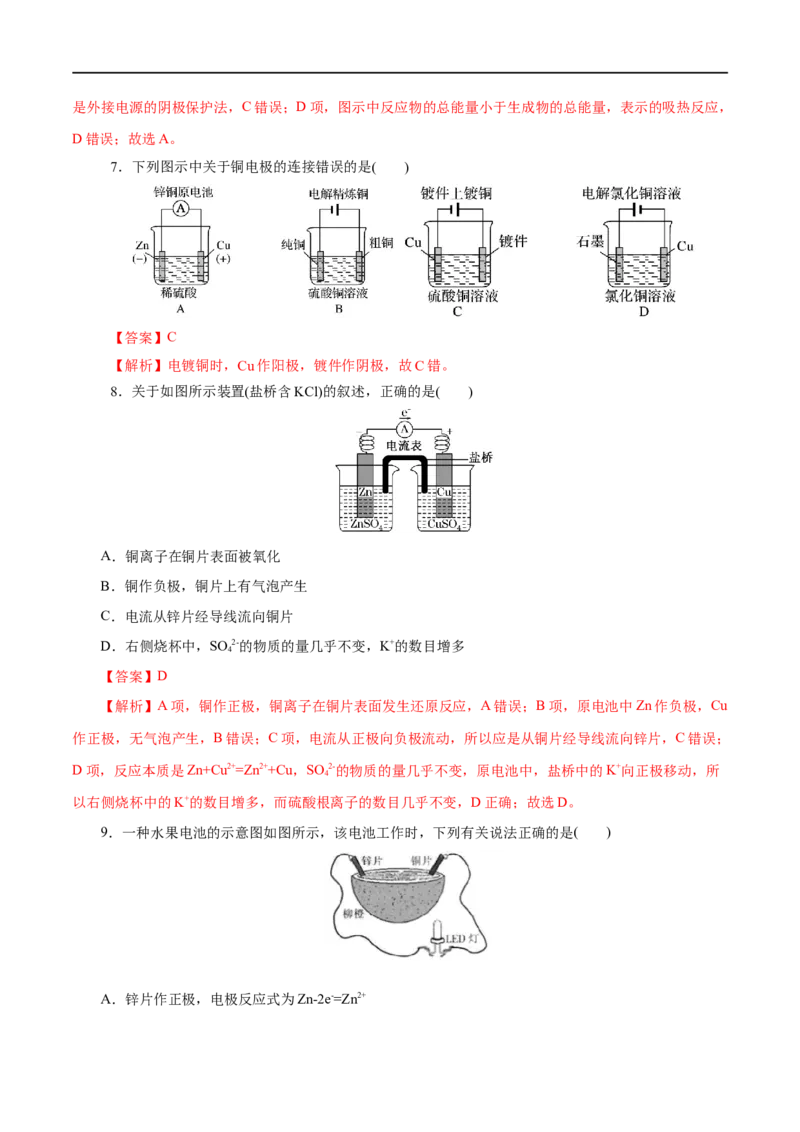
护,应该外界电源作阴极,Fe应该与电源的负极相连,B错误;C项,该保护措施利用的是电解池的原理,是外接电源的阴极保护法,C错误;D项,图示中反应物的总能量小于生成物的总能量,表示的吸热反应,
D错误;故选A。
7.下列图示中关于铜电极的连接错误的是( )
【答案】C
【解析】电镀铜时,Cu作阳极,镀件作阴极,故C错。
8.关于如图所示装置(盐桥含KCl)的叙述,正确的是( )
A.铜离子在铜片表面被氧化
B.铜作负极,铜片上有气泡产生
C.电流从锌片经导线流向铜片
D.右侧烧杯中,SO 2-的物质的量几乎不变,K+的数目增多
4
【答案】D
【解析】A项,铜作正极,铜离子在铜片表面发生还原反应,A错误;B项,原电池中Zn作负极,Cu
作正极,无气泡产生,B错误;C项,电流从正极向负极流动,所以应是从铜片经导线流向锌片,C错误;
D项,反应本质是Zn+Cu2+=Zn2++Cu,SO 2-的物质的量几乎不变,原电池中,盐桥中的K+向正极移动,所
4
以右侧烧杯中的K+的数目增多,而硫酸根离子的数目几乎不变,D正确;故选D。
9.一种水果电池的示意图如图所示,该电池工作时,下列有关说法正确的是( )
A.锌片作正极,电极反应式为Zn-2e-=Zn2+B.内外电路中电流均由电子定向移动形成
C.柳橙的成分不会发生变化
D.若将锌片换为铁片,LED灯仍然发光
【答案】D
【解析】A项,Zn比Cu活泼,Zn做负极,故A错误;B项,外电路由电子的定向移动形成,内电路
由电解质中离子定向移动形成,故B错误;C项,柳橙中的电解质氢离子得电子生成氢气,其成分会改变,
故C错误;D项,将锌片换为铁片,Fe与Cu有活泼性差异,能构成原电池,能产生电流,LED灯仍然发
光,故D正确;故选D。
10.关于下列装置,叙述不正确的是( )
A.石墨电极反应式: O+4H++4e-=2H O
2 2
B.温度计的示数会上升
C.加入少量NaCl ,会加快 Fe 生锈
D.加入 HCl,石墨电极反应式: 2H++2e-=H ↑
2
【答案】A
【解析】A项,电解质溶液不是酸性的,所以石墨电极反应式为O+4e-+2H O=4OH-,故A错误;B项,
2 2
原电池放电时会放出热量,所以温度计的示数会上升,故 B正确;C项,加入少量NaCl,溶液中自由移动
离子浓度增大,溶液导电能力增强,会加快 Fe 生锈,故C正确;D项,加入 HCl,溶液呈酸性,在正极
石墨上是H+得到电子,电极反应式为 2H++2e-=H ↑,故D正确;故选A。
2
11.如图所示实验装置,下列说法不正确的是( )
A.装置为铁的吸氧腐蚀实验
B.一段时间后,向插入铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的溶液有沉淀产生
C.向插入石墨棒的玻璃筒内滴入石蕊溶液,可观察到石墨附近的溶液变红
D.若将装置中饱和食盐水换成稀硫酸,装置为析氢腐蚀【答案】C
【解析】食盐水显中性,装置为铁的吸氧腐蚀实验,A正确;一段时间后,有亚铁离子产生,向插入
铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的溶液有沉淀产生,B正确;石墨棒是正极,氧气
得到电子转化为氢氧根,滴入石蕊溶液,可观察到石墨附近的溶液变蓝,C错误;若将装置中饱和食盐水
换成稀硫酸,装置为析氢腐蚀,D正确,答案选C。
12.中科院研制出一种陶瓷基混合导体透氧膜,它允许电子和O2-同时透过,可实现水连续分解制
H,工作时,CO、HO分别在透氧膜的两侧反应,工作原理如图所示。下列说法错误的是( )
2 2
A.CO在b侧反应
C.当产生H 33.6 L时,CO消耗1.5 mol
2
D.a侧的电极反应式为:HO + 2e- = H ↑+ O2-
2 2
B.该装置实现了太阳能转化为化学能
【答案】B
【解析】A项,由图知,CO在b侧失去电子被氧化,电子从b侧透过膜进入a侧,水得电子转变为氢
气,A正确;B项,未指明处于标准状况,当产生H 33.6 L时,不能计算出消耗CO的物质的量,B不正
2
确;C项,a侧,水得电子转变为氢气,电极反应式为:HO + 2e- = H ↑+ O2-,C正确;D项,光照下,水
2 2
得电子生成H 和 O2-,O2-经过透氧膜进入b侧,CO在b侧失去电子被氧化、在O2-参与下生成二氧化碳,
2
则该装置实现了太阳能转化为化学能,D正确;故选B。
13.下列指定反应的离子方程式正确的是( )
A.铅蓄电池放电时负极反应:PbO +2e—+4H++SO2-=PbSO+2H O
2 4 4 2
B.电解饱和MgCl 溶液:2Cl-+2H O电 H↑+Cl↑+2OH-
2 2 解 2 2
C.用惰性电极电解CuCl 溶液:Cu2++2Cl-+2H O电 Cu(OH) ↓+Cl↑+H ↑
2 2 解 2 2 2
D.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
【答案】D
【解析】A项,铅蓄电池放电时,铅为电池的负极,铅失去电子发生氧化反应生成硫酸铅,电极反应
式为Pb—2e—+ SO 2-=PbSO,A错误;B项,电解饱和MgCl 溶液会生成氢氧化镁沉淀,离子方程式应为:
4 4 2
Mg 2++2Cl-+2H O电 H↑+Cl↑+ Mg(OH) ↓,B错误;C项,用惰性电极电解CuCl 溶液,Cu2+氧化性比H+强,
2 解 2 2 2 2
故Cu2+先放电,正确的离子方程式为CuCl电 Cu+Cl↑,C错误;D项,银作阳极,阳极的电极反应式为Ag-
2 解 2
e-=Ag+,铜片作阴极,阴极的电极反应式为Ag++e-=Ag,总反应为Ag(阳极) Ag(阴极),D正确;故选D。
14.我国千吨级“液态太阳燃料合成示范项目”在兰州通过了鉴定,该工艺具有完全自主知识产权,
整体技术处于国际领先,其技术路线如图所示。下列有关说法错误的是( )
A.太阳能最终转化为电能和热能
B.燃料电池正极反应式为H -2e- =2H+
2
C.HO和CO 可循环利用
2 2
D.该技术的关键是氢气如何安全、高效储存及转移
【答案】B
【解析】A项,从图中可以看出,通过光伏发电,太阳能转化为电能,水在电能作用下分解为氧气和
氢气,最后氢气和氧气生成水,所以太阳锌专化为电能、热能和化学能,A不符合题意;B项,发生还原
反应的是正极,所以燃料电池正极反应式为O+4H++4e- =2H O,B符合题意;C项,水分解为氢气和氧气,
2 2
最后氢气和氧气又生成水,故水可以循环使用,氢气和二氧化碳反应生成水和甲醇,水和甲醇又生成二氧
化碳,所以二氧化碳也可以循环利用,C不符合题意;D项,氢气易燃易爆,使用氢气时如何安全、高效
储存及转移是关键,D不符合题意;故选B。
15.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
B.14.0gFe发生吸氧腐蚀生成Fe O·xH O,电极反应转移的电子数为0.5N
2 3 2 A
C.用电解粗铜的方法精炼铜,当电路中通过的电子数为N 时,阳极应有32 g Cu转化为Cu2+
A
D.利用2ClO +2Cl- 2ClO -+Cl 生成1 mol Cl 时转移电子数为8N
2 2 2 2 A
【答案】B
【解析】A项,电解饱和食盐水时电极总反应为:2NaCl+2H O 2NaOH+H ↑+Cl↑,若阴阳两极产
2 2 2
生气体分别是氢气与氯气,且物质的量之比为1:1,若气体的总质量为73g,则说明反应生成的氢气与氯气
的物质的量各自为1mol,根据关系式H 2e-可知,转移的电子数为2N ,A错误;B项,14.0gFe的物质
2 A的量为 ,Fe发生吸氧腐蚀的负极反应式为Fe-2e- = Fe2+,则电极反应转移的电子数为
0.25mol×2N =0.5N ,B正确;C项,电解精炼铜时,阳极为粗铜,阳极发生的电极反应有:比铜活泼的杂
A A
质金属失电子发生氧化反应以及Cu失电子的氧化反应:Cu-2e-=Cu2+,当电路中通过的电子数为N 时,即
A
电路中通过1mol电子,Cu失去的电子应小于1mol,阳极反应的Cu的物质的量小于0.5mol,则阳极反应
的Cu的质量小于0.5mol×64g/mol=32g,C错误;D项,根据氧化还原反应的规律,ClO →ClO -,2Cl-
2 2
→Cl,氯气只作氧化产物,ClO -只作还原产物,生成1molCl 时转移电子物质的量为1mol×2×[0-(-
2 2 2
1)]=2mol,D错误;故选B。
16.深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图
示,下列与此原理有关说法错误的是( )
A.正极反应为:SO 2-+5H O+8e-=HS-+9OH-
4 2
B.输送暖气的管道不易发生此类腐蚀
C.这种情况下,Fe腐蚀的最终产物为Fe O·xH O
2 3 2
D.管道上刷富锌油漆可以延缓管道的腐蚀
【答案】C
【解析】A项,原电池的正极发生还原反应,由图示可知发生的电极反应为SO 2-+5H O+8e-=HS-
4 2
+9OH-,故A正确;B项,硫酸盐还原菌是蛋白质,在高温下易变性,失去催化效率,则输送暖气的管道
不易发生此类腐蚀,故B正确;C项,由图示可知,Fe腐蚀的最终产物为FeO,故C错误;D项,管道上
刷富锌油漆,形成Zn—Fe原电池,Fe变为正极,可以延缓管道的腐蚀,故D正确;故选C。
17.电渗析法是海水淡化的方法之一,具有选择性离子交换膜交错排列构成的多层式电渗析槽,其工
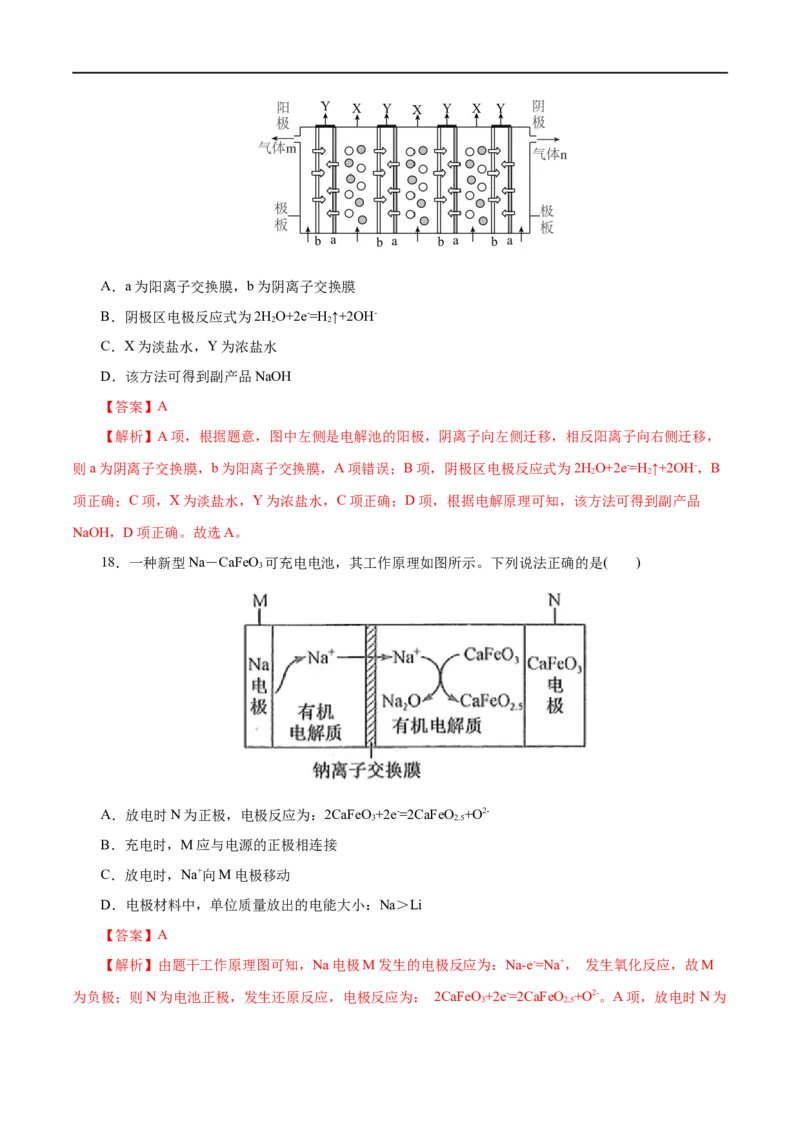
作原理如图所示(a、b为不同离子交换膜)。下列有关说法错误的是( )A.a为阳离子交换膜,b为阴离子交换膜
B.阴极区电极反应式为2HO+2e-=H ↑+2OH-
2 2
C.X为淡盐水,Y为浓盐水
D.该方法可得到副产品NaOH
【答案】A
【解析】A项,根据题意,图中左侧是电解池的阳极,阴离子向左侧迁移,相反阳离子向右侧迁移,
则a为阴离子交换膜,b为阳离子交换膜,A项错误;B项,阴极区电极反应式为2HO+2e-=H ↑+2OH-,B
2 2
项正确;C项,X为淡盐水,Y为浓盐水,C项正确;D项,根据电解原理可知,该方法可得到副产品
NaOH,D项正确。故选A。
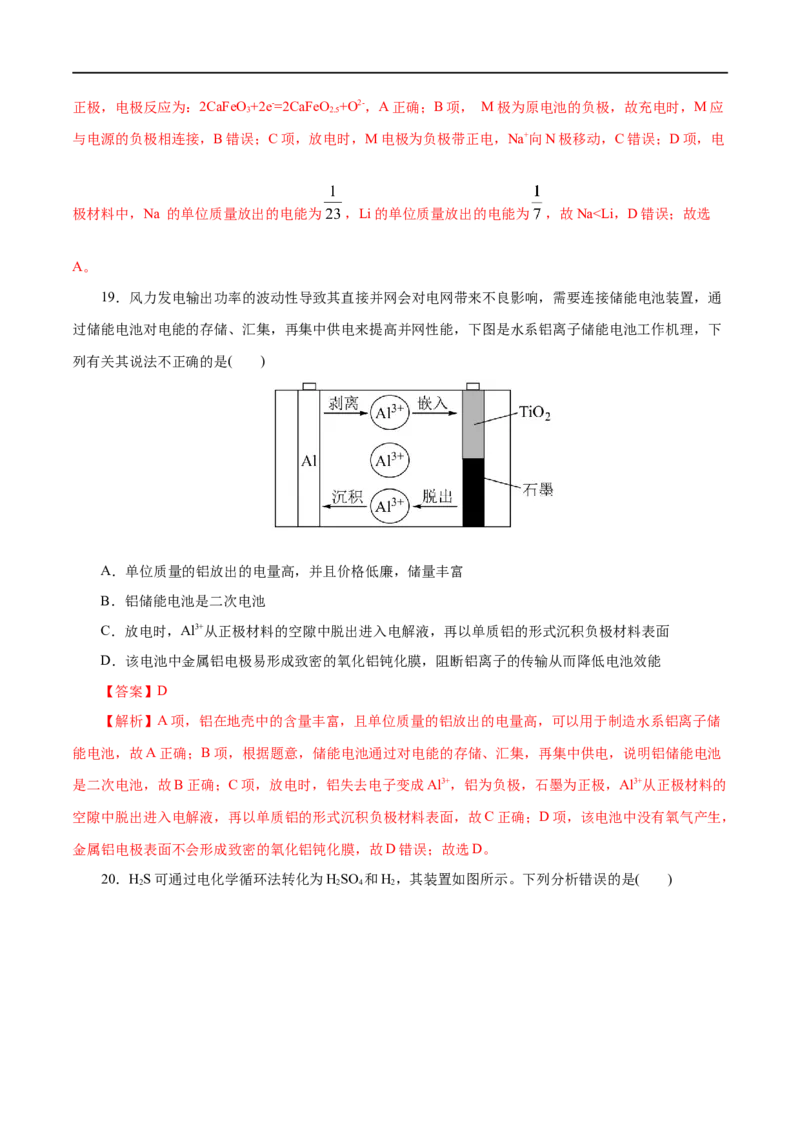
18.一种新型Na-CaFeO 可充电电池,其工作原理如图所示。下列说法正确的是( )
3
A.放电时N为正极,电极反应为:2CaFeO+2e-=2CaFeO +O2-
3 2.5
B.充电时,M应与电源的正极相连接
C.放电时,Na+向M电极移动
D.电极材料中,单位质量放出的电能大小:Na>Li
【答案】A
【解析】由题干工作原理图可知,Na电极M发生的电极反应为:Na-e-=Na+, 发生氧化反应,故M
为负极;则N为电池正极,发生还原反应,电极反应为: 2CaFeO+2e-=2CaFeO +O2-。A项,放电时N为
3 2.5正极,电极反应为:2CaFeO+2e-=2CaFeO +O2-,A正确;B项, M极为原电池的负极,故充电时,M应
3 2.5
与电源的负极相连接,B错误;C项,放电时,M电极为负极带正电,Na+向N极移动,C错误;D项,电
极材料中,Na 的单位质量放出的电能为 ,Li的单位质量放出的电能为 ,故Na