文档内容
题 12 化学实验方案的设计(表格图象型)
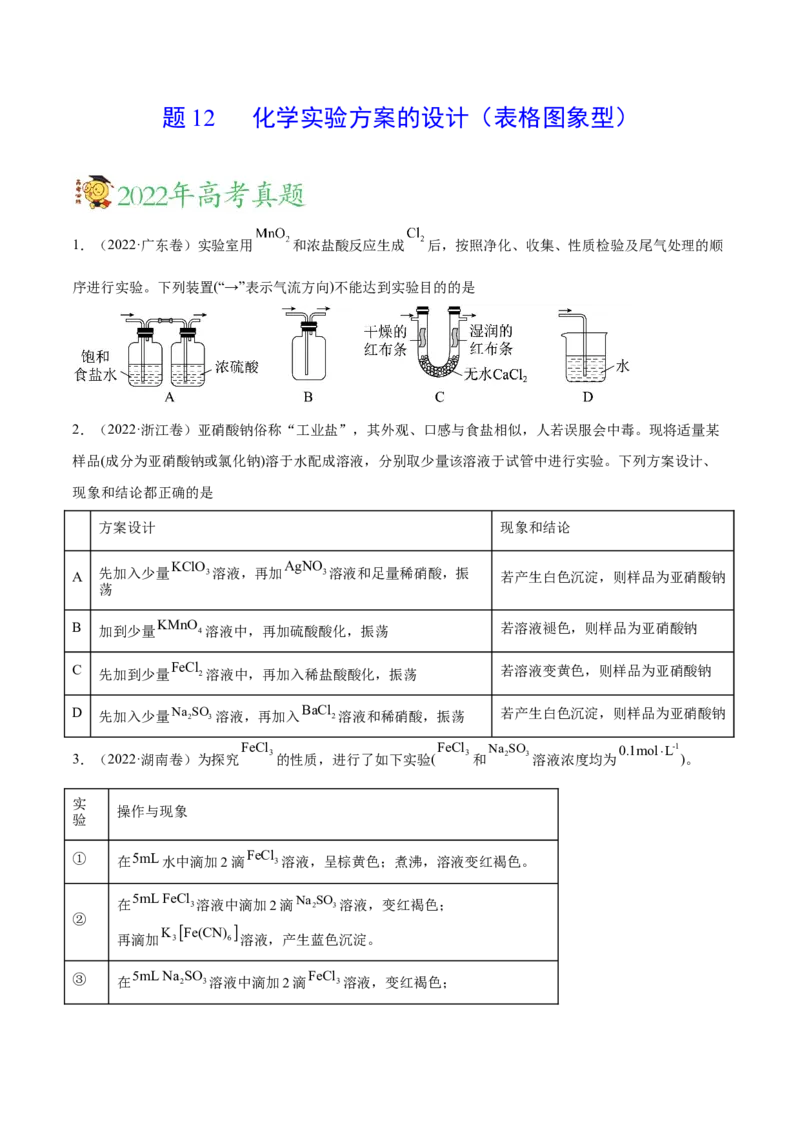
1.(2022·广东卷)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气处理的顺
序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
2.(2022·浙江卷)亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某
样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、
现象和结论都正确的是
方案设计 现象和结论
KClO AgNO
A
先加入少量 3溶液,再加 3溶液和足量稀硝酸,振
若产生白色沉淀,则样品为亚硝酸钠
荡
B 加到少量 KMnO 4溶液中,再加硫酸酸化,振荡 若溶液褪色,则样品为亚硝酸钠
C 先加到少量 FeCl 2溶液中,再加入稀盐酸酸化,振荡 若溶液变黄色,则样品为亚硝酸钠
D 先加入少量Na 2 SO 3溶液,再加入 BaCl 2溶液和稀硝酸,振荡 若产生白色沉淀,则样品为亚硝酸钠
FeCl FeCl Na SO 0.1molL-1
3.(2022·湖南卷)为探究 3的性质,进行了如下实验( 3和 2 3溶液浓度均为 )。
实
操作与现象
验
① 在5mL水中滴加2滴 FeCl 3溶液,呈棕黄色;煮沸,溶液变红褐色。
在 5mL FeCl 3溶液中滴加2滴Na 2 SO 3溶液,变红褐色;
②
K Fe(CN)
再滴加 3 6 溶液,产生蓝色沉淀。
③ 在 5mL Na 2 SO 3溶液中滴加2滴 FeCl 3溶液,变红褐色;K Fe(CN)
将上述混合液分成两份,一份滴加 3 6 溶液,无蓝色沉淀生;
另一份煮沸,产生红褐色沉淀。
Fe3+
依据上述实验现象,结论不合理的是A.实验①说明加热促进 水解反应
Fe3+
B.实验②说明 既发生了水解反应,又发生了还原反应
Fe3+
C.实验③说明 发生了水解反应,但没有发生还原反应
SO2- Fe3+
D.整个实验说明 3 对 的水解反应无影响,但对还原反应有影响
1.(2021·浙江)下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
取 乙醇,加入 浓硫酸、少量
探究乙醇消去反应的 若溴水褪色,则乙醇消去反应的
A 沸石,迅速升温至140℃,将产生的气体
产物 产物为乙烯
通入 溴水中
取少量样品,加入 蒸馏水和少量乙
探究乙酰水杨酸样品 若有紫色沉淀生成,则该产品中
B
中是否含有水杨酸 醇,振荡,再加入1-2滴 溶液 含有水杨酸
若无气体生成,则固体粉末为
探究金属钠在氧气中
;若有气体生成,则固体
C 燃烧所得固体粉末的 取少量固体粉末,加入 蒸馏水
成分
粉末为
取少量待测样品溶于蒸馏水,加入足量稀
探究 固体样品 若有白色沉淀产生,则样品已经
D
是否变质 盐酸,再加入足量 溶液 变质
2.(2021·湖南)下列实验设计不能达到实验目的的是
实验目的 实验设计
A 检验溶液中 是否被氧化 取少量待测液,滴加 溶液,观察溶液颜色变化
B 净化实验室制备的 气体依次通过盛有饱和 溶液、浓 的洗气瓶
C 测定 溶液的pH 将待测液滴在湿润的pH试纸上,与标准比色卡对照
D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
3.(2021·广东)化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是选项 操作或做法 目的
A 将铜丝插入浓硝酸中 制备
B 将密闭烧瓶中的 降温 探究温度对平衡移动的影响
C 将溴水滴入 溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余 固体放回原试剂瓶 节约试剂
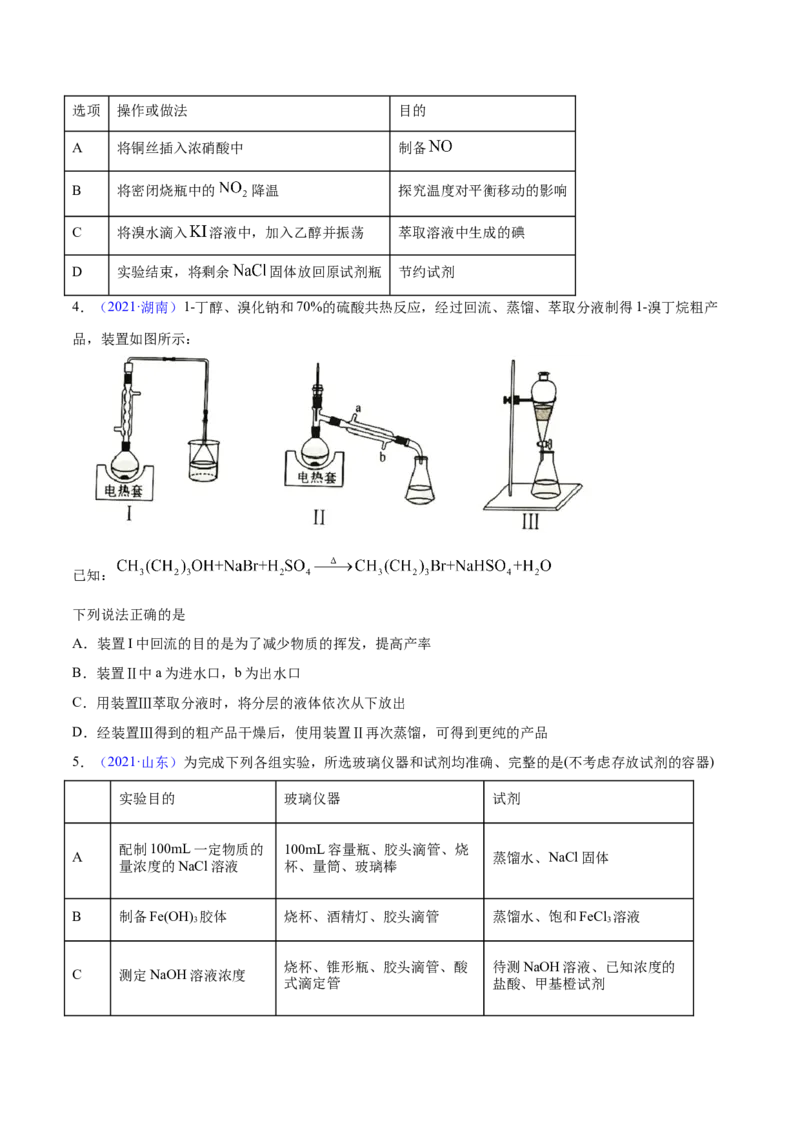
4.(2021·湖南)1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液制得1-溴丁烷粗产
品,装置如图所示:
已知:
下列说法正确的是
A.装置I中回流的目的是为了减少物质的挥发,提高产率
B.装置Ⅱ中a为进水口,b为出水口
C.用装置Ⅲ萃取分液时,将分层的液体依次从下放出
D.经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
5.(2021·山东)为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器)
实验目的 玻璃仪器 试剂
配制100mL一定物质的 100mL容量瓶、胶头滴管、烧
A 蒸馏水、NaCl固体
量浓度的NaCl溶液 杯、量筒、玻璃棒
B 制备Fe(OH) 胶体 烧杯、酒精灯、胶头滴管 蒸馏水、饱和FeCl 溶液
3 3
烧杯、锥形瓶、胶头滴管、酸 待测NaOH溶液、已知浓度的
C 测定NaOH溶液浓度
式滴定管 盐酸、甲基橙试剂冰醋酸、无水乙醇、饱和
D 制备乙酸乙酯 试管、量筒、导管、酒精灯
NaCO 溶液
2 3
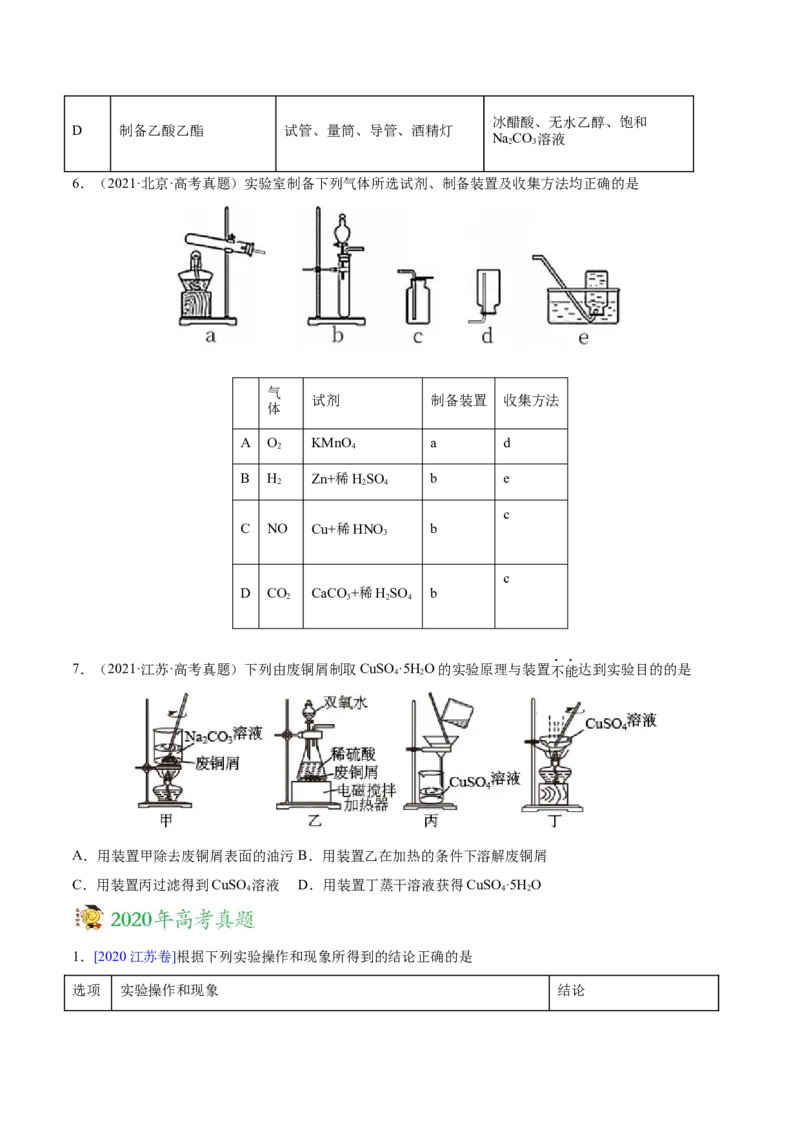
6.(2021·北京·高考真题)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气
试剂 制备装置 收集方法
体
A O KMnO a d
2 4
B H Zn+稀HSO b e
2 2 4
c
C NO Cu+稀HNO b
3
c
D CO CaCO +稀HSO b
2 3 2 4
7.(2021·江苏·高考真题)下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2
A.用装置甲除去废铜屑表面的油污B.用装置乙在加热的条件下溶解废铜屑
C.用装置丙过滤得到CuSO 溶液 D.用装置丁蒸干溶液获得CuSO ·5H O
4 4 2
1.[2020江苏卷]根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论向淀粉溶液中加适量20%H SO 溶液,加热,冷却后加NaOH溶液至
A 2 4 淀粉未水解
中性,再滴加少量碘水,溶液变蓝
室温下,向 HCl溶液中加入少量镁粉,产生大量气泡,
B 镁与盐酸反应放热
测得溶液温度上升
室温下,向浓度均为 的BaCl 和CaCl 混合溶液中加入
C 2 2 白色沉淀是BaCO
3
NaCO 溶液,出现白色沉淀
2 3
D 向 HO 溶液中滴加 KMnO 溶液,溶液褪色 HO 具有氧化性
2 2 4 2 2
2.[2020天津卷]检验下列物所选用的试剂正确的是
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的 NaOH溶液,湿润的蓝色石蕊试纸
3.[2020年山东新高考]利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A.用甲装置制备并收集CO
2
B.用乙装置制备溴苯并验证有HBr产生
C.用丙装置制备无水MgCl
2
D.用丁装置在铁上镀铜
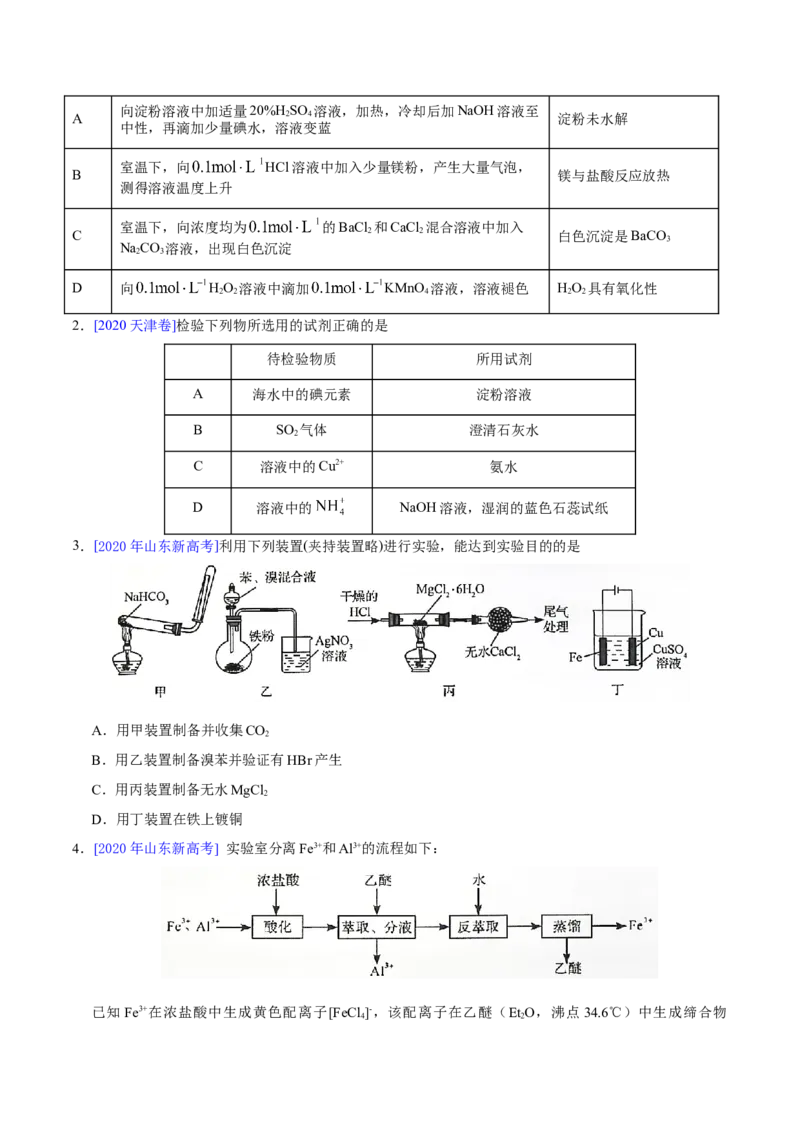
4.[2020年山东新高考] 实验室分离Fe3+和Al3+的流程如下:
已知Fe3+在浓盐酸中生成黄色配离子[FeCl]-,该配离子在乙醚(EtO,沸点34.6℃)中生成缔合物
4 2。下列说法错误的是
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
5.[2020年山东新高考] 下列操作不能达到实验目的的是
目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
B 证明酸性:碳酸>苯酚 将盐酸与NaHCO 混合产生的气体直接通入苯酚钠溶液
3
C 除去碱式滴定管胶管内的气泡 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出
向试管中加入 2mL10%NaOH溶液,再滴加数滴 2%CuSO 溶
D 配制用于检验醛基的氢氧化铜悬浊液 4
液,振荡