文档内容
专题 12 大题突破——物质结构与性质综合
目录
01 模拟基础练
【题型一】电子排布、电负性、电离能及等电子体
【题型二】立体构型、杂化类型、晶体类型的判断及原因解释
【题型三】晶胞的计算
02 重难创新练
03 真题实战练
题型一 电子排布、电负性、电离能及等电子体
1.(2025·海南省一模,节选)Cu O广泛应用于太阳能电池领域,制备过程如图所示:
2
。回答下列问题:
(1)基态Cu2+的核外电子排布式为 。
(3)N H ·H O中N原子的杂化方式为 ;基态N原子中未成对电子数为 个。
2 4 2
2.(2025·天津市滨海新区高三第二次高三联考,节选)回答下列问题
(1) Fe位于元素周期表中的 区;基态Mn原子的价电子轨道表示式为 ;基态
Cu2+核外电子的空间运动状态有 种。
(2)氟硼铍酸钾(KBeBO F)是制备激光器的核心材料。
3 2
①基态氟原子占据最高能级的核外电子的电子云形状为 形。
②氟硼铍酸钾中非金属元素的电负性由大到小的顺序是 。
③Be和B的第一电离能:I(Be)>I(B),其原因是 。
1 1
④氟硼酸钾(KBF )是制备氟硼铍酸钾的原料之一,氟硼酸钾在高温下分解为KF和BF,二者的沸点分
4 3
别为1500℃、-101℃。KF的沸点远高于BF 的原因是 。
3
3.(2025·山东省聊城市高三教学质量检测,节选)我国在新材料领域研究的重大突破,为“天宫”空
间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、 等元素。回答下列
问题:(1)下列不同状态的碳原子中,失去一个电子需要吸收能量最多的是_______(填标号)。
A. B.
C. D.
(2)基态镓原子核外价电子排布式为 ;同周期主族元素基态原子与其具有相同数目未成对电子
的有 (写元素符号)。
(5) 的第二电离能[I(Cr)]和Mn的第二电离能[I(Mn)]分别为1590.6 kJ·mol−1、1509.0 kJ·mol−1,
2 2
[I(Cr)]>[I(Mn)]的原因是 。
2 2
题型二 立体构型、杂化类型、晶体类型的判断及原因解释
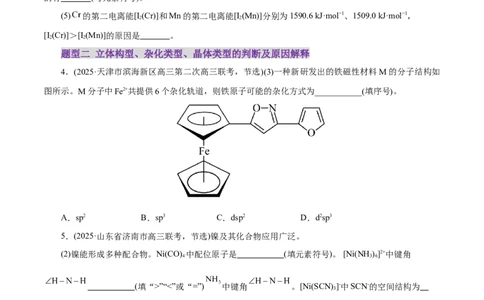
4.(2025·天津市滨海新区高三第二次高三联考,节选)(3)一种新研发出的铁磁性材料M的分子结构如
图所示。M分子中Fe2+共提供6个杂化轨道,则铁原子可能的杂化方式为___________(填序号)。
A.sp2 B.sp3 C.dsp2 D.d2sp3
5.(2025·山东省济南市高三联考,节选)镍及其化合物应用广泛。
(2)镍能形成多种配合物。Ni(CO) 中配位原子是 (填元素符号)。[Ni(NH )]2+中键角
4 3 6
(填“>”“<”或“=”) 中键角 。[Ni(SCN) ]-中SCN-的空间结构为
3
,SCN-中的大π键可表示为 (用 表示,n为原子数,m为电子数)。
6.(2025·江西省九校联考高三期中,节选)硼及其化合物在材料制造、有机合成等方面用途非常广泛,
其在化合物中常显+3价。
(2)氨硼烷(NH BH)是目前最具潜力的储氢材料之一。
3 3
①研究表明氨硼烷中的N-B键为配位键,其中 原子提供孤电子对。H-N-H的键角 (填
“>”、“<”或“=”)H——B—H的键角,理由是 。②氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作
用,称为双氢键,用“N-H…H-B”表示。以下物质之间可能形成双氢键的是 (填序号)。
a. NH 和 AlH b. C H 和C H c. B H 和HCN d. HO 和 HO
2 4 3 3 6 3 8 2 6 2 2 2
7.(2025·北京市海淀区高三模拟,节选)(3)SnCl 和SnCl 是锡的常见氯化物,SnCl 可被氧化得到
2 4 2
SnCl 。
4
①SnCl 分子的VSEPR模型名称是 。
2
②SnCl 的Sn—Cl键是由锡的 轨道与氯的3p轨道重叠形成σ键。
4
③SnCl 分子中,Cl—Sn—Cl键角小于120°的原因是 。
2
(4)C、Si是与Sn同主族的两种元素。
①二者电负性C Si,从原子结构角度解释原因 。
②金刚石的熔点高于晶体硅,说明原因 。
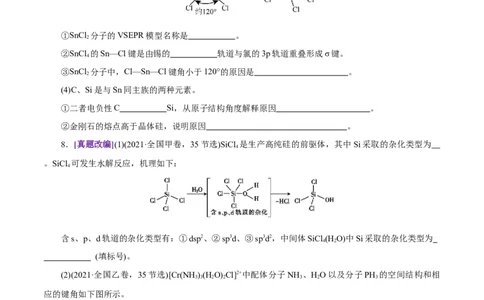
8.[真题改编](1)(2021·全国甲卷,35节选)SiCl 是生产高纯硅的前驱体,其中Si采取的杂化类型为
4
。SiCl 可发生水解反应,机理如下:
4
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl (H O)中Si采取的杂化类型为
4 2
(填标号)。
(2)(2021·全国乙卷,35节选)[Cr(NH )(H O) Cl]2+中配体分子NH 、HO以及分子PH 的空间结构和相
3 3 2 2 3 2 3
应的键角如下图所示。
PH 中P的杂化类型是 。HO的键角小于NH 的,分析原因 。
3 2 3
9.(2025·安徽省江准十校高三第二次联考)胆矾(CuSO ·5H O)是一种络合物,其组成也可写为
4 2
[Cu(H O) ]SO ·H O。往硫酸铜溶液中逐滴加入氨水,溶液由蓝色转变为深蓝色。这是因为四水合铜(Ⅱ)离
2 4 4 2子经过反应,最后生成铜氨络离子[Cu(NH )]2+而使溶液呈深蓝色。
3 4
(1)铜元素位于元素周期表的 区,Cu2+的价电子排布式为 。
(2)胆矾晶体中含有的化学键有: 。
(3)[Cu(NH )]SO 中非金属元素电负性由大到小的顺序是 (用元素符号表示)。
3 4 4
(4)H O的中心原子轨道杂化类型为 杂化;SO 2-的VSEPR构型是 。
2 4
(5) [Cu(H O) ]2+和[Cu(NH )]2+中的配位键哪一个更强?并解释原因: 。
2 4 3 4
题型三 晶胞的计算
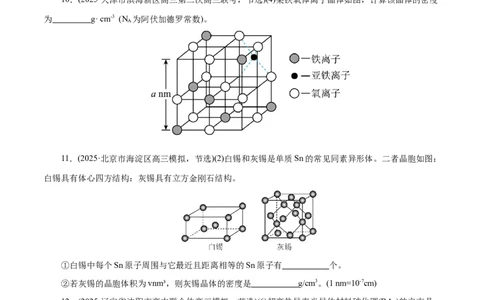
10.(2025·天津市滨海新区高三第二次高三联考,节选)(4)某铁氧体离子晶体如图,计算该晶体的密度
为 g· cm-3 (N 为阿伏加德罗常数)。
A
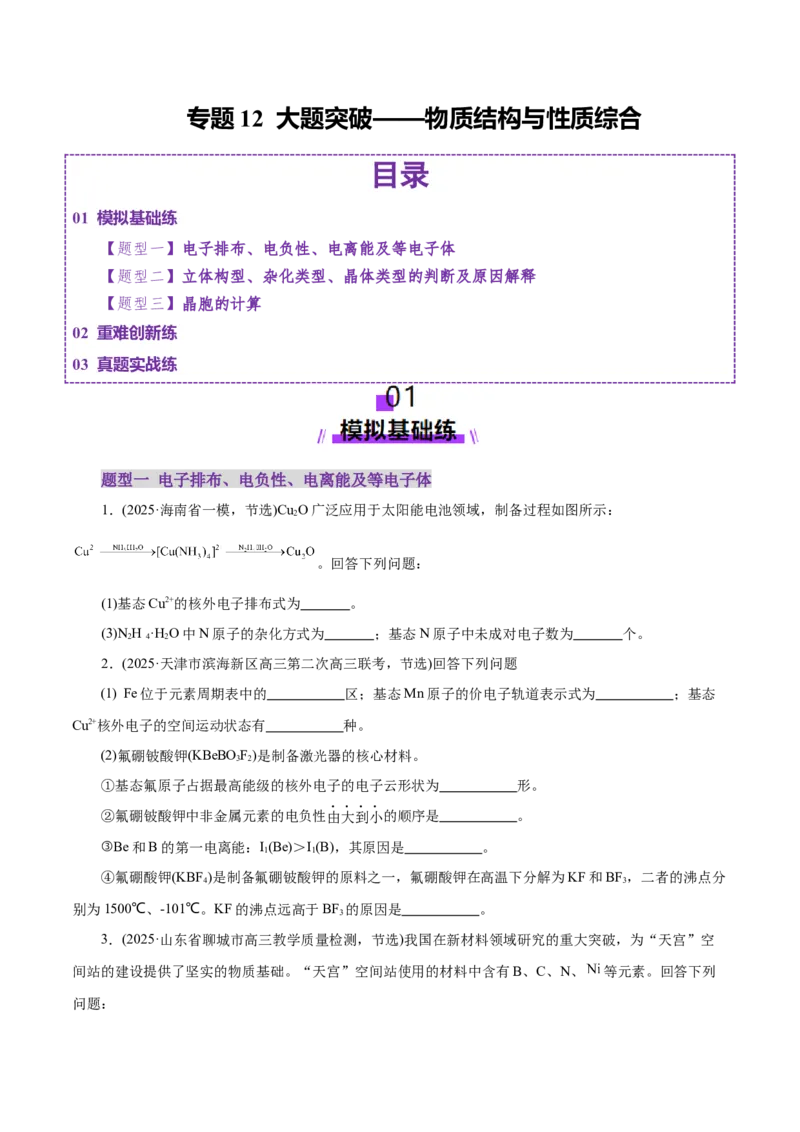
11.(2025·北京市海淀区高三模拟,节选)(2)白锡和灰锡是单质Sn的常见同素异形体。二者晶胞如图:
白锡具有体心四方结构:灰锡具有立方金刚石结构。
①白锡中每个Sn原子周围与它最近且距离相等的Sn原子有 个。
②若灰锡的晶胞体积为vnm³,则灰锡晶体的密度是 g/cm3。(1 nm=10-7cm)
12.(2025·辽宁省沈阳市高中联合体高三模拟,节选)(6)超高热导率半导体材料砷化硼(BAs)的立方晶
胞结构如下图所示,则1号砷原子的原子坐标为 。若晶胞中As原子到B原子最近距离为apm,则
该晶体的密度ρ= g· cm-3 (列出计算式,阿伏加德罗常数的值为N )。
A13.(2025·江西省九校联考高三期中,节选)硼及其化合物在材料制造、有机合成等方面用途非常广泛,
其在化合物中常显+3价。
(3)在铁系储氢合金中引入硼可降低储氢量,提升储氢合金活化性能,某种储氢材料的晶胞如图,八面
体中心为金属铁的离子,顶点均为 NH 配体;四面体中心为硼原子,顶点均为氢原子。
3
①该晶体的化学式为 。
②该晶体中阴离子的配位数为 。
③已知该晶体的晶胞参数为a nm,N 代表阿伏加德罗常数的值,则该晶体的密度ρ= g· cm-3
A
用含a、N 的代数式表示)。
A
1.(2025·湖南省炎德英才名校联考联合体高三第四次联考)最近,科学家构筑新型整体式催化剂
(Co O/Fe-S)高效降解甲苯( ),以减轻甲苯带来的污染。根据上述涉及的元素,回答下列问
3 4
题:
(1)基态Fe原子价层电子排布式为 。甲苯中碳原子杂化类型有 。
(2)H O 和HS的相对分子质量相同,但是在常温常压下,HO 呈液态,HS呈气态,其状态不同的主
2 2 2 2 2 2
要原因可能是 。
(3)SO 2-的空间结构是 。SO 的VSEPR模型是 。
3 3
(4)O 在超高压下转化为平行六面体的O 分子(结构如图)。
2 8
1molO 分子含 molσ键。O 中存在 种氧氧键。
8 8(5)钴能形成多种配合物。
①[Co(NH )]3+空间结构为正八面体,如图所示。由此推知,[Co(NH )Cl]+的同分异构体有 种。
3 6 3 4 2
②配离子颜色与分裂能大小有关,1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量
为d轨道的分裂能。则d轨道的分裂能:[Co(H O) ]2+(呈粉色) (填“>”或“<”)[Co(H O) ]3+(呈红色)。
2 6 2 6
(6)一种铁的硫化物的晶胞如图所示( 为硫, 为铁)。已知:六棱柱底面边长为apm,高为bpm,
N 为阿伏加德罗常数的值。该晶体的化学式为 ;Fe的配位数为 。
A
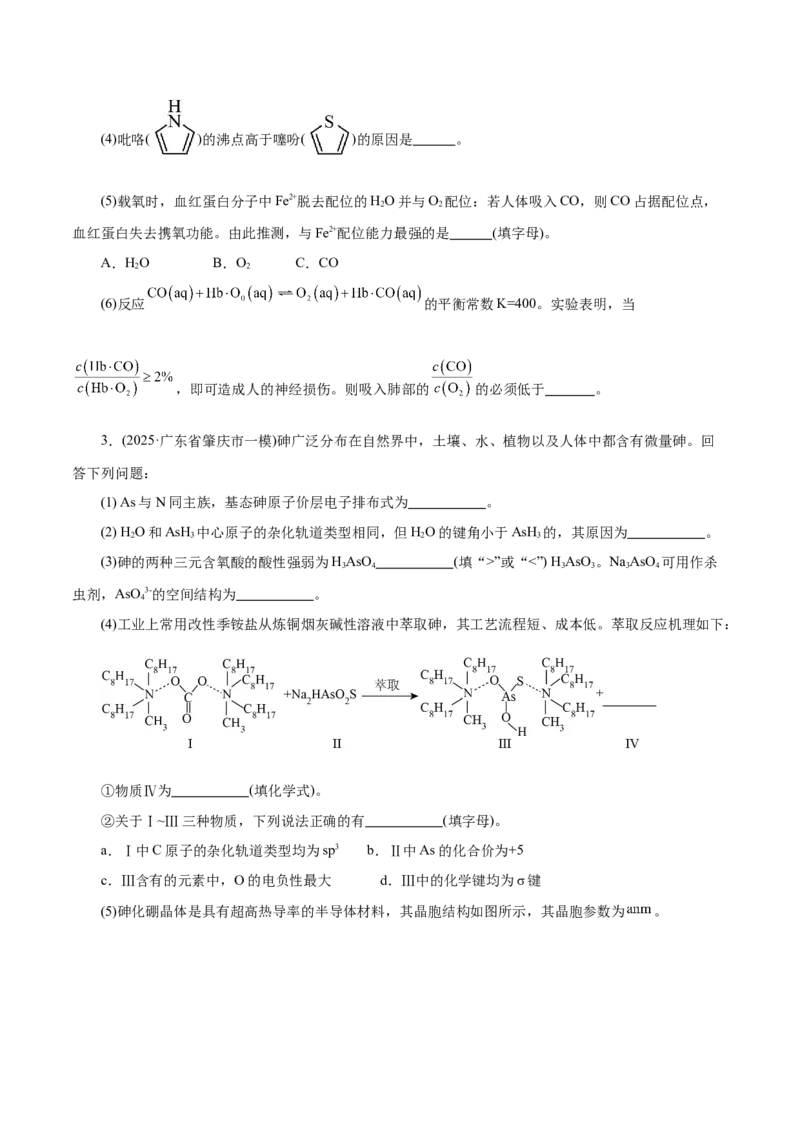
2.(2025·上海市上海师大附中高三期中)铁是人体必须的痕量元素之一,人体血液中血红蛋白中血红
素结构如图。
(1)血红素中铁微粒(Fe2+)的基态价电子排布式是 。
(2)血红素中C、N、O的第一电离能大小顺序为 。
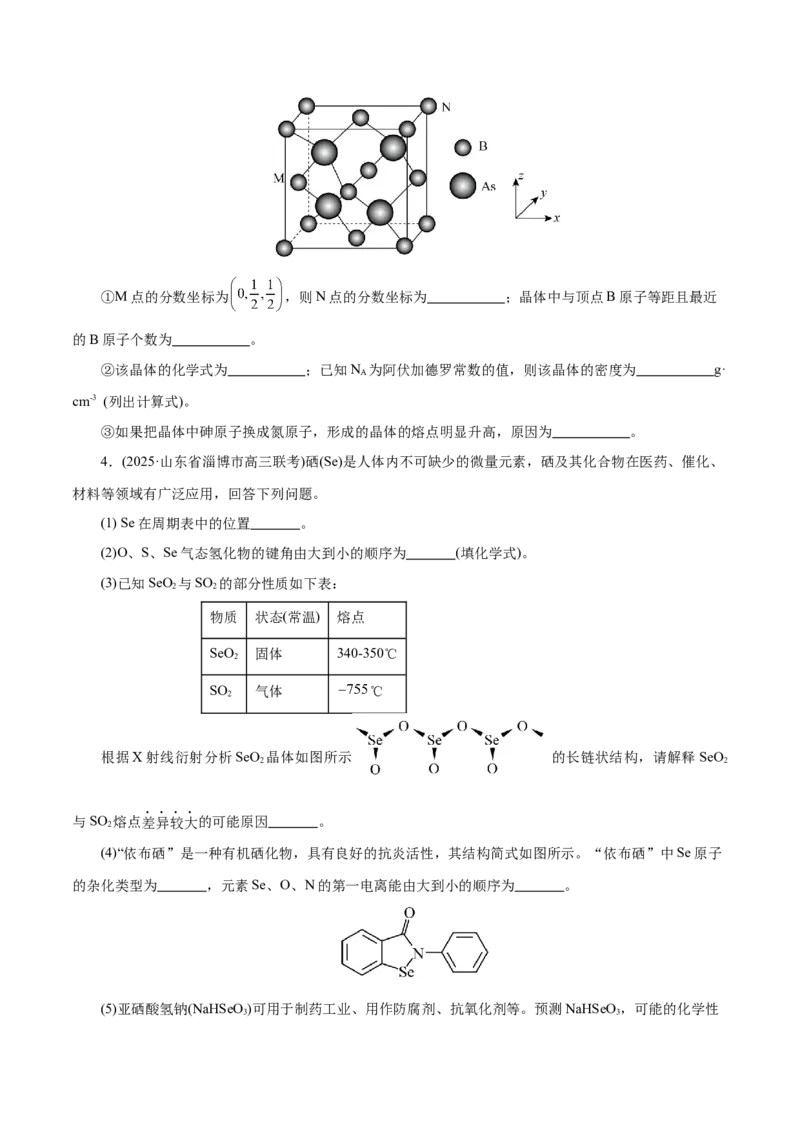
(3)血红素结构中含有吡咯( )单元。吡咯能与盐酸反应,从结构角度解释原因 。(4)吡咯( )的沸点高于噻吩( )的原因是 。
(5)载氧时,血红蛋白分子中Fe2+脱去配位的HO并与O 配位:若人体吸入CO,则CO占据配位点,
2 2
血红蛋白失去携氧功能。由此推测,与Fe2+配位能力最强的是 (填字母)。
A.HO B.O C.CO
2 2
(6)反应 的平衡常数K=400。实验表明,当
,即可造成人的神经损伤。则吸入肺部的 的必须低于 。
3.(2025·广东省肇庆市一模)砷广泛分布在自然界中,土壤、水、植物以及人体中都含有微量砷。回
答下列问题:
(1) As与N同主族,基态砷原子价层电子排布式为 。
(2) H O和AsH 中心原子的杂化轨道类型相同,但HO的键角小于AsH 的,其原因为 。
2 3 2 3
(3)砷的两种三元含氧酸的酸性强弱为HAsO (填“>”或“<”) HAsO 。NaAsO 可用作杀
3 4 3 3 3 4
虫剂,AsO 3-的空间结构为 。
4
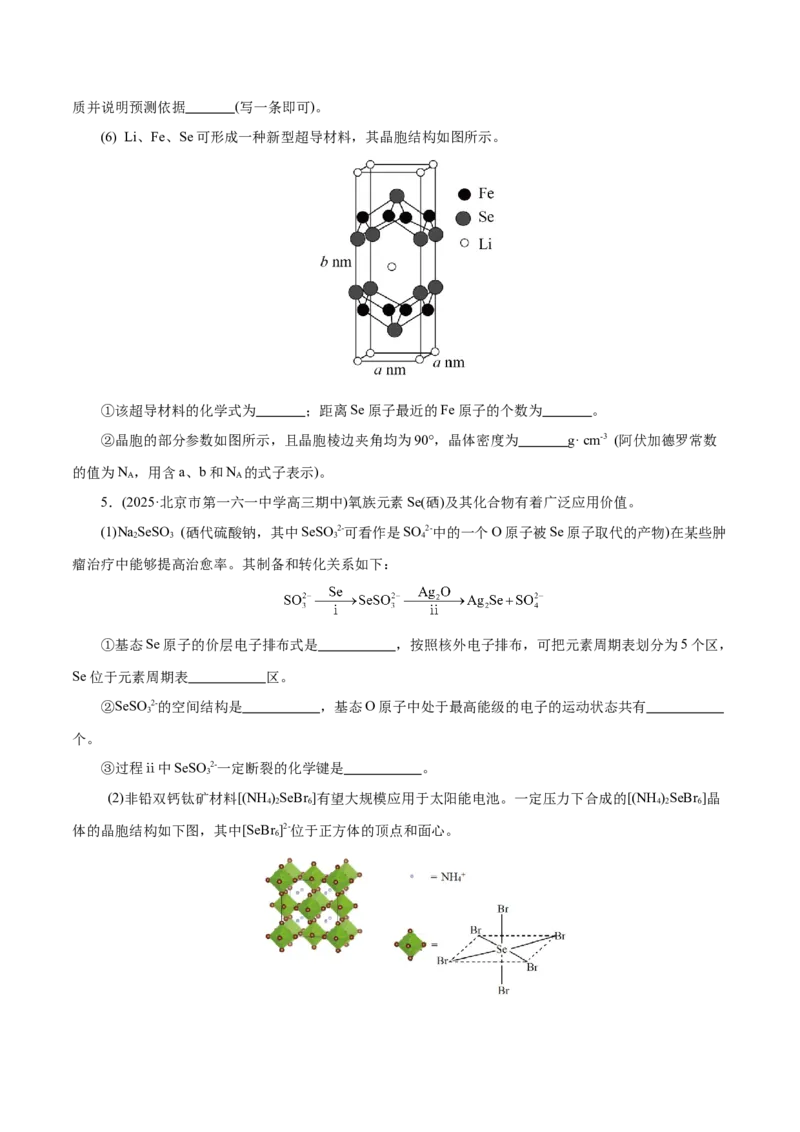
(4)工业上常用改性季铵盐从炼铜烟灰碱性溶液中萃取砷,其工艺流程短、成本低。萃取反应机理如下:
①物质Ⅳ为 (填化学式)。
②关于Ⅰ~Ⅲ三种物质,下列说法正确的有 (填字母)。
a.Ⅰ中C原子的杂化轨道类型均为sp3 b.Ⅱ中As的化合价为+5
c.Ⅲ含有的元素中,O的电负性最大 d.Ⅲ中的化学键均为σ键
(5)砷化硼晶体是具有超高热导率的半导体材料,其晶胞结构如图所示,其晶胞参数为 。①M点的分数坐标为 ,则N点的分数坐标为 ;晶体中与顶点B原子等距且最近
的B原子个数为 。
②该晶体的化学式为 ;已知N 为阿伏加德罗常数的值,则该晶体的密度为 g·
A
cm-3 (列出计算式)。
③如果把晶体中砷原子换成氮原子,形成的晶体的熔点明显升高,原因为 。
4.(2025·山东省淄博市高三联考)硒(Se)是人体内不可缺少的微量元素,硒及其化合物在医药、催化、
材料等领域有广泛应用,回答下列问题。
(1) Se在周期表中的位置 。
(2)O、S、Se气态氢化物的键角由大到小的顺序为 (填化学式)。
(3)已知SeO 与SO 的部分性质如下表:
2 2
物质 状态(常温) 熔点
SeO 固体 340-350℃
2
SO 气体 ℃
2
根据X射线衍射分析SeO 晶体如图所示 的长链状结构,请解释SeO
2 2
与SO 熔点差异较大的可能原因 。
2
(4)“依布硒”是一种有机硒化物,具有良好的抗炎活性,其结构简式如图所示。“依布硒”中Se原子
的杂化类型为 ,元素Se、O、N的第一电离能由大到小的顺序为 。
(5)亚硒酸氢钠(NaHSeO )可用于制药工业、用作防腐剂、抗氧化剂等。预测NaHSeO ,可能的化学性
3 3质并说明预测依据 (写一条即可)。
(6) Li、Fe、Se可形成一种新型超导材料,其晶胞结构如图所示。
①该超导材料的化学式为 ;距离Se原子最近的Fe原子的个数为 。
②晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 g· cm-3 (阿伏加德罗常数
的值为N ,用含a、b和N 的式子表示)。
A A
5.(2025·北京市第一六一中学高三期中)氧族元素Se(硒)及其化合物有着广泛应用价值。
(1)Na SeSO (硒代硫酸钠,其中SeSO 2-可看作是SO 2-中的一个O原子被Se原子取代的产物)在某些肿
2 3 3 4
瘤治疗中能够提高治愈率。其制备和转化关系如下:
①基态Se原子的价层电子排布式是 ,按照核外电子排布,可把元素周期表划分为5个区,
Se位于元素周期表 区。
②SeSO 2-的空间结构是 ,基态O原子中处于最高能级的电子的运动状态共有
3
个。
③过程ⅱ中SeSO 2-一定断裂的化学键是 。
3
(2)非铅双钙钛矿材料[(NH )SeBr ]有望大规模应用于太阳能电池。一定压力下合成的[(NH )SeBr ]晶
4 2 6 4 2 6
体的晶胞结构如下图,其中[SeBr]2-位于正方体的顶点和面心。
6①比较Se原子和Br原子的第一电离能大小,并从原子结构的角度说明理由 。
②NH +中H-N-H键角 (填“>”或“<”)NH 中H-N-H键角。
4 3
③一定压力下形成的[(NH )SeBr ]晶胞形状为正方体,边长为a nm。已知[(NH )SeBr ]的摩尔质量是
4 2 6 4 2 6
M g·molˉ1,阿伏加德罗常数为N ,该晶体密度为 g· cm-3。( )
A
(3) Cu Se是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下
2-x
图所示(晶胞内未标出因放电产生的0价Cu原子)。
每个NaSe晶胞完全转化为Cu Se晶胞,转移电子数为 。
2 2-x
6.(2025·河北省邢台市邢襄联盟高三联考)铁、锰、铬、铜等金属及其化合物在科学研究和工业生产
中用途广泛。请回答下列问题:
(1)基态铁原子中最高能层符号为 ,其最外层电子所占据轨道的电子云轮廓图为
形。
(2)锰和铬的第一电离能分别为717.3kJ·mol−1和652.9 kJ·mol−1,而锰、铬的第二电离能分别为
1509.0kJ·mol−1、1590.6kJ·mol−1,从核外电子排布角度解释铬的第二电离能比锰大的原因: 。
(3)烟酸铬(Ⅲ)可促进动物生长发育和蛋白质合成,在工业上主要用作饲料添加剂、医药保健品、食品
添加剂等,其结构如图所示。
①该配合物中的配体有 种。
②C、N、O三种元素形成的最简单氢化物的键角由大到小的顺序是 (填化学式),原因为
。(4)铜的某种常见氧化物的晶胞结构如图,已知晶胞棱长为apm,1号 原子的坐标为 ,3号
原子的坐标为(1,1,1),设N 为阿伏加德罗常数的值。
A
①Cu原子的配位数为 。
②2号原子的坐标为 。
③该晶体的密度为 g· cm-3。
7.(2025·河南省示范性高中高三质量监测)卤族元素形成的单质和化合物有很多,我们可以利用所学
物质结构与性质的相关知识去认识和理解它们。回答下列问题:
(1)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF) 形式存在的,使氢氟酸分子缔合的作用力是
2
。
(2)溴原子的M能层电子排布式为 。
(3)氯化镀在气态时存在二聚体分子[(BeCl )]。该二聚体分子为平面结构,其结构式为
2 2
,其中Be的杂化方式为 。
(4)(CN) (氰)与卤素单质性质相似,与HО反应生成HCN(氢氰酸)和HOCN(氰酸),反应中所涉及的第
2 2
二周期元素的第一电离能由大到小的顺序为 (填元素符号)。
(5)已知羧酸:①CFCOOH,②CHCOOH,③CHFCOOH,④CHClCOOH,⑤CHCHCOOH,其
3 3 2 2 3 2
酸性由强到弱的顺序为 (填序号)。
(6)溴化碘(IBr)的化学性质也和卤素单质类似,溴化碘和水反应生成了一种三原子分子,反应的化学方
程式为 。
(7)一定条件下,SbCl 与GaCl 以物质的量之比为1:1混合得到一种固态离子化合物,其结构组成可
3 3
能为:(a)[SbCl ]+[GaCl ]-或(b)[GaCl ]+[SbCl ]-,该离子化合物最可能的结构组成为 (填“a”或
2 4 2 4
“b”),理由是 。
(8)卤族元素除F外,CI、Br、I均可形成多种含氧酸根离子。ClO -、IO -、BrO-中键角最大的是
2 3 4
(填离子符号)。(9)碘与锰形成的某种晶体的晶胞结构及晶胞参数如图所示(已知图中I原子与所连接的3个Mn原子的
距离相等),阿伏加德罗常数的值为N 则该晶体的化学式是 ,晶体的密度为
A.
g·cm-3(列出计算式)。
1.(2024·全国甲卷,11,15分)ⅣA族元素具有丰富的化学性质,其化合物有着广泛的应用。回答下列
问题:
(1)该族元素基态原子核外未成对电子数为 ,在与其他元素形成化合物时,呈现的最高化合价为
。
(2) CaC 俗称电石,该化合物中不存在的化学键类型为 (填标号)。
2
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)一种光刻胶薄膜成分为聚甲基硅烷 ,其中电负性最大的元素是 ,硅原子的杂化轨道类
型为 。
(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原因: 。
物质 SnF SnCl SnBr SnI
4 4 4 4
熔点/ 442 29 143
(5)结晶型 可作为放射性探测器元件材料,其立方晶胞如图所示。其中 的配位数为 。设N
A
为阿伏加德罗常数的值,则该晶体密度为 g· cm-3 (列出计算式)。2.(2024· 重庆卷,15,14分)含钌( )催化剂在能源等领域应用广泛。Ru(NO)(NO ) 方是制备负载型
3 3
钌催化剂的前驱体。一种制备高纯Ru(NO)(NO ) 的技术路线如下(部分试剂、步骤及反应条件略)。
3 3
回答下列问题:
(1)已知基态 的核外电子排布式为[Kr]4d75s1,则 在元素周期表中位于第 周期第 族。
KNO 中,NO -的空间结构为 。
2 2
(2)为验证Ru与 形成了配位键,对所得Ru(NO)Cl 的表征结果如图所示,表征所用仪器是_______。
3
A.核磁共振仪 B.质谱仪 C.红外光谱仪 D.X射线衍射仪
(3)步骤①中无气体生成,除生成 配合物外,生成的盐还有 (填化学式)。
(4)步骤②生成的Ru(NO)(OH) 为难溶物,反应的化学方程式为 。
3
(5)步骤③在加入稀硝酸前,需要将难溶物加入AgNO 溶液中,以除去残留的Cl-;为使Cl-沉淀完全,
3
Ag+浓度应大于 mol·L-1。(已知AgCl的K =1.8×10-10)
sp
(6)Ru(NO)(NO ) 受热易分解,在 时完全分解,失重率为 ,剩余固体为 的氧化物,则该氧
3 3
化物的化学式为 。