文档内容
专题 13 化学实验基础
一、单选题
1.某化工厂发生了氯气泄漏,以下自救得当的是( )
A. 喷射氢氧化钠溶液将泄露的氯气吸收 B. 向地势低的地方撤离
C. 观察风向,顺风撤离
D. 用湿毛巾或蘸有肥皂水的毛巾捂住口鼻撤退
2.下列物质对应的组成正确的是( )
A. 芒硝:NaSO ·H O B. 消石灰:CaO
2 4 2
C. 碳铵:NH HCO D. 摩尔盐:NH Fe(SO )·6H O
4 3 4 4 2 2
3.下列物质对应的组成错误的是( )
A. 甘氨酸:HOOCCH NH B. 生石膏:CaSO·2H O
2 2 4 2
C. 重晶石:BaCO D. 硬脂酸:C H COOH
3 17 35
4.下列仪器在蒸馏实验中需要用到的是( )
A. B. C. D.
5.下列图示对应的操作不规范的是( )
A B C D
称量 溶解 过滤 转移溶液
A. A B. B C. C D. D
6.仪器名称为“容量瓶”的是( )
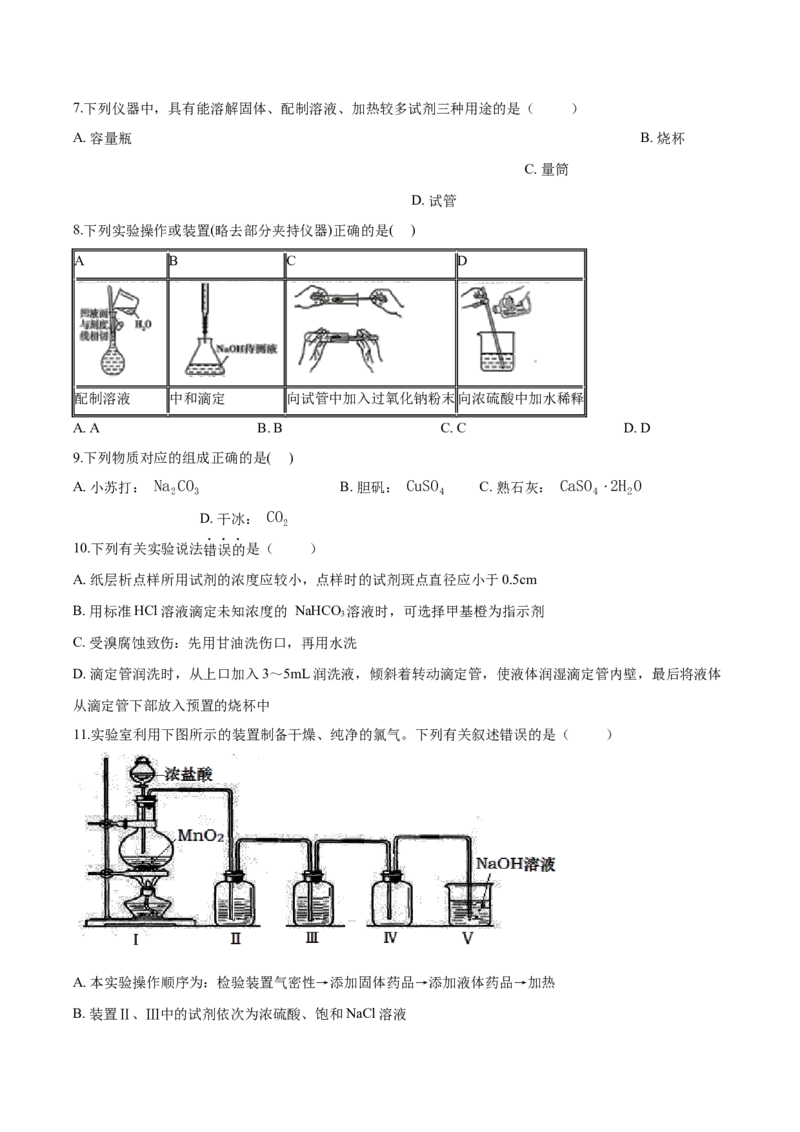
A. B. C. D.7.下列仪器中,具有能溶解固体、配制溶液、加热较多试剂三种用途的是( )
A. 容量瓶 B. 烧杯
C. 量筒
D. 试管
8.下列实验操作或装置(略去部分夹持仪器)正确的是( )
A B C D
配制溶液 中和滴定 向试管中加入过氧化钠粉末向浓硫酸中加水稀释
A. A B. B C. C D. D
9.下列物质对应的组成正确的是( )
A. 小苏打: Na CO B. 胆矾: CuSO C. 熟石灰: CaSO ⋅2H O
2 3 4 4 2
D. 干冰: CO
2
10.下列有关实验说法错误的是( )
A. 纸层析点样所用试剂的浓度应较小,点样时的试剂斑点直径应小于0.5cm
B. 用标准HCl溶液滴定未知浓度的 NaHCO 溶液时,可选择甲基橙为指示剂
3
C. 受溴腐蚀致伤:先用甘油洗伤口,再用水洗
D. 滴定管润洗时,从上口加入3~5mL润洗液,倾斜着转动滴定管,使液体润湿滴定管内壁,最后将液体
从滴定管下部放入预置的烧杯中
11.实验室利用下图所示的装置制备干燥、纯净的氯气。下列有关叙述错误的是( )
A. 本实验操作顺序为:检验装置气密性→添加固体药品→添加液体药品→加热
B. 装置Ⅱ、Ⅲ中的试剂依次为浓硫酸、饱和NaCl溶液C. 氯气密度比空气大,故装置Ⅳ中长导管进气,短导管出气
D. 装置Ⅴ中反应的离子方程式为:Cl+2OH﹣=Cl﹣+ClO﹣+ H O
2 2
12.下列化学实验操作正确的是( )
A. 钠着火可用CO 灭火
2
B. 水和碘的四氯化碳溶液分液时,水从分液漏斗上口倒出,碘的四氯化碳溶液从漏斗下口流出
C. 用试管加热碳酸氢钠固体时使试管口竖直向上
D. 为了使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动
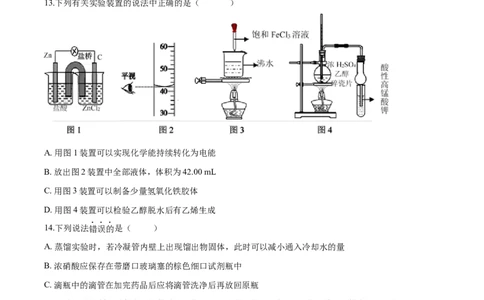
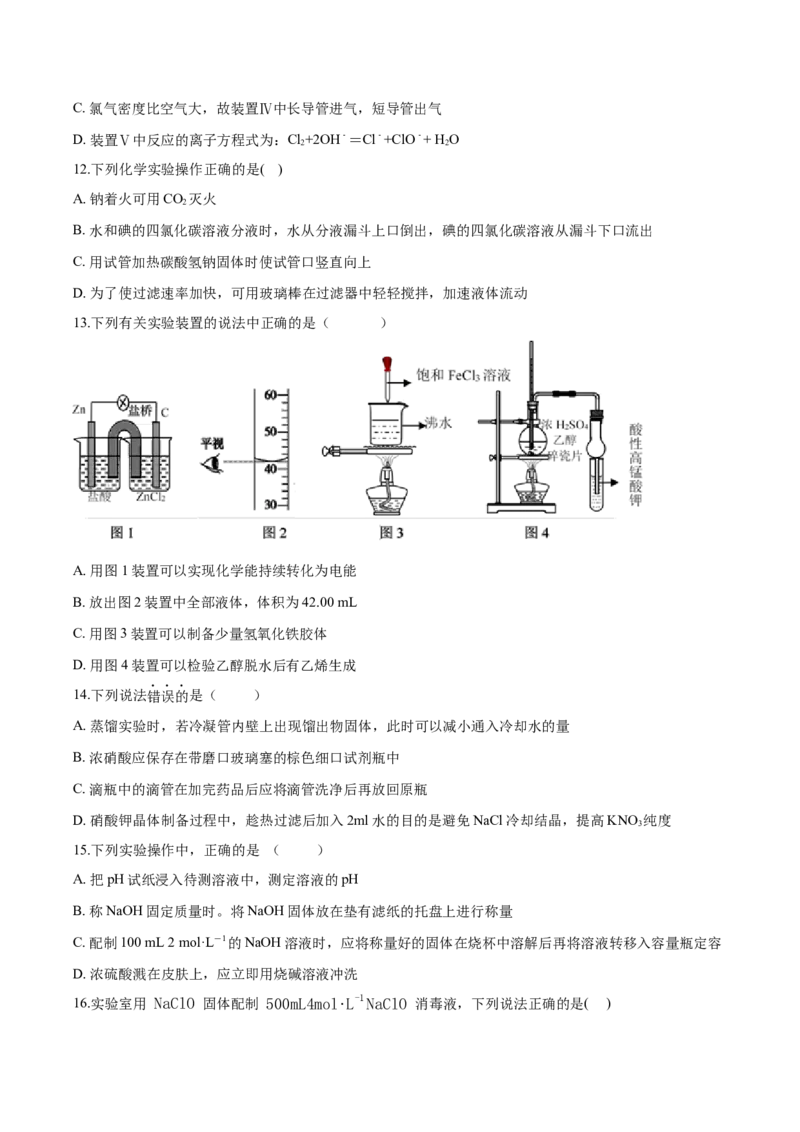
13.下列有关实验装置的说法中正确的是( )
A. 用图1装置可以实现化学能持续转化为电能
B. 放出图2装置中全部液体,体积为42.00 mL
C. 用图3装置可以制备少量氢氧化铁胶体
D. 用图4装置可以检验乙醇脱水后有乙烯生成
14.下列说法错误的是( )
A. 蒸馏实验时,若冷凝管内壁上出现馏出物固体,此时可以减小通入冷却水的量
B. 浓硝酸应保存在带磨口玻璃塞的棕色细口试剂瓶中
C. 滴瓶中的滴管在加完药品后应将滴管洗净后再放回原瓶
D. 硝酸钾晶体制备过程中,趁热过滤后加入2ml水的目的是避免NaCl冷却结晶,提高KNO 纯度
3
15.下列实验操作中,正确的是 ( )
A. 把pH试纸浸入待测溶液中,测定溶液的pH
B. 称NaOH固定质量时。将NaOH固体放在垫有滤纸的托盘上进行称量
C. 配制100 mL 2 mol·L-1的NaOH溶液时,应将称量好的固体在烧杯中溶解后再将溶液转移入容量瓶定容
D. 浓硫酸溅在皮肤上,应立即用烧碱溶液冲洗
16.实验室用 NaClO 固体配制 500mL4mol·L-1NaClO 消毒液,下列说法正确的是( )A. 如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器即可
B. 容量瓶用蒸馏水洗净后,应烘干后才能用于配制溶液
C. 用放置时间较长 NaClO 来配制溶液,可能导致所配溶液浓度偏低
D. 定容时,俯视容量瓶刻度线,会导致所配溶液浓度偏低
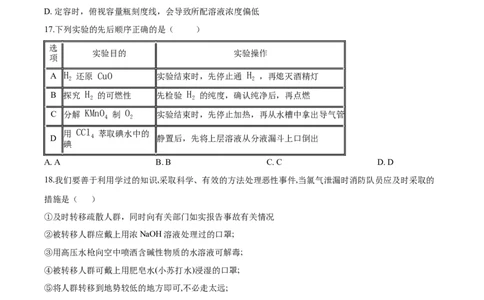
17.下列实验的先后顺序正确的是( )
选
实验目的 实验操作
项
A H 还原 CuO 实验结束时,先停止通 H ,再熄灭酒精灯
2 2
B 探究 H 的可燃性 先检验 H 的纯度,确认纯净后,再点燃
2 2
C 分解 KMnO 制 O 实验结束时,先停止加热,再从水槽中拿出导气管
4 2
用 CCl 萃取碘水中的
D 4 静置后,先将上层溶液从分液漏斗上口倒出
碘
A. A B. B C. C D. D
18.我们要善于利用学过的知识,采取科学、有效的方法处理恶性事件,当氯气泄漏时消防队员应及时采取的
措施是( )
①及时转移疏散人群,同时向有关部门如实报告事故有关情况
②被转移人群应戴上用浓NaOH溶液处理过的口罩;
③用高压水枪向空中喷洒含碱性物质的水溶液可解毒;
④被转移人群可戴上用肥皂水(小苏打水)浸湿的口罩;
⑤将人群转移到地势较低的地方即可,不必走太远;
⑥及时清理现场,检查水源和食物等是否被污染;
⑦常温下氯气能溶于水,所以只要向空气中喷洒水就可以解毒。
A. ②③④⑤ B. ①③④⑥ C. ①②⑤⑥ D. ①③⑤
19.氯气是有毒的,曾被制成毒气弹用于侵略战争,当这种毒气弹顺风爆炸时,通常可用的防御方法是( )
A. 人应躲到低洼的地方
B. 人、畜应到较高的地方去C. 人、畜应多饮豆浆和牛乳
D. 可用NaOH溶液浸湿软布蒙面
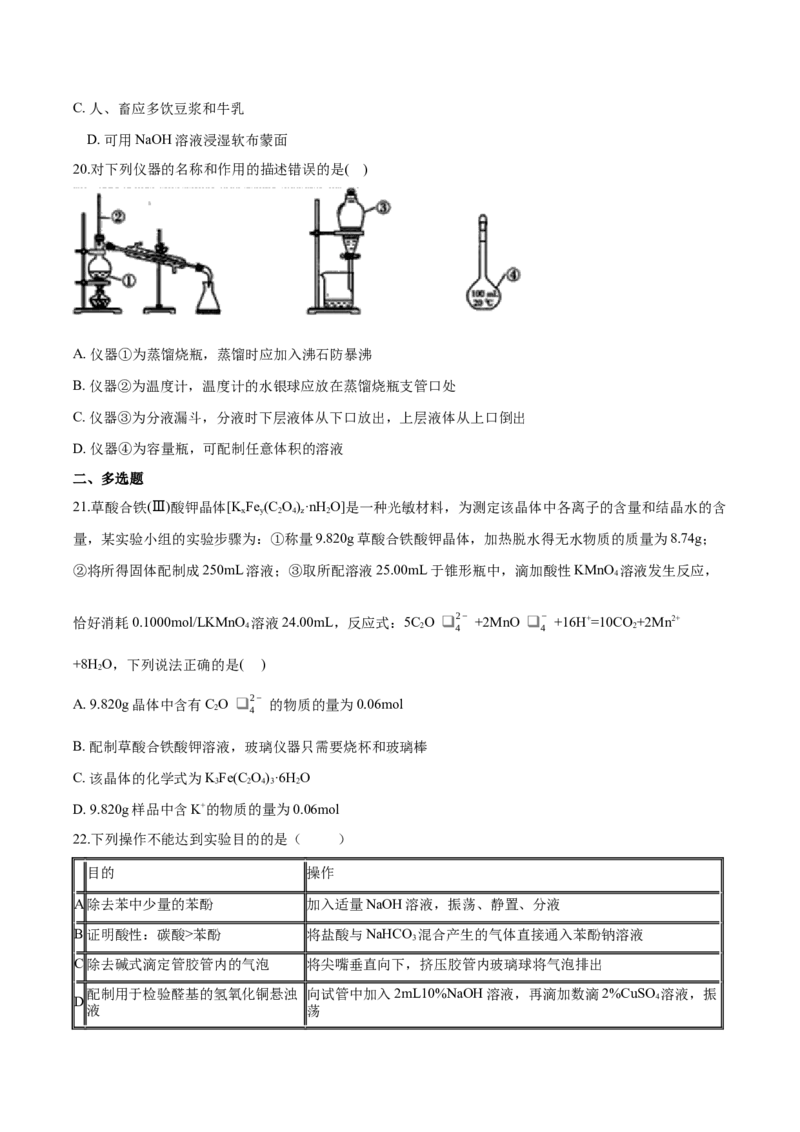
20.对下列仪器的名称和作用的描述错误的是( )
A. 仪器①为蒸馏烧瓶,蒸馏时应加入沸石防暴沸
B. 仪器②为温度计,温度计的水银球应放在蒸馏烧瓶支管口处
C. 仪器③为分液漏斗,分液时下层液体从下口放出,上层液体从上口倒出
D. 仪器④为容量瓶,可配制任意体积的溶液
二、多选题
21.草酸合铁(Ⅲ)酸钾晶体[K Fe (C O)·nH O]是一种光敏材料,为测定该晶体中各离子的含量和结晶水的含
x y 2 4 z 2
量,某实验小组的实验步骤为:①称量9.820g草酸合铁酸钾晶体,加热脱水得无水物质的质量为8.74g;
②将所得固体配制成250mL溶液;③取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO 溶液发生反应,
4
恰好消耗0.1000mol/LKMnO 溶液24.00mL,反应式:5C O ❑ 2− +2MnO ❑ − +16H+=10CO +2Mn2+
4 2 4 4 2
+8H O,下列说法正确的是( )
2
2−
A. 9.820g晶体中含有C O ❑ 的物质的量为0.06mol
2 4
B. 配制草酸合铁酸钾溶液,玻璃仪器只需要烧杯和玻璃棒
C. 该晶体的化学式为KFe(C O)·6H O
3 2 4 3 2
D. 9.820g样品中含K+的物质的量为0.06mol
22.下列操作不能达到实验目的的是( )
目的 操作
A除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
B证明酸性:碳酸>苯酚 将盐酸与NaHCO 混合产生的气体直接通入苯酚钠溶液
3
C除去碱式滴定管胶管内的气泡 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出
配制用于检验醛基的氢氧化铜悬浊 向试管中加入2mL10%NaOH溶液,再滴加数滴2%CuSO 溶液,振
D 4
液 荡A. A B. B C. C D. D
23.下列说法正确的是( )
A. 抽滤实验洗涤晶体时,应先关小水龙头停止抽气,再在布氏漏斗中加少量洗涤剂,用玻璃 棒小心搅动
使晶体润湿,静置一会再打开水龙头慢慢抽气
B. 容量瓶、量筒和滴定管上都要标明使用温度,容量瓶无“0”刻度,量筒、滴定管有“0”刻度
C. 在比较乙醇和苯酚与钠反应的实验中,要把乙醇和苯酚配成同物质的量浓度的水溶液,再与相同大小的
金属钠反应,来判断两者羟基上氢的活性
D. 中和滴定实验中锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必须干燥或润洗后
方可使用
24.下列实验操作中正确的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 B. 称量时,将固体
NaOH直接放在天平右盘上
C. 蒸馏时,冷却水应从冷凝管的下口通入,上口流出。 D. 用托盘天平称量NaCl固
体5.85g
25.下列叙述错误的是( )
A. 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火,可以使用干粉灭火器灭火
B. 探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温
度,则测得的反应速率偏高
C. 蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置
D. 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加
蒸馏水至刻度线
三、填空题
26.同学根据 Mg 与 CO 反应原理,推测钠也应能在 CO 中燃烧。为了确 定其生成产物并进行实验论
2 2
证,请你参与以下研究过程。该同学按实验要求,用下列装置(图中装置之间橡胶管连接处止水夹已省
去)进行实验(已知 PdCl 溶液能 被 CO 还原得到黑色的 Pd),请完成下列问题:
2①装置 1 气密性的检验方法________。
②若装置 6 中有黑色沉淀,装置 4 中的残留固体(只有一种物质)加盐酸有能使石灰 水变浑浊的气体
放出,则钠与二氧化碳反应的化学方程式为:________。
③指导老师认为,不仅要检验残留固体中是否有碳酸钠还要检验其中是否有氧化钠和 碳,当确认钠充分
反应后,请你设计一个简单实验,验证装置 4 中得到的残留固体 中是否含有碳:________。
四、实验探究题
27.PCl 是磷的常见氯化物,可用于半导体生产的外延、扩散工序。有关物质的部分性质如表:
3
熔点/℃沸点/℃密度/g/mL化学性质
加热
2P+3Cl (少量) ¿ 2PCl
2 ¿ 3
黄 ¿
44.1 280.5 1.82
磷 加热
2P+5Cl (过量) ¿ 2PCl
2 ¿ 5
¿
PCl -112 75.5 1.574 遇水生成HPO 和HCl,遇氧气生成POCl
3 3 3 3
(1)Ⅰ.PCl 的制备
3
如图是实验室制备PCl 的装置(部分仪器已省略)。
3
回答下列问题:
通入仪器甲中的冷却水从________(填“M”或 “N”)口出来;仪器乙为下端浸在冷水中的仪器,乙的名称
为________。
(2)检查装置气密性并装入药品后,先关闭K , 打开K 通入干燥的CO , 一段时间后,关闭K
1 2 2 2
, 加热曲颈瓶同时打开K 通入干燥氯气,反应立即进行。通干燥CO 的作用是________。
1 2
(3)实验室利用A装置制备Cl 的离子方程式为________;实验过程中,通入氯气的速率不宜过快的原因
2
是________。
(4)II.测定PCl 的纯度
3
测定产品中PCl 纯度的方法如下:迅速称取4.400g产品,水解完全后配成500mL溶液,取出25.00mL加
3
入过量0.1000mol/L20.00mL碘溶液,充分反应后再用0.1000mol/LNa SO 溶液滴定过量的碘,终点时消耗
2 2 312.00mLNa SO 溶液。已知:HPO +H O+I =H PO +2HI,I+2Na SO=2NaI+Na SO , 假设测定过程
2 2 3 3 3 2 2 3 4 2 2 2 3 2 4 6
中没有其他反应。
根据上述数据,该产品中PCl 的质量分数为________ [已知:M(PCl )=137.5g/mol];若滴定终点时仰视读
3 3
数,则PCl 的质量分数________(填“偏大”、“偏小”或“无影响”)。
3
(5)Ⅲ.PCl 水解生成的HPO 性质探究
3 3 3
请你设计一个实验方案,证明HPO 为二元酸:________。
3 3
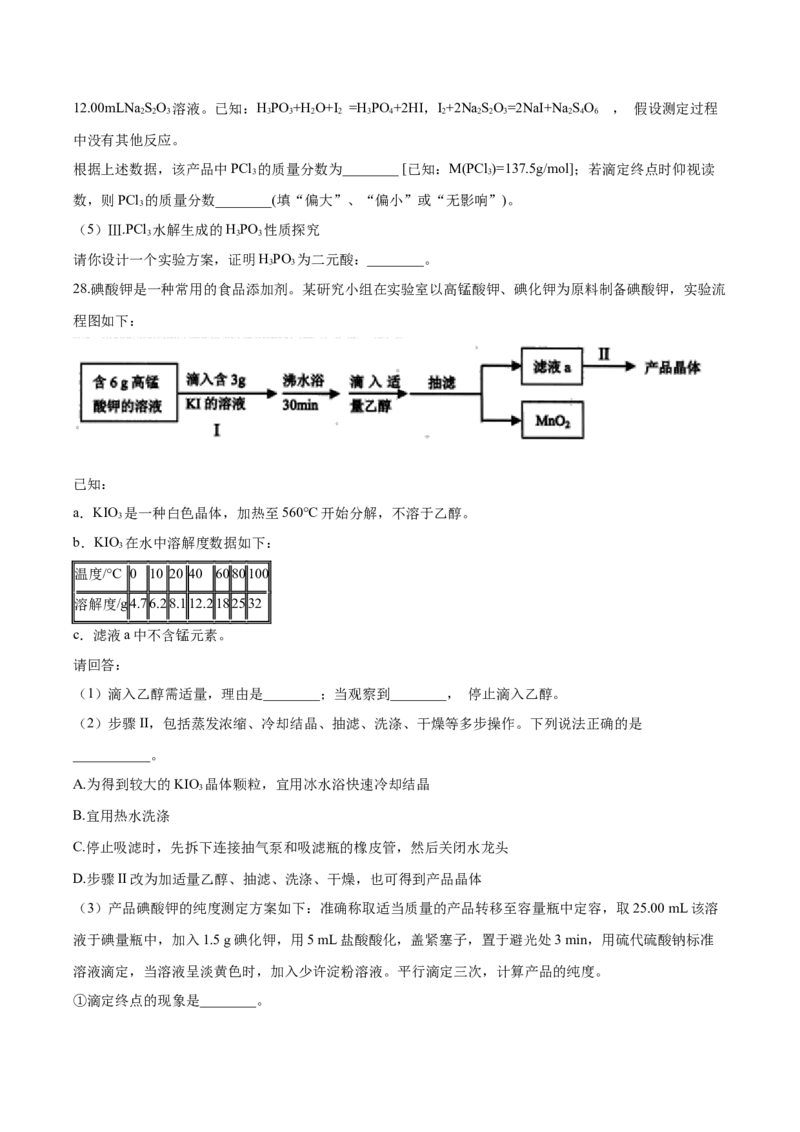
28.碘酸钾是一种常用的食品添加剂。某研究小组在实验室以高锰酸钾、碘化钾为原料制备碘酸钾,实验流
程图如下:
已知:
a.KIO 是一种白色晶体,加热至560°C开始分解,不溶于乙醇。
3
b.KIO 在水中溶解度数据如下:
3
温度/°C 0 10 20 40 6080100
溶解度/g4.76.28.112.2182532
c.滤液a中不含锰元素。
请回答:
(1)滴入乙醇需适量,理由是________;当观察到________, 停止滴入乙醇。
(2)步骤II,包括蒸发浓缩、冷却结晶、抽滤、洗涤、干燥等多步操作。下列说法正确的是
___________。
A.为得到较大的KIO 晶体颗粒,宜用冰水浴快速冷却结晶
3
B.宜用热水洗涤
C.停止吸滤时,先拆下连接抽气泵和吸滤瓶的橡皮管,然后关闭水龙头
D.步骤II改为加适量乙醇、抽滤、洗涤、干燥,也可得到产品晶体
(3)产品碘酸钾的纯度测定方案如下:准确称取适当质量的产品转移至容量瓶中定容,取25.00 mL该溶
液于碘量瓶中,加入1.5 g碘化钾,用5 mL盐酸酸化,盖紧塞子,置于避光处3 min,用硫代硫酸钠标准
溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液。平行滴定三次,计算产品的纯度。
①滴定终点的现象是________。②若滴定结束时仰视读数,则测定的结果________(填 “偏大”、“偏小”或“无影响”)。
29.在工业上经常用水蒸气蒸馏的方法从橙子等水果果皮中收集橙油(主要成分是柠檬烯 )。实验
步骤如下:
Ⅰ提取柠檬烯
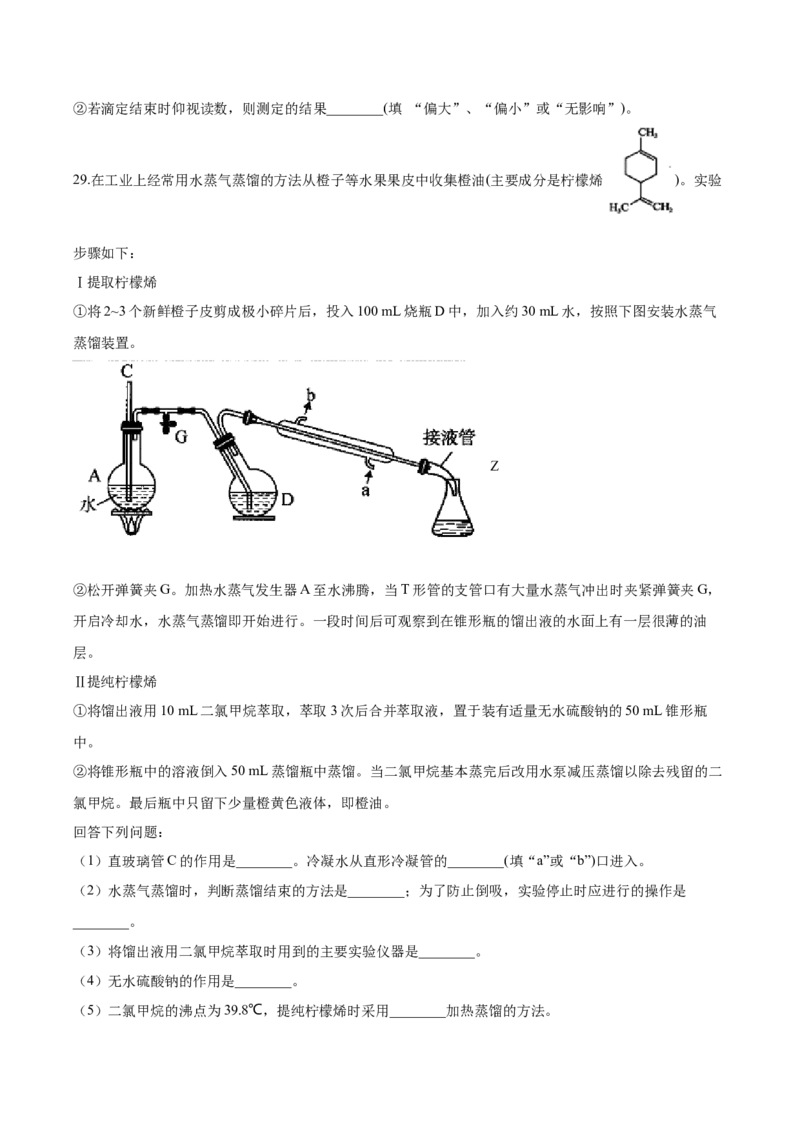
①将2~3个新鲜橙子皮剪成极小碎片后,投入100 mL烧瓶D中,加入约30 mL水,按照下图安装水蒸气
蒸馏装置。
Z
②松开弹簧夹G。加热水蒸气发生器A至水沸腾,当T形管的支管口有大量水蒸气冲出时夹紧弹簧夹G,
开启冷却水,水蒸气蒸馏即开始进行。一段时间后可观察到在锥形瓶的馏出液的水面上有一层很薄的油
层。
Ⅱ提纯柠檬烯
①将馏出液用10 mL二氯甲烷萃取,萃取3次后合并萃取液,置于装有适量无水硫酸钠的50 mL锥形瓶
中。
②将锥形瓶中的溶液倒入50 mL蒸馏瓶中蒸馏。当二氯甲烷基本蒸完后改用水泵减压蒸馏以除去残留的二
氯甲烷。最后瓶中只留下少量橙黄色液体,即橙油。
回答下列问题:
(1)直玻璃管C的作用是________。冷凝水从直形冷凝管的________(填“a”或“b”)口进入。
(2)水蒸气蒸馏时,判断蒸馏结束的方法是________;为了防止倒吸,实验停止时应进行的操作是
________。
(3)将馏出液用二氯甲烷萃取时用到的主要实验仪器是________。
(4)无水硫酸钠的作用是________。
(5)二氯甲烷的沸点为39.8℃,提纯柠檬烯时采用________加热蒸馏的方法。30.亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水反应生成一种氯化物和两种氮
化物。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl , 制备装置如下图所示:
2
①制备NO发生装置可以选用________(填写字母代号),请写出发生反应的离子方程式:________。
②欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→ ________(按气流方向,用小写字母表示)。
(2)乙组同学利用甲组制得的NO和Cl 制备NOCl,装置如图所示:
2
①实验室也可用X装置制备NO,X装置的优点为________。
②检验装置气密性并装入药品,打开K , 然后再打开 ________,通入一段时间气体,其目的为
2
________,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中NOCl可能发生反应的化学方程式为________。
④若尾气处理装置连接上图烧杯中导管d,则烧杯中可加入 ________溶液。参考答案
一、单选题
1.【答案】 D
【解析】A.氢氧化钠具有强腐蚀性,不符合题意
B.氯气密度比空气大,应向地势较高的地方撤离,不符合题意
C.应逆风撤离,不符合题意
D.用湿毛巾或者蘸有肥皂水的毛巾捂住口鼻可吸收氯气,减少人吸入氯气,符合题意
故答案为:D
2.【答案】 C
【解析】A.十水硫酸钠的俗称是芒硝,化学式为:NaSO ·10H O,A不符合题意;
2 4 2
B.氢氧化钙的俗称是消石灰,化学式为:Ca(OH) , B不符合题意;
2
C.碳酸氢铵的俗称是碳铵,化学式为:NH HCO , C符合题意;
4 3
D.硫酸亚铁铵俗名为莫尔盐、摩尔盐,化学式为:Fe(NH )·(SO )·6H O,D不符合题意;
4 2 4 2 2
故答案为:C。
3.【答案】 C
【解析】A.甘氨酸是α-氨基乙酸,化学式为HOOCCH NH , A不符合题意;
2 2
B.生石膏是二水合硫酸钙,化学式为CaSO·2H O,B不符合题意;
4 2
C.重晶石是硫酸钡,化学式为BaSO , C符合题意;
4
D.硬脂酸又名十八烷酸,示性式为C H COOH,D不符合题意;
17 35
故答案为:C。
4.【答案】 A
【解析】A.蒸馏烧瓶,A符合题意;
B.蒸发皿,用于蒸发操作,B不符合题意;
C.容量瓶,用于配制一定物质的量浓度的溶液,C不符合题意;
D.球形干燥管,用于放固体干燥剂,或防倒吸装置,D不符合题意;
故答案为:A。
5.【答案】 D
【解析】A. 称量时左物右码,药品不能直接放在托盘上,图中操作合理,A不符合题意;
B. 溶解在烧杯中进行,且玻璃棒搅拌可加速溶解,B不符合题意;C. 过滤遵循一贴二低三靠,图中过滤装置合理,C不符合题意;
D. 转移需要玻璃棒引流,图中缺少玻璃棒,D符合题意;
故答案为:D。
6.【答案】 C
【解析】A.为圆底烧瓶,故A不符合题意;
B.为试管,故B不符合题意;
C.容量瓶是一种带有磨口玻璃塞的细长颈、梨形的平底玻璃瓶,颈上有刻度,该仪器为容量瓶,故C符
合题意;
D.为烧杯,故D不符合题意;
故答案为:C。
7.【答案】 B
【解析】A、容量瓶只能作配制一定物质的量浓度溶液的仪器,不能作溶解、稀释、反应、长期贮存溶液
的仪器,故A不符合题意;
B、烧杯可以作溶解、配制溶液和加热较多试剂的仪器,故B符合题意;
C、量筒作量取液体的仪器,不能作溶解和加热试剂的仪器,故C不符合题意;
D、试管加热液体时,液体体积不能超过试管容积的1/3,因此作加热较多试剂的仪器,故D不符合题意。
8.【答案】 C
【解析】A.用容量瓶配制一定物质的量浓度的溶液时,当用烧杯加水至距离刻度线1~2cm处时,应该用
胶头滴管进行定容,故A不符合题意;
B.滴定NaOH溶液要用酸性标准液,酸性标准液应盛放在酸式滴定管中,图示滴定管为碱式滴定管,故
B不符合题意;
C.固体粉末药品的取用可以用纸槽或药匙来取,放入试管时,先将试管横放,把纸槽或药匙伸入试管内
慢慢将试管竖起,固体粉末药品的取用量为盖满试管底部即可,故C符合题意;
D.浓硫酸稀释时放热,为了防止暴沸发生危险,应将水加入浓硫酸中进行稀释,故D不符合题意;
故答案为:C。
9.【答案】 D
【解析】A.小苏打是NaHCO , 故A不符合题意;
3
B.胆矾是 CuSO ·5H O ,故B不符合题意;
4 2
C.熟石灰是由生石灰与水反应后生成的,成分是Ca(OH) , 故C不符合题意;
2
D.干冰是CO 的晶体形式,故D符合题意;
2
故答案为:D。10.【答案】 A
【解析】A.纸层析点样所用的试剂的浓度不宜过,过小会使得现象不明显,A符合题意;
B.用标准HCl溶液滴定未知浓度 NaHCO 溶液时,滴定终点呈弱酸性,可选择甲基橙或石蕊作为指示
3
剂,B不符合题意;
C.受溴腐蚀致伤,先用甘油洗伤口,再用水洗,甘油能溶解溴,而且毒性小,C不符合题意;
D.润洗滴定管时,从上口加入3~5mL润洗液,倾斜着转动滴定管,使液体润湿滴定管内壁,最后将液
体从滴定管下部放入预置的烧杯中,D不符合题意;
故答案为:A。
11.【答案】 B
【解析】A. 本实验操作顺序为:检验装置气密性→在圆底烧瓶中添加固体药品二氧化锰→通过分液漏斗
添加液体药品浓盐酸→加热制取氯气,净化干燥后收集,且注意尾气处理,选项A不符合题意;
B. 装置Ⅱ、Ⅲ中的试剂依次为饱和NaCl溶液、浓硫酸,以除去氯气中的氯化氢气体和干燥氯气,选项B
符合题意;
C. 氯气密度比空气大,故装置Ⅳ中长导管进气,短导管出气,利用排空气法收集且有尾气吸收,选项C
不符合题意;
D. 装置Ⅴ中多余的氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl+2OH
2
﹣=Cl﹣+ClO﹣+ H O,选项D不符合题意。
2
故答案为:B。
12.【答案】 B
【解析】A.钠燃烧生成过氧化钠,过氧化钠与二氧化碳反应生成氧气,燃烧更旺,钠着火不能用CO 灭
2
火,应选沙土扑灭,故A不符合题意;
B.水和碘的四氯化碳溶液分层,四氯化碳的密度大于水,水在上层,则分液时,水从分液漏斗上口倒
出,碘的四氯化碳溶液从漏斗下口流出,故B符合题意;
C.用试管加热碳酸氢钠固体时,试管口应略向下倾斜,防止生成的水倒流使试管炸裂,故C不符合题
意;
D.过滤时不能搅拌,易捣破滤纸,应使水自然流下,故D不符合题意;
故答案为:B。
13.【答案】 C
【解析】A.要实现化学能持续转化为电能,应该把Zn电极放入ZnCl 溶液中,把石墨电极放入盐酸中,
2
A不符合题意;B.图示的仪器小刻度在下,大刻度在上,表示的是量筒,精确度是0.1 mL,不能精确到0.01 mL,因此放
出图2装置中全部液体,体积为42.0 mL,B不符合题意;
C.氢氧化铁胶体的制取方法是:向沸腾的蒸馏水中滴加几滴饱和氯化铁饱和溶液,继续加热液体呈红褐
色,停止加热,得到的红褐色液体就是氢氧化铁胶体,C符合题意 ;
D.乙醇易挥发,乙醇能被酸性高锰酸钾溶液氧化而使溶液褪色,同时乙醇与浓硫酸发生氧化还原反应生
成的二氧化硫也能使酸性高锰酸钾溶液褪色,因此不能确定是否产生了乙烯,D不符合题意;
故答案为:C。
14.【答案】 C
【解析】A.蒸馏实验时,冷凝管内壁上出现馏出物固体,说明冷却效果太好,此时可以减小通入冷却水
的流速,A不符合题意;
B.浓硝酸见光分解且会氧化橡胶塞,浓硝酸应保存在带磨口玻璃塞的棕色细口试剂瓶中,B不符合题
意;
C.滴瓶中的滴管在加完药品后洗净后再放回原瓶会导致试剂浓度变化,C符合题意;
D.硝酸钾的溶解度随温度变化影响较大,趁热过滤后加入2ml水,可以避免NaCl因温度变化过大而析
出,影响硝酸钾纯度,D不符合题意;
故答案为:C。
15.【答案】 C
【解析】A.使用pH试纸时不能直接将试纸浸到溶液中,应用玻璃棒蘸取溶液滴在PH试纸上,防止污染溶
液,故A不符合题意;
B.NaOH具有吸水性能与空气中二氧化碳反应,称量时应尽量减小与空气的接触面积,应放在小烧杯中称
量,故B不符合题意;
C.配制100 mL2mol·L-1的NaOH溶液时,应将称量好的固体在烧杯中溶解冷却后再将溶液转移入容量瓶,
在加水定容即可,故C符合题意;
D.因浓硫酸能与烧碱反应放出大量的热,如果用烧碱溶液清洗会增大烧伤面积,所以先用抹布擦拭,再用
大量的水冲洗,故D不符合题意;
故答案为:C。
16.【答案】 C
【解析】A.称量用到F托盘天平和药匙,溶解用到E烧杯和玻璃棒,转移用到G容量瓶和玻璃棒、烧
杯,定容用到胶头滴管,故A圆底烧瓶、B酸式滴定管、C移液管、D分液漏斗共4种仪器用不到,还缺
玻璃棒、胶头滴管共2种玻璃仪器,A不符合题意;
B.因定容时需要加水,故容量瓶洗涤后,不用烘干(如底部有少量水)也能使用,B不符合题意;C.放置时间较长的 NaClO 有部分NaClO和空气中的二氧化碳、水反应变质,NaClO物质的量偏小,导
致浓度偏低,C符合题意;
D.定容时,俯视容量瓶刻度线,导致溶液体积偏小,浓度偏高,D不符合题意。
故答案为:C。
【分析】用固体药品配制一定物质的量浓度的溶液的一般步骤为计算→称量→溶解→冷却→转移→洗涤→
定容→摇匀,结合步骤分析解答。
17.【答案】 B
【解析】A.氢气还原氧化铜,实验结束时,应先熄灭酒精灯,再停止通氢气,以防铜再次被氧化,故A
不选;
B.点燃可燃性气体前,为了防止气体不纯而爆炸,必须先检验气体的纯度,确认纯净后再点燃,故B
选;
C.分解KMnO 制取氧气,实验结束时,为防止倒吸,应先从水槽中拿出导气管,再停止加热,故C不
4
选;
D.用 CCl 萃取碘水中的碘,静置后,应将下层溶液从分液漏斗下口流出,故D不选;
4
故答案为:B。
18.【答案】 B
【解析】①及时转移疏散人群,同时向有关部门如实报告事故有关情况,故①符合及时采取的措施;②被
转移人群应戴上用浓NaOH溶液处理过的口罩,烧碱具有腐蚀性,不能用于捂住口鼻,故②不符合及时采
取的措施;③用高压水枪向空中喷洒含碱性物质的水溶液可解毒,氯气与碱性物质反应,故③符合及时采
取的措施;④被转移人群可戴上用肥皂水(小苏打水)浸湿的口罩,小苏打和氯气反应,用肥皂水(小苏打水)
浸湿的口罩可防止吸入大量氯气而中毒,故④符合及时采取的措施;⑤氯气密度大于空气的密度,和空气
混合时,氯气在下方,空气在上方,因此人群不能转移到地势较低的地方,故⑤不符合及时采取的措施;
⑥及时清理现场,检查水源和食物等是否被污染,故⑥符合及时采取的措施;⑦常温下氯气微溶于水,所
以只要向空气中喷洒水就不能解毒,故⑦不符合及时采取的措施;
因此①③④⑥符合及时采取的措施,故B符合题意。
故答案为B。
19.【答案】 B
【解析】A.氯气的密度比空气大,躲避氯气应往较高的地方去,故A不符合题意;
B.根据A项分析,氯气的密度比空气大,躲避氯气应往较高的地方去,故B符合题意;
C.多饮用牛乳和豆浆不能减轻氯气中毒,故C不符合题意;D.NaOH属于强碱,具有较强的腐蚀性,会腐蚀皮肤,不能用NaOH溶液浸湿软布蒙面,故D不符合题
意;
故答案为:B。
20.【答案】 D
【解析】A. 仪器①为蒸馏烧瓶,液体加热时加入沸石,防止暴沸,A不符合题意;
B. 仪器②为温度计,是为了测量出来的气体的温度,所以温度计的水银球应放在蒸馏烧瓶支管口处,B
不符合题意;
C. 仪器③为分液漏斗,为了能很好的将上下层的液体分开,分液时下层液体从下口放出,上层液体从上
口倒出,C不符合题意;
D. 仪器④为容量瓶,该容量瓶能配制100mL的溶液,不能任意体积,D符合题意。
故答案为:D。
二、多选题
21.【答案】 A,D
2−
【解析】A.高锰酸钾得到电子等于C O ❑ 失去的电子,n =0.1000mol/L×0.024L×(7﹣2)
2 4 得
2− 2−
=0.012mol;C O ❑ 全部转化成CO , 化合价变化+3→+4,根据电子守恒 n(C O ❑ )=
2 4 2 2 4
0.012mol
=0.006mol,反应从250mL溶液中取25.00mL,草酸根总量为0.06mol,故A符合题意;
(2−1)×2
B.需要配制成250mL溶液,必须使用到250容量瓶和胶头滴管,故B不符合题意;
1
C.250mL原溶液C O2﹣的物质的量为0.006mol×10=0.06mol,故n[K Fe(C O)]=0.06mol×
2 4 3 2 4 3 3
=0.02mol,9.820g三草酸合铁酸钾晶体中结晶水的质量为:9.820﹣8.74=1.08(g),故n(HO)=
2
1.08g
=0.06mol,即0.02molKFe(C O) 中还有0.06molHO,结晶水数目为3,故该晶体的化学式
18g/mol 3 2 4 3 2
为KFe(C O)•3H O,故C不符合题意;
3 2 4 3 2
D.9.820g样品即0.02molKFe(C O) 中含K+的物质的量为0.06mol,故D符合题意;
3 2 4 3
故答案为:AD。
22.【答案】 B,C
【解析】A. 苯酚可与氢氧化钠溶液反应生成可溶于水的苯酚钠,最后与苯混合后互不相溶,分层,该操
作能达到实验目的,A不符合题意;B. 盐酸易挥发,若将盐酸与碳酸氢钠溶液混合产生的气体直接通入苯酚钠,可能挥发的HCl会与苯酚钠
反应生成常温下难溶于水的苯酚,不能证明是二氧化碳与其发生的反应,达不到实验目的,应该先除去二
氧化碳中可能挥发的HCl再进行实验操作,B符合题意;
C. 除去碱式滴定管胶管内气泡时,尖嘴不应该垂直向下,应向上挤压橡胶管,利用空气排出,该实验操
作达不到实验目的,C符合题意;
D. 为检验醛基,配制氢氧化铜悬浊液时,碱需过量,保证醛基是在碱性条件下发生反应,该操作可达到
实验目的,D不符合题意;
故答案为:BC
23.【答案】 A,D
【解析】A、抽滤实验洗涤晶体时,应先关小水龙头停止抽气,再在布氏漏斗中加少量洗涤剂,用玻璃棒
小心搅动使晶体润湿,静置一会再打开水龙头慢慢抽气,故A符合题意;
B、容量瓶标有温度、规格、刻度线,量筒标有温度、规格,滴定管标有温度、规格,量筒、容量瓶
无“0”刻度,滴定管有“0”刻度在最上面,故B不符合题意;
C、配成溶液时都含有水,而水的羟基活性大于乙醇中的羟基活性,不能比较出乙醇和苯酚羟基上氢的活
性,应分别用纯液体与钠反应来判断两者羟基上氢的活性
D、酸碱中和滴定实验中,如果将滴定管和移液管用蒸馏水洗净后,不干燥或润洗直接使用,会导致待测
液或标准液浓度偏低,影响实验结果,故D符合题意;
故答案为:A、D
24.【答案】 A,C
【解析】A.分液时上下层液体不能混合,则分液时,分液漏斗中下层液体从下口放出,上层液体从上口
倒出,选项A符合题意;
B、用托盘天平称量固体时应遵循左物右码的规则,氢氧化钠固体应放到小烧杯中称量,即氢氧化钠固体
应在小烧杯中放于托盘天平的左盘来称量,选项B不符合题意;
C.蒸馏时,冷却水下进上出在冷凝管中的时间长,则冷却效果好,选项C符合题意;
D、因为托盘天平能准确到0.1g,用托盘天平不能称取5.85g氯化钠固体,选项D不符合题意;
故答案为:AC。
25.【答案】 A,B
【解析】解:A.过氧化钠、过氧化钾与二氧化碳反应,镁可在二氧化碳中燃烧,则钾、钠、镁等活泼金
属着火时,不能用泡沫灭火器灭火,也不能使用干粉灭火器灭火,一般可用沙子扑灭,A符合题意;B.该实验要求开始时温度相同,然后改变温度,探究温度对反应速率的影响,应先分别水浴加热硫代硫酸
钠溶液、硫酸溶液到一定温度后再混合,若是先将两种溶液混合后再用水浴加热,随着热量的散失,测得
的反应速率偏低,B符合题意;
C.蒸馏时,应充分冷凝,应先停止加热,待装置冷却后,停止通水,防止温度过高而混入杂质,C不符合
题意;
D.配制溶液时,注意定容时不能使液面超过刻度线,应用胶头滴管滴加,D不符合题意。
故答案为:AB。
三、填空题
26.【答案】 用止水夹紧 1-2 处橡胶管,向分液漏斗中加一定量的水,然后打开分液漏斗的活塞向锥形瓶
加水,滴加一段时间后,液滴不再下滴,证明气密性良好;2Na+2CO =Na CO+CO;将 4 中固体加足量
2 2 3
水,有不溶黑色固体, 则生成有 C
【解析】①根据图示,检验装置1的气密性的方法为:用止水夹紧1-2处橡胶管,打开向分液漏斗活塞,
然后向分液漏斗加水至形成一段液柱,一段时间后液柱不再下降证明气密性良好,故答案为:用止水夹紧
1-2处橡胶管,打开向分液漏斗活塞,然后向分液漏斗加水至形成一段液柱,一段时间后液柱不再下降证
明气密性良好;
②由题意可知,装置4中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳
酸钠,装置6中有黑色沉淀,说明PdCl 溶液能被CO还原得到黑色的Pd,所以反应物为碳酸钠和CO,反
2
应的化学方程式为2Na+2CO =Na CO+CO,故答案为:2Na+2CO =Na CO+CO;
2 2 3 2 2 3
③根据C不溶于水分析,将装置4中固体加足量水,有不溶黑色固体,则生成物中有C,故答案为:将4
中固体加足量水,有不溶黑色固体,则生成物中有C。
四、实验探究题
27.【答案】 (1)M;蒸馏烧瓶
(2)排尽空气,防止红磷被氧气氧化以及生成的PCl 与空气中氧气和水反应
3
加热
(3)MnO + 4H+ + 2Cl﹣ ¿ Mn2+ + 2H O + Cl↑;防止生成PCl
2 ¿ 2 2 5
¿
(4)87.50%(87.5%也给分);偏小
(5)取10 mL 0.1 mol/L H PO 溶液于锥形瓶中,加入酚酞作指示剂,用0.1 mol/L NaOH进行滴定,若消
3 3
耗NaOH的体积近似等于20 mL,则说明HPO 为二元酸。
3 3【解析】Ⅰ(1)冷凝水下进上出,故冷却水从N口进入冷凝管,从M口出来,此处填“M”;仪器乙为带支
管的烧瓶,故为蒸馏烧瓶;
(2)由于红磷能与空气中氧气反应,需排尽装置中的空气,通入干燥的气体是为了防止产物PCl 与水反应,
3
故此处填:排尽空气,防止红磷被氧气氧化以及生成的PCl 与空气中氧气和水反应;
3
加热
(3)实验室可用MnO 与浓盐酸反应制取Cl , 对应离子方程式为:MnO + 4H+ + 2Cl﹣ ¿ Mn2+ +
2 2 2 ¿
¿
2HO + Cl↑;Cl 过量会将PCl 氧化为PCl , 故通入Cl 不能过快,此处填:防止生成PCl ;
2 2 2 3 5 2 5
Ⅱ(4)由题意知,该测量方法为返滴定,NaSO 标准液测出的是剩余的I , 与样品反应的I 等于I 的总
2 2 3 2 2 2
量减去剩余的I , 再依据关系式:PCl ~H PO ~I , 可求出PCl 的量,进而求出其质量分数,计算过
2 3 3 3 2 3
程如下:由关系式I~2Na SO , 得n(I , 余)=
2 2 2 3 2
n(Na S O ) 0.1 mol/L×12.00 mL×10-3L/mL
2 2 3 = =6×10-4mol ,则与样品反应的n(I)=n(I , 总)-
2 2 2 2
n(I , 余)=0.1 mol/L×20 mL×10-3 L/mL-6×10-4 mol=1.4×10-3 mol,由关系式PCl ~H PO ~I , 得
2 3 3 3 2
1.4×10-3mol×137.5 g/mol×20
n(PCl )= n(I )= 1.4×10-3 mol,故PCl 的质量分数= ×100%=87.50%
3 2 3 4.4 g
;若终点仰视读数,导致读数偏大,所计NaSO 溶液体积偏大,对应求出剩余的I 偏多,则与样品反应
2 2 3 2
的I 偏少,故导致PCl 质量分数偏小;
2 3
Ⅲ(5) 以酚酞为指示剂,用与HPO 浓度相等的氢氧化钠溶液进行滴定,滴定终点时消耗的碱的体积为酸
3 3
的两倍,即可得证,具体方案为:取10 mL 0.1 mol/L H PO 溶液于锥形瓶中,加入酚酞作指示剂,用0.1
3 3
mol/L NaOH进行滴定,若消耗NaOH的体积近似等于20 mL,则说明HPO 为二元酸。
3 3
28.【答案】 (1)除去过量的KMnO , 防止产品KIO 不纯;溶液由紫红色变为无色
4 3
(2)A,C,D
(3)溶液有蓝色变为无色,且半分钟内不恢复颜色;偏大
【解析】(1)流程中加入酸性高锰酸钾过量,过量的KMnO 将使获得的KIO 不纯,故需用乙醇除去,当观
4 3
察到观察到溶液颜色由紫红色变为无色时,说明KMnO 已经除尽,应立即停止滴入乙醇,故答案为:除
4
去过量的KMnO , 防止产品KIO 不纯;溶液由紫红色变为无色;
4 3
(2) A.由题干信息可知,KIO 的溶解度随温度升高而增大,故为得到较大的KIO 晶体颗粒,宜用冰水浴
3 3
快速冷却结晶,A正确;B.由题干信息可知,KIO 的溶解度随温度升高而增大,故不宜用热水洗涤,否则导致KIO 因溶解而造成
3 3
更多的损失,B不正确;
C.停止吸滤时,先拆下连接抽气泵和吸滤瓶的橡皮管,然后关闭水龙头,以防止倒吸,C正确;
D.由于KIO 不溶于酒精,故步骤II改为加适量乙醇即可析出KIO 晶体,再抽滤、洗涤、干燥,也可得
3 3
到产品晶体,D正确;
故答案为:ACD;
(3)本实验发生的反应有:5I-+ IO- +6H+=3I +3H O,I+2 S O2- =2I-+ S O2- ,用淀粉溶液作指示剂,三
3 2 2 2 2 3 4 6
次测量取平均值减小误差,故有 IO- ~3I ~6 S O2- ,据此可以算出KIO 的质量和纯度,据此分析解题:
3 2 2 3 3
①滴定前溶液中含有I 遇到淀粉呈蓝色,滴定终点使即I 完全反应,则溶液变为无色,故滴定终点的现象
2 2
是溶液有蓝色变为无色,且半分钟内不恢复颜色,故答案为:溶液有蓝色变为无色,且半分钟内不恢复颜
色;
②若滴定结束时仰视读数,将导致使用的硫代硫酸钠溶液的体积偏大,则KIO 的量偏大,故测定的结果偏
3
大,故答案为:偏大。
29.【答案】 (1)平衡圆底烧瓶A中压强;a
(2)馏出液澄清透明(或取少量馏出液滴入水中,无油珠存在);松开弹簧夹G,然后停止加热(或先把D
中的导气管从溶液中移出,再停止加热)
(3)分液漏斗
(4)干燥除水
(5)水浴
【解析】(1)水蒸气发生器A中压强过大,直玻璃管C中液面上升,所以直玻璃管C的作用是避免圆底烧
瓶A中压强过大。冷凝水从直形冷凝管的下口a进入,使馏分充分冷凝。故答案为:平衡圆底烧瓶A中压
强;a;
(2)馏出液澄清透明或取少量馏出液滴入水中,无油珠存在说明蒸馏结束。为了防止倒吸,实验停止时应打
开弹簧夹G,然后停止加热或者先将末端导气管从溶液中移出后再停止加热,故答案为:馏出液澄清透明
(或取少量馏出液滴入水中,无油珠存在);松开弹簧夹G,然后停止加热(或先把D中的导气管从溶液中移
出,再停止加热);
(3)萃取时用到的实验仪器是分液漏斗。故答案为:分液漏斗;
(4)无水硫酸钠作为干燥剂除去萃取液中的水。故答案为:干燥除水;(5)提纯柠檬烯时,先将萃取剂二氯甲烷蒸岀,三氯甲烷的沸点为39.8℃,釆用水浴加热蒸馏。故答案为:
水浴;
30.【答案】 (1)B;3Cu+8H++NO-=3Cu2++2NO↑+4HO;f→g→c→ b→d→e→j→h
3 2
(2)排除装置内空气的干扰,可以随开随用,随关随停;K;排干净三颈瓶中的空气,防NO和NOCl变
3
质;2NOCl+HO=2HCl+NO↑+NO ↑;NaOH
2 2
【解析】(1)①实验室制备NO,可用稀硝酸与铜在常温下反应,选用B装置制取,反应的离子方程式为
3Cu+8H++NO-=3Cu2++2NO↑+4HO;
3 2
②用浓盐酸和二氧化锰在加热条件下制备氯气,制取的氯气中含有杂质HCl及水蒸气,先用F除去HCl杂
质,再用D干燥氯气,然后用向上排空气法收集,最后连接G,可防止氯气污染环境,洗气时,气体应从
长导管进,则连接顺序为:a→f→g→c→b→d→e→j→h;
(2)①实验室也可用X装置制备NO,X装置的优点为排除装置内空气的干扰,可以随开随用,随关随停;
②检验装置气密性并装入药品,打开K , 然后再打开K , 通入一段时间气体,其目的为排干净三颈
2 3
瓶中的空气,防NO和NOCl变质;
③若无装置Y,空气中的水与NOCl反应,NOCl可能发生反应的化学方程式为
2NOCl+HO=2HCl+NO↑+NO ↑
2 2
④尾气含有氯气、HCl以及二氧化氮,这些气体都可以与NaOH反应,产生无害物质,所以可用氢氧化钠
溶液吸收。