文档内容
专题 13 工艺流程综合题
(本卷共10小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
一、非选择题:本题共10个小题,共100分。
1.北京冬奥会奖牌中铜牌的主要成分为铜和锌。已知一种从硫中毒而失活的废甲醇催化剂(主要成分为
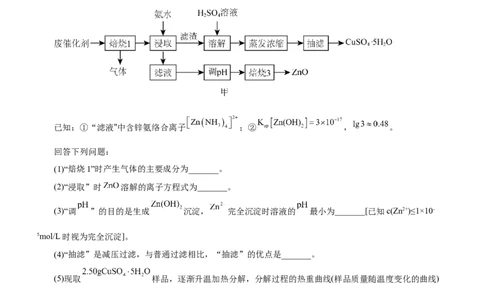
等)中回收铜和锌的工艺流程如图甲所示。
已知:①“滤液"中含锌氨络合离子 ;② , 。
回答下列问题:
(1)“焙烧1”时产生气体的主要成分为_______。
(2)“浸取”时 溶解的离子方程式为_______。
(3)“调 ”的目的是生成 沉淀, 完全沉淀时溶液的 最小为_______[已知c(Zn2+)≤1×10-
5mol/L时视为完全沉淀]。
(4)“抽滤”是减压过滤,与普通过滤相比,“抽滤”的优点是_______。
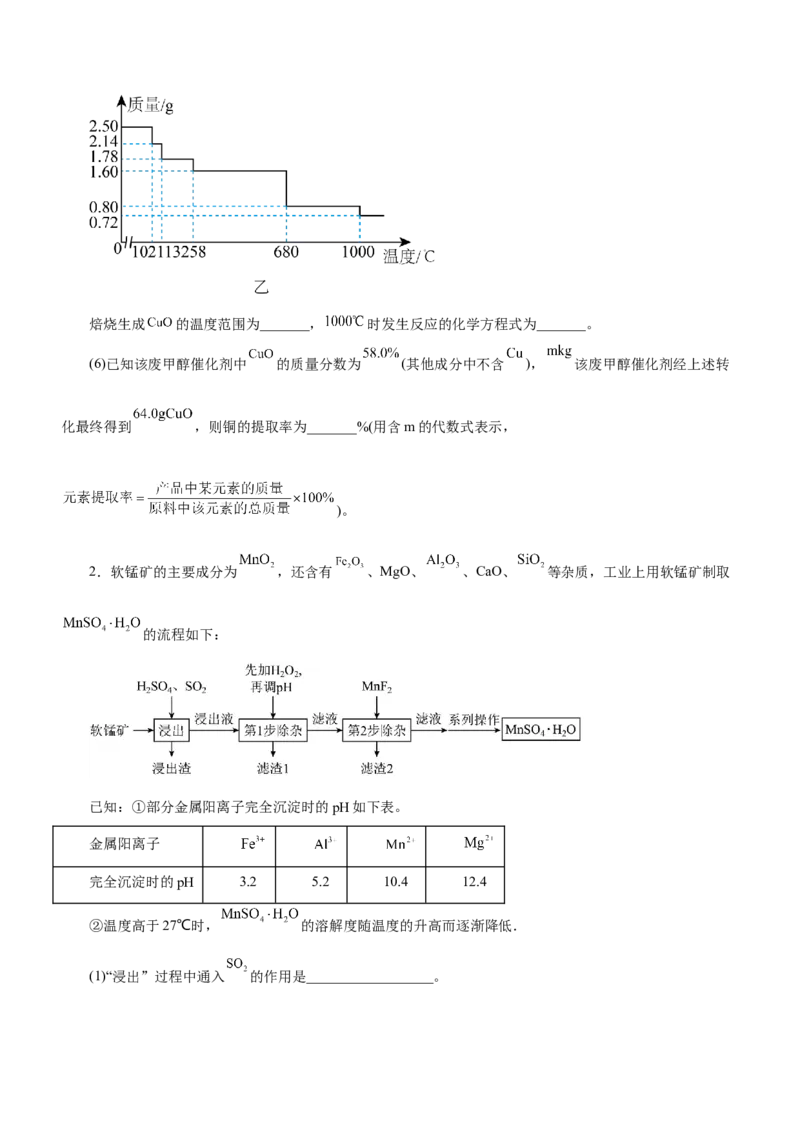
(5)现取 样品,逐渐升温加热分解,分解过程的热重曲线(样品质量随温度变化的曲线)
如图乙所示。焙烧生成 的温度范围为_______, 时发生反应的化学方程式为_______。
(6)已知该废甲醇催化剂中 的质量分数为 (其他成分中不含 ), 该废甲醇催化剂经上述转
化最终得到 ,则铜的提取率为_______%(用含m的代数式表示,
)。
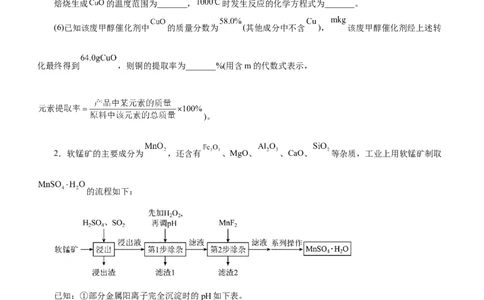
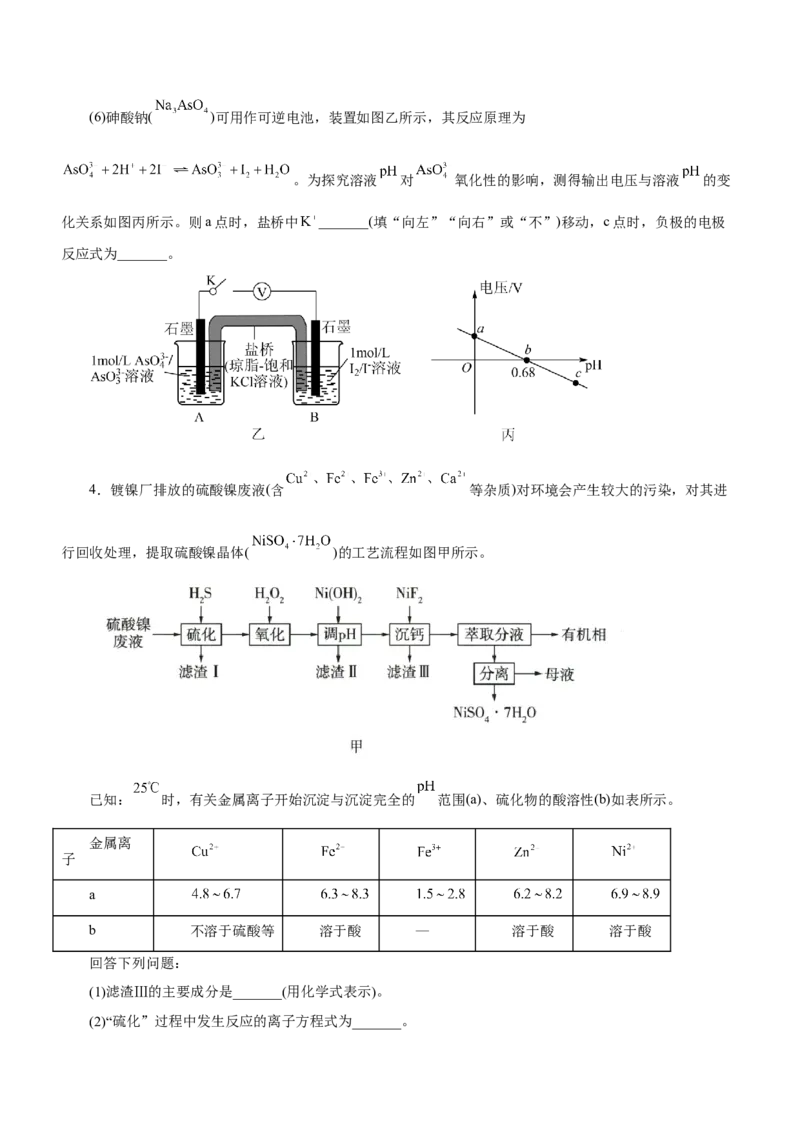
2.软锰矿的主要成分为 ,还含有 、MgO、 、CaO、 等杂质,工业上用软锰矿制取
的流程如下:
已知:①部分金属阳离子完全沉淀时的pH如下表。
金属阳离子
完全沉淀时的pH 3.2 5.2 10.4 12.4
②温度高于27℃时, 的溶解度随温度的升高而逐渐降低.
(1)“浸出”过程中通入 的作用是__________________。(2)第1步除杂中加入 的目的是__________________(用离子方程式表示)。.
(3)第1步除杂中需要调整溶液pH的范围是______到______,调pH时可选择的试剂为______(填字母)。
a.氨水 b. c.CaO d.MgO
(4)第2步除杂,主要是将 、 转化为相应氟化物沉淀除去,写出 除去 的离子方程式:
________________________,该反应的平衡常数为__________________。
(已知: 的 ; 的 ; 的 )
(5)“系列操作”中的具体操作有__________________,经干燥得到 。
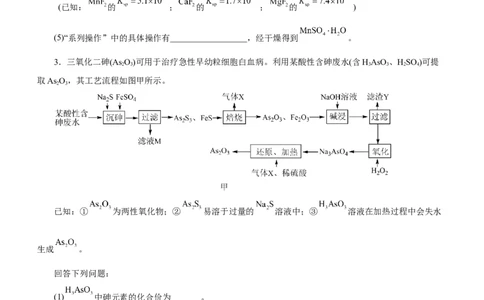
3.三氧化二砷(As O)可用于治疗急性早幼粒细胞白血病。利用某酸性含砷废水(含HAsO 、HSO )可提
2 3 3 3 2 4
取As O,其工艺流程如图甲所示。
2 3
已知:① 为两性氧化物;② 易溶于过量的 溶液中;③ 溶液在加热过程中会失水
生成 。
回答下列问题:
(1) 中砷元素的化合价为_______。
(2)“焙烧”操作中, 参与反应的化学方程式为_______。
(3)“碱浸”的目的是_______,滤渣Y的主要成分是_______(填化学式)。
(4)“氧化”操作的目的是_______(用离子方程式表示)。
(5)“还原、加热”过程中制得 ,则消耗标准状况下气体X的体积为_______L。(6)砷酸钠( )可用作可逆电池,装置如图乙所示,其反应原理为
。为探究溶液 对 氧化性的影响,测得输出电压与溶液 的变
化关系如图丙所示。则a点时,盐桥中 _______(填“向左”“向右”或“不”)移动,c点时,负极的电极
反应式为_______。
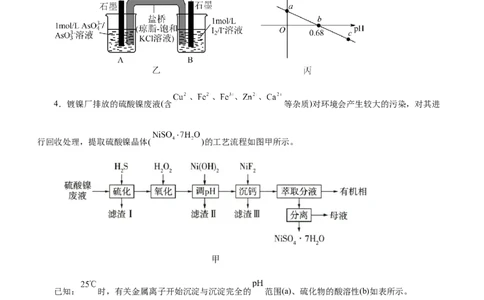
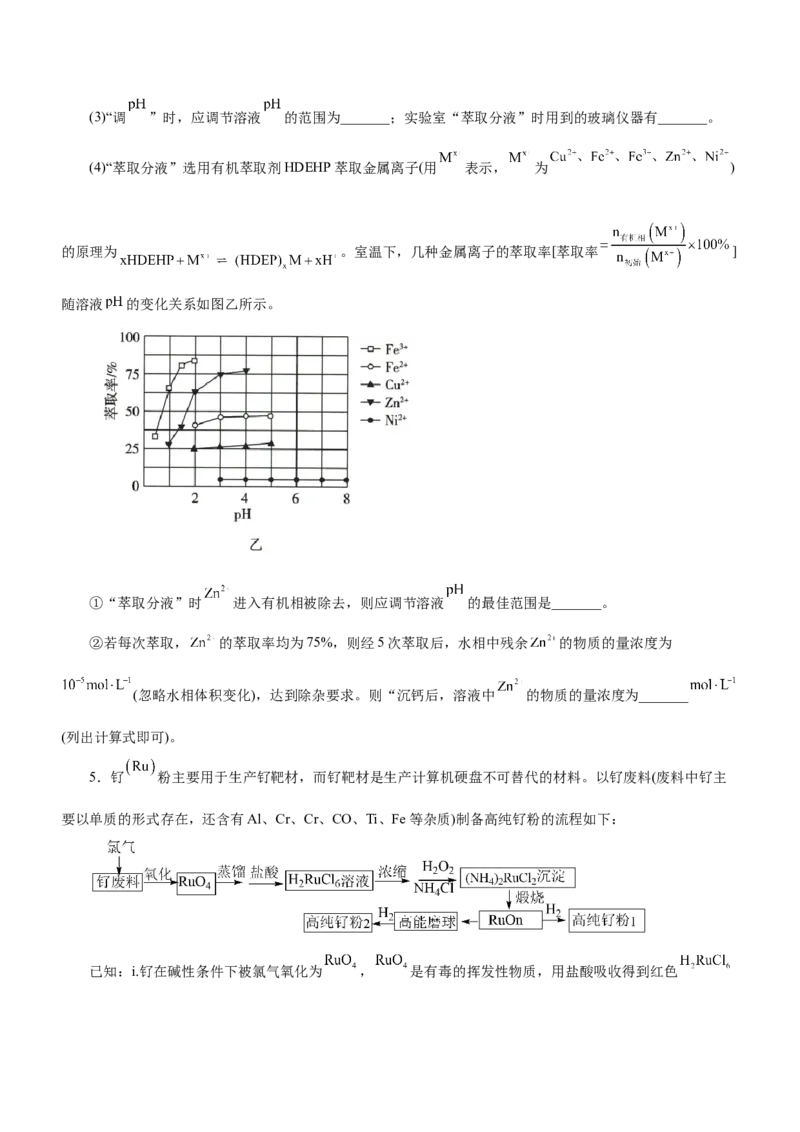
4.镀镍厂排放的硫酸镍废液(含 等杂质)对环境会产生较大的污染,对其进
行回收处理,提取硫酸镍晶体( )的工艺流程如图甲所示。
已知: 时,有关金属离子开始沉淀与沉淀完全的 范围(a)、硫化物的酸溶性(b)如表所示。
金属离
子
a
b 不溶于硫酸等 溶于酸 — 溶于酸 溶于酸
回答下列问题:
(1)滤渣Ⅲ的主要成分是_______(用化学式表示)。
(2)“硫化”过程中发生反应的离子方程式为_______。(3)“调 ”时,应调节溶液 的范围为_______;实验室“萃取分液”时用到的玻璃仪器有_______。
(4)“萃取分液”选用有机萃取剂HDEHP萃取金属离子(用 表示, 为 )
的原理为 。室温下,几种金属离子的萃取率[萃取率 ]
随溶液 的变化关系如图乙所示。
①“萃取分液”时 进入有机相被除去,则应调节溶液 的最佳范围是_______。
②若每次萃取, 的萃取率均为75%,则经5次萃取后,水相中残余 的物质的量浓度为
(忽略水相体积变化),达到除杂要求。则“沉钙后,溶液中 的物质的量浓度为_______
(列出计算式即可)。
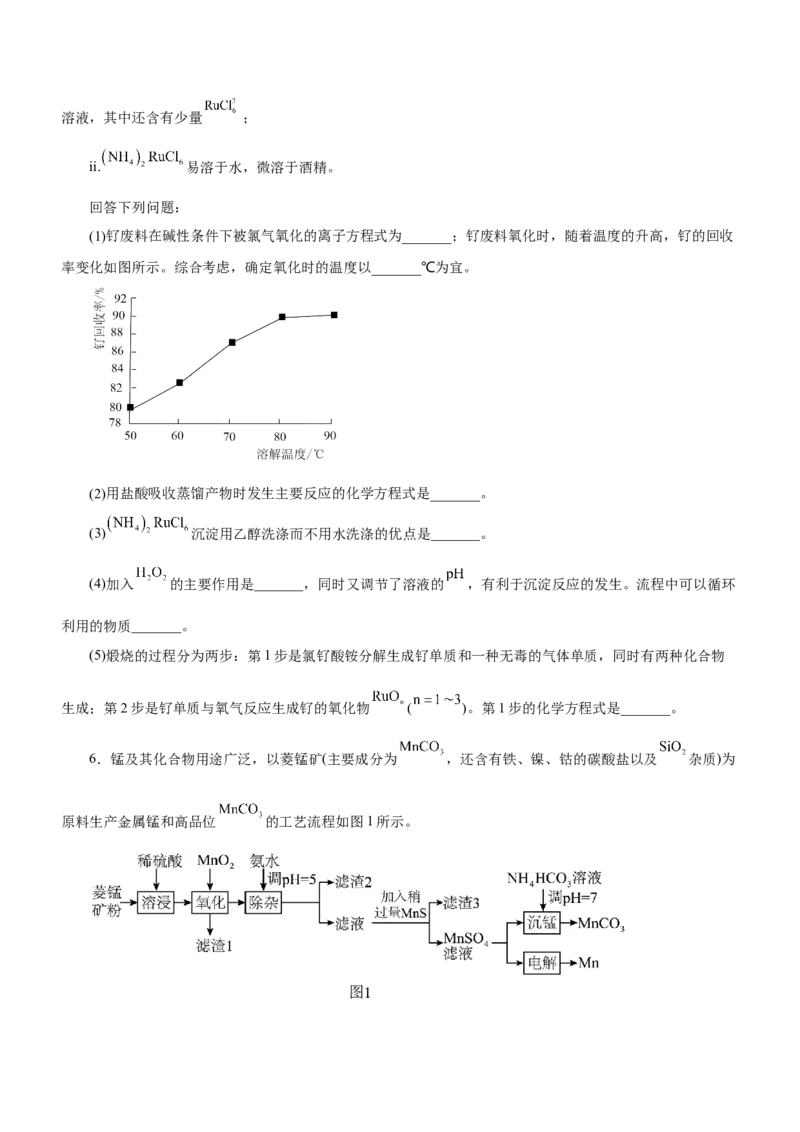
5.钌 粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以钌废料(废料中钌主
要以单质的形式存在,还含有Al、Cr、Cr、CO、Ti、Fe等杂质)制备高纯钌粉的流程如下:
已知:i.钌在碱性条件下被氯气氧化为 , 是有毒的挥发性物质,用盐酸吸收得到红色溶液,其中还含有少量 ;
ii. 易溶于水,微溶于酒精。
回答下列问题:
(1)钌废料在碱性条件下被氯气氧化的离子方程式为_______;钌废料氧化时,随着温度的升高,钌的回收
率变化如图所示。综合考虑,确定氧化时的温度以_______℃为宜。
(2)用盐酸吸收蒸馏产物时发生主要反应的化学方程式是_______。
(3) 沉淀用乙醇洗涤而不用水洗涤的优点是_______。
(4)加入 的主要作用是_______,同时又调节了溶液的 ,有利于沉淀反应的发生。流程中可以循环
利用的物质_______。
(5)煅烧的过程分为两步:第1步是氯钌酸铵分解生成钌单质和一种无毒的气体单质,同时有两种化合物
生成;第2步是钌单质与氧气反应生成钌的氧化物 ( )。第1步的化学方程式是_______。
6.锰及其化合物用途广泛,以菱锰矿(主要成分为 ,还含有铁、镍、钴的碳酸盐以及 杂质)为
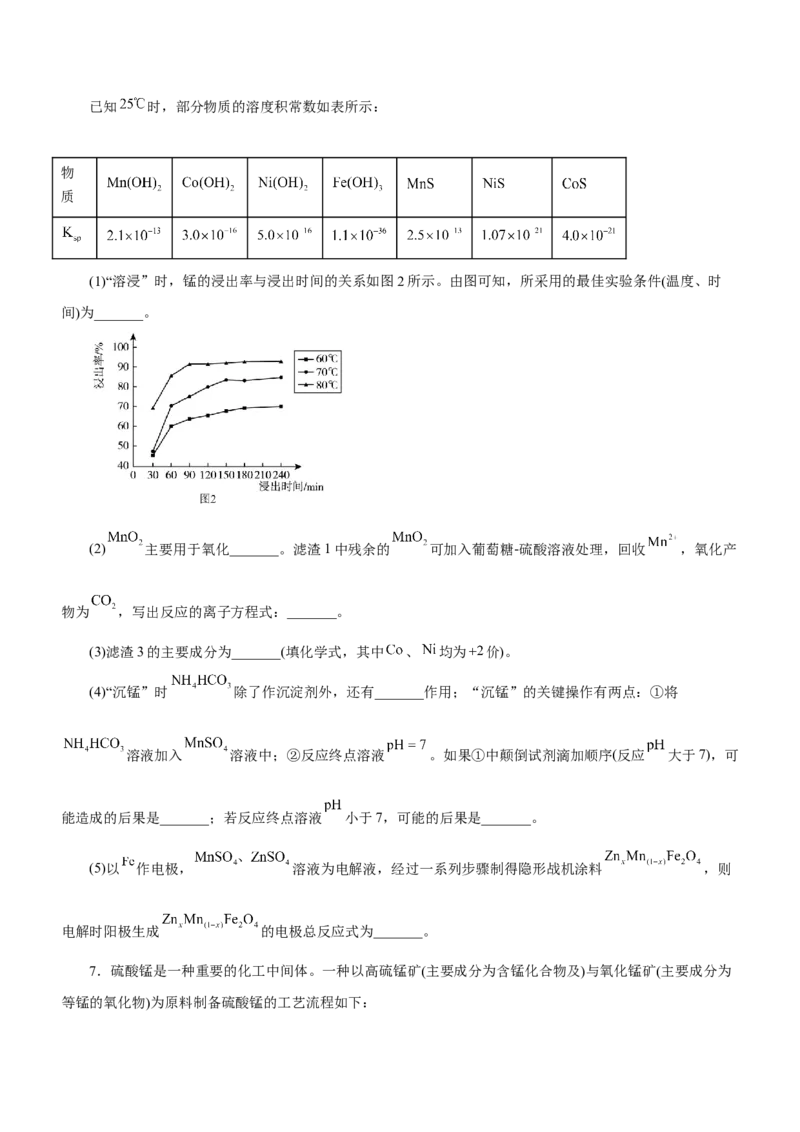
原料生产金属锰和高品位 的工艺流程如图1所示。已知 时,部分物质的溶度积常数如表所示:
物
质
(1)“溶浸”时,锰的浸出率与浸出时间的关系如图2所示。由图可知,所采用的最佳实验条件(温度、时
间)为_______。
(2) 主要用于氧化_______。滤渣1中残余的 可加入葡萄糖-硫酸溶液处理,回收 ,氧化产
物为 ,写出反应的离子方程式:_______。
(3)滤渣3的主要成分为_______(填化学式,其中 、 均为 价)。
(4)“沉锰”时 除了作沉淀剂外,还有_______作用;“沉锰”的关键操作有两点:①将
溶液加入 溶液中;②反应终点溶液 。如果①中颠倒试剂滴加顺序(反应 大于7),可
能造成的后果是_______;若反应终点溶液 小于7,可能的后果是_______。
(5)以 作电极, 溶液为电解液,经过一系列步骤制得隐形战机涂料 ,则
电解时阳极生成 的电极总反应式为_______。
7.硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰化合物及)与氧化锰矿(主要成分为
等锰的氧化物)为原料制备硫酸锰的工艺流程如下:已知:①“混合焙烧”后烧渣含 及少量 。
②金属离子在水溶液中沉淀的 范围如下表所示( ):
物质
开始沉淀的
1.9 7.6 7.3 3.0
完全沉淀的
3.2 9.6 9.3 5.2
③离子浓度 时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______。
(2)若试剂a为 ,则氧化步骤发生反应的离子方程式为_______,若省略“氧化”步骤,造成的影响
是_______。
(3)“中和除杂”时,应控制溶液的 范围是_______。
(4)“氟化除杂”后,溶液中 浓度为 。则溶液中 _______[已知:
; ]。
(5)“碳化结晶”时发生反应的离子方程式为_______。
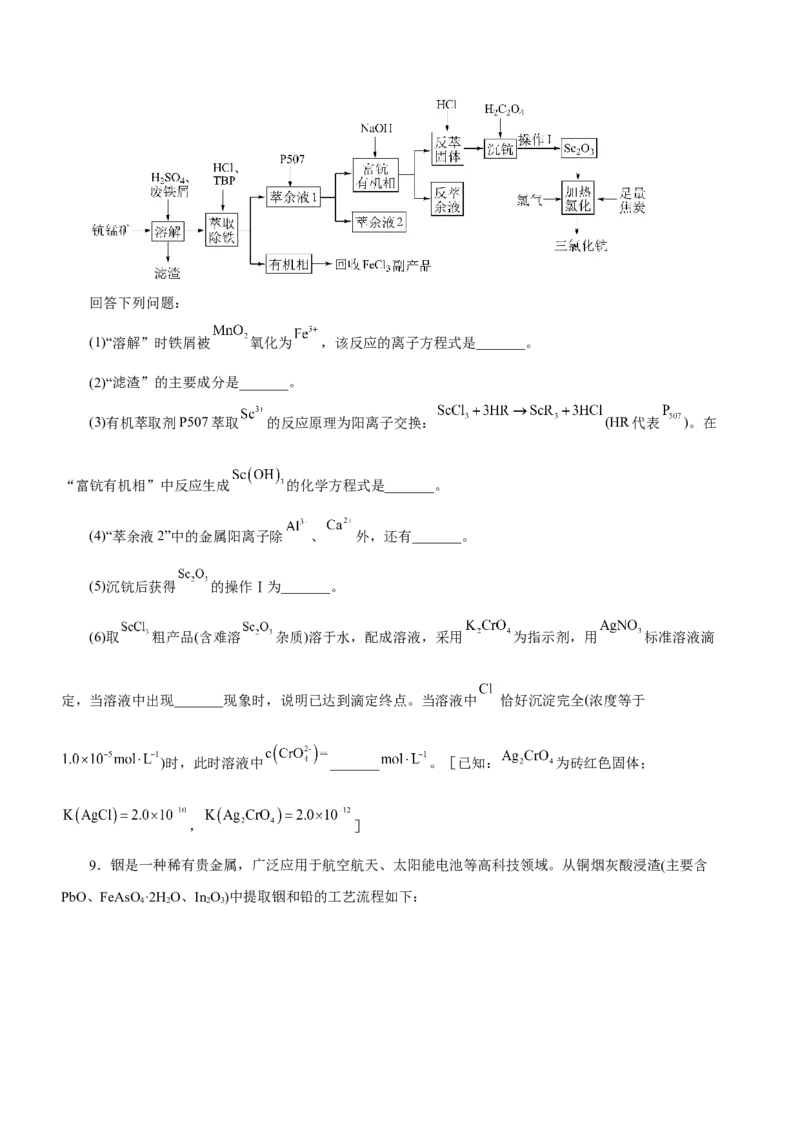
8.氧化钪(Sc O)是一种稀土氧化物,广泛应用于航天、激光、导弹等尖端科学领域。以钪锰矿石(主要含
2 3
MnO 、SiO 及少量Sc O、Al O、CaO、FeO)为原料制备Sc O 和三氯化钪(ScCl )的工艺流程如图,其中TBP
2 2 2 3 2 3 2 3 3
和P507均为有机萃取剂。回答下列问题:
(1)“溶解”时铁屑被 氧化为 ,该反应的离子方程式是_______。
(2)“滤渣”的主要成分是_______。
(3)有机萃取剂P507萃取 的反应原理为阳离子交换: (HR代表 )。在
“富钪有机相”中反应生成 的化学方程式是_______。
(4)“萃余液2”中的金属阳离子除 、 外,还有_______。
(5)沉钪后获得 的操作Ⅰ为_______。
(6)取 粗产品(含难溶 杂质)溶于水,配成溶液,采用 为指示剂,用 标准溶液滴
定,当溶液中出现_______现象时,说明已达到滴定终点。当溶液中 恰好沉淀完全(浓度等于
)时,此时溶液中 _______ 。[已知: 为砖红色固体;
, ]
9.铟是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从铜烟灰酸浸渣(主要含
PbO、FeAsO ·2H O、InO)中提取铟和铅的工艺流程如下:
4 2 2 3已知:①焙烧后金属元素均以硫酸盐的形式存在;
②In(OH) 性质与Al(OH) 类似。
3 3
回答下列问题:
(1)FeAsO ·2H O中铁元素化合价为_______。
4 2
(2)生成PbO粗品的化学反应方程式为_______。
(3)PbO在NaOH溶液中溶解度曲线如图所示,PbO粗品中的杂质难溶于NaOH溶液。结合溶解度曲线,
简述提纯PbO粗品的操作_______。
(4)“还原铁”反应的离子方程式为________
(5)“萃取除铁”中,发现当溶液pH>1.5后,钢萃取率随pH的升高而下降,原因是_______
(6)为测定PbO产品的纯度,探究小组同学准确称取PbO1.161g,加入稀硝酸使其完全溶解,再加入蒸馏
水配制成50.00mL溶液:冷却至25℃,用0.100mol·L-1HSO 滴定该溶液,滴定曲线如图所示。
2 4已知: ;a点的坐标为(50,3.8)
①25℃,PbSO 的K =_______。
4 sp
②PbO产品的纯度为_______。
10.碳酸锶( )难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量
等)制备高纯碳酸锶的工艺流程如图所示。
已知:I. 为两性氢氧化物;
II.常温下,各物质的溶度积常数如表所示。
化合物
近似
值
回答下列问题:
(1)气体A的电子式为_______。
(2)“沉钡、铅”时,溶液 过低会导致 的利用率降低,原因是_______(结合化学用语解释);
“还原”时发生反应的离子方程式为_______。
(3)滤渣1的主要成分为_______(填化学式)。(4)用氨水和 分步调节溶液 ,而不是直接调节溶液的 的原因为_______。
(5)“调 ”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为_______。
(6)已知:碳酸的电离常数 、 ,则“碳化”时,反应
的平衡常数 ____(结果保留3位有效数字)。
(7)“系列操作”中,将结晶过滤后,不经洗涤,直接以 热风烘干,便可得到高纯 ,故“系列
操作”烘干过程中除蒸发水外,还能够除去 中的微量可溶性杂质,微量杂质除 外还可能为
_______(填化学式)。