文档内容
专题 15 化学实验基础
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.提倡绿色化学是指从源头上杜绝污染。某同学设计利用铁屑制备硝酸铁晶体的合理方案:先在空
气中灼烧铁屑,后用稀硝酸溶解,再经过蒸发浓缩、降温结晶、过滤可得硝酸铁晶体。上述方案中,不需
用到的实验仪器为( )
A. B. C. D.
【答案】C
【解析】A项,溶解需要用到烧杯,选项A为烧杯,选项A不符合;B项,灼烧需要用到坩埚,选项
B为坩埚,选项B不符合;C项,整个实验方案中无需用冷凝管,选项C符合;D项,过滤需要用到漏斗,
选项D为漏斗,选项D不符合;故选C。
2.下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是( )
选项 实验器材 相应实验
A 试管、铁架台、导管 乙酸乙酯的制备
锥形瓶、漏斗、双孔塞、导管、带火星的木条、
B 检验MnO 对HO 分解速率的影响
药匙 2 2 2
C 500 mL容量瓶、烧杯、玻璃棒、天平 配制500 mL 1.00 mol/L NaCl溶液
D 三脚架、坩埚、酒精灯、坩埚钳 钠在空气中燃烧
【答案】B
【解析】A项,制备乙酸乙酯需要加热,缺少酒精灯,不能完成实验,故错误;B项,MnO 作催化剂,
2
加速HO 的分解,所给器材能够完成实验,故正确;C项,缺少胶头滴管,故错误;D项,缺少泥三角,
2 2
故错误。
3.下列有关实验基本操作不能达到目的的是( )
A.配制10%CuSO 溶液:称取5. 0 g CuSO •5H O,加入27.0 g水,搅拌溶解
4 4 2
B.在实验室中,采用加热氯酸钾和二氧化锰混合物的方法制取氧气。我们可以用溶解、过滤、洗涤、
干燥的方法从反应产物中得到二氧化锰
C.可以用酒精灯、玻璃棒、坩埚、泥三角这些仪器从食盐水中获取NaCl晶体D.配制100 mL 1 mol·Lˉ1的NaCO 溶液可将固体放于天平左盘称其质量
2 3
【答案】C
【解析】A项,5. 0gCuSO •5H O中所含CuSO 的质量为: ,,加入27.0g水,所得
4 2 4
溶液的溶质质量分数= ,故A正确;B项,氯酸钾和二氧化锰混合加热后,氯酸
钾分解成氯化钾和氧气,二氧化锰不反应且不溶于水,因此将反应后混合物溶解、过滤、洗涤、干燥后可
得到二氧化锰,故B正确;C项,从食盐水中获取NaCl晶体需要通过蒸发结晶的方法,蒸发需用到蒸发
皿,故C错误;D项,托盘天平的使用“左物右码”,所成药品在左盘中称量,故D正确;故选C。
4.下列各组混合物的分离或提纯方法不正确的是( )
A.用过滤法分离Fe(OH) 胶体和FeCl 溶液的混合物
3 3
B.用结晶法提纯NaCl和KNO 的混合物中的KNO
3 3
C.用蒸馏法分离乙醇和苯酚的混合物
D.除去FeCl 溶液中的少量FeCl :加入足量铁屑,充分反应后,过滤
2 3
【答案】A
【解析】胶体不能透过半透膜,能透过滤纸,不能用过滤的方法分离Fe(OH) 胶体和FeCl 溶液的混合
3 3
物。
5.下列有关实验说法正确的是( )
A.易燃物钠、钾、白磷未用完,不能放回原试剂瓶
B.酸碱中和滴定实验中,滴至接近终点时,需改为半滴滴加
C.定容时仰视刻度线导致所配的溶液浓度偏高
D.向 溶液中滴加氨水至沉淀溶解得深蓝色溶液,再加入乙醇无明显变化
【答案】B
【解析】A项,钠、钾与水反应生成氢气具有可燃性,白磷易自燃,则未用完需放回原瓶,故 A错误;
B项,滴至接近终点时,避免滴加液体过多,需改为半滴滴加,操作合理,故 B正确;C项,定容时仰视
刻度线,会使溶液的体积偏大,溶液的浓度偏低,故C错误;D项,CuSO 溶液中滴加氨水至沉淀溶解得
4
深蓝色溶液,生成硫酸四氨合铜,再加入乙醇,析出深蓝色的晶体,故D错误;故选B。
6.下列说法不正确的是( )A.在酸性KCr O 溶液中,若加入 ,溶液由橙色变成黄色;若加入NaSO ,溶液则变成绿色
2 2 7 2 3
B.用KCr O 标准液润洗酸式滴定管后,应将润洗液从酸式滴定管下口放出
2 2 7
C.酸或碱对酯的水解都有催化作用,在其他条件相同时,等量的酯在酸或碱催化下,水解效果差别
不大
D.为增强高锰酸钾的氧化性常对其进行酸化,酸化时常使用稀硫酸而不采用盐酸或硝酸
【答案】C
【解析】A项,在水溶液中橙红色的Cr O2-与黄色的CrO2-有下列平衡关系:Cr O2-+H O
2 7 4 2 7 2
2CrO2-+2H+,KCr O 溶液呈橙色,加入少量NaOH固体,中和氢离子,氢离子浓度降低,平衡向右移动,
4 2 2 7
溶液呈黄色;若将NaOH溶液改成NaSO 溶液,KCr O 与NaSO 溶液发生氧化还原反应生成Cr3+,溶液
2 3 2 2 7 2 3
变成绿色,A正确;B项,用 KCr O 标准液润洗酸式滴定管后,应将润洗液从酸式滴定管下口放出,B
2 2 7
正确;C项,酸或碱对酯的水解都有催化作用,在其他条件相同时,等量的酯在酸催化下,生成酸和醇,
为可逆反应,而等量的酯在碱催化下,生成盐和醇,为不可逆反应,水解效果更彻底,C错误;D项,为
增强高锰酸钾的氧化性常对其进行酸化,酸化时常使用稳定的稀硫酸而不采用具有还原性的盐酸或具有氧
化性的硝酸,D正确;故选C。
7.下列有关实验基本操作不能达到目的的是( )
A.配制10%CuSO 溶液:称取5. 0 g CuSO •5H O,加入27.0 g水,搅拌溶解
4 4 2
B.在实验室中,采用加热氯酸钾和二氧化锰混合物的方法制取氧气。我们可以用溶解、过滤、洗涤、
干燥的方法从反应产物中得到二氧化锰
C.可以用酒精灯、玻璃棒、坩埚、泥三角这些仪器从食盐水中获取NaCl晶体
D.配制100 mL 1 mol·Lˉ1的NaCO 溶液可将固体放于天平左盘称其质量
2 3
【答案】C
【解析】A项,5. 0gCuSO •5H O中所含CuSO 的质量为: ,,加入27.0g水,所得
4 2 4
溶液的溶质质量分数= ,故A正确;B项,氯酸钾和二氧化锰混合加热后,氯酸
钾分解成氯化钾和氧气,二氧化锰不反应且不溶于水,因此将反应后混合物溶解、过滤、洗涤、干燥后可
得到二氧化锰,故B正确;C项,从食盐水中获取NaCl晶体需要通过蒸发结晶的方法,蒸发需用到蒸发
皿,故C错误;D项,托盘天平的使用“左物右码”,所成药品在左盘中称量,故D正确;故选C。
8.下列图示对应的操作规范的是( )A.称量 B.过滤 C.将剩余钠放回试剂瓶 D.转移溶液
【答案】C
【解析】A项,称量时应该左物右码,氢氧化钠具有腐蚀性,应该在小烧杯中称量,操作不规范,故
A不选;B项,过滤时需要用玻璃棒引流,故B不选;C项,钠的性质非常活泼,随意丢弃易发生事故,
实验中剩余的钠,需要放回试剂瓶,操作规范,故C选;D项,转移溶液时玻璃棒下端应该靠在容量瓶颈
部刻度线以下,操作不规范,故D不选;故选C。
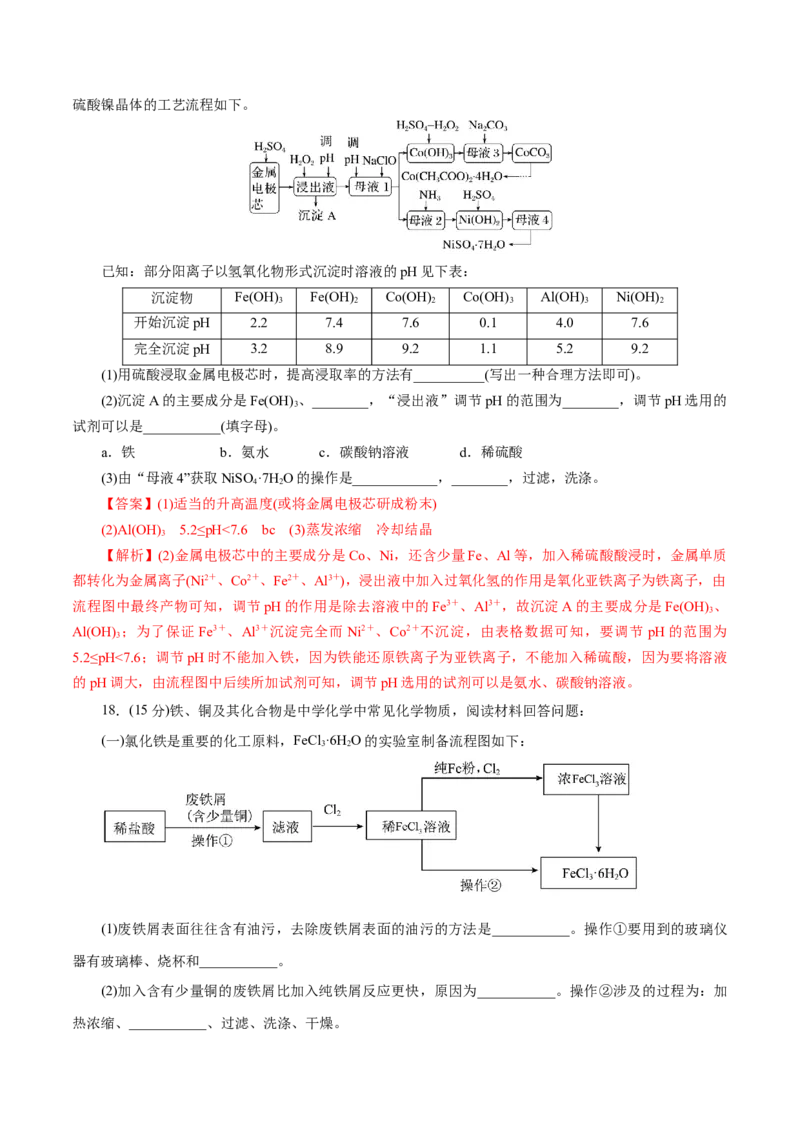
9.利用下列装置和操作不能达到实验目的的是( )
A.从含碘CCl 溶液中
4 B.萃取操作过程中的 C.定量测定化学反应 D.比较KMnO 、
提取碘和回收CCl 溶 4
4 放气 速率 Cl、S的氧化性
剂 2
【答案】C
【解析】I 和CCl 互溶但沸点差距较大,所以可以根据两者沸点的差别进行蒸馏来分离,A项正确;
2 4
振荡过程中产生大量气泡,增加了分液漏斗内的压强,所以为了防止活塞被顶出,要中途放气,B项正确;
要用分液漏斗,气体会从长颈漏斗管口逸出,缺少秒表,C项错误;高锰酸钾能氧化浓盐酸生成氯气,反
应中高锰酸钾作氧化剂,氧化产物是氯气,所以高锰酸钾的氧化性大于氯气;氯气和硫离子反应生成硫单
质,氯气是氧化剂,硫是氧化产物,所以氯气的氧化性大于硫,由此得出高锰酸钾的氧化性大于氯气,氯
气的氧化性大于硫,D项正确。
10.下列除杂方案错误的是( )
选项 被提纯的物质 杂质 除杂试剂 除杂方法
A CO(g) CO(g) NaOH 溶液、浓 HSO 洗气
2 2 4
B NH Cl(aq) Fe3+(aq) NaOH溶液 过滤
4
C Cl(g) HCl(g) 饱和食盐水、浓HSO 洗气
2 2 4
D NaCO(s) NaHCO (s) — 灼烧
2 3 3
【答案】B
【解析】A项,CO 与NaOH溶液反应生成NaCO ,而CO与NaOH溶液不反应,A正确;B项,
2 2 3NaOH溶液不仅与Fe3+反应也会与NH发生反应,B错误;C项,HCl极易溶于水,而Cl 在饱和食盐水中
2
溶解度较小,C正确;D项,加热灼烧可以使NaHCO 固体分解,且生成NaCO,D正确。
3 2 3
11.实验室以磷石膏[主要成分为CaSO,含少量SiO、Ca (PO ) 等杂质]为原料制备轻质CaCO ,流程
4 2 3 4 2 3
如下图。下列说法错误的是( )
A.“转化”中,包含反应CaSO+ CO===SO+ CaCO
4 3
B.“滤液”的pH约为6.5,阴离子主要是SO和CO
C.“高温煅烧”需要的仪器有酒精喷灯、坩埚、坩埚钳、泥三角、三脚架等
D.“浸取”时,适当升高温度有利于Ca2+的浸出
【答案】B
【解析】A项,“转化”时,通入二氧化碳,生成碳酸根离子,将硫酸钙转化为碳酸钙,A项正确;B
项,pH约为6.5,呈酸性,碳酸根不可能大量存在,B项错误;C项,“高温煅烧”需要的仪器有酒精喷
灯、坩埚、坩埚钳、泥三角、三脚架等,C项正确;D项,氯化钙的溶解度随着温度的升高而增大,所以
适当升高温度有利于Ca2+的浸出,D项正确;故选B。
12.某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl ·2H O的工艺流
2 2
程如下:
下列说法正确的是( )
A.焙烧后的废气能使酸性高锰酸钾溶液褪色
B.通氯气的主要目的是提高CuCl ·2H O的产率
2 2
C.调节pH选用的试剂可以是NaOH溶液
D.CuCl ·2H O直接加热可制得CuCl 固体
2 2 2
【答案】A
【解析】焙烧时发生反应:2CuS+3O=====2CuO+2SO ,生成的SO 废气具有还原性,能使酸性高
2 2 2
锰酸钾溶液褪色,A项正确;通入氯气的主要目的是将溶液中的二价铁全部氧化成三价铁,便于后续调节
pH除去,B项错误;调节pH时用NaOH溶液会引入NaCl杂质,可用CuO等进行调节,C项错误;将CuCl ·2H O直接加热脱水,CuCl 水解生成Cu(OH) 和HCl,HCl挥发促进 CuCl 的水解,最终得不到
2 2 2 2 2
CuCl 固体,D项错误。
2
13.下列方案设计、现象和结论都正确的是( )
实验目的 实验方案 现象和结论
溶液先变红后褪色,说明SO 能与水生成酸性物
A 检验SO 的性质 SO 通入石蕊试液中 2
2 2 质,并具有漂白性
探究不同价态硫元素 向NaS与NaSO 的 溶液变浑浊,证明NaS与NaSO 发生了氧化还原
B 2 2 3 2 2 3
的转化 混合液中加入硝酸 反应
检验某苯酚溶液中是 将溶液加到饱和碳酸
C 无气泡产生,证明不含苯甲酸
否混有少量苯甲酸 钠溶液中
向鸡蛋清溶液中滴加 先产生白色沉淀,加热后沉淀变黄色,说明鸡蛋清
D 检验蛋白质的性质
适量浓硝酸并加热 溶液中含有蛋白质
【答案】D
【解析】A项,二氧化硫具有漂白性,但不能使酸碱指示剂石蕊试液漂白褪色,故A错误;B项,硝
酸具有强氧化性,也能与硫化钠溶液发生氧化还原反应生成硫沉淀,则溶液变混浊不能说明硫化钠溶液和
亚硫酸钠溶液酸性条件下发生了氧化还原反应,故B错误;C项,将含有少量苯甲酸的苯酚溶液加入碳酸
钠溶液中,苯甲酸溶液与过量碳酸钠溶液反应生成苯甲酸钠和碳酸氢钠,无二氧化碳气体生成,则无气泡
产生不能证明不含苯甲酸,故C错误;D项,蛋白质能与浓硝酸发生显色反应变为黄色,则向鸡蛋清溶液
中滴加适量浓硝酸并加热,先产生白色沉淀,加热后沉淀变黄色说明鸡蛋清溶液中含有蛋白质,故D正确;
故选D。
14.下列实验方案、现象和结论都正确的是( )
实验方案 现象 结论
A 向某黄色溶液中加入淀粉KI溶液 溶液呈蓝色 溶液中含Br
2
将足量SO 通入NaCO 溶液中逸出的气体 酸性KMnO 溶液颜
2 2 3 4
B 通入足量的酸性KMnO 溶液,再通入澄 色变浅,澄清石灰水 K (H SO )>K (H CO)
4 a1 2 3 a2 2 3
清石灰水中 变浑浊
向NaCrO 溶液中加硝酸银溶液至不再产
2 4 红棕色沉淀逐渐转化
C 生红棕色沉淀(Ag CrO)时,滴加稀NaCl K (AgCl) <K (Ag CrO)
2 4 为白色 sp sp 2 4
溶液
向少量蒸馏水中逐渐加入苯酚晶体并振荡 加热后可得到澄清溶 较高温度,苯酚能与水互溶;
D 至浑浊,静置片刻后,将试管放在热水浴 液,冷却后溶液变浑 温度降低,苯酚溶解度降低且
中,片刻后取出,冷却静置。 浊, 析出晶体【答案】B
【解析】A项,Fe3+在溶液中也呈黄色,Fe3+也能将I-氧化为I,所以不能确定该溶液中一定含有Br ,
2 2
故A错误;B项,将足量SO 通入NaCO 溶液中逸出的气体是二氧化碳,二氧化碳通入足量的酸性
2 2 3
KMnO 溶液除掉SO ,再通入澄清石灰水中,澄清石灰水变浑浊,则说明SO 与NaCO 溶液反应生成了二
4 2 2 2 3
氧化碳,说明亚硫酸酸性>碳酸酸性,即K (H SO )>K (H CO),故B正确;C项,Ag CrO 与AgCl的沉
a1 2 3 a1 2 3 2 4
淀类型不同,由沉淀的颜色变化不能直接比较K (AgCl)、K (Ag CrO)的大小,故C错误;D项,析出的
sp sp 2 4
苯酚不是固体,是乳浊液,故D错误;故选B。
15.下列方案设计与操作、现象与结论均正确的是( )
选项 实验目的 方案设计与操作 现象与结论
验证乙醇在Al O 在
2 3 将乙醇与Al O 共热产生的气体 若观察到溴水褪色,则证明乙醇Al O
A 催化下发生消去反 2 3 2 3
依次通入溴水、NaOH溶液 催化下发生消去反应
应
①取一定量的甲苯与一定体积、
若②褪色耗时更少,则证明冠醚中O
验证冠醚识别碱金 一定浓度的酸性高锰酸钾水溶液
B 与K+之间形成配位键,实现对 的识
属离子(如K+) 混合振荡。②在实验①试剂取量
别
基础上,再加入一定量冠醚振荡
分别向相同浓度、相同体积的 若观察到两溶液均出现沉淀,且ZnCl
比较Zn和Fe的金 2
C ZnCl 溶液和FeCl 溶液加入相同 溶液中生成的沉淀溶解,则说明Fe的
属性强弱 2 3
浓度相同体积且足量的氨水 金属性更强
比较三种二元弱酸
分别测定相同温度下等浓度的 若测量结果为:pH(NaHA)<pH(NaHB)
HA、HB、HC第
D 2 2 2 NaHA、NaHB、NaHC溶液的 <pH(NaHC),则证明K (H A)>
二步电离平衡常数 a2 2
pH K (H B)>K (H C)
大小 a2 2 a2 2
【答案】A
【解析】A项,乙醇消去生成乙烯,乙烯能使溴水褪色,故溴水褪色能说明乙醇在氧化铝条件下发生
消去反应,A正确;B项,高锰酸钾溶液的颜色是高锰酸根离子的颜色,不是钾离子的颜色,故溶液褪色
时间与冠醚识别碱金属离子无关,B错误;C项,金属性的强弱与沉淀的转化没有关系,C错误;D项,
盐溶液中阴离子水解程度越大,溶液的碱性越强,说明该对应酸的酸性越弱,应该使用酸对应的正盐,而
不是酸式盐,酸式盐中存在电离和水解,D错误;故选A。
二、非选择题(本题包括4小题,共55分)
16.(12分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要作用。
(1)下列关于实验的叙述中正确的有 (填字母)。
A.不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抹布灭火B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗
C.先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称
D.把试剂瓶中的NaCO 溶液倒入试管中,发现取量过多,为了不浪费,又把多余的试剂倒入原试剂
2 3
瓶中
E.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
F.使用分液漏斗前要检查其是否漏水
G.用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液中的水全部加热蒸干
(2)可用于分离或提纯物质的方法有:A.过滤;B.结晶;C.蒸馏;D.加热;e.分液。
请将相应分离提纯物质方法的序号填入空白处:
①除去澄清石灰水中悬浮的CaCO 颗粒: 。
3
②除去CaO中混有的CaCO : 。
3
③分离酒精和水的混合物: 。
④分离水和CCl 的混合物: 。
4
⑤分离NaCl和KNO 的混合物: 。
3
(3)某学校实验室从化学试剂商店买回18.4 mol·L-1的硫酸。
现有该浓硫酸配制100 mL 1 mol·L-1的稀硫酸。可供选用的仪器有:
a.胶头滴管 b.烧瓶 c.烧杯 d.药匙 e.量筒 f.托盘天平
请回答下列问题:
①配制稀硫酸时,上述仪器中不需要使用的有 (选填序号),还缺少的仪器有 (写仪器
名称)。
②配制100 mL 1 mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为 mL(保留一位小数),量
取浓硫酸时应选用 (填序号)规格的量筒。
A.10 mL B.50 mL C.100 mL
【答案】(1)AE (2)①a ②d ③c ④e ⑤b
(3)①bdf 100 mL容量瓶、玻璃棒 ②5.4 a
【解析】(1)B项,应立即先用布拭去,再用大量水冲洗,再涂上3%~5%的NaHCO 溶液;C项,
3
NaOH易潮解,应放在小烧杯内称量,不能放在纸上称量;D项,剩余的药品一般不放回原试剂瓶;G项,
应加热到有大量晶体析出时停止加热,利用余热蒸干。(3)①用浓硫酸配制稀硫酸,无需烧瓶、药匙、托盘
天平,还缺少100 mL容量瓶、玻璃棒。②根据稀释前后溶液中溶质的物质的量不变可得 0.1 L×1 mol·L-1
=18.4 mol·L-1×V,V≈0.005 4 L,即5.4 mL,应选用10 mL量筒。
17.(12分)利用废镍电池的金属电极芯(主要成分为Co、 Ni,还含少量Fe、Al等)生产醋酸钴晶体、硫酸镍晶体的工艺流程如下。
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Co(OH) Al(OH) Ni(OH)
3 2 2 3 3 2
开始沉淀pH 2.2 7.4 7.6 0.1 4.0 7.6
完全沉淀pH 3.2 8.9 9.2 1.1 5.2 9.2
(1)用硫酸浸取金属电极芯时,提高浸取率的方法有__________(写出一种合理方法即可)。
(2)沉淀A的主要成分是Fe(OH) 、________,“浸出液”调节pH的范围为________,调节pH选用的
3
试剂可以是___________(填字母)。
a.铁 b.氨水 c.碳酸钠溶液 d.稀硫酸
(3)由“母液4”获取NiSO ·7H O的操作是____________,________,过滤,洗涤。
4 2
【答案】(1)适当的升高温度(或将金属电极芯研成粉末)
(2)Al(OH) 5.2≤pH<7.6 bc (3)蒸发浓缩 冷却结晶
3
【解析】(2)金属电极芯中的主要成分是Co、Ni,还含少量Fe、Al等,加入稀硫酸酸浸时,金属单质
都转化为金属离子(Ni2+、Co2+、Fe2+、Al3+),浸出液中加入过氧化氢的作用是氧化亚铁离子为铁离子,由
流程图中最终产物可知,调节pH的作用是除去溶液中的Fe3+、Al3+,故沉淀A的主要成分是Fe(OH) 、
3
Al(OH) ;为了保证Fe3+、Al3+沉淀完全而Ni2+、Co2+不沉淀,由表格数据可知,要调节 pH的范围为
3
5.2≤pH<7.6;调节pH时不能加入铁,因为铁能还原铁离子为亚铁离子,不能加入稀硫酸,因为要将溶液
的pH调大,由流程图中后续所加试剂可知,调节pH选用的试剂可以是氨水、碳酸钠溶液。
18.(15分)铁、铜及其化合物是中学化学中常见化学物质,阅读材料回答问题:
(一)氯化铁是重要的化工原料,FeCl ·6H O的实验室制备流程图如下:
3 2
(1)废铁屑表面往往含有油污,去除废铁屑表面的油污的方法是___________。操作①要用到的玻璃仪
器有玻璃棒、烧杯和___________。
(2)加入含有少量铜的废铁屑比加入纯铁屑反应更快,原因为___________。操作②涉及的过程为:加
热浓缩、___________、过滤、洗涤、干燥。(3)检验FeCl 稀溶液中是否残留Fe2+的试剂可以是___________。为增大FeCl 溶液的浓度,向稀FeCl
3 3 3
溶液中加入纯Fe粉后通入Cl。此过程中发生的主要反应的离子方程式为___________、___________。
2
(二)为测定CuSO 溶液的浓度,某同学设计了如下方案:
4
(4)判断SO 2-沉淀完全的操作为___________。
4
(5)固体质量为w g,则c(CuSO )=___________mol/L。若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测
4
得c(CuSO )___________(填“偏高”、“偏低”或“无影响”)。
4
【答案】(1) 碱煮水洗 漏斗
(2) Fe、Cu在稀盐酸中形成原电池,加快反应速率 冷却结晶
(3) K [Fe(CN) ]溶液(或酸性KMnO 溶液,合理即可) 2Fe3++Fe=3Fe2+ 2Fe2++Cl=2Fe3++2Cl-
3 6 4 2
(4)向上层清液中继续滴加BaCl 溶液,无白色沉淀生成,则沉淀完全
2
(5) 偏低
【解析】【解析】(1)废铁屑表面往往含有油污,可以加入碱液去除,则去除废铁屑表面的油污的方法
是碱煮水洗。操作①为过滤,要用到的玻璃仪器有玻璃棒、烧杯和漏斗;(2)加入含有少量铜的废铁屑可以
构成Cu-Fe盐酸原电池,故比加入纯铁屑反应更快,原因为 Fe、Cu在稀盐酸中形成原电池,加快反应速
率。操作②为由溶液制取晶体,涉及的过程为:加热浓缩、冷却结晶、过滤、洗涤、干燥。(3)亚铁离子遇
到铁氰化钾溶液(或使酸性高锰酸钾溶液褪色)生成蓝色沉淀,则检验FeCl 稀溶液中是否残留Fe2+的试剂可
3
以是K[Fe(CN) ]溶液(或酸性KMnO 溶液,合理即可)。为增大FeCl 溶液的浓度,向稀FeCl 溶液中加入纯
3 6 4 3 3
Fe粉后通入Cl ,主要反应的离子方程式为2Fe3++Fe=3Fe2+、2Fe2++Cl=2Fe3++2Cl-;(4)结合钡离子和硫酸根
2 2
离子生成硫酸钡沉淀,判断SO 2-沉淀完全的操作为向上层清液中继续滴加BaCl 溶液,无白色沉淀生成,
4 2
则沉淀完全;(5)根据硫酸根离子守恒,n(CuSO )=n(BaSO ),固体质量为 w g,则 c(CuSO )=
4 4 4
mol/L。若步骤①从烧杯中转移沉淀时未洗涤烧杯,导致沉淀损失,硫酸钡质量减少,则
测得c(CuSO )偏低。
4
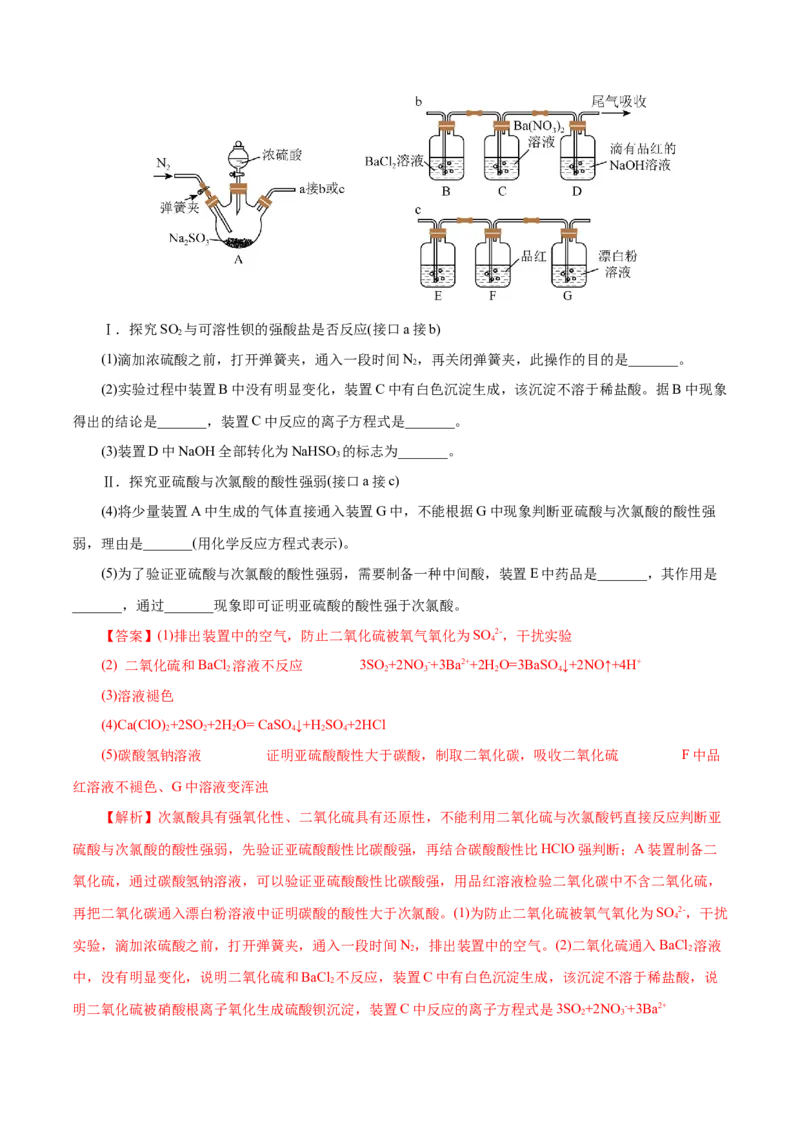
19.(16分)某研究性学习小组利用下列有关装置制备SO ,并对SO 的性质进行探究(装置的气密性已
2 2
检查)。已知:NaHSO 溶液显酸性。
3Ⅰ.探究SO 与可溶性钡的强酸盐是否反应(接口a接b)
2
(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间N,再关闭弹簧夹,此操作的目的是_______。
2
(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象
得出的结论是_______,装置C中反应的离子方程式是_______。
(3)装置D中NaOH全部转化为NaHSO 的标志为_______。
3
Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强
弱,理由是_______(用化学反应方程式表示)。
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是_______,其作用是
_______,通过_______现象即可证明亚硫酸的酸性强于次氯酸。
【答案】(1)排出装置中的空气,防止二氧化硫被氧气氧化为SO 2-,干扰实验
4
(2) 二氧化硫和BaCl 溶液不反应 3SO +2NO-+3Ba2++2H O=3BaSO↓+2NO↑+4H+
2 2 3 2 4
(3)溶液褪色
(4)Ca(ClO) +2SO+2H O= CaSO ↓+H SO +2HCl
2 2 2 4 2 4
(5)碳酸氢钠溶液 证明亚硫酸酸性大于碳酸,制取二氧化碳,吸收二氧化硫 F中品
红溶液不褪色、G中溶液变浑浊
【解析】次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚
硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强判断;A装置制备二
氧化硫,通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用品红溶液检验二氧化碳中不含二氧化硫,
再把二氧化碳通入漂白粉溶液中证明碳酸的酸性大于次氯酸。(1)为防止二氧化硫被氧气氧化为SO 2-,干扰
4
实验,滴加浓硫酸之前,打开弹簧夹,通入一段时间N,排出装置中的空气。(2)二氧化硫通入BaCl 溶液
2 2
中,没有明显变化,说明二氧化硫和BaCl 不反应,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸,说
2
明二氧化硫被硝酸根离子氧化生成硫酸钡沉淀,装置C中反应的离子方程式是3SO +2NO-+3Ba2+
2 3+2H O=3BaSO↓+2NO↑+4H+。(3)二氧化硫能使品红溶液褪色,装置D中NaOH全部转化为NaHSO 的标志
2 4 3
为溶液褪色;(4)次氯酸具有强氧化性、二氧化硫具有还原性,二氧化硫被次氯酸钙氧化为硫酸钙,反应方
程式为Ca(ClO) +2SO+2H O= CaSO ↓+H SO +2HCl,所以不能根据G中生成沉淀判断亚硫酸与次氯酸的酸
2 2 2 4 2 4
性强弱。(5)为了验证亚硫酸与次氯酸的酸性强弱,需要证明酸性:亚硫酸>碳酸>次氯酸,二氧化硫和碳酸
氢钠反应生成亚硫酸氢钠和二氧化碳,所以装置E中盛放碳酸氢钠溶液证明亚硫酸酸性大于碳酸、制取二
氧化碳、吸收二氧化硫,通过F中品红溶液不褪色、G中溶液变浑浊即可证明亚硫酸的酸性强于次氯酸。