文档内容
专题 16 工艺流程题
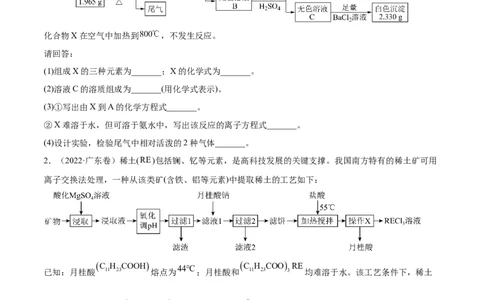
1.(2022·浙江卷)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
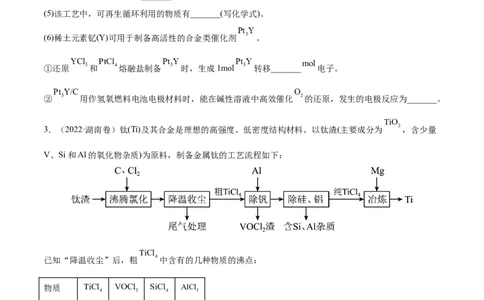
2.(2022·广东卷)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用
离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
C H COOH 44C C H COO RE
已知:月桂酸 11 23 熔点为 ;月桂酸和 11 23 3 均难溶于水。该工艺条件下,稀土
3 C H COO Mg K 1.8108 Al(OH)
离子保持 价不变; 11 23 2 的 sp , 3开始溶解时的pH为8.8;有关金属离子
沉淀的相关pH见下表。
离子 Mg2 Fe3 Al3 RE3
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。(2)“过滤1”前,用NaOH溶液调pH至_______的范围内,该过程中Al3发生反应的离子方程式为_______。
Mg Mg2 2.7gL1 RE3
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,可提
c
C H
COO-
高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 11 23
低于_______molL1
(保留两位有效数
字)。
(4)①“加热搅拌”有利于加快RE3溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
Pt Y
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 3 。
YCl PtCl Pt Y Pt Y mol
①还原 3和 4熔融盐制备 3 时,生成1mol 3 转移_______ 电子。
Pt Y/C O
② 3 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 2的还原,发生的电极反应为_______。
TiO
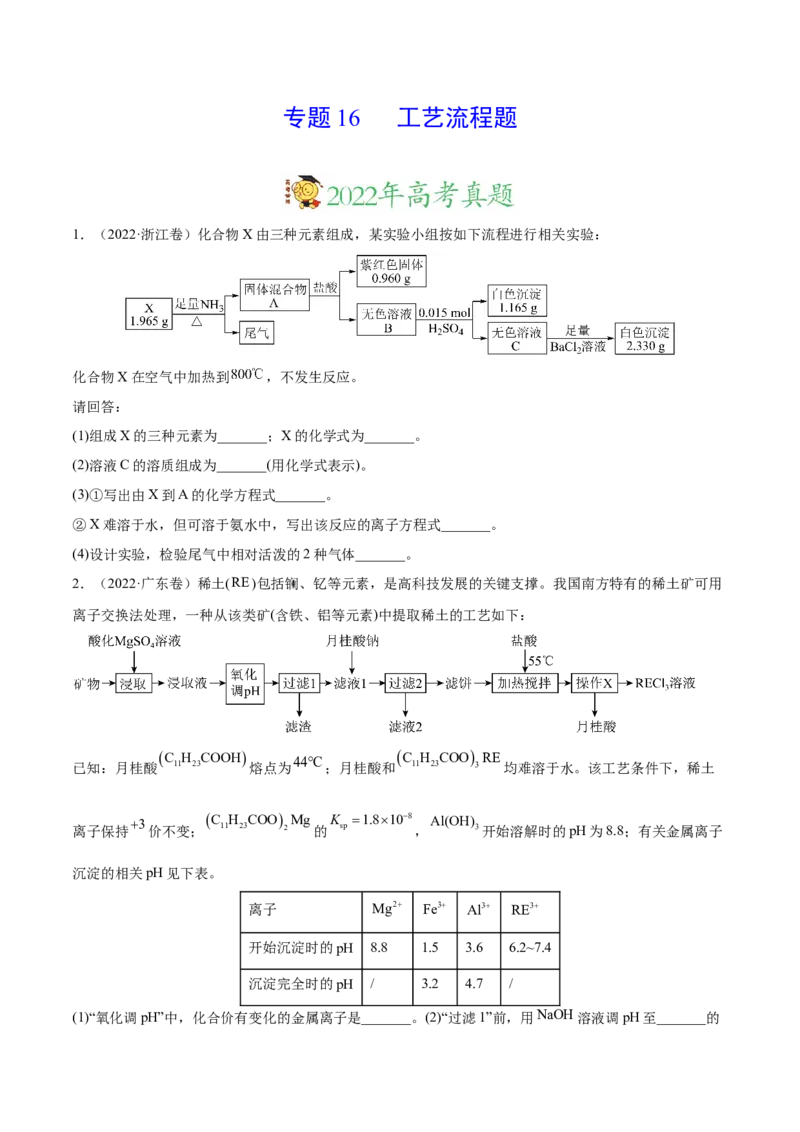
3.(2022·湖南卷)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 2,含少量
V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
TiCl
已知“降温收尘”后,粗 4中含有的几种物质的沸点:
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(1)已知ΔG=ΔH-TΔS,ΔG的值只决定于反应体系的始态和终态,忽略ΔH、ΔS随温度的变化。若ΔG<0,
则该反应可以自发进行。根据下图判断:600℃时,下列反应不能自发进行的是_______。C(s)O (g)CO (g)
A. 2 2
2C(s)O (g)2CO(g)
B. 2
TiO (s)2Cl (g)TiCl (g)O (g)
C. 2 2 4 2
TiO (s)C(s)2Cl (g)TiCl (g)CO (g)
D. 2 2 4 2
TiO Cl 600℃
(2) 2与C、 2,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
物质 TiCl CO CO Cl
4 2 2
分压
4.59102 1.84102 3.70102 5.98109
MPa
TiO Cl
①该温度下, 2与C、 2反应的总化学方程式为_______;
②随着温度升高,尾气中CO的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离 TiCl 4中含 Si 、 Al 杂质的方法是
_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠
C.铝热反应制锰 D.氧化汞分解制汞
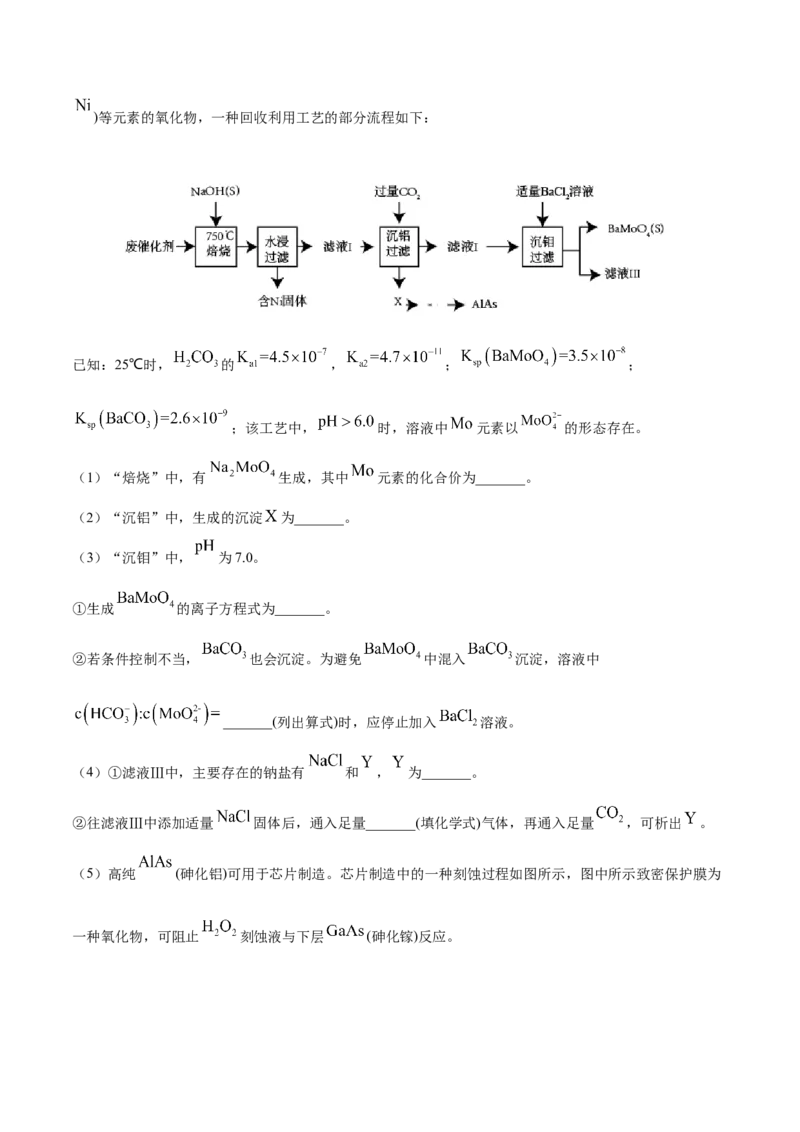
1.(2021·广东)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、镍()等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 ,可析出 。
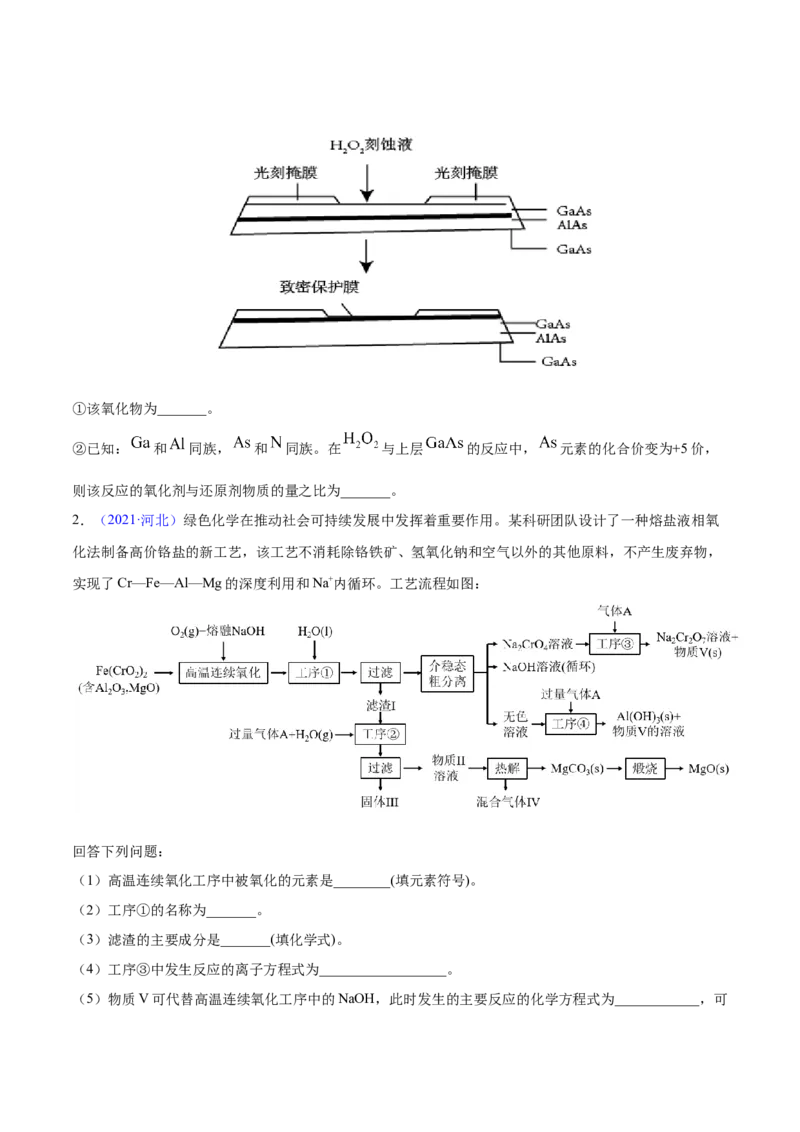
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为
一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价变为+5价,
则该反应的氧化剂与还原剂物质的量之比为_______。
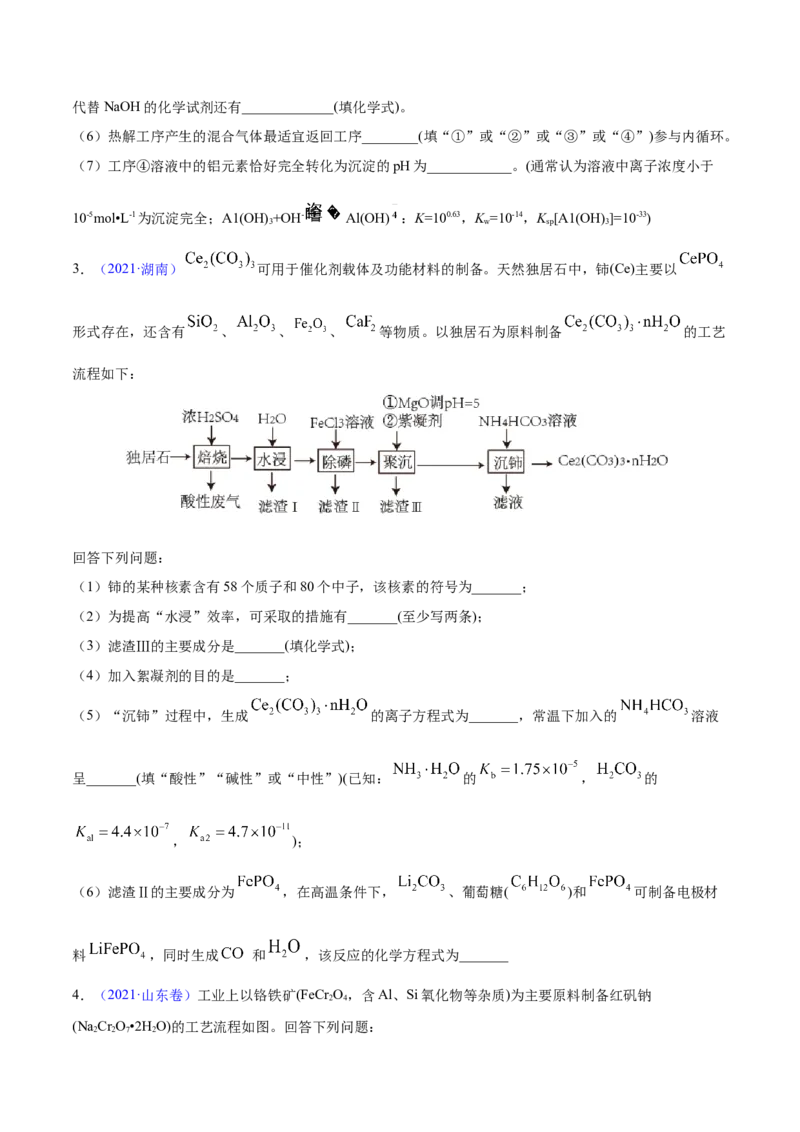
2.(2021·河北)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧
化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,
实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是________(填元素符号)。
(2)工序①的名称为_______。
(3)滤渣的主要成分是_______(填化学式)。
(4)工序③中发生反应的离子方程式为__________________。
(5)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为____________,可代替NaOH的化学试剂还有_____________(填化学式)。
(6)热解工序产生的混合气体最适宜返回工序________(填“①”或“②”或“③”或“④”)参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为____________。(通常认为溶液中离子浓度小于
10-5mol•L-1为沉淀完全;A1(OH) +OH- Al(OH) :K=100.63,K =10-14,K [A1(OH) ]=10-33)
3 w sp 3
3.(2021·湖南) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
形式存在,还含有 、 、 、 等物质。以独居石为原料制备 的工艺
流程如下:
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
(3)滤渣Ⅲ的主要成分是_______(填化学式);
(4)加入絮凝剂的目的是_______;
(5)“沉铈”过程中,生成 的离子方程式为_______,常温下加入的 溶液
呈_______(填“酸性”“碱性”或“中性”)(已知: 的 , 的
, );
(6)滤渣Ⅱ的主要成分为 ,在高温条件下, 、葡萄糖( )和 可制备电极材
料 ,同时生成 和 ,该反应的化学方程式为_______
4.(2021·山东卷)工业上以铬铁矿(FeCr O,含Al、Si氧化物等杂质)为主要原料制备红矾钠
2 4
(NaCr O•2HO)的工艺流程如图。回答下列问题:
2 2 7 2(1)焙烧的目的是将FeCr O 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆
2 4 2 4
流而行,目的是___。
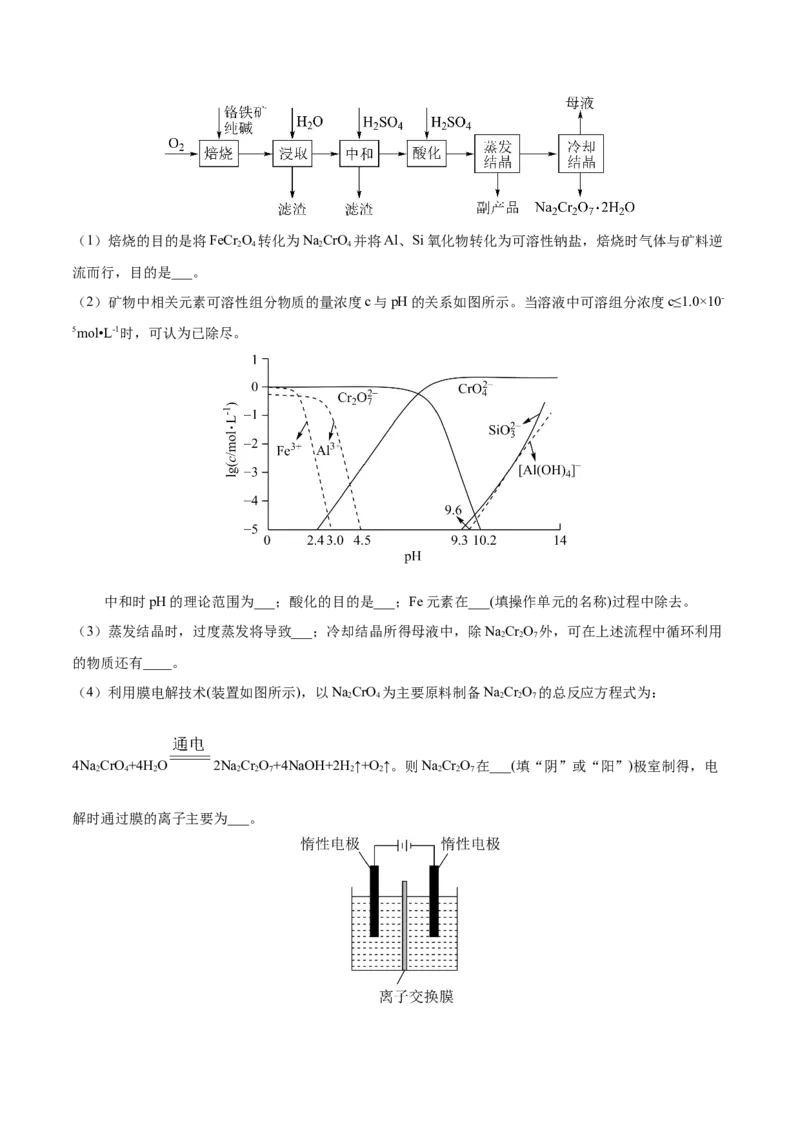
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度c≤1.0×10-
5mol•L-1时,可认为已除尽。
中和时pH的理论范围为___;酸化的目的是___;Fe元素在___(填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致___;冷却结晶所得母液中,除NaCr O 外,可在上述流程中循环利用
2 2 7
的物质还有____。
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反应方程式为:
2 4 2 2 7
4NaCrO+4HO 2NaCr O+4NaOH+2H↑+O↑。则NaCr O 在___(填“阴”或“阳”)极室制得,电
2 4 2 2 2 7 2 2 2 2 7
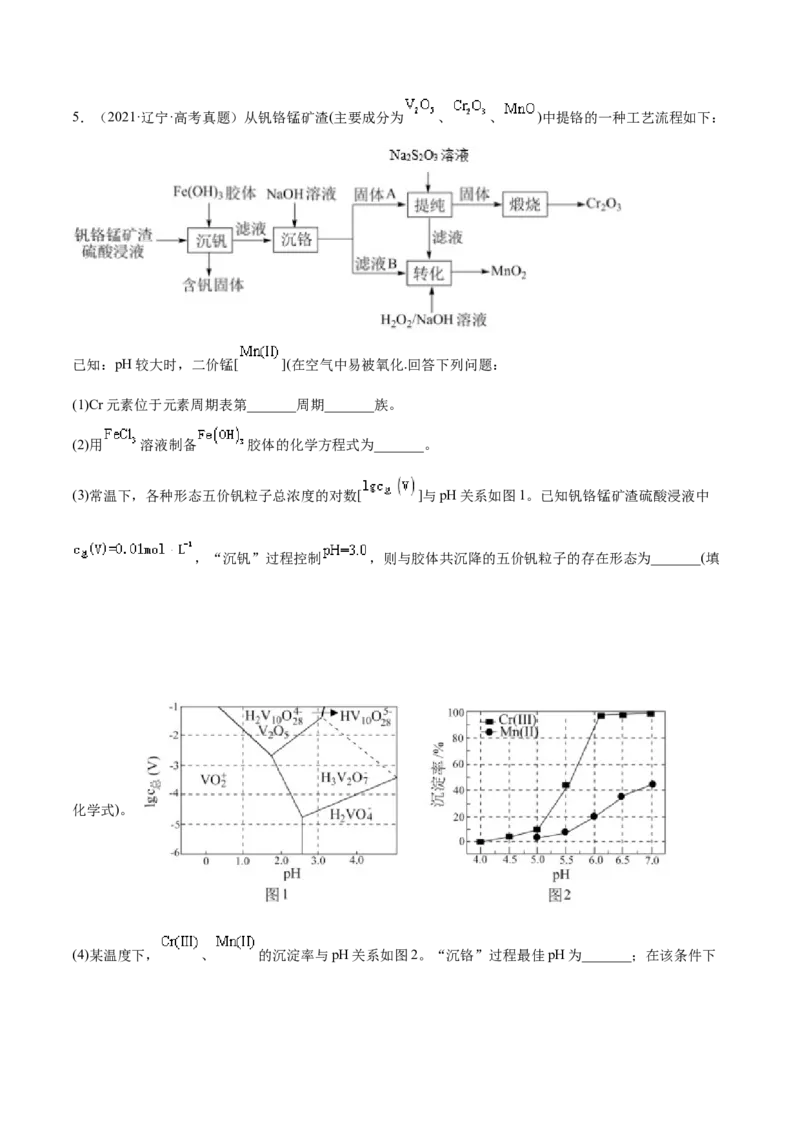
解时通过膜的离子主要为___。5.(2021·辽宁·高考真题)从钒铬锰矿渣(主要成分为 、 、 )中提铬的一种工艺流程如下:
已知:pH较大时,二价锰[ ](在空气中易被氧化.回答下列问题:
(1)Cr元素位于元素周期表第_______周期_______族。
(2)用 溶液制备 胶体的化学方程式为_______。
(3)常温下,各种形态五价钒粒子总浓度的对数[ ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为_______(填
化学式)。
(4)某温度下, 、 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为_______;在该条件下滤液B中 _______ 【 近似为 , 的 近似为 】。
(5)“转化”过程中生成 的离子方程式为_______。
(6)“提纯”过程中 的作用为_______。
6.
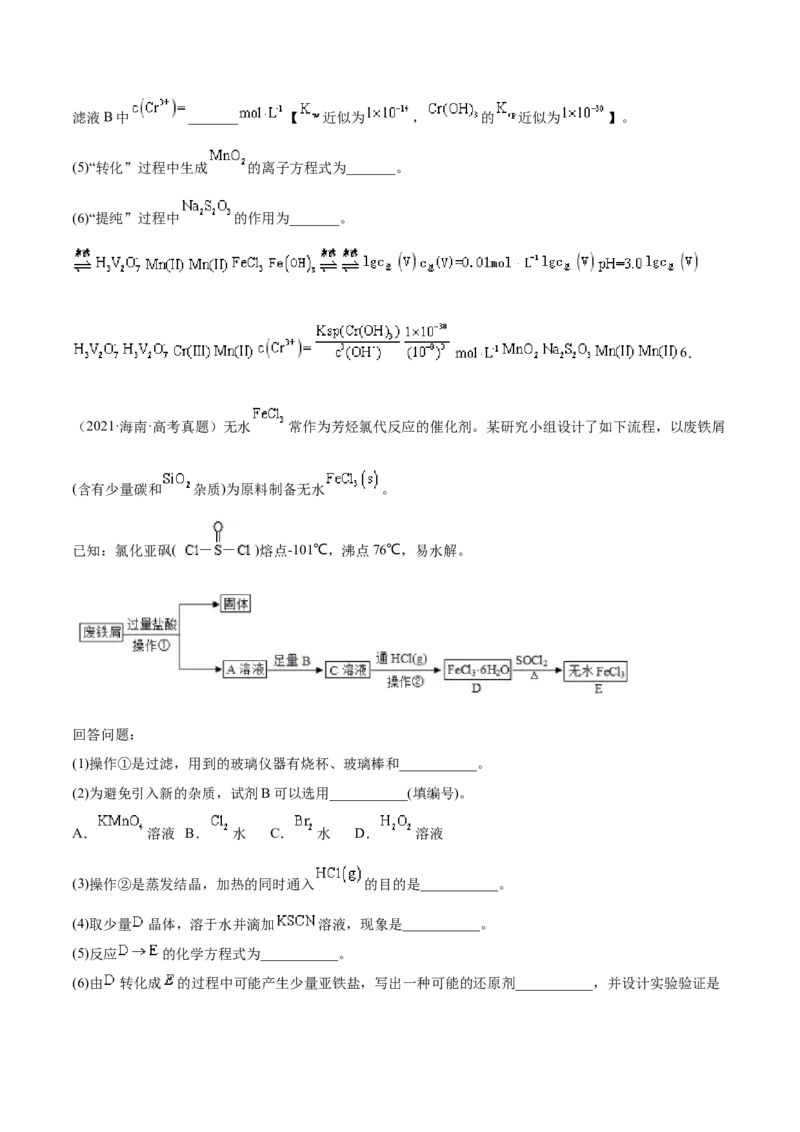
(2021·海南·高考真题)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑
(含有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 B. 水 C. 水 D. 溶液
(3)操作②是蒸发结晶,加热的同时通入 的目的是___________。
(4)取少量 晶体,溶于水并滴加 溶液,现象是___________。
(5)反应 的化学方程式为___________。
(6)由 转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________,并设计实验验证是该还原剂将 还原___________。
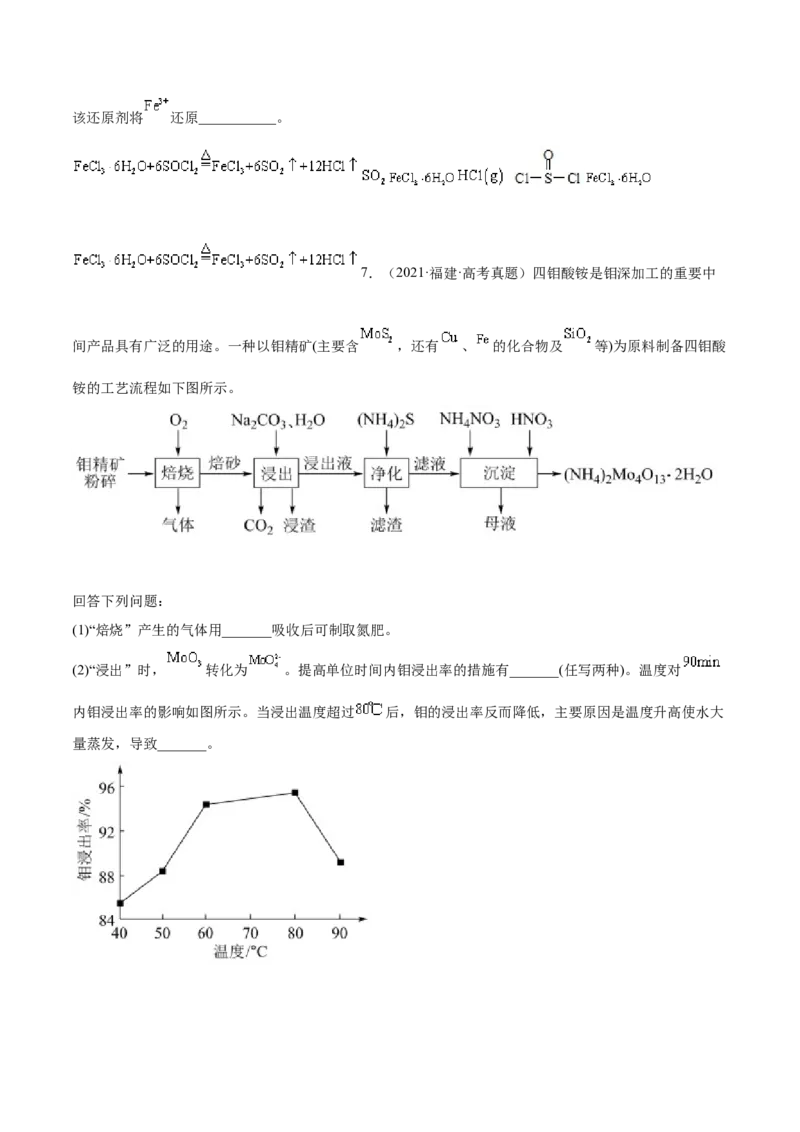
7.(2021·福建·高考真题)四钼酸铵是钼深加工的重要中
间产品具有广泛的用途。一种以钼精矿(主要含 ,还有 、 的化合物及 等)为原料制备四钼酸
铵的工艺流程如下图所示。
回答下列问题:
(1)“焙烧”产生的气体用_______吸收后可制取氮肥。
(2)“浸出”时, 转化为 。提高单位时间内钼浸出率的措施有_______(任写两种)。温度对
内钼浸出率的影响如图所示。当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度升高使水大
量蒸发,导致_______。(3)“净化”时,浸出液中残留的 、 转化为沉淀除去。研究表明,该溶液中 和pH的关系为:
。为了使溶液中的杂质离子浓度小于 ,应控制溶液的pH不小于_______。
(已知: ; 和 的 分别为35.2和17.2)
(4)“净化”后,溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,反应的离子方程式
为_______。
(5)“沉淀”时,加入 的目的是_______。
(6)高温下用 还原(NH )MoO 可制得金属钼,反应的化学方程式为_______。【已知:(NH )MoO 受
4 2 4 13 4 2 4 13
热分解生成 】
8.(2021·湖北·
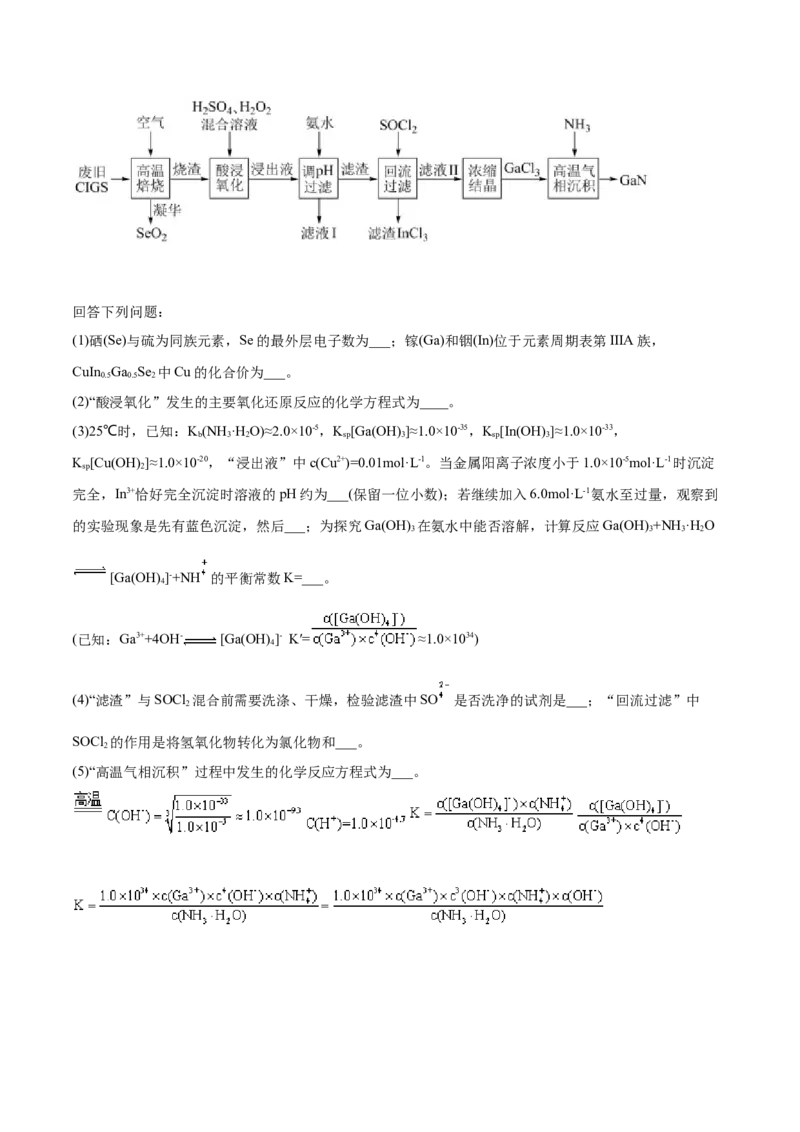
高考真题)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为CuIn Ga Se 。某探究小组回
0.5 0.5 2
收处理流程如图:回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为___;镓(Ga)和铟(In)位于元素周期表第IIIA族,
CuIn Ga Se 中Cu的化合价为___。
0.5 0.5 2
(2)“酸浸氧化”发生的主要氧化还原反应的化学方程式为____。
(3)25℃时,已知:K(NH ·H O)≈2.0×10-5,K [Ga(OH)]≈1.0×10-35,K [In(OH) ]≈1.0×10-33,
b 3 2 sp 3 sp 3
K [Cu(OH) ]≈1.0×10-20,“浸出液”中c(Cu2+)=0.01mol·L-1。当金属阳离子浓度小于1.0×10-5mol·L-1时沉淀
sp 2
完全,In3+恰好完全沉淀时溶液的pH约为___(保留一位小数);若继续加入6.0mol·L-1氨水至过量,观察到
的实验现象是先有蓝色沉淀,然后___;为探究Ga(OH) 在氨水中能否溶解,计算反应Ga(OH) +NH·H O
3 3 3 2
[Ga(OH)]-+NH 的平衡常数K=___。
4
(已知:Ga3++4OH- [Ga(OH)]- K′= ≈1.0×1034)
4
(4)“滤渣”与SOCl 混合前需要洗涤、干燥,检验滤渣中SO 是否洗净的试剂是___;“回流过滤”中
2
SOCl 的作用是将氢氧化物转化为氯化物和___。
2
(5)“高温气相沉积”过程中发生的化学反应方程式为___。9.
(2021·江苏·高考真题)以锌灰(含ZnO及少量PbO、CuO、Fe O、SiO)和Fe (SO ) 为原料制备的ZnFe O
2 3 2 2 4 3 2 4
脱硫剂,可用于脱除煤气中的HS。脱硫剂的制备、硫化、再生过程可表示为
2
(1)“除杂”包括加足量锌粉、过滤加HO 氧化等步骤。除Pb2+和Cu2+外,与锌粉反应的离子还有___(填化
2 2
学式)。
(2)“调配比”前,需测定ZnSO 溶液的浓度。准确量取2.50mL除去Fe3+的ZnSO 溶液于100mL容量瓶中,
4 4
加水稀释至刻度;准确量取20.00mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用
0.0150mol·L-1EDTA(Na HY)溶液滴定至终点(滴定反应为Zn2++Y4-=ZnY2-),平行滴定3次,平均消耗EDTA
2 2
溶液25.00mL。计算ZnSO 溶液的物质的量浓度___(写出计算过程)。
4
(3)400℃时,将一定比例H、CO、CO 和HS的混合气体以一定流速通过装有ZnFe O 脱硫剂的硫化反应
2 2 2 2 4
器。
①硫化过程中ZnFe O 与H、HS反应生成ZnS和FeS,其化学方程式为___。
2 4 2 2
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了HS与CO 生成COS的反应,反应前后ZnS
2 2
的质量不变,该反应过程可描述为___。
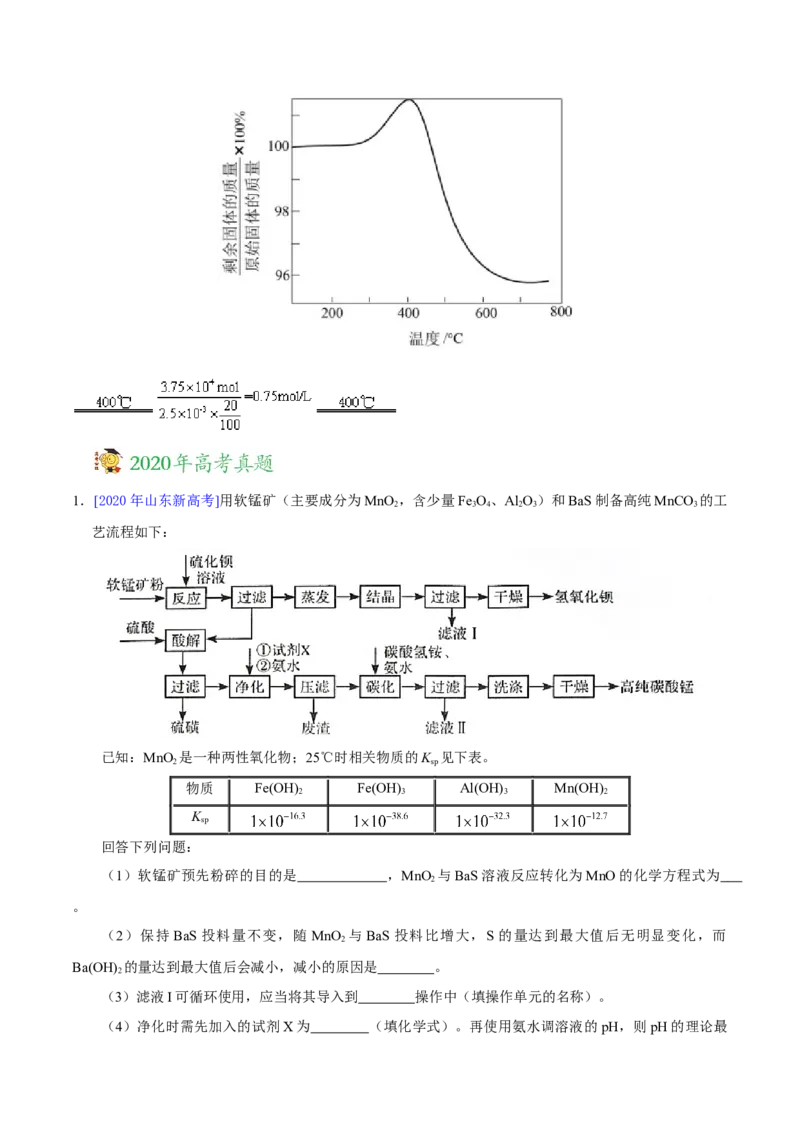
(4)将硫化后的固体在N:O=95:5(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所示。
2 2
在280~400℃范围内,固体质量增加的主要原因是___。1.[2020年山东新高考]用软锰矿(主要成分为MnO ,含少量Fe O 、Al O )和BaS制备高纯MnCO 的工
2 3 4 2 3 3
艺流程如下:
已知:MnO 是一种两性氧化物;25℃时相关物质的K 见下表。
2 sp
物质 Fe(OH) Fe(OH) Al(OH) Mn(OH)
2 3 3 2
K
sp
回答下列问题:
(1)软锰矿预先粉碎的目的是 ,MnO 与BaS溶液反应转化为MnO的化学方程式为
2
。
(2)保持 BaS 投料量不变,随 MnO 与BaS 投料比增大,S的量达到最大值后无明显变化,而
2
Ba(OH) 的量达到最大值后会减小,减小的原因是 。
2
(3)滤液I可循环使用,应当将其导入到 操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为 (填化学式)。再使用氨水调溶液的pH,则pH的理论最小值为_______(当溶液中某离子浓度 时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为 。
2.[2020江苏卷]实验室由炼钢污泥(简称铁泥,主要成份为铁的氧化物)制备软磁性材料α−Fe O。
2 3
其主要实验流程如下:
(1)酸浸。用一定浓度的HSO 溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能
2 4
提高铁元素浸出率的有 ▲ (填序号)。
A.适当升高酸浸温度 B.适当加快搅拌速度 C.适当缩短酸浸时间
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使 Fe3+完全转化为Fe2+。“还原”过程中除生成
Fe2+外,还会生成 ▲ (填化学式);检验Fe3+是否还原完全的实验操作是 ▲ 。
(3)除杂。向“还原”后的滤液中加入NH F溶液,使Ca2+转化为CaF 沉淀除去。若溶液的pH偏低、
4 2
将会导致CaF 沉淀不完全,其原因是 ▲ [ , ]。
2
(4)沉铁。将提纯后的FeSO 溶液与氨水−NH HCO 混合溶液反应,生成FeCO 沉淀。
4 4 3 3
①生成FeCO 沉淀的离子方程式为 ▲ 。
3
②设计以FeSO 溶液、氨水-NH HCO 混合溶液为原料,制备FeCO 的实验方案: ▲ 。
4 4 3 3
[FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5]。
3 2