文档内容
专题 21 分子结构与性质
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 分子的空间结构
考点二 分子的性质及应用
考点一 分子的空间结构
1.(2023·江苏盐城·盐城市伍佑中学校考模拟预测)CsCl是一种分析试剂,制备方法
。下列说法正确的是
A.CsCl的电子式: B.基态 的核外电子排布式:
C. 的空间构型:三角锥形 D.中子数为18的Cl原子:
【答案】B
【解析】A.CsCl属于离子化合物,即电子式 ,A错误;B.基态 的核外电子排布式:
,B正确;C. 的空间构型为平面三角形,C错误;D.中子数为18的Cl原子 ,D错误;
故选B。
2.(2023·天津滨海新·天津市滨海新区塘沽第一中学校联考二模)下列有关化学用语表示正确的是
A. 的VSEPR模型: B.2-甲基-1-丁烯的键线式:
C. 的名称:1-甲基乙醇 D.Ge原子的价电子排布式:
【答案】D
【解析】A. 分子中价层电子对数为2,且不存在孤对电子,其VSEPR模型为直线形,A错误;B.
该键线式应该是3-甲基-1-丁烯的键线式,B错误;C.该有机物的名称是2-丙醇,C错误;D.Ge是第
ⅣA族元素,其原子的价电子排布式为 ,D正确;答案选D。
3.(2023·江苏·校联考模拟预测) 可发生水解反应 ,下列说法正确的是
A. 空间构型为平面三角形
B. 分子的空间填充模型为
1
原创精品资源学科网独家享有版权,侵权必究!C. 分子的电子式为
D.HClO分子的结构式为
【答案】B
【解析】A. 分子中,N原子轨道杂化方式为 ,分子呈三角锥形,A错误;B.模型
能真实地反映H、O原子的相对大小以及水分子的V形结构,B正确;C. 分子中N原子价层电子
有4对,电子式为 ,C错误;D.HClO中,H、Cl分别以单键与O相连,结构式为
,D错误;故选:B。
4.(2023·江苏南通·统考三模) 可用作涂料,可由反应
制得。下列说法正确的是
A.基态Cu的电子排布式为 B.Cu O中O元素的化合价为-4
2
C. 的空间构型为平面四边形 D. 晶体的类型为共价晶体
【答案】A
【解析】A.已知Cu为29号元素,故基态Cu的电子排布式为[Ar]3d104s1,A正确;
B.已知O的最外层上有6个电子,故O的最低负价为-2价,故Cu O中O元素的化合价为-2,Cu为+1价,
2
B错误;C. 中心原子S原子周围的价层电子对数为:4+ =4,故其空间构型为正四面体形,
C错误;D.SO 晶体是由SO 分子通过范德华力作用形成的分子晶体,D错误;故答案为:A。
2 2
5.(2023·江苏南通·统考三模)乙硼烷 常应用于有机合成领域,可通过反应
制得。下列说法正确的是
A.基态B原子的轨道表示式为
B.基态F原子核外电子排布式为
C. 分子空间构型为三角锥形
D. 中含有配位键
【答案】D
【解析】A.基态B原子的轨道表示式为 ,A错误;B. F是9号元素,基态F原子
核外电子排布式为 ,B错误;C. 形成3个σ键,中心原子B无孤电子对,所以BF 分子空间
3构型为平面三角形,C错误;D. 中Na+与BF 离子键结合,BF 含有共价键和配位键,D正确;故
答案选D。
6.(2023·山西晋城·晋城市第一中学校校考模拟预测)油画创作通常需要用到多种无机颜料。研究发现,
在不同的空气湿度和光照条件下,颜料雌黄 褪色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A.反应I和II中,元素 和 都被氧化
B.反应I和II中,氧化 转移的电子数之比为
C. 和 的空间结构都是正四面体形
D.反应I和II中,参加反应的 :IO>C>H
D.由结构推测,固态的甘氨酸易溶于水
【答案】C
【解析】A.在分子中碳原子有sp2、sp3两种杂化形式,A正确;B.甘氨酸分子中有羧基,可以和氢氧化
钠反应生成相盐,有氨基,可以和盐酸反应生成盐,B正确;C.同周期主族元素从左到右电负性逐渐增
大,故电负大小顺序为:O>N>C>H,C错误;D.甘氨酸分子中存在氨基、羧基,均可以与水形成氢键,
故固态的甘氨酸易溶于水,D正确;
故选C。
4.(2023·湖南株洲·统考一模)已知吡啶( )中含有与苯类似的 大π键,下列有关叙述正确的是A.吡啶中N原子的价层孤电子对占据sp杂化轨道
B.在水中的溶解度,吡啶远大于苯的原因只是相似相溶原理
C. 、 、 的碱性随N原子电子云密度的增大而增强,则其中碱性最
弱的是
D. 与 互为同系物
【答案】D
【解析】A.吡啶中N原子的价层孤电子对占据sp2轨道,A错误;B.吡啶分子能与水分子形成分子间氢
键,吡啶分子和HO分子均为极性分子,相似相溶,所以吡啶在水中的溶解度大于苯在水中的溶解度,B
2
错误;C.已知甲基为推电子集团,氯原子为吸电子基团,则氮原子的电子云密度为 >
> ,碱性最最若的为 ,C错误;D. 与 结
构相似,分子组成上相差了1个CH,故两者互为同系物,D正确;故选D。
2
5.(2023·广东深圳·翠园中学校考模拟预测)金属镍粉在要CO气流中轻微加热,生成无色挥发性液态
,其构型如图。下列说法不正确的是
A. 中含有的非极性共价键和离子键
B. 难溶于水,易溶于有机溶剂
C.较高温度下, 可分解生成Ni和CO
D. 为分子晶体,其中心原子采取 杂化
【答案】A
【解析】A. 为共价化合物,含有镍碳、碳氧极性键,故A错误;B. 分子结构对称,
为非极性分子,根据相似相溶原理可知,其难溶于水,易溶于有机溶剂,故B正确;C.金属镍粉在要CO
气流中轻微加热,生成无色挥发性液态 ,推测 不稳定,从结构上看,碳原子正电性强、故碳原子与镍的配位键不牢固,容易分解镍和一氧化碳,故C正确;D.由题干可知, 熔沸点较
低,为分子晶体,其中心原子Ni形成4个共价键,采取 杂化,故D正确;答案为A。
6.(2023·广东汕头·金山中学校考三模)结构决定性质,下列有关性质的比较正确的是
A.沸点: B.酸性:
C.白磷 在溶剂中的溶解度: D.熔点:金刚石>晶体硅
【答案】D
【解析】A.HF能形成分子间氢键,其沸点高于HCl,A错误;B.元素的非金属性越强,其最高价氧化
物对应的水化物的酸性越强,非金属性:P>S,因此酸性: HPO >H SiO,B错误;C.P 和CS 为非极
3 4 2 3 4 2
性分子,HO为极性分子,根据相似相溶的原理,白磷在溶剂中的溶解度:CS>H O,C错误;D.金刚石
2 2 2
和晶体硅均为共价晶体,原子半径:CSi-Si,共价键的键能越大,破
坏所需耗费的能量越高,熔点越高,因此熔点:金刚石>晶体硅,D正确;故选D。
7.(2023·湖南·校联考一模)下列有关说法错误的是
A.有手性异构体的分子叫做手性分子
B.臭氧是极性分子,可用于自来水的消毒
C.冠醚可利用其空穴大小适配相应碱金属离子,两者能通过弱相互作用形成超分子
D.乳酸加聚得到聚乳酸,聚乳酸因具有良好的生物相容性和可吸收性,可用于手术缝合
【答案】D
【解析】A.有手性异构体的分子叫做手性分子,故A正确;B.臭氧是V形分子,正负电荷的重心不重
合,臭氧是极性分子,臭氧具有强氧化性,可用于自来水的消毒,故B正确;C.冠醚可利用其空穴大小
适配相应碱金属离子,两者能通过弱相互作用形成超分子,故C正确;D.乳酸分子中含有羧基、羟基,
发生缩聚反应得到聚乳酸,故D错误;选D。
8.(2023·湖北武汉·华中师大一附中校考模拟预测)下列有关物质结构与性质的说法错误的是
A.环己烷 的椅式比船式稳定(椅式: ;船式: )
B. 分子间存在氢键,而 分子间不存在,所以 比 稳定
C. 的极性大于 的极性,所以三氟乙酸的酸性比三氯乙酸的酸性强
D.孤电子对有较大斥力,所以中心原子含孤电子对的分子的实测键角几乎都小于VSEPR模型的预测值
【答案】B
【解析】A.船式的位阻较大,故环己烷 的椅式比船式稳定(椅式: ;船式:),A正确;B.稳定性是化学性质,氢键只影响物质的物理性质,O—H键的键能大于
S—H键的,因此 比 稳定,B错误;C. 的极性大于 的极性,三氟乙酸的羧基中羟基
的极性强于三氯乙酸的羧基中羟基的极性,所以三氟乙酸的酸性比三氯乙酸的酸性强,C正确;D.孤电
子对有较大斥力,所以中心原子含孤电子对的分子的实测键角几乎都小于VSEPR模型的预测值,D正确;
故选B。
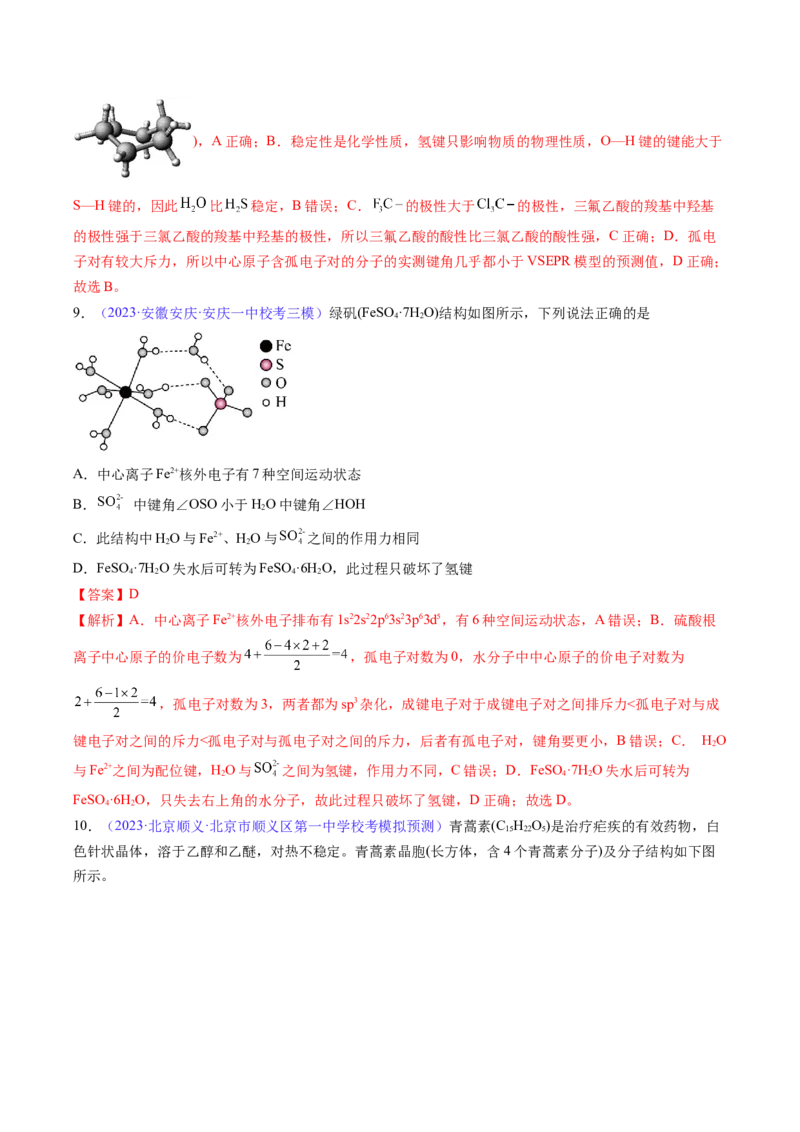
9.(2023·安徽安庆·安庆一中校考三模)绿矾(FeSO ·7H O)结构如图所示,下列说法正确的是
4 2
A.中心离子Fe2+核外电子有7种空间运动状态
B. 中键角∠OSO小于HO中键角∠HOH
2
C.此结构中HO与Fe2+、HO与 之间的作用力相同
2 2
D.FeSO ·7H O失水后可转为FeSO ·6H O,此过程只破坏了氢键
4 2 4 2
【答案】D
【解析】A.中心离子Fe2+核外电子排布有1s22s22p63s23p63d5,有6种空间运动状态,A错误;B.硫酸根
离子中心原子的价电子数为 ,孤电子对数为0,水分子中中心原子的价电子对数为
,孤电子对数为3,两者都为sp3杂化,成键电子对于成键电子对之间排斥力<孤电子对与成
键电子对之间的斥力<孤电子对与孤电子对之间的斥力,后者有孤电子对,键角要更小,B错误;C. HO
2
与Fe2+之间为配位键,HO与 之间为氢键,作用力不同,C错误;D.FeSO ·7H O失水后可转为
2 4 2
FeSO ·6H O,只失去右上角的水分子,故此过程只破坏了氢键,D正确;故选D。
4 2
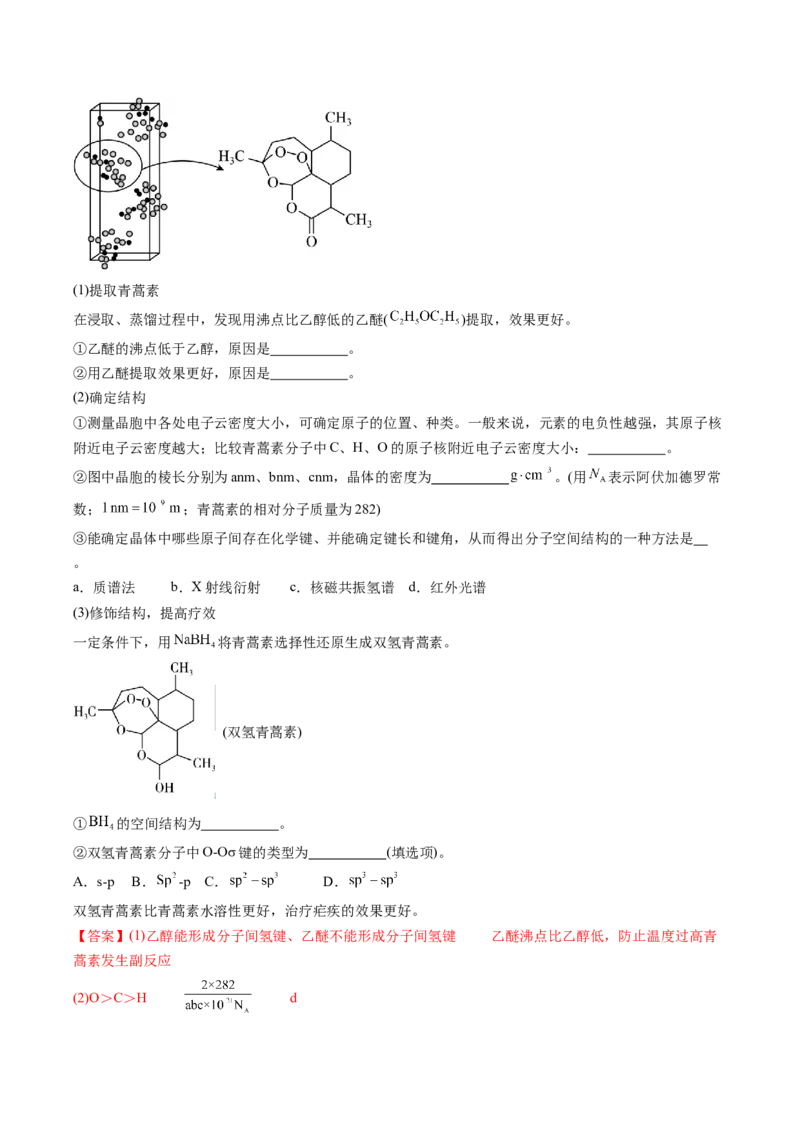
10.(2023·北京顺义·北京市顺义区第一中学校考模拟预测)青蒿素(C H O)是治疗疟疾的有效药物,白
15 22 5
色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图
所示。(1)提取青蒿素
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚( )提取,效果更好。
①乙醚的沸点低于乙醇,原因是 。
②用乙醚提取效果更好,原因是 。
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。一般来说,元素的电负性越强,其原子核
附近电子云密度越大;比较青蒿素分子中C、H、O的原子核附近电子云密度大小: 。
②图中晶胞的棱长分别为anm、bnm、cnm,晶体的密度为 。(用 表示阿伏加德罗常
数; ;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
(双氢青蒿素)
① 的空间结构为 。
②双氢青蒿素分子中O-Oσ键的类型为 (填选项)。
A.s-p B. -p C. D.
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
【答案】(1)乙醇能形成分子间氢键、乙醚不能形成分子间氢键 乙醚沸点比乙醇低,防止温度过高青
蒿素发生副反应
(2)O>C>H d(3)正四面体形 D
【解析】(1)①能形成分子间氢键的物质熔沸点较高,乙醇能形成分子间氢键、乙醚不能形成分子间氢
键,所以乙醚的沸点低于乙醇,故答案为:乙醇能形成分子间氢键、乙醚不能形成分子间氢键;②乙醚沸
点比乙醇低,防止温度过高青蒿素发生副反应,所以用乙醚提纯效果较好,故答案为:乙醚沸点比乙醇低,
防止温度过高青蒿素发生副反应;
(2)①原子的电负性越大,该原子吸引电子能力越强,原子核附近电子云密度越大,电负性:O>C>
H,所以青蒿素分子中C、H、O的原子核附近电子云密度大小顺序是O>C>H;②该晶胞体积=(a×10-
7cm)×(b×10-7cm)×(c×10-7cm)=abc×10-21cm3,该晶胞中分子个数=4× =2,晶体的密度ρ= =
g.cm-3,故答案为: ;③a.质谱法测定相对分子质量,a错误;b.X射线衍射判断晶体和非晶体,
b错误;c.核磁共振氢谱判断氢原子种类,c错误;d.红外光谱核外光谱判断化学键,d正确;故答案为:
d;
(3)① 中B原子价层电子对数=4+ =4且不含孤电子对,该离子为正四面体形结构,故答
案为:正四面体形;②双氢青蒿素分子中氧原子的价层电子对数为4,采用sp3杂化,则O-Oσ键的类型为
sp3-sp3σ键,故答案为:D。