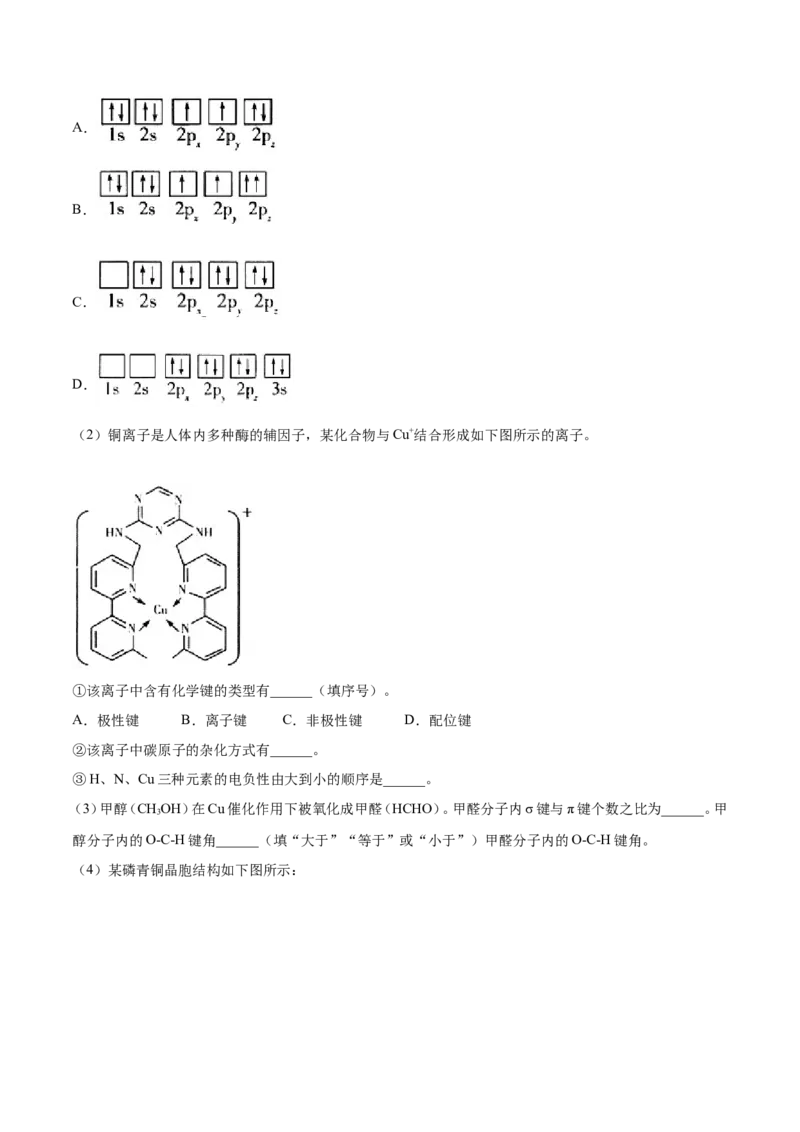
文档内容
1.铂钻合金是以铂为基含钻二元合金,在高温下,铂与钻可无限互溶,其固溶体为面心立方晶格。铂钻合金磁
性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表电子钟表磁控管等。
(1)基态钴原子的价电子排布图为______。
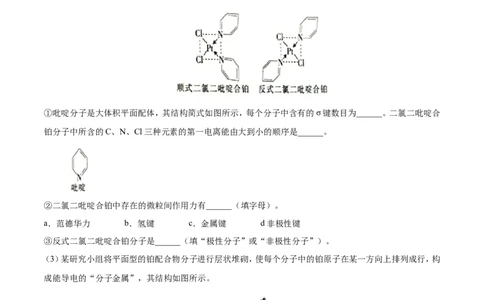
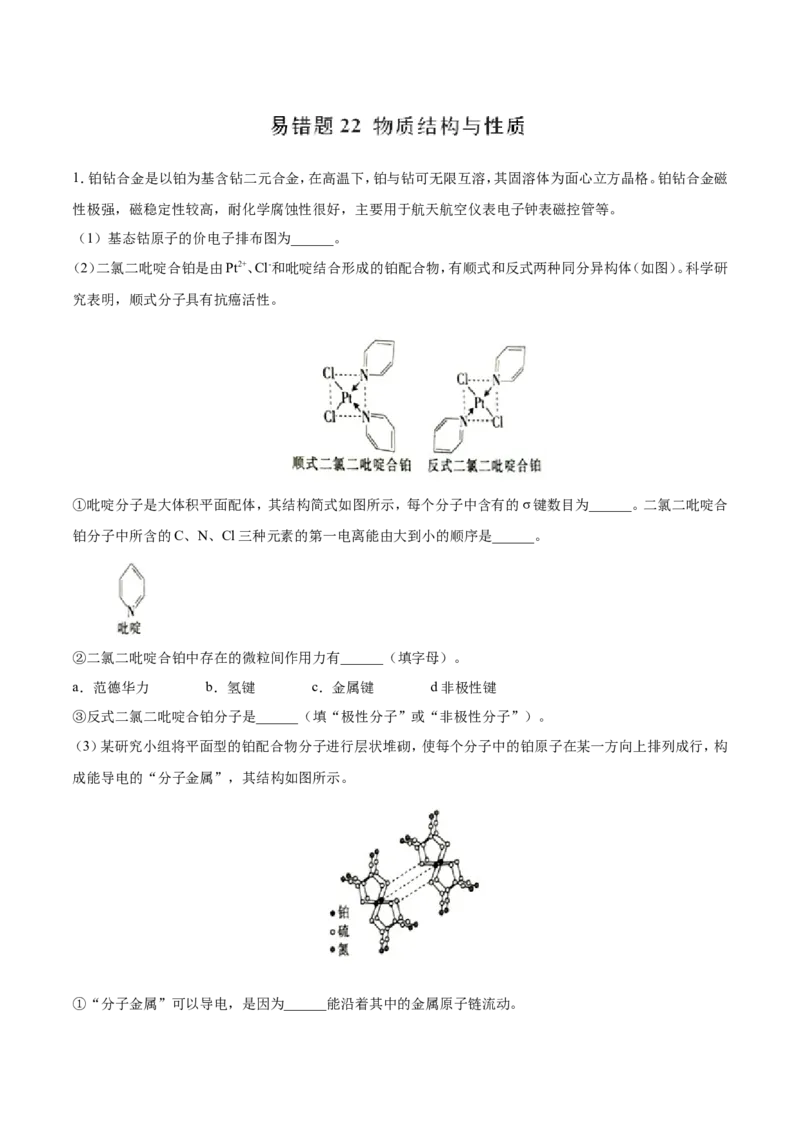
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如图)。科学研
究表明,顺式分子具有抗癌活性。
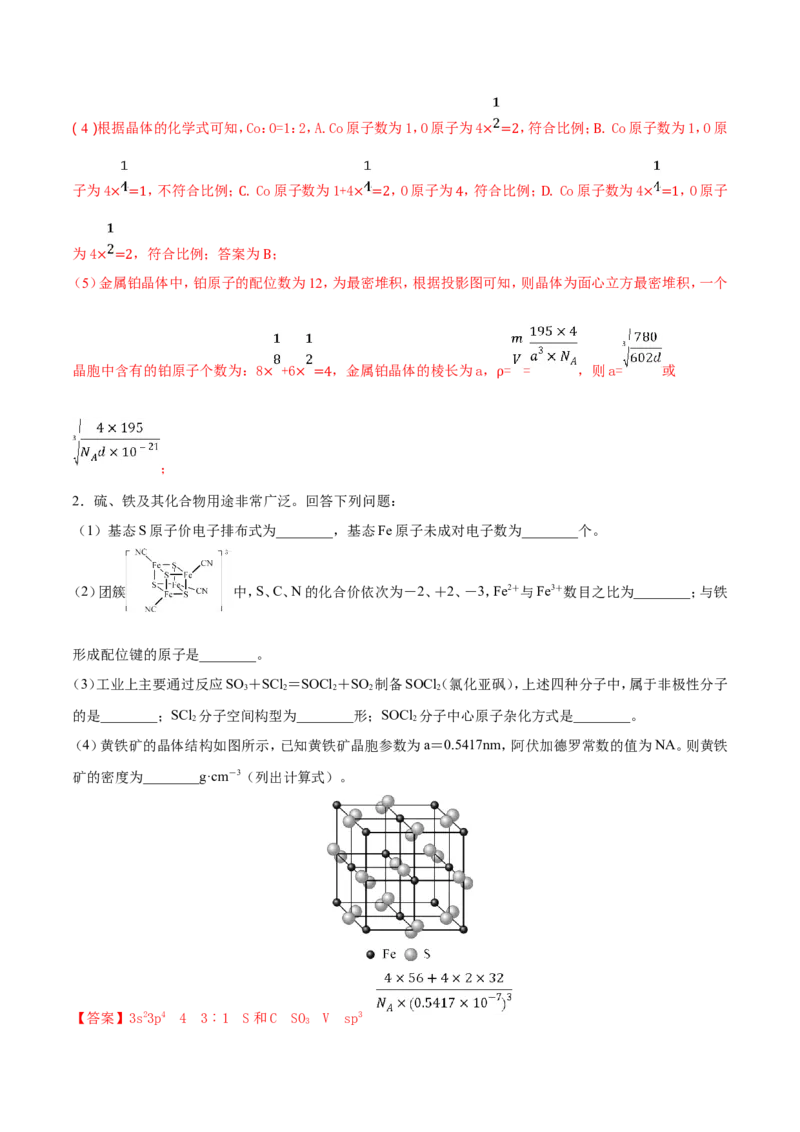
①吡啶分子是大体积平面配体,其结构简式如图所示,每个分子中含有的σ键数目为______。二氯二吡啶合
铂分子中所含的C、N、Cl三种元素的第一电离能由大到小的顺序是______。
②二氯二吡啶合铂中存在的微粒间作用力有______(填字母)。
a.范德华力 b.氢键 c.金属键 d非极性键
③反式二氯二吡啶合铂分子是______(填“极性分子”或“非极性分子”)。
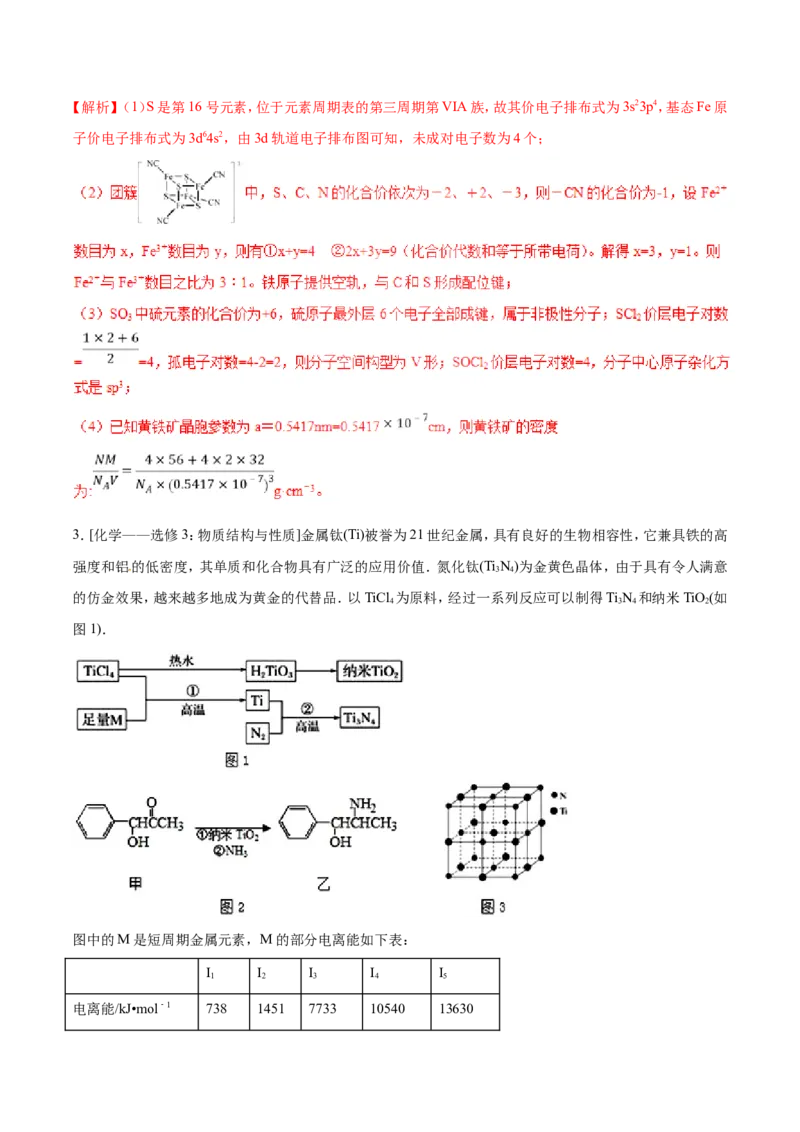
(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构
成能导电的“分子金属”,其结构如图所示。
①“分子金属”可以导电,是因为______能沿着其中的金属原子链流动。②“分子金属”中,铂原子是否以sp3的方式杂化?______(填“是”或“否”),其理由是______。
(4)筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体CoO,该晶体具有层状结构
2
(如图所示,小球表示Co原子,大球表示O原子),图中用粗线画出的重复结构单元示意图不能描述CoO 的
2
化学组成的是______(填字母)。
(5)金属铂品体中,铂原子的配位数为12,其立方晶胞沿式x、y或z轴的投影图如图所示,若金属铂的密度为
dg•m-3,则晶胞参数a=______nm(列计算式)。
【答案】 11 N>Cl>C ad 非极性分子 电子 否 若铂原子轨道为sp3杂
化,则该分子结构为四面体,非平面结构 B 或
(3)①已知,每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,则Pt金属的价电子可
在金属Pt间传递而导电;
②“分子金属”中,铂原子的配位数为4,若铂原子以sp3的方式杂化,则为四面体构型,如图中给定的信息可知,
“分子金属”为平面构型,答案为否;若铂原子轨道为sp3杂化,则该分子结构为四面体,非平面结构;(4)根据晶体的化学式可知,Co:O=1:2,A.Co原子数为1,O原子为4 ,符合比例; Co原子数为1,O原
× =2 B.
子为4 ,不符合比例; Co原子数为1+4 ,O原子为 ,符合比例; Co原子数为4 ,O原子
× =1 C. × =2 4 D. × =1
为4 ,符合比例;答案为 ;
(5)×金属=2铂晶体中,铂原子的配B位数为12,为最密堆积,根据投影图可知,则晶体为面心立方最密堆积,一个
晶胞中含有的铂原子个数为:8 +6 ,金属铂晶体的棱长为a, = = ,则a= 或
× × =4 ρ
;
2.硫、铁及其化合物用途非常广泛。回答下列问题:
(1)基态S原子价电子排布式为________,基态Fe原子未成对电子数为________个。
(2)团簇 中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为________;与铁
形成配位键的原子是________。
(3)工业上主要通过反应SO +SCl =SOCl +SO 制备SOCl(氯化亚砜),上述四种分子中,属于非极性分子
3 2 2 2 2
的是________;SCl 分子空间构型为________形;SOCl 分子中心原子杂化方式是________。
2 2
(4)黄铁矿的晶体结构如图所示,已知黄铁矿晶胞参数为a=0.5417nm,阿伏加德罗常数的值为NA。则黄铁
矿的密度为________g·cm-3(列出计算式)。
【答案】3s23p4 4 3︰1 S和C SO V sp3
3【解析】(1)S是第16号元素,位于元素周期表的第三周期第VIA族,故其价电子排布式为3s23p4,基态Fe原
子价电子排布式为3d64s2,由3d轨道电子排布图可知,未成对电子数为4个;
3.[化学——选修3:物质结构与性质]金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高
强度和铝的低密度,其单质和化合物具有广泛的应用价值.氮化钛(Ti N)为金黄色晶体,由于具有令人满意
3 4
的仿金效果,越来越多地成为黄金的代替品.以TiCl 为原料,经过一系列反应可以制得Ti N 和纳米TiO(如
4 3 4 2
图1).
图中的M是短周期金属元素,M的部分电离能如下表:
I I I I I
1 2 3 4 5
电离能/kJ•mol﹣1 738 1451 7733 10540 13630[来源:学§科§网]
请回答下列问题:
(1)Ti的基态原子外围电子排布式为_____________.
(2)M是_____(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为_____。
(3)纳米TiO 是一种应用广泛的催化剂,纳米TiO 催化的一个实例如图2所示.化合物甲的分子中采取sp2方
2 2
式杂化的碳原子有__ 个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为
________________。
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮
化钛的密度为____________________g•cm﹣3(N 为阿伏加德罗常数的值,只列计算式)。该晶体中与N原子距
A
离相等且最近的N原子有__________。
(5)科学家通过X﹣射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶
格能数据如下:
离子晶体 NaCl KCl CaO
晶格能/kJ•mol﹣1 786 715 3401
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为_____________________.
【答案】3d24s2 Mg 12 7 O>N>C 12 TiN>CaO>KCl
(4)根据均摊法,可知该晶胞中N原子个数为:6×1/2+8×1/8=4,该晶胞中Ti原子个数为:1+12×1/4=4,所以
晶胞的质量m= g,而晶胞的体积V=(2a×10-10)3cm3,所以晶体的密度ρ= ;以晶胞顶点N原子研究,与之距离相等且最近的N原子处于面心位置,每个顶点为8个晶胞共用,每个面为2个晶胞共
用,故与之距离相等且最近的N原子为 =12;
(5)离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有TiN>CaO,由表中数
据可知CaO>KCl,则TiN>CaO>KCl。
4.[化学——选修3:物质结构与性质]
近年来随着石墨烯等二维层状纳米材料研究热潮的兴起,二维层状化合物——类石墨烯二硫化钼引起了物
理、化学、材料、电子等众多领域研究人员的广泛关注。类石墨烯二硫化钼有类似石墨烯的片状结构,单层或
多层二硫化钼可组成具有“夹心三明治”式的层状结构的化合物。
目前合成方法主要有:
方法l:一定量NaMoO 、S粉、NH·H O和去离子水在一定条件合成纳米级二硫化钼。
2 4 2 4 2
方法2:以MoO 和KSCN为原料,在一定条件下合成二硫化钼。
3
请回答下列问题:
(1)在周期表中,钼位于第五周期且与铬同族。基态钼原子价电子排布图为_________,它的核外有
___________个运动状态不同的电子。
(2)“三明治”式层状结构的二硫化钼晶体中,单层MoS 结构内存在的作用力是___;层与层之间存在的作
2
用力是_____。
(3)方法l使用原料含有的相关元素中,N、O、S原子的第一电离能由小到大排序为__,从原子结构的角度分
析,原因是______。
(4)方法2中使用了KSCN,与 SCN−互为等电子体的分子有___________(写一种即可)。已知SCN−中每个
原子最外层都达到8电子稳定结构且为直线形,l mol SCN−中含π键的数目为___________。SCN− 可参与配
合物的形成,其中可作配位原子的是_________。
(5)金属钼的晶胞结构如图所示,其晶胞堆积模型是___________;已知钼晶体密度为ρ g·cm−3,用N 表示阿
A
伏加德罗常数的值,则金属钼的晶胞中两个钼原子的最小核间距为___________pm。【答案】 42 极性共价键(或共价键) 范德华力(或分子间作用力) SH>Cu 3:1 小于 ( , , ) 4 平面正方形 ×1010
【解析】(1)原子的核外电子离核越近能量越低,离核越远能量越高,故D项所示的核外排布图能量最高,故
D项正确,
答案为:D;
(2)①该离子中,氮原子和氮原子之间、碳原子和碳原子之间都存在非极性键,碳原子和氮原子之间、氮原子
和氢原子之间、碳原子和氢原子之间都存在极性键,铜原子和氮原子间存在配位键;
故答案为:ACD;
(2)一个共价单键由一个σ键组成,一个共价双键由一个σ键与一个π键组成,而甲醛分子的结构式为:
,其分子内所含σ键的个数为3,π键个数为1,因此σ键与π键个数之比为3:1;甲醛中C原子形
成3个σ键,为sp2杂化,是平面三角形结构,键角为120,甲醇分子内碳原子形成4个σ键,无孤电子对,杂
∘
化方式为sp3杂化,是四面体结构,O−C−H键角约为10928′,键角小于120 ,所以甲醇分子内O−C−H键角比
∘
甲醛分子内O−C−H键角小, ∘故答案为:3:1;小于;
(4)①对照晶胞图示、坐标系及A、B点坐标,选A为参照点,P在晶胞内的体心处,由空间立体几何关系可推
知D的坐标为:( , , ),
故答案为:( , , );
②该晶体中距离Cu原子最近的Sn原子有4个,这些Sn原子所呈现的构型为平面正方形,
故答案为:4;平面正方形;
③由均摊法可知,该晶体的一个晶胞中有1个Sn、3个Cu和1个P原子,故该晶胞的摩尔质量为 342 g/mol,
则一个晶胞质量 g,设立方体边长为x,铜原子间最近距离为d,则d2=( )2+( )2,d = x,结合密度ρ= ,
V = x3 = = cm3,x = cm,则d = x = cm = ×1010 pm,
故答案为: ×1010。
9.(化学——选修3:物质结构与性质)
2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分
子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB族元素对应离子的萃取,如La3+、Sc2+。写出基态二价钪离子
(Sc2+)的核外电子排布式:________,其中电子占据的轨道数为________个。
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为________,羟基间的相互作用力
为________。
(3)不同大小的苯芳烃能识别某些离子,如: 、SCN-等。一定条件下,SCN-与MnO 反应可得到(SCN) ,试
2 2
写出(SCN) 的结构式______________________________。
2
(4)NH 分子在独立存在时H-N-H键角为106.7°。如图 [Zn(NH )]2+离子的部分结构以及H-N-H键角
3 3 6
的测量值。解释配合物中H-N-H键角变为109.5°的原因:______。
(5)橙红色的八羰基二钴[Co (CO) ]的熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂。该晶体属于________
2 8
晶体,八羰基二钴在液氨中被金属钠还原成四羰基钴酸钠[NaCo(CO) ],四羧基钴酸钠中含有的化学键为
4_________________。
(6)已知C 分子结构和C 晶胞示意图(如图Ⅱ、图Ⅲ所示):
60 60
则一个C 分子中含有σ键的个数为________,C 晶体密度的计算式为________ g·cm-3。(N 为阿伏伽德罗
60 60 A
常数的值)
【答案】1s22s22p63s23p63d1或[Ar]3d1 10 sp3 氢键 N≡C—S—S—C≡N 氨分子与Zn2+形成配合物后,
孤对电子与Zn2+成键,原孤对电子与键对电子间的排斥作用变为键对电子间的排斥,排斥减弱,故H-N-H
键角变大 分子 离子键、配位键、极性键 90 4×12×60×1030/(a3×N )
A
【解析】(1)Sc是21号元素,核外电子排布式为[Ar]3d14s2,则Sc2+的电子排布式为1s22s22p63s23p63d1或
[Ar]3d1;s能级有1个轨道,p能级有3个轨道,d能级只有1个电子,占有1个轨道,因此电子占据的轨道有
1+1+3+1+3+1 = 10个,
故答案为:1s22s22p63s23p63d1或[Ar]3d1;10;
故答案为:氨分子与Zn2+形成配合物后,孤对电子与Zn2+成键,原孤对电子与键对电子间的排斥作用变为键
对电子间的排斥,排斥减弱,故H-N-H键角变大;
(5)熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂,则可知Co (CO) 属于分子晶体;
2 8NaCo(CO) 内,存在钠离子与Co(CO) -阴离子,在Co(CO) -内界有CO与中心钴离子形成配位键,而配体内部
4 4 4
C原子与O原子之间存在极性共价键,所以四羧基钴酸钠中含有的化学键为离子键、配位键、极性键,
故答案为:分子;离子键、配位键、极性键;
(4)根据C 分子结构,C 分子中1个碳原子有2个C-C键、1个"C=C",根据均摊法,一个碳原子真正含有
60 60
的σ键的个数为 ,即一个C 分子中含有σ键的个数为60× = 90;根据C 晶胞结构,离C 最近的C 上面
60 60 60 60
有4个,中间有4个,下面有4个,即有12个;C 的个数为8×1/8+6×1/2=4,晶胞的质量为
60
= g,晶胞的体积为(a×10-10)3 = a3×10-30 cm3,根据密度的定义,晶胞的密度计算式为
= 4×12×60×1030/(a3×N ),
A
故答案为:4×12×60×1030/(a3×N )。
A
10.铜、银和金是日常生活中常用金属
(1)基态铜原子的价层电子排布式为___________.
(2)银氨溶液主要成分是[Ag(NH )]OH,配制方法是,向AgNO 溶液中滴加氨水至沉淀刚好完全溶解为止,
3 2 3
得到澄清的银氨溶液
①AgNO 中阴离子的空间构型是_______________;
3
②[Ag(NH )]+中银离子的配位数为___________;NH 分子中N的杂化类型是__________。
3 2 3
③与NH 互为等电子体的离子有:_____________。
3
(3)现代工业冶金中,2Au(CN)-+Zn====2Au+Zn(CN)2-。CN-是常见的配体,提供孤电子对是C不是N,
2 4
其主要原因是_________________________________。
(4)铜、银是有机反应常见的催化剂如 CHCHOH CHCHO+H ↑。CHCHOH的沸点高于
3 2 3 2 3 2
CHCHO的主要原因是________;从原子轨道重叠方式分类,H 分子中σ键类型是____________。
3 2
(5)一种铜镍合金(俗称白铜)的晶胞如图1所示,铜、镍原子个数比为___________。(6)金晶胞如图2所示,这种晶体堆积方式称为___________堆积。该晶胞中原子空间利用率( )为
___________ (用π含的式子表示),(提示原子空间利用率= )
【答案】3d104s1 平面三角形 2 sp3 HO+ C的电负性比N小,吸引孤电子对的能力比N弱 乙
3
醇分子间形成氢键 s-s 3:1 面心立方最密
(4)H 中H与H原子只有σs-s键。
2
(5)面心立方中,顶点贡献率为1/8,面心贡献率为1/4,一个晶胞含3个铜原子、1个镍原子,因此铜、镍原子
个数比为3:1。
(6)设金原子半径为r,晶胞参数为a。面心立方晶胞中,面对角线上3个金原子相切,有:(4r)2=2a2,r= a,1个
金晶胞含4个金原子, =
11.决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca (PO )F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能
5 4 3
量(即电离能,用符号I 至I 表示)如表所示:
1 5I I I I I
1 2 3 4 5
电离能 589.8 1145.4 4912.4 6491 8153
元素M化合态常见化合价是_________价,其基态原子电子排布式为_________。
(2)Ca (PO )F中非金属元素电负性由大到小的顺序为_________。
3 4 3
(3)PO 3-的中心原子的杂化方式为_________,该离子的空间构型为_________,键角为________,其等电子体
4
有_________ (请写出两种)。
(4)CaF 晶胞结构如图所示,则CaF 晶体中与Ca2+最近且等距离的Ca2+数目为_________;已知Ca2+和F−半径
2 2
分别为a cm、b cm,阿伏加德罗常数为N ,M为摩尔质量,则晶体密度为________g·cm−3(不必化简)。
A
(5)已知MgO与CaO的晶体结构相似,其摩氏硬度的大小关系为_________,原因为___________。
【答案】+2 [Ar]4s2 F>O>P sp3 正四面体形 109°28′ SO 2-、CCl 等 12 MgO>CaO
4 4
Mg2+半径比Ca2+小,晶格能较大
(2)Ca (PO )F中非金属元素有P、O、F三种,元素的非金属性F>O>P,元素的非金属性越强,其电负性就越大,
3 4 3
所以按电负性由大到小的顺序排列为F>O>P;
(3) PO3-的中心原子P的价层电子对数是4,故P原子杂化为sp3杂化;由于孤对电子对数为0,该离子的空间
4
构型为正四面体形,键角为109°28′,其等电子体有SO 2-、CCl ;
4 4
(4)根据CaF 晶胞结构可知:在每个晶胞中与Ca2+离子距离最近且等距离的Ca2+有3个,通过每个Ca2+可形成
2
8个晶胞,每个Ca2+计算了2次,所以与Ca2+离子距离最近且等距离的Ca2+有(3×8)÷2=12个;将CaF 晶胞分成
28个小正方体,正方体中心为F-离子,顶点为Ca2+,晶胞中共有4个钙离子、8个氟离子。立方体的对角线为
2(a+b),则晶胞的对角线为4(a+b),晶胞的边长为 ,根据晶体密度计算公式可得该晶体的密度 =
g/cm3;
(5)MgO与CaO的晶体结构相似,由于离子半径Ca2+>Mg2+,离子半径越大,与O2-形成的离子键的键长就越大,
晶格能就越小,物质的硬度就越小,故其摩氏硬度的大小关系为MgO>CaO。
12.CaF 、CaC 都是工业生产的重要物质。回答下列问题:
2 2
(1)基态钙原子的电子排布式___________,钙原子核外有___________种能量状态的电子。
(2)CaC 与水反应生成乙炔(C H),乙炔中碳原子的杂化类型为___________,乙炔中的σ键与π键数之比为
2 2 2
___________。
(3)CaF 与浓HSO 反应生成HF,HF的沸点高于C H,原因是:___________;HF能的BF 化合得到HBF ,从
2 2 4 2 2 3 4
化学键形成角度分析HF与BF 能化合的原因___________。
3
(4)NO F分子与BF 互为等电子体,则NO F分子的立体构型为______________________。
2 3 2
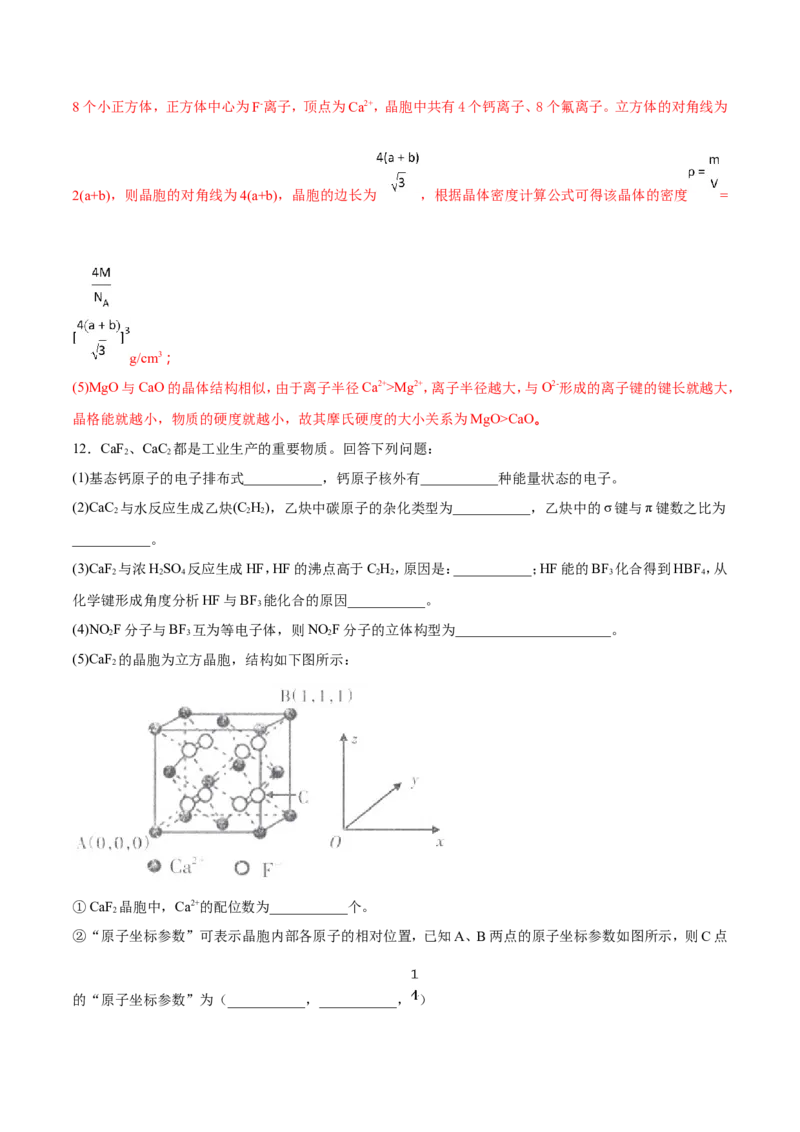
(5)CaF 的晶胞为立方晶胞,结构如下图所示:
2
①CaF 晶胞中,Ca2+的配位数为___________个。
2
②“原子坐标参数”可表示晶胞内部各原子的相对位置,已知A、B两点的原子坐标参数如图所示,则C点
的“原子坐标参数”为(___________,___________, )③晶胞中两个F-的最近距离为273.1pm,用N 表示阿伏加德罗常数,则晶胞的密度为___________g/cm3(列出
A
计算式即可)。
【答案】[Ar]4s2 6 sp 3:2 HF分子之间存在氢键 BF 中硼原子有空轨道,HF中氟原子有孤对电子,
3
两者之间可形成配位键 平面三角形 8
在BF 分子中的B原子上有空轨道,而HF分子中的F原子上有孤对电子,当BF 与HF靠近时,HF分子中F
3 3
原子的孤对电子填充BF 分子中B原子的空轨道,二者形成配位键,从而结合形成HBF ;
3 4
(4)BF 分子中B原子的价层电子对数为3+ =3,没有孤电子对,所以分子的空间构型是平面三角形,
3
而NO F与BF 是等电子体,二者结构相似,所以NO F分子的空间构型也是平面三角形;
2 3 2
(5)以面心Ca2+为研究对象,在一个晶胞中连接4个F-,通过该Ca2+可形成2个晶胞,所以与该Ca2+距离相等且
最近的F-共有8个,因此Ca2+的配位数是8;
观察A、B、C的相对位置,可知C点的x轴坐标是 ,y轴坐标是 ,z轴坐标是 ;
根据晶胞结构可知,在一个晶胞中含有Ca2+: ,含有F-:1×8=8,即一个晶胞中含有4个
CaF ,根据C点的坐标可知:晶胞中F-离子之间的距离为晶胞边长的一半,所以晶胞参数
2
L=2×273.1pm=546.2pm,则该晶胞的密度为 = = g/cm3。
13.硼元素对植物生长及人体健康有着十分重要的作用,硼的化合物被广泛应用于新材料制备、生活生产等
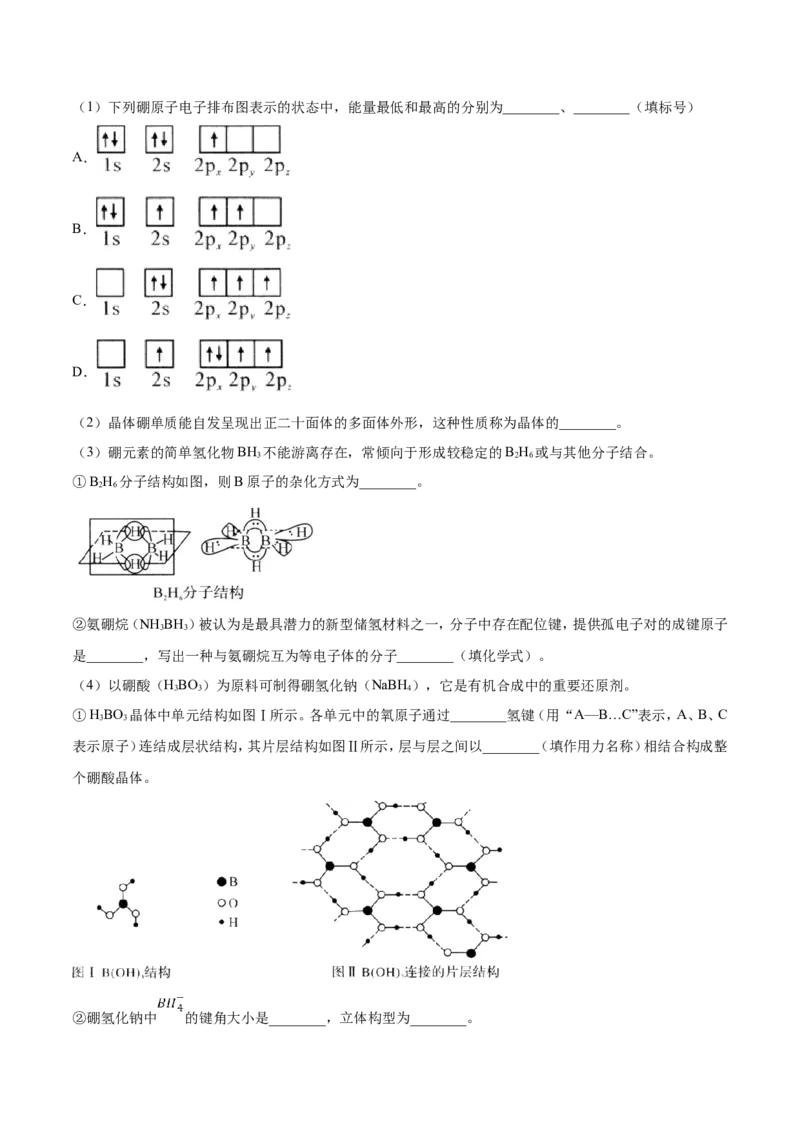
诸多领域。(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为________、________(填标号)
[来源:Zxxk.Com]
A.
B.
C.
D.
(2)晶体硼单质能自发呈现出正二十面体的多面体外形,这种性质称为晶体的________。
(3)硼元素的简单氢化物BH 不能游离存在,常倾向于形成较稳定的B H 或与其他分子结合。
3 2 6
①B H 分子结构如图,则B原子的杂化方式为________。
2 6
②氨硼烷(NH BH)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子
3 3
是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。
(4)以硼酸(HBO)为原料可制得硼氢化钠(NaBH ),它是有机合成中的重要还原剂。
3 3 4
①HBO 晶体中单元结构如图Ⅰ所示。各单元中的氧原子通过________氢键(用“A—B…C”表示,A、B、C
3 3
表示原子)连结成层状结构,其片层结构如图Ⅱ所示,层与层之间以________(填作用力名称)相结合构成整
个硼酸晶体。
②硼氢化钠中 的键角大小是________,立体构型为________。③根据上述结构判断下列说法正确的是________
a.HBO 分子的稳定性与氢键有关
3 3
b.硼酸晶体有滑腻感,可作润滑剂
c.HBO 分子中硼原子最外层为8e-稳定结构
3 3
d.含1mol HBO 的晶体中有3 mol氢键
3 3
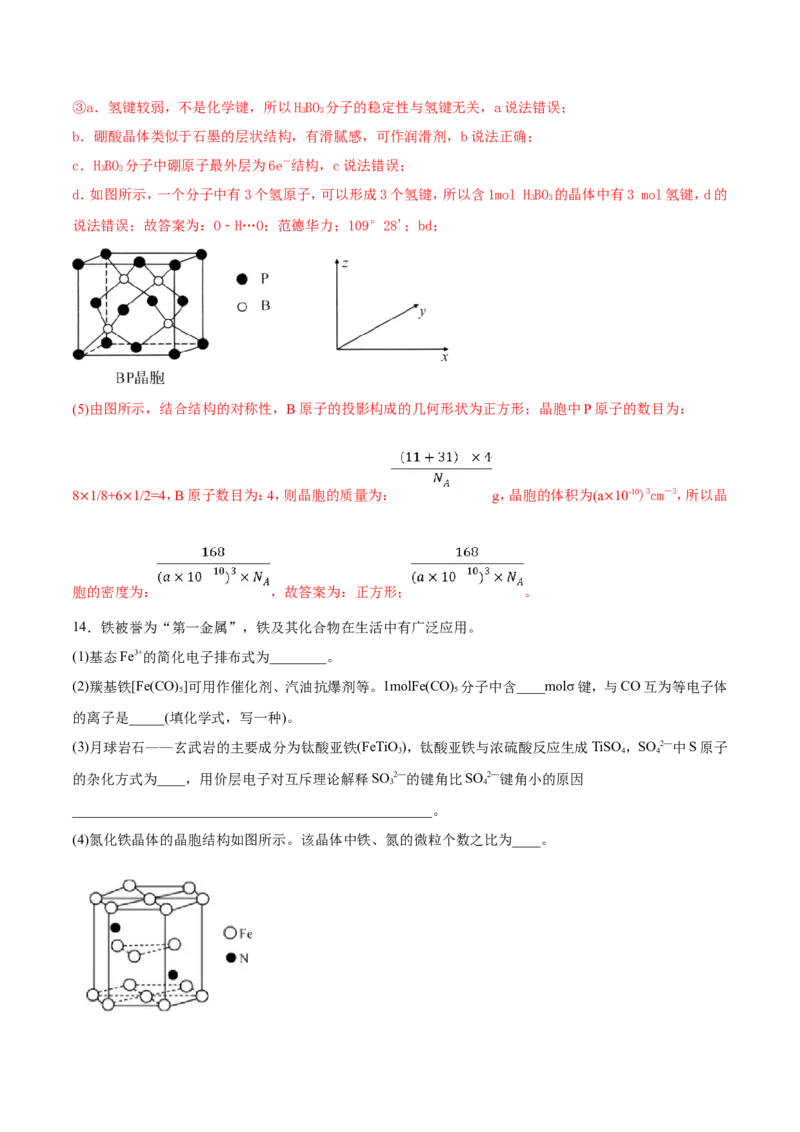
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图
所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是________;已知晶胞边长为a pm,则磷
化硼晶体的密度是________g·cm-3(列出含a、N 的计算式即可)。
A
【答案】A D 自范性 sp3杂化 N CH O﹣H…O 范德华力 109°28' 正四面体 bd 正方
2 6
形
(4)①根据HBO 晶体中单元结构知,各单元中的氧原子通过 O﹣H…O连结成层状结构;如图Ⅱ所示,层与层
3 3
之间没有化学键,以范德华力相结合构成整个硼酸晶体;
②硼氢化钠中 与甲烷为等电子体,所以键角和甲烷中键角相同,大小是109°28'; 立体构型为正四面
体;③a.氢键较弱,不是化学键,所以HBO 分子的稳定性与氢键无关,a说法错误;
3 3
b.硼酸晶体类似于石墨的层状结构,有滑腻感,可作润滑剂,b说法正确;
c.HBO 分子中硼原子最外层为6e-结构,c说法错误;
3 3
d.如图所示,一个分子中有3个氢原子,可以形成3个氢键,所以含1mol HBO 的晶体中有3 mol氢键,d的
3 3
说法错误;故答案为:O﹣H…O;范德华力;109°28';bd;
(5)由图所示,结合结构的对称性,B原子的投影构成的几何形状为正方形;晶胞中P原子的数目为:
8 1/8+6 1/2=4,B原子数目为:4,则晶胞的质量为: g,晶胞的体积为(a 10-10)3cm-3,所以晶
× × ×
胞的密度为: ,故答案为:正方形; 。
14.铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的简化电子排布式为________。
(2)羰基铁[Fe(CO) ]可用作催化剂、汽油抗爆剂等。1molFe(CO) 分子中含____molσ键,与CO互为等电子体
5 5
的离子是_____(填化学式,写一种)。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO),钛酸亚铁与浓硫酸反应生成TiSO,SO 2—中S原子
3 4 4
的杂化方式为____,用价层电子对互斥理论解释SO 2—的键角比SO 2—键角小的原因
3 4
___________________________________________________。
(4)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为____。(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,N 代表阿伏加德罗常数的值。在
A
该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为____;Fe2+与O2—的最短核间距为____pm。
【答案】[Ar]3d5 10 CN-或C2- SP3杂化 SO2-中孤电子对对成键电子对的排斥比SO2-中的成键电
2 3 4
子对间的排斥作用大 3:1 12 (36/ρ×N )1/3×1010
A
(4)氮化铁晶胞为六棱柱,顶点贡献率为1/6,棱点贡献率为1/3,面点贡献率为1/2,观察晶胞可知,12个铁位
于顶点,2个铁位于面心,3个铁位于体内,2个N位于体内,用“均摊法”可知,1个晶胞中含铁微粒数:
12×1/6+2×1/2+3=6个,含氮微粒数:2个,该晶体中铁、氮的微粒个数之比为=6:2=3:1,
故答案为:3:1。
(5)根据晶胞图可知,氧化亚铁晶胞类似氯化钠晶胞,棱上3个离子相切,晶胞参数等于相邻两个离子核间距
的2倍。上、中、下三层各4个氧离子(共12个氧离子)与中心的氧离子紧邻且等距离,用“均摊法”,晶胞中
含Fe2+:8×1/8+6×1/2=4个,含O2-:12×1/4+1=4个,晶胞的化学式为FeO,氧化亚铁中氧离子、亚铁离子个
数比为1:1,所以,有12个Fe2+与Fe2+紧邻且等距离。1个氧化亚铁晶胞中含4个FeO,设Fe2+与O2-的最短核
间距为dpm,1molFeO的质量为72g,氧化亚铁晶体的密度为ρgcm-3,则有ρ=m/V=72×4/N(2d×10-10)3,解
A
得d=(36/ρ×N )1/3×1010pm,所以Fe2+与O2-的最短核间距为(36/ρ×N )1/3×1010pm,故答案为:12;
A A
(36/ρ×N )1/3×1010pm。
A15.我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外未成对电子数为____。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,
其碳原子的杂化方式为____。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子
属____分子(选填“极性”“非极性”),其中心原子的VSEPR构型为____。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co (CO) ,是一种重要的无机金属配合物,可溶于多数有机
2 8
溶剂。该晶体属于______晶体,三种元素电负性由大到小的顺序为(填元素符号)____。配体CO的任意一种
等电子体的电子式:_________。配体CO中与Co形成配位键的原子是C非O,原因是_________。
(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如图所示,分子内的作用力不可能含
有__________(填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键 F. 范德华力
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的密度为ρ g·cm-3,则每个钨原子的半径r
=____nm。(只需列出计算式) 。
【答案】3 sp2 极性 平面三角形 分子 O>C>Co N、CN-、O2+、C2-等电子式如:氮气的电子式为:
2 2 2
,CN-的电子式这 C原子半径比O大,电负性小,对孤对电子吸引较弱,更容易形
成配位键 ACF × ×107
[来源:学科网ZXXK](3)羰基钴熔点低,溶于有机溶剂,属于分子晶体;同周期主族元素自左而右电负性增大,一般非金属性越强
电负性越大,故电负性:O>C>Co,CO与氮气分子互为等电子体,其结构式为C≡O,三键含有1个键、2个
π键,氮气的电子式为: ,CN-的电子式这 。配体CO中与Co形成配位键的原子是C非
O,原因是C原子半径比O大,电负性小,对孤对电子吸引较弱,更容易形成配位键。
(4)Ni与N原子之间形成配位键,非金属原子之间形成共价键,氢键中H与O可能形成氢键,没有离子键、
金属键、范德华力,故选ACF;
(5)处于体对角线上原子紧密相邻,体对角线长度等于原子半径的4倍,体对角线长度等于晶胞棱长的 倍,
晶胞中W原子数目=1+8×1/8=2,晶胞质量=2×184/Ng,晶胞体积=2×184/N g÷ρ
A A
g·cm-3=2×184/ρNcm3,晶胞棱长= cm,故每个钨原子的半径r=1/4× × cm,即 ×
A
×107nm
16.氮及其化合物在科学研究和化工生产等领域都有着广泛的应用。请回答下列问题:
(1)与氮元素同族的第四周期元素的基态原子价层电子轨道表达式为___________。
(2)尿素分子的结构简式为:CO(NH),该分子中σ键数目为___________,实验测得:分子中的所有原子在
2 2
同一平面内,尿素中的碳氧键(125pm)比典型的碳氧双键(121pm)长,而尿素中的碳氮键(137pm)比典型的
碳氮单键(147pm)短,说明分子中存在____________。
(3)氨分子构型为_________,氨晶体中,氨分子中的每个H 均参与一个氢键的形成,1 mol固态氨中有
_____mol氢键。
(4)通常认为Cu N是离子晶体,其晶格能可通过图(a)的Born-Haber循环计算得到。
3
可知, Cu原子的第一电离能为_____kJ∙mol−1,N≡N键键能为_____kJ∙mol−1,Cu N晶格能为_____kJ∙mol−1。
3
(5)Cu N晶体的晶胞如图(b)所示。晶胞边长为anm,晶胞中N3- 位于Cu+所形成的正八 面体的体心,该正八
3面体的边长为____nm。
【答案】 7 π6 三角锥形 3 756 936 5643 a
4
【解析】(1)与氮元素同族的第四周期元素为As,其原子价层电子轨道式为 ;
(2)尿素的结构简式为 ,成键原子之间只能形成一个σ键,因此该尿素分子中含有σ键的
数目为7,实验测得:分子中的所有原子在同一平面内,尿素中的碳氧键(125pm)比典型的碳氧双键(121pm)
长,而尿素中的碳氮键(137pm)比典型的碳氮单键(147pm)短,类似与苯中碳碳键介于碳碳单键和碳碳双键
之间的键,说明尿素分子中氮原子的孤电子对与C=O中的π键形成了一个4中心6电子的离域大π键,即
分子中含有π6;
4
(4)根据第一电离能的定义,Cu原子的第一电离能为2268/3kJ·mol-1=756kJ·mol-1;键能是形成1mol化学
键时需要放出最低的热量,即氮氮三键的键能为468kJ·mol-1×2=936kJ·mol-1;设氮化亚铜的晶格能为
U,根据盖斯定律可知,1017+2268+468-1290-U=-3180(注意铜原子变为亚铜离子是吸热的,而氮原子变为氮
离子是放热的),则U=5643kJ·mol-1,所以,Cu N的晶格能为5643kJ·mol-1;
3
(5)晶胞中N3- 位于Cu+所形成的正八面体的体心,白球是Cu+,黑球为N3-,则正八面体的边长为面对角线
为一半,即为 anm。
17.由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态Cl原子核外电子排布式为__________________________,P、S、Cl的第一电离能由大到小顺序为
____________________。
(2)SCl 分子中的中心原子杂化轨道类型是_____________,该分子构型为__________。
2
(3)Ni与CO能形成配合物Ni(CO) ,该分子中配位键个数为_______;以“—”表示σ键、“→”表示配位键,
4该分子空间结构示意图可以画为__________。
(4)已知MgO与NiO的晶体结构(如图1)相同, 其中Mg2+和Ni2+的离子半径分别为66 pm和69pm。则熔点:
MgO_____NiO(填“>”、“<”或“=”),理由是_______________________________。
(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+ 填充其中,
已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______g。(用a、N 表示)
A
【答案】1s22s22p63s23p5 Cl> P > S sp3 V形 1∶1 > Mg2+半径比Ni2+小,MgO的晶格能比NiO大
(1,1/2,1/2) 或
(4)晶体结构相同时,离子半径越小离子键强度越大,Mg2+比Ni2+半径小,MgO的晶格能比NiO大,所以熔点
MgO>NiO。
(5)NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则晶胞是边长为1的正方体,C在右侧面心处,根据立体几何知识,则C离子坐标参数为(1, , )。
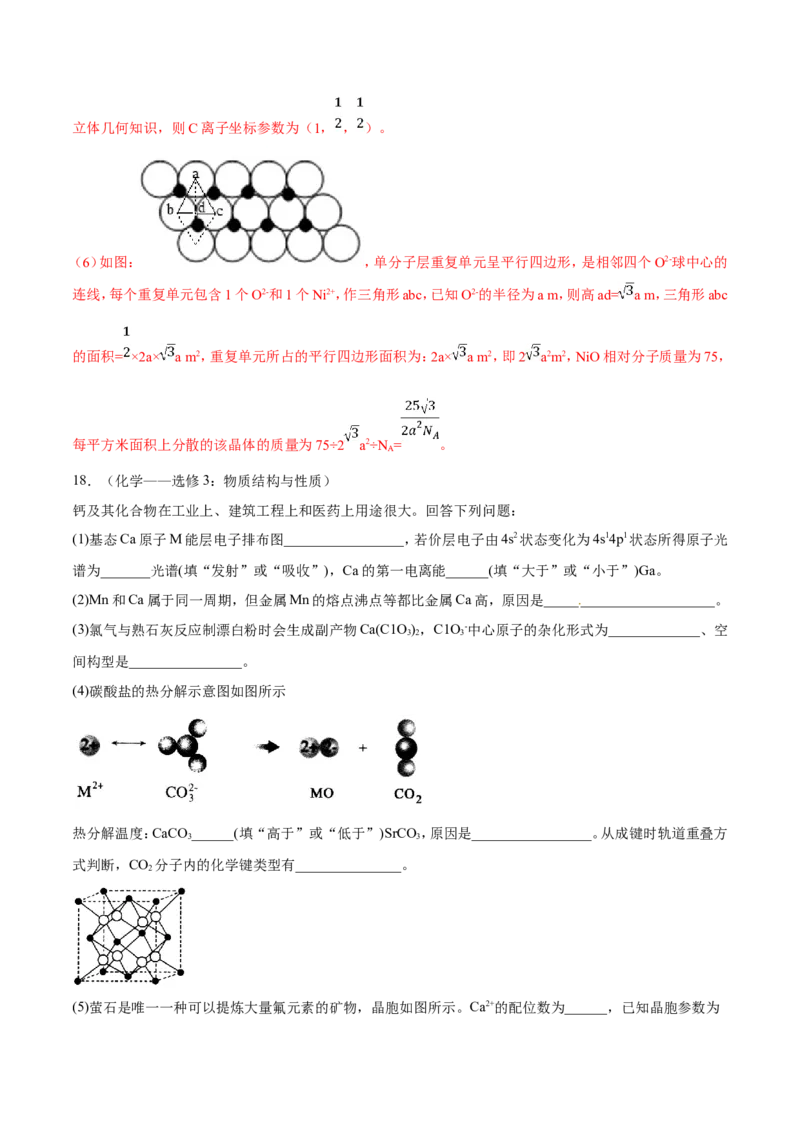
(6)如图: ,单分子层重复单元呈平行四边形,是相邻四个O2-球中心的
连线,每个重复单元包含1个O2-和1个Ni2+,作三角形abc,已知O2-的半径为a m,则高ad= a m,三角形abc
的面积= ×2a× a m2,重复单元所占的平行四边形面积为:2a× a m2,即2 a2m2,NiO相对分子质量为75,
每平方米面积上分散的该晶体的质量为75÷2 a2÷N = 。
A
18.(化学——选修3:物质结构与性质)
钙及其化合物在工业上、建筑工程上和医药上用途很大。回答下列问题:
(1)基态Ca原子M能层电子排布图_________________,若价层电子由4s2状态变化为4s14p1状态所得原子光
谱为_______光谱(填“发射”或“吸收”),Ca的第一电离能______(填“大于”或“小于”)Ga。
(2)Mn和Ca属于同一周期,但金属Mn的熔点沸点等都比金属Ca高,原因是________________________。
(3)氯气与熟石灰反应制漂白粉时会生成副产物Ca(C1O),C1O-中心原子的杂化形式为_____________、空
3 2 3
间构型是________________。
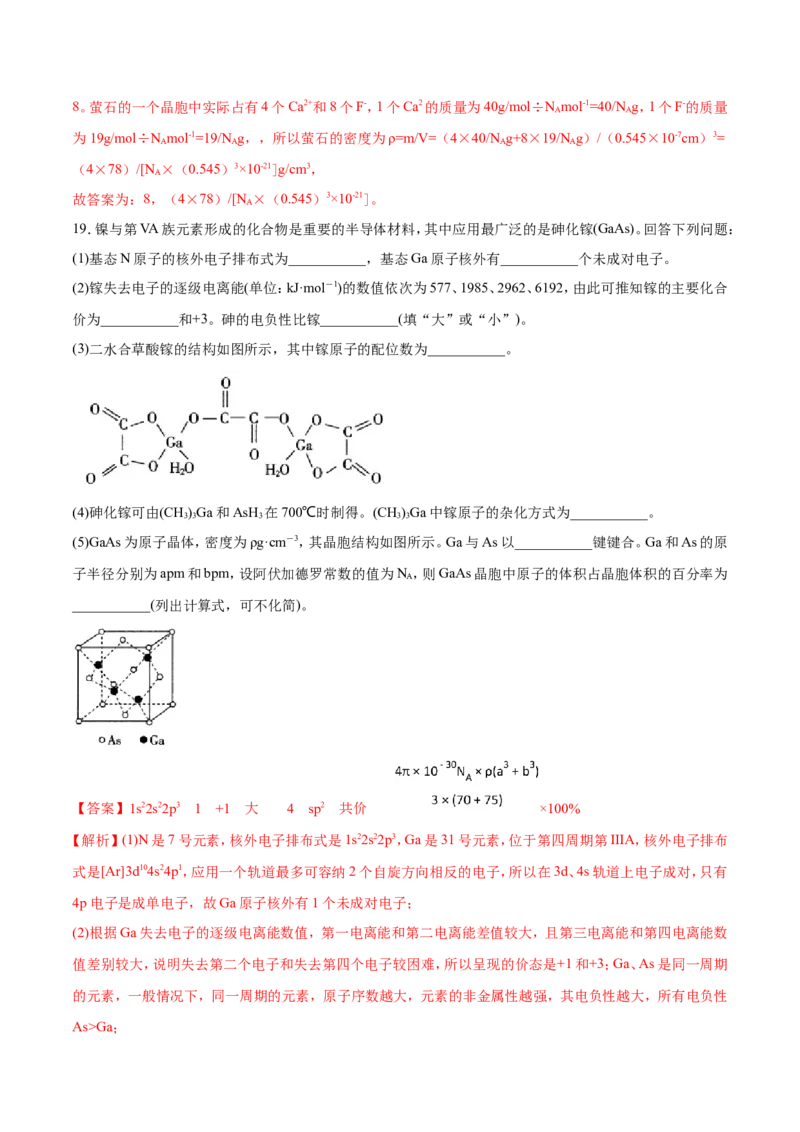
(4)碳酸盐的热分解示意图如图所示
热分解温度:CaCO ______(填“高于”或“低于”)SrCO ,原因是_________________。从成键时轨道重叠方
3 3
式判断,CO 分子内的化学键类型有_______________。
2
(5)萤石是唯一一种可以提炼大量氟元素的矿物,晶胞如图所示。Ca2+的配位数为______,已知晶胞参数为0.545nm,阿伏加德罗常数的值为N ,则萤石的密度为________g· cm-3(列计算式)。
A
【答案】 吸收 大于 Mn原子半径小且价电子数越多,金属键越强 sp3 三角
锥形 低于 (r Ca2+)< (r Sr2+),CaO晶格能大于SrO晶格能,故CaCO 更易分解为CaO σ键、π键
3
8 (4×78)/[N ×(0.545)3×10-21]
A
(2)Mn和Ca属于同一周期,同周期从左至右原子半径逐渐减小,Mn原子的价层电子排布为3d5S2,Ca原子
的价层电子排布为4S2,价电子Mn比Ca多,原子半径越小,价电子越多,金属键越强。所以,金属Mn的熔点
沸点等都比金属Ca高的原因是:Mn原子半径小且价电子数越多,金属键越强,
故答案为:Mn原子半径小且价电子数越多,金属键越强。学#科网
(3)Ca(C1O) 中的阴离子的化学式为C1O-,中心原子氯的孤电子对数为1/2×(7+1-3×2)=1,σ键数=3,中心
3 2 3
原子氯的价层电子对数为1+3=4,根据价层电子对互斥理论,C1O-的空间构型是三角锥形,中心原子氯的杂
3
化形式为sp3,
故答案为:sp3,三角锥形。
(4)由碳酸盐的热分解示意图看出,CaCO 热分解生成CaO,SrCO 热分解生成SrO,CaO和SrO都是离子晶
3 3
体,因为离子半径(r Ca2+)< (r Sr2+),CaO晶格能大于SrO晶格能,故CaCO 更易分解为CaO,所以CaCO 的
3 3
热分解温度低于SrCO ,CO 的分子结构为O=C=O,C=O双键中1条σ键,1条π键,所以CO 分子内的化学
3 2 2
键类型有σ键,π键,
故答案为:低于;r(Ca2+)< r(Sr2+),CaO晶格能大于SrO晶格能,故CaCO 更易分解为CaO;σ键,π键。
3
(5)萤石的化学式为CaF ,即晶胞中钙离子与氯离子个数比为1:2,从晶胞示意图看,每个晶胞中实际占有黑
2
球的个数=8×1/8+6×1/2=4,晶胞中实际占有白球的个数为8,据此可知黑球代表Ca2+,白球代表F-。将该面心
立方体晶胞分割成8个小立方,每个小立方的4个顶点上是Ca2+,体心是F-,先选取1个顶点(Ca2+)作为考查
对象,经过该顶点的小立方体有8个,即与该顶点的Ca2+距离相等且最近的F-共有8个,所以Ca2+的配位数为8。萤石的一个晶胞中实际占有4个Ca2+和8个F-,1个Ca2的质量为40g/mol÷N mol-1=40/N g,1个F-的质量
A A
为19g/mol÷N mol-1=19/N g,,所以萤石的密度为ρ=m/V=(4×40/N g+8×19/N g)/(0.545×10-7cm)3=
A A A A
(4×78)/[N ×(0.545)3×10-21]g/cm3,
A
故答案为:8,(4×78)/[N ×(0.545)3×10-21]。
A
19.镍与第VA族元素形成的化合物是重要的半导体材料,其中应用最广泛的是砷化镓(GaAs)。回答下列问题:
(1)基态N原子的核外电子排布式为___________,基态Ga原子核外有___________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合
价为___________和+3。砷的电负性比镓___________(填“大”或“小”)。
(3)二水合草酸镓的结构如图所示,其中镓原子的配位数为___________。
[来源:Z§xx§k.Com]
(4)砷化镓可由(CH)Ga和AsH 在700℃时制得。(CH)Ga中镓原子的杂化方式为___________。
3 3 3 3 3
(5)GaAs为原子晶体,密度为ρg·cm-3,其晶胞结构如图所示。Ga与As以___________键键合。Ga和As的原
子半径分别为apm和bpm,设阿伏加德罗常数的值为N ,则GaAs晶胞中原子的体积占晶胞体积的百分率为
A
___________(列出计算式,可不化简)。
【答案】1s22s22p3 1 +1 大 4 sp2 共价 ×100%
【解析】 (1)N是7号元素,核外电子排布式是1s22s22p3,Ga是31号元素,位于第四周期第IIIA,核外电子排布
式是[Ar]3d104s24p1,应用一个轨道最多可容纳2个自旋方向相反的电子,所以在3d、4s轨道上电子成对,只有
4p电子是成单电子,故Ga原子核外有1个未成对电子;
(2)根据Ga失去电子的逐级电离能数值,第一电离能和第二电离能差值较大,且第三电离能和第四电离能数
值差别较大,说明失去第二个电子和失去第四个电子较困难,所以呈现的价态是+1和+3;Ga、As是同一周期
的元素,一般情况下,同一周期的元素,原子序数越大,元素的非金属性越强,其电负性越大,所有电负性
As>Ga;20.N、Fe是两种重要的元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态N 原子最高能级的电子云轮廓图形状为_____________;N原子的第一电离能比O原子的大,其原
因是_________________________,基态铁原子的价电子排布图为_______
(2)在高压下氮气会发生聚合得到高聚氮,晶体结构如图所示。晶体中每个氮原子与另外三个氮原子结合形
成空间网状结构。氮原子的杂化轨道类型为_________。这种高聚氮N-N 键的键能为160kJ/mol,而N 的键能
2
为942kJ/mol,其可能潜在的应用是______________________。
(3)叠氮化钠和氢叠氮酸(HN )已一步步进入我们的生活,如汽车安全气囊等。
3
①写出与N-属于等电子体的一种分子__________(填分子式) 。
3
②氢叠氮酸(HN )可由肼(N H)被HNO 氧化制得,同时生成水。下列叙述错误的是___(填标号)
3 2 4 2
A.上述生成HN 的化学方程式为:NH+HNO = HN +2 H O
3 2 4 2 3 2
B.NaN 的晶格能大于KN 的晶格能
3 3
C.氢叠氮酸(HN )和水能形成分子间氢键
3
D.HN 和NH 都是由极性键和非极性键构成的非极性分子。
3 2 4E.HN 分子中四个原子可能在一条直线上
3
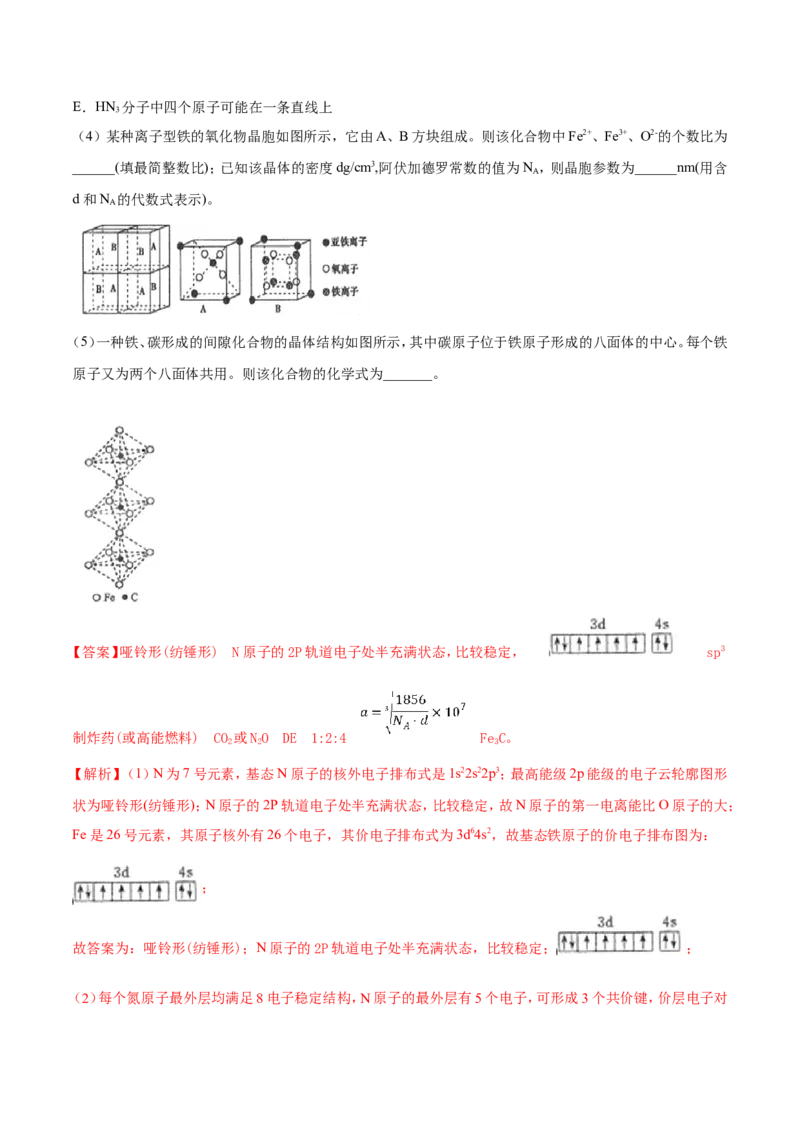
(4)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为
______(填最简整数比);已知该晶体的密度dg/cm3,阿伏加德罗常数的值为N ,则晶胞参数为______nm(用含
A
d和N 的代数式表示)。
A
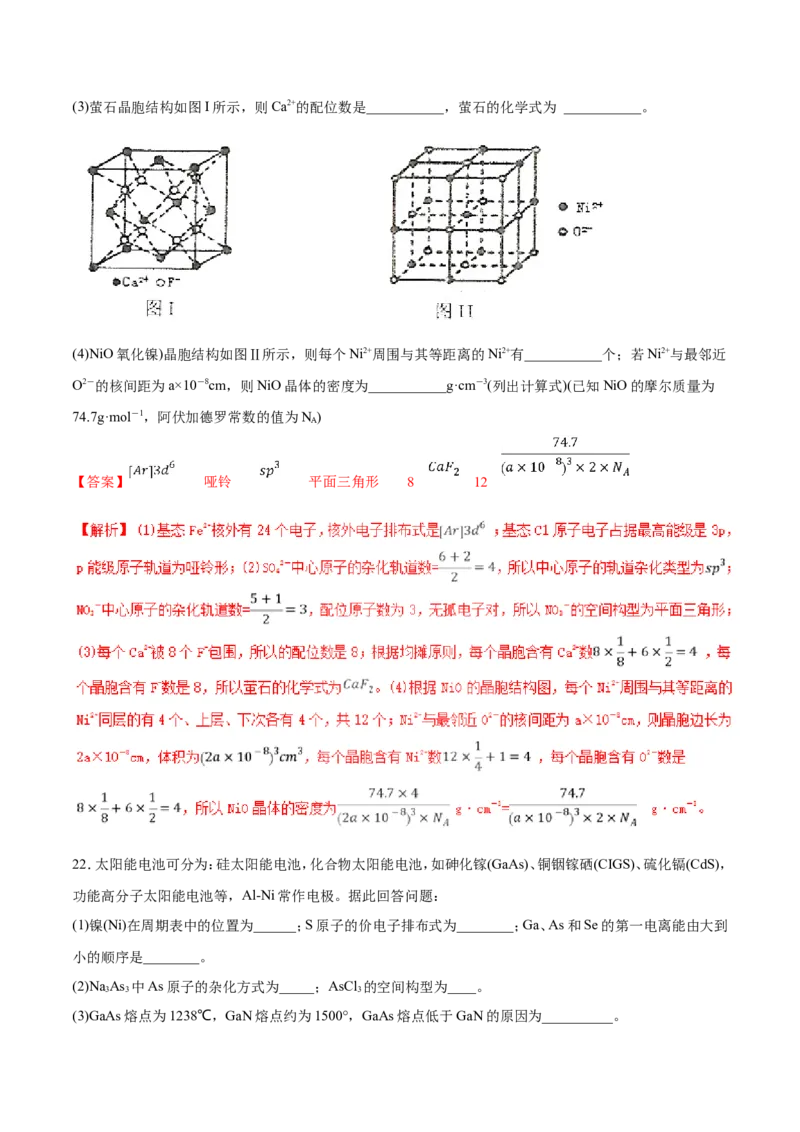
(5)一种铁、碳形成的间隙化合物的晶体结构如图所示,其中碳原子位于铁原子形成的八面体的中心。每个铁
原子又为两个八面体共用。则该化合物的化学式为_______。
【答案】哑铃形(纺锤形) N原子的2P轨道电子处半充满状态,比较稳定, sp3
制炸药(或高能燃料) CO 或NO DE 1:2:4 FeC。
2 2 3
【解析】(1)N为7号元素,基态N 原子的核外电子排布式是1s22s22p3;最高能级2p能级的电子云轮廓图形
状为哑铃形(纺锤形);N原子的2P轨道电子处半充满状态,比较稳定,故N原子的第一电离能比O原子的大;
Fe是26号元素,其原子核外有26个电子,其价电子排布式为3d64s2,故基态铁原子的价电子排布图为:
;
故答案为:哑铃形(纺锤形);N原子的2P轨道电子处半充满状态,比较稳定; ;
(2)每个氮原子最外层均满足8电子稳定结构,N原子的最外层有5个电子,可形成3个共价键,价层电子对个数=σ键个数+孤电子对个数=3+ =4,氮原子的杂化轨道类型为sp3;这种高聚氮N-N 键的键能为
160kJ/mol,而N 的键能为942kJ/mol,其可能潜在的应用是制炸药(或高能燃料);
2
故答案为:sp3;制炸药(或高能燃料);
E.HN 分子结构示意图为 ,靠近H原子的第1个N原子是sp2杂化的,第二个N原
3
子是sp杂化的,端位的N原子不杂化,故四个原子不在一条直线上,E不正确。综上所述,叙述错误的是DE
。
故答案为:CO 或NO;DE;
2 2
(4)A含有1.5个亚铁离子、4个氯离子,B含有0.5个亚铁离子、4个氧离子、4个铁离
子,则该氧化物中Fe2+、Fe3+、O2-的个数比为1:2:4。
晶胞含有Fe2+、Fe3+、O2-的个数分别是为4、8、16,它们的相对质量之和是8×232,根据m= V可得8×232g=
dg/cm3 a3 N,a= 107nm;
A [来源:学科网ZXXK]
故答案为:1:2:4; 107;
(5)根据均摊原则每个铁原子又为两个八面体共用,所以铁与碳原子数比是6 :1=3:1,
则该化合物的化学式为FeC;
3
故答案为:FeC。
3
21.(1)写出基态Fe2+的核外电子排布式______________________;基态C1原子电子占据最高能级的电子云
轮廓图为___________形。
(2)SO 2-中心原子的轨道杂化类型为___________;NO -的空间构型为___________。
4 3(3)萤石晶胞结构如图I所示,则Ca2+的配位数是___________,萤石的化学式为 ___________。
(4)NiO氧化镍)晶胞结构如图Ⅱ所示,则每个Ni2+周围与其等距离的Ni2+有___________个;若Ni2+与最邻近
O2-的核间距为a×10-8cm,则NiO晶体的密度为___________g·cm-3(列出计算式)(已知NiO的摩尔质量为
74.7g·mol-1,阿伏加德罗常数的值为N )
A
【答案】 哑铃 平面三角形 8 12
22.太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),
功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______;S原子的价电子排布式为________;Ga、As和Se的第一电离能由大到
小的顺序是________。
(2)Na As 中As原子的杂化方式为_____;AsCl 的空间构型为____。
3 3 3
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________。(4)写出一种与SO 2-互为等电子体的分子_________。
4
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子
所处空隙类型为_____。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 M g/mol和M g/mol,则
Ga As
GaAs晶胞中Ga之间的最短距离为________pm。
【答案】第四周期第Ⅷ族 3s23p4 As>Se>Ga sp3 三角锥形 均为原子晶体,且GaN中N原子半径小,
Ga-N 键长比Ga-As短,键能更大,熔点更高 CCl 、SiCl 、 SiF、 CF(填其中一种即可) 正四面体形
4 4 4 4
×1010
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN是因为两种晶体均为原子晶体,且GaN中
N原子半径比Ga小,Ga-N 键长比Ga-As短,键能更大,断裂化学键需要的能量大,因此熔点更高;
(4)根据等电子体的概念是原子数相同,最外层电子数也相同的微粒,则SO 2-相应的等电子体是CCl 、SiCl 、
4 4 4
SiF、 CF;
4 4
(5)该晶胞中Ga原子处于与它最近的四个As原子所构成的正四面体的几何中心,因此Ga所处空隙类型为正
四面体;在该晶胞中含有的As原子数目为: =4,含有的Ga原子数目为:1×4=4,因此该晶胞在含有4个GaAs,则晶胞的质量为m= g,由于晶胞的密度为ρg/cm3,所以晶胞的体积为V=
cm3,则晶胞的边长L= cm= ×1010pm。在该晶体在两个Ga原子
之间的距离为晶胞边长的 倍,所以两个Ga原子之间的距离为 ×1010pm。
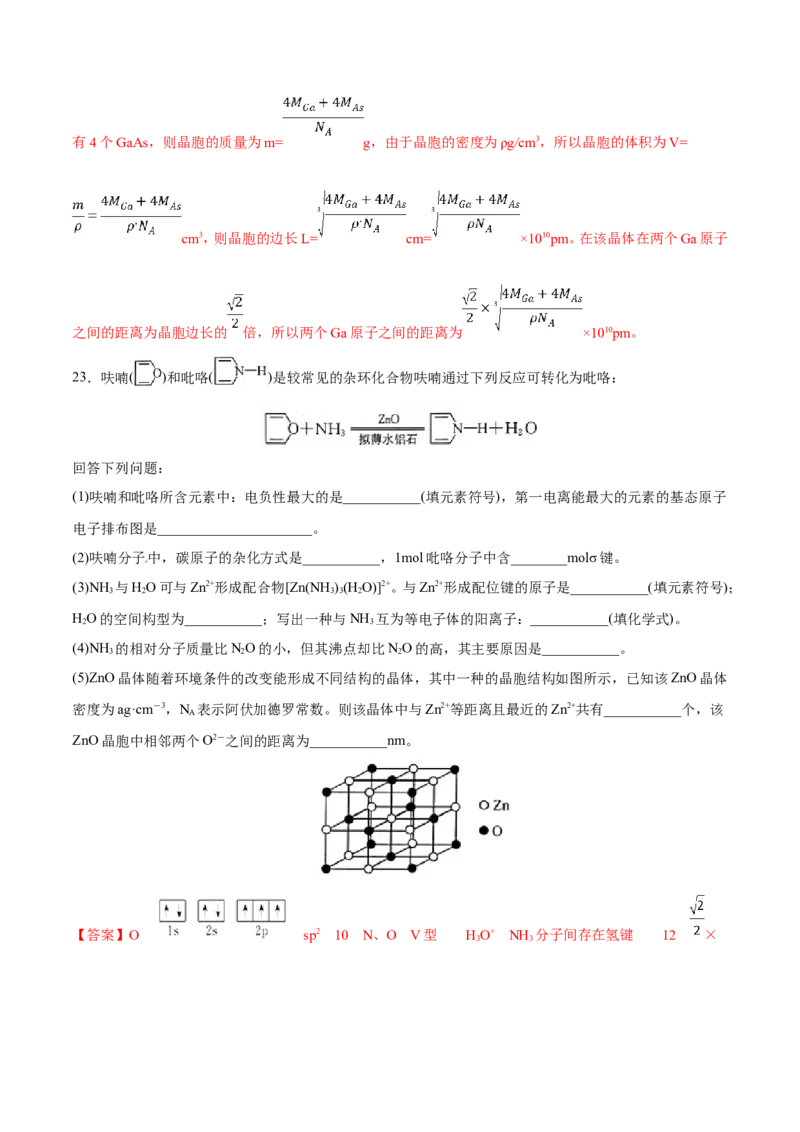
23.呋喃( )和吡咯( )是较常见的杂环化合物呋喃通过下列反应可转化为吡咯:
回答下列问题:
(1)呋喃和吡咯所含元素中:电负性最大的是___________(填元素符号),第一电离能最大的元素的基态原子
电子排布图是______________________。
(2)呋喃分子中,碳原子的杂化方式是___________,1mol吡咯分子中含________molσ键。
(3)NH 与HO可与Zn2+形成配合物[Zn(NH )(H O)]2+。与Zn2+形成配位键的原子是___________(填元素符号);
3 2 3 3 2
HO的空间构型为___________;写出一种与NH 互为等电子体的阳离子:___________(填化学式)。
2 3
(4)NH 的相对分子质量比NO的小,但其沸点却比NO的高,其主要原因是___________。
3 2 2
(5)ZnO晶体随着环境条件的改变能形成不同结构的晶体,其中一种的晶胞结构如图所示,已知该ZnO晶体
密度为ag·cm-3,N 表示阿伏加德罗常数。则该晶体中与Zn2+等距离且最近的Zn2+共有___________个,该
A
ZnO晶胞中相邻两个O2-之间的距离为___________nm。
【答案】O sp2 10 N、O V型 HO+ NH 分子间存在氢键 12 ×
3 3×107
【解析】 (1) 同周期自左向右电负性增大,同主族自上而下电负性逐渐降低,非金属性越强电负性越强;同一
周期元素中,元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族、第VA族元素的第一电离
能大于相邻元素,同主族自上而下第一电离能逐渐减小,呋喃和吡咯所含元素中含有C、H、O、N四种元素,
其中电负性最大的是O,第一电离能最大的元素是N,N的基态原子电子排布图是 ;
故答案为:O; ;
(2) 呋喃( )分子中,C形成2个双键,则碳原子的杂化方式是sp2;单键均为σ键,双键中有1个σ键,
则1mol吡咯( )分子中含10molσ键;
故答案为:sp2;10;
(5)由题给图示可知,正六面体的体心和每个棱的中间各有一个Zn2+。若选体心的Zn2+为研究对象,则与体心
的Zn2+等距离且最近的Zn2+为棱的中间的Zn2+,共有12个;
利用“均摊法”,可知一个晶胞含有Zn2+和O2-均为4。一个晶胞的质量:m(晶胞)= ×4g,一个晶胞的体积:V(晶胞)= = = cm3。则晶胞棱长= cm,
晶胞中相邻两个O2-之间的距离为面对角线的一半,即 × cm= × ×107nm。
故答案为:12; × ×107。
24.微量元素硼对植物的生长和人体骨骼的健康有着十分重要的作用。请回答下列问題:
(1)区分晶体硼和无定硼形科学的方法为_________________________________。
(2)下列B原子基态的价层电子排布图中正确的是___________
A. B.
C. D.
(3)NaBH 是重要的储氢载体,阴离子的立体构型为___________。
4
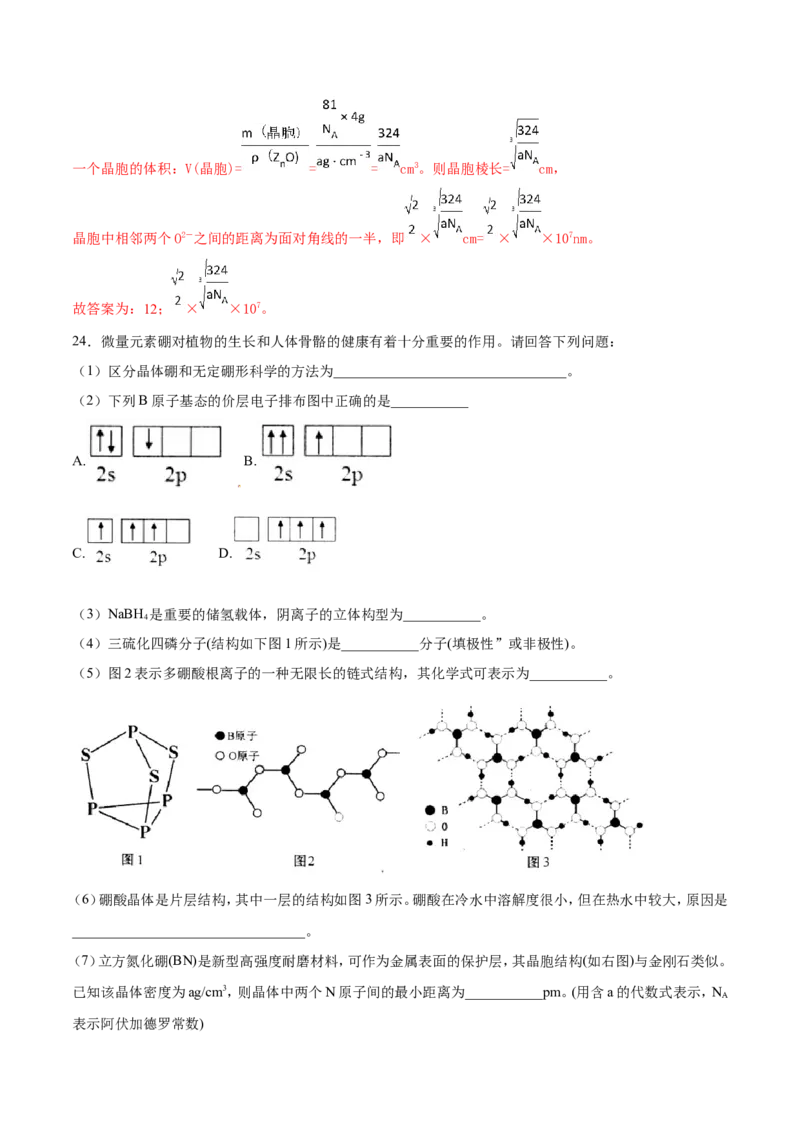
(4)三硫化四磷分子(结构如下图1所示)是___________分子(填极性”或非极性)。
(5)图2表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为___________。
(6)硼酸晶体是片层结构,其中一层的结构如图3所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是
_________________________________。
(7)立方氮化硼(BN)是新型高强度耐磨材料,可作为金属表面的保护层,其晶胞结构(如右图)与金刚石类似。
已知该晶体密度为ag/cm3,则晶体中两个N原子间的最小距离为___________pm。(用含a的代数式表示,N
A
表示阿伏加德罗常数)【答案】X-射线衍射实验 A 正四面体 极性 BO- 或 (BO)n- 或 B O n- 晶体中硼酸分子间以氢键
2 2 n n 2n
缔合在一起,难以溶解;加热时,晶体中部分氢键被破坏,硼酸分子与水分子形成氢键,溶解度增大
×1010
【解析】(1)区分晶体硼和无定形硼最可靠的科学方法为进行X-射线衔射实验;
(2)B原子外围电子有3个电子,2s能级上有2个电子,2p能级上有1个电子,其外围电子排布图为
,答案选A;
(3)NaBH 是一种重要的储氢载体,阴离子的化学式为BH-,则其结构式为 ,立体构型为为正四
4 4
面体;
(7)一个晶胞中B原子数目= ,含N原子数=4,一个晶胞的质量 ,根据 ,,晶胞棱长为 ,仔细观察BN的晶胞结构不难发现N
位于晶胞中8个小立方体中互不相邻的4个小立方体的体心,N与之间距离就是晶胞面对角线的一半,因此
晶体中两个最近的N原子间的距离为: ×1010pm。
25.前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻。已知元素X最高价氧化物的化学式为
XO,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸(本题
2 5
中出现的B、C均为字母,不是元素符号)。
(1)D元素基态原子的外围电子排布式为____________________。
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为________________(用相应的元素符号作答)。
(3)B、X、D氢化物的沸点由高到低的顺序为_______________(用相应的化学式作答)。
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
微粒 CO 2- CO2-
3 4
立体构型名称 _________ ______________
(5)元素B的一种氢化物B H 具有重要的用途。有关B H 的说法正确的是___。
2 4 2 4
A.B H 分子间可形成氢键 B.B原子是sp3杂化
2 4
C.B H 分子中含有5个σ键和1个π键 D.B H 晶体变为液态时破坏共价键
2 4 2 4
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH) 为两性氢氧化物,在浓的强碱溶液
2
中可形成E(OH) 2-,写出E(OH) 酸式电离的电离方程式_____________________________。
4 2
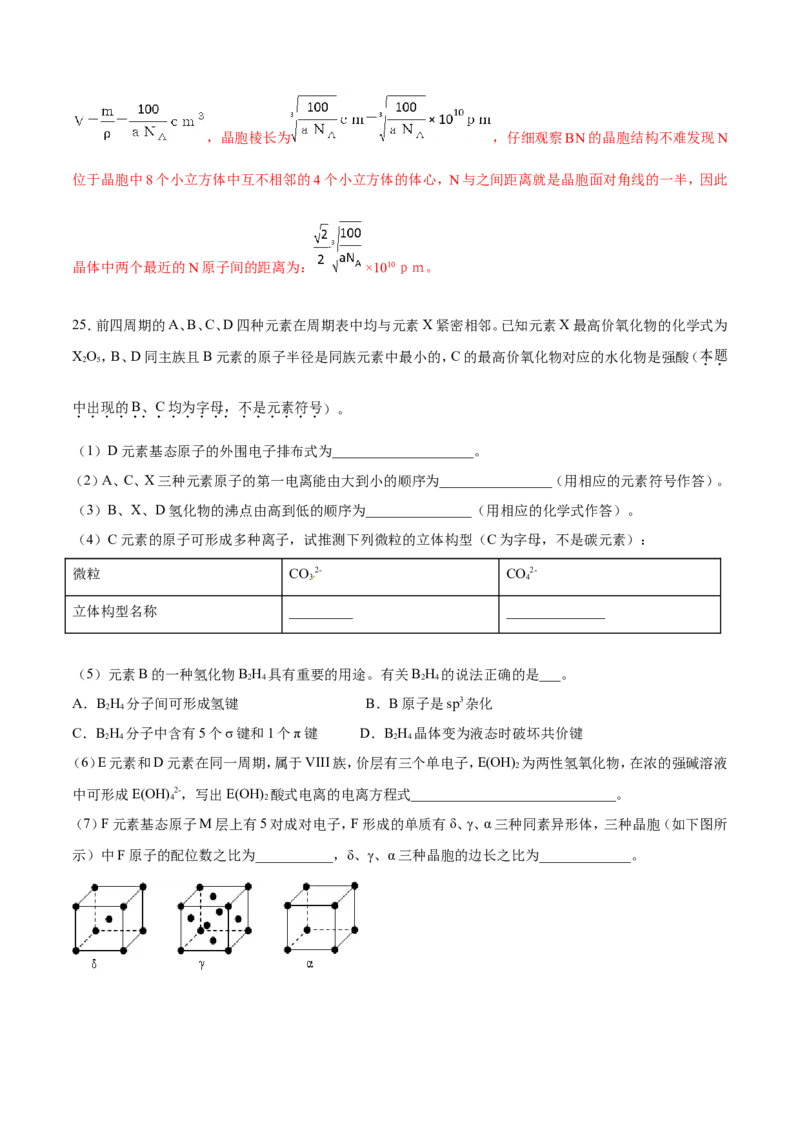
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如下图所
示)中F原子的配位数之比为___________,δ、γ、α三种晶胞的边长之比为_____________。【答案】4s24p3 P>S>Si NH>AsH>PH 三角锥形 正四面体形 AB Co(OH)+2HO Co(OH)2-
3 3 3 2 2 4
+2H+ 4:6:3 2
根据元素周期律,同周期元素从左向右,第一电离逐渐增大,但第ⅡA族和第ⅤA族由于最外层处于全满和
半满状态,第一电离能高于相邻族的元素,所以Si、S、P的第一电离能大小顺序为P>S>Si;(3)B、X、D氢
化物分别为NH 、PH 、AsH ,因为氨分子之间有氢键的存在,所以氨的沸点较大,AsH 的相对分子质量大于
3 3 3 3
PH ,所以沸点也高于PH ,所以它们的沸点由高到低的顺序为NH >AsH >PH ;(4)SO 2-的中心原子硫原子
3 3 3 3 3 3
的价层电子对数为4,含有一对孤对电子,空间构型为三角锥形;SO 2-的中心原子硫原子的价层电子对数为
4
4,没有孤对电子,空间构型为正四面体形;(5)B H 为NH,A.NH 分子间与NH 相似,可形成氢键,A正确;
2 4 2 4 2 4 3
B.NH 分子中N原子的价层电子对数为(5+1+1+1)/2=4,所以氮原子是sp3杂化,B正确;C.NH 分子中N原
2 4 2 4
子之间是单键,所以没有π键,C错误;D.NH 是分子晶体,所以晶体变为液态时破坏的是分子间作用力和
2 4
氢键,D错误;答案选AB;(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E是Co,
Co(OH) 为两性氢氧化物,在浓的强碱溶液中可形成Co(OH) 2-,因此Co(OH) 酸式电离的电离方程式为
2 4 2
Co(OH) +2H O Co (OH) 2-+2H+。(7)δ晶胞中,以顶点Fe原子研究,与之最近的Fe原子处于晶胞的体心,
2 2 4
补全晶胞可知配位数为8,γ晶胞中,以顶点Fe原子研究,与之最近的Fe原子处于面心上,补全晶胞可知,
有3层,每层有4个,故Fe原子的配位数为4×3=12。α晶胞中,以顶点Fe原子研究,与之最近的Fe原子处于
所在棱的顶点上,补全晶胞可知配位数为6,所以δ、γ、α三种晶胞中Fe原子的配位数之比为4:6:3;设铁
原子的直径为a,根据晶胞结构图可知,δ晶胞的边长为 、γ晶胞的边长为 、α晶胞的边长为a,所以
δ、γ、α三种晶胞的边长之比为2 。