文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题28 化学反应原理综合题
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
该类题主要把热化学、电化学、化学反应速率及四大平衡知识融合在一起命题。预计2025年高考,题
目将结合图像或图表形式,重点考查热化学(或离子、电极)方程式的书写、离子浓度大小比较、反应速率
大小、平衡常数及转化率的计算、电化学装置、平衡曲线的识别与绘制等。
“化学反应原理”大题的常考点:
(1)热化学方程式的书写或反应热的计算。
(2)转化率的影响因素及计算。
(3)平衡常数的表达式或计算。
(4)借助图像分析化学反应速率和化学平衡的影响因素。
(5)电极反应式的书写。
(6)通过信息获取解题数据,根据三段式进行化学平衡常数K、K 、K 以及转化率的计算。
p x
1.(2024·福建·高考真题) 是制造多晶硅的原料,可由 和 耦合加氢得到,相关反应如下:
Ⅰ.
Ⅱ.
Ⅲ.
(1)生成 的总反应:
Ⅳ.
(2)体系达到平衡状态且其他条件不变时:
①压缩平衡体系体积,重新达到平衡后物质的量分数增大的组分为 。(填标号)
a. b. c. d.
②反应温度升高不利于提高平衡时产物 选择性的原因是 。
(3)在压强为 的恒压体系中通入 和 ,达到平衡时,气体组分的物质的量分数随温度变化如图所示(忽略气体组分在硅表面的吸附量)。已知: 为用气体分压表示的平衡常数,分压=物质的
量分数×总压。
①图中n代表的组分为 。(填化学式)
② 时,反应Ⅲ的平衡常数 。(列出计算式)
③ 时, 的平衡转化率为f,消耗硅的物质的量为 。(列出计算式)
(4) 下、其他条件相同时,用 和 分别催化上述反应,一段时间内 的转化率如下表
所示。(产物 选择性均高于98.5%)
催化剂
的转化率/% 7.3 14.3 22.3
①使用不同催化剂时,反应Ⅳ的 催化剂 催化剂(填“>”“<”或“=”);反应Ⅳ的活化
能: 催化剂 催化剂(填“>”“<”或“=”)。
②使用 催化剂,初始投料 该段时间内得到 ,则 的选择性
。(列出计算式)
【答案】
(1)
(2)bc 因 ,升温反应 向逆反应方向进行, 的产量反而减小
(3) 或
(4)= >【详解】(1)根据盖斯定律可知, 。
故答案为:-80。
(2)①压缩平衡体系体积,相当于增大压强,重新达到平衡后,对于反应 ,除压强对反应I无影
响,对 的反应都是平衡向正反应方向移动,因此 和 的量增大;因 、
,升温反应 向逆反应方向进行,反应 向正反应方向进行, 的产量反而减小。
故答案为:bc;因 ,升温反应 向逆反应方向进行, 的产量反而减小。
(3)在压强为 的恒压体系中通入 和 ,①根据反应 可知,温度升高反应 和
向正反应方向进行,产物含量增加,结合图可知n为HCl,m为 ;② 时按照反应 进行:
,由图中可知道平衡时 ,
, ,则 ;③ ,1mol
的平衡转化率为f,则转化的 为fmol,剩余的 为( )mol,平衡时的物质与物质的量分数分别
为: x、 z和 y,设平衡时混合物的总物质的量为Mmol,则可以根据剩余的
计算出M, mol,再计算出 、
,根据硅原子守恒,消耗硅的物质的量=平衡物质中硅的总物质的
量-起始时的1mol , 或者消耗硅的物质的量=
平衡物质中 和 物质的量之和-消耗的fmol ,
。
故答案为: ; ; 或 。
(4)①使用不同催化剂时,反应 的 催化剂与 催化剂相比较,由于反应热只和反应物
的始态与生成物的终态有关,与催化剂无关,所以 催化剂= 催化剂;根据表中数据,在
相同单位时间内, 作催化剂 的转化率为7.3%、 作催化剂 的转化率为22.3%,由此可以
得出 作催化剂时活化能更低,效率更高,则反应 的活化能: 催化剂 催化剂;②根据反
应 : ,初始投料 该段时间内得到 ,列式,得出生成 所消耗的 的物质的量
,根据表的转化率可知所消耗的 的总物质的量为 ,最后根据公式
。
故答案为:=;>; 。
2.(2024·广西·高考真题)二氯亚砜( )是重要的液态化工原料。回答下列问题:
(1)合成 前先制备 。有关转化关系为:
则 的 。
(2)密闭容器中,以活性炭为催化剂,由 和 制备 。反应如下:
Ⅰ
Ⅱ
①反应Ⅱ的 ( 为平衡常数)随 ( 为温度)的变化如图,推断出该反应为 (填“吸热”或“放
热”)反应。
②466K时,平衡体系内各组分的物质的是分数 随 的变化如图。反应Ⅱ的平衡常数 (保留1位小数)。保持 和 不变,增大 平衡转化率的措施有
(任举一例)。
③改变 ,使反应Ⅱ的平衡常数 ,导致图中的曲线变化,则 等于 的新交点将出
现在 (填“ ”“ ”“ ”或“ ”)处。
(3)我国科研人员在含 的 溶液中加入 ,提高了 电池的性能。该电池放电时,正极的物
质转变步骤如图。其中, 的作用是 ;正极的电极反应式为 。
【答案】
(1)-50
(2)放热 32.4 移走 或加入SO Cl d
2 2
(3)催化作用
【详解】(1)由盖斯定律可知, 的焓变为
,则 的;
(2)①由图可知反应Ⅱ的 与 成正比,则温度升高即 减小随之lgK减小,那么K值减小,平衡逆
向移动,反应Ⅱ为放热反应;
②由图可知, =2.0时,平衡体系物质的量分数x(SCl )=x(SOCl)=0.13,由于
2 2 2
为非可逆反应,故O 应完全转化,即平衡体系中不存在O,则x(SOCl )=1-
2 2 2
x(SCl )-x(SO Cl)=0.74,反应Ⅱ 是气体体积不变的反应,则平衡常数可
2 2 2
用物质的量分数代替计算,反应Ⅱ的平衡常数 ;保持 和 不变,减小生成物
浓度或加入其他反应物均能使平衡正移,增大 平衡转化率的措施有移走 或加入SO Cl;
2 2
③反应Ⅱ为放热反应,改变 ,使反应Ⅱ的平衡常数 ,其平衡常数减小,则为升高温度,反应Ⅱ
逆向移动,使得 含量减小、 增加,则图中 等于 的新交点将会提前,出现在d
处;
(3)由图可知, 在反应中被消耗又生成,作用是催化作用;放电时,正极上 得到电子发生还原转
化为S、SO ,正极电极反应为: 。
2
3.(2024·重庆·高考真题)高辛烷值的汽油可提升发动机的抗爆震性能,异构烷烃具有较高的辛烷值。
(1)在密闭容器中, (正戊烷)发生异构化反应,可同时生成 (异戊烷)和 (新戊烷),其平
衡常数 随温度的变化如下表所示。
异构化反应
反应1 2.80 2.50 2.31
反应2 1.40 1.00 0.77
①体系平衡后,增加压强,反应1的平衡 (填“正向移动”“逆向移动”或“不移动”)。
② 平衡时, 和 的体积比值为 。
③根据上表数据推断 为吸热反应,其推断过程是 。(2)加入 后, 在双功能催化剂 /分子筛上发生异构化反应且选择性高,主要产物为 ,其
反应机理如下( 表示分子筛固体酸催化剂):
对于 反应,下列说法正确的是_______。
A. 只能催化脱氢反应,不能催化加氢反应
B. 的加入增大了平衡常数,有利于反应的进行
C.分子筛固体酸催化剂酸性越强,越有利于 的形成
D. 的加入促进了 的加氢反应,减少了副反应的发生
(3) (四乙基铅)能提高汽油的辛烷值,可电解合成。电解池的阳极为 ,阴极为碳钢,电解液
为溶有格氏试剂( )的有机体系。
①阳极上生成 的电极反应式为 。
②为了实现阴极产物的循环利用,电解一段时间后,需在阴极区不断加入适量的 ,其原理是
。
③为减少铅污染, 被限制使用。 是一种潜在替代品,其电解合成的原理如图所
示( 为催化剂)。总反应化学方程式为 ;外电路转移 电子时,理论上可生成 的
物质的量为 。
【答案】
(1)不移动 2 由盖斯定律可知,反应1-反应2得 ,根据上表数据,
、 、 ,升高温度,K值增大,反应正向进行
(2)C(3) 阴极 得到电子发生还原反应生成镁单质:
,在阴极区不断加入适量的 ,发生反应 ,实
现阴极产物的循环利用 0.5
【详解】(1)①反应1为气体分子数不变的反应,体系平衡后,增加压强,反应1的平衡不移动。
②由盖斯定律可知,反应1-反应2得 ,则 平衡时, ,则
和 的体积比值为2;
③由盖斯定律可知,反应1-反应2得 ,根据上表数据, 、
、 ,升高温度,K值增大,反应正向进行,则 为吸
热反应;
(2)A.反应为可逆反应,由图可知 能催化脱氢反应,也能催化加氢反应,错误;
B.平衡常数受温度影响, 的加入不改变平衡常数,错误;
C.分子筛固体酸催化剂酸性越强,氢离子浓度越大,越有利于 的形成,正确;
D. 的加入促进了 的加氢反应,但是也会和 加成,副反应也会增多,错误;
故选C;
(3)①电解池的阳极为 ,阳极上Pb失去电子发生氧化反应生成 ,电极反应式为
。
②阴极 得到电子发生还原反应生成镁单质: ,在阴极区不断加入适量的
,发生反应 ,实现阴极产物的循环利用;
③由图,A极二氧化碳得到电子发生还原生成CO和 : ,CO
和 再和Pt2+反应生成 : ,则总反应为二氧化碳和甲
醇反应生成 和水: ;反应中电子转移为 ,
则外电路转移 电子时,理论上可生成 的物质的量为0.5 。
4.(2024·贵州·高考真题)在无氧环境下,CH 经催化脱氢芳构化可以直接转化为高附加值的芳烃产品。
4
一定温度下,CH 芳构化时同时存在如下反应:
4
ⅰ.ⅱ.
回答下列问题:
(1)反应ⅰ在1000K时 (选填“能”或“不能”)自发进行。
(2)已知25℃时有关物质的燃烧热数据如表,则反应ⅱ的 (用含 的代数式表
示)。
物质
(3)受反应ⅰ影响,随着反应进行,单位时间内甲烷转化率和芳烃产率逐渐降低,原因是 。
(4)对催化剂在不同的pH条件下进行处理,能够改变催化剂的活性。将催化剂在5种不同pH条件下处理后
分别用于催化CH 芳构化,相同反应时间内测定相关数据如下表,其中最佳pH为 ,理由是
4
。
pH CH 平均转化率/% 芳烃平均产率/% 产物中积碳平均含量/%
4
2.4 9.60 5.35 40.75
4.0 9.80 4.60 45.85
7.0 9.25 4.05 46.80
10.0 10.45 6.45 33.10
12.0 9.95 4.10 49.45
(5) 下,在某密闭容器中按 充入气体,发生反应
,平衡时 与 的分压比为4:1,则 的平衡转化率为
,平衡常数K= (用平衡分压代替平衡浓度计算,分压 总压 物质的量分数,列出计算式即可)。
p
(6)引入丙烷可促进甲烷芳构化制备苯和二甲苯,反应如下:
(两个反应可视为同级数的平行反应)
对于同级数的平行反应有 ,其中v、k分别为反应速率和反应速率常数,E 为反应活
a化能,A、A 为定值,R为常数,T为温度,同一温度下 是定值。已知 ,若要提高苯的产
1 2
率,可采取的措施有 。
【答案】
(1)能
(2)6a-b-9c
(3)反应ⅰ有积炭生成,随着反应的进行,生成的积炭逐渐增多,覆盖在催化剂表面,使催化剂催化性能逐
渐降低,化学反应速率减小
(4)10.0 pH=10.0时,产物中积炭平均含量最低,CH 平均转化率最大,芳烃平均产率最高
4
(5)20% 或
(6)加入合适的催化剂(合理即可)
【详解】(1)反应ⅰ. ,在1000K
时,ΔG=ΔH-TΔS=+74.6 kJ·mol-1-1000K×80.84×10-3kJ·mol-1·K-1=-6.24 kJ·mol-1<0,故反应ⅰ在1000K时能自
发进行。
(2)ⅱ.
由题给数据可得出以下热化学方程式:
③CH (g)+2O(g)=CO(g)+2HO(l) ΔH=akJ·mol-1
4 2 2 2
④C H(l)+7.5O(g)=6CO(g)+3HO(l) ΔH=bkJ·mol-1
6 6 2 2 2
⑤H(g)+0.5O (g)=HO(l) ΔH=c kJ·mol-1
2 2 2
依据盖斯定律,将反应③×6-④-⑤×9得,反应ⅱ的 (6a-b-9c) kJ·mol-1。
(3)由于反应ⅰ生成固态炭,会覆盖在催化剂表面,从而减小气体与催化剂的接触面积,因此随着反应
进行,单位时间内甲烷转化率和芳烃产率逐渐降低。
(4)比较表中数据可以看出,pH=10.0时,CH 平均转化率为最大值10.45%,芳烃平均产率为最大值
4
6.45%,产物中积炭平均含量为最小值33.10%,所以最佳pH为10.0。
(5) 下,在某密闭容器中按 充入气体,发生反应
,平衡时 与 的分压比为4:1,设起始时C H 的物质的量为
6 6
1mol,CH 的物质的量为5mol,参加反应C H 的物质的量为xmol,则可建立如下三段式:
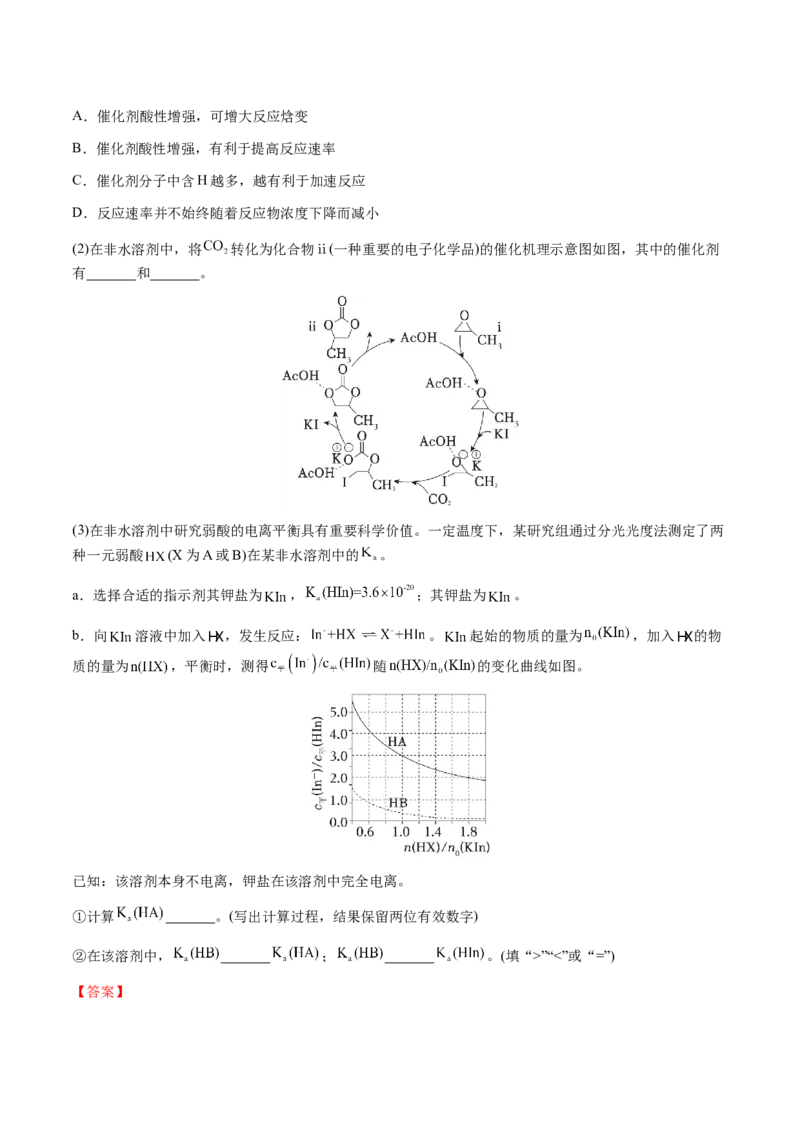
4 6 6依题意, ,解得x=0.2,平衡时,n(C H)=0.8mol,n(CH)=4.8mol,n(C H)=0.2mol,
6 6 4 7 8
n(H )=0.2mol,则 的平衡转化率为 =20%,平衡常数K=
2 p
或 。
(6)已知 ,加入合适的催化剂,选择性降低E ,加快生成苯的速率,提高苯的产率。所以
a,苯
若要提高苯的产率,可采取的措施有:加入合适的催化剂(合理即可)。
5.(2024·广东·高考真题)酸在多种反应中具有广泛应用,其性能通常与酸的强度密切相关。
(1)酸催化下 与 混合溶液的反应(反应a),可用于石油开采中油路解堵。
①基态N原子价层电子的轨道表示式为 。
②反应a:
已知:
则反应a的 。
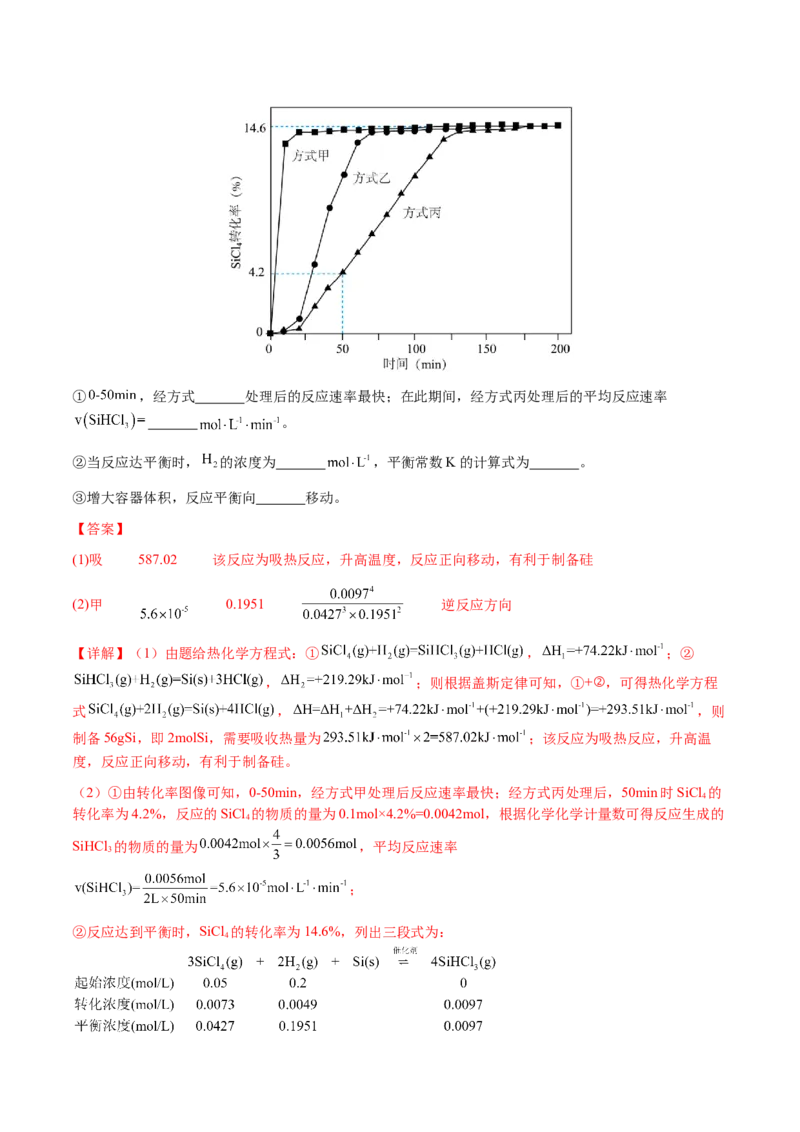
③某小组研究了3种酸对反应a的催化作用。在相同条件下,向反应体系中滴加等物质的量的少量酸,测
得体系的温度T随时间t的变化如图。
据图可知,在该过程中 。A.催化剂酸性增强,可增大反应焓变
B.催化剂酸性增强,有利于提高反应速率
C.催化剂分子中含H越多,越有利于加速反应
D.反应速率并不始终随着反应物浓度下降而减小
(2)在非水溶剂中,将 转化为化合物ⅱ(一种重要的电子化学品)的催化机理示意图如图,其中的催化剂
有 和 。
(3)在非水溶剂中研究弱酸的电离平衡具有重要科学价值。一定温度下,某研究组通过分光光度法测定了两
种一元弱酸 (X为A或B)在某非水溶剂中的 。
a.选择合适的指示剂其钾盐为 , ;其钾盐为 。
b.向 溶液中加入 ,发生反应: 。 起始的物质的量为 ,加入 的物
质的量为 ,平衡时,测得 随 的变化曲线如图。
已知:该溶剂本身不电离,钾盐在该溶剂中完全电离。
①计算 。(写出计算过程,结果保留两位有效数字)
②在该溶剂中, ; 。(填“>”“<”或“=”)
【答案】(1) BD
(2)AcOH KI
(3) > >
【详解】(1)
①N的原子序数为7,位于第二周期第ⅤA族,基态N原子价层电子的轨道表示式为
;
②由已知可得:
Ⅰ. , ;
Ⅱ. , ;
Ⅲ. , ;
Ⅳ. , ;
由盖斯定律可知,目标方程式 可由方程式Ⅰ-Ⅱ-Ⅲ+Ⅳ得到,故反应
;
③A.催化剂不能改变反应的焓变,A项错误;
B.由图示可知,酸性:硫酸>磷酸>乙酸,催化剂酸性增强,反应速率提高,B项正确;
C.一个硫酸分子中含有2个H,一个磷酸分子中含有3个H,一个乙酸分子中含有4个H,但含H最少的
硫酸催化时,最有利于加速反应,C项错误;
D.由图示可知,反应开始一段时间,反应物浓度减小,但反应速率加快,反应速率并不始终随着反应物
浓度下降而减小,D项正确;
故选BD。
(2)催化剂参与化学反应,但反应前后质量和化学性质并未改变,由催化机理示意图可知,催化剂有
AcOH和KI;
(3)由变化曲线图可知,当 时, ,设初始 ,则初始
,转化的物质的量浓度为 ,可列出三段式如下:由 ,即 ,解得 ,则该反应的平衡常数为
解得 ;
②根据图像可知,当 时,设此时转化的物质的量浓度为 ,可列出三段式如下:
此时 ,即 ,则 ,则平衡常数 ,则 ;
由于 ,则 , 。
6.(2024·甘肃·高考真题) 是制备半导体材料硅的重要原料,可由不同途径制备。
(1)由 制备 :
已知
时,由 制备 硅 (填“吸”或“放”)热 。升高温
度有利于制备硅的原因是 。
(2)在催化剂作用下由粗硅制备 : 。 , 密闭容器
中,经不同方式处理的粗硅和催化剂混合物与 和 气体反应, 转化率随时间的变
化如下图所示:① ,经方式 处理后的反应速率最快;在此期间,经方式丙处理后的平均反应速率
。
②当反应达平衡时, 的浓度为 ,平衡常数K的计算式为 。
③增大容器体积,反应平衡向 移动。
【答案】
(1)吸 587.02 该反应为吸热反应,升高温度,反应正向移动,有利于制备硅
(2)甲 0.1951 逆反应方向
【详解】(1)由题给热化学方程式:① , ;②
, ;则根据盖斯定律可知,①+②,可得热化学方程
式 , ,则
制备56gSi,即2molSi,需要吸收热量为 ;该反应为吸热反应,升高温
度,反应正向移动,有利于制备硅。
(2)①由转化率图像可知,0-50min,经方式甲处理后反应速率最快;经方式丙处理后,50min时SiCl 的
4
转化率为4.2%,反应的SiCl 的物质的量为0.1mol×4.2%=0.0042mol,根据化学化学计量数可得反应生成的
4
SiHCl 的物质的量为 ,平均反应速率
3
;
②反应达到平衡时,SiCl 的转化率为14.6%,列出三段式为:
4当反应达平衡时,H 的浓度为 ,平衡常数K的计算式为 ;
2
③增大容器体积,压强减小,平衡向气体体积增大的方向移动,即反应平衡向逆反应方向移动。
7.(2024·湖南·高考真题)丙烯腈( )是一种重要的化工原料。工业上以 为载气,用 作
催化剂生产 的流程如下:
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定:
②反应釜Ⅰ中发生的反应:
ⅰ:
③反应釜Ⅱ中发生的反应:
ⅱ:
ⅲ:
④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应 (用
含 、 、和 的代数式表示);
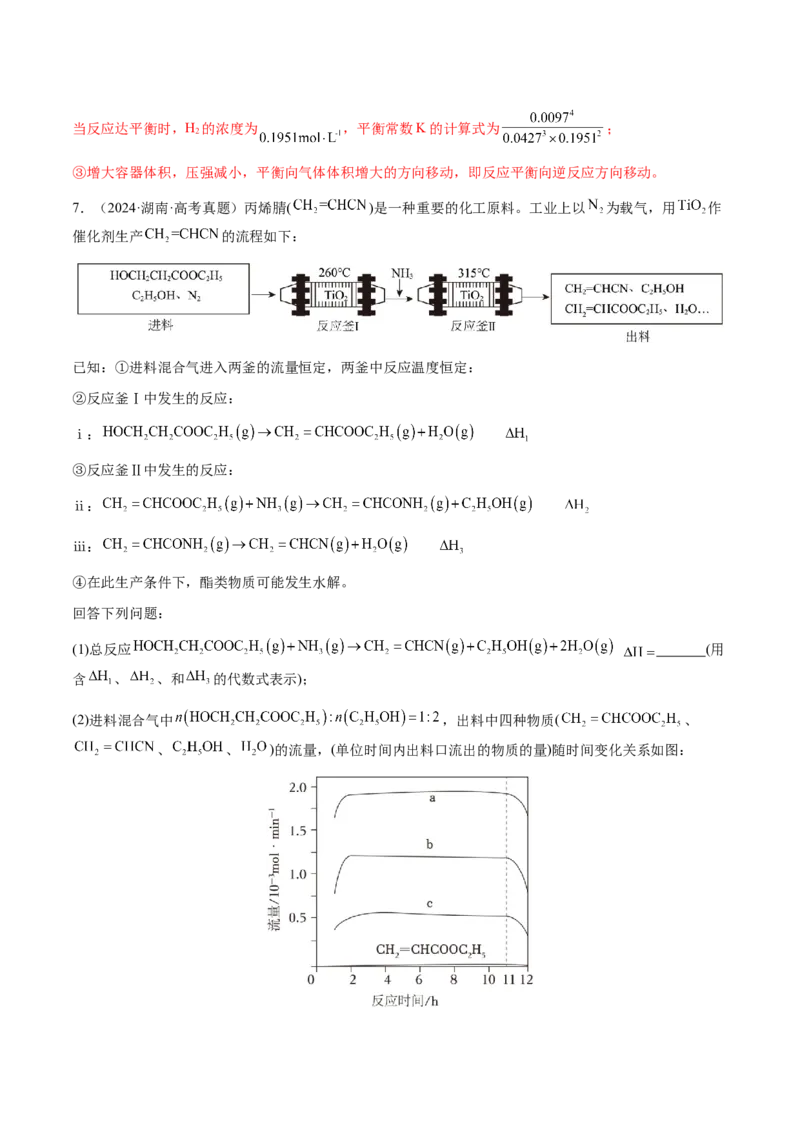
(2)进料混合气中 ,出料中四种物质( 、
、 、 )的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:①表示 的曲线是 (填“a”“b”或“c”);
②反应釜Ⅰ中加入 的作用是 。
③出料中没有检测到 的原因是 。
④反应 后,a、b、c曲线对应物质的流量逐渐降低的原因是 。
(3)催化剂 再生时会释放 ,可用氨水吸收获得 。现将一定量的 固体(含
水)置于密闭真空容器中,充入 和 ,其中 的分压为 ,在 ℃下进行干燥。为保证
不分解, 的分压应不低于 (已知
分解的平衡常数 );
(4)以 为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得 ,其阴极
反应式 。
【答案】
(1)ΔH +ΔH +ΔH
1 2 3
(2)c 抑制酯的水解从而提高产率 反应iii的速率远大于反应ii 反应时间过长,催化剂中毒活
性降低,反应速率降低,故产物减少
(3)40
(4)Sn+4CH=CHCN+4e-+4H+=Sn(CHCHCN)
2 2 2 4
【详解】(1)根据盖斯定律,总反应HOCH CHCOOC H(g)+NH (g)→CH =CHCN(g)+C HOH(g)
2 2 2 5 3 2 2 5
+2H O(g)可以由反应i+反应ii+反应iii得到,故ΔH=ΔH+ΔH +ΔH ;
2 1 2 3
(2)①根据总反应HOCH CHCOOC H(g)+NH (g)→CH =CHCN(g)+C HOH(g)+2H O(g),设进料混合气
2 2 2 5 3 2 2 5 2
中n(HOCHCHCOOC H)=1mol,n(C HOH)=2mol,出料气中CH=CHCOOC H 含量很少,则生成
2 2 2 5 2 5 2 2 5
CH=CHCN(g)、C HOH(g)物质的量约为1mol,生成HO(g)的物质的量约为2mol,故出料气中C HOH(g)
2 2 5 2 2 5
物质的量共约3mol,故出料气中CH=CHCN、C HOH、HO物质的量之比约为1:3:2,故曲线c表示
2 2 5 2
CH=CHCN的曲线;
2
②反应釜Ⅰ中发生反应i生成丙烯酸乙酯和水,若丙烯酸乙酯水解会生成乙醇,因此,加入C HOH可以
2 5
抑制酯的水解从而提高产率;
③反应釜Ⅱ中发生的两个反应是竞争反应,其选择性由速率决定,出料中没有检测到CH=CHCONH 的原
2 2
因是:反应iii的速率远大于反应ii;
④反应11h后,a、b、c曲线对应物质的流量逐渐降低的原因是反应时间过长,催化剂中毒活性降低,反
应速率降低,故产物减少;
(3)0.72g水的物质的量为0.04mol,故p(H O)=2.5×102kPa⋅mol−1×n(H O)=10kPa,NH HCO 分解的反应式
2 2 4 3
为NH HCO =NH↑+CO ↑+H O↑,故NH HCO 分解的平衡常数K=p(NH)p(CO )p(H O)=4×104(kPa)3,解得
4 3 3 2 2 4 3 p 3 2 2
p(NH )=40kPa,故为保证NH HCO 不分解,NH 的分压应不低于40kPa;
3 4 3 3(4)Sn(CH CHCN) 是有机化合物,与水不溶,水中不电离,以CH=CHCN为原料在Sn做的阴极得电子
2 2 4 2
制得Sn(CH CHCN) ,故阴极的电极反应式为Sn+4CH=CHCN+4e-+4H+=Sn(CHCHCN) 。
2 2 4 2 2 2 4
8.(2024·浙江·高考真题)氢是清洁能源,硼氢化钠( )是一种环境友好的固体储氢材料,其水解生
氢反应方程式如下:(除非特别说明,本题中反应条件均为 , )
请回答:
(1)该反应能自发进行的条件是_______。
A.高温 B.低温 C.任意温度 D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是_______。
A.升高溶液温度 B.加入少量异丙胺
C.加入少量固体硼酸 D.增大体系压强
(3)为加速 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,
测得反应开始时生氢速率v与投料比 之间的关系,结果如图1所示。请解释ab段变
化的原因 。
(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如
图2所示,正极上的电极反应式是 。该电池以 恒定电流工作14分钟,消耗 体积为 ,
故可测得该电池将化学能转化为电能的转化率为 。[已知:该条件下 的摩尔体积为 ;
电荷量 电流 时间 ; ; 。](5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方
法,将反应副产物偏硼酸钠( )再生为 。(已知: 是反应的自由能变化量,其计算方法也遵
循盖斯定律,可类比 计算方法;当 时,反应能自发进行。)
I.
II.
III.
请书写一个方程式表示 再生为 的一种制备方法,并注明 。(要求:反应物不超过
三种物质;氢原子利用率为 。)
【答案】
(1)C
(2)AC
(3)随着投料比 增大,NaBH 的水解转化率降低
4
(4)O +4e-+2CO =2 70%
2 2
(5)
【详解】(1)反应 , ,由 可知,任意
温度下,该反应均能自发进行,故答案选C;
(2)A.升高温度,活化分子数增多,有效碰撞几率增大,反应速率加快,A符合题意;
B.该反应的本质是NaBH 与H+反应,加入少量异丙胺 ,异丙胺水溶液呈碱性,溶液中
4
H+浓度减小,化学反应速率降低,B不符合题意;
C. 加入少量固体硼酸 ,硼酸溶液呈酸性,溶液中H+浓度增大,化学反应速率加快,C符合题
意;D.增大体系压强,忽略体积变化,则气体浓度不变,化学反应速率不变,D不符合题意;
答案选AC。
(3)随着投料比 增大,NaBH 的水解转化率降低,因此生成氢气的速率不断减小。
4
(4)根据题干信息,该燃料电池中H 为负极,O 为正极,熔融碳酸盐为电解质溶液,故正极的电极反应
2 2
式为:O+4e-+2CO =2 , 该条件下,0.49L H 的物质的量为 ,工作时,H
2 2 2 2
失去电子:H-2e-=2H+,所带电荷量为:2×0.02mol×6.0×1023mol-1×1.60×10-19= 3840C,工作电荷量为:
2
3.2×14×60=2688C,则该电池将化学能转化为电能的转化率为: ;
(5)结合题干信息,要使得氢原子利用率为100%,可由(2×反应3)-(2×反应Ⅱ+反应Ⅰ)得
,
。
9.(2024·河北·高考真题)氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及
1,4-二(氯甲基)苯等可通过氯化反应制备。
(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
。
①若正反应的活化能为 ,则逆反应的活化能 (用含 的代数式表示)。
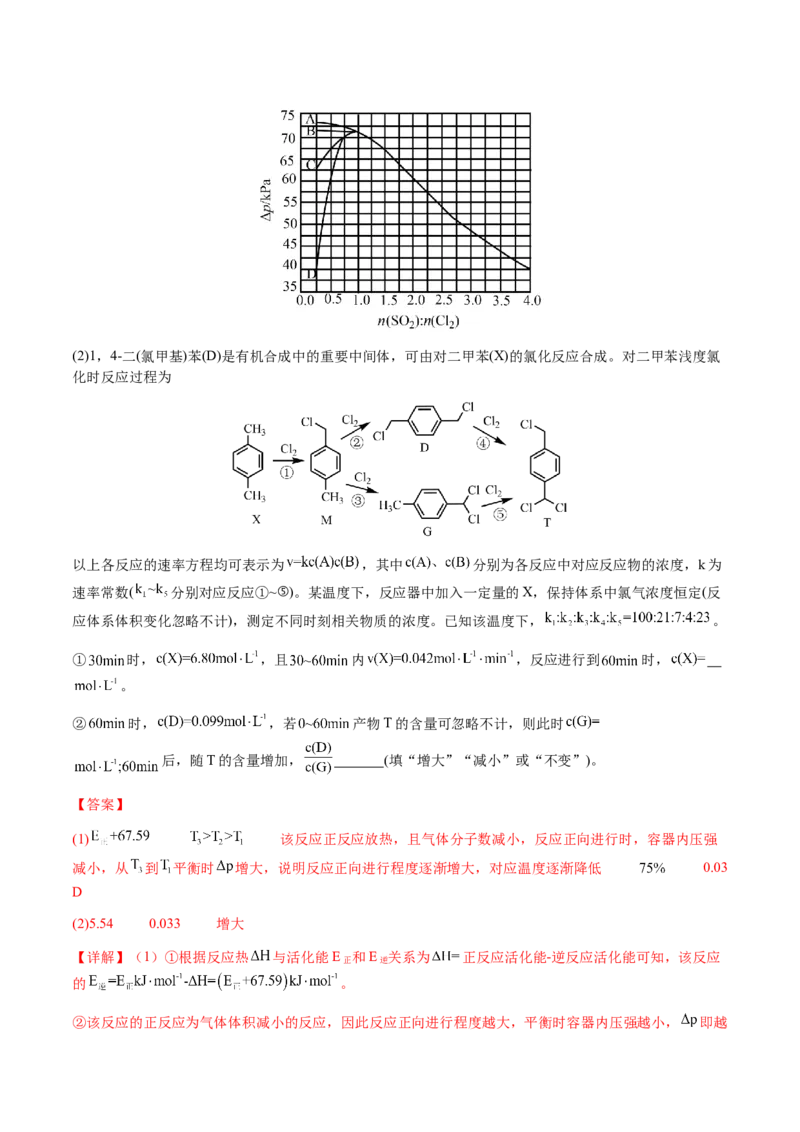
②恒容密闭容器中按不同进料比充入 和其 ,测定 温度下体系达平衡时的 (
为体系初始压强, ,P为体系平衡压强),结果如图。
上图中温度由高到低的顺序为 ,判断依据为 。M点 的转化率为 , 温度下用分
压表示的平衡常数 。
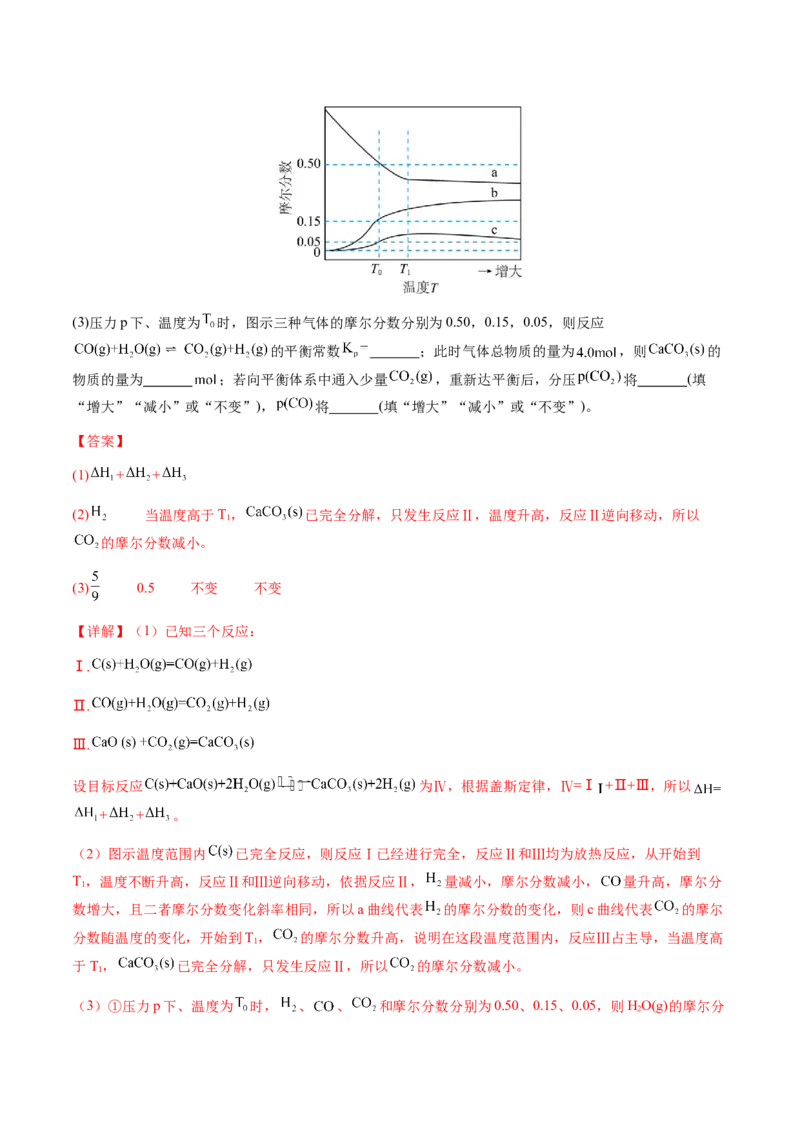
③下图曲线中能准确表示 温度下 随进料比变化的是 (填序号)。(2)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅度氯
化时反应过程为
以上各反应的速率方程均可表示为 ,其中 分别为各反应中对应反应物的浓度,k为
速率常数( 分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气浓度恒定(反
应体系体积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下, 。
① 时, ,且 内 ,反应进行到 时,
。
② 时, ,若 产物T的含量可忽略不计,则此时
后,随T的含量增加, (填“增大”“减小”或“不变”)。
【答案】
(1) 该反应正反应放热,且气体分子数减小,反应正向进行时,容器内压强
减小,从 到 平衡时 增大,说明反应正向进行程度逐渐增大,对应温度逐渐降低 0.03
D
(2)5.54 0.033 增大
【详解】(1)①根据反应热 与活化能E 和E 关系为 正反应活化能-逆反应活化能可知,该反应
正 逆
的 。
②该反应的正反应为气体体积减小的反应,因此反应正向进行程度越大,平衡时容器内压强越小, 即越大。从 到 , 增大,说明反应正向进行程度逐渐增大,已知正反应为放热反应,则温度由 到 逐
渐降低,即 。由题图甲中M点可知,进料比为 ,平衡时 ,已知恒温
恒容情况下,容器内气体物质的量之比等于压强之比,可据此列出“三段式”。
可计算得 , 。
③由题图甲中M点可知,进料比为2时, ,结合“三段式”,以及 时化学平衡常数可知,进
料比为0.5时, 也为 ,曲线D上存在(0.5,60)。本题也可以快解:根据“等效平衡”原理,该
反应中 和 的化学计量数之比为 ,则 和 的进料比互为倒数(如2与0.5)时, 相等。
(2)①根据化学反应速率的计算公式时, , 时,
。
②已知 ,又由题给反应速率方程推知, ,则
,即 后 。 后,D和G转化为T的速率比为
,G消耗得更快,则 增大。
10.(2024·山东·高考真题)水煤气是 的主要来源,研究 对 体系制 的影响,涉及主要反
应如下:
回答下列问题:
(1) 的焓变 (用代数式表示)。
(2)压力p下, 体系达平衡后,图示温度范围内 已完全反应, 在 温度时完全分
解。气相中 , 和 摩尔分数随温度的变化关系如图所示,则a线对应物质为 (填化学式)。
当温度高于 时,随温度升高c线对应物质摩尔分数逐渐降低的原因是 。(3)压力p下、温度为 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应
的平衡常数 ;此时气体总物质的量为 ,则 的
物质的量为 ;若向平衡体系中通入少量 ,重新达平衡后,分压 将 (填
“增大”“减小”或“不变”), 将 (填“增大”“减小”或“不变”)。
【答案】
(1) + +
(2) 当温度高于T, 已完全分解,只发生反应Ⅱ,温度升高,反应Ⅱ逆向移动,所以
1
的摩尔分数减小。
(3) 0.5 不变 不变
【详解】(1)已知三个反应:
Ⅰ.
Ⅱ.
Ⅲ.
设目标反应 为Ⅳ,根据盖斯定律,Ⅳ=Ⅰ +Ⅱ+Ⅲ,所以
+ + 。
(2)图示温度范围内 已完全反应,则反应Ⅰ已经进行完全,反应Ⅱ和Ⅲ均为放热反应,从开始到
T,温度不断升高,反应Ⅱ和Ⅲ逆向移动,依据反应Ⅱ, 量减小,摩尔分数减小, 量升高,摩尔分
1
数增大,且二者摩尔分数变化斜率相同,所以a曲线代表 的摩尔分数的变化,则c曲线代表 的摩尔
分数随温度的变化,开始到T, 的摩尔分数升高,说明在这段温度范围内,反应Ⅲ占主导,当温度高
1
于T, 已完全分解,只发生反应Ⅱ,所以 的摩尔分数减小。
1
(3)①压力p下、温度为 时, 、 、 和摩尔分数分别为0.50、0.15、0.05,则HO(g)的摩尔分
2数为: ,则反应 的平衡常数
;
②气体总物质的量为4.0mol,则H、CO、CO、HO(g)的物质的量依次为2mol、0.6mol、0.2mol、
2 2 2
1.2mol,设反应Ⅰ生成CO和H 物质的量都为xmol,反应Ⅱ消耗CO物质的量为ymol、生成H 物质的量
2 2
为ymol,则x+y=2、x-y=0.6,解得x=1.3、y=0.7,反应Ⅱ生成CO 物质的量为0.7mol,反应Ⅲ消耗CO 物
2 2
质的量为0.7mol-0.2mol=0.5mol,则由反应Ⅲ知,此时CaCO (s)物质的量为0.5mol;
3
③若向平衡体系中通入少量 ,重新达平衡后,反应 的K= ,温
p
度不变,K 不变,则分压 不变;将反应Ⅰ-反应Ⅱ得C(s)+CO(g)=2CO(g),温度不变,该反应的
p 2
K= 不变,则 不变。
p
11.(2024·全国甲卷·高考真题)甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙烯(
)的研究所获得的部分数据如下。回答下列问题:
(1)已知如下热化学方程式:
计算反应 的 。
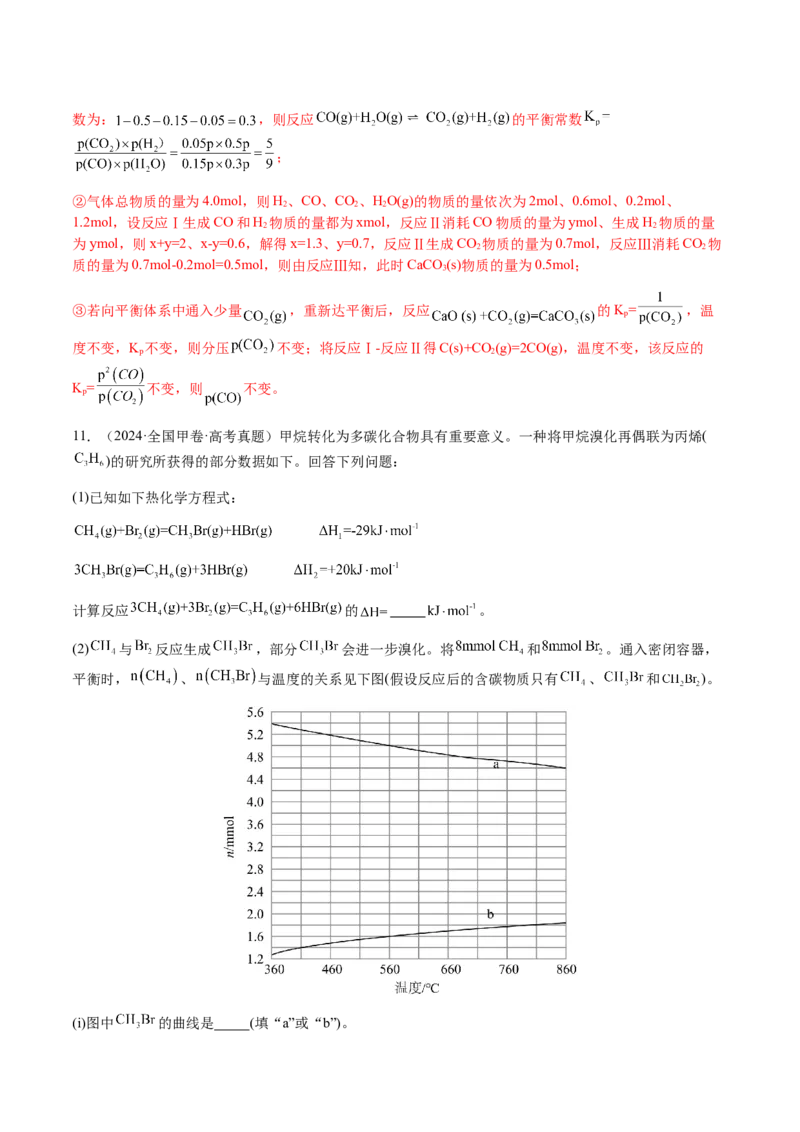
(2) 与 反应生成 ,部分 会进一步溴化。将 和 。通入密闭容器,
平衡时, 、 与温度的关系见下图(假设反应后的含碳物质只有 、 和 )。
(i)图中 的曲线是 (填“a”或“b”)。(ii) 时, 的转化率 , 。
(iii) 时,反应 的平衡常数 。
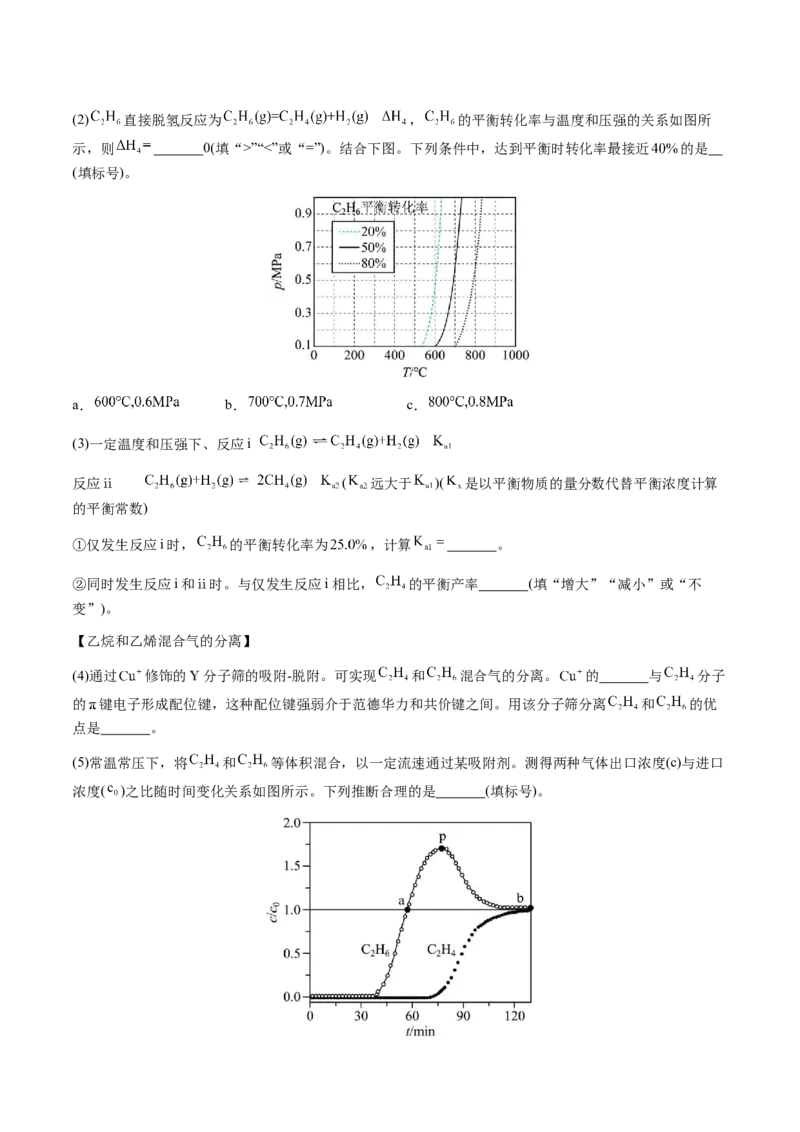
(3)少量 可提高生成 的选择性。 时,分别在有 和无 的条件下,将 和
,通入密闭容器,溴代甲烷的物质的量(n)随时间(t)的变化关系见下图。
(i)在 之间,有 和无 时 的生成速率之比 。
(ii)从图中找出 提高了 选择性的证据: 。
(ⅲ)研究表明, 参与反应的可能机理如下:
①
②
③
④
⑤
⑥
根据上述机理,分析 提高 选择性的原因: 。
【答案】
(1)-67
(2)a 80% 7.8 10.92(3) (或3:2) 5s以后有I 催化的CHBr 的含量逐渐降低,有I 催化的CHBr的含量陡然上升 I
2 2 2 2 3 2
的投入消耗了部分CHBr ,使得消耗的CHBr 发生反应生成了CHBr
2 2 2 2 3
【详解】(1)将第一个热化学方程式命名为①,将第二个热化学方程式命名为②。根据盖斯定律,将方
程式①乘以3再加上方程式②,即①×3+②,故热化学方程式3CH(g)+3Br (g)=C H(g)+6HBr(g)的
4 2 3 6
∆H=-29×3+20=-67kJ·mol-1。
(2)(i)根据方程式①,升高温度,反应向吸热反应方向移动,升高温度,平衡逆向移动,CH(g)的含量增
4
多,CHBr(g)的含量减少,故CHBr的曲线为a;
3 3
(ii)560℃时反应达平衡,剩余的CH(g)的物质的量为1.6mmol,其转化率α=
4
×100%=80%;若只发生一步反应,则生成6.4mmol CH Br,但此时剩余CHBr的物质的量为5.0mmol,说
3 3
明还有1.4mmol CH Br发生反应生成CHBr ,则此时生成的HBr的物质的量n=6.4+1.4=7.8mmol;
3 2 2
(iii)平衡时,反应中各组分的物质的量分别为n(CHBr)=5.0mmol、n(Br)=0.2mmol、n(CHBr )=1.4mmol、
3 2 2 2
n(HBr)=7.8mmol,故该反应的平衡常数K= = =10.92。
(3)(i)11~19s时,有I 的生成速率v= = mmol·(L·s)-1,无I 的生成速率v= =
2 2
mmol·(L·s)-1。生成速率比 = = ;
(ii)从图中可以看出,大约4.5s以后有I 催化的CHBr 的含量逐渐降低,有I 催化的CHBr的含量陡然上
2 2 2 2 3
升,因此,可以利用此变化判断I 提高了CHBr的选择性;
2 3
(iii)根据反应机理,I 的投入消耗了部分CHBr ,同时也消耗了部分HBr,使得消耗的CHBr 发生反应生
2 2 2 2 2
成了CHBr,提高了CHBr的选择性。
3 3
12.(2024·安徽·高考真题)乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。回答
下列问题:
【乙烷制乙烯】
(1) 氧化脱氢反应:
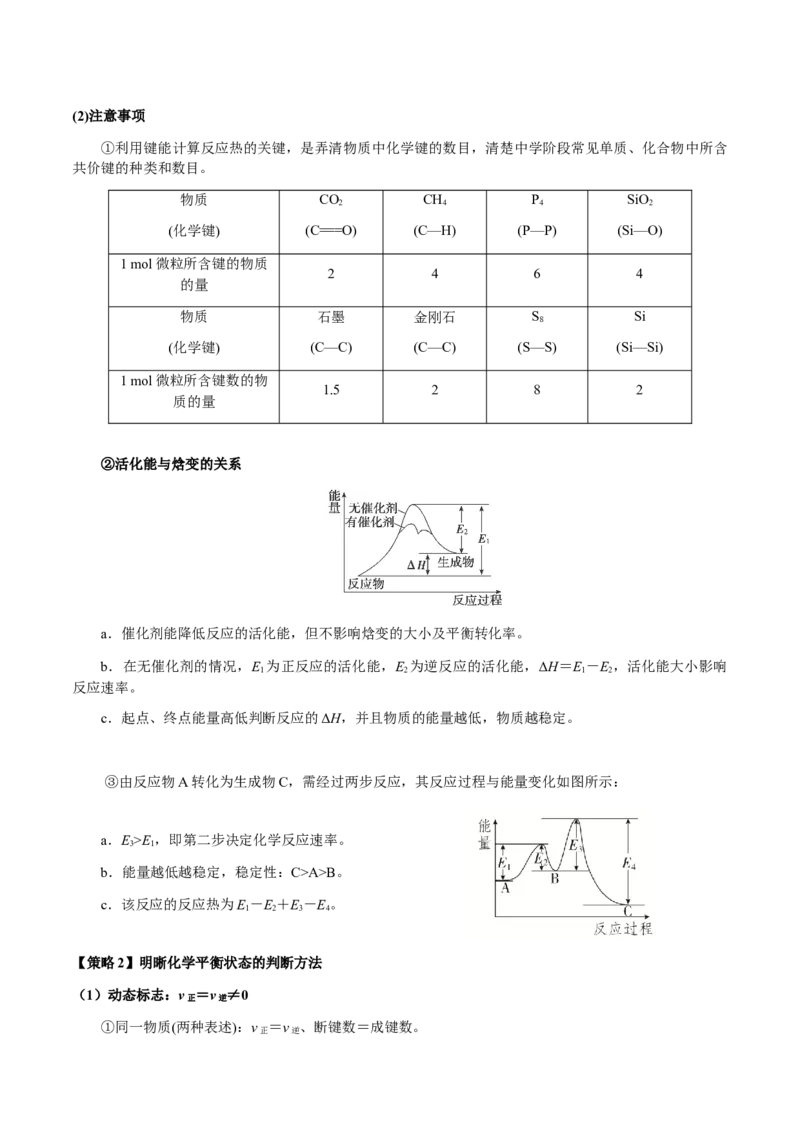
计算:(2) 直接脱氢反应为 , 的平衡转化率与温度和压强的关系如图所
示,则 0(填“>”“<”或“=”)。结合下图。下列条件中,达到平衡时转化率最接近 的是
(填标号)。
a. b. c.
(3)一定温度和压强下、反应i
反应ⅱ ( 远大于 )( 是以平衡物质的量分数代替平衡浓度计算
的平衡常数)
①仅发生反应i时, 的平衡转化率为 ,计算 。
②同时发生反应i和ⅱ时。与仅发生反应i相比, 的平衡产率 (填“增大”“减小”或“不
变”)。
【乙烷和乙烯混合气的分离】
(4)通过 修饰的Y分子筛的吸附-脱附。可实现 和 混合气的分离。 的 与 分子
的 键电子形成配位键,这种配位键强弱介于范德华力和共价键之间。用该分子筛分离 和 的优
点是 。
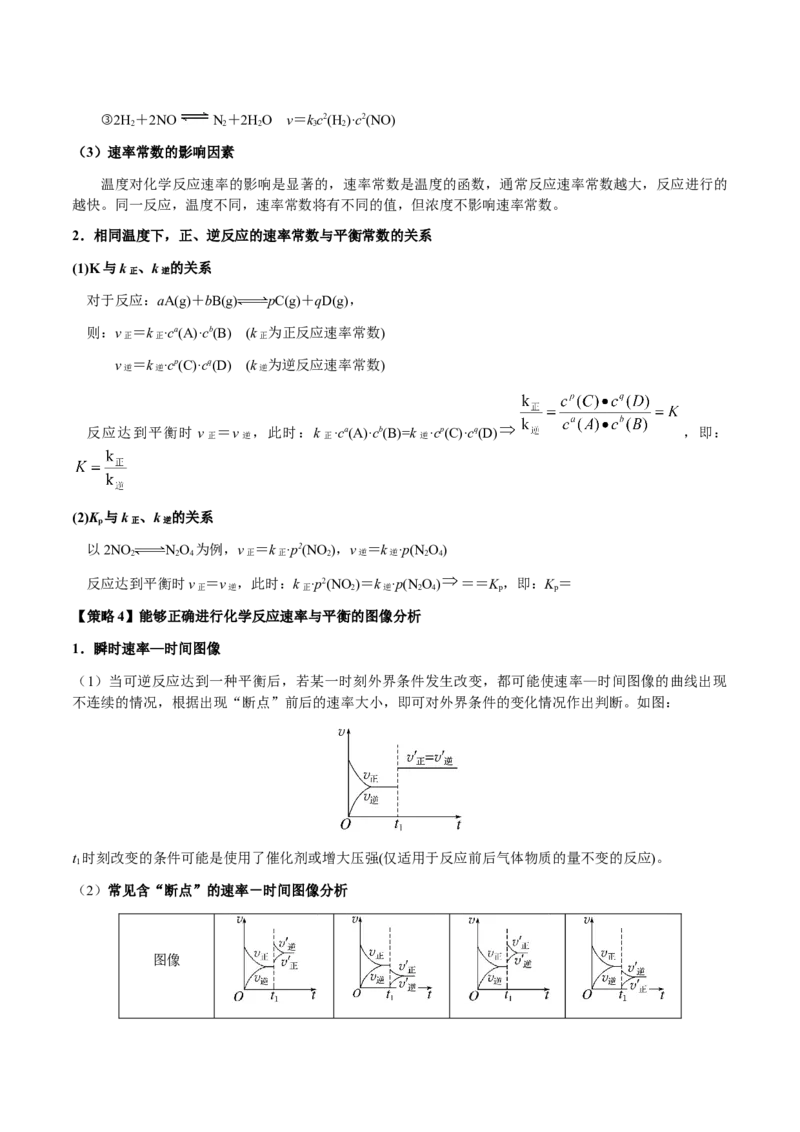
(5)常温常压下,将 和 等体积混合,以一定流速通过某吸附剂。测得两种气体出口浓度(c)与进口
浓度( )之比随时间变化关系如图所示。下列推断合理的是 (填标号)。A.前 ,两种气体均未被吸附
B.p点对应的时刻,出口气体的主要成分是
C.a-b对应的时间段内,吸附的 逐渐被 替代
【答案】
(1)-566
(2)> b
(3) 增大
(4)4s空轨道 识别度高,能有效将C H 和C H 分离,分离出的产物中杂质少,纯度较高
2 4 2 6
(5)BC
【详解】(1)将两个反应依次标号为反应①和反应②,反应①-反应②×2可得目标反应,则ΔH=ΔH -
3 1
2ΔH=(-209.8-178.1×2)kJ/mol=-566kJ/mol;
2
(2)从图中可知,压强相同的情况下,随着温度升高,C H 的平衡转化率增大,因此该反应为吸热反
2 6
应,ΔH>0;
4
a.600℃,0.6MPa时,C H 的平衡转化率约为20%,a错误;
2 6
b.700℃,0.7MPa时,C H 的平衡转化率约为50%,最接近40%,b正确;
2 6
c.700℃,0.8MPa时,C H 的平衡转化率接近50%,升高温度,该反应的化学平衡正向移动,C H 转化
2 6 2 6
率增大,因此800℃,0.8MPa时,C H 的平衡转化率大于50%,c错误;
2 6
故答案选b;
(3)①仅发生反应i,设初始时C H 物质的量为1mol,平衡时C H 转化率为25%,则剩余的C H 物质的
2 6 2 6 2 6
量为1-0.25=0.75mol,生成C H0.25mol,生成H0.25mol,容器内气体总物质的量为
2 4 2
(0.75+0.25+0.25)=1.25mol,K = ;
a1
②反应i压强平衡常数 ,反应ⅱ按 消耗了反应i的反应物C H 和产物H,则
2 6 2
,现要比较K 和Q 的大小,因 ,所以比较
p1 p1
与 的大小关系, ,故 ,反应i平
衡正向移动,生成更多的C H,因此C H 的平衡产率增大;
2 4 2 4(4)配合物中,金属离子通常提供空轨道,配体提供孤电子对,则Cu+的4s空轨道与C H 分子的π键电
2 4
子形成配位键。C H 能与Cu+形成配合物而吸附在Y分子筛上,C H 中无孤电子对不能与Cu+形成配合物
2 4 2 6
而无法吸附,通过这种分子筛分离C H 和C H,优点是识别度高,能有效将C H 和C H 分离,分离出的
2 4 2 6 2 4 2 6
产物中杂质少,纯度较高;
(5)A.前30min, 等于0,出口浓度c为0,说明两种气体均被吸附,A错误;
B.p点时,C H 对应的 约为1.75,出口处C H 浓度较大,而C H 对应的 较小,出口处C H 浓度较
2 6 2 6 2 4 2 4
小,说明此时出口处气体的主要成分为C H,B正确;
2 6
C.a点处C H 的 =1,说明此时C H 不再吸附在吸附剂上,而a点后C H 的 >1,说明原来吸附在吸
2 6 2 6 2 6
附剂上的C H 也开始脱落,同时从图中可知,a点后一段时间,C H 的 仍为0,说明是吸附的C H 逐渐
2 6 2 4 2 6
被C H 替代,p点到b点之间,吸附的C H 仍在被C H 替代,但是速率相对之前有所减小,同时吸附剂可
2 4 2 6 2 4
能因吸附量有限等原因无法一直吸附C H,因此p点后C H 的 也逐步增大,直至等于1,此时吸附剂不
2 4 2 4
能再吸附两种物质,C正确;
故答案选BC。
【策略1】熟练掌握反应焓变的计算
(1)根据化学反应过程中的能量变化来计算
ΔH=生成物的总能量-反应物的总能量
ΔH=反应物的总键能-生成物的总键能
ΔH=正反应活化能-逆反应活化能
图示
意义 a表示正反应的活化能;b表示逆反应的活化能;c表示该反应的反应热
图1:ΔH=(a-b)kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b)kJ·mol-1=c kJ·mol-1,表示吸热反应(2)注意事项
①利用键能计算反应热的关键,是弄清物质中化学键的数目,清楚中学阶段常见单质、化合物中所含
共价键的种类和数目。
物质 CO CH P SiO
2 4 4 2
(化学键) (C===O) (C—H) (P—P) (Si—O)
1 mol微粒所含键的物质
2 4 6 4
的量
物质 石墨 金刚石 S Si
8
(化学键) (C—C) (C—C) (S—S) (Si—Si)
1 mol微粒所含键数的物
1.5 2 8 2
质的量
②活化能与焓变的关系
a.催化剂能降低反应的活化能,但不影响焓变的大小及平衡转化率。
b.在无催化剂的情况,E 为正反应的活化能,E 为逆反应的活化能,ΔH=E -E ,活化能大小影响
1 2 1 2
反应速率。
c.起点、终点能量高低判断反应的ΔH,并且物质的能量越低,物质越稳定。
③由反应物A转化为生成物C,需经过两步反应,其反应过程与能量变化如图所示:
a.E>E,即第二步决定化学反应速率。
3 1
b.能量越低越稳定,稳定性:C>A>B。
c.该反应的反应热为E-E+E-E。
1 2 3 4
【策略2】明晰化学平衡状态的判断方法
(1)动态标志:v =v ≠0
正 逆
①同一物质(两种表述):v =v 、断键数=成键数。
正 逆②不同物质:必须标明是“异向”的反应速率关系。
如aA+bB cC+dD,=时,反应达到平衡状态。
(2)“变量不变”:如果一个量是随反应进行而改变的(即变量),当其“不变”时反应就达到平衡状态。
A. 混合体系中各组分的物质的量、质量、物质的量浓度、百分含量(体积分数、质量分数)、转化率、
颜色(某组分有颜色)等会随时间变化而变化,为变量,当其不随时间而改变时,反应达到平衡。
B. 绝热体系中温度为变量,当其不随时间而改变时,反应达到平衡。
C. M、ρ、p 等,不一定为变量,要根据不同情况进行判断:
总
注:若有非气体物质参与反应,无论Δn(g)是否等于0,M、ρ均为变量,若其恒定不变,则化学反应
达到平衡状态。
mA(s)+nB(g) pC(g)+qD(g),若A为固体或液体,则 是否是平衡状态
混合气体的平均摩尔质量一定 平衡
混合气体的密度一定 平衡
(3)常见的判断依据:以mA(g)+nB(g) pC(g)+qD(g)为例
类型 判断依据 是否是平衡状态①各物质的物质的量或各物质的物质的量的分数一定 平衡
②各物质的质量或各物质质量分数一定 平衡
混合物体系中各
成分的含量
③各气体的体积或体积分数一定 平衡
④总体积、总压强、总物质的量一定 不一定平衡
①在单位时间内消耗了 m molA 同时生成 m molA,即
平衡
v(正)=v(逆)
②在单位时间内消耗了 n molB 同时消耗了 p molC,则
正、逆反应 平衡
v(正)=v(逆)
速率的关系
③在单位时间内生成 n molB,同时消耗了 q molD,因均指
不一定平衡
v(逆)
④v(A):v(B):v(C):v(D)=m:n:p:q,v(正)不一定等于v(逆) 不一定平衡
①m+n≠p+q时,总压强一定 (其他条件一定) 平衡
压强
②m+n=p+q时,总压强一定 (其他条件一定) 不一定平衡
混合气体平均相 ① 一定时,只有当m+n≠p+q时 平衡
对分子质量
② 一定时,但m+n=p+q时 不一定平衡
温度 任何反应都伴随着能量变化,当体系温度一定时 平衡
颜色 反应体系内有色物质的颜色一定 平衡
恒温恒容时,密度一定 不一定平衡
体系的密度 恒温恒压时,若m+n≠p+q,则密度一定时 平衡
恒温恒压时,若m+n=p+q,则密度一定时 不一定平衡
【策略3】掌握化学平衡的相关计算
一.化学平衡常数和转化率的有关计算(“三段法”)
(1)掌握一个方法——“三段式”法
“三段式法”是有效解答化学平衡计算题的“万能钥匙”。解题时,要注意准确地列出起始量、变化
量、平衡量,按题目要求进行计算,同时还要注意单位的统一。
对以下反应:mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量(mol)分别为a、b,达到平衡
后,A的消耗量为mx mol,容器容积为V L。
mA(g)+nB(g) pC(g)+qD(g)
起始/mol a b 0 0变化/mol mx nx px qx
平衡/mol a-mx b-nx px qx
(2)明确三个量的关系
①三个量:即起始量、变化量、平衡量。
②关系:
对于同一反应物,起始量-变化量=平衡量。
对于同一生成物,起始量+变化量=平衡量。
各转化量之比等于各反应物的化学计量数之比。
(3)掌握以下公式
①平衡常数:K=。
②A的平衡浓度:c(A)= mol·L-1。
③A的转化率:α(A)=×100%,α(A)∶α(B)=∶=。
(转化率=×100%=×100%)
④A的体积分数:φ(A)=×100%。
(某组分的体积分数=×100%)
⑤平衡混合物中某组分的百分含量=×100%。
⑥平衡压强与起始压强之比:=。
⑦混合气体的平均密度:ρ = g·L-1。
混
⑧混合气体的平均摩尔质量:M= g·mol-1。
⑨生成物的产率:实际产量(指生成物)占理论产量的百分数。一般来讲,转化率越大,原料利用率越
高,产率越大。
产率=×100%。
二.压强平衡常数(K )
p
1.压强平衡常数(K )
p
(1)当把化学平衡常数K表达式中各物质的浓度用该物质的分压来表示时,就得到该反应的压强平衡常
数K ,其表达式的意义相同。
p
对于一般可逆反应mA+nB pC+qD,当在一定温度下达到平衡时,其压强平衡常数K =,其中
p
p(A)、p(B)、p(C)、p(D)表示反应物和生成物的分压,平衡分压计算方法如下:
某气体的分压=总压p(总)×该气体的物质的量分数(或体积分数)。p(总)=p(A)+p(B)+p(C)+p(D);
(2)K 仅适用于气相发生的反应。
p
2.计算步骤及模板
(1)计算步骤
①根据三段式法计算平衡体系中各组分的物质的量或物质的量浓度。
②计算各气体组分的物质的量分数或体积分数。
③根据分压计算公式求出各气体物质的分压。
④根据平衡常数计算公式代入计算。
(2)两种K 的计算模板:
p
模板一 模板二
①平衡总压为p ②刚性容器起始压强为p,平衡转化率为α。
0 0
N(g) + 3H(g) 2NH (g) 2NO (g) NO(g)
2 2 3 2 2 4
n(平) a b c p(始) p 0
0
p(分压) p p p Δp pα pα
0 0 0 0 0
K = p(平) p-pα pα
p 0 0 0
K =
p
三.速率常数与平衡常数的计算
1.速率常数
(1)速率常数含义
速率常数(k)是指在给一定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,
可用速率常数大小来比较化学反应的反应速率。
化学反应速率与反应物浓度(或浓度的次方)成正比,而速率常数是其比例常数,在恒温条件下,速率
常数不随反应物浓度的变化而改变。因此,可以应用速率方程求出该温度下任意浓度时的反应速率。
(2)速率方程
一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比。
对于基元反应(能够一步完成的反应):aA+bB===gG+hH,则v=kca(A)·cb(B)(其中k为速率常数)。如
①SO Cl SO +Cl v=kc(SO Cl)
2 2 2 2 1 2 2
②2NO 2NO+O v=kc2(NO )
2 2 2 2③2H+2NO N+2HO v=kc2(H )·c2(NO)
2 2 2 3 2
(3)速率常数的影响因素
温度对化学反应速率的影响是显著的,速率常数是温度的函数,通常反应速率常数越大,反应进行的
越快。同一反应,温度不同,速率常数将有不同的值,但浓度不影响速率常数。
2.相同温度下,正、逆反应的速率常数与平衡常数的关系
(1)K与k 、k 的关系
正 逆
对于反应:aA(g)+bB(g) pC(g)+qD(g),
则:v =k ·ca(A)·cb(B) (k 为正反应速率常数)
正 正 正
v =k ·cp(C)·cq(D) (k 为逆反应速率常数)
逆 逆 逆
反应达到平衡时 v =v ,此时:k ·ca(A)·cb(B)=k ·cp(C)·cq(D) ,即:
正 逆 正 逆
(2)K 与k 、k 的关系
p 正 逆
以2NO NO 为例,v =k ·p2(NO ),v =k ·p(NO)
2 2 4 正 正 2 逆 逆 2 4
反应达到平衡时v =v ,此时:k ·p2(NO )=k ·p(N O) ==K ,即:K =
正 逆 正 2 逆 2 4 p p
【策略4】能够正确进行化学反应速率与平衡的图像分析
1.瞬时速率—时间图像
(1)当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率—时间图像的曲线出现
不连续的情况,根据出现“断点”前后的速率大小,即可对外界条件的变化情况作出判断。如图:
t 时刻改变的条件可能是使用了催化剂或增大压强(仅适用于反应前后气体物质的量不变的反应)。
1
(2)常见含“断点”的速率-时间图像分析
图像升高 降低 升高 降低
温
t 1 时刻 度 正反应为放热反应 正反应为吸热反应
所改变
增大 减小 增大 减小
的条件 压
强
正反应为气体物质的量增大的反应 正反应为气体物质的量减小的反应
(3)“渐变”类速率-时间图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增
1 正 逆
大;v′ >v′ ,平衡向正反应方 t 时其他条件不变,增大反应物的浓度
正 逆 1
向移动
t 时v′ 突然减小,v′ 逐渐减
1 正 逆
小;v′ >v′ ,平衡向逆反应方 t 时其他条件不变,减小反应物的浓度
逆 正 1
向移动
t 时v′ 突然增大,v′ 逐渐增
1 逆 正
大;v′ >v′ ,平衡向逆反应方 t 时其他条件不变,增大生成物的浓度
逆 正 1
向移动
t 时v′ 突然减小,v′ 逐渐减
1 逆 正
小;v′ >v′ ,平衡向正反应方 t 时其他条件不变,减小生成物的浓度
正 逆 1
向移动
2.全程速率—时间图像
(1)Zn与足量盐酸的反应,反应速率随时间的变化如图所示
AB段:Zn与盐酸的反应是放热反应,使溶液的温度升高,化学反应速率逐渐增
大。
BC段:随着反应的进行,盐酸的浓度逐渐减小,化学反应速率逐渐减小。
(2)HC O 溶液中加入酸性KMnO 溶液,随着反应的进行,反应速率随时间的变化如图所示
2 2 4 4
反应方程式 2KMnO +5HC O+3HSO ===K SO +2MnSO +10CO↑+8HO
4 2 2 4 2 4 2 4 4 2 2AB段:反应产生的Mn2+对该反应起催化作用。
BC段:随着反应的进行,反应物的浓度逐渐减小,化学反应速率逐渐减小。
3.物质的量(或浓度)—时间图像
例如:某温度时,在定容(V L)容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
(1)由图像得出的信息
①X、Y是反应物,Z是生成物。
②t s时反应达到平衡状态,X、Y并没有全部反应,该反应是可逆反应。
3
③0~t s时间段:Δn(X)=n-nmol,Δn(Y)=n-nmol,Δn(Z)=nmol。
3 1 3 2 3 2
(2)根据图像可进行如下计算
①某物质的平均速率、转化率,如v(X)= mol·L-1·s-1;Y的转化率=×100%。
②确定化学方程式中的化学计量数之比,X、Y、Z三种物质的化学计量数之比为(n-n)∶(n-n)∶n。
1 3 2 3 2
4.含量—时间—温度(压强)图像
(1)识图技巧
分析反应由开始(起始物质相同时)达到平衡所用时间的长短可推知反应条件的变化。
①若为温度变化引起,温度较高时,反应达平衡所需时间短。
②若为压强变化引起,压强较大时,反应达平衡所需时间短。
③若为是否使用催化剂,使用适宜催化剂时,反应达平衡所需时间短。
(2)应用举例
C%指生成物的质量分数,B%指反应物的质量分数。【技法解读】
“先拐先平,数值大”,即曲线先出现拐点的首先达到平衡,反应速率快,以此判断温度或压强的高
低。再依据外界条件对平衡的影响分析判断反应的热效应及反应前后气体体积的变化。
5.“A的转化率(或C的含量)-温度-压强”四种图像
以mA(g)+nB(g) pC(g)+qD(g) ΔH=Q kJ·mol-1为例
m+n>p+q,ΔH>0 m+np+q,ΔH<0 m+n0
【技法解读】
解答时应用“定一议二”原则,即把自变量(温度、压强)之一设为恒量,讨论另外两个变量的关系。
通过分析相同温度下不同压强时,反应物A的转化率大小来判断平衡移动的方向,从而确定反应方程式中反应物与产物气体物质间的化学计量数的大小关系。如图甲中任取一条温度曲线研究,压强增大,A
的转化率增大,平衡正向移动,则正反应为气体体积减小的反应,图丙中任取横坐标一点作横坐标垂线,
也能得出相同结论。
通过分析相同压强下不同温度时,反应物A的转化率的大小来判断平衡移动的方向,从而确定反应的
热效应。如图丙中任取一条压强曲线研究,温度升高,A的转化率减小,平衡逆向移动,则正反应为放热
反应,图乙中任取横坐标一点作垂线,也能得出相同结论。
6.速率—温度(压强)图
解题方法:曲线的意义是外界条件(温度、压强)对正、逆反应速率影响的变化趋势及变化幅度。图中交点
是平衡状态,压强增大(或温度升高)后正反应速率增大得快,平衡正向移动.
v-P图像:交点即为平衡状态,当压强增大,v >v ,表明平衡正向移动,正反应为气体体积减小的反
正 逆
应。
v-T图像:交点即为平衡状态,当温度升高,v >v ,表明平衡正向移动,正反应为吸热反应。
正 逆
7.“点-线-面”三维度分析特殊平衡图像
(1)对于化学反应:mA(g)+nB(g) pC(g)+qD(g),如图所示:M点前,表示从反应开始,v >v ;
正 逆
M点恰好达到平衡;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,
平衡左移,故正反应ΔH<0。
(2)对于化学反应:mA(g)+nB(g) pC(g)+qD(g),L线上所有的点都是平衡点(如图)。L线的左上方
(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以E点满足v >v ;同理,L线的右下
正 逆
方(F点)满足v <v 。
正 逆
8.化工生产中的复杂图像分析除通过图像获取有用信息和对获取的信息进行加工处理外,还需注意以下4点:
(1)曲线上的每个点是否都达到平衡
往往需要通过曲线的升降趋势或斜率变化来判断,如果还未达到平衡则不能使用平衡移动原理,只有
达到平衡以后的点才能应用平衡移动原理。
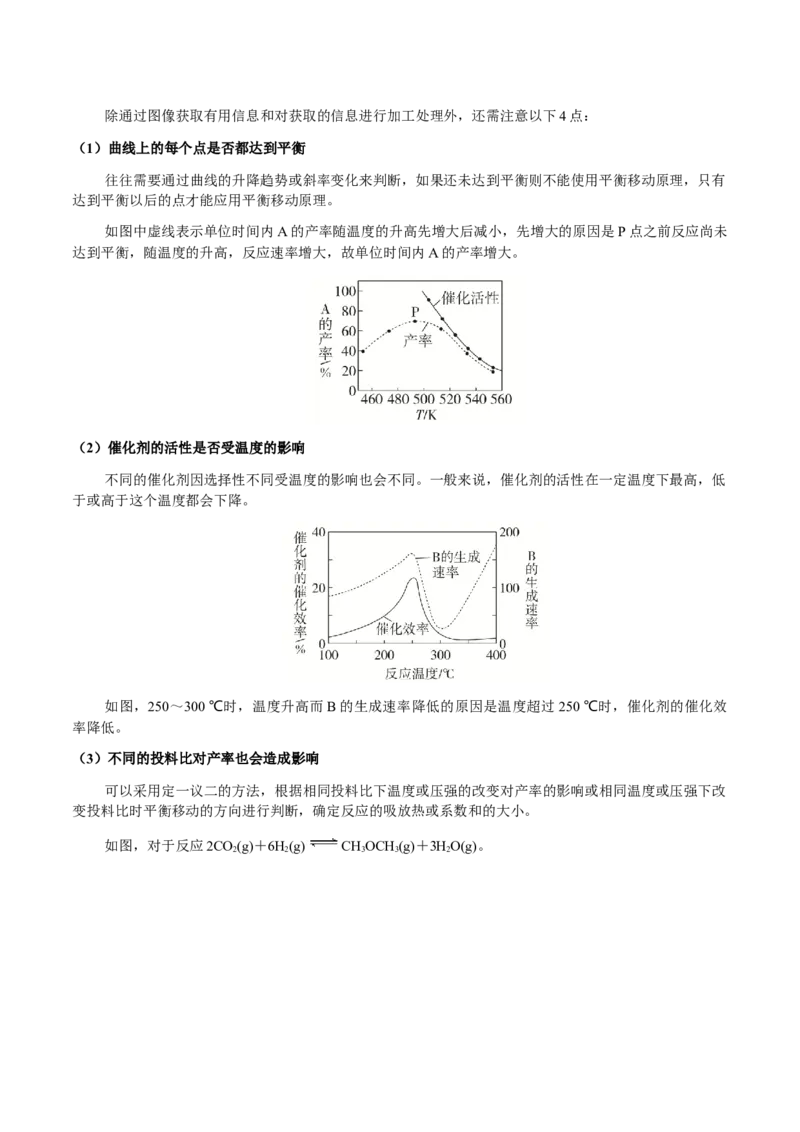
如图中虚线表示单位时间内A的产率随温度的升高先增大后减小,先增大的原因是P点之前反应尚未
达到平衡,随温度的升高,反应速率增大,故单位时间内A的产率增大。
(2)催化剂的活性是否受温度的影响
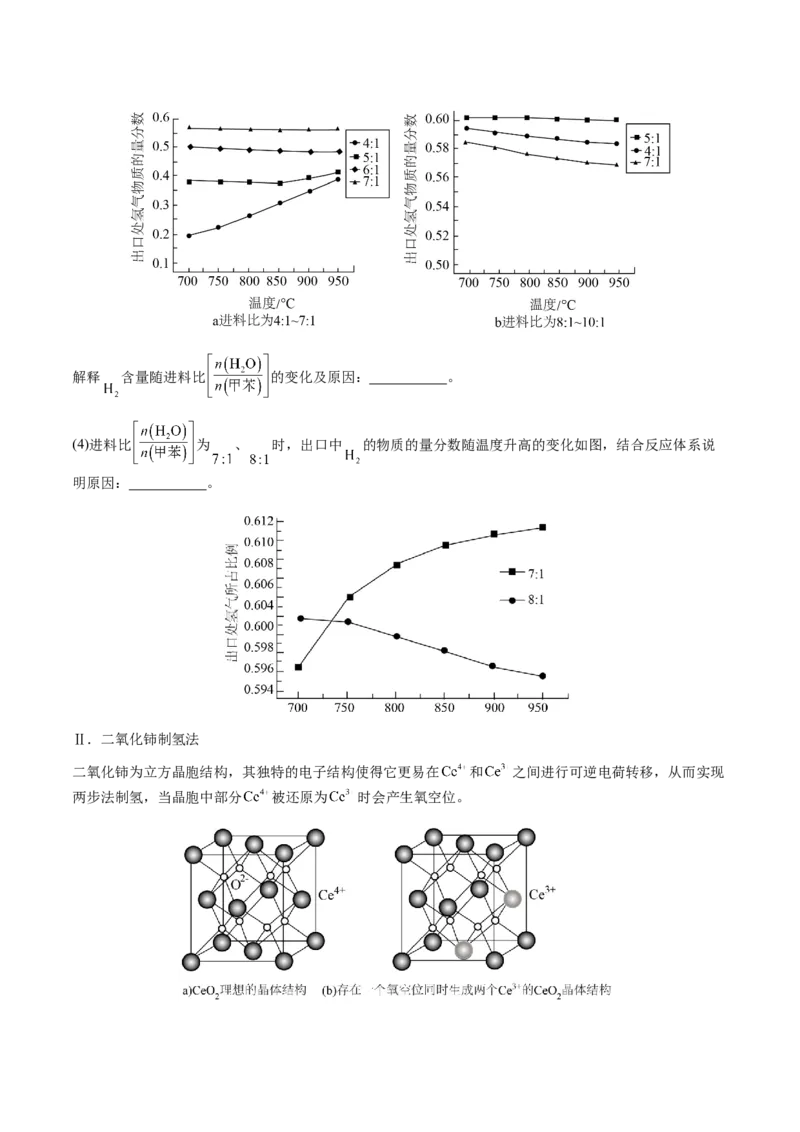
不同的催化剂因选择性不同受温度的影响也会不同。一般来说,催化剂的活性在一定温度下最高,低
于或高于这个温度都会下降。
如图,250~300 ℃时,温度升高而B的生成速率降低的原因是温度超过250 ℃时,催化剂的催化效
率降低。
(3)不同的投料比对产率也会造成影响
可以采用定一议二的方法,根据相同投料比下温度或压强的改变对产率的影响或相同温度或压强下改
变投料比时平衡移动的方向进行判断,确定反应的吸放热或系数和的大小。
如图,对于反应2CO(g)+6H(g) CHOCH (g)+3HO(g)。
2 2 3 3 2当投料比一定时,温度越高,CO 的转化率越低,所以升温,平衡左移,正反应为放热反应。若温度
2
不变,提高投料比[n(H )/n(CO)],则提高了二氧化碳的转化率。
2 2
(4)考虑副反应的干扰或影响
往往试题会有一定的信息提示,尤其温度的改变影响较大。
1.(2025·湖南株洲·一模)氢能是一种理想的绿色能源。有科学家预言,氢能有可能成为人类未来的主要
能源。我国科学家研制了下列三种制氢方法。
Ⅰ.甲苯催化重整制氢。主要反应有:
a.甲苯水蒸气重整:①
b.甲苯二氧化碳重整:②
c.水汽变换反应:③
d.甲烷化反应:④
⑤
(1)甲苯催化重整最适宜的条件是:___________(填标号)。
A.高温高压 B.高温低压 C.低温低压 D.低温高压
(2)反应: 。
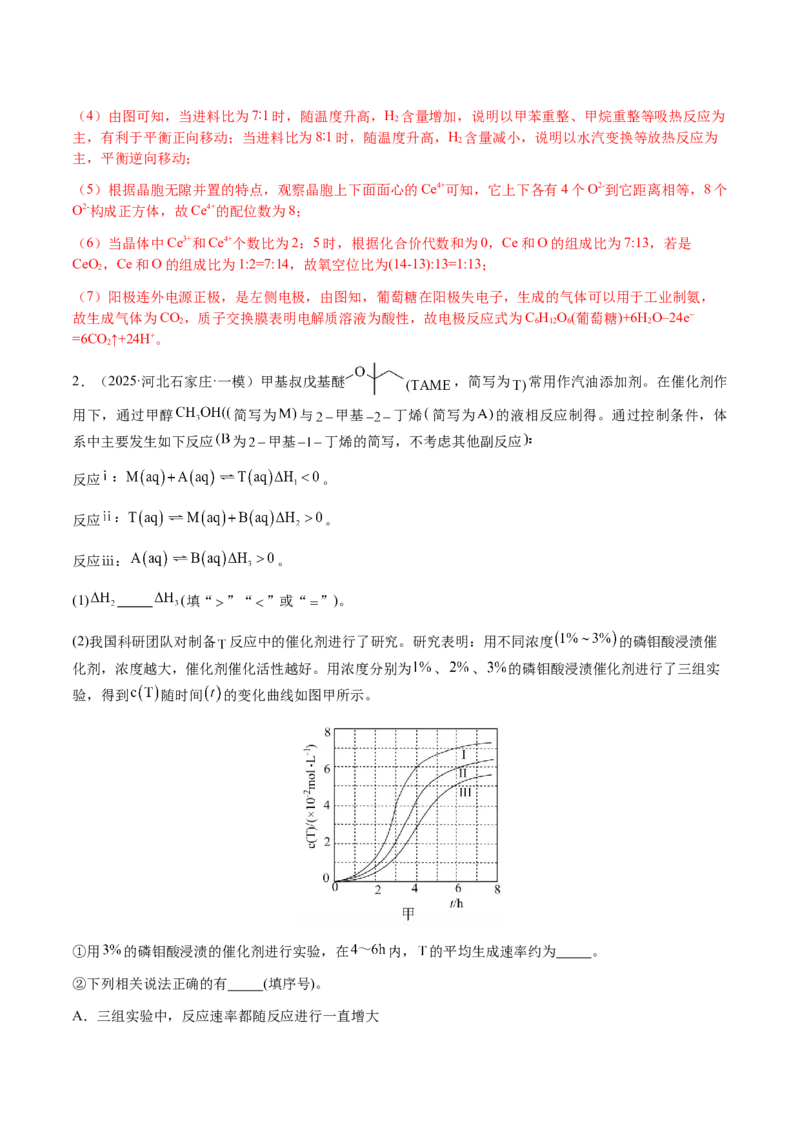
(3)一定压强下,反应釜出口 含量随温度、进料比 变化如图:解释 含量随进料比 的变化及原因: 。
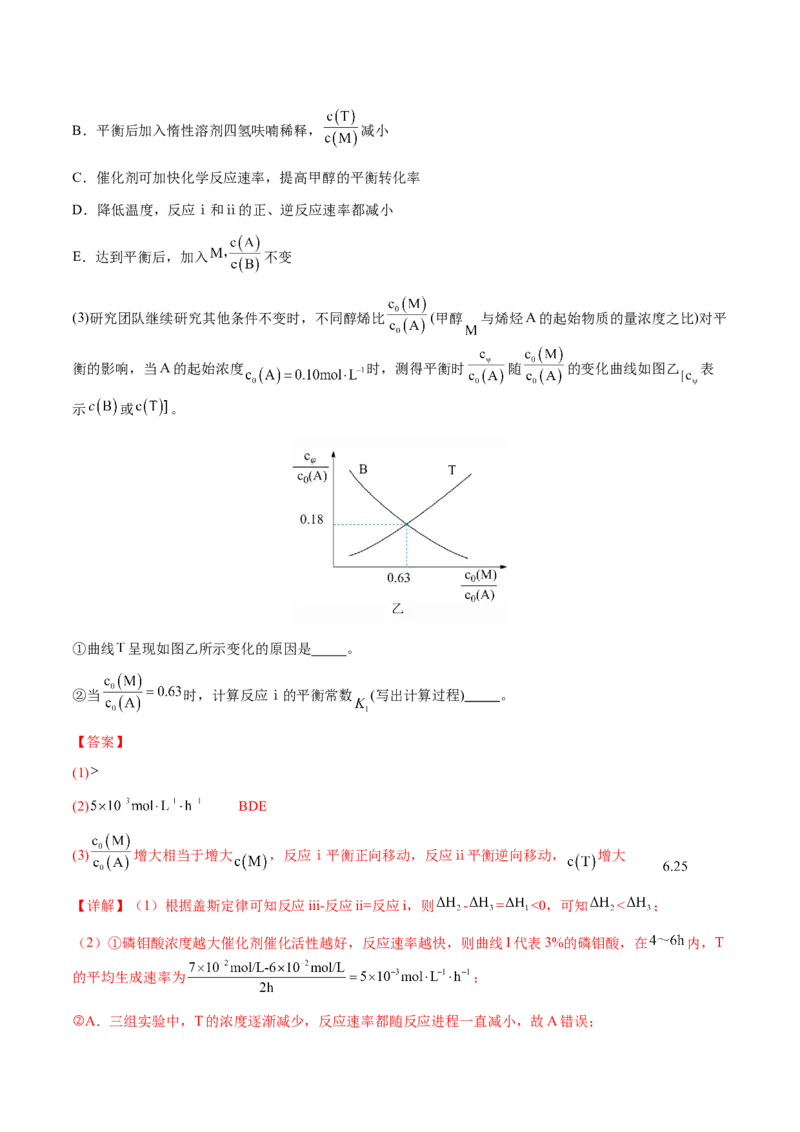
(4)进料比 为 、 时,出口中 的物质的量分数随温度升高的变化如图,结合反应体系说
明原因: 。
Ⅱ.二氧化铈制氢法
二氧化铈为立方晶胞结构,其独特的电子结构使得它更易在 和 之间进行可逆电荷转移,从而实现
两步法制氢,当晶胞中部分 被还原为 时会产生氧空位。(5)二氧化铈晶胞中 的配位数为: 。
(6)当晶体中 和 个数比为2:5时,氧空位比为 [ ]
Ⅲ.酸性葡萄糖溶液电催化制氢的原理如图:
(7)写出阳极的电极反应式: 。
【答案】
(1)B
(2)–573.6kJ/mol
(3)一定温度下,出口处H 的含量随进料比增加先增大后减小。进料比小于7∶1时,随水蒸气的增加平衡向
2
生成H 方向移动,出口处H 含量增加;进料比大于8∶1时,水蒸气过量,稀释了H 的含量
2 2 2
(4)当进料比为7∶1时,甲苯重整、甲烷重整等吸热反应为主;当进料比为8∶1时,水汽变换反应为主
(5)8
(6)1∶13
(7)C H O(葡萄糖)+6H O–24e–=6CO ↑+24H+
6 12 6 2 2
【详解】(1)甲苯催化重整无论是水蒸气重整还是二氧化碳重整的反应都是气体物质的量增大的反应,
且反应都吸热,故高温低压条件有利于反应正向进行,故选B;
(2)根据已知:
反应① C
7
H
8
(g)+7H
2
O(g)⇌7CO(g)+11H
2
(g) ΔH
1
=+869.1kJ/mol
反应⑤ CH
4
(g)+H
2
O(g)⇌CO(g)+3H
2
(g) ΔH
5
=+206.1kJ/mol
反应C H(g)+10H(g)=7CH (g)可以由反应①-反应⑤×7得到,则该反应的 ΔH= ΔH -ΔH ×7=–573.6kJ/mol;
7 8 2 4 1 5
(3)温度一定时,左图中,进料比增大,H 含量增加,右图中,进料比增大,H 含量减小,因为甲苯水
2 2
蒸气重整反应HO和甲苯反应比是7:1,故进料比小于7∶1时,随水蒸气的增加平衡向生成H 方向移动,
2 2
出口处H 含量增加;进料比大于8∶1时,水蒸气过量,稀释了H 的含量,一定温度下,出口处H 的含量
2 2 2
随进料比增加先增大后减小;(4)由图可知,当进料比为7∶1时,随温度升高,H 含量增加,说明以甲苯重整、甲烷重整等吸热反应为
2
主,有利于平衡正向移动;当进料比为8∶1时,随温度升高,H 含量减小,说明以水汽变换等放热反应为
2
主,平衡逆向移动;
(5)根据晶胞无隙并置的特点,观察晶胞上下面面心的Ce4+可知,它上下各有4个O2-到它距离相等,8个
O2-构成正方体,故Ce4+的配位数为8;
(6)当晶体中Ce3+和Ce4+个数比为2:5时,根据化合价代数和为0,Ce和O的组成比为7:13,若是
CeO,Ce和O的组成比为1:2=7:14,故氧空位比为(14-13):13=1:13;
2
(7)阳极连外电源正极,是左侧电极,由图知,葡萄糖在阳极失电子,生成的气体可以用于工业制氨,
故生成气体为CO,质子交换膜表明电解质溶液为酸性,故电极反应式为C H O(葡萄糖)+6H O–24e–
2 6 12 6 2
=6CO ↑+24H+。
2
2.(2025·河北石家庄·一模)甲基叔戊基醚 ,简写为 常用作汽油添加剂。在催化剂作
用下,通过甲醇 简写为 与 甲基 丁烯 简写为 的液相反应制得。通过控制条件,体
系中主要发生如下反应 为 甲基 丁烯的简写,不考虑其他副反应
反应 。
反应 。
反应ⅲ: 。
(1) (填“ ”“ ”或“ ”)。
(2)我国科研团队对制备 反应中的催化剂进行了研究。研究表明:用不同浓度 的磷钼酸浸渍催
化剂,浓度越大,催化剂催化活性越好。用浓度分别为 、 、 的磷钼酸浸渍催化剂进行了三组实
验,得到 随时间 的变化曲线如图甲所示。
①用 的磷钼酸浸渍的催化剂进行实验,在 内, 的平均生成速率约为 。
②下列相关说法正确的有 (填序号)。
A.三组实验中,反应速率都随反应进行一直增大B.平衡后加入惰性溶剂四氢呋喃稀释, 减小
C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应ⅰ和ⅱ的正、逆反应速率都减小
E.达到平衡后,加入 不变
(3)研究团队继续研究其他条件不变时,不同醇烯比 (甲醇 与烯烃A的起始物质的量浓度之比)对平
衡的影响,当A的起始浓度 时,测得平衡时 随 的变化曲线如图乙 表
示 或 。
①曲线 呈现如图乙所示变化的原因是 。
②当 时,计算反应ⅰ的平衡常数 (写出计算过程) 。
【答案】
(1)
(2) BDE
(3) 增大相当于增大 ,反应ⅰ平衡正向移动,反应ⅱ平衡逆向移动, 增大
【详解】(1)根据盖斯定律可知反应iii-反应ii=反应i,则 - = <0,可知 < ;
(2)①磷钼酸浓度越大催化剂催化活性越好,反应速率越快,则曲线I代表3%的磷钼酸,在 内,T
的平均生成速率为 ;
②A.三组实验中,T的浓度逐渐减少,反应速率都随反应进程一直减小,故A错误;B.平衡后加入惰性溶剂四氢呋喃稀释,c(A)减小,温度不变,反应i的平衡常数K= 不变,则
=K∙c(A)减小,故B正确;
C.催化剂可加快化学反应速率,但不能提高甲醇的平衡转化率,故C错误;
D.降低温度,反应i和ii的正、逆反应速率都减小,故D正确;
E.反应iii的平衡常数K= ,达到平衡后,加入M,K值不变, 不变,故E正确;
故选BDE。
(3)① 增大相当于增大c(M),反应i平衡正向移动,c(T)增大,反应ii平衡逆向移动,c(B)减小;
②根据已知条件列出“三段式”
平衡时c(T)=c(B)=0.018mol/L=(x-y)mol/L=(z+y)mol/L,则x+z=0.036,c(M)=(0.063-x+y)mol/L=[0.063-(x-
y)]mol/L=0.045mol/L,c(A)=(0.1-x-z)mol/L=[0.1-(x+z)]mol/L=0.064mol/L,则反应I的平衡常数K=
= 。
3.(2025·陕西宝鸡·一模)三氧化钼( )是石油工业中常用的催化剂,也是瓷轴药的颜料,该物质常
使用辉钼矿(主要成分为 )通过一定条件来制备。回答下列相关问题:
(1)已知:①
②
③则 的 (用含 、 、 的代数式表示)。
(2)若在恒温恒容条件下,仅发生反应
①下列说法正确的是 (填序号)
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加 的量,平衡正向移动
②达到平衡时 的浓度为 ,充入一定量的 ,反应再次达到平衡, 浓度
(选填“>”、“<”或“=”)
(3)在2L恒容密闭容器中充入 和 ,若仅发生反应: ,
5min后反应达到平衡,此时容器压强为起始时的80%,则0~5min内, 的反应速率为
。
(4)在恒容密闭容器中,加入足量 和 ,仅发生反应: 。
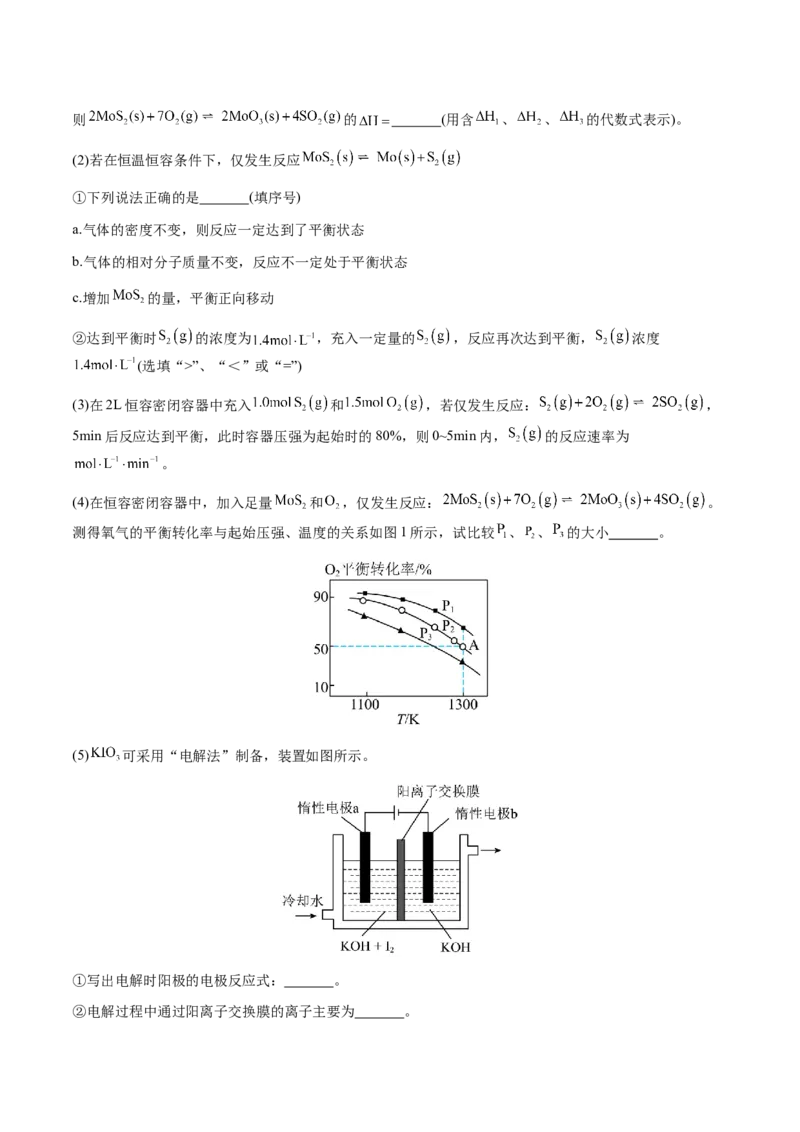
测得氧气的平衡转化率与起始压强、温度的关系如图1所示,试比较 、 、 的大小 。
(5) 可采用“电解法”制备,装置如图所示。
①写出电解时阳极的电极反应式: 。
②电解过程中通过阳离子交换膜的离子主要为 。【答案】
(1)
(2)ab
(3)0.05
(4)
(5)
【详解】(1)根据盖斯定律 得该反应,则反应热 。
(2)①a.只有S(g)为气体,随反应进行气体的总质量逐渐增大,容积不变,则气体密度逐渐增大,当气
2
体的密度不变,则反应一定达到了平衡状态,故a正确;
b.只有S(g)为气体,气体的相对分子质量始终不变,故当气体的相对分子质量不变,反应不一定处于平
2
衡状态,故b正确;
c.MoS 为固体,增加MoS 的量,平衡不移动,故c错误;
2 2
故答案为ab;
②只有S(g)为气体,K=c(S ),温度不变,K不变,则反应再次达到平衡,S(g)浓度=1.4mol/L。
2 2 2
(3)恒温恒容条件下,压强比等于物质的量之比,则平衡时,气体的总物质的量为 ,
则混合气体的减少量为 ,根据S(g)+2O(g)=2SO(g)可知,当有1molS (g)参加反应时,气体减
2 2 2 2
少1mol,故当气体减少0.5mol时,有0.5molS (g)参加反应,故S(g)的反应速率为
2 2
。
(4)该反应的正反应为气体物质的量减少的反应,加压平衡正向移动,氧气的平衡转化率增大,故
。
(5)电解时,阳极区的反应为碱性条件下单质碘发生氧化反应生成 ,阳极的电极反应式为
;溶液中的阳离子主要是钾离子,因此电解过程中通过阳离子交换膜的离子
主要是钾离子。
4.(2025·重庆·一模)重庆正着力打造“西部氢谷”,推动建设“成渝氢走廊”。利用甲酸(HCOOH)来制
氢和储氢是氢能研究的一个方向。
(1)我国科学家发现,Rh催化单分子甲酸分解制 的过程如图所示,其中带“*”的物质表示吸附在Rh表
面,该反应过程中决定反应速率步骤的反应方程式为 ;甲酸分解制 的热化学方程式可表示为
(图1中能量单位为eV,阿伏加德罗常数用 表示)(2)一定条件下, 可转化为储氢物质甲酸等。已知 与 在固载金属催化剂上可发生以下反应:
反应ⅰ.
反应ⅱ.
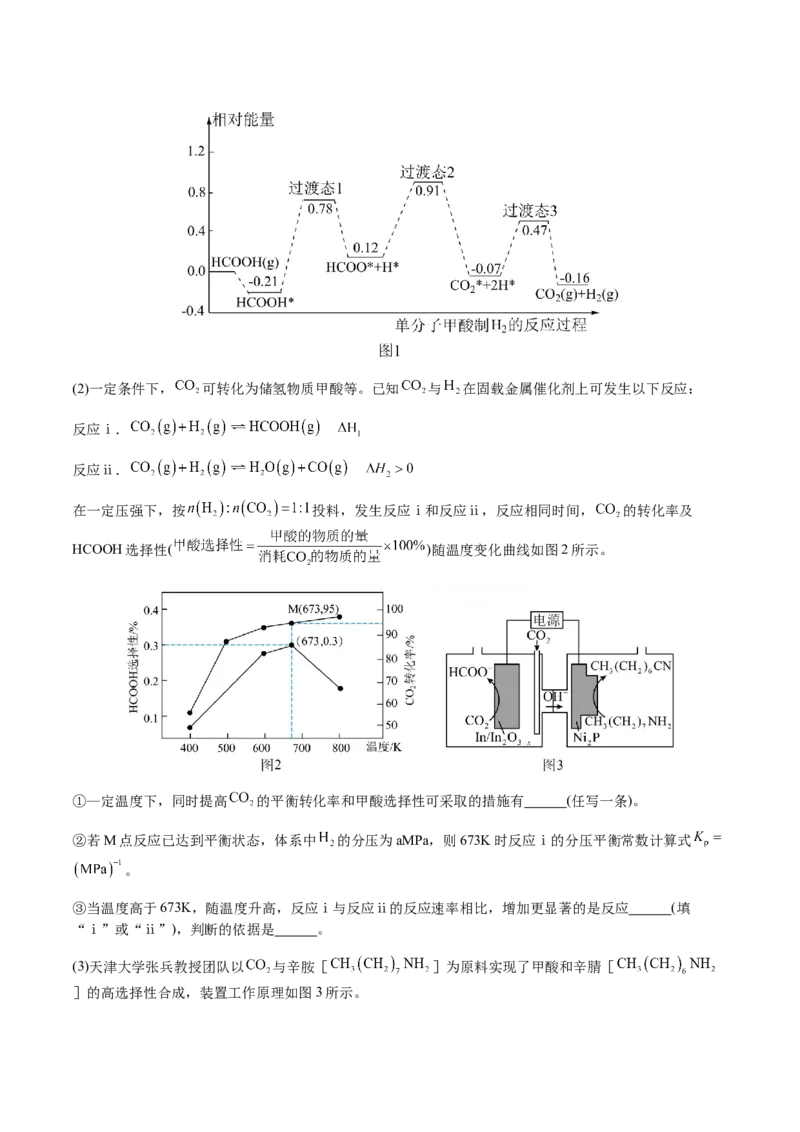
在一定压强下,按 投料,发生反应ⅰ和反应ⅱ,反应相同时间, 的转化率及
HCOOH选择性( )随温度变化曲线如图2所示。
①—定温度下,同时提高 的平衡转化率和甲酸选择性可采取的措施有 (任写一条)。
②若M点反应已达到平衡状态,体系中 的分压为aMPa,则673K时反应ⅰ的分压平衡常数计算式
。
③当温度高于673K,随温度升高,反应ⅰ与反应ⅱ的反应速率相比,增加更显著的是反应 (填
“ⅰ”或“ⅱ”),判断的依据是 。
(3)天津大学张兵教授团队以 与辛胺[ ]为原料实现了甲酸和辛腈[
]的高选择性合成,装置工作原理如图3所示。①工作时, 电极上发生 (填“氧化反应”或“还原反应”)。
②工作时,每转移2mol电子,理论上 电极上有 g辛腈生成。
【答案】
(1) -0.16
(2)加压(或其他合理答案) ⅱ 随温度升高, 的转化率升高,但HCOOH的选择性
却迅速下降
(3)还原反应 62.5
【详解】(1)活化能越大反应速率越慢,而慢反应决定总反应速率的快慢,由图可知该反应过程中的决
速步骤为: ;由图可知 相对能量为0,生成物 的相对能
量和为-0.16,则反应 ;
(2)①增加压强,反应ⅰ平衡正向移动,反应ⅱ不移动,故加压可以提高 的平衡转化率和甲酸选择
性;
②设 和 初始物质的量均为 ,发生反应i和反应ii,673K时 转化率为95%,即 共计消
耗 ,根据甲酸选择性为0.3%可计算,在反应i中生成 ,
同时消耗 ,则在反应ii中,消耗 ,同时生成
,平衡时 , ,
,平衡常数 ;
③当温度高于673K时,随温度升高,CO 转化率增大,但HCOOH的选择性却显著降低,可能得原因:升
2
高温度,反应i和反应ii的反应速率均加快,但反应ii速率加快的更显著;
(3)①由图中In/In O 电极上CO→HCOO-可知,CO 发生得电子的还原反应,In/In O 电极为阴极;
2 3-x 2 2 2 3-x
②由图中In/In O 电极为阴极,阴极反应为:CO+2e-+H O=HCOO-+OH-,则Ni P电极为阳极,辛胺在阳
2 3-x 2 2 2
极上发生失电子的氧化反应生成辛腈,电极反应为CH(CH)CHNH +4OH--4e-=CH (CH)CN+4HO, 每
3 2 6 2 2 3 2 6 2
转移2mol电子,理论上 电极上有0.5mol辛腈生成,质量为62.5g。
5.(2025·广东深圳·一模)铁及其化合物化学性质丰富,应用广泛。
(1)基态 的价电子排布式为 ;结合价电子排布式,解释 易被氧化为 的原因 。
(2)某含铁催化剂可催化苯的羟基化反应,其催化机理如图所示:①上述过程中,催化剂为 。
②该过程总反应为 (有机物写结构简式,不需注明反应条件)。
(3)标准摩尔生成焓是指一定温度与标准压强(101kPa)下由元素最稳定的单质生成1mol纯物质时的焓
变。已知:常温下, 与 的标准摩尔生成焓分别为 与 ,则在该条件下,
分解转化为 和 的 (用含 的式子表示)。
一定温度下, 与 混合溶液存在如下平衡(不考虑碘单质的挥发与阳离子的水解):
反应i:
反应ii:
(4)关于上述平衡体系的说法正确的有_____(填标号)。
A.加入 ,平衡时 增大
B.加入 固体,平衡时 的值增大
C.升高温度,反应 速率增大,反应 速率减小
D.加水稀释,溶液中离子总数增大
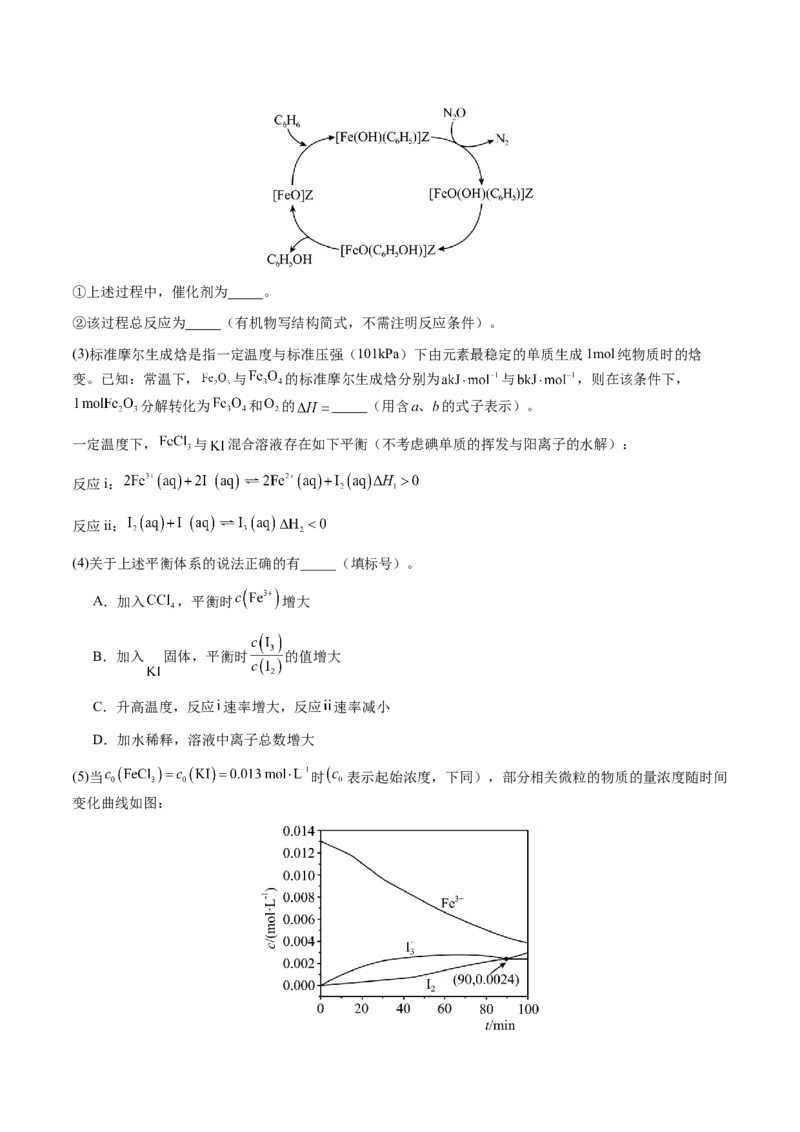
(5)当 时 表示起始浓度,下同),部分相关微粒的物质的量浓度随时间
变化曲线如图:①结合图中 变化分析,反应i的活化能 (填“大于”或“小于”)反应ii的活化能。
② 内,上述体系中 的平均反应速率 (保留两位有效数字)。
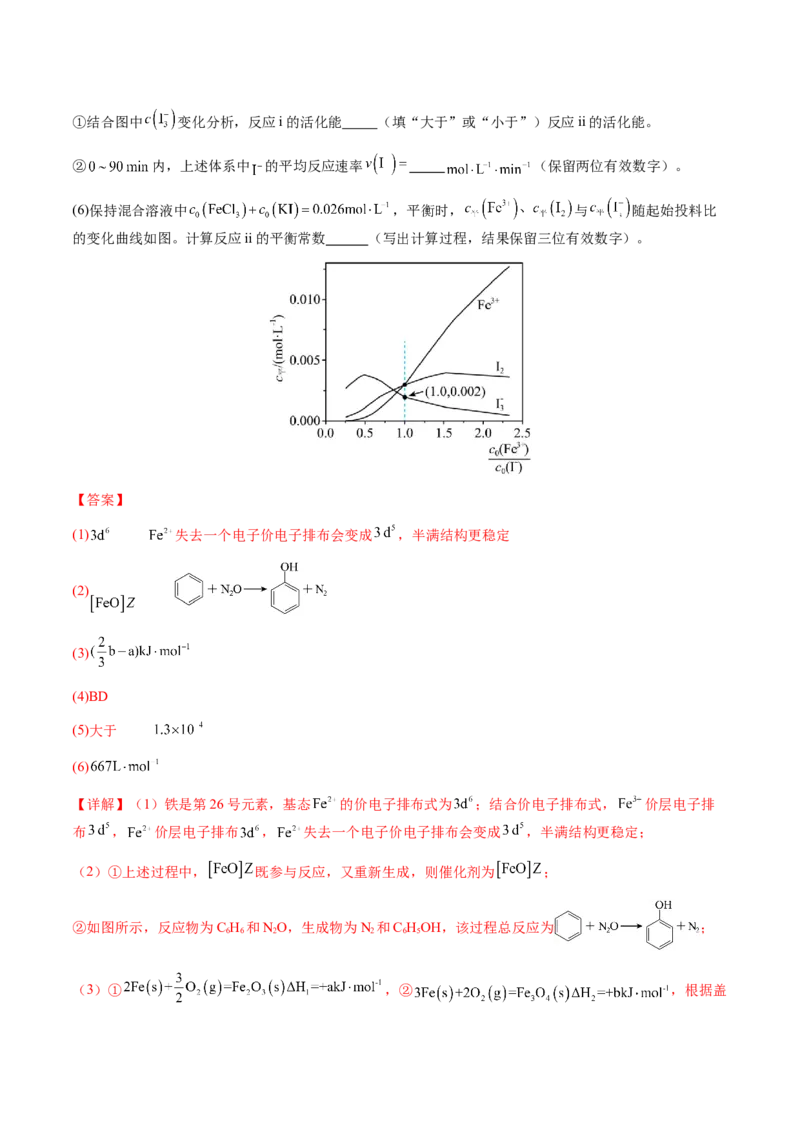
(6)保持混合溶液中 ,平衡时, 与 随起始投料比
的变化曲线如图。计算反应ii的平衡常数 (写出计算过程,结果保留三位有效数字)。
【答案】
(1) 失去一个电子价电子排布会变成 ,半满结构更稳定
(2)
(3)
(4)BD
(5)大于
(6)
【详解】(1)铁是第26号元素,基态 的价电子排布式为 ;结合价电子排布式, 价层电子排
布 , 价层电子排布 , 失去一个电子价电子排布会变成 ,半满结构更稳定;
(2)①上述过程中, 既参与反应,又重新生成,则催化剂为 ;
②如图所示,反应物为C H 和NO,生成物为N 和C HOH,该过程总反应为 ;
6 6 2 2 6 5
(3)① ,② ,根据盖斯定律, ´②-①可得 , ;
(4)A.加入 ,碘单质 中溶解度大,由水层进入有机层,则水层碘单质浓度降低,反应i平衡正
向进行,在平衡时 减小,A错误;
B.加入 固体, 增大,反应ii平衡正向移动,平衡时 的值增大,B正确;
C.升高温度,反应 速率增大,反应 速率增大,C错误;
D.加水稀释,离子总浓度减小,平衡向着离子总浓度增大的方向移动,故溶液中离子总数增大,D正
确;
故选BD;
(5)①图中 的斜率大于 的斜率,故生成 的速率快于生成 的速率,故反应i的活化能大于反
应ii的活化能;
② 内,上述体系中 的平均反应速率 ;
(6)从图中可知, ,当 ,平衡时
, ,设平衡时,反应i和反应ii中 的变化量为 ,
,列三段式,反应i:
反应ii:
可列式, , , ,
,解得x=0.005,y=0.002,则 , ,
,反应ii的平衡常数 。
6.(2025·福建·一模)工业上以合成气CO和 ,少量 和稀有气体)为原料制二甲醚(DME),主
要发生下列反应:
ⅰ:ⅱ:
ⅲ:
ⅳ:……
(1)在标准状态下,由最稳定的单质生成1mol纯物质的焓变称为该物质的标准摩尔生成焓 。几种物
质的标准摩尔生成焓如下表:
物质
由表中数据推测, 。
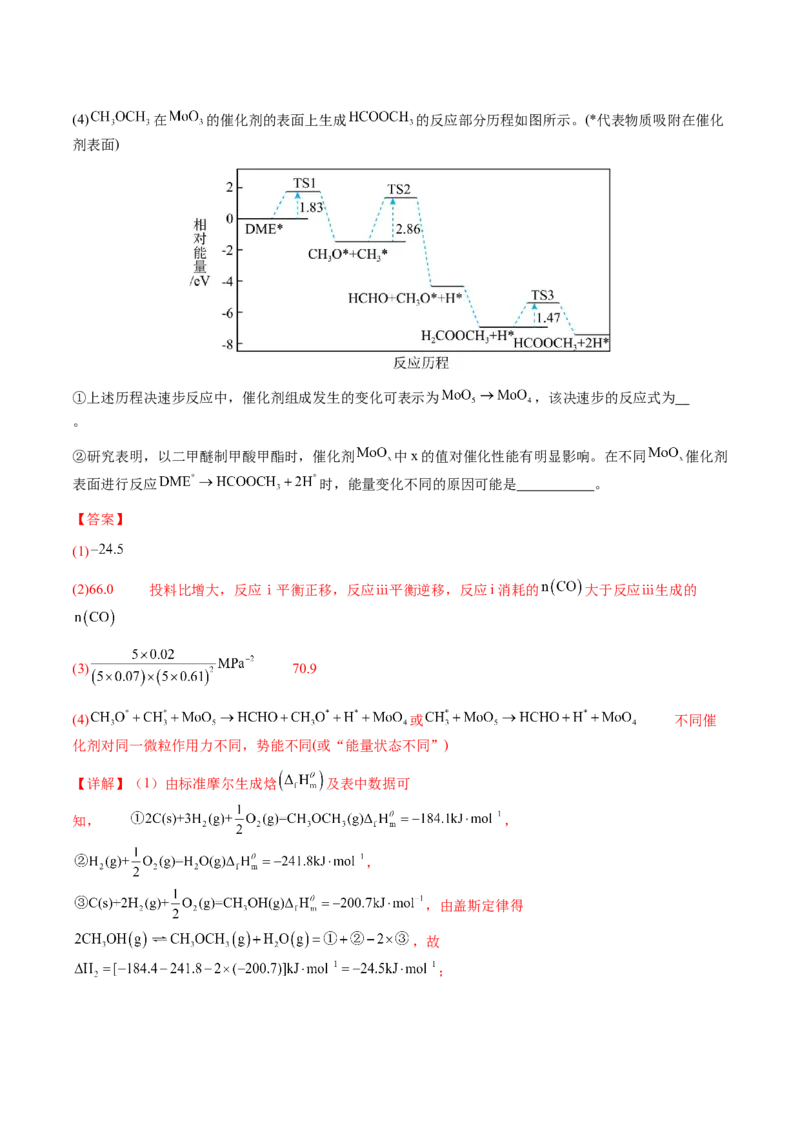
(2)500K、5MPa时,只发生反应i~iii,初始投料比 与平衡时(X)转化率 、二甲醚产率
和二甲醚选择性 的关系如图:
当 时,DME的选择性为 %(保留一位小数);当 时,CO的平衡转化率随
投料比增大而增大的原因是 。
(3)573K、5MPa时,反应前后气体组成如下表(与反应无关的气体未列出):
CO
原料气组成/mol a 29.2 0 0 0 2.2
平衡气体组成/% 61 7.0 2.0 12.7 3.2 12.7
则反应i用气体分压表示平衡常数 (列出计算式), 。(4) 在 的催化剂的表面上生成 的反应部分历程如图所示。(*代表物质吸附在催化
剂表面)
①上述历程决速步反应中,催化剂组成发生的变化可表示为 ,该决速步的反应式为
。
②研究表明,以二甲醚制甲酸甲酯时,催化剂 中x的值对催化性能有明显影响。在不同 催化剂
表面进行反应 时,能量变化不同的原因可能是 。
【答案】
(1)
(2)66.0 投料比增大,反应ⅰ平衡正移,反应ⅲ平衡逆移,反应i消耗的 大于反应ⅲ生成的
(3) 70.9
(4) 或 不同催
化剂对同一微粒作用力不同,势能不同(或“能量状态不同”)
【详解】(1)由标准摩尔生成焓 及表中数据可
知, ,
,
,由盖斯定律得
,故
;(2)由图知,当 时, , ,设 ,则消耗的
, ,DME的选择性为
;当 时,投料比增大,反应ⅰ平衡正移,反应ⅲ平衡逆移,
反应i消耗的 大于反应ⅲ生成的 ,故CO的平衡转化率随投料比增大而增大;
(3)在573K、5MPa时, , ,
,则则反应i用气体分压表示平衡常数
;设平衡时气体的总物质的量为xmol;则 、
、 、 、 、
,则由C守恒得 ,解 ,
由H守恒得 ,解 ;
(4)①正反应活化能越大,反应速率越慢,为总反应得决速步,由图知,该反应得决速步为
,催化剂组成发生的变化可表示为 ,故决速步的反应
式为 或 ;
②由于不同催化剂对同一微粒作用力不同,势能不同(或“能量状态不同”),在不同 催化剂表面进行
反应 时,能量变化不同。
7.(2025·广西·一模)为实现“碳中和”和“碳达峰”,碳的循环利用是重要措施。
Ⅰ.甲烷干重整反应(DRM)可以将两种温室气体( 和 )直接转化为合成气(主要成分为CO和 ),
反应方程式为 。
(1)几种物质的燃烧热如下表:
物质
燃烧热( ) 893 283 285.8
请计算甲烷干重整反应 的 。
(2)合成气可以用于生成液体燃料甲醇, ,该反应在
条件下能自发进行(填“高温”“低温”或“任何温度”)。将CO和 按照等物质的量进行反应,测得
CO在不同温度下的平衡转化率与压强的关系如图所示,a、b、c三点对应化学平衡常数大小关系为
。Ⅱ. 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。
(3)催化循环中产生的中间体微粒共 种。
(4) 催化加氢制甲醇总反应的化学方程式为 。
Ⅲ.利用甲醇一定条件下直接脱氢可制化工原料甲醛,涉及的反应如下:
反应①:
反应②:
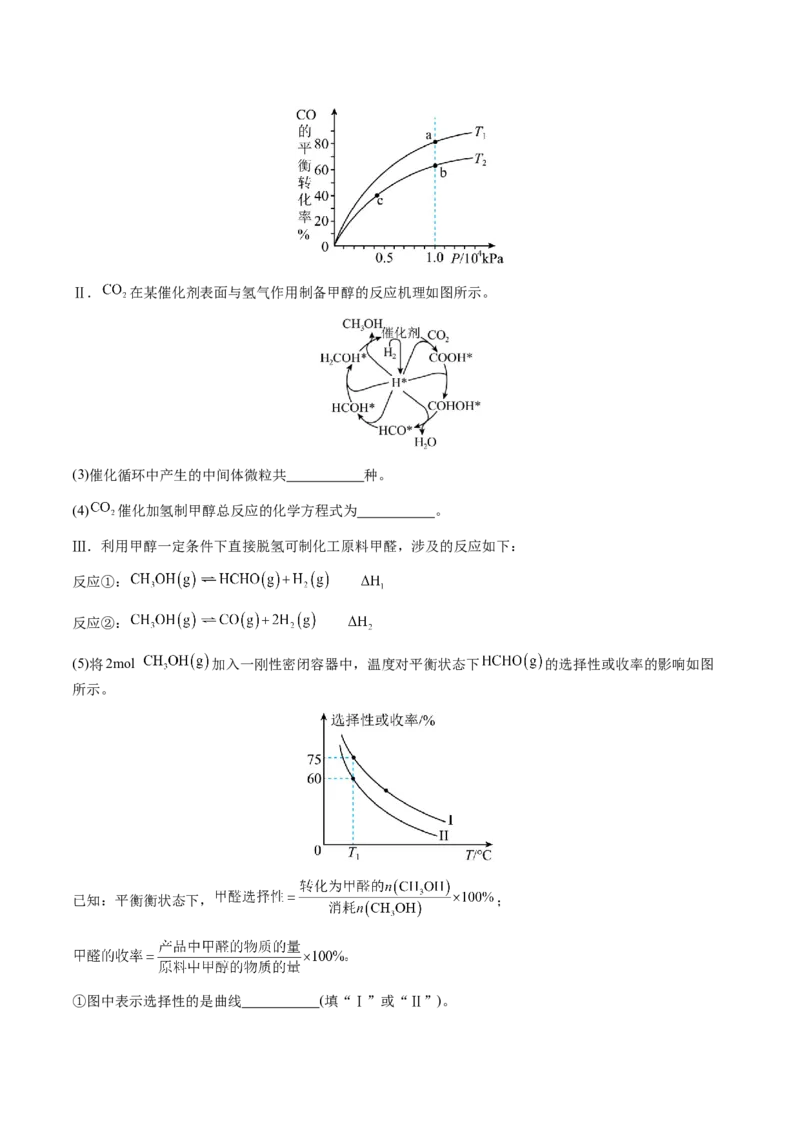
(5)将2mol 加入一刚性密闭容器中,温度对平衡状态下 的选择性或收率的影响如图
所示。
已知:平衡衡状态下, ;
①图中表示选择性的是曲线 (填“Ⅰ”或“Ⅱ”)。② ℃时 的平衡转化率为 ,反应Ⅱ的平衡常数 (
,x为物质的量分数)。
【答案】
(1)+244.6
(2)低温 K> K= K
a b c
(3)6
(4)
(5)Ⅰ 80% 0.25
【详解】(1)CH 、CO 和H,的燃烧热分别为-893kJ/mol、-283kJ/mol和-285.8kJ/mol,根据盖斯定律:
4 2
可计算应 的 =[-893-(2×-283)-(2×-285.8)]kJ/mol=+244.6kJ/mol;
(2)该反应 均小于0,根据 反应自发,可知该反应低温下自发进行;升温平衡逆向
移动,CO的平衡转化率下降,由图可知,a点温度小于b点,则a点平衡常数大于b点,平衡常数是温度
函数,温度不变,平衡常数不变,由图可知,b点温度与c点相同,则b点平衡常数等于c点,所以a、b、
c三点平衡常数的大小关系为K> K= K;
a b c
(3)由流程可知,催化循环中产生了H*和5种含碳离子等共6种中间粒子;
(4)由图可知反应物为CO 和H,最终产物为CHOH和HO,总反应方程式为:
2 2 3 2
;
(5)①甲醇分解反应为可逆反应,可逆反应不可能完全反应,则原料中甲醇的物质的量大于消耗甲醇的
物质的量,由方程式可知,转化为甲醛的甲醇的物质的量与产品中甲醛的物质的量相等,则相同温度时,
甲醛的选择性大于甲醛的收率,所以表示选择性的是曲线I;
②由图可知,T℃平衡时,甲醛的收率为60%、选择性为75%,则平衡体系中甲醛的物质的量
1
2mol×60%=1.2mol,消耗的甲醇的物质的量为1.2mol÷75%=1.6mol,由题意可得:
由上述数据可知,甲醇的转化率为 80% ;
平衡时,CHOH 的物质的量为0.4mol,HCHO的物质的量为1.2mol,CO的物质的量为0.4mol,H的物质
3
的量为2mol,混合气体的总物质的量为4 mol,CO的物质的量分数为0.1,H 的物质的量分数为 0.5,
2CHOH的物质的量分数为0.1,反应Ⅱ的平衡常数K= 。
3
8.(2025·云南昆明·一模)甲烷化学链干重整联合制氢是基于化学链概念开发的新型能源转化技术。甲烷
干法重整为 。回答下列问题:
(1)为提高 的平衡转化率,可以采取的措施是 (填标号)。
a.高温低压 b.低温高压 c.高温高压 d.低温低压
(2)在恒容绝热容器中发生上述反应,下列能够说明反应已达到平衡状态的是 (填标号)。
a.气体的密度不再发生变化
b.温度不再发生变化
c.断裂 键的同时断裂 键
d.
(3)在恒温恒容的容器中,按 投料,初始总压 ,达到平衡时总压强为
,则 的转化率为 , (用含 的式子表示)。
(4)反应过程中,下列三个反应均会使体系中产生积碳,影响催化剂的催化效果。
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
①较高温下,导致积碳的主要原因是发生反应 (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②压强为 , , 或 投料时,发生甲烷干法重整反
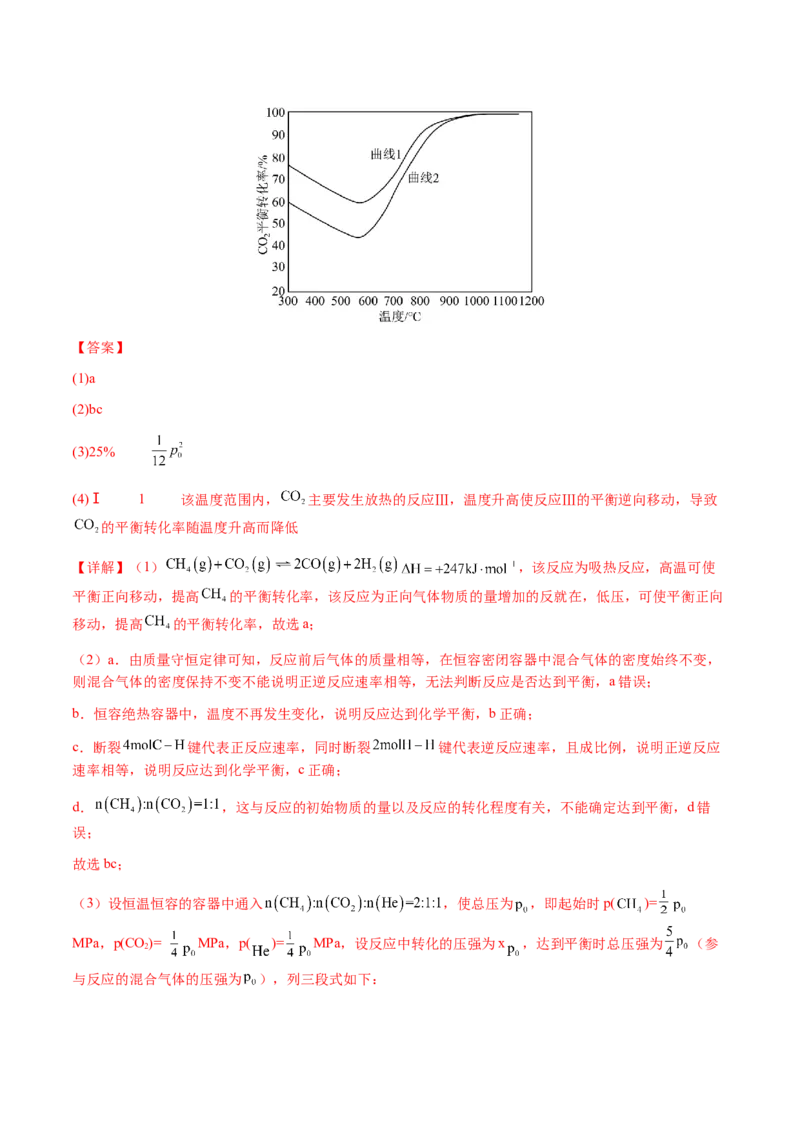
应、积碳反应, 的平衡转化率随温度升高而增大, 的平衡转化率随温度的变化如图所示。图中代
表 的是曲线 (填“1”或“2”); 时, 平衡转化率随温度
升高而降低的原因可能是 。【答案】
(1)a
(2)bc
(3)25%
(4)Ⅰ 1 该温度范围内, 主要发生放热的反应Ⅲ,温度升高使反应Ⅲ的平衡逆向移动,导致
的平衡转化率随温度升高而降低
【详解】(1) ,该反应为吸热反应,高温可使
平衡正向移动,提高 的平衡转化率,该反应为正向气体物质的量增加的反就在,低压,可使平衡正向
移动,提高 的平衡转化率,故选a;
(2)a.由质量守恒定律可知,反应前后气体的质量相等,在恒容密闭容器中混合气体的密度始终不变,
则混合气体的密度保持不变不能说明正逆反应速率相等,无法判断反应是否达到平衡,a错误;
b.恒容绝热容器中,温度不再发生变化,说明反应达到化学平衡,b正确;
c.断裂 键代表正反应速率,同时断裂 键代表逆反应速率,且成比例,说明正逆反应
速率相等,说明反应达到化学平衡,c正确;
d. ,这与反应的初始物质的量以及反应的转化程度有关,不能确定达到平衡,d错
误;
故选bc;
(3)设恒温恒容的容器中通入 ,使总压为 ,即起始时p( )=
MPa,p(CO)= MPa,p( )= MPa,设反应中转化的压强为x ,达到平衡时总压强为 (参
2
与反应的混合气体的压强为 ),列三段式如下:,解得 ,
的转化率为: , ;
(4)①较高温下,反应Ⅰ平衡正向移动,导致积碳;
② 与 比,相当于 降低,反应Ⅲ平衡逆向进行, 转化
率降低,故代表 的是曲线1;该温度范围内, 主要发生放热的反应Ⅲ,温度升高
使反应Ⅲ的平衡逆向移动,导致 的平衡转化率随温度升高而降低。
9.(2025·河南郑州·模拟预测)工业上以煤炭、二氧化碳等为原料,经过系列反应可以得到不同需求的原
料气。回答下列问题:
I.在C和 的反应体系中:
反应1:
反应2:
反应3:
(1) 。
(2)①设 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
(填字母)。
②已知y<0更有利于反应发生,根据①中的图判断一定压强下随着温度的升高,气体中 与 的物质
的量之比 (填字母)。
A.不变 B.增大 C.减小
Ⅱ.二氧化碳加氢制乙烯反应i(主反应): ;
反应ⅱ(副反应):
向密闭容器中通入 和 发生反应,在不同压强下, 的平衡转化率随温度的变化如图所
示。
(3) 由小到大的顺序为 。
(4) 压强下,650℃后 的平衡转化率随温度升高而增大的原因是 。
(5)A点,乙烯的选择性 ,则 的转化率为 (保留两位有效数字,下
同)。该温度下,反应ⅱ的平衡常数 (用平衡分压代替平衡浓度,分压=总压×物质的量分
数)。
【答案】
(1)-222kJ/mol
(2)a B
(3)
(4)反应ⅰ为放热反应、反应ⅱ为吸热反应,650℃以后,升高温度对反应ⅱ平衡正向移动的影响大于对反
应ⅰ平衡逆向移动的影响,使得 的平衡转化率随着温度的升高而增大
(5)63% 0.39
【详解】(1)由已知方程式:(2×反应1-反应2)可得反应3,结合盖斯定律得:
;
(2)①反应1前后气体分子数不变,升温y不变,对应线条b,反应2气体分子数减少,熵减,升高温度
y值增大,对应线条c,反应3气体分子数增加,熵增,温度升高y值减小,对应线条a;②反应3-反应1可得到:C(s)+CO(g)=2CO(g),△H=+172kJ/mol,温度升高,反应正向进行,反应2逆向
2
进行,气体中CO和CO 的物质的量之比增大,选B;
2
(3)200~650℃时,以反应I为主,△H<0,温度升高,反应I平衡逆向移动,CO 的转化率减小,650℃
2
以后,I为放热反应、Ⅱ为吸热反应,升高温度对反应Ⅱ平衡正向移动的影响大于对反应I平衡逆向移动的
影响,使得CO 的平衡转化率随着温度的升高而增大,故在200~650℃时,增大压强,CO 的转化率增
2 2
大,则 。
(4)反应ⅰ为放热反应、反应ⅱ为吸热反应,650℃以后,升高温度对反应ⅱ平衡正向移动的影响大于对
反应ⅰ平衡逆向移动的影响,使得 的平衡转化率随着温度的升高而增大;
(5)A点,转化的二氧化碳的物质的量为2mol×70%=1.4mol,发生反应i的氢气的物质的量:
,发生反应ⅱ的氢气的物质的量: ,则 的转化率为
63%;
设平衡时压强为p,根据已知列三段式 ,
, 0.39。
10.(2024·福建福州·二模)3-羟基丙酸乙酯( )高效合成丙烯腈( )的原理如
下:
反应i: (g) (g)+HO(g) >0
2
反应ⅱ: (g)+NH (g) CH=CHCN(g)+H O(g)+C HOH(g) >0
3 2 2 2 5
(1)反应i正反应活化能 (选填“大于”或“小于”)反应ii;上述两个反应一定条件下均可以自
发进行的原因是 。
(2)绝热恒容条件下,下列选项可表明反应体系一定达到平衡状态的是___________。(填序号)
A.容器内混合气体质量不再变化
B.每断裂3mol N-H键,同时生成1mol HO
2C.容器内混合气体的平均相对分子质量不再变化
D.容器内温度不再变化
(3)下列选项中可以提高丙烯腈平衡产率的措施有___________(填序号)。
A.高温低压 B.低温高压 C.增加 的用量 D.延长反应时间
(4)在装有 催化剂、压强为101kPa的恒压密闭容器中,按物质的量之比为1:8:1通入3-羟基丙酸乙
酯、 ,测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度的变化如图所示。[如
的 ]
①图中温度升高,丙烯酸乙酯( )的物质的量分数先增大后降低,请解释原因: 。
② 反应ⅱ的平衡常数 (以平衡时各物质的物质的量分数代替平衡浓度计算)。
【答案】
(1)大于 两个反应均为熵增反应
(2)CD
(3)A
(4)低温时,主要发生反应①,生成丙烯酸乙酯。随着温度升高,反应②占主导,开始消耗丙烯酸乙酯
【详解】(1)反应i为吸热反应,则正反应的活化能大于逆反应的活化能;两个反应为吸热反应,熵增反
应,即△H>0,△S>0,当△G=△H-T△S<0,反应高温条件下可自发进行;(2)A.反应过程中气体质量始终不变,容器内混合气体质量不再变化,不能表明达到平衡状态,A不符
合题意;
B.每断裂3mol N-H键,同时生成1mol HO都是指正反应方向,不能表明达到平衡状态,B不符合题
2
意;
C.反应为气体物质的量增加的反应,反应过程中气体质量始终不变,容器内混合气体的平均相对分子质
量为变量,混合气体的平均相对分子质量不再变化,表明达到平衡状态,C符合题意;
D.反应为吸热反应,绝热容器内温度不再变化,能表明达到平衡状态,D符合题意;
故选CD;
(3)A.两个反应都是吸热反应,也都是气体分子数增多的反应,升高温度、减压平衡正向移动,能提高
丙烯腈平衡产率,A选;
B.低温高压使平衡逆向移动,降低丙烯腈平衡产率,B不选;
C. 为催化剂,增加 的用量,不影响平衡移动,不能提高丙烯腈平衡产率,C不选;
D.延长反应时间,不影响平衡移动,D不选;
故选A;
(4)①反应ⅰ、ⅱ均为吸热反应,低温时,主要发生反应①,最高点前反应i进行程度大,生成丙烯酸乙
酯,随着温度升高,反应②占主导,反应ⅱ进行程度大,开始消耗丙烯酸乙酯所以随着温度的升高,丙烯
酸乙酯平衡的物质的量分数先增大后减小。
② , 与 的物质的量分数相等,假设3-羟基丙酸乙酯投料为1mol, 投料为
8mol, 投料为1mol;平衡时,3-羟基丙酸乙酯为0, 与 的物质的量,根据三段式
可知,平衡时 与 物质的量均为0.5mol,相当于先生成1mol ,随后又消耗
0.5mol,由此可知,水蒸气的物质的量为1.5mol,乙醇的物质的量为0.5mol, 剩余为7.5mol,总物质
的量分数为0.5+0.5+1.5+7.5+1+0.5=11.5mol,反应ⅱ的平衡常数 ;
11.(2024·浙江绍兴·一模)苯甲醛是香料、医药、农化等行业的重要中间体,被广泛地应用于食品、化
妆品、塑料工业等行业中。以下是制备苯甲醛的两种方法:
Ⅰ.甲苯氧化法:
Ⅱ.苯甲醇氧化法:
请回答:
(1)方法Ⅰ中的反应能自发进行的条件是 。(2)方法Ⅰ中,得到苯甲醛有两种途径(图1),途径一是甲苯先氧化得到苯甲醇,再深度氧化得到苯甲醛,
途径二为甲苯直接氧化得到苯甲醛。已知:在反应起始阶段,可认为甲苯与 发生平行反应,分别生成苯
甲醇(浓度为 )和苯甲醛(浓度为 ),两产物的浓度之比与时间无关: 时, 时,
。
①请计算,反应 的焓变
②反应过程中,甲苯和各产物含量变化如图2所示,下列说法正确的是 。
A.分析可知,
B.增加氧化剂 的浓度,可以提高甲苯的转化率和苯甲醛的选择性
C.在一定的反应时间内,选择合适的催化剂,可以提高生成苯甲醇的比例
D.降低反应温度,会使得途径二对苯甲醛生成的贡献更大
③甲苯氧化制备苯甲醛过程中,还产生了另一种有机产物苯甲酸,请在图2中画出c(苯甲酸)随时间变化的
曲线图(以左侧坐标轴为纵坐标) 。
(3)方法Ⅱ中,采用 为固体催化剂,反应的历程包含反应物分子在催化剂表面的吸附、反应等过程。
在一定时间内,随着n(苯甲醇)/n(催化剂)比值的增大,苯甲醇的转化率先增大后减小,试解释原因
。
(4)利用纳米 电极电解 和 的混合溶液(如图3),电解一段时间后,将电解液与甲苯混
合可制得苯甲醛,已知适当增大 和 浓度可以抑制 的歧化倾向,电解过程中,阳极表面有少量
气泡产生,且溶液中有极少量黑色固体物质生成。请写出:①产生气泡对应的电极反应方程式: 。
②溶液中生成黑色固体的离子方程式: 。
【答案】
(1)低温
(2)-303.5 ACD
(3)n(苯甲醇)/n(催化剂)比值较小时,催化剂的量相对于苯甲醇较多,随着比值的增大,更多的苯甲醇与催
化剂接触,从而提高了苯甲醇的转化率;比值较大时,催化剂提供的活性位点较少,不能满足反应所需的
活性位点数量,因此转化率下降
(4)
【详解】(1)方法Ⅰ中的反应 ,依据 反应能自发进行,则反应在低温下自发
进行;
(2)①根据盖斯定律,反应 的焓变
;
②A.由图可知,刚开始反应时,苯甲醛是优势产物,说明生成苯甲醛的反应活化能低,即: ,A
正确;
B.增加氧化剂 的浓度,可以提高反应物甲苯的转化率,但氧气浓度过大,会继续氧化苯甲醛为苯甲
酸,不利于提高苯甲醛的选择性,B错误;
C.在一定的反应时间内,选择对生成苯甲醇更有利的催化剂,可以提高生成苯甲醇的比例,C正确;D.由题干信息可知, 时, 时, ,降低反应温度, 降低,可以理解为
变小或 变大,则对苯甲醛生成的贡献更大,D正确;
故选ACD;
③甲苯氧化制备苯甲醛过程中,还产生了另一种有机产物苯甲酸,由图可知,随着反应进行,甲苯的含量
降低,但是苯甲醇与苯甲醛的含量也降低,说明发生了苯甲醛氧化为苯甲酸的副反应,因此苯甲酸的含量
始终保持增大: ;
(3)随着n(苯甲醇)/n(催化剂)比值的增大,苯甲醇的转化率先增大后减小,增大是因为:n(苯甲醇)/n(催
化剂)比值较小时,催化剂的量相对于苯甲醇较多,随着比值的增大,更多的苯甲醇与催化剂接触,从而提
高了苯甲醇的转化率;减小的原因是:比值较大时,催化剂提供的活性位点较少,不能满足反应所需的活
性位点数量,因此转化率下降;
(4)①由题可知,阳极发生氧化反应: ,阳极还产生少量气泡,说明存在竞争反应,只
能是溶液中的 在阳极放电生成氧气,电极反应为 ;
②溶液中有极少量黑色固体物质生成,由题给信息可知,增大 和 浓度可以抑制 的歧化倾向,
说明 的歧化倾向被抑制所以生成的黑色固体很少,则 发生歧化反应生成+4价的MnO 和+2价的
2
Mn2+,该黑色固体是 ,离子方程式为 。
12.(2024·浙江金华·一模)甲酸( )被认为是潜在的贮氢物质之一。请回答:
(1)加热甲酸可发生两种分解反应,反应过程中的能量变化如图所示。Ⅰ.
Ⅱ.
①根据能量变化图,计算 的 。
②已知 只能催化反应Ⅰ而对于反应Ⅱ无影响。
根据前面的信息判断,下列说法正确的是 (选填序号)。
A.升温,有利于提高产物中 的体积分数
B.加入 ,可使 能达到的极大值更大
C.加入 ,有利于提高 的平衡浓度
D.当 时,反应达到平衡状态
(2)在催化剂作用下, 能与 反应生成 : 。 的电
离、双聚均会影响放氢速率,反应历程如下图所示:
①用 代替 ,通过检验气体产物中的 (填分子式)可确认上述机理。
②实验发现,水适当过量能促进 释放 ,可能原因是 。
(3) (25℃, )溶液中加入两种可溶性钠盐 、 ,发生反应:
( 、B)。平衡时 随起始时 与
物质的量浓度之比 的变化曲线如下图。①弱酸 的电离平衡常数 。
② (选填“<”或“>”)。
【答案】
(1) AB
(2)HD 适当过量的水促进 电离,防止 通过氢键聚合
(3) <
【详解】(1)①由图可知Ⅰ. ;
Ⅱ.
根据盖斯定律,反应Ⅰ-反应Ⅱ得到 ,则
= ;
②A.由图可知,该反应 的 ,升温,平衡逆向移动, 的体积
分数增大,A正确;
B.两个分解反应同时进行,加入 ,只催化反应Ⅰ而对于反应Ⅱ无影响,故单位时间内生成的CO更
多,可以使 能达到的极大值更大,B正确;
C.加入 ,氢氧化钠固体易吸水而潮解,反应Ⅰ和反应Ⅱ是两个竞争反应,氢氧化钠固体吸收水
分后,更有利于反应Ⅰ平衡正向移动,不利于提高 的平衡浓度,C错误;
D. 和水分别是两个反应的生成物,当 时,反应不一定达到平衡状态,D错误;
故选AB;(2)①由反应机理可知, 吸附在催化剂上,与水分子反应时, 上 键断裂,形成一个
, 与水分子通过配位键结合,随后水分子的1个 键断裂,形成一个 和 , 形
成氢气分子,故如果用 代替 ,形成的氢气分子是 ;
②水适当过量相当稀释 , 电离程度增大, 数量变多,可防止 通过氢键聚
合;
(3)①取图像上 , 的点, ,解得
, ,则 ,解得
,则 ;
② 当 , 平 衡 时 加 入 NaA 溶 液 的 , 平 衡 时 加 入 NaB 溶 液 的
,说明反应后,滴加 NaA溶液的酸性强,则说明 结合 能力强,HA的酸性强于
HB,故 。