文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2023 年高考化学第三次模拟考试卷
高三化学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
H1 C12 N14 O18 Na23 S32 Cl35.5
一、选择题:本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,仅有一个选项正确。
1.生活中处处有化学,下列叙述正确的是
A.HB铅笔芯的成分为二氧化铅 B.碳酸氢钠可做食品膨松剂
C.青铜和黄铜是不同结构的单质铜 D.焰火中红色来源于钠盐灼烧
2.下列有关电解质、强电解质、弱电解质的分类正确的是
选项 A B C D
电解质 Cu CO NaCl NaOH
2
强电解
HCl Ba(OH) HClO BaSO
质 2 4 4
弱电解
CHCOOH HO Cu(OH) 氨水
质 3 2 2
3.下列关于物质结构的命题表述中正确的是
A.元素Ge位于周期表第四周期IVA族,核外电子排布式为[Ar]4s24p2, 属于p区
B.乙醛分子中碳原子的杂化类型有sp2和sp3两种
C.氨水中大部分NH 与HO以氢键(用“…”表示)结合成NH ·H O分子,根据氨水的性质可知NH ·H O
3 2 3 2 3 2
的结构式可记为:
D.非极性分子往往具有高度对称性,如BF、PCl 、HO、CO 这样的分子
3 5 2 2 2
第 1 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
4.下列试剂实验室保存方法错误的是
A.浓硝酸保存在棕色细口瓶中 B.氢氧化钠固体保存在广口塑料瓶中
C.四氯化碳保存在广口塑料瓶中 D.高锰酸钾固体保存在棕色广口瓶中
5.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是
A.Cu与浓硫酸反应,只体现H SO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无H O生成
2
6.下列关于阿伏伽德罗定律说法中,正确的是
A.含有相同分子数的两种气体,占有相同的体积
B.同温同压下,相同质量的两种任何气体,含有相同的分子数
C.相同物质的量两种气体,占有相同的体积
D.同温同压下,2升O 与2升CO 含有相同的分子数
2 2
7.由键能数据大小,不能解释下列事实的是
化学键 C−H Si−H C=O C−O Si−O C−C Si-Si
键能/
411 318 799 358 452 346 222
kJ⋅mol−1
A.稳定性:CH >SiH B.键长:C=O晶体硅
2 2
8.某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合
要求的是
第 2 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
气体 液体 固体粉末
饱和Na CO 溶
A CO 2 3 CaCO
2 液 3
B Cl FeCl 溶液 Fe
2 2
C HCl Cu(NO ) 溶液 Cu
3 2
D NH H O AgCl
3 2
9.除去NaCl溶液中混有的少量NaSO ,选用的试剂(稍过量)及加入顺序正确的是( )
2 4
A.BaCl 、KCO、HCl B.Ba(NO )、KCO、HCl
2 2 3 3 2 2 3
C.BaCl 、NaCO、HCl D.Ba(NO )、NaCO、HCl
2 2 3 3 2 2 3
10.下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
HCO- 3 2
3
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 NO- NO- 2
3 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2 SO2-
3
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 Ag(NH ) + 2
3 2
11.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电
子数是X核外电子数的一半。下列叙述正确的是
A.WZ的水溶液呈碱性
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物是中强酸
第 3 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.该新化合物中Y不满足8电子稳定结构
12.同位素示踪是研究反应机理的重要手段之一、已知醛与HO在酸催化下存在如下平衡:
2
H+ 。据此推测,对羟基苯甲醛与10倍量的D18O在少量酸催化下反应,达到平衡后,
RCHO+H O
⇌
RCH(OH) 2
2 2
下列化合物中含量最高的是
A. B.
C. D.
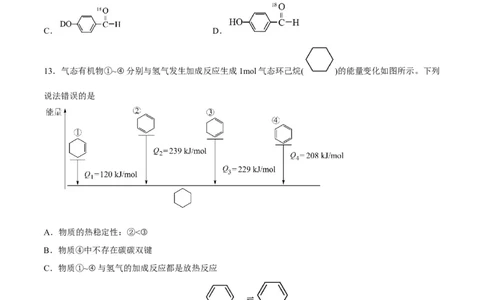
13.气态有机物①~④分别与氢气发生加成反应生成1mol气态环己烷( )的能量变化如图所示。下列
说法错误的是
A.物质的热稳定性:②<③
B.物质④中不存在碳碳双键
C.物质①~④与氢气的加成反应都是放热反应
⇌
D.物质③脱氢生成④的热化学方程式为: (g) (g)+H(g)-21kJ
2
14.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.12g NaHSO 中含有0.2N 个阳离子
4 A
B.11.2L乙烷和丙烯的混合气体中所含碳氢键数为3N
A
C.8g CH 含有中子数为3N
4 A
D.0.1mol H 和0.1mol I 于密闭容器中充分反应后,HI分子总数为0.2N
2 2 A
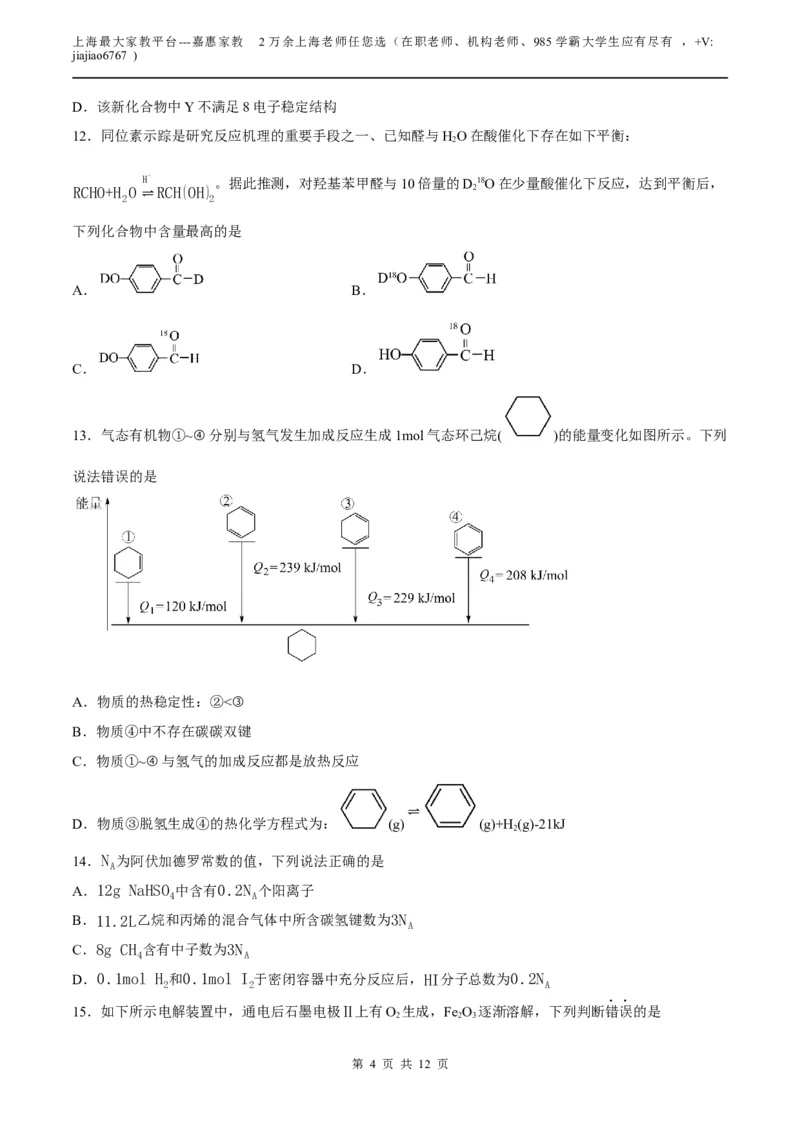
15.如下所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列判断错误的是
2 2 3
第 4 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
D.当0.01mol Fe O 完全溶解时,至少产生气体336mL (折合成标准状况下)
2 3
16.测定浓硫酸试剂中H SO 含量的主要操作包括:
2 4
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取20.00mL待测液,用0.1000mol/L的NaOH溶液滴定。
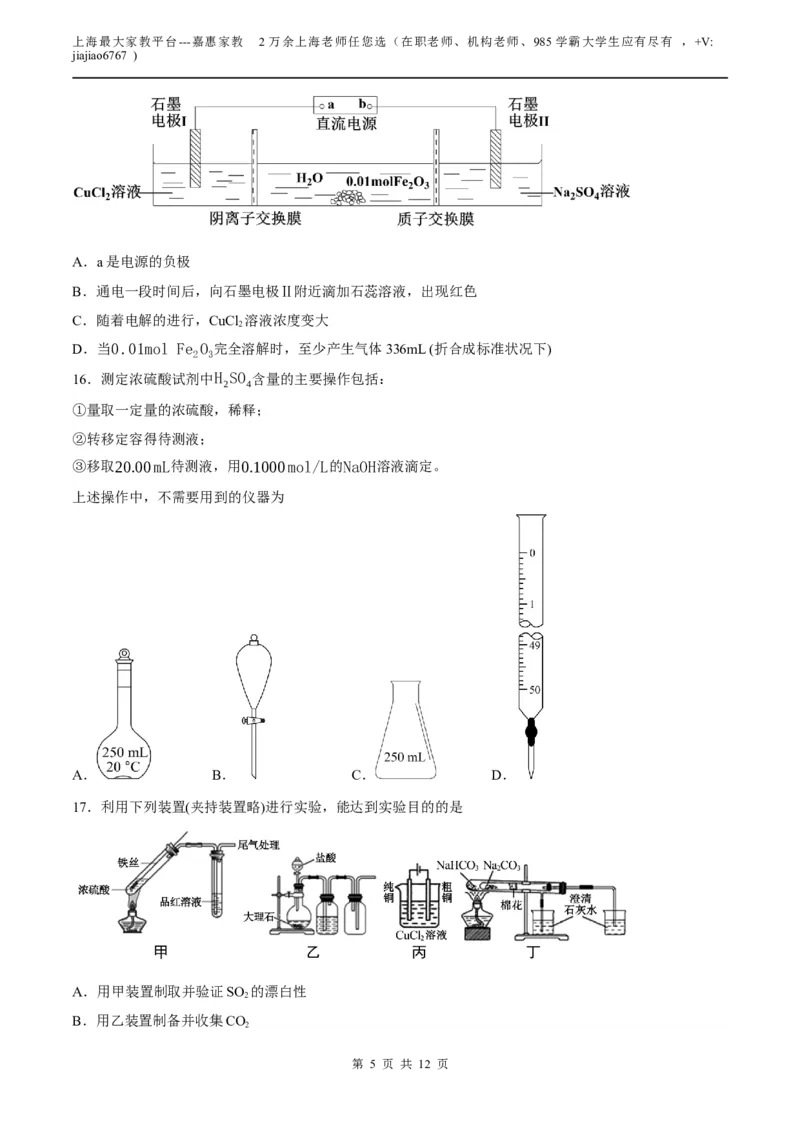
上述操作中,不需要用到的仪器为
A. B. C. D.
17.利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A.用甲装置制取并验证SO 的漂白性
2
B.用乙装置制备并收集CO
2
第 5 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.用丙装置精炼粗铜
D.用丁装置比较NaCO、NaHCO 的稳定性
2 3 3
❑
18.在恒温恒容条件下,向某容器中充入一定量的NO 气体发生下列反应:2NO(g) 4NO (g)
2 5 2 5 ⇌ 2
❑
+O (g) ΔH>0。温度T时,部分实验数据如表所示:
2
t/s 0 50 100 150
c(NO)/mol·L-1 4.00 2.5 2.00 2.00
2 5
下列有关说法错误的是
A.温度T时,该反应平衡常数K=64
B.150s后再充入一定量NO,再次达到平衡NO 的转化率将增大
2 5 2 5
C.达平衡后升高温度,该容器内混合气体的密度不会改变
D.其他条件不变,若将恒容改为恒压,则平衡时NO 的转化率增大
2 5
19.T℃时,在一个2 L的密闭容器中,加入4mol M(g)和2mol N(g)进行如下反应:
❑
3M(g)+2N(g)⇌4P(s)+2Q(g) ΔH<0,反应一段时间后达到平衡,测得生成1.6mol P(s) 。下列说法正
❑
确的是
A.该反应的化学平衡常数表达式为c4 (P)⋅c2 (Q)
c3 (M)⋅c2 (N)
B.N的平衡转化率为40%
C.升高温度,v 减小,v 增大
正 逆
D.增加N的量,平衡向右移动,N的平衡转化率增大
20.常温下,分别向25mL0.3mol/LNa CO 溶液和25mL0.3mol/LNaHCO 溶液中逐滴滴加0.3mol/L稀盐酸,
2 3 3
用压强传感器测得压强随盐酸体积的变化曲线如图所示,下列说法正确的是
A.Y曲线为NaHCO 溶液的滴定曲线
3
B.b、c两点溶液中水的电离程度:b>c
第 6 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.a点溶液中:c(Na+)+c(H+)>c(OH-)+c(HCO )+2c(CO )
− 2−
❑ ❑
3 3
D.c→d段离子方程式为:CO +2H+=CO ↑+H O
❑ 2− 2 2
3
第II卷(非选择题)
21.铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为 。由此可知,铁是第_______周期元素,铁原子核外3d轨道上共填充
了_______个电子。
(2)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是_______(选填编号)。
a.Fe b.FeO c.Fe O d.Fe O
2 3 3 4
(3)FeSO 可以用来净水、治疗缺铁性贫血等,实验室在配制FeSO 溶液时,为了防止FeSO 变质,经常向
4 4 4
溶液中加入铁粉,其原因是_______(用离子方程式表示)。
(4)向新配制的FeSO 溶液中,加入一定量的稀硝酸,发生如下反应:
4
_______Fe2++_______H++_______NO =_______Fe3++_______NO↑+_______HO
− 2
❑
3
①配平上述反应_______。
②每生成0.5molNO气体,转移的电子数为_______。
③要检验该反应后的溶液中是否还含有Fe2+,实验方案是_______。
现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:
(5)写出反应Ⅲ的平衡常数表达式_______。
(6)写出铁氧化物循环裂解水制氢的总反应的化学方程式:_______。
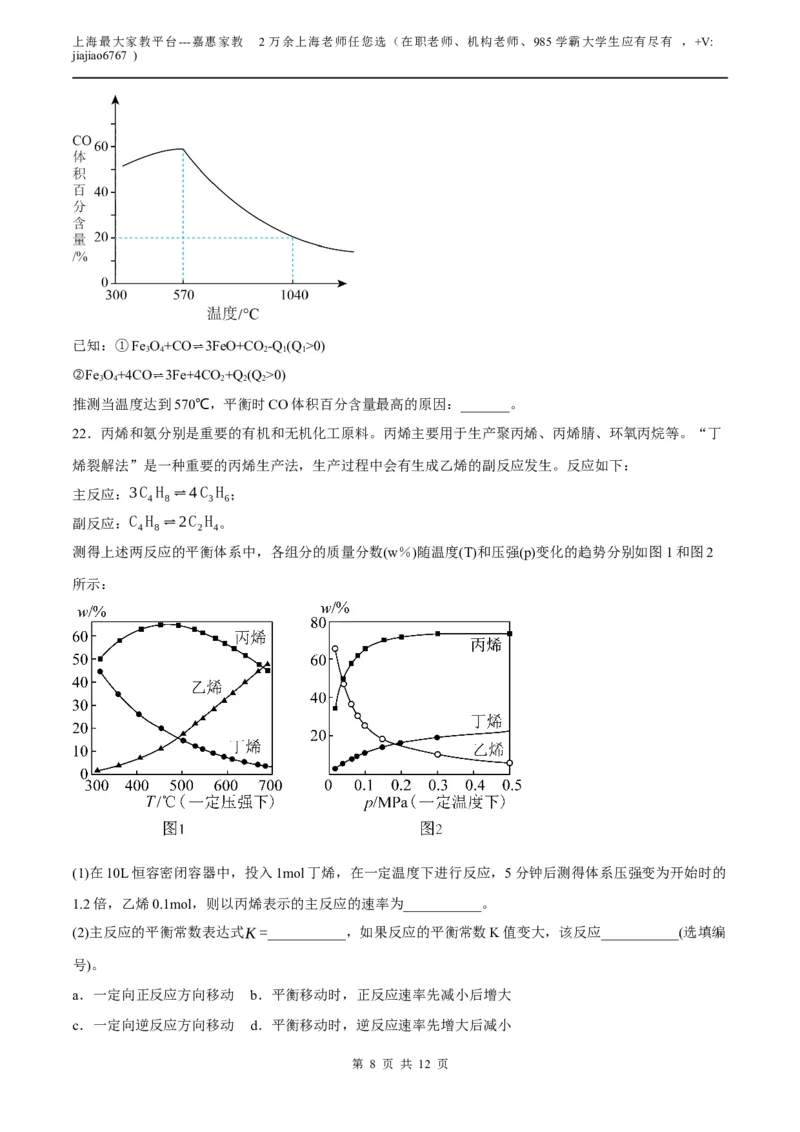
(7)Fe O 和CO的反应过程与温度密切相关。向某容器中加入Fe O 与CO,当其它条件一定时,达到平衡
3 4 3 4
时CO的体积百分含量随温度的变化关系如图所示。
第 7 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知:①Fe
3
O
4
+CO⇌3FeO+CO
2
-Q
1
(Q
1
>0)
②Fe
3
O
4
+4CO⇌3Fe+4CO
2
+Q
2
(Q
2
>0)
推测当温度达到570℃,平衡时CO体积百分含量最高的原因:_______。
22.丙烯和氨分别是重要的有机和无机化工原料。丙烯主要用于生产聚丙烯、丙烯腈、环氧丙烷等。“丁
烯裂解法”是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:
主反应:3C H ⇌4C H ;
4 8 3 6
副反应:C H ⇌2C H 。
4 8 2 4
测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2
所示:
(1)在10L恒容密闭容器中,投入1mol丁烯,在一定温度下进行反应,5分钟后测得体系压强变为开始时的
1.2倍,乙烯0.1mol,则以丙烯表示的主反应的速率为___________。
(2)主反应的平衡常数表达式K=___________,如果反应的平衡常数K值变大,该反应___________(选填编
号)。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
第 8 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(3)平衡体系中的丙烯和乙烯的质量比 [m(C 3 H 6 ) ] 是工业生产丙烯时选择反应条件的重要指标之一,从产物
m(C H )
2 4
的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是
___________(填字母)。
A.300℃ 0.1MPa B.700℃ 0.1MPa
C.300℃ 0.5MPa D.700℃ 0.5MPa
(4)有研究者结合图1数据并综合考虑各种因素,认为450℃的反应温度比300℃或700℃更合适,从反应原
理角度分析其理由可能是___________。
(5)图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是___________。
23.贝沙罗汀(分子式C H O)主要用于治疗顽固性早期皮肤T细胞淋巴瘤,其一种合成路线如下:
24 28 2
完成下列填空:
(1)①的反应类型是_______;③所需的无机试剂是_______;④中官能团的转化为:_______→_______(填
官能团名称)。
(2)②的反应式为_______。
(3)已知:1molC与1molD反应生成1molE,同时生成1molHCl。D的结构简式为_______。
(4)写出满足下列条件的A的一种同分异构体的结构简式_______。
i.属于芳香族化合物,能发生银镜反应
ⅱ.只含有2种化学环境不同的氢原子
(5)参考E→F的反应信息,写出以 为原料合成 的路线_______。(无机试剂与溶
反应试剂 反应试剂
剂任选,合成路线常用的表示方式为:A → ……B → 目标产物)
反应条件 反应条件
第 9 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
24.某同学查阅资料得知,无水三氯化铝能催化乙醇制备乙烯,为探究适宜的反应温度,设计如下反应装
置:
检验装置气密性后,在圆底烧瓶中加入5g无水三氯化铝,加热至100℃,通过A加入10mL无水乙醇,观
察并记录C中溶液褪色的时间。重复上述实验,分别观察并记录在110℃、120℃、130℃、140℃时C中溶
液褪色的时间,实验结果如图所示。
完成下列填空:
(1)仪器B的名称是_______;该实验所采用的加热方式优点是_______,液体X可能是_______(选填编号)。
a.水 b.酒精 c.油 d.乙酸
(2)根据实验结果,判断适宜的反应温度为_______。
(3)在140℃进行实验,长时间反应未观察到C中溶液褪色,可能的原因是_______。
(4)在120℃进行实验,若将B改为装有浓硫酸的洗气瓶,长时间反应未观察到C中溶液褪色,可能的原因
是_______。
(5)教材中用乙醇和浓硫酸在170℃时制备乙烯。和教材实验相比,用三氯化铝做催化剂制备乙烯的优点有
_______、_______(列举两点)。
第 10 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
工业无水氯化铝含量测定的主要原理是:Ag++Cl-=AgCl↓。将1.400g工业无水氯化铝样品溶解后配成
500mL溶液,量取25.00mL置于锥形瓶中,用浓度为0.1000mol·L-1的AgNO 标准溶液进行滴定,达到终点
3
时消耗标准液15.30mL。
(6)该样品中AlCl 的质量分数为_______(保留3位有效数字)。
3
(7)某次测定结果误差为-2.1%,可能会造成此结果的原因是_______(选填编号)。
a.称量样品时少量吸水潮解 b.配制AlCl 溶液时未洗涤烧杯
3
c.滴定管水洗后未用AgNO 标准溶液润洗 d.样品中含有少量Al(NO ) 杂质
3 3 3
第 11 页 共 12 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 12 页 共 12 页