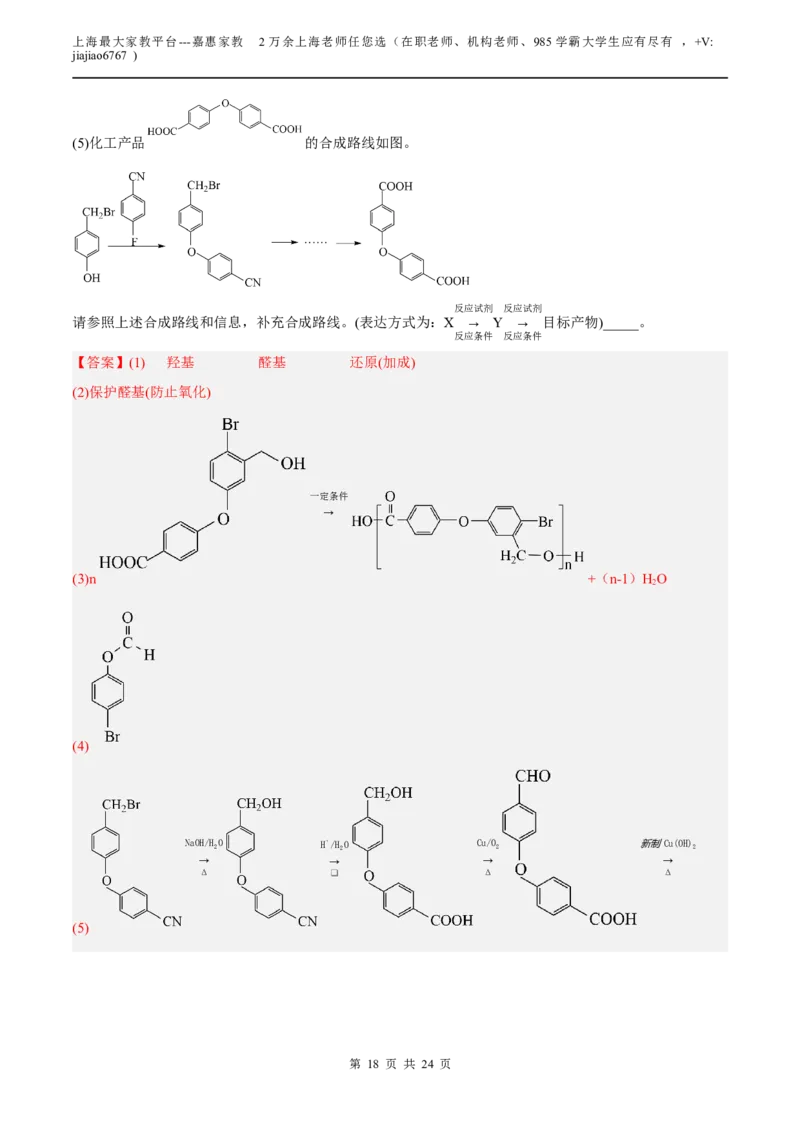
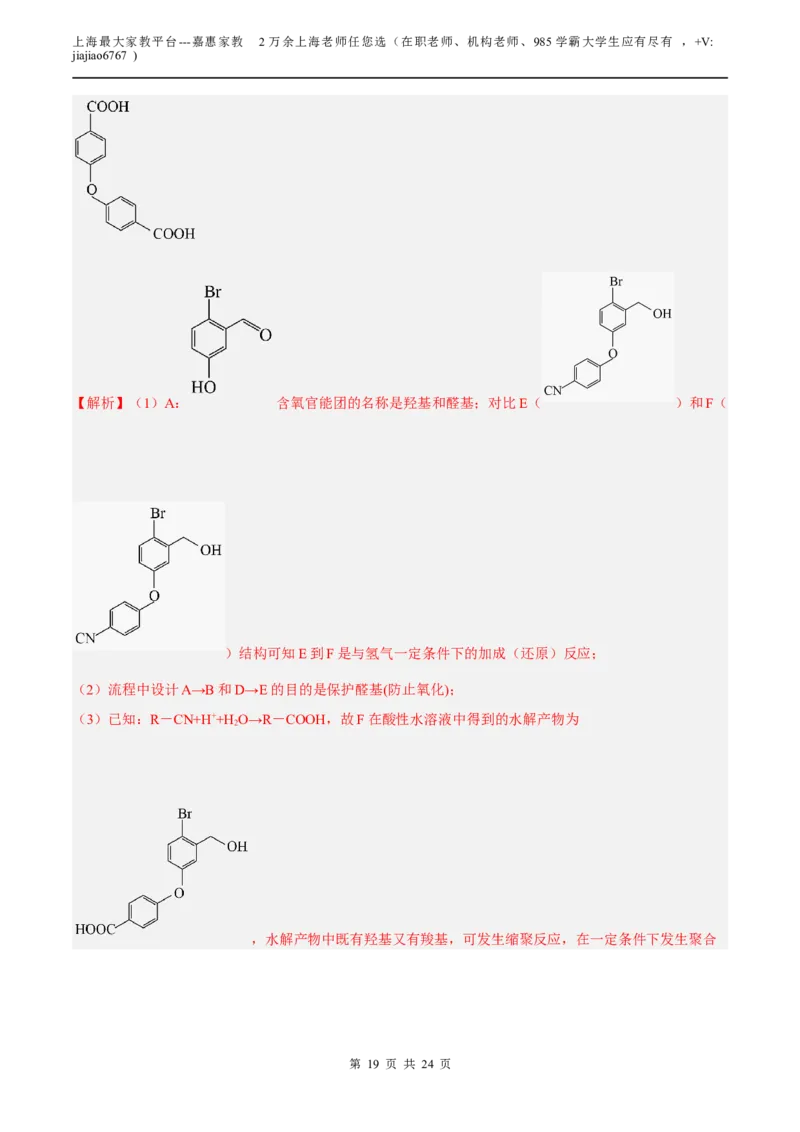
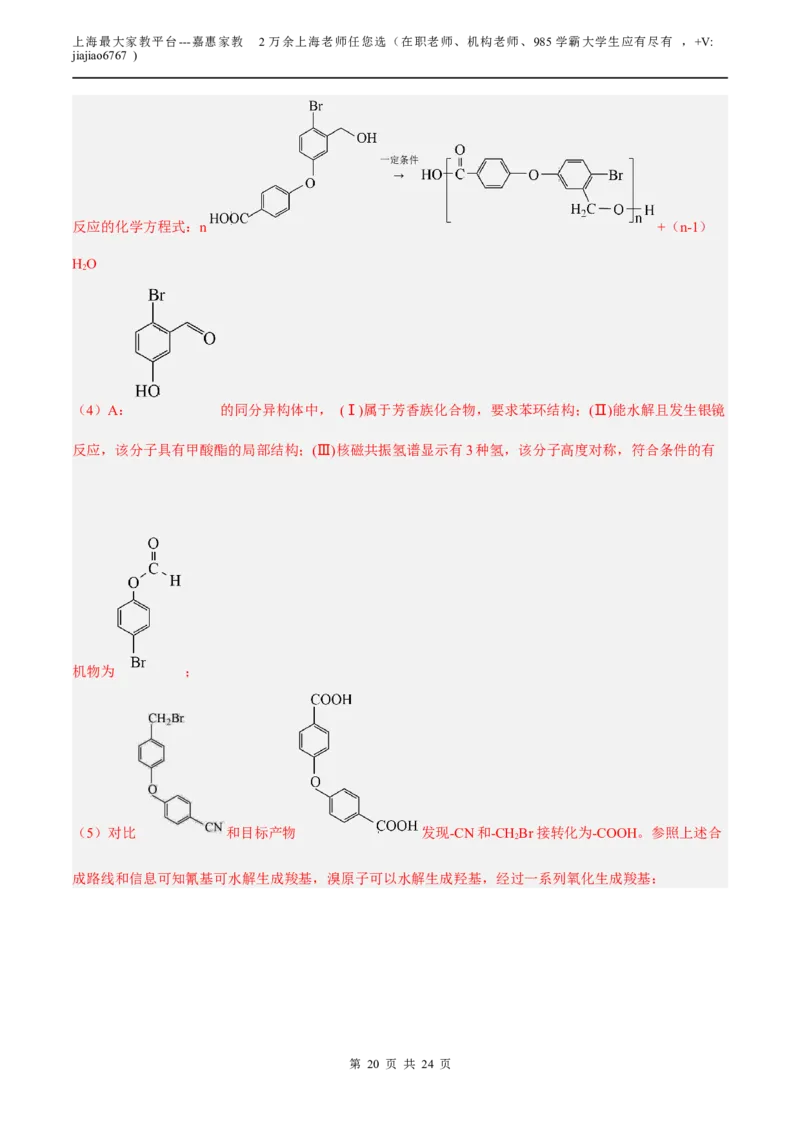
文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2023 年高考化学第三次模拟考试卷
高三化学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
一、选择题:本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,仅有一个选项正确。
1.2022年4月16日,王亚平等三位航天英雄乘坐“神州”十三号飞船顺利返航,这展示了我国科技发展
的巨大成就。下列说法不正确的是
A.飞船表面可使用能发生分解反应的覆盖材料
B.飞船内的氧气可由电解水的方式供给
C.被誉为“航天员手臂延长器”的操作棒是由高分子化合物碳纤维制成
D.“天宫课堂”的泡腾片实验利用了强酸制弱酸原理
【答案】C
【解析】A.飞船在飞行中表面与空气摩擦会产生大量的热,分解反应吸收热量从而可以降低飞船表面的
温度,A项正确;
B.电解水产生O 简单易得,能满足飞船内O 的需要,B项正确;
2 2
C.碳纤维为C的单质,不属于高分子化合物,C项错误;
D.泡腾片中含有碳酸盐遇酸产生CO,利用强酸制弱酸,D项正确;
2
故选C。
2.2022年3月“天宫课堂”中,神舟十三号航天员用过饱和CHCOONa溶液做结晶实验,制造了美丽的
3
“冰雪”,有关CHCOONa固体说法正确的是
3
A.是弱电解质 B.不含非极性键 C.是离子晶体 D.溶于水显酸性
【答案】C
【解析】A.醋酸钠在溶液中完全电离出自由移动的离子,属于强电解质,故A错误;
B.醋酸钠是含有离子键、极性键和非极性键的离子化合物,故B错误;
C.醋酸钠是含有离子键、极性键和非极性键的离子晶体,故C正确;
第 1 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.醋酸钠是强碱弱酸盐,醋酸根离子在溶液中水解使溶液呈碱性,故D错误;
故选C。
3.VA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。工业上用白磷(P )与Ba(OH) 反应生成PH 和
4 2 3
一种盐,该盐可与HSO 反应制备一元中强酸HPO 。下列说法正确的是
2 4 3 2
A.HPO 中P的杂化方式为sp3
3 2
B.P 是正四面体形分子,其中P-P-P夹角为109°28′
4
C.VA族元素单质的晶体类型相同
D.基态砷原子( As)核外电子排布式为[Ar]4s24p3
33
【答案】A
5+3−2×2
【解析】A.HPO 中心原子P的价层电子对数=2+ =4,P杂化方式为sp3,A正确;
3 2 2
B.P 是正四面体形分子,P-P-P夹角为60°,B项错误;
4
C.VA族氮、磷、砷(As)、锑(Sb)元素由非金属元素向金属过渡,氮、磷、砷形成的单质是分子晶体,锑
(Sb)单质晶体类型是金属晶体,C项错误;
D.基态砷原子(❑ As )核外电子排布式为[Ar]3d104s24p3,D项错误;
33
故选A。
4.下列现象或事实不能用同一原理解释的是
A.氯水和浓硝酸用棕色试剂瓶保存 B.加热碳酸氢铵晶体和氯化铵晶体都产生气体
C.常温下铁和金都不溶于浓硝酸 D.氯水、HO 均能使品红溶液褪色
2 2
【答案】C
【解析】A.氯水和浓硝酸不稳定,光照易分解,因此要用棕色试剂瓶保存,原理相同,选项A不符合;
B.加热碳酸氢铵晶体和氯化铵晶体,两者都会分解,产生氨气,选项B不符合;
C.常温下,铁遇浓硝酸发生钝化现象,而金性质不活泼,不与浓硝酸反应,二者不溶原理不相同,选项
C符合;
D.氯水、HO 都具有漂白性,故能使品红溶液褪色,选项D不符合;
2 2
答案选C。
5.下列水溶液因水解而呈碱性的是
A.NaCO B.BaCl C.(NH )SO D.Ca(OH)
2 3 2 4 2 4 2
【答案】A
【解析】A.碳酸钠是强碱弱酸盐,碳酸根离子在溶液中水解使溶液呈碱性,故A符合题意;
B.氯化钡是强酸强碱盐,在溶液中不水解,溶液呈中性,故B不符合题意;
C.硫酸铵是强酸弱碱盐,铵根离子在溶液中水解使溶液呈酸性,故C不符合题意;
第 2 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.氢氧化钙是强碱,溶于水的氢氧化钙在溶液中完全电离出的氢氧根离子使溶液呈碱性,故D不符合题
意;
故选A。
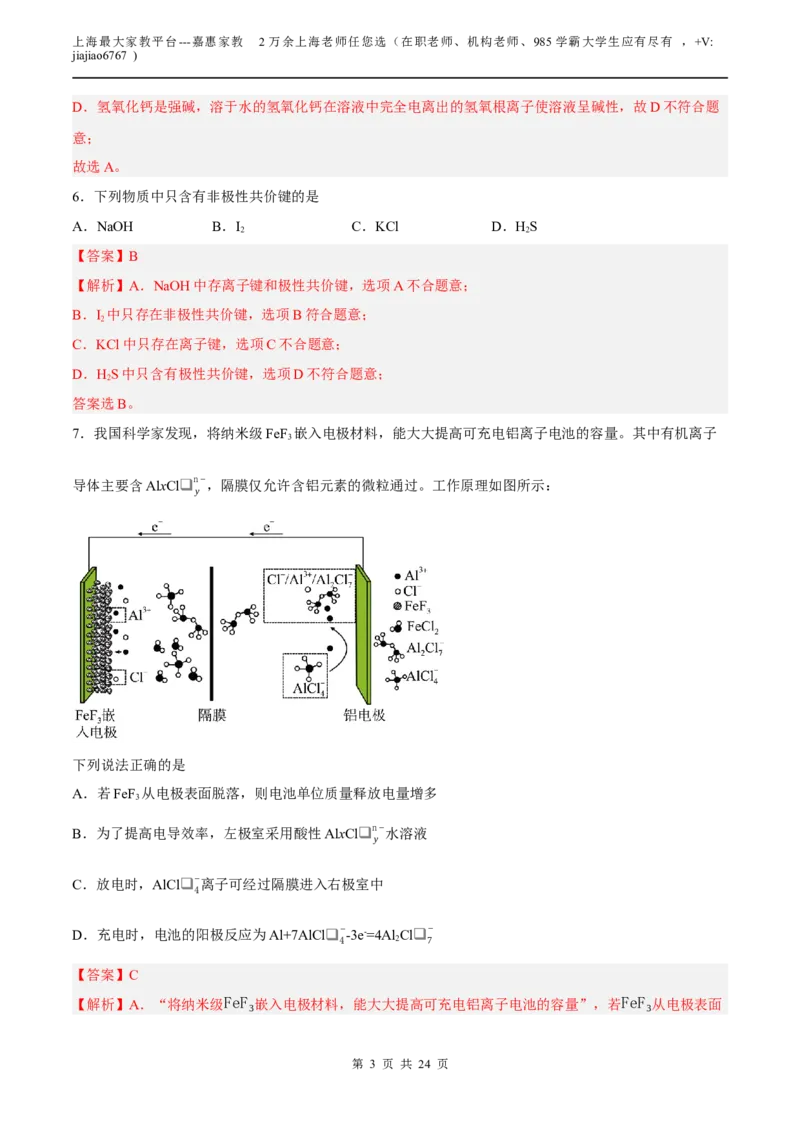
6.下列物质中只含有非极性共价键的是
A.NaOH B.I C.KCl D.HS
2 2
【答案】B
【解析】A.NaOH中存离子键和极性共价键,选项A不合题意;
B.I 中只存在非极性共价键,选项B符合题意;
2
C.KCl中只存在离子键,选项C不合题意;
D.HS中只含有极性共价键,选项D不符合题意;
2
答案选B。
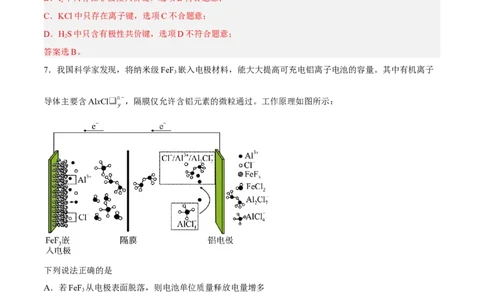
7.我国科学家发现,将纳米级FeF 嵌入电极材料,能大大提高可充电铝离子电池的容量。其中有机离子
3
导体主要含AlxCl❑
n−,隔膜仅允许含铝元素的微粒通过。工作原理如图所示:
y
下列说法正确的是
A.若FeF 从电极表面脱落,则电池单位质量释放电量增多
3
B.为了提高电导效率,左极室采用酸性AlxCl❑
n−水溶液
y
C.放电时,AlCl❑ −离子可经过隔膜进入右极室中
4
D.充电时,电池的阳极反应为Al+7AlCl❑ − -3e-=4AlCl❑ −
4 2 7
【答案】C
【解析】A.“将纳米级FeF 嵌入电极材料,能大大提高可充电铝离子电池的容量”,若FeF 从电极表面
3 3
第 3 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
脱落,电池容量减小,则电池单位质量释放电量减少,A错误;
B.把左极室的有机离子导体改成水溶液后,会使左极室溶液中的离子总浓度减小,导致电导效率下降,B
错误;
C.放电时,左边电极为正极,右边电极为负极,阴离子向负极移动,结合分析可知右边负极需要消耗
AlCl− ,故AlCl−
离子经过隔膜进入右极室中,C正确;
4 4
D.电池充电时为电解池装置,电池的负极与外接电源负极相连为阴极,电极反应为放电时正极反应的逆
过程,反应为Fe2+-e-=Fe3+,D错误;
故选C。
8.化学创造美好生活。下列劳动项目所涉及反应的离子方程式错误的是
A.工程师用FeS除去废水中的Hg2+ :FeS(s) + Hg2+ (aq) = HgS(s) + Fe2+ (aq)
B.消防员使用泡沫灭火器灭火:A13+
+3HCO-
= Al(OH) ↓+3CO ↑
3 3 2
C.环保人员用漂白粉溶液脱除废气中的SO :Ca2++2ClO- +SO+H O=CaSO↓+2HClO
2 2 2 3
D.工人用醋酸处理水垢中的氢氧化镁:Mg(OH) + 2CHCOOH= 2CH COO-+Mg2+ +2H O
2 3 3 2
【答案】C
【解析】A.硫化汞溶度积小于硫化亚铁,硫化亚铁与汞离子反应生成硫化汞和亚铁离子,实现沉淀的转
化,A正确;
B.灭火器中铝离子与碳酸氢根发生双水解产生二氧化碳,B正确;
C.次氯酸根具有氧化性,二氧化硫具有还原性,发生氧化还原反应:
Ca2++ClO−+SO +H O=CaSO ↓+Cl−+2H+ ,C错误;
2 2 4
D.醋酸及氢氧化镁均为弱电解质,不能拆,D正确;
故答案为:C。
9.实验室利用如图所示的装置进行甲烷与氯气的混合气体在光照下反应的实验。U形管的左端中V(甲烷):
V(氯气)=1:4,忽略氯气在水中的溶解,光照下反应一段时间后,下列说法正确的是
第 4 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A.若甲烷与氯气完全反应,U形管的右端液面上升
B.甲烷和氯气在光照条件下反应,最多能生成4种含氯化合物
C.产物之一CHCl 的结构只有1种
2 2
D.生成的各有机物的物质的量之和与消耗的氯气的物质的量相等
【答案】C
【解析】A.甲烷与氯气完全反应会生成氯化氢,氯化氢溶于水,导致左侧压强减小,U形管的左端液面
上升,A错误;
B.甲烷和氯气在光照条件下反应,最多能生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷、氯化氢,5种
含氯化合物,B错误;
C.甲烷结构为四面体形结构,产物之一CHCl 的结构只有1种,C正确;
2 2
D.由于一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷消耗氯气量不同,故生成的各有机物的物质的量之和
与消耗的氯气的物质的量不相等,D错误;
故选C。
10.厌氧腐蚀是指在缺氧的深层潮湿土壤中,钢管表面附着的硫酸盐还原菌会促进钢铁的腐蚀,反应原理
如图所示。下列说法正确的是
A.厌氧腐蚀属于化学腐蚀
B.发生厌氧腐蚀会使土壤碱性增强
C.镀锌钢管破损后钢铁腐蚀加速
D.每生成1molFeS,共转移2mol电子
【答案】B
【解析】A.钢管中含有碳元素,铁、碳与潮湿的土壤形成原电池,则厌氧腐蚀属于电化学腐蚀,A错误;
第 5 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
B.发生厌氧腐蚀会使土壤碱性增强,正极生成氢气与氢氧根,B正确;
C.镀锌的钢管破损后锌比铁活泼,锌作负极,保护铁不被腐蚀,镀锌钢管破损后钢铁腐蚀减慢,C错误;
D.硫酸根离子变为硫离子时转移8个电子,则每生成 1mol FeS,最终转移的电子数为8N ,D错误;
A
故选B。
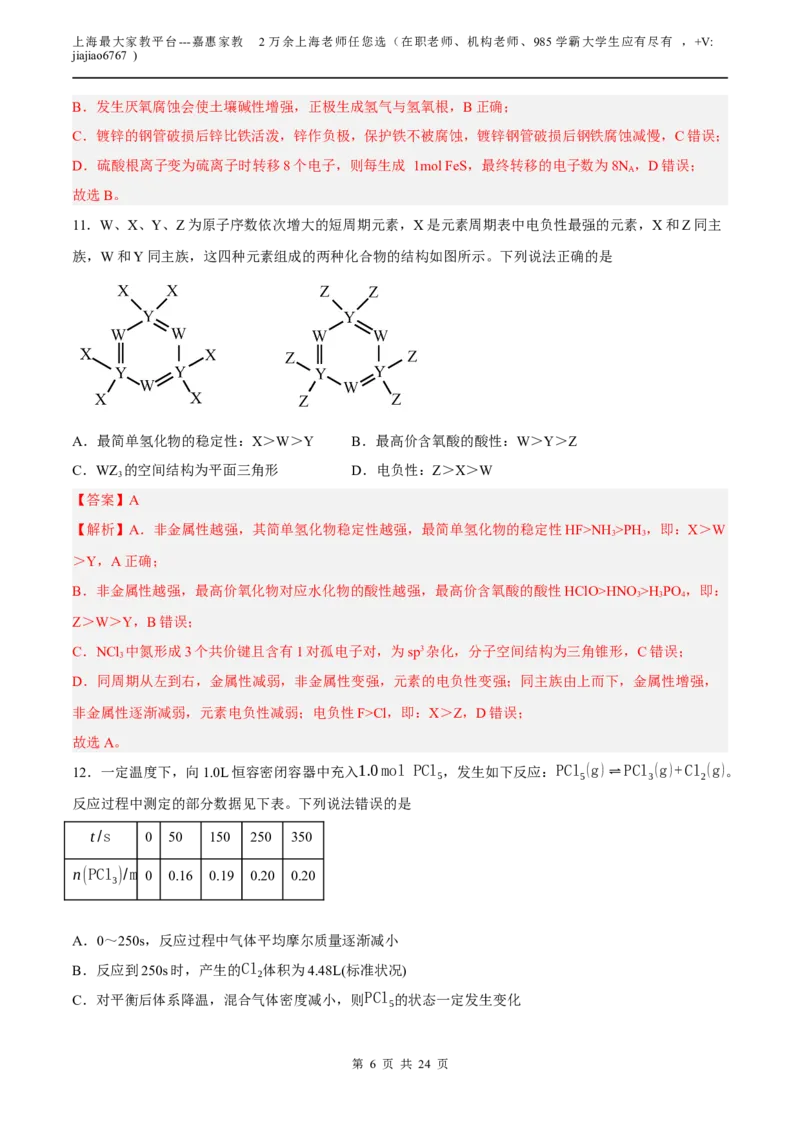
11.W、X、Y、Z为原子序数依次增大的短周期元素,X是元素周期表中电负性最强的元素,X和Z同主
族,W和Y同主族,这四种元素组成的两种化合物的结构如图所示。下列说法正确的是
A.最简单氢化物的稳定性:X>W>Y B.最高价含氧酸的酸性:W>Y>Z
C.WZ 的空间结构为平面三角形 D.电负性:Z>X>W
3
【答案】A
【解析】A.非金属性越强,其简单氢化物稳定性越强,最简单氢化物的稳定性HF>NH >PH,即:X>W
3 3
>Y,A正确;
B.非金属性越强,最高价氧化物对应水化物的酸性越强,最高价含氧酸的酸性HClO>HNO >H PO ,即:
3 3 4
Z>W>Y,B错误;
C.NCl 中氮形成3个共价键且含有1对孤电子对,为sp3杂化,分子空间结构为三角锥形,C错误;
3
D.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属性增强,
非金属性逐渐减弱,元素电负性减弱;电负性F>Cl,即:X>Z,D错误;
故选A。
12.一定温度下,向1.0L恒容密闭容器中充入1.0mol PCl ,发生如下反应:PCl (g)⇌ PCl (g)+Cl (g)。
5 5 3 2
反应过程中测定的部分数据见下表。下列说法错误的是
t/s 0 50 150 250 350
n(PCl )/mo0l 0.16 0.19 0.20 0.20
3
A.0~250s,反应过程中气体平均摩尔质量逐渐减小
B.反应到250s时,产生的Cl 体积为4.48L(标准状况)
2
C.对平衡后体系降温,混合气体密度减小,则PCl 的状态一定发生变化
5
第 6 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.其它条件相同时,向平衡后体系再充入等物质的量的PCl 和PCl ,此时v(正)>v(逆)
5 3
【答案】D
【解析】A.该反应是气体总物质的量增大、质量不变的反应,则0~250s,气体平均摩尔质量逐渐减小,
故A正确;
B.反应到250s时,PCl 气体的物质的量为0.2mol,根据反应方程式可知生成氯气的物质的量为0.2mol,
3
所以产生的Cl 体积为4.48L(标准状况),故B正确;
2
C.PCl 相对分子质量大,沸点高,对平衡后体系降温,混合气体密度减小,说明气体总质量减小,则
5
PCl 的状态一定发生变化,故C正确;
5
c(PCl )c(Cl ) 0.2×0.2
D.一定温度下,K= 3 2 = =0.05 ;其它条件相同时,向平衡后体系再充入等物质的
c(PCl ) 0.8
5
c(PCl )c(Cl ) 1.2×0.2 0.4
量的PCl 和PCl ,假设加入的PCl 和PCl 都是1mol,Q= 3 2 = = >K=0.05,所
5 3 5 3 c(PCl ) 1.8 3
5
以反应逆向进行,此时v(正)n,C错误;
D.CHCOONa溶液、NaCO 溶液水解导致溶液显碱性,且碳酸钠水解程度更大;NaOH 溶液电离使溶液
3 2 3
显碱性,则pH相同的CHCOONa溶液、NaCO 溶液、NaOH 溶液,氢氧化钠浓度更小、醋酸钠浓度更大,
3 2 3
D错误;
故选B。
14.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.2.0gD 16O和14ND 的混合物中含有的电子数为N
2 3 A
B.120g由NaHSO 和MgSO 组成的混合固体中SO2-数目为N
4 4 4 A
C.60gSiO 含有硅氧键的数目为2N
2 A
D.5.6gFe2+中未成对电子数为0.6N
A
【答案】A
【解析】A.D16O和14ND 的摩尔质量均为20g/ mol,2.0gD 16O和14ND 的混合物的物质的量为0.1mol,
2 3 2 3
D16O和14ND 的分子中含电子数都为10,则含有的电子数为N ,A项正确;
2 3 A
B.硫酸氢钠固体含有钠离子和硫酸氢根离子,不含硫酸根离子,B项错误;
C.60g二氧化硅的物质的量为1mol,而1mol二氧化硅中含4mol硅氧键,故含有硅氧键的数目为4N ,C
A
项错误;
5.6g
D.Fe2+核外电子排布式为[Ar]3d6,则5.6gFe2+中未成对电子数为 ×4×N mol−1=0.4N ,D项
56g/mol A A
错误;
答案选A。
15.有机物M是合成塑身药物利莫那班的重要中间体,其结构简式如图所示:
下列关于M的叙述正确的是
A.M的分子式为C H OCl
15 18 4
B.M能使Br 的CCl 溶液褪色
2 4
C.M在碱性条件下能稳定存在
D.M苯环上的二溴代物有4种
【答案】D
【解析】A.根据M的结构简式,M的分子式为C H OCl,故A错误;
15 17 4
第 8 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
B.M中不含碳碳不饱和键和醛基,因此M不能使溴的四氯化碳溶液褪色,故B错误;
C.该结构中含有酯基,在碱性条件下发生水解,因此M在碱性条件下不能稳定存在,故C错误;
D.苯环上有两种不同的氢原子,根据定一移一,苯环上的二溴代物有4种,故D正确;
答案为D。
❑
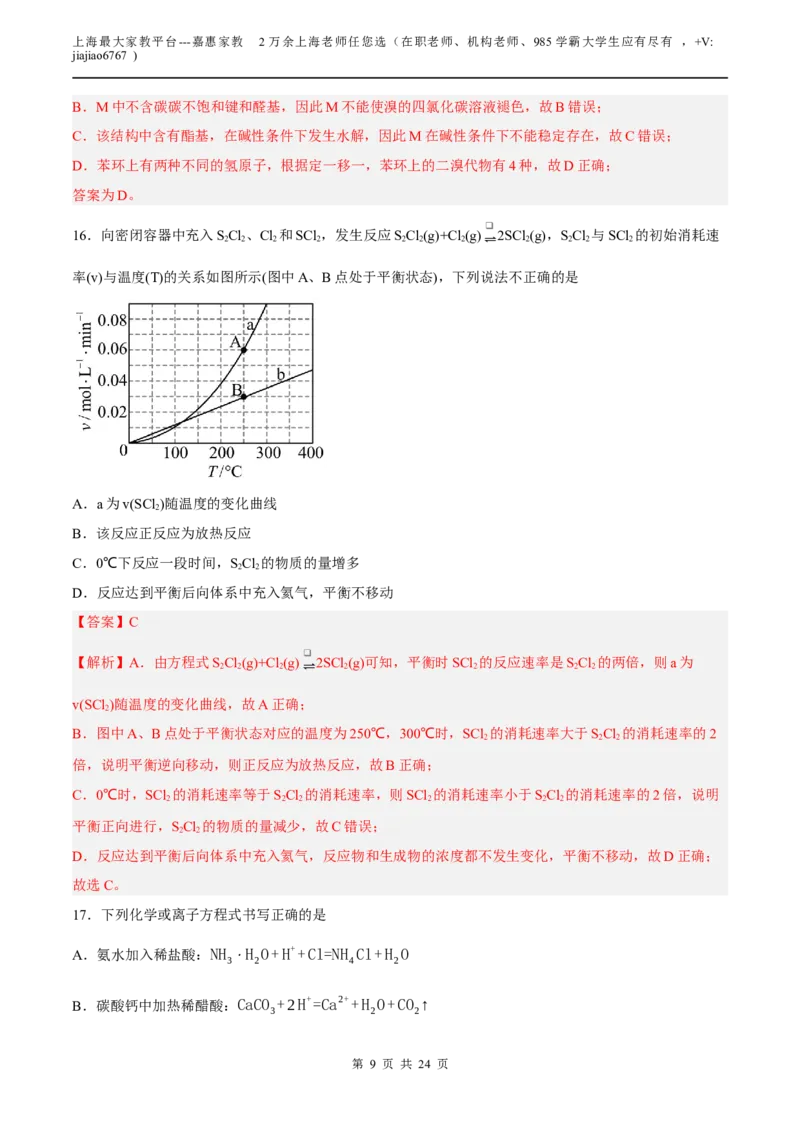
16.向密闭容器中充入SCl、Cl 和SCl ,发生反应SCl(g)+Cl (g) 2SCl (g),SCl 与SCl 的初始消耗速
2 2 2 2 2 2 2 ⇌ 2 2 2 2
率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
A.a为v(SCl )随温度的变化曲线
2
B.该反应正反应为放热反应
C.0℃下反应一段时间,SCl 的物质的量增多
2 2
D.反应达到平衡后向体系中充入氦气,平衡不移动
【答案】C
❑
【解析】A.由方程式SCl(g)+Cl (g) 2SCl (g)可知,平衡时SCl 的反应速率是SCl 的两倍,则a为
2 2 2 ⇌ 2 2 2 2
v(SCl )随温度的变化曲线,故A正确;
2
B.图中A、B点处于平衡状态对应的温度为250℃,300℃时,SCl 的消耗速率大于SCl 的消耗速率的2
2 2 2
倍,说明平衡逆向移动,则正反应为放热反应,故B正确;
C.0℃时,SCl 的消耗速率等于SCl 的消耗速率,则SCl 的消耗速率小于SCl 的消耗速率的2倍,说明
2 2 2 2 2 2
平衡正向进行,SCl 的物质的量减少,故C错误;
2 2
D.反应达到平衡后向体系中充入氦气,反应物和生成物的浓度都不发生变化,平衡不移动,故D正确;
故选C。
17.下列化学或离子方程式书写正确的是
A.氨水加入稀盐酸:NH ⋅H O+H++Cl=NH Cl+H O
3 2 4 2
B.碳酸钙中加热稀醋酸:CaCO +2H+=Ca2++H O+CO ↑
3 2 2
第 9 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.少量的SO 通到氯化钡溶液中:SO +Ba2++H O=BaSO ↓+2H+
2 2 2 3
D.在加热条件下,足量的铁粉与少量的氯气反应:2Fe+3Cl
≜
2FeCl
2 3
【答案】D
【解析】A.氨水加入稀盐酸生成氯化铵和水,其反应的离子方程式为NH ⋅H O+H+=NH++H O,故A错
3 2 4 2
误;
B.碳酸钙中加热稀醋酸生成醋酸钙、二氧化碳和水,其反应的离子方程式为
CaCO +2CH COOH=Ca2++2CH COO−+H O+CO ↑,故B错误;
3 3 3 2 2
C.SO 通到氯化钡溶液中不发生反应,故C错误;
2
D.氯气具有强氧化性,在加热条件下,足量的铁粉与少量的氯气反应生成氯化铁:2Fe+3Cl ≜ 2FeCl ,
2 3
故D正确;
故选D。
18.用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理,下列说法错误的是
A.图1烧瓶中固体X可以是CaO或NaOH
B.工业上,若出现液氨泄漏,喷洒稀盐酸比喷洒水处理效果好
C.将湿润的蓝色石蕊试纸置于三颈烧瓶c口,试纸变红,说明NH 已经集满
3
D.关闭a,封闭c,打开b,引发喷泉实验,三颈烧瓶内压强变化如图2,则D点时喷泉最剧烈
【答案】C
【解析】A.CaO或NaOH溶于水放出大量热,浓氨水遇热分解反应生成氨气,故图1烧瓶中固体X可以是
CaO或NaOH,选项A正确;
B.液氨是氨气的液态,氨气是碱性气体,在酸中的溶解度大于其在水中的溶解度,因此若出现液氨泄漏,
喷洒稀盐酸比喷洒水处理效果好,选项B正确;
第 10 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.氨气是碱性气体,不能用湿润的蓝色石蕊试纸检验,应用湿润的红色石蕊试纸检验,选项C错误;
D.为引发喷泉实验应:关闭a,封闭c,打开b,根据图2可知,C点时压强最低,此时喷泉最剧烈,选
项D正确;
答案选C。
19.下列各组离子一定能大量共存的是
A.滴加苯酚显紫色的溶液中:NH+ 、Na+、Cl−、SCN−
4
B.在强碱溶液中:Na+、K+、AlO−、CO2−
2 3
C.pH=1的溶液中:K+、Fe2+、Cl−、NO−
3
D.c(H+)=10−13mol/L的溶液中:NH+ 、Al3+、NO−、SO2−
4 3 4
【答案】B
【解析】A. 滴加苯酚显紫色的溶液中有铁离子,与SCN−不共存,A错误;
B. 在强碱溶液中:Na+、K+、AlO−、CO2−与氢氧根离子互不反应,可以共存, B正确;
2 3
C. pH=1的溶液呈酸性,酸性条件下硝酸根具有氧化性,亚铁离子具有还原性,能发生氧化还原反应,
故pH=1的溶液中Fe2+、NO−不能大量共存,C错误;
3
D. c(H+)=10−13mol/L的溶液中,说明水的电离受到了抑制,溶液可能显酸性,也可能显碱性,碱性下,
氢氧根与NH+
反应生成弱碱一水合氨不能共存,D错误;
4
答案选B。
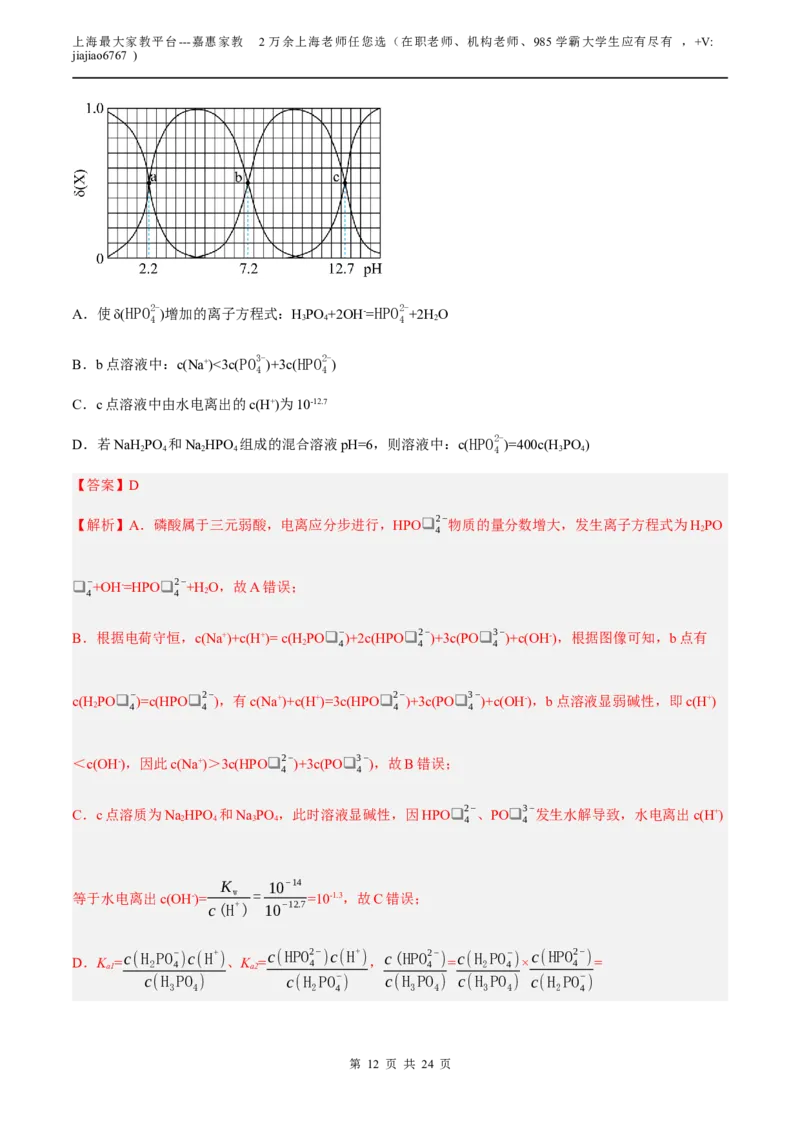
20.NaH PO 、NaHPO 是新型冠状病毒灭活疫苗的辅料之一。298K时,向HPO 溶液中逐滴加入NaOH
2 4 2 4 3 4
溶液至过量,所得溶液中HPO 、H PO- 、HPO2-、PO3-的物质的量分数δ(X)随溶液pH的变化如图所示
3 4 2 4 4 4
c(X)
[δ(X)= ]。下列叙述正确的是(已知:lg2=0.3)
c(H PO )+c(H PO-)+c(HPO2-)+c(PO3-)
3 4 2 4 4 4
第 11 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A.使δ(HPO2- )增加的离子方程式:HPO +2OH-=HPO2- +2H O
4 3 4 4 2
B.b点溶液中:c(Na+)<3c(PO3- )+3c(HPO2-
)
4 4
C.c点溶液中由水电离出的c(H+)为10-12.7
D.若NaH PO 和NaHPO 组成的混合溶液pH=6,则溶液中:c(HPO2- )=400c(H PO )
2 4 2 4 4 3 4
【答案】D
【解析】A.磷酸属于三元弱酸,电离应分步进行,HPO❑ 2−物质的量分数增大,发生离子方程式为HPO
4 2
❑ − +OH-=HPO❑ 2− +H O,故A错误;
4 4 2
B.根据电荷守恒,c(Na+)+c(H+)= c(HPO❑ − )+2c(HPO❑ 2− )+3c(PO❑ 3− )+c(OH-),根据图像可知,b点有
2 4 4 4
c(HPO❑ − )=c(HPO❑ 2− ),有c(Na+)+c(H+)=3c(HPO❑ 2− )+3c(PO❑ 3− )+c(OH-),b点溶液显弱碱性,即c(H+)
2 4 4 4 4
<c(OH-),因此c(Na+)>3c(HPO❑ 2− )+3c(PO❑ 3− ),故B错误;
4 4
C.c点溶质为NaHPO 和NaPO ,此时溶液显碱性,因HPO❑ 2−、PO❑ 3−发生水解导致,水电离出c(H+)
2 4 3 4 4 4
K 10−14
等于水电离出c(OH-)= w = =10-1.3,故C错误;
c(H+) 10−12.7
D.K a1 = c(H 2 PO− 4 )c(H+ )、K a2 = c(HPO2 4 − )c(H+ ),c(HPO2 4 − )= c(H 2 PO− 4 )× c(HPO2 4 − ) =
c(H PO ) c(H PO− ) c(H PO ) c(H PO ) c(H PO− )
3 4 2 4 3 4 3 4 2 4
第 12 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
K K 10−2.2 10−7.2 =102.6=400,因此c( )=400c(H PO ),故D正确;
a1 ⋅ a2 = × HPO2- 3 4
c(H+) c(H+) 10−6 10−6 4
答案为D。
二、填空题(共四题,每题15分,60分)
21.捕集CO 的技术对解决全球温室效应意义重大。回答下列问题。
2
❑
I.国际空间站处理CO 的一个重要方法是将CO 还原,所涉及的反应方程式为:CO(g)+4H(g) CH(g)
2 2 2 2 ⇌ 4
+2H O(g)
2
(1)碳原子核外有_____种能量不同的电子。HO分子空间构型为_____。已知上述反应中,反应物能量总和
2
大于生成物能量总和,则该反应为_____反应。(填“放热”或“吸热”)
II.将CO 富集、活化、转化为具有高附加值的化学品对实现碳中和有重要意义。回答下列问题。
2
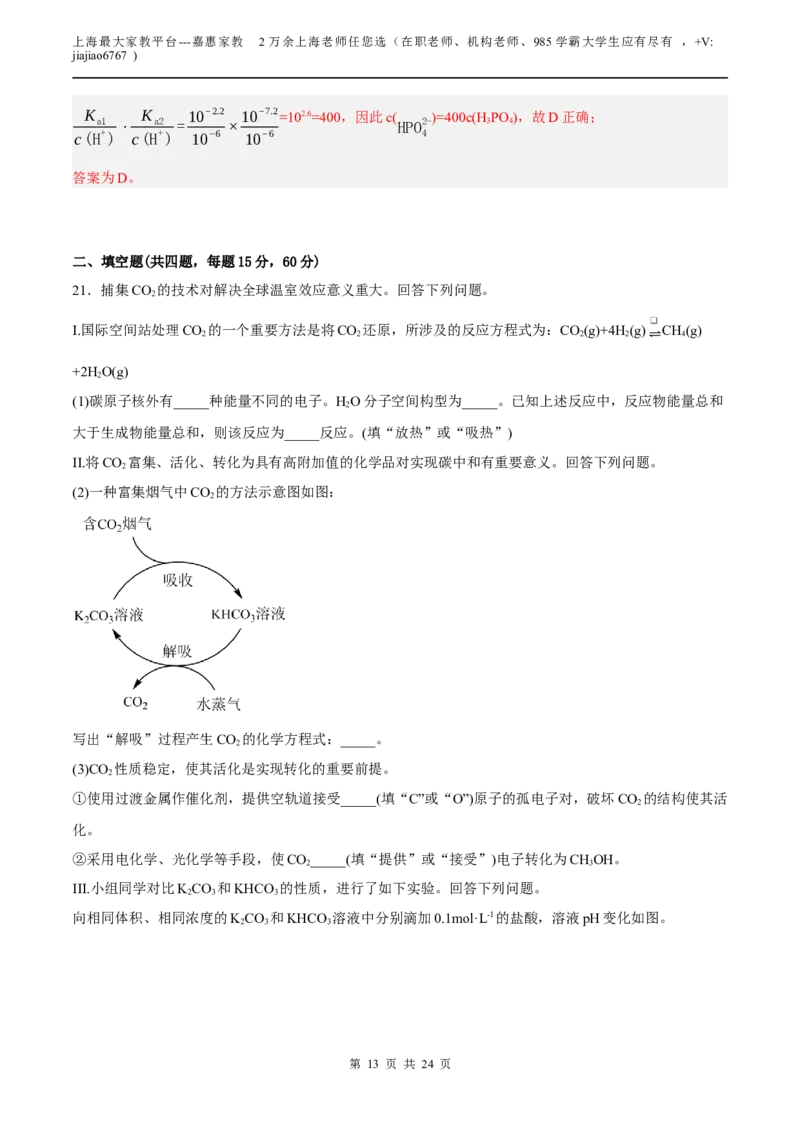
(2)一种富集烟气中CO 的方法示意图如图:
2
写出“解吸”过程产生CO 的化学方程式:_____。
2
(3)CO 性质稳定,使其活化是实现转化的重要前提。
2
①使用过渡金属作催化剂,提供空轨道接受_____(填“C”或“O”)原子的孤电子对,破坏CO 的结构使其活
2
化。
②采用电化学、光化学等手段,使CO_____(填“提供”或“接受”)电子转化为CHOH。
2 3
III.小组同学对比KCO 和KHCO 的性质,进行了如下实验。回答下列问题。
2 3 3
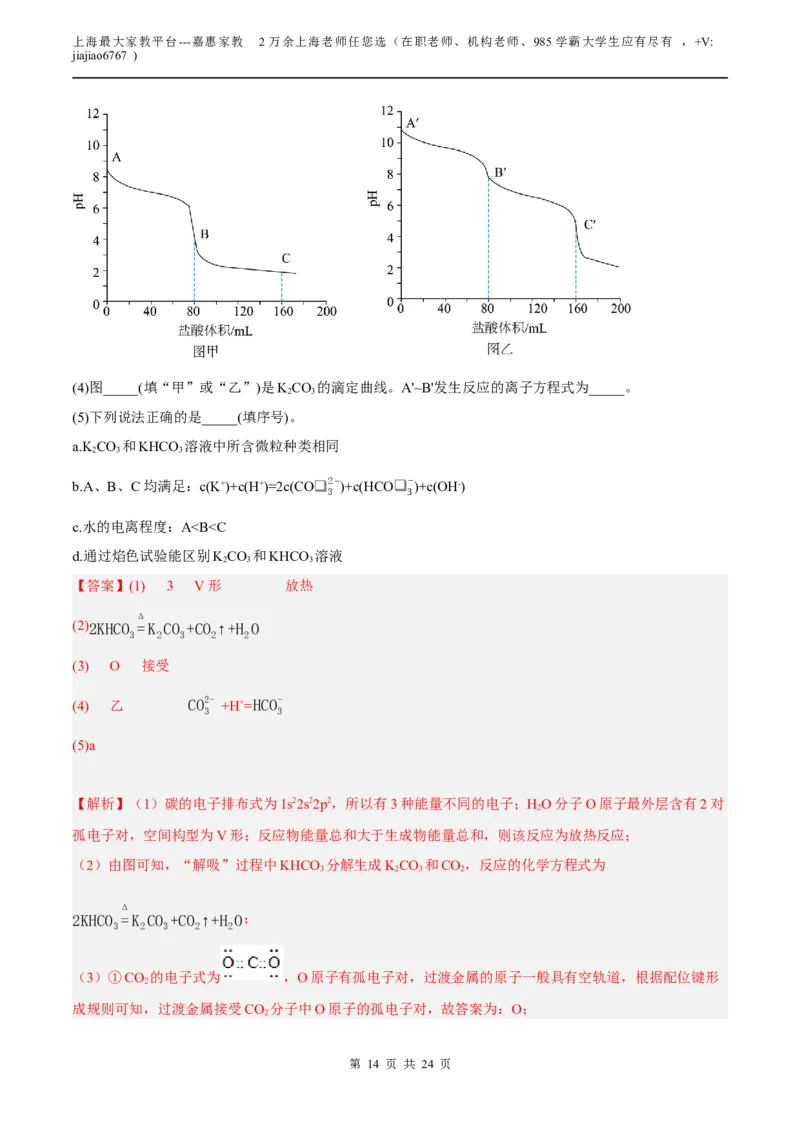
向相同体积、相同浓度的KCO 和KHCO 溶液中分别滴加0.1mol·L-1的盐酸,溶液pH变化如图。
2 3 3
第 13 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)图_____(填“甲”或“乙”)是KCO 的滴定曲线。A'~B'发生反应的离子方程式为_____。
2 3
(5)下列说法正确的是_____(填序号)。
a.K CO 和KHCO 溶液中所含微粒种类相同
2 3 3
b.A、B、C均满足:c(K+)+c(H+)=2c(CO❑ 2− )+c(HCO❑ − )+c(OH-)
3 3
c.水的电离程度:AB>C,故c错误;
d.KCO 和KHCO 溶液的金属阳离子相同,焰色试验的颜色相同,则不能鉴别,故d错误;
2 3 3
故答案为:a。
22.CO 和SO 的大量排放会对环境产生影响,科学家在积极探索用化学方法吸收并综合利用CO 和SO 。
2 2 2 2
I.重整吸收CO 主要反应如下:
2.
①CO(g)+CH (g) 2H(g)+2CO(g) -Q (Q 大于0)
2 4 2 1 1
②CO
2
(g)+H
2
(g) ⇌H
2
O(g)+CO(g) -Q
2
(Q
2
大于0)
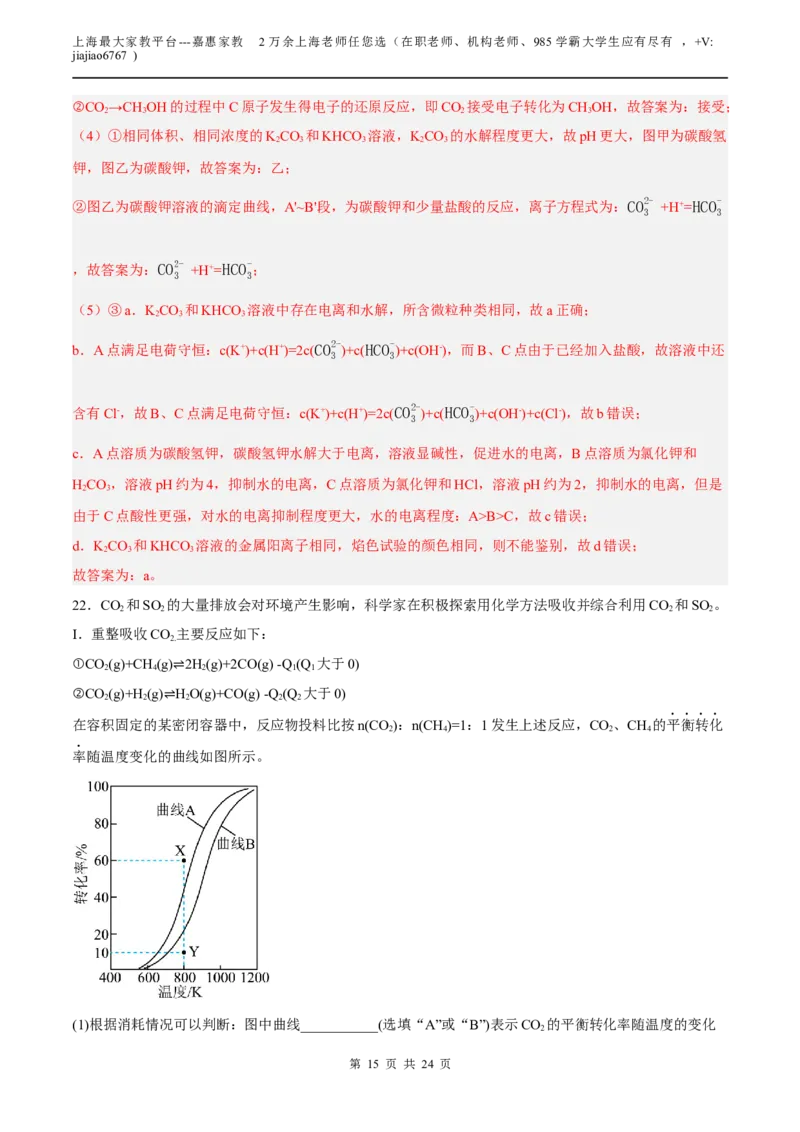
在容积固定的某⇌密闭容器中,反应物投料比按n(CO):n(CH)=1:1发生上述反应,CO、CH 的平衡转化
2 4 2 4
率随温度变化的曲线如图所示。
(1)根据消耗情况可以判断:图中曲线___________(选填“A”或“B”)表示CO 的平衡转化率随温度的变化
2
第 15 页 共 24 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
趋势。提高CH 的平衡转化率的措施为___________(列举一条)。
4
(2)图中X点的v(CH,正)___________v(CH ,逆)。(选填“>”、“<”或“=”)若起始c(CO)=2mol·L-1,反应
4 4 2
至5min时,CH 的转化率到达Y点,且c(H)为0.2mol·L-1,则0~5min内HO(g)的平均反应速率
4 2 2
v=___________mol·L-1·min-1。
II.ZnO悬浊液吸收SO ,再催化氧化得到硫酸盐。
2
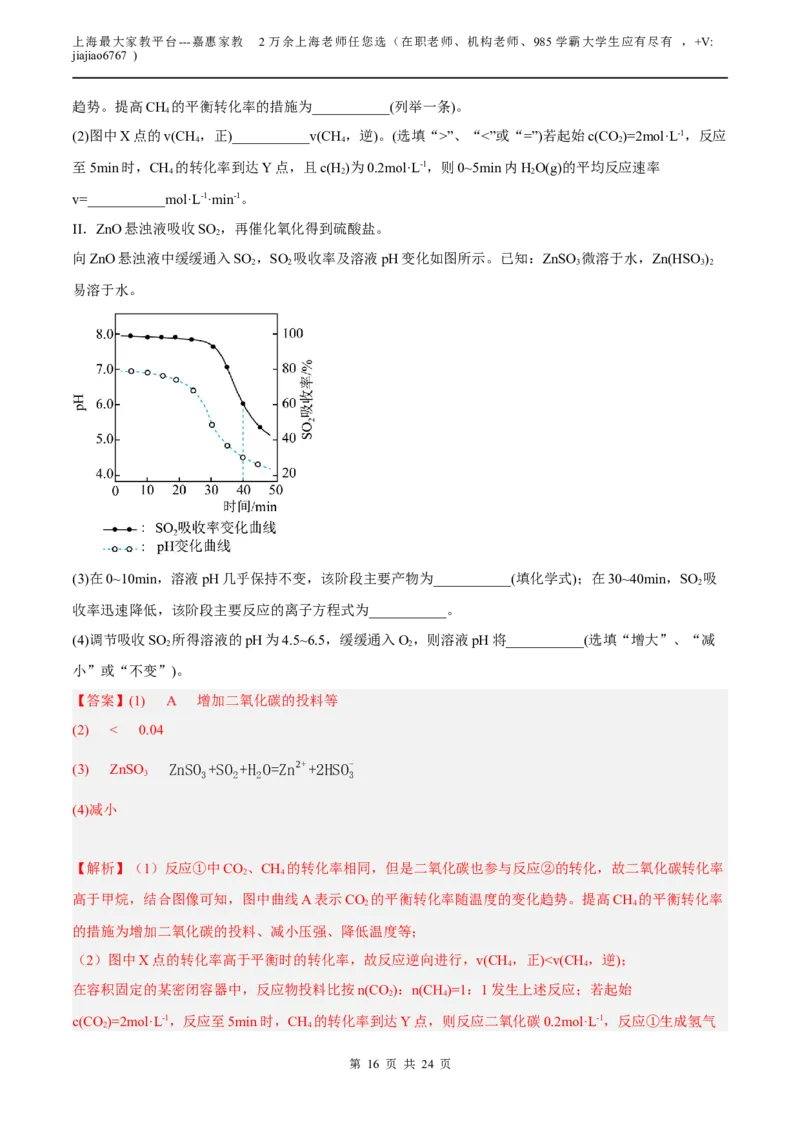
向ZnO悬浊液中缓缓通入SO ,SO 吸收率及溶液pH变化如图所示。已知:ZnSO 微溶于水,Zn(HSO )
2 2 3 3 2
易溶于水。
(3)在0~10min,溶液pH几乎保持不变,该阶段主要产物为___________(填化学式);在30~40min,SO 吸
2
收率迅速降低,该阶段主要反应的离子方程式为___________。
(4)调节吸收SO 所得溶液的pH为4.5~6.5,缓缓通入O,则溶液pH将___________(选填“增大”、“减
2 2
小”或“不变”)。
【答案】(1) A 增加二氧化碳的投料等
(2) < 0.04
(3) ZnSO ZnSO +SO +H O=Zn2++2HSO-
3 3 2 2 3
(4)减小
【解析】(1)反应①中CO、CH 的转化率相同,但是二氧化碳也参与反应②的转化,故二氧化碳转化率
2 4
高于甲烷,结合图像可知,图中曲线A表示CO 的平衡转化率随温度的变化趋势。提高CH 的平衡转化率
2 4
的措施为增加二氧化碳的投料、减小压强、降低温度等;
(2)图中X点的转化率高于平衡时的转化率,故反应逆向进行,v(CH,正)