文档内容
合格演练测评(七)
(几种重要的金属化合物)
姓名: 班级: 正确率:
题号 1 2 3 4 5 6 7 8 9 10
答案
题号 11 12 13 14 15 16 17 18 19 20
答案
一、单项选择题
1.1989年世界卫生组织把铝确定为食品污染源之一而加以控制,铝在下列应用中应加以控制的是(
)
①制铝合金 ②制电线 ③制炊具 ④制银色漆颜料 ⑤用明矾净水 ⑥用明矾与苏打制食品膨松
剂材料 ⑦用氢氧化铝凝胶制胃舒平药品 ⑧用铝箔包装糖果和食品 ⑨制易拉罐
A.③④⑧⑨ B.⑥⑧⑨
C.①②③⑤⑨ D.③⑤⑥⑦⑧⑨
解析:与食品加工和食品包装有关的应用均应加以控制。
答案:D
2.下列各组中两瓶无标签的无色溶液,不用其他试剂能鉴别出来的一组是( )
A.AlCl 和NaOH B.NaHCO 和NaOH
3 3
C.NaSO 和BaCl D.AgNO 和NaCl
2 4 2 3
解析:AlCl 逐滴加入NaOH溶液中,开始阶段无沉淀,之后生成沉淀,而NaOH加入AlCl 中先产生沉淀,
3 3
后沉淀溶解,两过程现象不一致,可鉴别,A项正确;B项互滴无明显现象;C、D项互滴现象相同。
答案:A
3.为了除去MgO中混有的少量杂质AlO,可选用的试剂是( )
2 3
A.KOH溶液 B.氨水
C.稀盐酸 D.稀醋酸解析:要除去MgO中混有的少量杂质AlO,所加试剂只能与AlO 反应而不能与MgO反应,反应完全后
2 3 2 3
过滤即可。氨水与AlO 不反应,稀盐酸、稀醋酸均能与MgO反应,只有KOH溶液能与AlO 反应而与MgO不反
2 3 2 3
应,故选A项。
答案:A
4.等量镁铝合金粉末分别与下列四种过量物质充分反应,放出氢气最多的是( )
A.NaOH溶液 B.HSO 稀溶液
2 4
C.蔗糖溶液 D.NaCl溶液
解析:镁、铝均反应生成氢气时,产生氢气最多。A项NaOH溶液只能与铝反应;B项HSO 溶液能与镁、
2 4
铝都反应生成氢气;C、D项与镁、铝都不反应。故选B项。
答案:B
5.下列离子方程式书写错误的是( )
A.AlCl 溶液中加入过量氨水:Al3++4OH-===[Al(OH)]-
3 4
B.Al(OH) 溶于NaOH溶液中:Al(OH)+OH-===
3 3
[Al(OH)]-
4
C.Al(OH) 溶于盐酸溶液中:Al(OH)+3H+===Al3++
3 3
3HO
2
D.AlO 粉末溶于NaOH溶液中:AlO+2OH-+3HO===
2 3 2 3 2
2[Al(OH)]-
4
解析:AlCl 溶液加入过量氨水,生成Al(OH) 沉淀,且Al(OH) 不溶于氨水。
3 3 3
答案:A
6.铝、氧化铝、氢氧化铝和可溶性铝盐分别与过量强碱溶液反应,下列对其生成物的说法正确的是(
)
A.都有HO生成 B.都有H 生成
2 2
C.都有[Al(OH)]-生成 D.都有Al3+生成
4
解析:铝与过量强碱溶液反应没有水生成;氧化铝与过量强碱溶液反应没有H 生成;铝、可溶性铝盐
2
与过量强碱溶液反应都没有Al3+生成。
答案:C7.下列变化不可能通过一步实验直接完成的是( )
A.[Al(OH)]-→Al3+ B.AlO→Al(OH)
4 2 3 3
C.Al3+→[Al(OH)]- D.AlCl→Al(OH)
4 3 3
解析:AlO 不能一步转化为Al(OH),应需二步,即AlO→Al3+→Al(OH)。
2 3 3 2 3 3
答案:B
8.下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl 反应
2
②Fe与过量稀硫酸反应
③FeCl 溶液中通入少量Cl
2 2
④Fe和FeO 的混合物溶于盐酸中
2 3
A.只有① B.①③
C.①②③ D.全部
答案:B
9.向氯化亚铁溶液中加入过量的氨水,有沉淀生成。过滤,加热沉淀物至质量不再发生变化,得到红
棕色的残渣。上述沉淀和残渣分别为( )
A.Fe(OH)、Fe(OH);FeO
2 3 3 4
B.Fe(OH);FeO
2
C.Fe(OH)、Fe(OH);FeO
2 3 2 3
D.FeO;Fe(OH)
2 3 3
解析:氯化亚铁溶液与氨水反应先生成白色的Fe(OH) 沉淀,Fe(OH) 很快又被氧化成红褐色Fe(OH)
2 2 3
沉淀,Fe(OH) 沉淀受热发生分解反应:2Fe(OH)=====FeO+3HO。
3 3 2 3 2
答案:C
10.除去FeCl 溶液中少量的FeCl,最好的办法是( )
2 3
A.加入氢氧化钠溶液 B.通入氯气
C.加入铜粉 D.加入铁粉
解析:要实现“Fe3+→Fe2+”的转化,需要加入还原剂,且不引入新的杂质离子,最好的办法是加入足量铁粉充分反应后过滤,发生的化学反应为2FeCl+Fe===3FeCl。
3 2
答案:D
11.下列物质中既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
A.Al(OH) B.NaCl溶液
3
C.KSO 溶液 D.稀HSO
2 4 2 4
解析:本题考查两性物质,而两性物质在选项中只有Al(OH),选A。
3
答案:A
12.在一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可以看到灰黑色粉末,其中有
些已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加KSCN溶液,马上出现红色。
以下结论不正确的是( )
A.该灰黑色粉末用作抗氧化剂
B.该灰黑色粉末不可食用
C.小袋中原来装有铁粉
D.小袋中原来装有氧化铁
解析:从溶液遇KSCN出现红色看,黑色粉末应该含铁元素。氧化铁为红棕色粉末,D错误;该灰黑色粉
末为还原铁粉,起到吸收包装盒中的氧气,防止高档茶叶、点心等食品变质的作用,故A、B、C正确。
答案:D
13.在下列反应中,能置换出铁的是( )
A.Cu+FeCl(溶液) B.Na+FeSO(溶液)
2 4
C.Ag+FeSO(溶液) D.Al+FeO(高温)
4 3 4
答案:D
14.可用KSCN溶液检验的离子为( )
A.Na+ B.Ag+
C.Fe2+ D.Fe3+
答案:D
15.只用NaOH溶液不能除去括号中杂质的是( )A.Mg(AlO) B.MgCl(AlCl)
2 3 2 3
C.Fe(Al) D.FeO(AlO)
2 3 2 3
答案:B
16.下列物质的溶液既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A.MgSO B.NaCO
4 2 3
C.NaHCO D.(NH)SO
3 4 2 4
答案:C
17.可用于鉴别葡萄糖溶液和淀粉溶液的试剂是( )
A.氨水 B.NaCO 溶液
2 3
C.FeCl 溶液 D.新制Cu(OH) 悬浊液
2 2
答案:D
18.要除去NaHCO 溶液中少量的NaCO,最好使用( )
3 2 3
A.饱和石灰水 B.NaOH溶液
C.盐酸 D.通入CO
2
解析:饱和碳酸钠溶液与CO 反应生成碳酸氢钠溶液。
2
答案:D
19.下列有关NaCO 和NaHCO 的说法中,正确的是( )
2 3 3
A.热稳定性:NaCO<NaHCO
2 3 3
B.相同温度下在水中的溶解度:NaCO<NaHCO
2 3 3
C.等质量的两种固体,分别与过量盐酸反应,生成CO 的质量相等
2
D.取1 mol·L-1的两种溶液,分别滴入酚酞,溶液颜色较深的是NaCO 溶液
2 3
答案:D
20.为除去实验室制得的CO 气体中的少量HCl气体,最好将混合气体通过( )
2
A.烧碱溶液 B.饱和碳酸氢钠溶液
C.饱和碳酸钠溶液 D.水解析:饱和碳酸钠溶液与CO 反应生成碳酸氢钠溶液。
2
答案:B
二、非选择题
21.化合物A、B组成元素相同,且B为白色。C是一种与B含有相同价态该金属元素的硫酸盐,向C中
加入适量的NaOH溶液,可观察到生成的沉淀迅速变为灰绿色,最后变为红褐色沉淀A,加热A可得红棕色粉
末D。回答下列问题:
(1)写出各物质的化学式:A 、B 、C 、D 。
(2)写出B转化为A的化学方程式________________________
____________________________________________________。
写出A受热分解的化学方程式___________________________
____________________________________________________。
解析:解答本题的关键是抓住C与NaOH溶液反应的特征现象,确定A是Fe(OH) ,C是FeSO ,B为
3 4
Fe(OH),D为FeO。
2 2 3
答案:(1)Fe(OH) Fe(OH) FeSO FeO
3 2 4 2 3
(2)4Fe(OH)+O+2HO===4Fe(OH) 2Fe(OH)=====FeO+3HO
2 2 2 3 3 2 3 2
22.(1)用氯化铝溶液与氢氧化钠溶液反应时,当Al3+的物质的量与OH-的物质的量之比(以下均填物
质的量之比)为 时,Al(OH) 沉淀最多; 时,Al(OH) 恰好全部溶解。
3 3
(2)四羟基合铝酸钠溶液与盐酸反应时,[Al(OH)]-的物质的量与H+的物质的量之比为 时,
4
Al(OH) 沉淀量最多。
3
解析:反应的离子方程式:Al3++3OH-===Al(OH)↓;Al3++4OH-===[Al(OH)]-;[Al(OH)]-+H+
3 4 4
===Al(OH)↓+HO。由此可得到相应的答案。
3 2
答案:(1)1∶3 1∶4 (2)1∶1
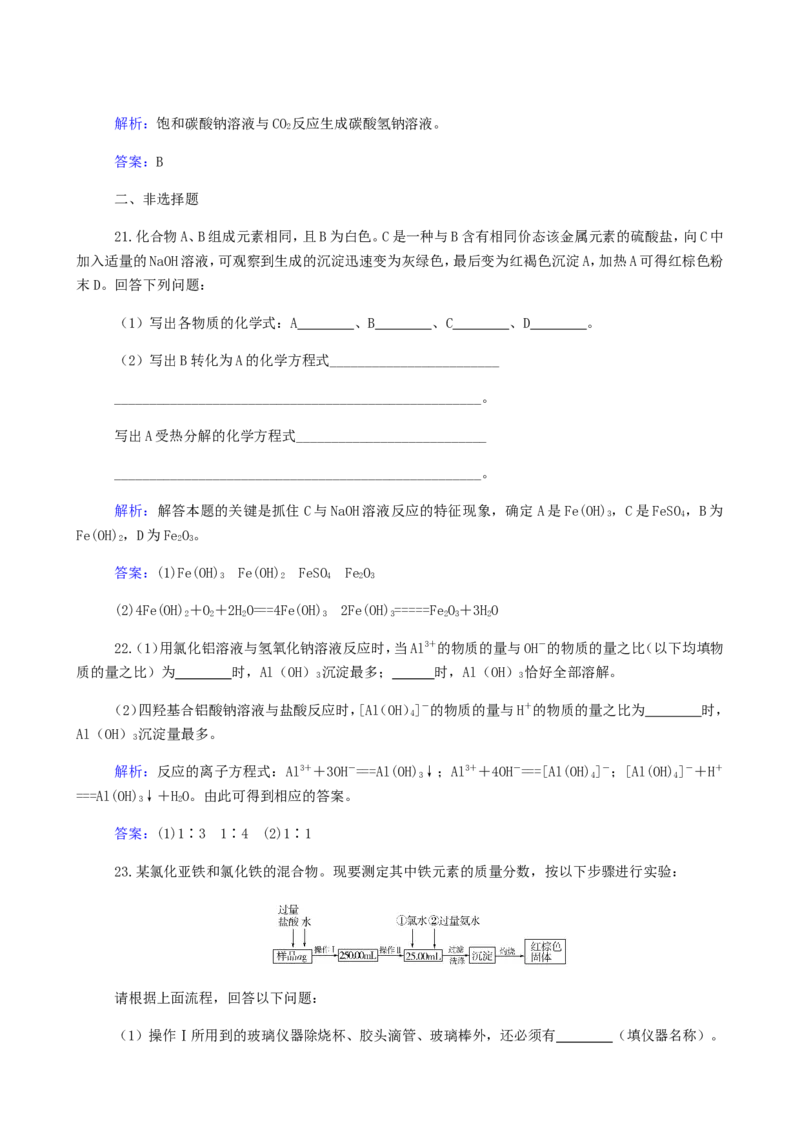
23.某氯化亚铁和氯化铁的混合物。现要测定其中铁元素的质量分数,按以下步骤进行实验:
请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、胶头滴管、玻璃棒外,还必须有 (填仪器名称)。(2)请写出加入氯水发生反应的离子方程式_______________
____________________________________________________。
(3)将沉淀物加热、灼烧,冷却至室温,反复称量至质量不变。若蒸发皿质量是Wg,蒸发皿与加热后固
1
体总质量是Wg,计算样品中铁元素的质量分数。
2
答案:(1)250 mL容量瓶
(2)2Fe2++Cl===2Fe3++2Cl-
2
(3)×100%