文档内容
专题七 化学反应与能量 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
一、选择题(本题含16小题,每题3分,共48分。每题只有一个选项符合题意)
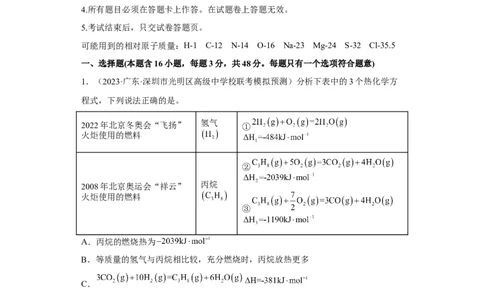
1.(2023·广东·深圳市光明区高级中学校联考模拟预测)分析下表中的3个热化学方
程式,下列说法正确的是。
2022年北京冬奥会“飞扬” 氢气 ①
火炬使用的燃料
②
2008年北京奥运会“祥云” 丙烷
火炬使用的燃料
③
A.丙烷的燃烧热为
B.等质量的氢气与丙烷相比较,充分燃烧时,丙烷放热更多
C.
D.
【答案】C
【详解】A.燃烧热是在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出
的热量;由反应②可知,1mol丙烷燃烧生成液体水时,放出热量大于 ,
A错误;
B.等质量的氢气与丙烷相比较,假设质量均为44g,则两者的物质的量分别为22mol、1mol,则由反应①②比较可知,充分燃烧时,氢气放热更多,B错误;
C.由盖斯定律可知,反应①×5-②得:
,C正确;
D.由盖斯定律可知,反应①× -③得:
,D错误;
故选C。
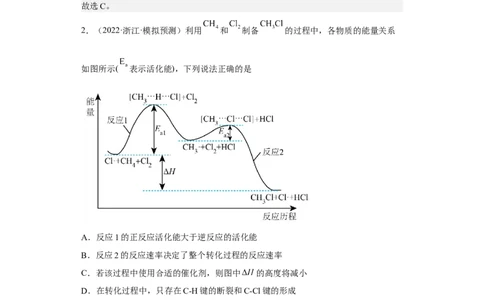
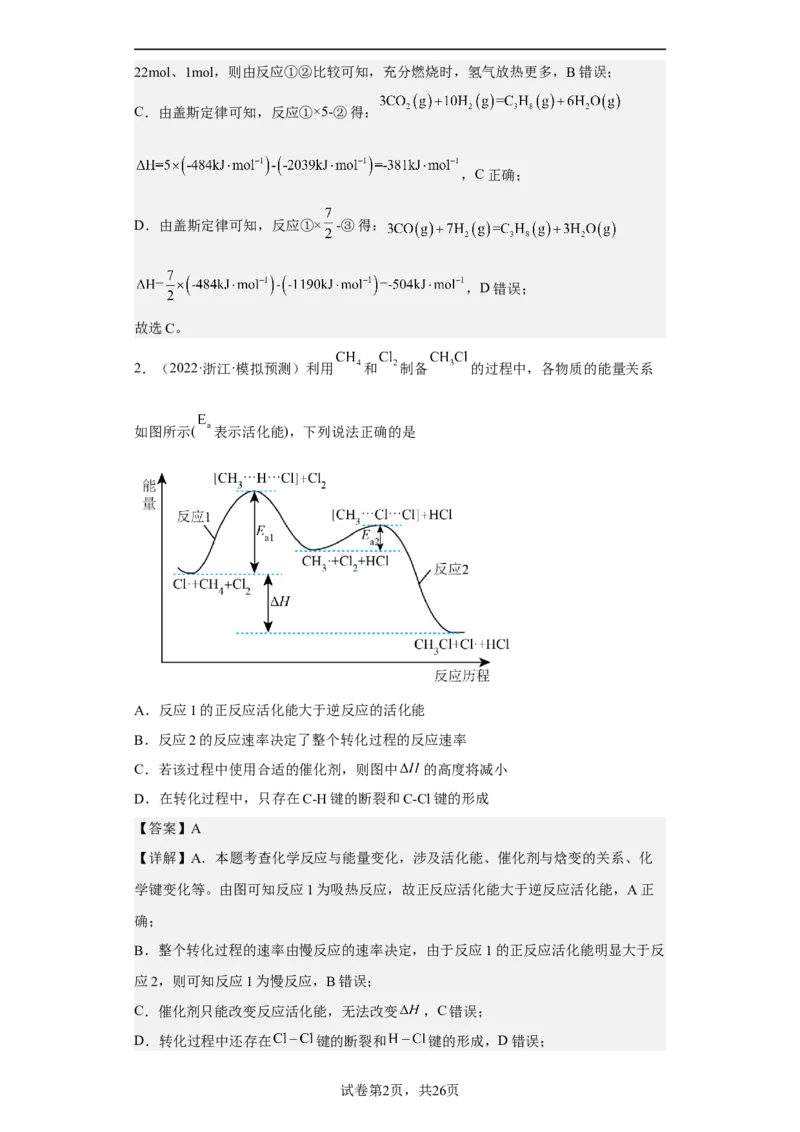
2.(2022·浙江·模拟预测)利用 和 制备 的过程中,各物质的能量关系
如图所示( 表示活化能),下列说法正确的是
A.反应1的正反应活化能大于逆反应的活化能
B.反应2的反应速率决定了整个转化过程的反应速率
C.若该过程中使用合适的催化剂,则图中 的高度将减小
D.在转化过程中,只存在C-H键的断裂和C-Cl键的形成
【答案】A
【详解】A.本题考查化学反应与能量变化,涉及活化能、催化剂与焓变的关系、化
学键变化等。由图可知反应1为吸热反应,故正反应活化能大于逆反应活化能,A正
确;
B.整个转化过程的速率由慢反应的速率决定,由于反应1的正反应活化能明显大于反
应2,则可知反应1为慢反应,B错误;
C.催化剂只能改变反应活化能,无法改变 ,C错误;
D.转化过程中还存在 键的断裂和 键的形成,D错误;
试卷第2页,共26页故答案为:A。
3.(2023秋·天津河北·高三天津外国语大学附属外国语学校校考期末)碘在不同状态
下(固态或气态)与氢气反应的热化学方程式如下所示。
① H(g) + I (?) 2HI(g) ΔH = −9.48 kJ/mol
2 2
② H(g) + I (?) 2HI(g) ΔH = +26.48 kJ/mol
2 2
下列判断正确的是
A.HI(g)比 HI(s)热稳定性更好
B.1mol 固态碘升华时将吸热 17 kJ
C.①中的 I 为固态,②中的 I 为气态
2 2
D.①的反应物总能量比②的反应物总能量高
【答案】D
【分析】气态碘的能量比固态碘的能量高,所以气态碘和氢气反应生成气态HI放出热
量,而固态碘和氢气反应生成气态HI会吸收热量,所以反应①中的碘为气体,反应②
中的碘为固体。
【详解】A.一般地,能量越低越稳定,同一物质,固态能量低于液态能量,液态能
量低于气态能量,所以HI(s)比 HI(g)热稳定性更好,故A错误;
B.由以上分析可知,反应①中的碘为气体,反应②中的碘为固体,将反应②减去反应
①,即可得到I(s)= I (g)的ΔH=+35.96kJ/mol,即1mol 固态碘升华时将吸热 35.96
2 2
kJ,故B错误;
C.由以上分析可知,反应①中的碘为气态,反应②中的碘为固态,故C错误;
D.一般地,同一物质,气态能量高于固态能量,所以①的反应物总能量比②的反应
物总能量高,故D正确;
故选D。
4.(2023秋·天津南开·高三崇化中学校考期末)以下反应均可制取O。下列有关说法
2
正确的是
反应①:2HO(l)=2H(g)+O(g) △H=+571.6 kJ·mol-1
2 2 2 1
反应②:2HO(l)=2HO(1)+O (g) △H=-196.4 kJ·mol-1
2 2 2 2 2
A.制取O 的反应一定是吸热反应
2
B.H 的燃烧热为-571.6 kJ·mol-1
2
C.若使用催化剂,反应②的△H将减小
D.反应2HO(l)=2HO(g)+O (g)的△H>-196.4 kJ·mol-1
2 2 2 2
【答案】D
【详解】A.制取O 的反应可能是放热反应,如过氧化氢在催化剂作用下的分解反应
2的△H<0,为放热反应,故A错误;
B.燃烧热是完全燃烧1mol物质得到最稳定的化合物所放出的热量,根据2HO(l)=
2
2H(g)+O(g)△H=+571.6 kJ·mol-1可知,H 的燃烧热为
2 2 1 2
0.5×571.6kJ•mol-1=285.8kJ•mol-1,故B错误;
C.使用催化剂,只能改变反应速率,不影响反应的△H,故C错误;
D.液态水变成气态水需要吸热,双氧水分解生成气态水放出的热量更小,△H更大,
因此2HO(l)═2H O(g)+O (g)的△H>-196.4kJ•mol-1,故D正确;
2 2 2 2
故选D。
5.(2021·浙江绍兴·校考模拟预测)镁和氯气反应生成氯化镁的能量关系图如图所示。
已知,气态的卤素原子得电子生成气态的卤离素子是放热过程。下列说法正确的是
A.∆H=∆H+∆H+∆H+∆H+∆H
6 1 2 3 4 5
B.Ca(g)–2e-=Ca2+(g) ∆H,则∆H>∆H
7 7 3
C.I(g)+e-=I-(g) ∆H,则∆H>∆H
8 8 4
D.MgCl (s)=Mg2+(aq)+2Cl-(aq) ∆H,则∆H>∆H
2 9 9 5
【答案】C
【详解】A.根据盖斯定律可知,∆H=∆H+∆H+∆H+∆H-∆H,故A错误;
6 1 2 3 4 5
B.原子失去电子变为离子属于吸热过程,Ca和Mg属于同主族,Ca的金属性强于
Mg,Ca→Ca2+吸收热量小于Mg→Mg2+吸收热量,即∆H<∆H,故B错误;
7 3
C.原子得电子变为离子属于放热过程,Cl非金属性强于I,即Cl→Cl-放出热量比I→I-
放出热量多,即∆H>∆H,故C正确;
8 4
D.MgCl (s)=Mg2+(g)+2Cl-(g)属于吸热反应,即∆H>0,Mg2+(g)、2Cl-(g)转化成Mg2+
2 5
(aq)、2Cl-(aq)要放出热量,发生MgCl (s)=Mg2+(aq)+2Cl-(aq)吸收热量比MgCl (s)=Mg2+
2 2
(g)+2Cl-(g)少,即∆H<∆H,故D错误;
9 5
答案为C。
6.(2023秋·安徽·高三校联考期末)环己烷有多种不同构象,其中椅式、半椅式、船
式、扭船式较为典型。各构象的相对能量图(位能)如图所示。下列说法正确的是
试卷第4页,共26页A.相同条件下扭船式环己烷最稳定
B. (椅式)的燃烧热大于 (船式)
C. (半椅式) (船式)
D.环己烷的扭船式结构一定条件下可自发转化成椅式结构
【答案】D
【详解】A.能量越低越稳定,由图图像可知椅式最稳定,A错误;
B.四种结构中,椅式能量最低最稳定,故椅式环己烷充分燃烧释放的热量最少,B错
误;
C. (半椅式) (船式) ,反应放热,
C错误;
D.扭船式结构转化成椅式结构释放能量,焓变小于0,根据△H-T△S<0反应自发进
行,一定条件下可自发转化,D正确;
故选D。
7.(2023秋·北京朝阳·高三统考期末)已知某些化学键键能如下,下列说法不正确的
是
化学键
键能/ 436 243 194 432 a
A.根据键能可估算反应 的
B.根据原子半径可知键长: ,进而推测
C. 与 反应生成 时,放出热量小于
D.常温下 和 的状态不同,与 和 的键能有关【答案】D
【详解】A.根据反应热=反应物总键能-生成物总键能,则:H(g)+Cl (g)=2HCl(g)中
2 2
有:△H=+436 kJ/mol+243 kJ/mol-2×432kJ/mol =-185kJ/mol,选项A正确;
B.Cl原子半径小于Br原子,H—Cl键的键长比H—Br键长短, H—Cl键的键能比H
—Br键大,进而推测 ,选项B正确;
C.键能 > ,反应生成HBr比生成HCl更难,放出的热量更低,故生成
时,放出热量小于 ,选项C正确;
D.Cl-Cl键能大于Br-Br键能,说明Cl 分子比Br 分子稳定,破坏的是共价键,而状
2 2
态由分子间作用力决定,选项D不正确;
答案选D。
8.(2023·广东·深圳市光明区高级中学校联考模拟预测)已知:298K时,相关物质的
相对能量如图所示。下列说法错误的是。
A.CO燃烧的热化学方程式为2CO(g)+O(g) 2CO(g) ∆H=-566kJ∙mol-1
2 2
B.H 的燃烧热为∆H=-242kJ∙mol-1
2
C.C H 比C H 稳定
2 6 2 4
D.CO(g)+HO(g) CO(g)+H(g)是放热反应
2 2 2
【答案】B
【详解】A.CO燃烧的热化学方程式为2CO(g)+O(g) 2CO(g) ∆H=[(-393×2)-
2 2
(-110×2+0)] kJ∙mol-1=-566kJ∙mol-1,A正确;
B.H 的燃烧热为∆H=[(-286)-(0+ ×0)] kJ∙mol-1=-286kJ∙mol-1,B错误;
2
试卷第6页,共26页C.C H 的能量为-84kJ∙mol-1,C H 的能量为52kJ∙mol-1,物质具有的能量越低,稳定性
2 6 2 4
越强,则C H 比C H 稳定,C正确;
2 6 2 4
D.CO(g)+HO(g) CO(g)+H(g) ∆H=[(-393+0)-(-110-242)] kJ∙mol-1=-41kJ∙mol-1,是放
2 2 2
热反应,D正确;
故选B。
9.(2023秋·天津河西·高二天津实验中学校考期末)已知可分别通过如下两个反应制
取氢气:
a.
b.
则下列说法正确的是
A.乙醇的燃烧热
B.升高反应a的反应温度,乙醇的平衡转化率减小
C.
D.制取等量的氢气,反应b吸收的能量更少
【答案】D
【详解】A.燃烧热指生成稳定的氧化物,应生成水、二氧化碳,根据题中信息,无
法得到乙醇的燃烧热,A错误;
B.反应a为吸热反应,升高温度,平衡正向移动,乙醇的平衡转化率增大,B错误;
C.根据盖斯定律,由反应b-反应a 2得
,C错误;
D.由热化学方程式可知,生成1mol氢气,反应a吸收热量 kJ,反应b吸收热量
kJ,所以制取等量的氢气,反应b吸收的能量低于反应a,D正确;
答案选D。
10.(2022·浙江·模拟预测)由金属单质和氯气反应得到 和 的能量关系如
图所示(M=Ca、Ba)。下列说法不正确的是A.
B.
C.
D.
【答案】A
【详解】A. 和 分别代表M元素的第一电离能和第二电离能,均大于0,所
以 ,A错误;
B. 断键形成两个气态氯原子,该过程吸热,所以 ,气态氯原子得到一
个电子可以形成稳定的8电子结构,该过程放热,所以 ,因此 ,B
正确;
C.同主族元素从上到下第一电离能逐渐减小,所以第一电离能: ,即
,C正确;
D.由盖斯定律可知: ,D正确。
故选A。
11.(2023·浙江金华·浙江省东阳中学校考模拟预测)乙烯是重要的工业原材料,中科
院设计并完成了 催化氧化 制取 的新路径,
试卷第8页,共26页其主要反应为:反应Ⅰ:
反应Ⅱ:
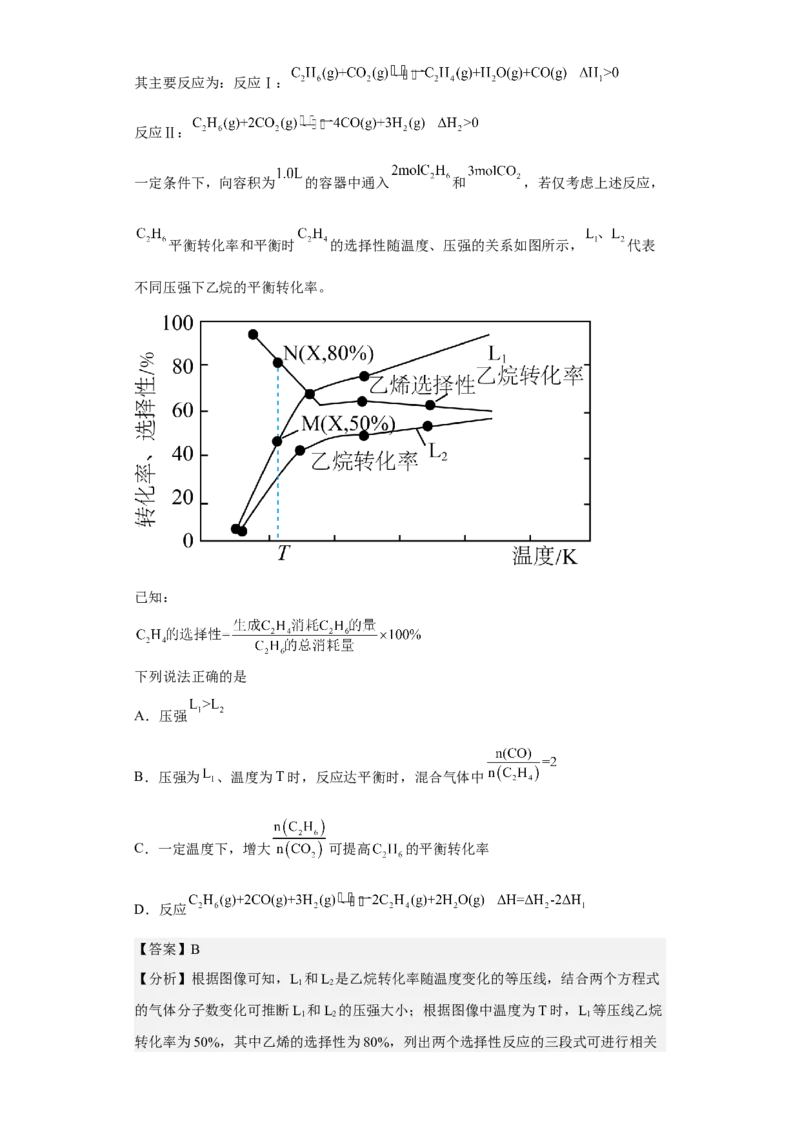
一定条件下,向容积为 的容器中通入 和 ,若仅考虑上述反应,
平衡转化率和平衡时 的选择性随温度、压强的关系如图所示, 代表
不同压强下乙烷的平衡转化率。
已知:
下列说法正确的是
A.压强
B.压强为 、温度为T时,反应达平衡时,混合气体中
C.一定温度下,增大 可提高 的平衡转化率
D.反应
【答案】B
【分析】根据图像可知,L 和L 是乙烷转化率随温度变化的等压线,结合两个方程式
1 2
的气体分子数变化可推断L 和L 的压强大小;根据图像中温度为T时,L 等压线乙烷
1 2 1
转化率为50%,其中乙烯的选择性为80%,列出两个选择性反应的三段式可进行相关计算。
【详解】A.Ⅰ和Ⅱ反应前后气体分子数都增大,相同温度下,压强越大都有利于Ⅰ
和Ⅱ反应的平衡逆移,乙烷的转化率减小,由图像可知,L 压强大乙烷转化率低,A
2
错误;
B.根据题意和分析,Ⅰ和Ⅱ反应的三段式为:
,
,平衡时混合气体中
,B正确;
C.一定温度下,增大 ,C H 的平衡转化率下降,C错误;
2 6
D.反应 ΔH=2ΔH-ΔH ,D错误;
1 2
答案选B。
【点睛】选择性的两个反应的平衡三段式要注意:相同物质的平衡量唯一且相同,按
选择性比例列出相应反应的转变量,相同反应物的平衡量是起始量减去两次的消耗量,
相同生成物的平衡量是起始量加上两次的生成量。
12.(2022·浙江·模拟预测)已知:在标准压强(101 kPa)、298 K下,由最稳定的单质
合成1 mol物质B的反应焓变叫做物质B的标准摩尔生成焓,用 表示。
有关物质的 如图所示。下列有关判断正确的是
试卷第10页,共26页A.2 mol NO(g)的键能大于1 mol 与1 mol 的键能之和-
B. 的
C. 标准燃烧热为
D. 比 稳定
【答案】D
【详解】A.根据题图,NO(g)的标准摩尔生成焓为 ,
的 反应物键能之和-生成物键能之和 ,即2mol
NO(g)的键能小于1mol 与1 mol 的键能之和,A错误;
B.同种物质气态时的能量高于液态时的能量, 的 ,B错
误;
C.由题图数据可计算出① ,②
,②-①可得
, 的标准燃烧热是指
生成液态水时放出的热量,应大于 ,C错误;
D. 的标准摩尔生成焓为 , 的标准摩尔生成焓为, 和 反应生成 放热,而生成 吸热,则 的能量比
低, 较稳定,D正确;
故选D。
13.(2022·浙江·模拟预测)在 下 催化 和 反应时的反应机理如下。
反应①:
反应②:
下列说法正确的是
A.反应①的
B. 在高温条件下能自发进行、低温条件下不能自发进行
C.
D.使用 可以降低反应的焓变
【答案】C
【详解】A. ,反应①为吸热反应,该反应能自发进行,说明 ,
即 ,A错误;
B. 为放热反应,即 ,反应过程中,气体分子数减
小,则 ,根据 时反应能自发进行,可知该反应低温下能自发进行、
高温下不能自发进行,B错误;
C. 的催化氧化反应为放热反应, 反应①+反应②得反应
,结合盖斯定律,则 ,已知 、
,则 ,C正确;
D. 为催化剂,催化剂可降低反应的活化能,但不能改变焓变,D错误。
故选C。
14.(2023秋·北京·高三统考期末)环已烯是有机合成的重要中间体,可由环已烷氧
试卷第12页,共26页化脱氢制备。已知几种物质的燃烧热(25℃, ):
名称 氢气 环已烯 环已烷
化学式(状态)
下列说法正确的是A.氢气燃烧的热化学方程式为
B.由燃烧热可知,环已烯的能量小于环已烷的能量
C. (l)= (l)+H (g)
2
D.环已烷氧化脱氢制备环已烯时,氧气和高锰酸钾均可作氧化剂
【答案】C
【详解】A.燃烧热是在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出
的热量;氢气燃烧的热化学方程式为 ,
A错误;
B.等量的环已烯、环已烷燃烧耗氧量、生成水的量不同,由燃烧热不能判断环已烯的
能量小于环已烷的能量,B错误;
C.由燃烧热可知,①
②
③
由盖斯定律可知,③-①-②得: (l)= (l)+H (g) ,C正
2
确;
D.环已烯中含有碳碳双键,会被高锰酸钾氧化,D错误;
故选C。
15.(2023秋·北京西城·高三统考期末) 转化可减少 排放并实现资源利用。催化氧化乙烷制乙烯的主要反应有:
①:
②:
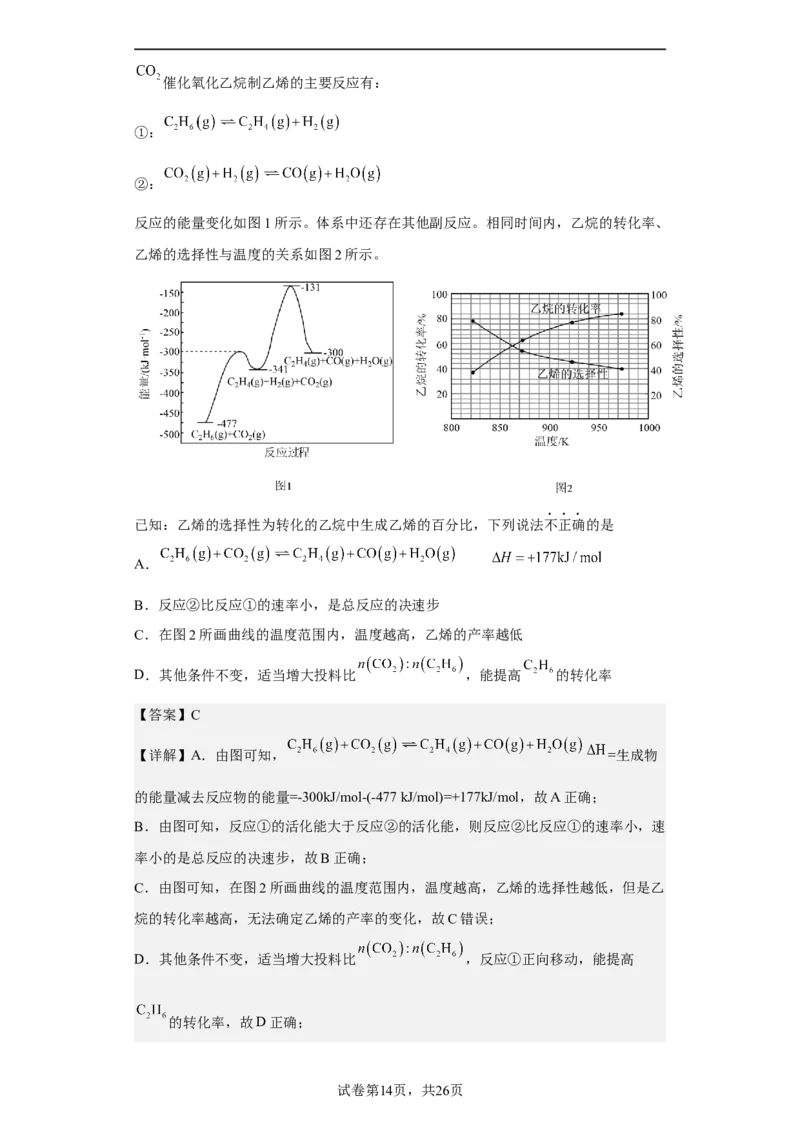
反应的能量变化如图1所示。体系中还存在其他副反应。相同时间内,乙烷的转化率、
乙烯的选择性与温度的关系如图2所示。
已知:乙烯的选择性为转化的乙烷中生成乙烯的百分比,下列说法不正确的是
A.
B.反应②比反应①的速率小,是总反应的决速步
C.在图2所画曲线的温度范围内,温度越高,乙烯的产率越低
D.其他条件不变,适当增大投料比 ,能提高 的转化率
【答案】C
【详解】A.由图可知, =生成物
的能量减去反应物的能量=-300kJ/mol-(-477 kJ/mol)=+177kJ/mol,故A正确;
B.由图可知,反应①的活化能大于反应②的活化能,则反应②比反应①的速率小,速
率小的是总反应的决速步,故B正确;
C.由图可知,在图2所画曲线的温度范围内,温度越高,乙烯的选择性越低,但是乙
烷的转化率越高,无法确定乙烯的产率的变化,故C错误;
D.其他条件不变,适当增大投料比 ,反应①正向移动,能提高
的转化率,故D正确;
试卷第14页,共26页故选C。
16.(2023秋·北京东城·高二汇文中学校考期末) 联合 和 制取 时,发
生的主要反应如下:
①
②
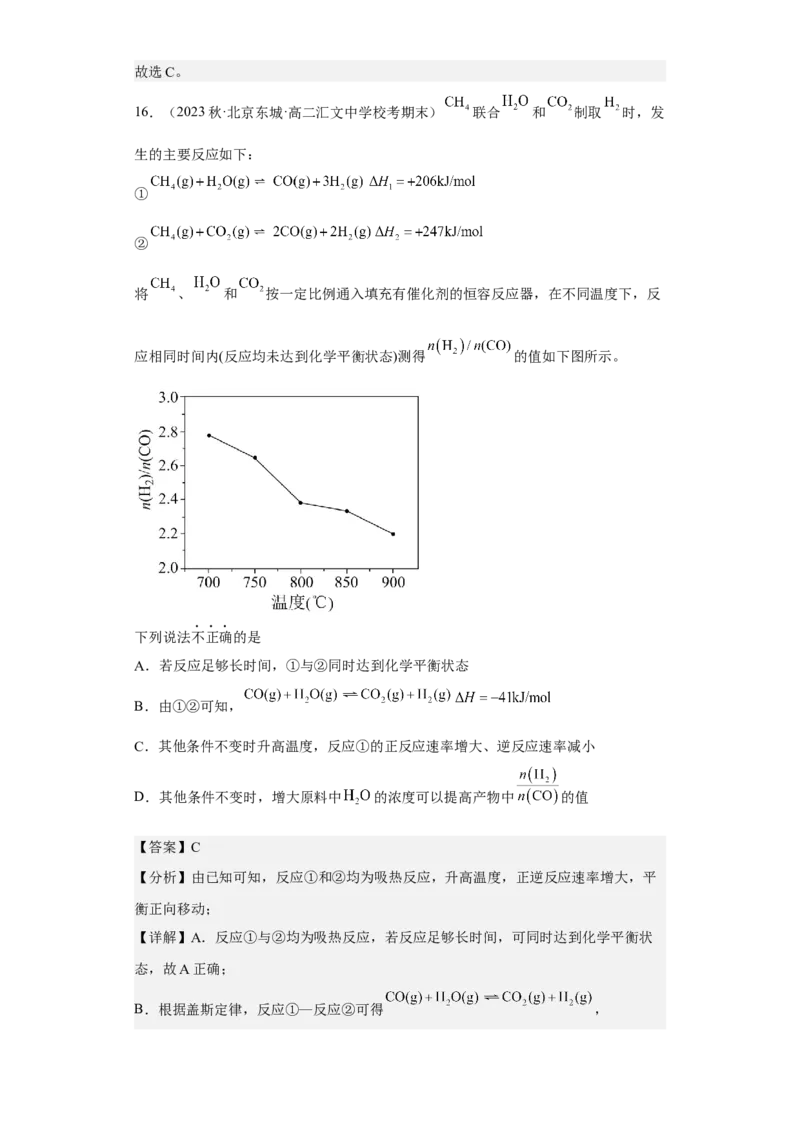
将 、 和 按一定比例通入填充有催化剂的恒容反应器,在不同温度下,反
应相同时间内(反应均未达到化学平衡状态)测得 的值如下图所示。
下列说法不正确的是
A.若反应足够长时间,①与②同时达到化学平衡状态
B.由①②可知,
C.其他条件不变时升高温度,反应①的正反应速率增大、逆反应速率减小
D.其他条件不变时,增大原料中 的浓度可以提高产物中 的值
【答案】C
【分析】由已知可知,反应①和②均为吸热反应,升高温度,正逆反应速率增大,平
衡正向移动;
【详解】A.反应①与②均为吸热反应,若反应足够长时间,可同时达到化学平衡状
态,故A正确;
B.根据盖斯定律,反应①—反应②可得 ,,故B正确;
C.其他条件不变时升高温度,反应①的正反应和逆反应速率均增大,故C错误;
D.其他条件不变时,增大原料中 的浓度, 转化率增大,根据反应①,生成
的氢气量增多,可以提高产物中 的值,故D正确;
故选C。
二、非选择题 (本题共5小题,1-3题每题10分,4-5题每题11分,共52分)
17.(2023秋·上海闵行·高二上海市七宝中学校考期末)环戊二烯( )重要的有机
合成中间体。一定条件下,存在以下转化:
反应①:
反应②:
反应③:
(1)反应①的 _______ 。
(2)反应③的化学平衡常数表达式 _______。
(3)在恒温恒容的容器中,当反应②达到化学平衡时,则下列一定正确的是_______。
a.气体分子数不变 b.
c. d.断裂 键的同时断裂 键
(4)恒温恒容时, 和 (g)发生反应③,测得平衡时容器内压强变
为起始的1.2倍,则环戊烯的转化率为_______。
(5)欲提高反应③的正反应速率,且K值不变,可采取的措施有_______(选填编号)。
a.通入 b.升高温度
c.提高环戊烯浓度 d.分离出
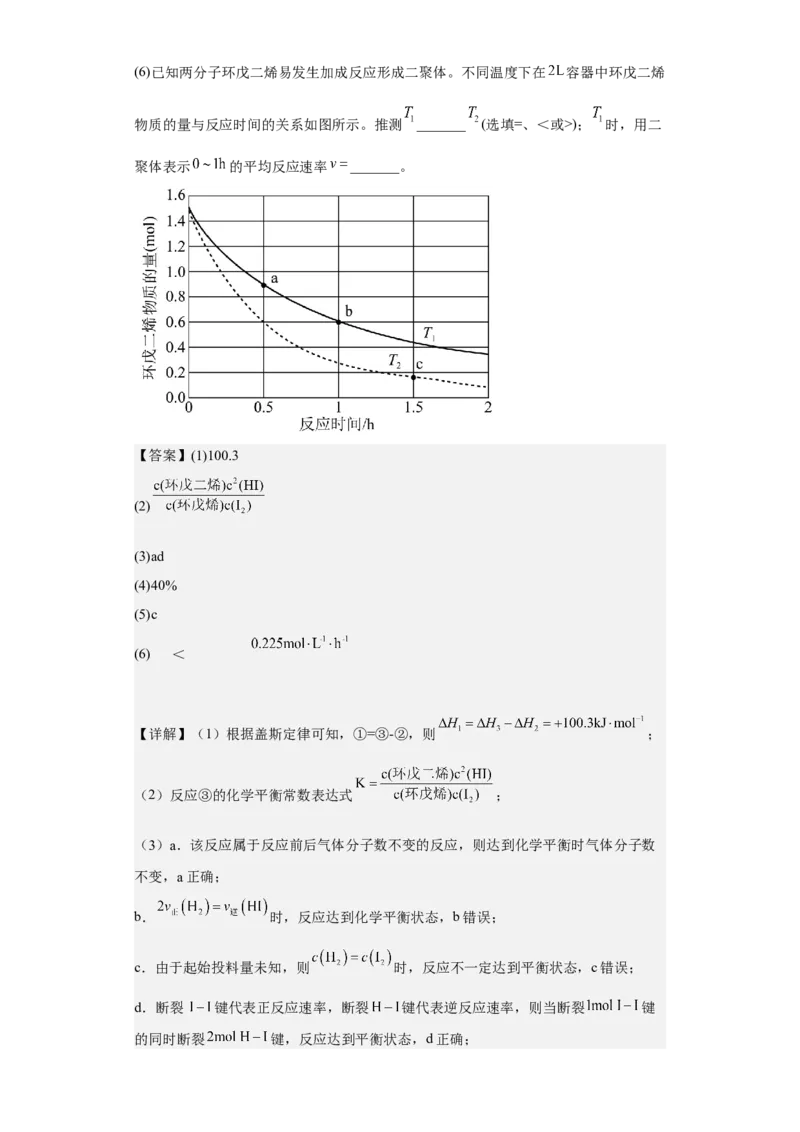
试卷第16页,共26页(6)已知两分子环戊二烯易发生加成反应形成二聚体。不同温度下在 容器中环戊二烯
物质的量与反应时间的关系如图所示。推测 _______ (选填=、<或>); 时,用二
聚体表示 的平均反应速率 _______。
【答案】(1)100.3
(2)
(3)ad
(4)40%
(5)c
(6) <
【详解】(1)根据盖斯定律可知,①=③-②,则 ;
(2)反应③的化学平衡常数表达式 ;
(3)a.该反应属于反应前后气体分子数不变的反应,则达到化学平衡时气体分子数
不变,a正确;
b. 时,反应达到化学平衡状态,b错误;
c.由于起始投料量未知,则 时,反应不一定达到平衡状态,c错误;
d.断裂 键代表正反应速率,断裂 键代表逆反应速率,则当断裂 键
的同时断裂 键,反应达到平衡状态,d正确;故选ad。
(4)设 变化xmol,根据题意列三段式有
恒温恒容下,压强之比等于物质的量之比,则 ,解得
x=0.2,环戊烯的转化率为 ;
(5)a.若是在恒温恒容条件下,通入惰性气体 ,各组分浓度不变,正逆反应
速率不变,若是在恒温恒压条件下,通入惰性气体 ,相当于增大容器体积,各
组分浓度均减小,正逆反应速率均减小,a不符合题意;
b.升高温度,平衡正向移动,K值增大,b不符合题意;
c.提高环戊烯浓度,即增大反应物浓度,加入反应物这一瞬间,正反应速率突然增大,
后逐渐减小,总的结果正反应速率增大,温度不变,K值不变,c符合题意;
d.分离出 ,即减小生成物的浓度,平衡正向移动,正反应速率减小,d不符合
题意;
故选c。
(6)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下2L溶液中
环戊二烯物质的量与反应时间的关系如图所示。b点时,0-1小时内环戊二烯的浓度变
化为: ,环戊二烯的二聚体的浓度为环戊二烯浓度变化的
,则b点时二聚体的浓度为 ,二聚体的生成速率v=
;温度越高反应速率越快,根据图示可知,在温度T
2
(虚线)的反应速率较大,则T<T。
1 2
18.(2023秋·甘肃武威·高二天祝藏族自治县第一中学校考期末)试回答下列问题:
试卷第18页,共26页i.
(1)实验测得,5 g甲醇( )液体在氧气中充分燃烧生成二氧化碳气体和液态水时
释放出113.5 kJ的热量,则表示甲醇燃烧热的热化学方程式为
__________________________________________.
(2)已知:
则 ______ 。
ii.二甲醚(DME)被誉为“21世纪的清洁燃料”,由合成气制备二甲醚的主要原理如下:
①
②
③
回答下列问题:
(3)反应 的 ______ ;
(4)下列措施中,能提高(1)中 产率的有______(填字母)。
A.使用过量的CO B.升高温度 C.增大压强
(5)已知某些化学键的键能数据如下表:
共价键 H—H Cl—Cl H—Cl
键能/( ) 436 247 434
则反应 的焓变 ______。
【答案】(1)
(2)>
(3)
(4)AC(5)
【详解】(1)1 mol 完全燃烧放出的热量为 kJ,反应的热
化学方程式为 ;
(2)甲醇的燃烧是放热反应,而对于放热反应,生成物及其聚集状态相同时,反应物
的能量越高,反应放出的热量越多.等物质的量的 的能量低于 ,
故2 mol 燃烧时放出的热量少于2 mol 燃烧放出的热量,而放热
反应的 ,故 ;
(3)根据盖斯定律可知,①×2+②+③得到
;
(4)为提高 的产率,应使平衡正向移动;A.使用过量的CO,平衡正向移
动, 产率增大,选项A符合;
B.升高温度,平衡向吸热反应的逆反应方向移动, 产率减小,选项B不符
合;
C.增大压强,平衡向气体体积缩小的正反应方向移动, 产率增大,选项C
符合;
答案选AC;
(5) 反应物总键能-生成物总键能,则该反应的
。
19.(2023秋·山东泰安·高二校考期末)氮氧化物的排放是造成大气污染的原因之一,
消除氮氧化物的污染对生态文明建设具有重要意义,回答下列问题:
(1)①
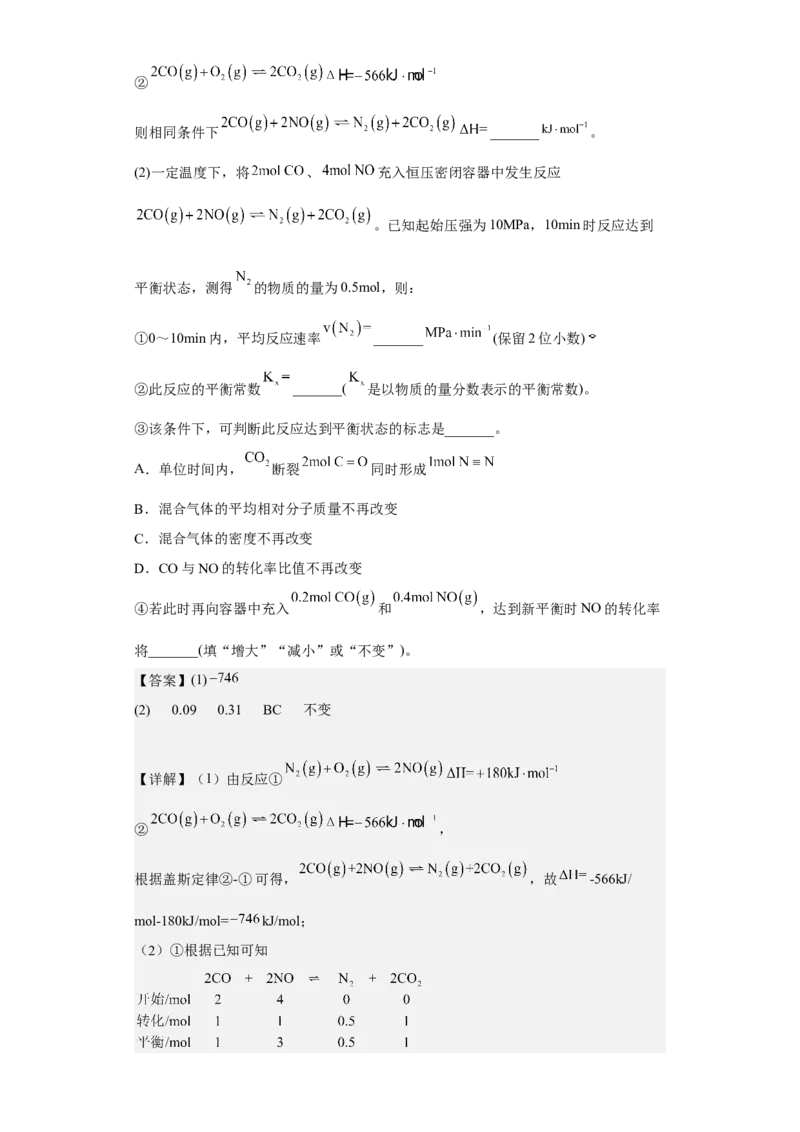
试卷第20页,共26页②
则相同条件下 _______ 。
(2)一定温度下,将 、 充入恒压密闭容器中发生反应
。已知起始压强为10MPa,10min时反应达到
平衡状态,测得 的物质的量为0.5mol,则:
①0~10min内,平均反应速率 _______ (保留2位小数)
②此反应的平衡常数 _______( 是以物质的量分数表示的平衡常数)。
③该条件下,可判断此反应达到平衡状态的标志是_______。
A.单位时间内, 断裂 同时形成
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.CO与NO的转化率比值不再改变
④若此时再向容器中充入 和 ,达到新平衡时NO的转化率
将_______(填“增大”“减小”或“不变”)。
【答案】(1)
(2) 0.09 0.31 BC 不变
【详解】(1)由反应①
② ,
根据盖斯定律②-①可得, ,故 -566kJ/
mol-180kJ/mol= kJ/mol;
(2)①根据已知可知的压强的变化为 ×10MPa≈0.9MPa,故0~10min内,平均反应速率
0.09 ;
②此反应的平衡常数 ≈0.31;
③A.单位时间内,断裂2molC=O同时形成 ,正反应速率和逆反应速率不相
等,不能说明达到平衡,选项A错误;
B.该反应是气体分子数不相等的反应,混合气体的平均相对分子质量不再改变,可以
说明达到平衡,选项B正确;
C.容器是恒压容器,反应是气体分子数不相等的反应,混合气体的密度不再改变可以
说明达到平衡,选项C正确;
D.CO与NO的转化量相等,设任一时刻转化量为amol,则CO与NO的转化率比值为
=2,始终为定值,则CO与NO的转化率比值不再改变,不能说明反应达到平衡,
选项D错误;
故答案为:BC;
④恒温恒压条件下,向容器中充入 和 ,与原平衡通入的反
应物的比值相同,属于等比等效平衡,故转化率不变。
20.(2023秋·新疆乌鲁木齐·高二乌市八中校考期末)I.以H 合成尿素CO(NH) 的有
2 2 2
关热化学方程式有:
①N(g)+3H(g)=2NH (g) ΔH=-92.4 kJ·mol-1
2 2 3 1
②NH (g)+ CO(g)= NH CONH (s) ΔH=-79.7 kJ·mol-1
3 2 2 2 4 2
③NH CONH (s)=CO(NH )(s)+HO(l) ΔH=+72.5 kJ·mol-1
2 2 4 2 2 2 3
(1)则N(g)、H(g)与CO(g)反应生成CO(NH)(s)和HO(l)的热化学方程式为_______。
2 2 2 2 2 2
II.一定条件下,在容积为5L的密闭容器中,发生反应A(g)+2B(g) 2C(g),已知达平
衡后,降低温度,A的体积分数减小。
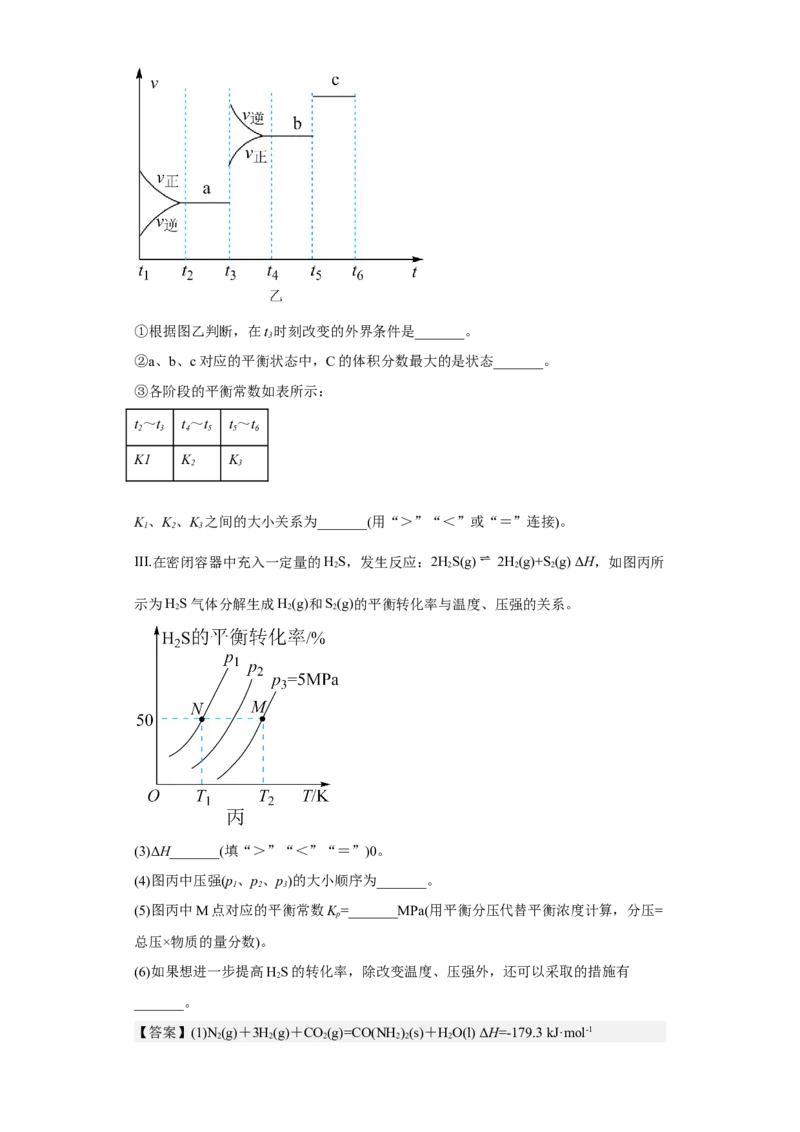
(2)该反应的反应速率v随时间t的关系如图乙所示。
试卷第22页,共26页①根据图乙判断,在t 时刻改变的外界条件是_______。
3
②a、b、c对应的平衡状态中,C的体积分数最大的是状态_______。
③各阶段的平衡常数如表所示:
t~t t~t t~t
2 3 4 5 5 6
K1 K K
2 3
K 、K 、K 之间的大小关系为_______(用“>”“<”或“=”连接)。
1 2 3
III.在密闭容器中充入一定量的HS,发生反应:2HS(g) 2H(g)+S (g) ΔH,如图丙所
2 2 2 2
示为HS气体分解生成H(g)和S(g)的平衡转化率与温度、压强的关系。
2 2 2
(3)ΔH_______(填“>”“<”“=”)0。
(4)图丙中压强(p、p、p)的大小顺序为_______。
1 2 3
(5)图丙中M点对应的平衡常数K =_______MPa(用平衡分压代替平衡浓度计算,分压=
p
总压×物质的量分数)。
(6)如果想进一步提高HS的转化率,除改变温度、压强外,还可以采取的措施有
2
_______。
【答案】(1)N (g)+3H(g)+CO(g)=CO(NH )(s)+HO(l) ΔH=-179.3 kJ·mol-1
2 2 2 2 2 2(2) 升高温度 a K >K =K
1 2 3
(3)>
(4)p>p>p
3 2 1
(5)1
(6)及时分离出产物
【详解】(1)已知反应①N(g)+3H(g)=2NH (g) ΔH=-92.4 kJ·mol-1;反应②NH (g)
2 2 3 1 3
+ CO(g)= NH CONH (s) ΔH=-79.7 kJ·mol-1;反应③NH CONH (s)=CO(NH )(s)
2 2 2 4 2 2 2 4 2 2
+HO(l) ΔH=+72.5 kJ·mol-1;N(g)、H(g)与CO(g)反应生成CO(NH)(s)和HO(l)的
2 3 2 2 2 2 2 2
化学方程式为N(g)+3H(g)+CO(g)=CO(NH )(s)+HO(l),根据盖斯定律可知,由
2 2 2 2 2 2
①+2×②+③可得目标方程式,则ΔH=-92.4 kJ·mol-1+2×(-79.7 kJ·mol-1) +72.5 kJ·mol-1-
179.3 kJ·mol-1,故热化学方程式为N(g)+3H(g)+CO(g)=CO(NH )(s)+HO(l) ΔH=
2 2 2 2 2 2
-179.3 kJ·mol-1。
(2)①降低温度,A的体积分数减小,即降温平衡正向移动,则正反应为放热反应,
在t 时刻,正逆反应速率瞬间均增大,则可能为升温或加压,逆反应速率大于正反应
3
速率,平衡逆向移动,而加压平衡正向移动,升温平衡逆向移动,故改变的外界条件
是升高温度。
②在t 时刻改变条件,平衡逆向移动,C的体积分数减小,t 时刻改变条件,正逆反应
3 5
速率相等,平衡不移动,则 a、b、c对应的平衡状态中,C的体积分数最大的是状态
a。
③平衡常数只与温度有关,t 时刻升温,升温平衡逆向移动,平衡常数减小,则K >
3 1
K ,t 时刻,平衡不移动,应该是加入的催化剂,平衡常数不变,则K =K ,故K 、
2 5 2 3 1
K 、K 之间的大小关系为K >K =K 。
2 3 1 2 3
(3)随温度升高,HS的平衡转化率增大,即升温平衡正向移动,则正反应为吸热反
2
应,ΔH>0。
(4)该反应的正反应为气体物质的量增大的反应,减压平衡正向移动,HS的平衡转
2
化率增大,则图丙中压强(p、p、p)的大小顺序为p>p>p。
1 2 3 3 2 1
(5)M点HS的平衡转化率为50%,设起始时HS的物质的量为1mol,则转化量为
2 2
0.5mol,平衡时剩余0.5mol,生成0.5molH,0.25mol S ,各气体的分压为:
2 2
、 、
试卷第24页,共26页,则图丙中M点对应的平衡常数
。
(6)如果想进一步提高HS的转化率,除改变温度、压强外,还可以采取的措施有及
2
时分离出产物,减小生成物浓度,平衡正向移动。
21.(2023秋·湖南长沙·高三统考期末)2021年中国政府工作报告中提出碳中和目标:
在2030年前达到最高值,2060年前达到碳中和。因此对二氧化碳的综合利用显得尤为
重要。
(1)通过电解的方式可实现对二氧化碳的综合利用。2022年7月香港中文大学王莹教授
研发新型电解槽实现二氧化碳回收转化效率达到60%以上。
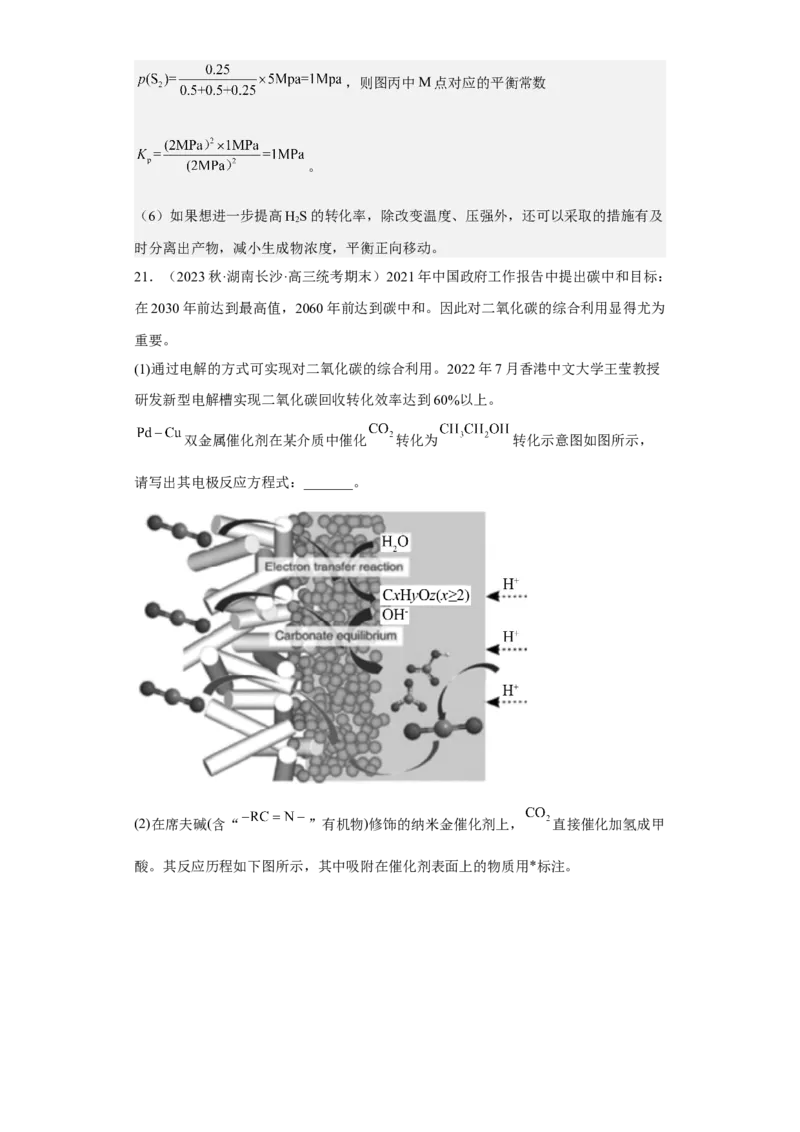
双金属催化剂在某介质中催化 转化为 转化示意图如图所示,
请写出其电极反应方程式:_______。
(2)在席夫碱(含“ ”有机物)修饰的纳米金催化剂上, 直接催化加氢成甲
酸。其反应历程如下图所示,其中吸附在催化剂表面上的物质用*标注。该历程中起决速步骤的化学方程式是_______;
(3)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚 (CHOCH )也有广
3 3
泛的应用。
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
① _______
②起始压强为4.0MPa、恒压条件下,通入氢气和二氧化碳的 的情况下,不
同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
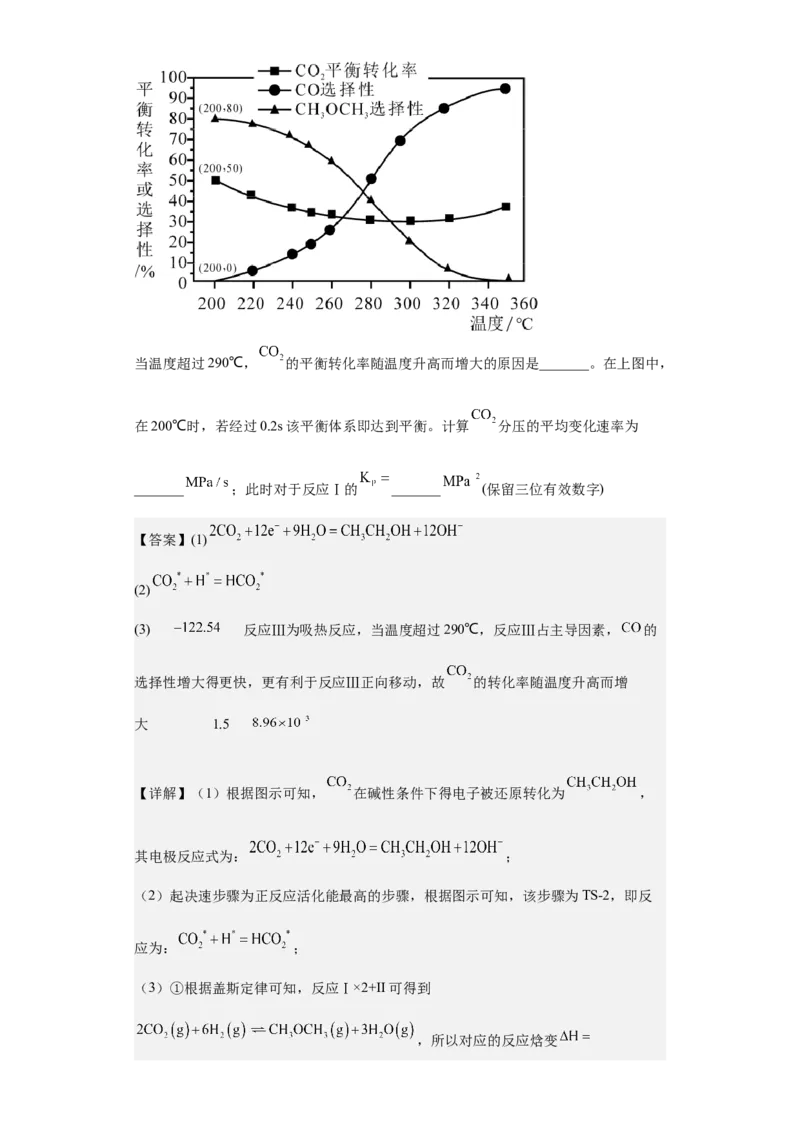
消耗总量的百分比)如下图所示:
试卷第26页,共26页当温度超过290℃, 的平衡转化率随温度升高而增大的原因是_______。在上图中,
在200℃时,若经过0.2s该平衡体系即达到平衡。计算 分压的平均变化速率为
_______ ;此时对于反应Ⅰ的 _______ (保留三位有效数字)
【答案】(1)
(2)
(3) 反应Ⅲ为吸热反应,当温度超过290℃,反应Ⅲ占主导因素, 的
选择性增大得更快,更有利于反应Ⅲ正向移动,故 的转化率随温度升高而增
大 1.5
【详解】(1)根据图示可知, 在碱性条件下得电子被还原转化为 ,
其电极反应式为: ;
(2)起决速步骤为正反应活化能最高的步骤,根据图示可知,该步骤为TS-2,即反
应为: ;
(3)①根据盖斯定律可知,反应Ⅰ×2+II可得到
,所以对应的反应焓变= ;
②反应Ⅲ为吸热反应,当温度超过290℃,反应Ⅲ占主导因素, 的选择性增大得更
快,更有利于反应Ⅲ正向移动,故 的转化率随温度升高而增大;
设起始 为 , 的起始分压 , 的平衡转化率50%,
则转化的 为 ,二甲醚的选择性为80%,则说明有 的 转化为二甲
醚。 的起始分压为 ,达平衡时分压为 ,则
, 分压的平均变化速率:
;
,则反应达到平衡后各物质的
物质的量分别为n(CO)=(1-0.5)mol=0.5mol,n(H )=(4-3×0.5)mol=2.5mol,
2 2
n(CHOH)=(0.5-0.5×80%)mol=0.1mol,n(CHOCH )=( )mol=0.2mol,
3 3 3
n(H O)= (0.5+ )mol=0.7mol,总气体的物质的量
2
,所以反应I的Kp= =
MPa。
试卷第28页,共26页