文档内容
专题九 化学实验(能力提升检测卷)
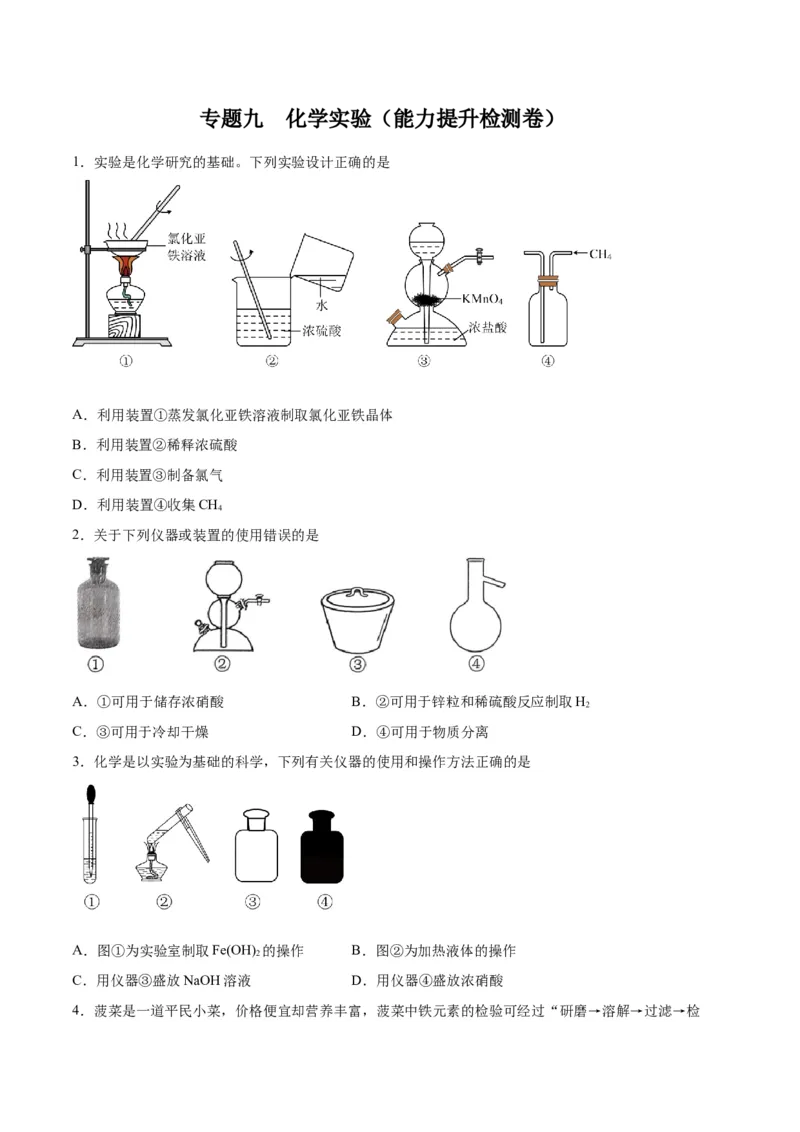
1.实验是化学研究的基础。下列实验设计正确的是
A.利用装置①蒸发氯化亚铁溶液制取氯化亚铁晶体
B.利用装置②稀释浓硫酸
C.利用装置③制备氯气
D.利用装置④收集CH
4
2.关于下列仪器或装置的使用错误的是
A.①可用于储存浓硝酸 B.②可用于锌粒和稀硫酸反应制取H
2
C.③可用于冷却干燥 D.④可用于物质分离
3.化学是以实验为基础的科学,下列有关仪器的使用和操作方法正确的是
A.图①为实验室制取Fe(OH) 的操作 B.图②为加热液体的操作
2
C.用仪器③盛放NaOH溶液 D.用仪器④盛放浓硝酸
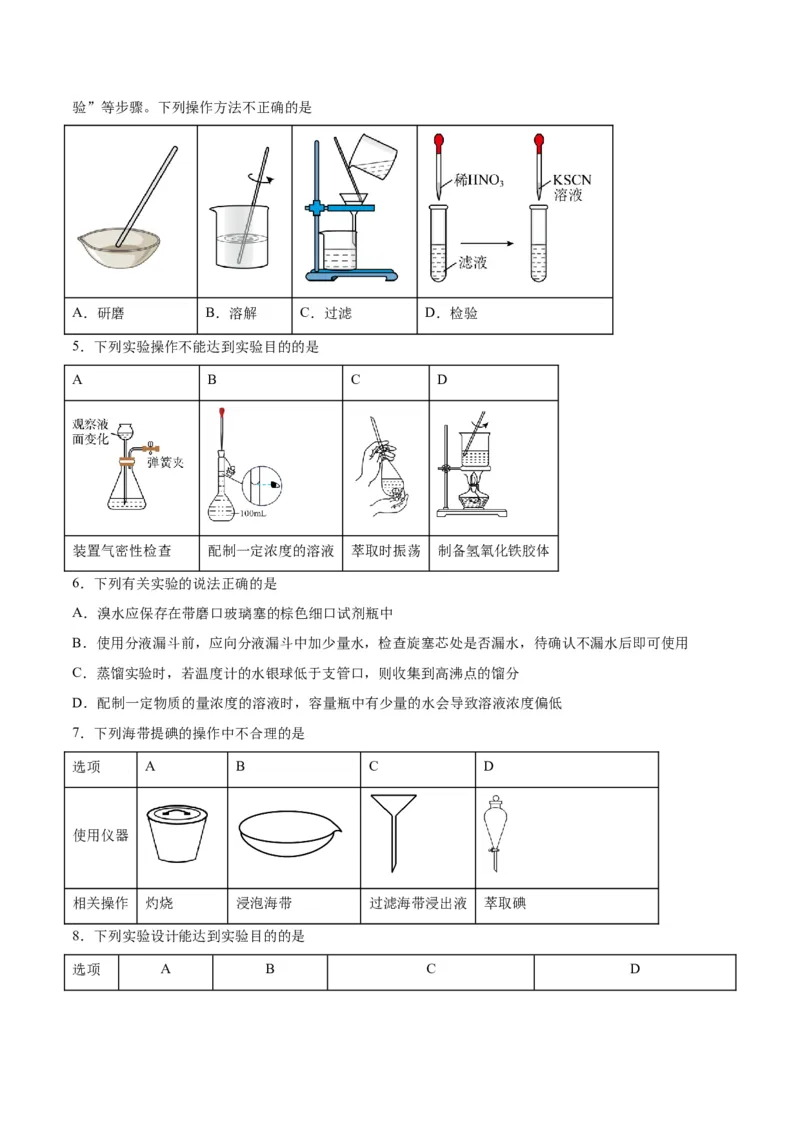
4.菠菜是一道平民小菜,价格便宜却营养丰富,菠菜中铁元素的检验可经过“研磨→溶解→过滤→检验”等步骤。下列操作方法不正确的是
A.研磨 B.溶解 C.过滤 D.检验
5.下列实验操作不能达到实验目的的是
A B C D
装置气密性检查 配制一定浓度的溶液 萃取时振荡 制备氢氧化铁胶体
6.下列有关实验的说法正确的是
A.溴水应保存在带磨口玻璃塞的棕色细口试剂瓶中
B.使用分液漏斗前,应向分液漏斗中加少量水,检查旋塞芯处是否漏水,待确认不漏水后即可使用
C.蒸馏实验时,若温度计的水银球低于支管口,则收集到高沸点的馏分
D.配制一定物质的量浓度的溶液时,容量瓶中有少量的水会导致溶液浓度偏低
7.下列海带提碘的操作中不合理的是
选项 A B C D
使用仪器
相关操作 灼烧 浸泡海带 过滤海带浸出液 萃取碘
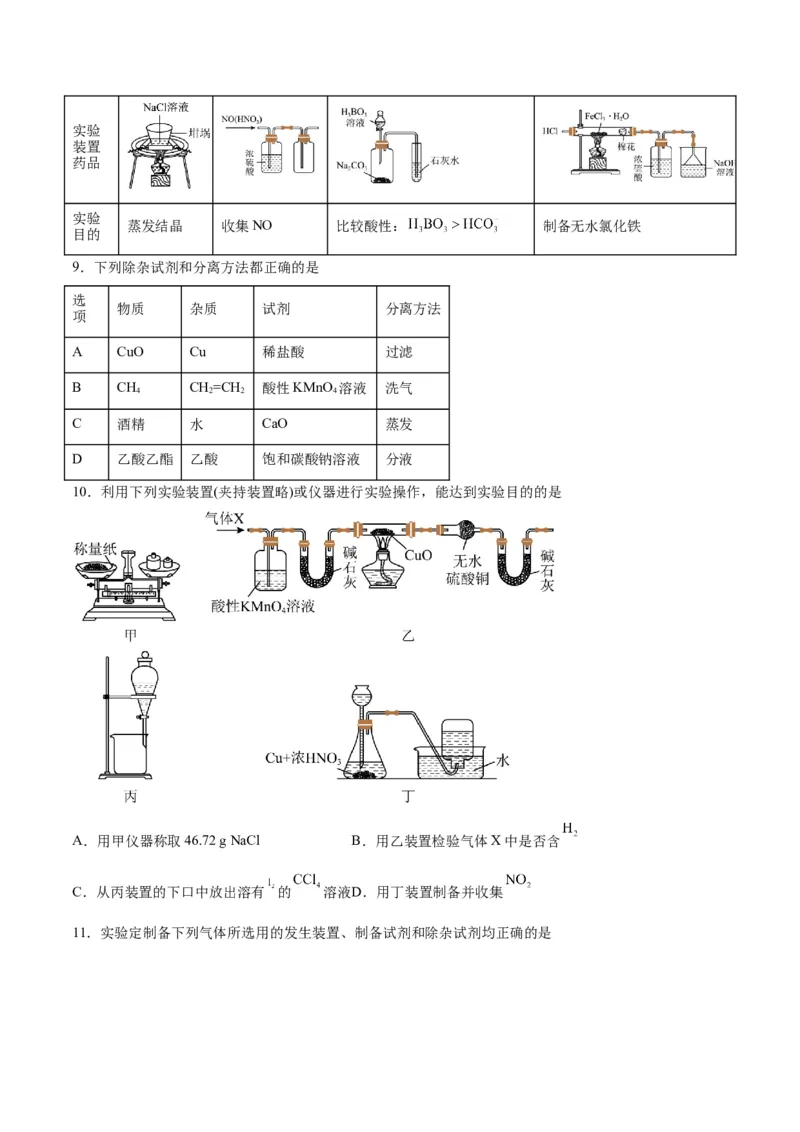
8.下列实验设计能达到实验目的的是
选项 A B C D实验
装置
药品
实验
蒸发结晶 收集NO 比较酸性: 制备无水氯化铁
目的
9.下列除杂试剂和分离方法都正确的是
选
物质 杂质 试剂 分离方法
项
A CuO Cu 稀盐酸 过滤
B CH CH=CH 酸性KMnO 溶液 洗气
4 2 2 4
C 酒精 水 CaO 蒸发
D 乙酸乙酯 乙酸 饱和碳酸钠溶液 分液
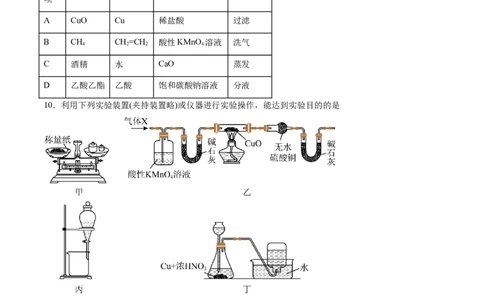
10.利用下列实验装置(夹持装置略)或仪器进行实验操作,能达到实验目的的是
A.用甲仪器称取46.72 g NaCl B.用乙装置检验气体X中是否含
C.从丙装置的下口中放出溶有 的 溶液D.用丁装置制备并收集
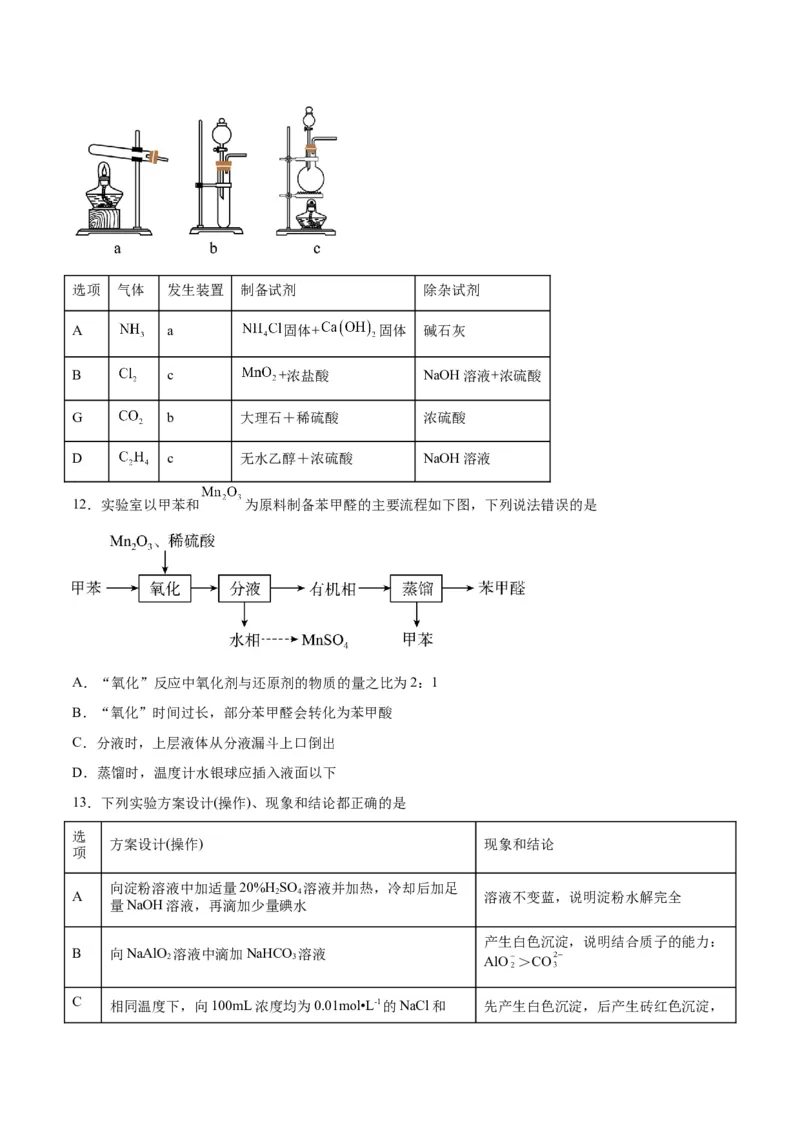
11.实验定制备下列气体所选用的发生装置、制备试剂和除杂试剂均正确的是选项 气体 发生装置 制备试剂 除杂试剂
A a 固体+ 固体 碱石灰
B c +浓盐酸 NaOH溶液+浓硫酸
G b 大理石+稀硫酸 浓硫酸
D c 无水乙醇+浓硫酸 NaOH溶液
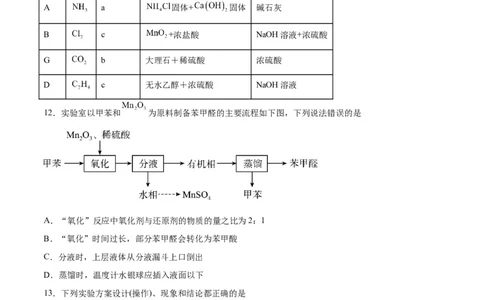
12.实验室以甲苯和 为原料制备苯甲醛的主要流程如下图,下列说法错误的是
A.“氧化”反应中氧化剂与还原剂的物质的量之比为2:1
B.“氧化”时间过长,部分苯甲醛会转化为苯甲酸
C.分液时,上层液体从分液漏斗上口倒出
D.蒸馏时,温度计水银球应插入液面以下
13.下列实验方案设计(操作)、现象和结论都正确的是
选
方案设计(操作) 现象和结论
项
向淀粉溶液中加适量20%H SO 溶液并加热,冷却后加足
A 2 4 溶液不变蓝,说明淀粉水解完全
量NaOH溶液,再滴加少量碘水
产生白色沉淀,说明结合质子的能力:
B 向NaAlO 溶液中滴加NaHCO 溶液
2 3 AlO >CO
C 相同温度下,向100mL浓度均为0.01mol•L-1的NaCl和 先产生白色沉淀,后产生砖红色沉淀,NaCrO 混合液中滴加0.01mol•L-1AgNO 溶液 说明K (AgCl)<K (Ag CrO)
2 4 3 sp sp 2 4
D 向Ba(NO ) 溶液中通入适量的SO 产生白色沉淀,该沉淀为BaSO
3 2 2 3
14.实验室通过对市售85%磷酸溶液进行减压蒸馏除水、结晶除杂得到纯磷酸晶体,实验装置如图。
已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成 (熔点为30℃),高于100℃则发生
分子间脱水生成焦磷酸。
下列实验装置和操作不能达到实验目的的是
A.图甲中使用的 、浓硫酸、 的目的均为干燥气体
B.向图乙得到的过饱和磷酸溶液中加入磷酸晶体,可以促进其结晶
C.图丙中冷凝管的进水口是b,具支烧瓶中得到磷酸溶液
D.磷酸中少量的水极难除去的原因是磷酸可与水分子间形成氢键
15.实验室以BaS为原料制备 晶体,装置如图所示。下列说法错误的是
A.a的作用是防倒吸
B.根据实验可得酸性顺序:
C.丙既可吸收尾气又可判断反应是否完全D.乙中所得溶液经蒸发浓缩、冷却结晶、过滤得产品
16.由下列实验操作及现象所得结论或解释正确的是
选
实验操作 现象 结论或解释
项
向5mL0.1mol·L-1KI溶液中加入10mL0.01mol·L-1FeCl 溶液,充分 I-与Fe3+的反应是
A 3 溶液变红
反应后滴加KSCN溶液 可逆反应
前者大于
B 常温下,测定等浓度NaHCO 溶液和NaHSO 溶液的pH 非金属性S>C
3 3 后者
原溶液中一定含有
C 将某溶液滴在KI一淀粉试纸上 试纸变蓝
Cl
2
产生白色
D 向蛋白质溶液中加入醋酸铅溶液 蛋白质发生了盐析
沉淀
17.氧钒(IV)碱式碳酸铵化学式为(NH )[(VO) (CO)(OH) ]•10H O,它是制备热敏材料VO 的原料,已知
4 5 6 3 4 9 2 2
VO2+在酸性条件下易被氧化,氧钒(IV)碱式碳酸铵的制备流程如图:
回答下列问题:
(1)步骤一盐酸不宜过量,原因可能 ;生成VOCl 的同时,还生成一种无色无污染的气体,该反应
2
的化学方程式为 。
(2)步骤二可在如图装置中进行。
①接口的连接顺序为a→ 。
②实验开始时,先关闭K,打开K,当 时(写实验现象),再关闭K,打开K,充分反应,静置,
2 1 1 2
得到固体。
(3)测定产品纯度称取mg样品用稀硫酸溶解后,加入50.0mL0.02mol•L-1KMnO 溶液,VO2+转化成VO ,向反应后溶液中滴
4
加0.025mol•L-1NaSO 标准液,至剩余的KMnO 溶液恰好反应完全,消耗NaSO 标准液40.00mL。
2 3 4 2 3
①滴定至反应终点的现象为 ;
②样品中氧钒(IV)碱式碳酸铵(摩尔质量为Mg•mol-1)的质量分数为 %;
③下列情况会导致产品纯度偏大的是 (填标号)。
A.NaSO 溶液部分变质
2 3
B.滴定达终点时,俯视刻度线读数
C.用标准液润洗滴定管后,液体从上口倒出
D.滴定达终点时,发现滴定管尖嘴内有气泡生成
18.苯氧乙酸为除草剂的中间体。制备苯氧乙酸的反应原理和装置(夹持仪器已省略)如图所示。相关物理
数据如下表。
副反应:ClCH COOH+2NaOH HOCH COONa+NaCl+H O
2 2 2
相对分子质量 熔点/℃ 沸点/℃ 溶解性
苯酚 94 43 181.75 易溶于热水,易溶于乙醇
苯氧乙酸 152 89~100 285 易溶于热水,不溶于冷水,溶于乙醇
氯乙酸 94.5 63 189 易溶于水, 溶于乙醇
羟基乙酸 76 79~80 分解 易溶于水, 易溶于乙醇
具体实验步骤如下:
Ⅰ、将 3.8g氯乙酸和5mL水加入100mL的仪器X中,开启搅拌器,缓慢加入7mL饱和碳酸钠溶液至溶液pH 为 7~8。
Ⅱ、加入2.35g 苯酚, 再滴加 35%氢氧化钠溶液至反应溶液pH为12,将反应物在沸水浴中加热
30min。
Ⅲ、反应过程中溶液pH下降,补充氢氧化钠使pH保持为12,在沸水浴中继续加热15min。
Ⅳ、反应结束,将溶液转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为3~4。
Ⅴ、冰水浴中冷却析出晶体,抽滤,冷水洗涤产物3次,在60~65℃下干燥得到黄色产品,再加入活性
炭,得到2.47g白色晶体。
请回答下列问题:
(1)仪器X的名称是 。
(2)球形冷凝管中冷水由 (填“a”或“b”) 口流进, 与直形冷凝管相比,其优点是 。
(3)步骤Ⅰ中用饱和碳酸钠溶液将pH调至7~8的原因: 。
(4)写出反应③的化学方程式: 。
(5)步骤Ⅳ用浓盐酸酸化至pH为3~4,其目的是 。
(6)步骤Ⅴ中,抽滤装置如图所示,采用“抽滤”的优点是 。
(7)步骤Ⅴ中加活性炭的目的是 。
(8)该过程中苯氧乙酸的产率为 。
19.某小组同学用银氨溶液制备银镜,并探究反应后银镜的处理方法。
Ⅰ.银镜的制备
(1)配制银氨溶液时,随着氨水滴加到硝酸银溶液中,观察到先产生棕黄色沉淀,然后沉淀消失,形成无色
透明的溶液。该过程中发生的反应有:
a.AgNO+NH•H O=AgOH↓+NH NO
3 3 2 4 3
b.AgOH+2NH •H O反应
3 2
c.2AgOH(白色沉淀)=Ag O(棕黑色沉淀)+H O
2 2
d. (补全d的反应)。
(2)写出乙醛与银氨溶液反应的化学方程式 。
(3)该小组探究银镜反应的最佳条件,部分实验数据如表:
实验序
银氨溶液/mL 乙醛/滴 水浴温度/℃ 出现银镜时间/min
号
1 1 3 65 5
2 1 5 65 t
3 1 3 50 64 1 a 50 0.5
①推测当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为60℃,出现银镜的时间范围是 。
②推测实验2中的t 5min(填“大于”、“小于”或“等于”)。
③a为3滴等浓度的葡萄糖溶液。对比实验3和4,可以得出 (从结构和性质角度作答)。
Ⅱ.银镜的处理
(4)取一支附有银镜的试管,加入2mL稀硝酸,银镜较快溶解,有气泡产生,该反应的离子方程式为
。
(5)在两支含等量银镜的试管中分别加入2mL1mol•L-1FeCl 和Fe(NO ) 溶液,充分振荡,两支试管中均发生
3 3 3
不同程度的溶解,前者银镜溶解的量明显多于后者,且前者有灰色沉淀生成。结合化学用语解释FeCl 比
3
Fe(NO ) 溶液溶解银镜效果好的原因 。
3 3
(6)取一支含银镜的试管,加入5mL10%H O 溶液,振荡,发生剧烈反应,产生大量气泡,银镜在气泡的影
2 2
响下呈颗粒状逐渐脱离试管内壁,并沉积在试管底部。结合实验现象,小组同学认为Ag催化HO 分解,
2 2
该过程分为两步:
i.2Ag+H O=Ag O+HO
2 2 2 2
ii. (补全ii的反应)。
进一步实验证实了该过程。
(7)反思:根据上述实验,清洗银镜首选试剂是HO 溶液,选择的依据是 (写出两条)。
2 2
20.硫代硫酸钠( Na SO)俗称海波,广泛应用于照相定影及纺织业等领域。某实验小组制备硫代硫酸钠并
2 2 3
探究其性质。
Ⅰ.硫代硫酸钠的制备
实验小组设计如下装置制备硫代硫酸钠
信息:NaSO,中S元素的化合价分别为-2和+6
2 2 3
(1)仪器a的名称是 。B中发生的化学反应方程式为 (该反应理论上钠元素的利用率为100%)。
Ⅱ.产品纯度的测定
①溶液配制:准确称取该硫代硫酸钠样品8. 000 g,配制成50. 00 mL溶液。
②滴定:向锥形瓶中加入20. 00 mL 0.10 mol·L-1KIO 溶液,加入过量KI溶液和HSO 溶液,然后加入淀粉
3 2 4
作指示剂,用硫代硫酸钠样品溶液滴定碘单质,发生反应: I+2 =2I-+
2
(2)生成碘单质的离子方程式为 。滴定终点现象为 , 消耗样品溶液25. 00 mL,则
样品纯度为 %。
Ⅲ.硫代硫酸钠性质的探究
①取NaSO 晶体,溶解,配成0. 20 mol·L-1溶液。
2 2 3
②取4mL溶液,向其中加入1.0mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑浊物为S。
实验小组研究S产生的原因,提出了以下假设:
假设1:氧化剂氧化:Cl、HClO等含氯的氧化性微粒氧化了-2价硫元素。
2
假设2:___________ ( 不考虑空气中氧气氧化)。
设计实验方案:
胶头滴管 现象
第①
1.0 mL饱和氯水 立即出现浑浊
组
第②
___________ 一段时间后出现浑浊,且浑浊度比①组小
组
(3)假设2是 。
(4)第②组实验中胶头滴管加入的试剂是 。
(5)依据现象,S产生的主要原因是 。
(6)结合Ⅱ、Ⅲ分析纯度较低的原因是 。