文档内容
专题二 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
Ca 40 Cr 52 Mn 55 Fe 56 Ni 59 Cu 64 La 139
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.在同温同压下,相同体积的甲、乙两种气体的质量比是17∶14。若乙气体是CO,则甲气体可能是( )
A.HS B.HCl
2
C.NH D.Cl
3 2
【答案】A
【解析】同温同压下,体积之比等于物质的量之比,同体积的甲、乙两种气体物质的量相同,质量比
是17∶14,根据m=nM可知,甲与乙的摩尔质量之比为17∶14,若乙气体是CO,则M(甲)∶28 g·mol-1=
17∶14,故M(甲)=34 g·mol-1,各选项中只有HS符合,故选A。
2
2.同温同压下,A容器中盛有H,B容器中盛有NH,若使它们所含的原子数相等,则两个容器的容积之
2 3
比是( )
A.2∶1 B.1∶5
C.2∶3 D.5∶1
【答案】A
【解析】假设二者物质的量分别为 x mol和y mol,则H 含2x mol原子,NH 含4y mol原子,有2x=
2 3
4y,x∶y=2∶1,同温同压下体积比也为2∶1。
3.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1 L 0.1 mol·L-1 NaClO溶液中含有ClO-的数目为0.1N
A
B.将1 mol NH 完全溶于水,所得溶液中N(NH ·H O)+N(NH)=N
3 3 2 A
C.1 L 0.1 mol·L-1 NaHSO 溶液中含有的阳离子数目为0.1N
4 A
D.将1 mol CH COONa溶于稀醋酸中使溶液呈中性,溶液中含CHCOO-数目为N
3 3 A
【答案】D
【解析】1 L 0.1 mol·L-1 NaClO溶液中,ClO-水解,因此含有ClO-的数目小于0.1N ,故A错误;氨
A
气溶于水是可逆反应,因此所得溶液中N(NH )+N(NH ·H O)+N(NH)=N ,故B错误;1 L 0.1 mol·L-1
3 3 2 A
NaHSO 溶液中,NaHSO 电离出钠离子和氢离子,因此含有的阳离子数目大于0.1N ,故C错误;将1 mol
4 4 A
CHCOONa溶于稀醋酸中使溶液呈中性,根据电荷守恒和溶液呈中性得到溶液中含CHCOO-数目为N ,
3 3 A故D正确。
4.已知N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.15.6 g Na O 中离子总数为0.6N
2 2 A
B.2.8 L臭氧含有的质子数为3N
A
C.一定条件下,1 mol N 与4 mol H 反应生成的NH 分子数为2N
2 2 3 A
D.1 L 0.1 mol·L-1CHCOOH溶液中H+数为0.1N
3 A
【答案】A
【解析】NaO 由Na+和O构成,15.6 g Na O 的物质的量为=0.2 mol,离子总数为0.6N ,A正确;根
2 2 2 2 A
据题给条件无法计算臭氧的物质的量,B错误;氮气和氢气合成氨为可逆反应,因此1 mol N 与4 mol H
2 2
反应生成的NH 分子数小于2N ,C错误;CHCOOH为一元弱酸,部分电离,1 L 0.1 mol·L-1 CHCOOH
3 A 3 3
溶液中H+数小于0.1N ,D错误。
A
5.中美科学家在银表面首次获得了二维结构的硼烯,该科研成果发表在顶级期刊《Science》上,并获得重
点推荐。二维结构的硼烯如图所示,下列说法错误的是( )
A.1 mol硼原子核外电子数为3N
A
B.1 mol BF 分子中共价键的数目为3N
3 A
C.1 mol NaBH 与水反应转移的电子数为4N
4 A
D.硼烯有望代替石墨烯作“硼烯—钠基”电池的负极材料
【答案】A
【解析】硼原子核外有5个电子,1 mol硼原子核外电子数为5N ,A错误;BF 的结构式为 ,1 mol
A 3
BF 分子中共价键的数目为3N ,B正确;NaBH 与水生成氢气,氢元素化合价由-1价升高为0价,1 mol
3 A 4
NaBH 反应转移的电子数为4N ,C正确;硼烯具有导电性,有望代替石墨烯作“硼烯—钠基”电池的负极材料,
4 A
D正确。
6.设N 为阿伏加德罗常数的值,下列对0.3 mol·L-1KSO 溶液的叙述正确的是( )
A 2 4
A.1 L溶液中含有0.3N 个K+
A
B.1 L溶液中含有K+和SO的总数为0.9N
AC.2 L溶液中K+的浓度为1.2 mol·L-1
D.将0.3 mol硫酸钾溶于1 L水中,所得硫酸钾溶液的浓度为0.3 mol·L-1
【答案】B
【解析】0.3 mol·L-1 KSO 溶液中,c(K+)=0.6 mol·L-1,c(SO)=0.3 mol·L-1,则1 L溶液中含K+的数目
2 4
为0.6N ,K+和SO的总数为0.9N ,A项错误,B项正确;物质的量浓度表示的是每升溶液中所含溶质的物质
A A
的量,不受溶液体积大小的影响,2 L 0.3 mol·L-1 KSO 溶液中K+的浓度为0.6 mol·L-1,C项错误;物质的量
2 4
浓度中的体积指的是溶液的体积而不是溶剂的体积,D项错误。
7.下列溶液中,跟100 mL 0.5 mol·L-1 NaCl溶液中所含的Cl-物质的量浓度相同的是( )
A.100 mL 0.5 mol·L-1 MgCl 溶液
2
B.200 mL 0.25 mol·L-1 AlCl 溶液
3
C.50 mL 1 mol·L-1 NaCl溶液
D.25 mL 0.5 mol·L-1 HCl溶液
【答案】D
【解析】物质的量浓度与溶液的体积无关,100 mL 0.5 mol·L-1 NaCl溶液中c(Cl-)=0.5 mol·L-1,而A、
B、C、D项中,c(Cl-)分别为1 mol·L-1、0.75 mol·L-1、1 mol·L-1、0.5 mol·L-1,故D项正确。
8.铍、铝化学性质相似,常温常压下,m g铍、铝分别与足量稀硫酸反应产生氢气的体积分别为V L和
1
V L。下列说法正确的是( )
2
A.=
B.m=×9=×18
C.铍、铝消耗硫酸的物质的量相等
D.若相同条件下用NaOH溶液代替硫酸,则产生的气体体积不变
【答案】D
【解析】根据Be+2H+===Be2++H↑、2Al+6H+===2Al3++3H↑,知==,A项错误;V L、V L是常
2 2 1 2
温常压下H 的体积,不能用22.4 L·mol-1计算其物质的量,B项错误;铍、铝消耗的硫酸的物质的量分别为
2
mol、× mol,C项错误;根据Be+2OH-===BeO+H↑、2Al+2OH-+2HO===2AlO+3H↑知,若相同条件下用
2 2 2
NaOH溶液代替硫酸,产生的氢气体积不变,D项正确。
9.为实现随处可上网,中国发射了“中星16号”卫星。NH ClO 是火箭的固体燃料,发生的反应为
4 4
2NH ClO =====N↑+Cl↑+2O↑+4HO↑,N 代表阿伏加德罗常数的值,下列说法正确的是( )
4 4 2 2 2 2 A
A.1 mol NH ClO 溶于水,含NH和ClO的数目均为N
4 4 A
B.反应中还原产物分子数与氧化产物分子总数之比为1∶3
C.产生6.4 g O 反应转移的电子总数为0.8N
2 AD.0.5 mol NH ClO 分解产生的气体体积为44.8 L
4 4
【答案】B
【解析】NH为弱碱阳离子,在水溶液中要水解,因此1 mol NH ClO 溶于水,含NH的数目少于N ,
4 4 A
故A错误;2NH ClO =====N↑+Cl↑+2O↑+4HO↑反应中,还原产物为氯气,氧化产物为氮气和氧气,
4 4 2 2 2 2
还原产物分子数与氧化产物分子总数之比为1∶3,故B正确;6.4 g O 的物质的量为=0.2 mol,根据反应可
2
知,产生6.4 g O 转移的电子总数为1.4N ,故C错误;未告知是否为标准状况,无法计算0.5 mol NH ClO
2 A 4 4
分解产生的气体的体积,故D错误。
10.下列关于实验操作的描述正确的是
A.氧化还原反应滴定时,用酸式滴定管盛装K Cr O 标准溶液
2 2 7
B.从食盐水中得到NaCl晶体,当坩埚中出现大量固体时,停止加热,利用余热蒸干
C.用苯萃取溴水中的Br ,分离时溴和苯的混合溶液从分液漏斗下口放出
2
D.配制一定物质的量浓度溶液时,将量取好的物质放入容量瓶中,加水溶解至刻度线
【答案】A
【解析】重铬酸钾溶液具有强氧化性,为防止重铬酸钾溶液氧化碱式滴定管中的橡胶管,氧化还原反
应滴定时,应用酸式滴定管盛装重铬酸钾标准溶液,故A正确;从食盐水中得到氯化钠晶体,当蒸发皿中
出现大量固体时,停止加热,利用余热蒸干,故B错误;苯的密度比水小,所以用苯萃取溴水中的溴,分
离时溴和苯的混合溶液从分液漏斗上口倒出,故C错误;容量瓶是精量器,不能用于溶解或稀释溶液,故
D错误;故选A。
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.有硫酸镁溶液500 mL,它的密度是1.20 g·cm-3,其中镁离子的质量分数是4.8%,则有关该溶液的说法
不正确的是( )
A.溶质的质量分数是25.0%
B.溶液的物质的量浓度是2.4 mol·L-1
C.溶质和溶剂的物质的量之比是1∶40
D.硫酸根离子的质量分数是19.2%
【答案】AC
【解析】由Mg2+的质量分数知MgSO 的质量分数为×4.8%=24.0%,其浓度c==2.4 mol·L-1,溶质与溶剂
4
的物质的量之比为∶≈1∶21,SO的质量分数为×4.8%=19.2%。
12.下图是某学校实验室从市场买回的试剂标签上的部分内容。据此下列说法不正确的是( )A.该硫酸和氨水的物质的量浓度分别约为18.4 mol·L-1和12.9 mol·L-1
B.各取5 mL与等质量的水混合后,c(HSO)<9.2 mol·L-1,c(NH)>6.45 mol·L-1
2 4 3
C.各取5 mL与等体积的水混合后,w(HSO)>49%,w(NH)<12.5%
2 4 3
D.各取10 mL于两烧杯中,再分别加入一定量的水即可得到较稀的硫酸溶液和氨水
【答案】D
【解析】利用c=计算:c(HSO)= mol·L-1=18.4 mol·L-1,c(NH)= mol·L-1≈12.9 mol·L-1,A正确;硫
2 4 3
酸的密度大于水,氨水的密度小于水,各取5 mL与等质量的水混合后,所得稀硫酸的体积大于10 mL,稀氨水
的体积小于10 mL,故有c(HSO)<9.2 mol·L-1,c(NH)>6.45 mol·L-1,B正确;5 mL浓硫酸和5 mL浓氨水的质
2 4 3
量分别为1.84 g·cm-3×5 mL=9.2 g、0.88 g·cm-3×5 mL=4.4 g,而5 mL水的质量约为5 g,故各取5 mL与等体
积的水混合后,w(HSO)>49%,w(NH)<12.5%,C正确;质量分数为98%的硫酸为浓硫酸,稀释时,不能将水
2 4 3
加入浓硫酸中,否则易引起暴沸,D错误。
13.用下列实验方案及所选玻璃仪器(非玻璃容器任选)能实现相应实验目的的是
选项 实验目的 实验方案 所选玻璃仪器
配制1mol⋅L−1CuSO
烧杯、容量
A 4 将160gCuSO ⋅5H O溶解在1000mL水中
溶液 4 2 瓶、玻璃棒
比较HClO和CH COOH 同温下用pH试纸测定0.1mol⋅L−1NaClO溶液 玻璃棒、玻璃
B 3
的酸性强弱 和0.1mol⋅L−1CH COONa溶液的pH 片
3
向MgCl 溶液中先滴加几滴NaOH溶液,出现白
C 比较K sp [Cu(OH) 2 ]和 色沉淀后 2 ,再向其中滴加与MgCl 溶液浓度相同 试管、胶头滴
K [Mg(OH) ]的大小 2 管
sp 2 的CuCl 溶液
2
用铂丝蘸取少量KCl溶液于酒精灯火焰上,观
D 检验K+ 蓝色钴玻璃
察焰色
【答案】CD
【解析】配制1mol⋅L−1CuSO 溶液,需称取250gCuSO ⋅5H O,同时溶液的体积为1000mL,A不
4 4 2
正确;NaClO具有强氧化性,会漂白pH试纸,所以不能用pH试纸测定NaClO溶液的pH,B不正确;比
较两种难溶物的溶度积时,应确保一种沉淀转化为另一种沉淀,MgCl 溶液中加入几滴NaOH溶液,再加
2
入同浓度的CuCl 溶液,生成的Cu(OH) 沉淀一定是Mg(OH) 转化的,C正确;做K+的焰色试验时,需要
2 2 2
透过蓝色钴玻璃,以排除Na+的干扰,D不正确;故选C。
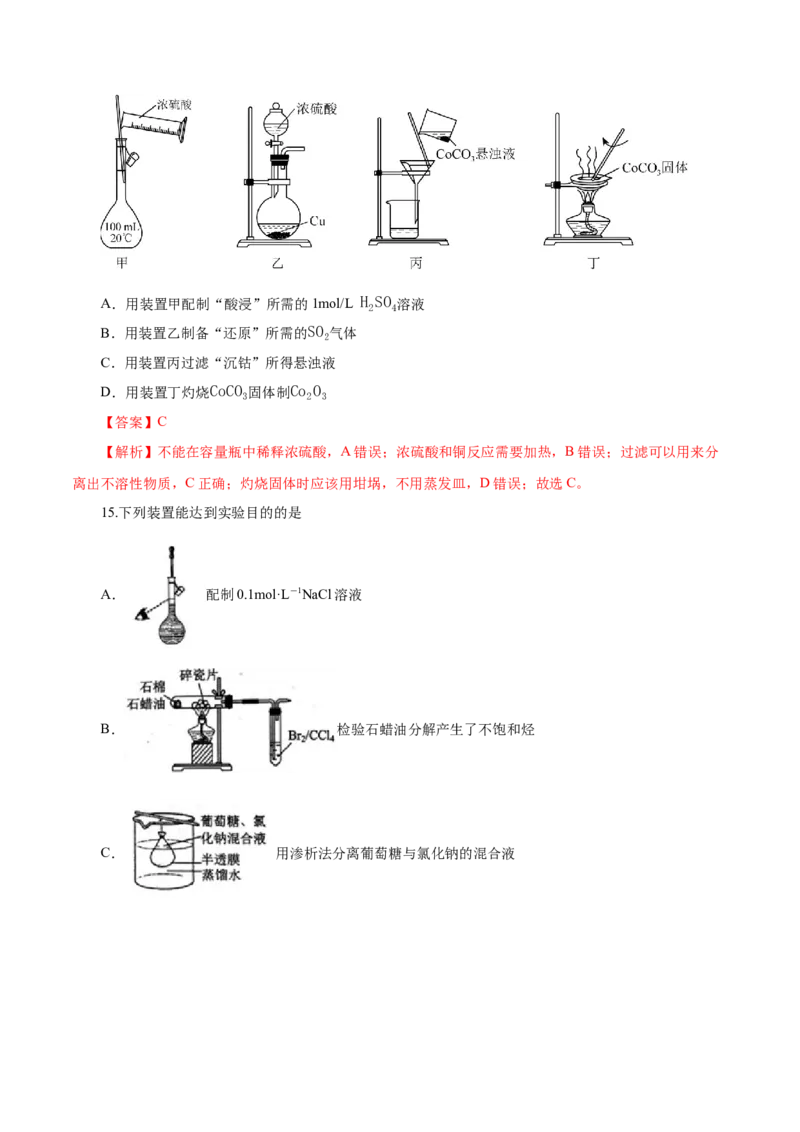
14.以含钴废渣(主要成分CoO、Co O ,还含有Al O 、ZnO等杂质)为原料制备Co O 需经历酸浸、
2 3 2 3 2 3
还原、沉钴、过滤、灼烧等操作。下列实验装置能达到实验目的的是A.用装置甲配制“酸浸”所需的1mol/L H SO 溶液
2 4
B.用装置乙制备“还原”所需的SO 气体
2
C.用装置丙过滤“沉钴”所得悬浊液
D.用装置丁灼烧CoCO 固体制Co O
3 2 3
【答案】C
【解析】不能在容量瓶中稀释浓硫酸,A错误;浓硫酸和铜反应需要加热,B错误;过滤可以用来分
离出不溶性物质,C正确;灼烧固体时应该用坩埚,不用蒸发皿,D错误;故选C。
15.下列装置能达到实验目的的是
A. 配制0.1mol·L-1NaCl溶液
B. 检验石蜡油分解产生了不饱和烃
C. 用渗析法分离葡萄糖与氯化钠的混合液D. 用陶瓷蒸发皿加热NaOH溶液获得纯净的NaOH固体
【答案】B
【解析】配制0.1mol·L-1NaCl溶液,定容时眼睛平视刻度线,A项错误;石蜡油分解得到乙烯,乙烯
和溴加成,使得溴的四氯化碳溶液褪色,因而可以检验,B项正确;葡萄糖与氯化钠的混合液为小分子和
离子溶液,可穿过半透膜,因而不能分离,C项错误;NaOH溶液会和空气中CO 反应,生成NaCO,因
2 2 3
而蒸发不能得到纯净的NaOH,而且氢氧化钠会腐蚀陶瓷蒸发皿,D项错误。故选B。
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常稀释100倍(体积之比)后使用。
请回答下列问题:
(1)该“84”消毒液的物质的量浓度约为____________mol·L-1(结果保留1位小数)。
(2)某同学取100 mL该“84”消毒液,稀释后用于消毒,稀释后的溶液中c(Na+)=________mol·L-1。
(3)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下
列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(4)“84”消毒液与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配
制2 L 2.3 mol·L-1的稀硫酸用于增强“84”消毒液的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________mL。
【解析】(1)由c=得,c(NaClO)= mol·L-1≈4.0 mol·L-1。
(2)稀释前后溶液中NaClO的物质的量不变,则有100 mL×10-3 L·mL-1×4.0 mol·L-1=100 mL×10-3 L·mL-
1×c(NaClO)×100,得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1。
(3)选项A,需用托盘天平称取NaClO固体,需用烧杯溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量
瓶和胶头滴管来定容,图示仪器中的a、b不需要,但还需要玻璃棒和胶头滴管;选项B,配制过程中需要加水,所以洗涤干净后的容量瓶不必烘干;选项C,未洗涤烧杯和玻璃棒将导致配制的溶液中溶质的物质的量减小,
结果偏低;选项D,应选取500 mL的容量瓶进行配制,然后取出480 mL即可,所以需要NaClO的质量为0.5
L×4.0 mol·L-1×74.5 g· mol-1=149.0 g。
(4)①根据HSO 的组成可知,溶液中c(H+)=2c(HSO)=4.6 mol·L-1。②2 L 2.3 mol·L-1的稀硫酸中溶质的
2 4 2 4
物质的量为2 L×2.3 mol·L-1=4.6 mol,设需要98%(密度为1.84 g·cm-3)的浓硫酸的体积为V mL,则有=4.6
mol,解得V=250.0。
【答案】(1)4.0 (2)0.04 (3)C (4)①4.6 ②250.0
17.(10分)用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需
要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)经计算需要________mL浓盐酸,在量取时宜选用下列量筒中的________(填字母)。
A.5 mL量筒 B.10 mL量筒
C.25 mL量筒 D.50 mL量筒
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入选定规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线 1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与
瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是________(填序号)。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,则配制的稀盐酸浓度________(填“偏高”
“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度
________(填“偏高”“偏低”或“无影响”)。
【解析】(2)c(HCl)== mol·L-1=11.6 mol·L-1。加水稀释前后HCl的物质的量不变,所以11.6 mol·L-
1×V(HCl)=250 mL×1 mol·L-1,解得V(HCl)≈21.6 mL,应该选择25 mL量筒量取。
(4)用刚刚洗涤洁净的量筒来量取浓盐酸,量取的盐酸被稀释了,其物质的量偏小,所配制溶液的浓度
偏低;若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则一部分溶质损失,所配制溶液的浓度偏低。
【答案】(1)250 (2)21.6 C (3)③①④② (4)偏低 偏低
18.(15分)如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
(1)该浓硫酸的物质的量浓度为_______mol/L。
(2)取用任意体积的该硫酸溶液时,下列物理量中不随所取体积的多少而变化的是_______。A.溶液中HSO 的物质的量 B.溶液的浓度
C.溶液中SO2-
的数
2 4 4
目 D.溶液的密度
(3)某学生欲用上述浓硫酸和蒸馏水配制480mL物质的量浓度为0.2mol/L稀硫酸。
①该学生需要量取_______mL上述浓硫酸进行配制。
②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)_______;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓硫酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢
慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入一定体积的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
③在配制过程中,下列实验操作使所配制的稀硫酸的物质的量浓度偏高的是_______
A.用量筒量取浓硫酸时仰视观察凹液面
B.稀释用的烧杯和玻璃棒未洗涤
C.洗净的容量瓶未经干燥就用于配制溶液
D.溶液注入容量瓶前没有恢复到室温就进行定容
E.定容时俯视观察凹液面
F.加水超过刻度线后,用胶头滴管吸出多余的液体
(4)现将100mL该硫酸与300mL 0.4mol/LCuSO
溶液混合,体积变化忽略不计,所得溶液中SO2-
的物质
4 4
的量浓度是_______mol/L。
【答案】 18.4 BD 5.4 BCAFED ADE 0.35
【解析】
1000ρ×w 1000×1.84×98%
(1)c(H SO )= = mol/L=18.4mol/L。答案为:18.4;
2 4 M 98
(2)溶液中硫酸的物质的量=c∙V,与溶液的体积有关,A不符合题意;溶液是均一的稳定的混合物,它
的浓度与所取溶液的体积无关,B符合题意;溶液中硫酸根的数目=n∙N =cVN ,与溶液的体积有关,C不
A A
符合题意;溶液是均一的混合物,它的密度与所取溶液的体积无关,D符合题意。故选BD;
0.5L×0.2mol/L
(3)①根据溶液稀释前后溶质的物质的量不变,可得如下等式:cV=cV,则V=
1 1 2 2 1 18.4mol/L=0.0054L≈5.4mL。
②配制溶液时,操作步骤为:计算、量取、溶解、移液、洗涤、定容、振荡等操作,故正确的操作顺
序是BCAFED。
③量取浓硫酸时,仰视观察凹液面读数,会导致量取的浓硫酸体积偏大,配制的溶液中溶质的物质的
量偏大,溶液浓度偏高,A符合题意;没有洗涤烧杯和玻璃棒,导致配制的溶液中溶质的物质的量偏小,
配制的溶液浓度偏低,B不符合题意;洗净的容量瓶未经干燥就用于配制溶液,配制的溶液中溶质的物质
的量和溶液的体积都不变,配制的溶液浓度不变,C不符合题意;热的溶液体积膨胀,冷却后溶液体积缩
小,则冷却后配制的溶液体积偏小,溶液的浓度偏高,D符合题意;定容时俯视观察凹液面,配制的溶液
体积偏小,溶液的浓度偏高,E符合题意;加水超过刻度线后,用胶头滴管吸出多余的液体,将导致有少
量溶质被吸出,配制的溶液中溶质的物质的量偏小,溶液的浓度偏低,F不符合题意;综合以上分析,
ADE符合题意。答案为:5.4;BCAFED;ADE;
(4)100mL0.2mol/L H SO 溶液中硫酸根的物质的量为:0.1L×0.2mol/L=0.02mol,
2 4
300mL 0.4mol/LCuSO 溶液中硫酸根的物质的量为:0.3L×0.4mol/L=0.12mol,
4
混合后溶液中硫酸根的总物质的量为:0.02moL+0.12mol=0.14mol,溶液的总体积为:
0.14mol
100ml+300ml=400ml,即0.4L,所以混合后溶液中硫酸根的物质的量浓度为: =0.35mol/L。
0.4L
19.(15分)实验室配制480mL0.2mol/L的NaOH溶液,实验操作步骤有:
A.在天平上称取一定质量的氢氧化钠固体,用适量的蒸馏水使它完全溶解并冷却至室温;
B.把制得的溶液小心地转移到容量瓶中;
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至_____;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶并轻轻振荡;
E.将容量瓶瓶塞塞紧,充分摇匀。
回答下列问题:
(1)操作步骤的正确顺序为(填序号)___________。
(2)操作A中,在天平上称取氢氧化钠固体的质量为___________g。
(3)本实验用到的基本仪器已经有烧杯、天平(带砝码、镊子)、药匙、玻璃棒,还缺少的仪器是
___________。
(4)请将操作C中缺少的文字补充完整___________。
(5)配制溶液时,下列操作中引起误差偏高的有___________。(填序号)
A.药品久置发生变质
B.原容量瓶配制溶液前未干燥C.氢氧化钠溶液未冷却至室温就转移至容量瓶
D.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
E.定容时,俯视刻度线
(6)下列操作中,容量瓶所不具备的功能有___________。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
【答案】(1)ABDCE
(2)4.0
(3)500mL容量瓶、胶头滴管
(4)凹液面与刻度线相切
(5)CE
(6)BC
【解析】
(1)配制该NaOH溶液的步骤有:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,因此答案为
ABDCE;
(2)没有480mL的容量瓶,实际上配制的为500mL 0.2mol/L的NaOH溶液,需称取NaOH固体的质量
为:40g/mol×0.2mol/L×0.5L=4.0g;
(3)配制该NaOH溶液的步骤有:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,结合操作方
法可知,使用的仪器有:托盘天平、烧杯、玻璃棒、药匙、胶头滴管、500mL容量瓶等,还缺少的仪器为
胶头滴管、500mL容量瓶;
(4)定容时需要用到胶头滴管,则C处操作为:继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,
改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相切;
(5)A.药品久置发生变质,溶质的质量减少,浓度偏低;B.原容量瓶配制溶液前未干燥,不影响配
制结果;
C.氢氧化钠溶液未冷却至室温就转移至容量瓶,冷却后溶液体积减少,浓度偏高;D.定容时,加蒸
馏水超过刻度线,又用胶头滴管吸出,溶质的质量减少,浓度偏低;E.定容时,俯视刻度线,加入蒸馏
水体积偏小,所得溶液浓度偏高;答案选CE;
(6)容量瓶是用来配制一定体积准确浓度的标准溶液,A不选;容量瓶不能贮存溶液,B选;容量瓶上
只有一条刻度线,不能测量容量瓶规格以下的任意体积的液体,C选;容量瓶可用来准确稀释某一浓度的溶液,D不选;答案选BC。