文档内容
化工生产中物质转化条件的控制
1.(10分)研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的
流程如下:
(1)反应釜中,溶液的pH、温度(T)与生成沉淀的关系如图,图中区域分别表示铁的化合物稳定存在的区域。
则制备FeOOH适宜的pH和温度分别为 (填字母)。
a.2,80 ℃ b.4,90 ℃
c.5,160 ℃ d.6,25 ℃
(2)制备磁性纳米铁棒时,加入NaBH 前先通入N 的作用是 。
4 2
(3)常温下,若在含Cd2+、Te4+滤液中加入NaOH溶液调节pH为7,溶液中c(Cd2+)的最大值为
(已知:K [Cd(OH) ]=5.3×10-15)。
sp 2
(4)从含TeO2-
滤液得到“吸附Te”,利用了磁性纳米铁棒的性质有 、 。
3
2.(6分)(2024·长沙雅礼中学高三模拟)废催化剂(含TiO 、V O 、WO 等成分)提取钛、钒工艺流程如图所示。
2 2 5 3已知:①钛酸钠(Na TiO )难溶于水;
2 3
②溶液的酸性较强时,+5价钒主要以V O+ 的形式存在。
2
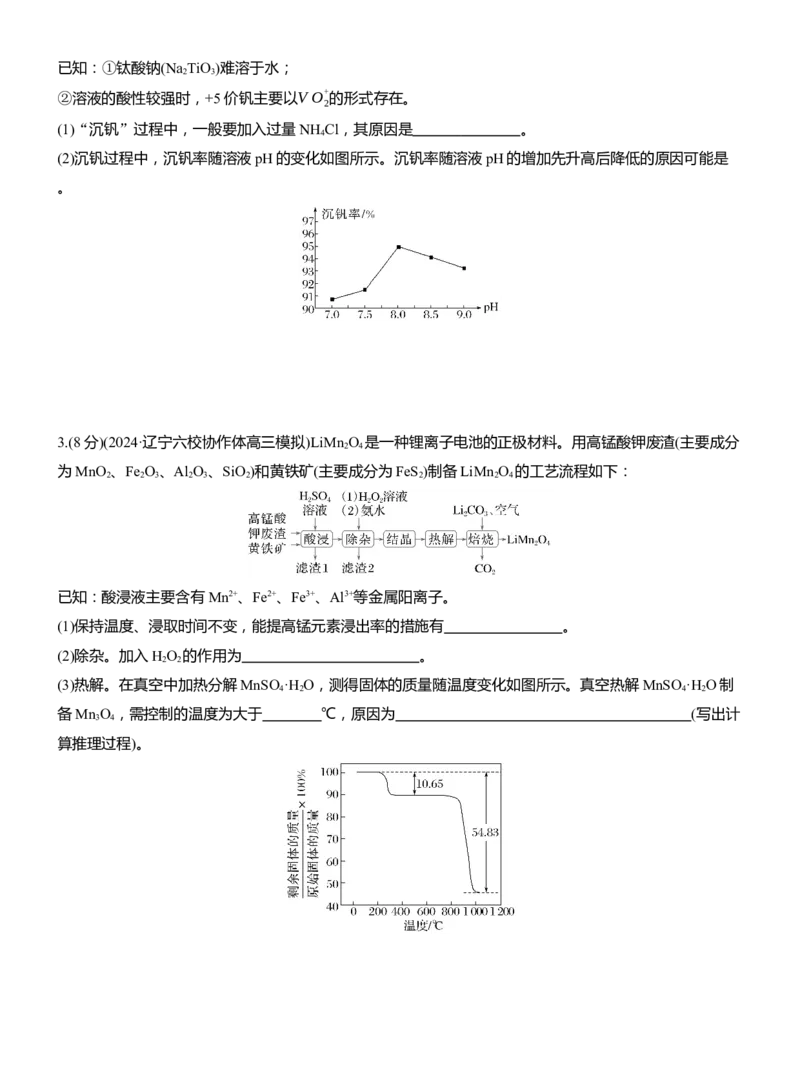
(1)“沉钒”过程中,一般要加入过量NH Cl,其原因是 。
4
(2)沉钒过程中,沉钒率随溶液pH的变化如图所示。沉钒率随溶液pH的增加先升高后降低的原因可能是
。
3.(8分)(2024·辽宁六校协作体高三模拟)LiMn O 是一种锂离子电池的正极材料。用高锰酸钾废渣(主要成分
2 4
为MnO 、Fe O 、Al O 、SiO )和黄铁矿(主要成分为FeS )制备LiMn O 的工艺流程如下:
2 2 3 2 3 2 2 2 4
已知:酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属阳离子。
(1)保持温度、浸取时间不变,能提高锰元素浸出率的措施有 。
(2)除杂。加入H O 的作用为 。
2 2
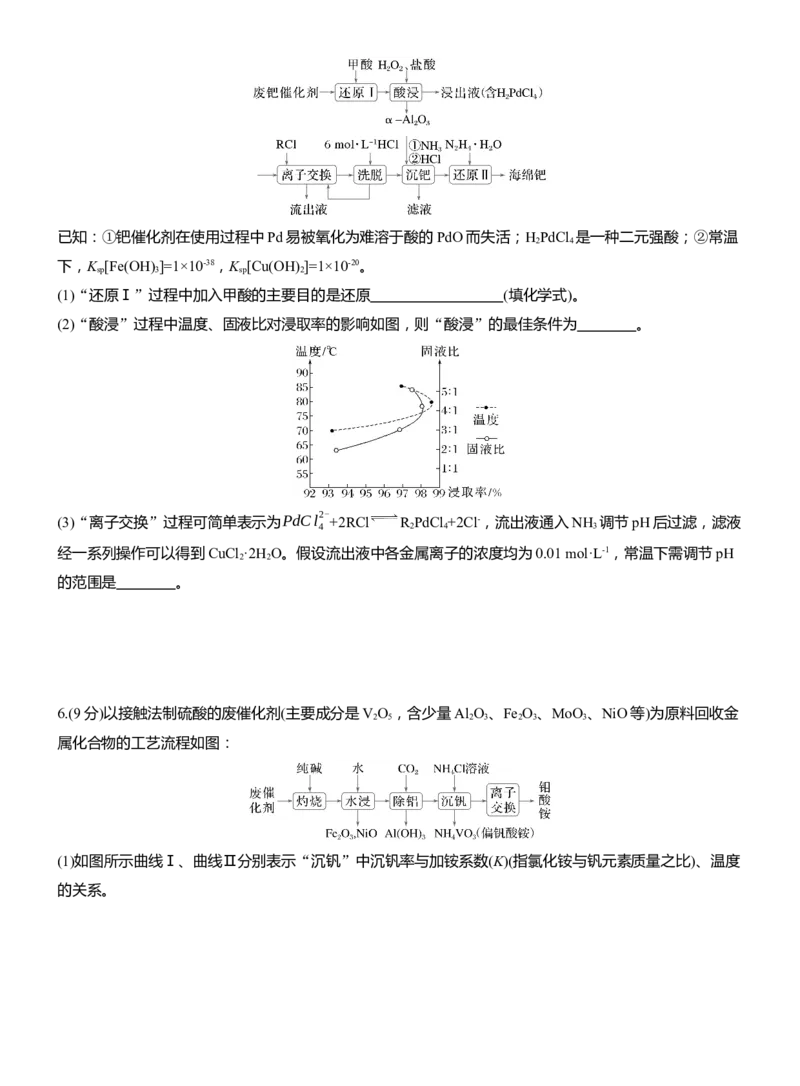
(3)热解。在真空中加热分解MnSO ·H O,测得固体的质量随温度变化如图所示。真空热解MnSO ·H O制
4 2 4 2
备Mn O ,需控制的温度为大于 ℃,原因为 (写出计
3 4
算推理过程)。4.(8分)(2024·辽宁省名校联盟高三联考)草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为
Co,含有一定量的NiO、Al O 、Fe、SiO 等)制备草酸钴晶体(CoC O ·2H O)的流程如下:
2 3 2 2 4 2
已知:①草酸钴晶体难溶于水。
②RH为有机物(难电离),Mn+代表金属离子,Mn++nRH MR +nH+。
n
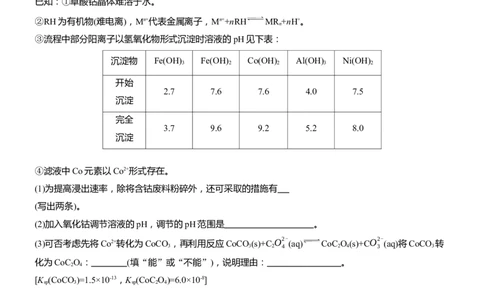
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Al(OH) Ni(OH)
3 2 2 3 2
开始
2.7 7.6 7.6 4.0 7.5
沉淀
完全
3.7 9.6 9.2 5.2 8.0
沉淀
④滤液中Co元素以Co2+形式存在。
(1)为提高浸出速率,除将含钴废料粉碎外,还可采取的措施有
(写出两条)。
(2)加入氧化钴调节溶液的pH,调节的pH范围是 。
(3)可否考虑先将Co2+转化为CoCO ,再利用反应CoCO (s)+C
O2-
(aq) CoC O
(s)+CO2-
(aq)将CoCO 转
3 3 2 4 2 4 3 3
化为CoC O : (填“能”或“不能”),说明理由: 。
2 4
[K (CoCO )=1.5×10-13,K (CoC O )=6.0×10-8]
sp 3 sp 2 4
5.(9分)(2024·山东潍坊联考)钯催化剂(主要成分为Pd、α⁃Al
2
O
3
,还含少量铁、铜等)是石油化工中催化加氢
和催化氧化等反应的重要催化剂。一种从废钯催化剂中回收海绵钯的工艺流程如下:已知:①钯催化剂在使用过程中Pd易被氧化为难溶于酸的PdO而失活;H PdCl 是一种二元强酸;②常温
2 4
下,K [Fe(OH) ]=1×10-38,K [Cu(OH) ]=1×10-20。
sp 3 sp 2
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原 (填化学式)。
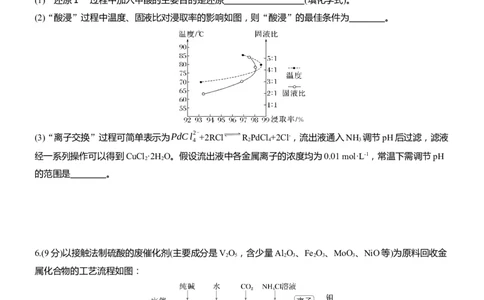
(2)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”的最佳条件为 。
(3)“离子交换”过程可简单表示为PdCl2-
+2RCl R PdCl +2Cl-,流出液通入NH 调节pH后过滤,滤液
4 2 4 3
经一系列操作可以得到CuCl ·2H O。假设流出液中各金属离子的浓度均为0.01 mol·L-1,常温下需调节pH
2 2
的范围是 。
6.(9分)以接触法制硫酸的废催化剂(主要成分是V O ,含少量Al O 、Fe O 、MoO 、NiO等)为原料回收金
2 5 2 3 2 3 3
属化合物的工艺流程如图:
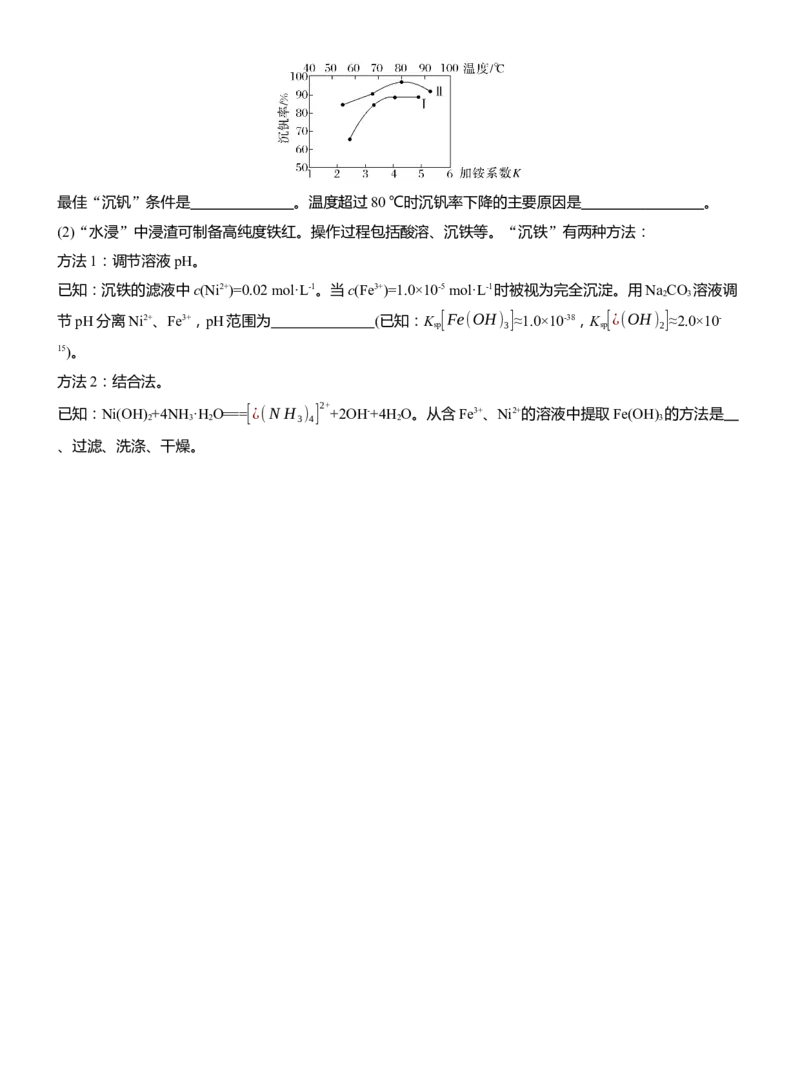
(1)如图所示曲线Ⅰ、曲线Ⅱ分别表示“沉钒”中沉钒率与加铵系数(K)(指氯化铵与钒元素质量之比)、温度
的关系。最佳“沉钒”条件是 。温度超过80 ℃时沉钒率下降的主要原因是 。
(2)“水浸”中浸渣可制备高纯度铁红。操作过程包括酸溶、沉铁等。“沉铁”有两种方法:
方法1:调节溶液pH。
已知:沉铁的滤液中c(Ni2+)=0.02 mol·L-1。当c(Fe3+)=1.0×10-5 mol·L-1时被视为完全沉淀。用Na CO 溶液调
2 3
节pH分离Ni2+、Fe3+,pH范围为 (已知:K [Fe(OH) ]≈1.0×10-38,K [¿(OH) ]≈2.0×10-
sp 3 sp 2
15)。
方法2:结合法。
2+
已知:Ni(OH) +4NH ·H O===[¿(N H ) ] +2OH-+4H O。从含Fe3+、Ni2+的溶液中提取Fe(OH) 的方法是
2 3 2 3 4 2 3
、过滤、洗涤、干燥。答案精析
1.(1)b (2)排出设备中的空气,防止磁性纳米铁棒和NaBH 被氧化 (3)0.53 mol·L-1 (4)吸附性 还原性
4
解析 (2)磁性纳米铁棒和NaBH 都容易被氧化,所以在加入NaBH 之前需通入N 排出反应容器中的空气。
4 4 2
(3)常温下,溶液的pH=7,则c(OH-)=1.0×10-7mol·L-1,根据K [Cd(OH) ]=5.3×10-15,则c(Cd2+)=
sp 2
K [Cd(OH) ] 5.3×10-15
sp 2 = mol·L-1=0.53 mol·L-1。(4)TeO2- 中Te的化合价降低,被磁性纳米铁棒还原,
c2 (OH-
)
(1.0×10-7
)
2 3
磁性纳米铁棒还能吸附Te,故在得到Te的过程中,磁性纳米铁棒呈现了还原性和吸附性。
2.(1)增大N H+ 浓度,使NH VO (s) NH+ (aq)+VO- (aq)平衡逆向移动,利于NH VO 尽可能析出完全
4 4 3 4 3 4 3
(2)pH过低,VO- 转化为VO+ 的程度较大;pH过高,NH+
转化为NH ·H O的程度较大;两因素均使沉钒率
3 2 4 3 2
降低
3.(1)适当增加硫酸浓度,将固体原料粉碎,加快搅拌速率(任答一条即可,其他合理答案也可) (2)氧化剂,
将Fe2+氧化为Fe3+
3M(MnSO ·H O)-M(Mn O )
(3)1 000 3MnSO ·H O~Mn O , 4 2 3 4 ×100%=
4 2 3 4 3M(MnSO ·H O)
4 2
3×169 g·mol-1-229 g·mol-1
×100%≈54.83%,所以需控制温度大于1 000 ℃
3×169 g·mol-1
4.(1)适当提高酸浸温度、适当增加硫酸浓度等(答案合理即可) (2)5.2≤pH<7.5 (3)不能 该反应的平衡常
数K=2.5×10-6,转化程度小,不能实现转化
解析 (2)加入氧化钴,发生CoO+2H+===Co2++H O,根据阳离子以氢氧化物形式沉淀时溶液的pH可知,
2
调节溶液的pH为5.2≤pH<7.5,使Fe3+和Al3+完全转化为沉淀Fe(OH) 、Al(OH) ,同时不能影响到镍和钴。
3 3
c(CO2-
)
c(CO2- )·c(Co2+
)
(3)CoCO (s)+C
O2-
(aq) CoC O
(s)+CO2-
(aq)的平衡常数K=
3
=
3
=
3 2 4 2 4 3 c(C O2- ) c(C O2- )·c(Co2+ )
2 4 2 4
K (CoCO ) 1.5×10-13
sp 3 = =2.5×10-6,转化程度小,不能实现该转化。
K (CoC O ) 6.0×10-8
sp 2 4
5.(1)PdO (2)温度80 ℃,固液比4∶1
(3)3≤pH<5
√K [Fe(OH) ] √1×10-38
解析 (3)通入NH 调节pH,对于铁离子:c(OH-)= 3 sp 3 =3 mol·L-1=10-11 mol·L-1,则对
3 c(Fe3+
)
1×10-5
√K [Cu(OH) ] √1×10-20
应最低pH为3,对于铜离子:c(OH-)< sp 2 = mol·L-1=10-9 mol·L-1,则对应pH=5,故
c(Cu2+ ) 0.01
需调节pH的范围是3≤pH<5。
6.(1)K为4附近、温度为80 ℃左右 温度过高,N H+ 水解程度增大,生成的NH 挥发,c(NH+ )降低较快,
4 3 4
故沉钒率下降 (2)3≤pH<7.5 向混合液中加入过量氨水解析 (1)加入NH Cl溶液调节pH,将钒元素以偏钒酸铵的形式分离出来,根据图像可知,当K在4附近
4
时,沉钒率可达到最大,温度最佳值约为80 ℃;因为NH Cl受热易分解,温度过高氯化铵分解,同时促
4
进铵根离子水解,溶液中铵根离子浓度下降,会使沉钒率下降。(2)铁离子完全沉淀时溶液中c(OH-)=
√1.0×10-38 √2.0×10-15
3 mol·L-1=10-11 mol·L-1,pH=3;当镍离子开始沉淀时溶液中c(OH-)= mol·L-1=10-6.5
10-5 0.02
2+
mol·L-1,pH=7.5,即沉铁的pH范围为3≤pH<7.5,根据Ni(OH) +4NH ·H O===[¿(N H ) ] +2OH-+4H O
2 3 2 3 4 2
可知,氢氧化镍能溶于过量的氨水中,氢氧化铁不能,则从含Fe3+、Ni2+的溶液中提取Fe(OH) 的方法是向
3
混合液中加入过量氨水、过滤、洗涤、干燥。