文档内容
2025新教材化学高考第一轮
专题十一 化学反应速率和化学平衡
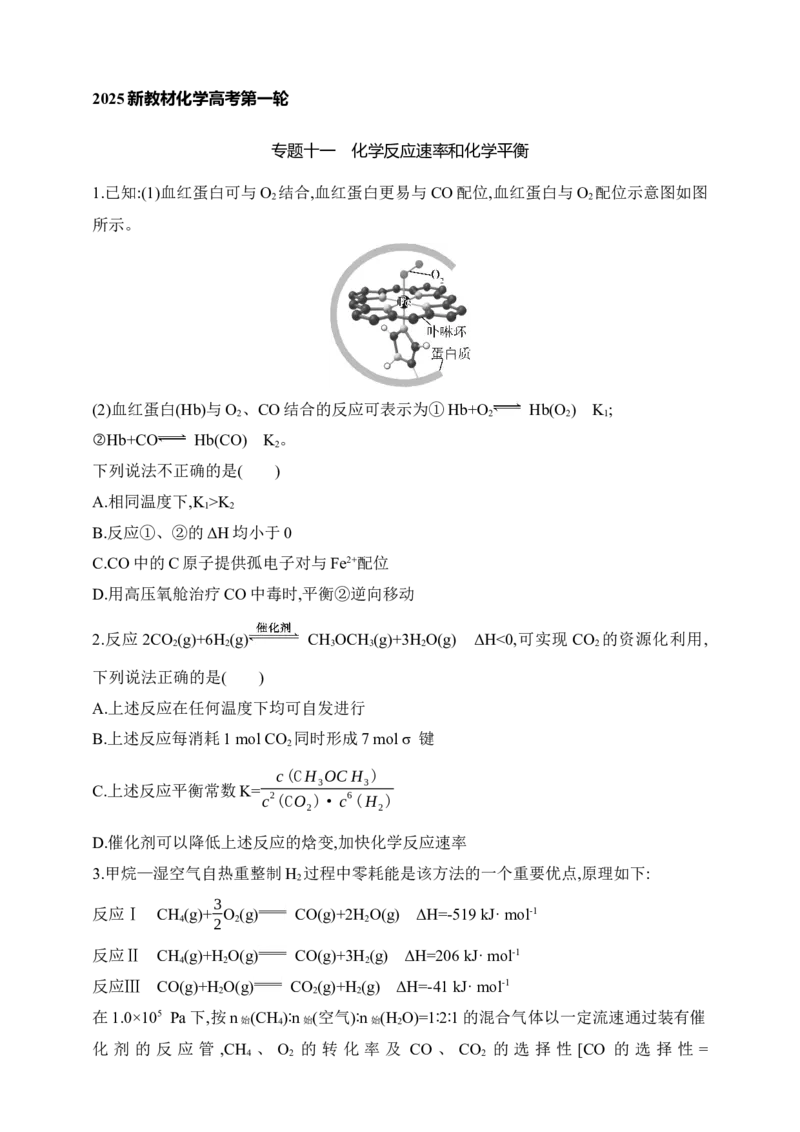
1.已知:(1)血红蛋白可与O 结合,血红蛋白更易与CO配位,血红蛋白与O 配位示意图如图
2 2
所示。
(2)血红蛋白(Hb)与O 、CO结合的反应可表示为①Hb+O Hb(O ) K ;
2 2 2 1
②Hb+CO Hb(CO) K 。
2
下列说法不正确的是( )
A.相同温度下,K >K
1 2
B.反应①、②的ΔH均小于0
C.CO中的C原子提供孤电子对与Fe2+配位
D.用高压氧舱治疗CO中毒时,平衡②逆向移动
2.反应 2CO (g)+6H (g) CH OCH (g)+3H O(g) ΔH<0,可实现 CO 的资源化利用,
2 2 3 3 2 2
下列说法正确的是( )
A.上述反应在任何温度下均可自发进行
B.上述反应每消耗1 mol CO 同时形成7 mol σ 键
2
c(CH OCH )
3 3
C.上述反应平衡常数K=
c2(CO )·c6(H )
2 2
D.催化剂可以降低上述反应的焓变,加快化学反应速率
3.甲烷—湿空气自热重整制H 过程中零耗能是该方法的一个重要优点,原理如下:
2
3
反应Ⅰ CH (g)+ O (g) CO(g)+2H O(g) ΔH=-519 kJ· mol-1
4 2 2 2
反应Ⅱ CH (g)+H O(g) CO(g)+3H (g) ΔH=206 kJ· mol-1
4 2 2
反应Ⅲ CO(g)+H O(g) CO (g)+H (g) ΔH=-41 kJ· mol-1
2 2 2
在1.0×105 Pa下,按n (CH )∶n (空气)∶n (H O)=1∶2∶1的混合气体以一定流速通过装有催
始 4 始 始 2
化 剂 的 反 应 管 ,CH 、 O 的 转 化 率 及 CO 、 CO 的 选 择 性 [CO 的 选 择 性 =
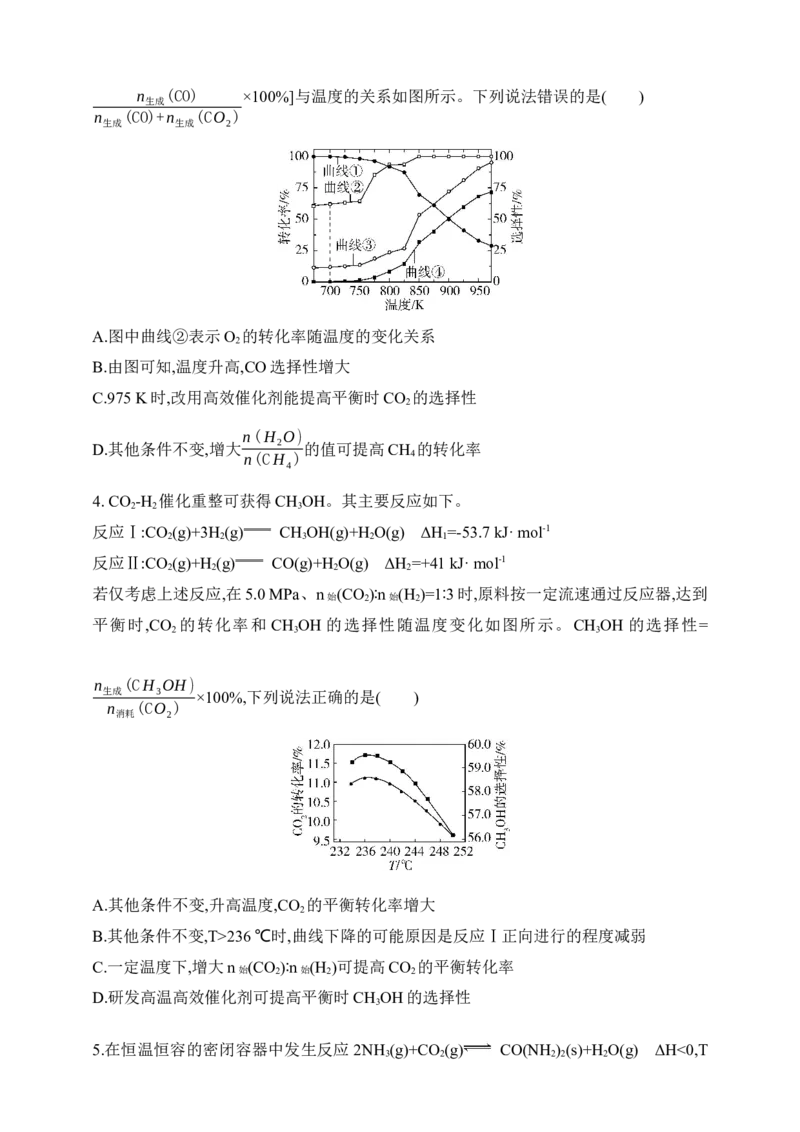
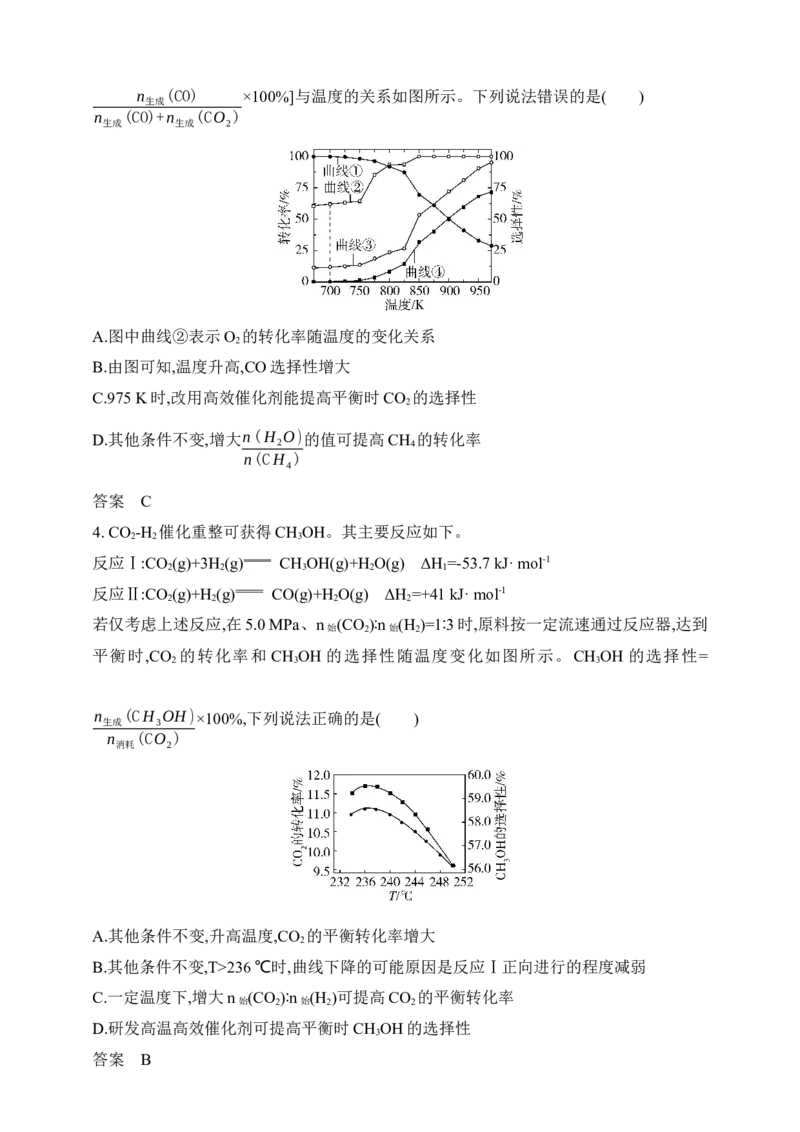
4 2 2n (CO) ×100%]与温度的关系如图所示。下列说法错误的是( )
生成
n (CO)+n (CO )
生成 生成 2
A.图中曲线②表示O 的转化率随温度的变化关系
2
B.由图可知,温度升高,CO选择性增大
C.975 K时,改用高效催化剂能提高平衡时CO 的选择性
2
n(H O)
D.其他条件不变,增大 2 的值可提高CH 的转化率
n(CH ) 4
4
4. CO -H 催化重整可获得CH OH。其主要反应如下。
2 2 3
反应Ⅰ:CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-53.7 kJ· mol-1
2 2 3 2 1
反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH =+41 kJ· mol-1
2 2 2 2
若仅考虑上述反应,在5.0 MPa、n (CO )∶n (H )=1∶3时,原料按一定流速通过反应器,达到
始 2 始 2
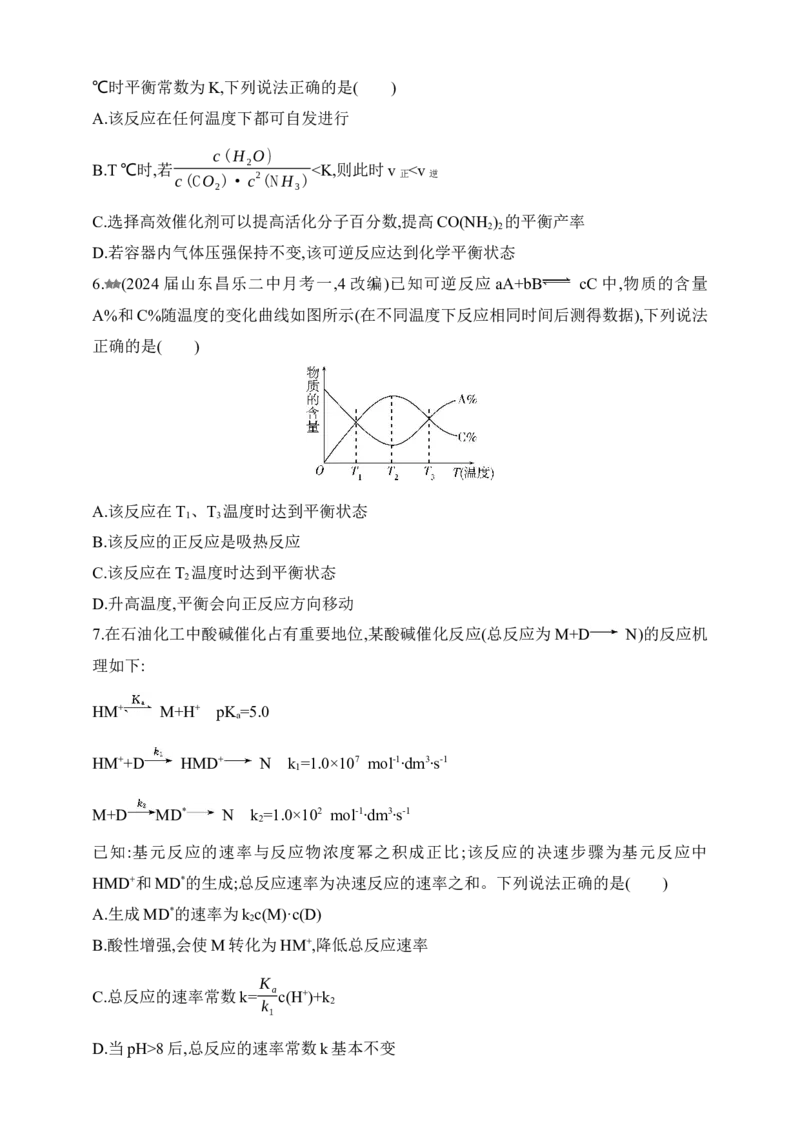
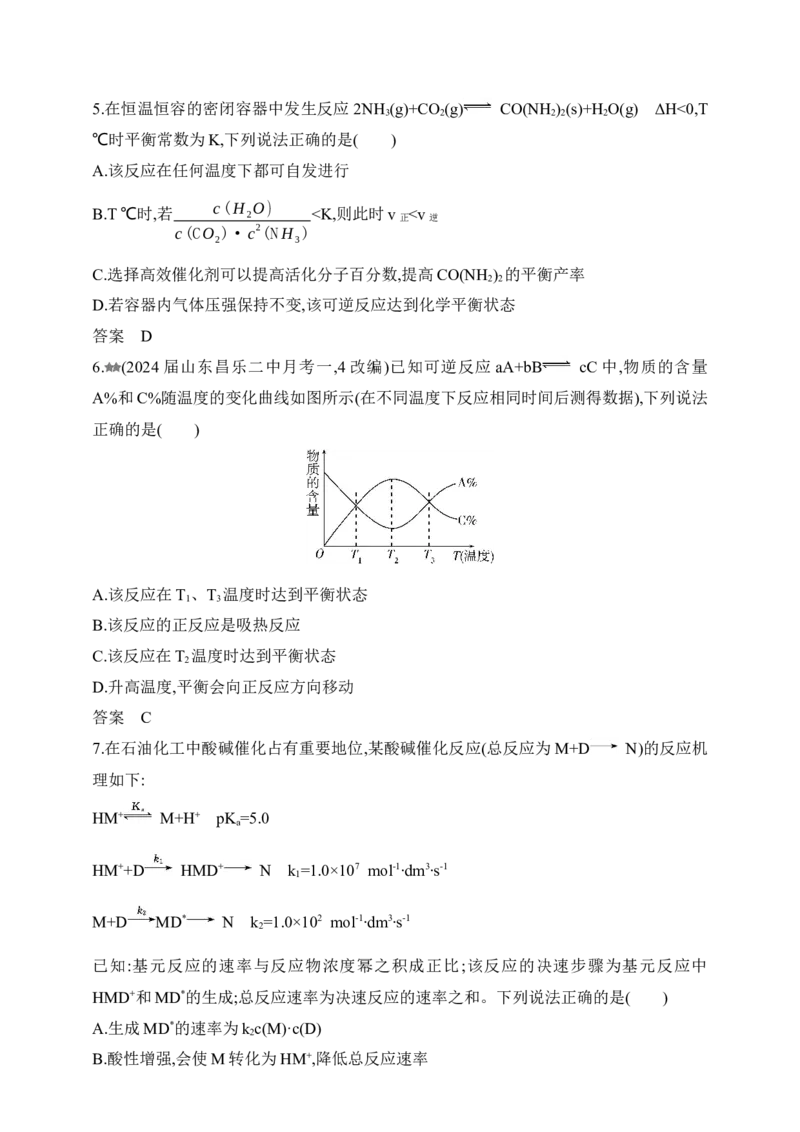
平衡时,CO 的转化率和 CH OH 的选择性随温度变化如图所示。CH OH 的选择性=
2 3 3
n (CH OH)
生成 3 ×100%,下列说法正确的是( )
n (CO )
消耗 2
A.其他条件不变,升高温度,CO 的平衡转化率增大
2
B.其他条件不变,T>236 ℃时,曲线下降的可能原因是反应Ⅰ正向进行的程度减弱
C.一定温度下,增大n (CO )∶n (H )可提高CO 的平衡转化率
始 2 始 2 2
D.研发高温高效催化剂可提高平衡时CH OH的选择性
3
5.在恒温恒容的密闭容器中发生反应 2NH (g)+CO (g) CO(NH ) (s)+H O(g) ΔH<0,T
3 2 2 2 2℃时平衡常数为K,下列说法正确的是( )
A.该反应在任何温度下都可自发进行
c(H O)
2
B.T ℃时,若 8后,总反应的速率常数k基本不变8. (2023湘潭二模,13)T ℃时,含等浓度的AgNO 与Fe(NO ) 的混合溶液中发生反应Fe2+
3 3 2
(aq)+Ag+(aq) Fe3+(aq)+Ag(s) ΔH<0,t s时,改变某一外界条件继续反应至t s(t =4t )
1 2 2 1
时,溶液中c(Ag+)和c(Fe3+)随时间的变化关系如图所示。下列说法正确的是( )
已知:T ℃时,该反应的化学平衡常数K=1。
A.若t s时未改变外界条件,则此时反应未平衡
1
B.若t s时反应达到平衡,则t 时刻改变的条件可能为升温
2 1
C.若始终保持温度不变,则平均反应速率v >v (v 表示0~t s内Fe2+的平均反应速率,v 表
t t t 1 t
1 2 1 2
示0~t s内Fe2+的平均反应速率)
2
0.04
D.0~t s内Ag+的平均反应速率为 mol·L-1·s-1
2 t
2
13. (2024届雅礼中学第一次月考,14)在催化剂作用下,CO 氧化C H 可获得C H 。其主
2 2 6 2 4
要化学方程式如下:
反应Ⅰ.CO (g)+C H (g) C H (g)+CO(g)+H O(g) ΔH =+177 kJ·mol-1
2 2 6 2 4 2 1
反应Ⅱ.2CO (g)+C H (g) 4CO(g)+3H (g) ΔH =+430 kJ·mol-1
2 2 6 2 2
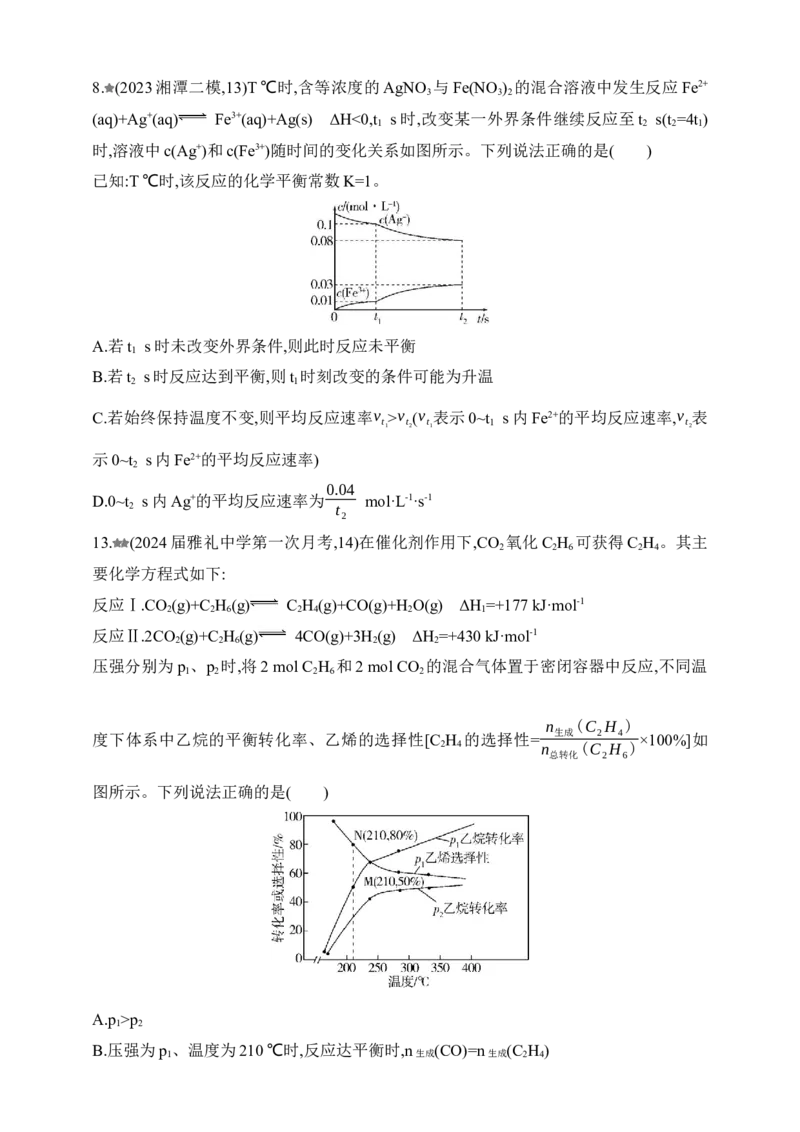
压强分别为p 、p 时,将2 mol C H 和2 mol CO 的混合气体置于密闭容器中反应,不同温
1 2 2 6 2
n (C H )
度下体系中乙烷的平衡转化率、乙烯的选择性[C H 的选择性= 生成 2 4 ×100%]如
2 4 n (C H )
总转化 2 6
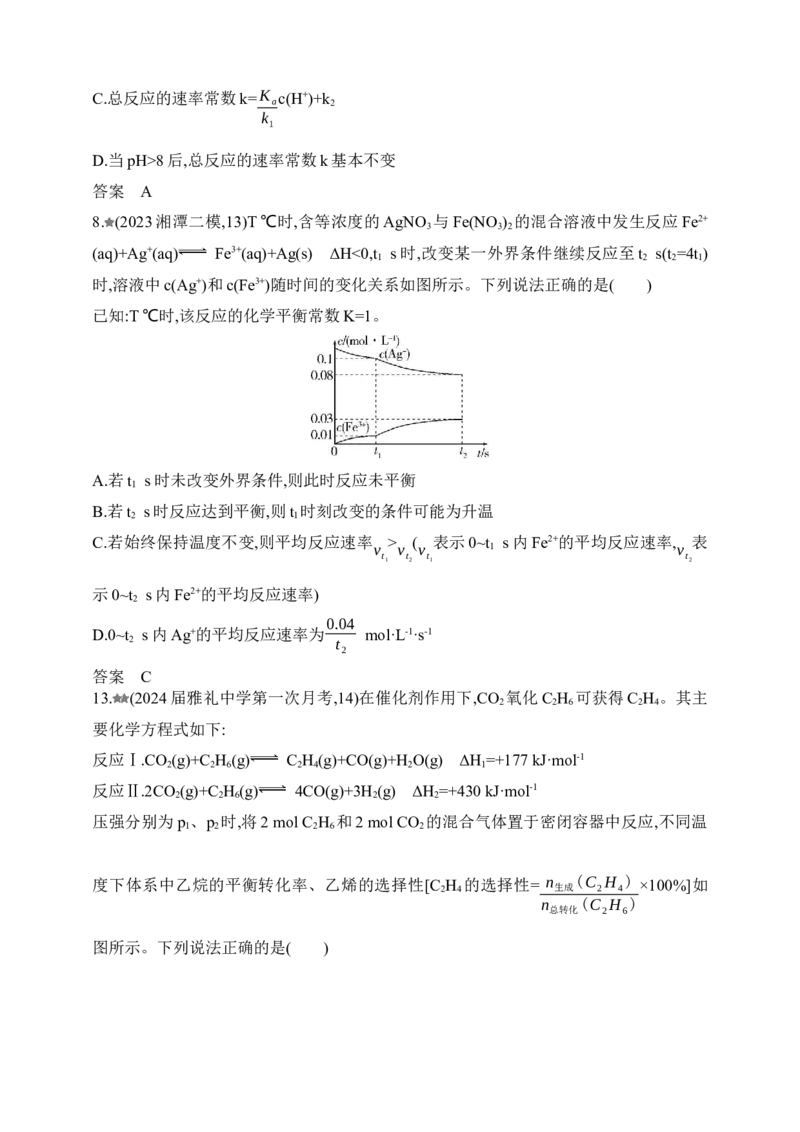
图所示。下列说法正确的是( )
A.p >p
1 2
B.压强为p 、温度为210 ℃时,反应达平衡时,n (CO)=n (C H )
1 生成 生成 2 4C.C H 的选择性下降的原因可能是随着温度的升高,反应Ⅱ中生成的CO抑制了反应Ⅰ的
2 4
进行
D.研发低温下C H 转化率高和C H 选择性高的催化剂,可以提高平衡时C H 的产率
2 6 2 4 2 4
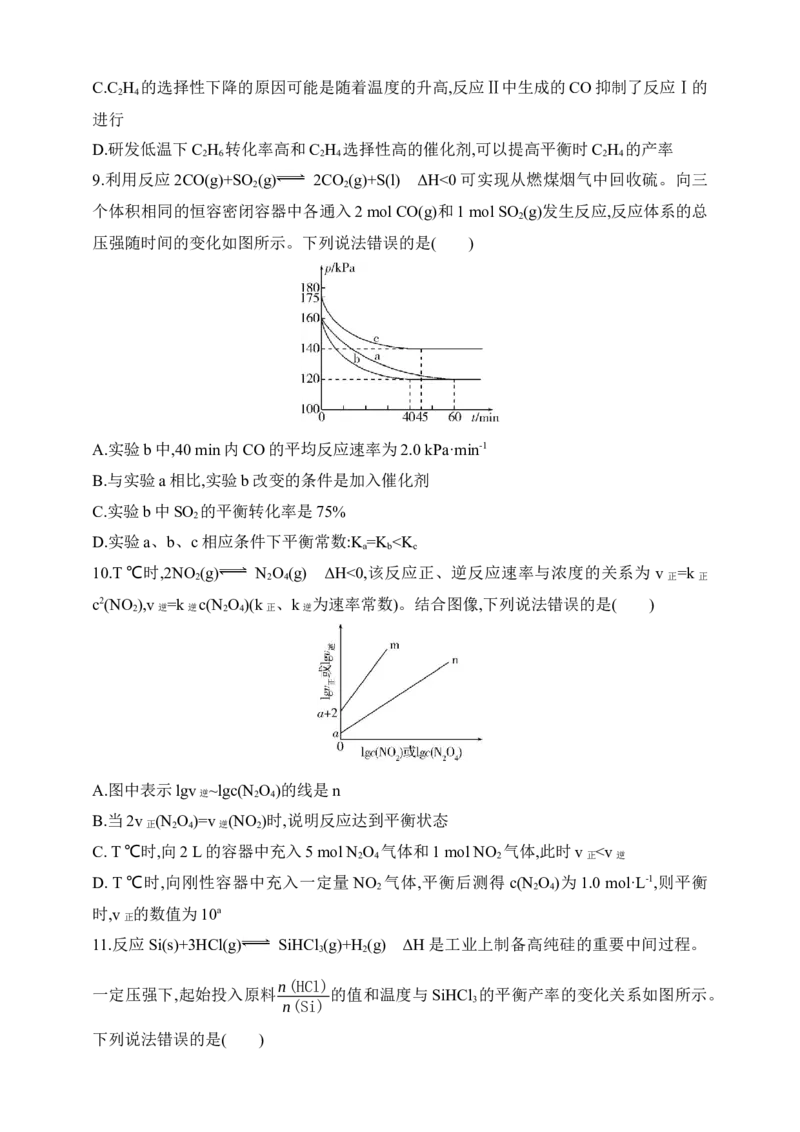
9.利用反应2CO(g)+SO (g) 2CO (g)+S(l) ΔH<0可实现从燃煤烟气中回收硫。向三
2 2
个体积相同的恒容密闭容器中各通入2 mol CO(g)和1 mol SO (g)发生反应,反应体系的总
2
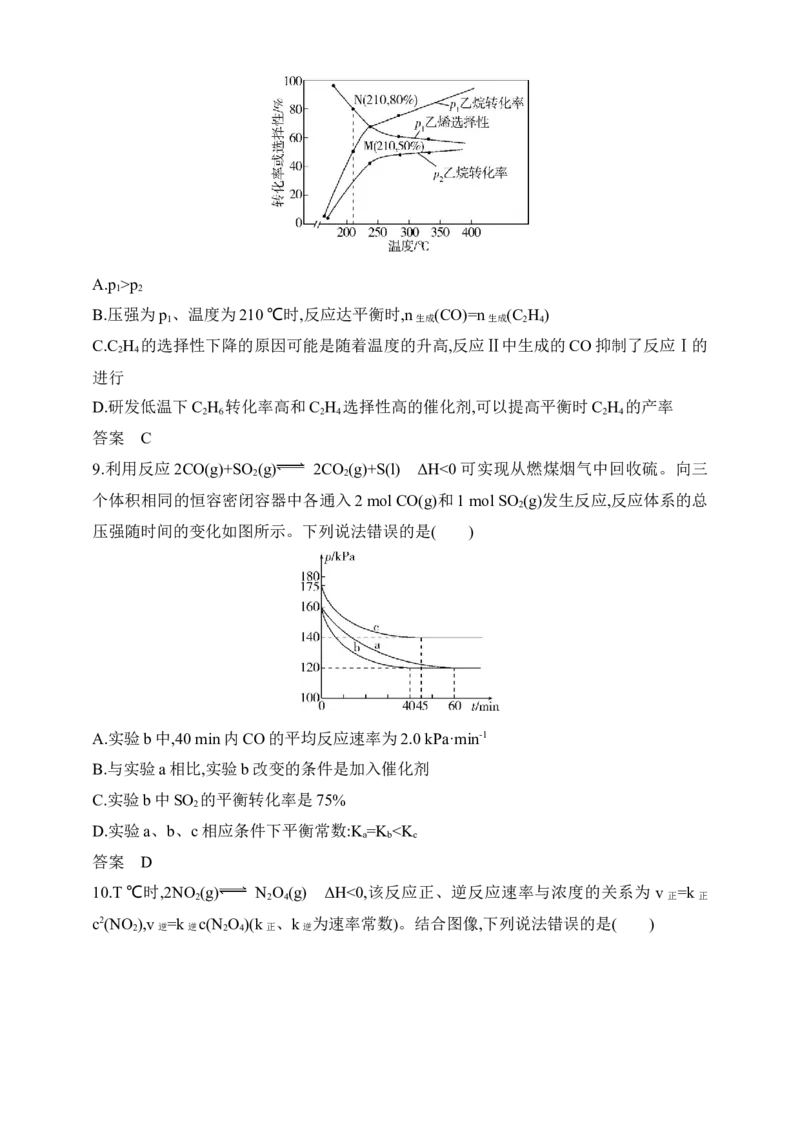
压强随时间的变化如图所示。下列说法错误的是( )
A.实验b中,40 min内CO的平均反应速率为2.0 kPa·min-1
B.与实验a相比,实验b改变的条件是加入催化剂
C.实验b中SO 的平衡转化率是75%
2
D.实验a、b、c相应条件下平衡常数:K =K N
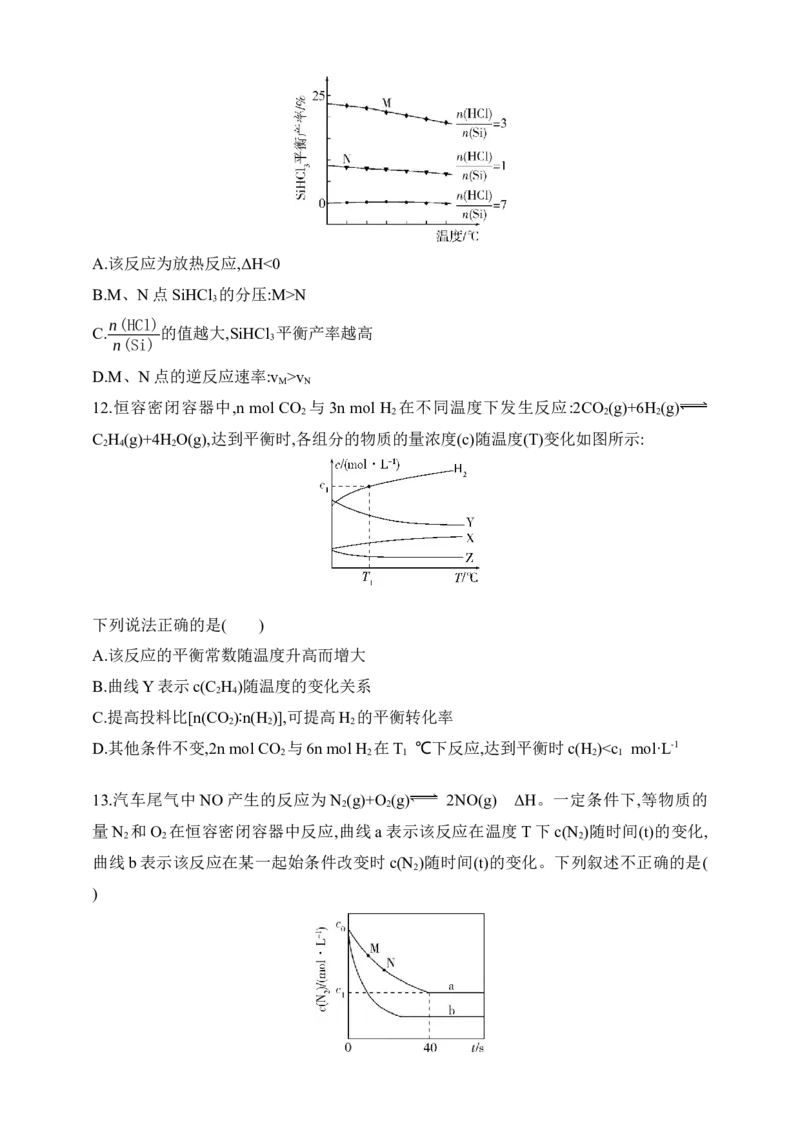
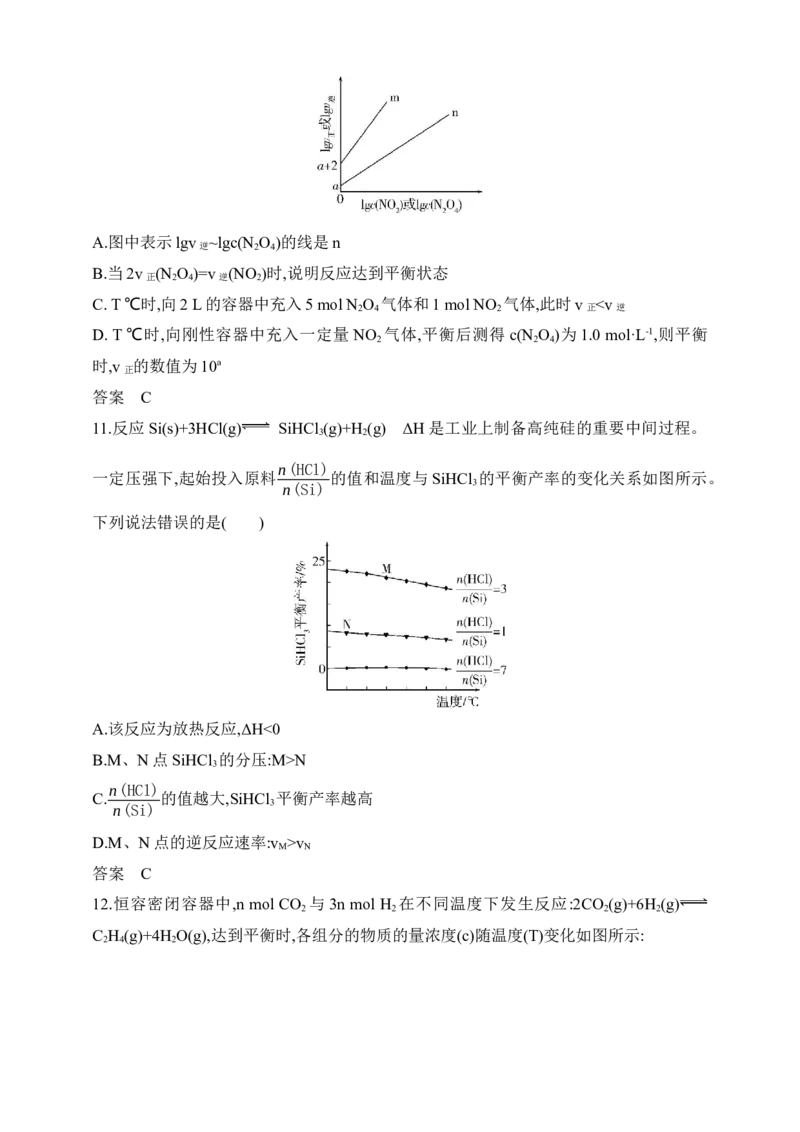
3
n(HCl)
C. 的值越大,SiHCl 平衡产率越高
n(Si) 3
D.M、N点的逆反应速率:v >v
M N
12.恒容密闭容器中,n mol CO 与3n mol H 在不同温度下发生反应:2CO (g)+6H (g)
2 2 2 2
C H (g)+4H O(g),达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:
2 4 2
下列说法正确的是( )
A.该反应的平衡常数随温度升高而增大
B.曲线Y表示c(C H )随温度的变化关系
2 4
C.提高投料比[n(CO )∶n(H )],可提高H 的平衡转化率
2 2 2
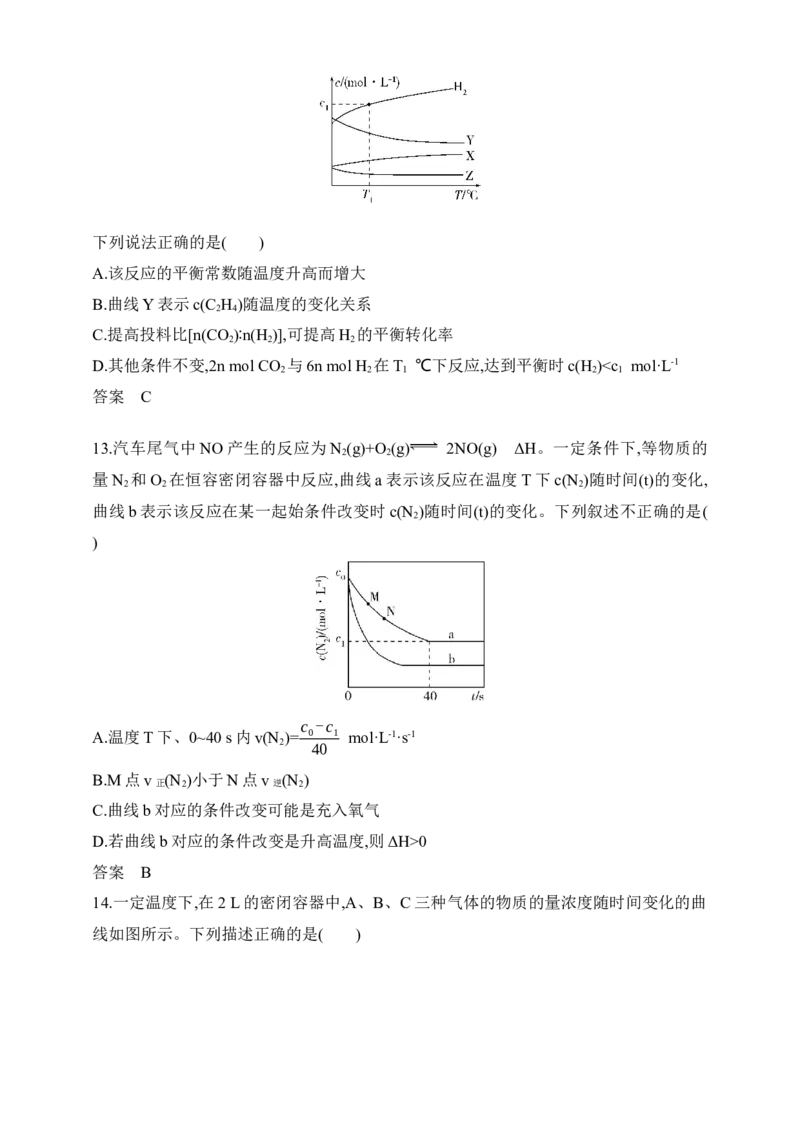
D.其他条件不变,2n mol CO 与6n mol H 在T ℃下反应,达到平衡时c(H )0
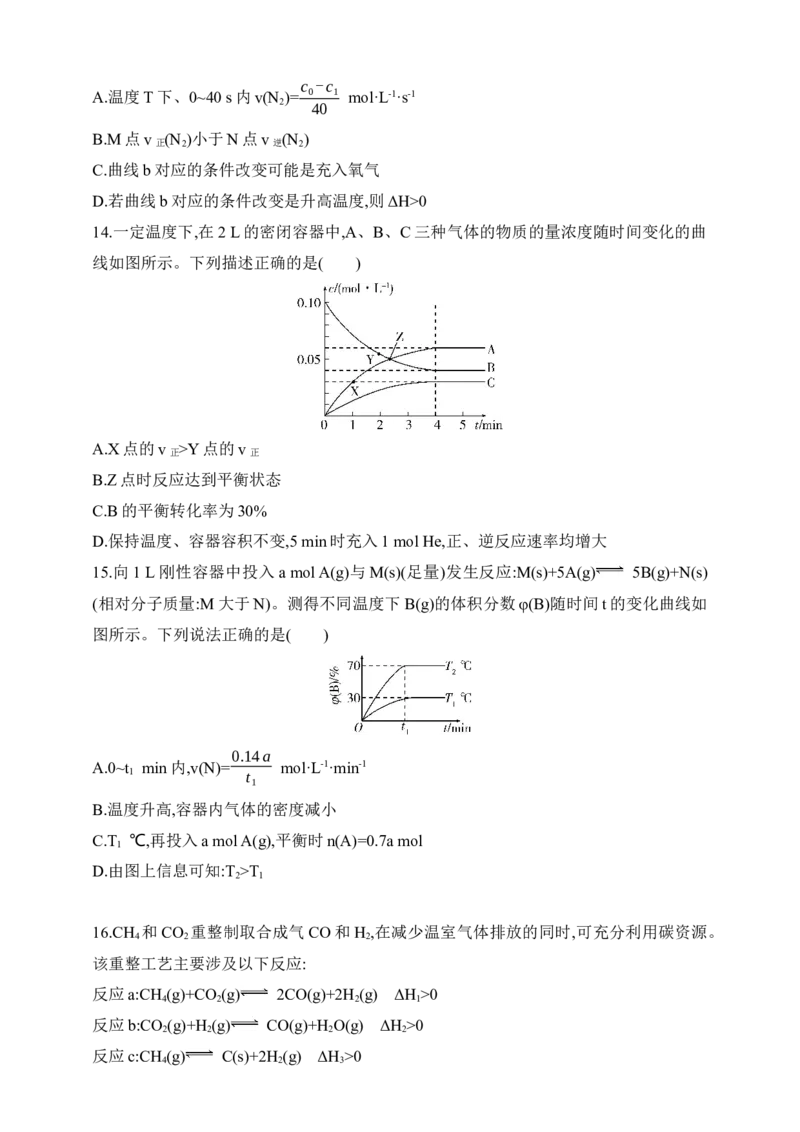
14.一定温度下,在2 L的密闭容器中,A、B、C三种气体的物质的量浓度随时间变化的曲
线如图所示。下列描述正确的是( )
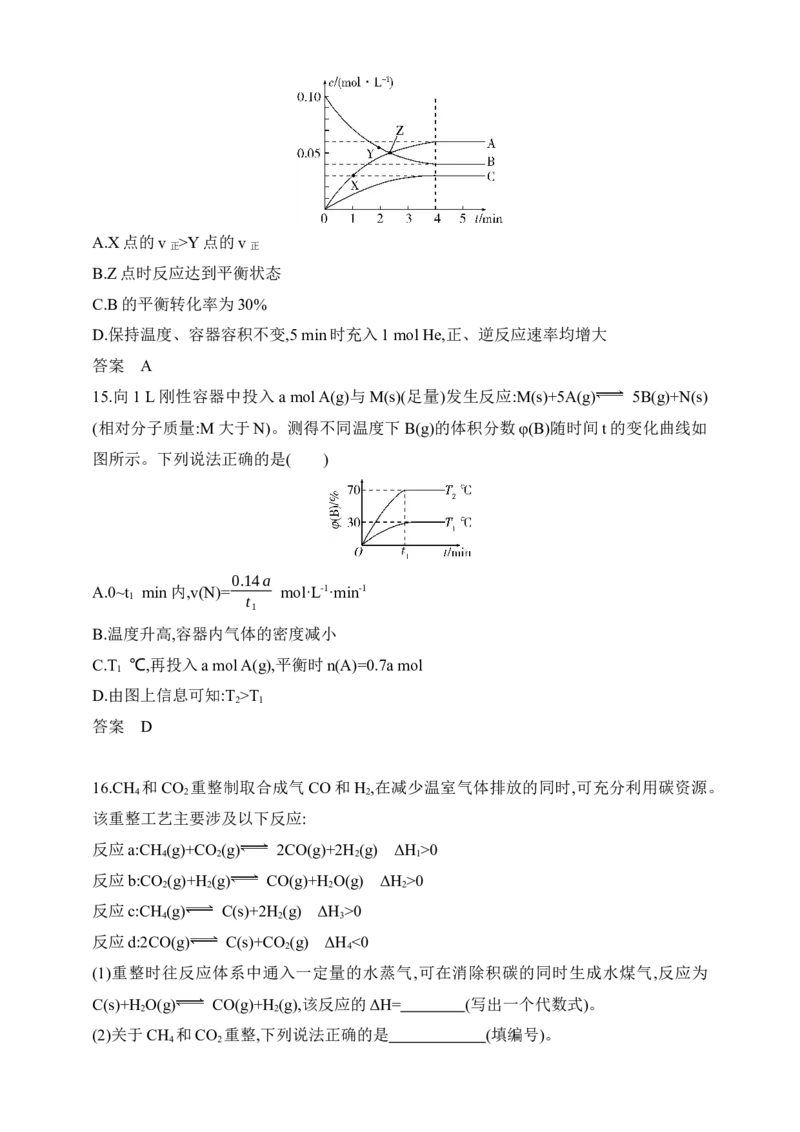
A.X点的v >Y点的v
正 正
B.Z点时反应达到平衡状态
C.B的平衡转化率为30%
D.保持温度、容器容积不变,5 min时充入1 mol He,正、逆反应速率均增大
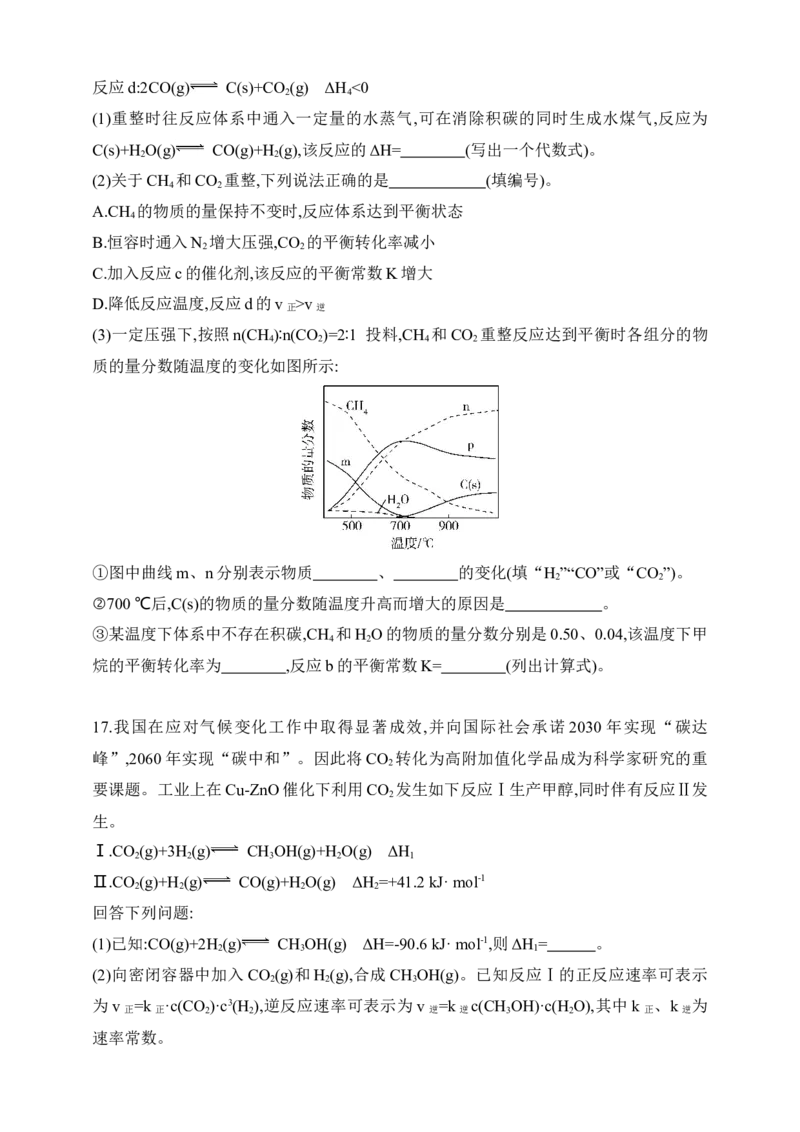
15.向1 L刚性容器中投入a mol A(g)与M(s)(足量)发生反应:M(s)+5A(g) 5B(g)+N(s)
(相对分子质量:M大于N)。测得不同温度下B(g)的体积分数φ(B)随时间t的变化曲线如
图所示。下列说法正确的是( )
0.14a
A.0~t min内,v(N)= mol·L-1·min-1
1 t
1
B.温度升高,容器内气体的密度减小
C.T ℃,再投入a mol A(g),平衡时n(A)=0.7a mol
1
D.由图上信息可知:T >T
2 1
16.CH 和CO 重整制取合成气CO和H ,在减少温室气体排放的同时,可充分利用碳资源。
4 2 2
该重整工艺主要涉及以下反应:
反应a:CH (g)+CO (g) 2CO(g)+2H (g) ΔH >0
4 2 2 1
反应b:CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 2
反应c:CH (g) C(s)+2H (g) ΔH >0
4 2 3反应d:2CO(g) C(s)+CO (g) ΔH <0
2 4
(1)重整时往反应体系中通入一定量的水蒸气,可在消除积碳的同时生成水煤气,反应为
C(s)+H O(g) CO(g)+H (g),该反应的ΔH= (写出一个代数式)。
2 2
(2)关于CH 和CO 重整,下列说法正确的是 (填编号)。
4 2
A.CH 的物质的量保持不变时,反应体系达到平衡状态
4
B.恒容时通入N 增大压强,CO 的平衡转化率减小
2 2
C.加入反应c的催化剂,该反应的平衡常数K增大
D.降低反应温度,反应d的v >v
正 逆
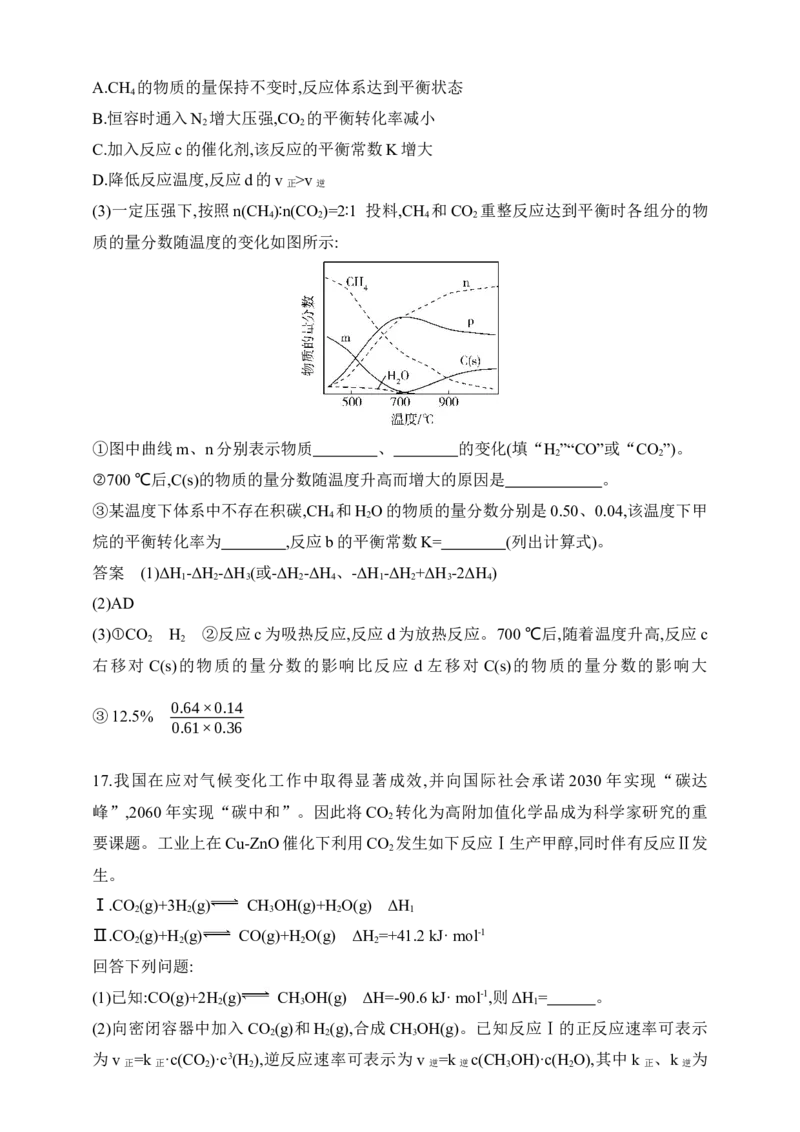
(3)一定压强下,按照n(CH )∶n(CO )=2∶1 投料,CH 和CO 重整反应达到平衡时各组分的物
4 2 4 2
质的量分数随温度的变化如图所示:
①图中曲线m、n分别表示物质 、 的变化(填“H ”“CO”或“CO ”)。
2 2
②700 ℃后,C(s)的物质的量分数随温度升高而增大的原因是 。
③某温度下体系中不存在积碳,CH 和H O的物质的量分数分别是0.50、0.04,该温度下甲
4 2
烷的平衡转化率为 ,反应b的平衡常数K= (列出计算式)。
17.我国在应对气候变化工作中取得显著成效,并向国际社会承诺 2030 年实现“碳达
峰”,2060年实现“碳中和”。因此将CO 转化为高附加值化学品成为科学家研究的重
2
要课题。工业上在Cu-ZnO催化下利用CO 发生如下反应Ⅰ生产甲醇,同时伴有反应Ⅱ发
2
生。
Ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH
2 2 3 2 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH =+41.2 kJ· mol-1
2 2 2 2
回答下列问题:
(1)已知:CO(g)+2H (g) CH OH(g) ΔH=-90.6 kJ· mol-1,则ΔH = 。
2 3 1
(2)向密闭容器中加入CO (g)和H (g),合成CH OH(g)。已知反应Ⅰ的正反应速率可表示
2 2 3
为v =k ·c(CO )·c3(H ),逆反应速率可表示为v =k c(CH OH)·c(H O),其中k 、k 为
正 正 2 2 逆 逆 3 2 正 逆
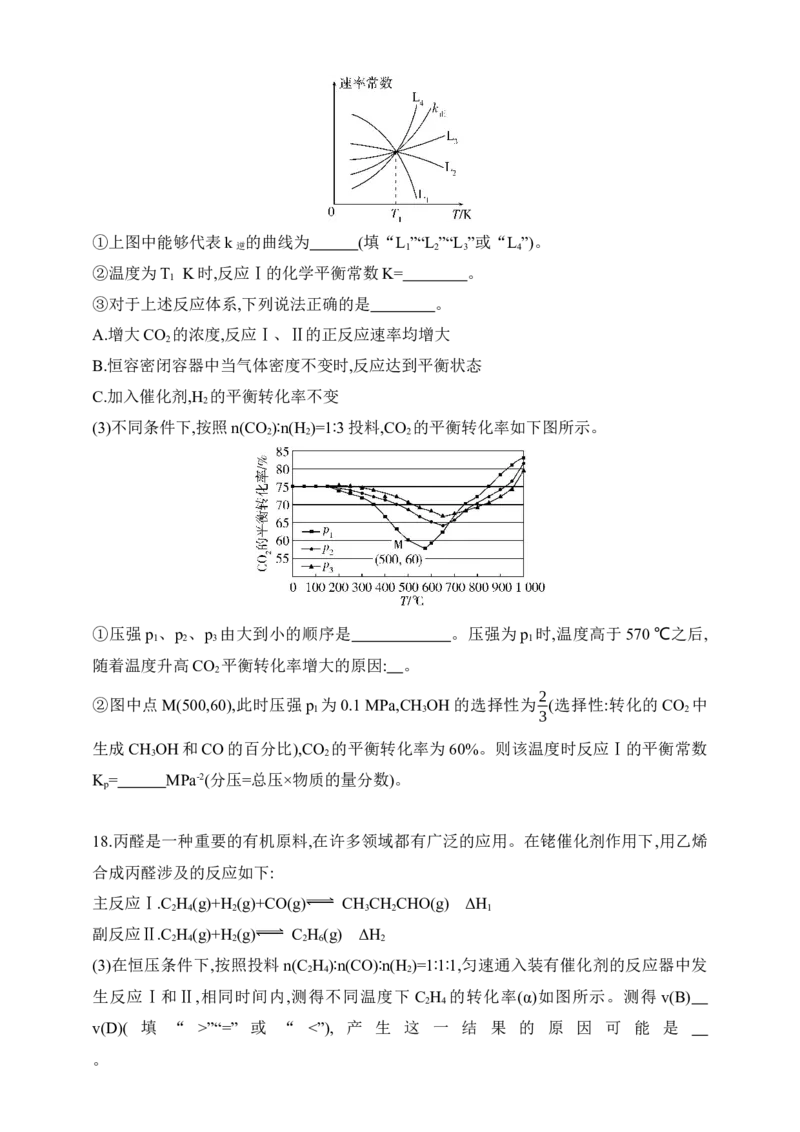
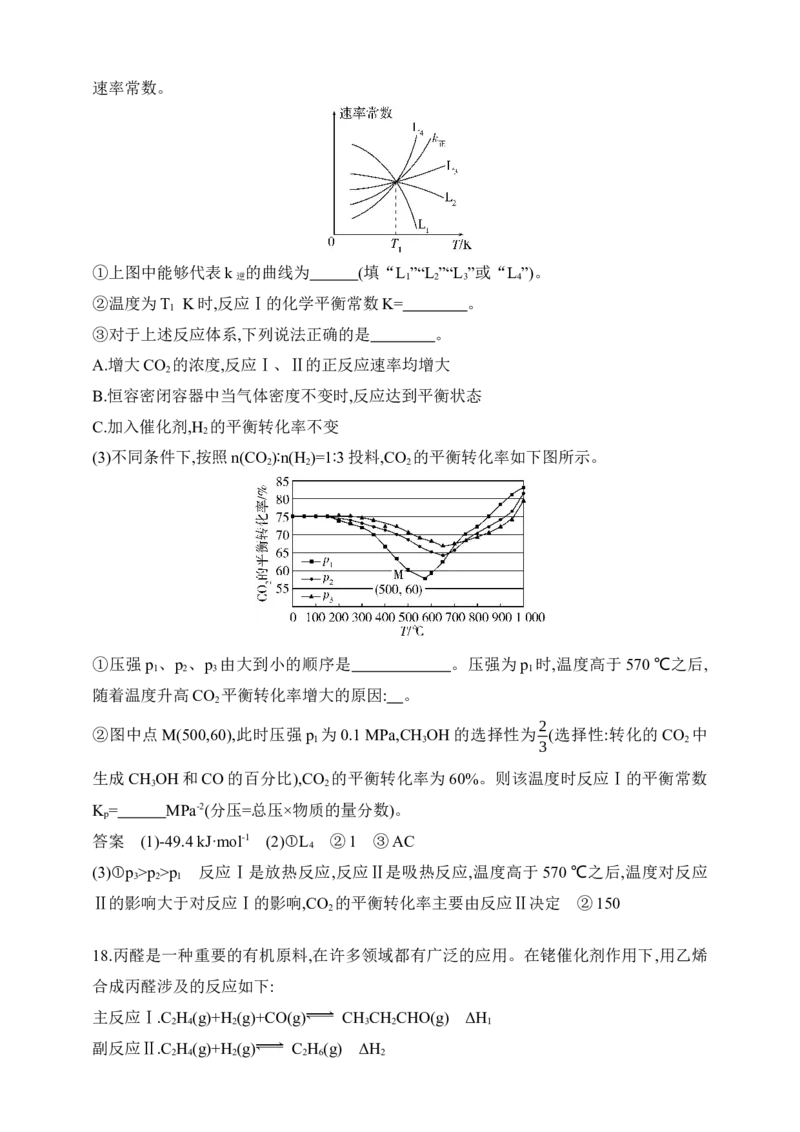
速率常数。①上图中能够代表k 的曲线为 (填“L ”“L ”“L ”或“L ”)。
逆 1 2 3 4
②温度为T K时,反应Ⅰ的化学平衡常数K= 。
1
③对于上述反应体系,下列说法正确的是 。
A.增大CO 的浓度,反应Ⅰ、Ⅱ的正反应速率均增大
2
B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,H 的平衡转化率不变
2
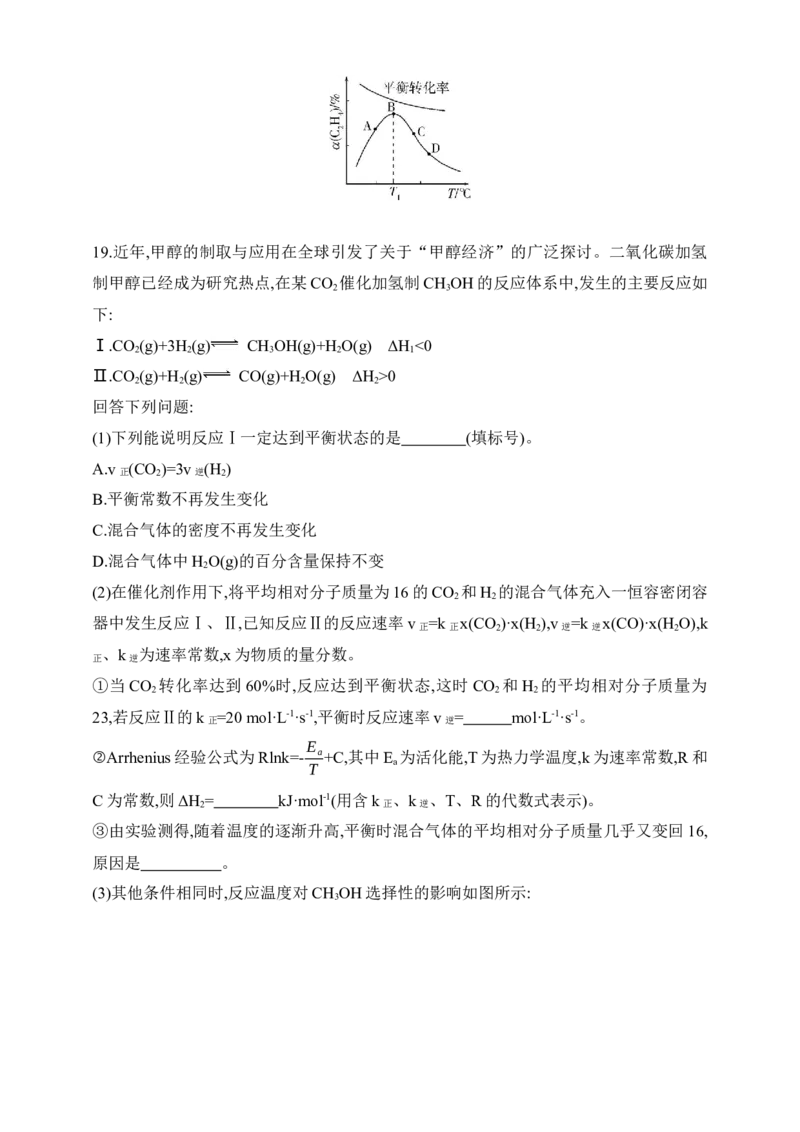
(3)不同条件下,按照n(CO )∶n(H )=1∶3投料,CO 的平衡转化率如下图所示。
2 2 2
①压强p 、p 、p 由大到小的顺序是 。压强为p 时,温度高于570 ℃之后,
1 2 3 1
随着温度升高CO 平衡转化率增大的原因: 。
2
2
②图中点M(500,60),此时压强p 为0.1 MPa,CH OH的选择性为 (选择性:转化的CO 中
1 3 2
3
生成CH OH和CO的百分比),CO 的平衡转化率为60%。则该温度时反应Ⅰ的平衡常数
3 2
K = MPa-2(分压=总压×物质的量分数)。
p
18.丙醛是一种重要的有机原料,在许多领域都有广泛的应用。在铑催化剂作用下,用乙烯
合成丙醛涉及的反应如下:
主反应Ⅰ.C H (g)+H (g)+CO(g) CH CH CHO(g) ΔH
2 4 2 3 2 1
副反应Ⅱ.C H (g)+H (g) C H (g) ΔH
2 4 2 2 6 2
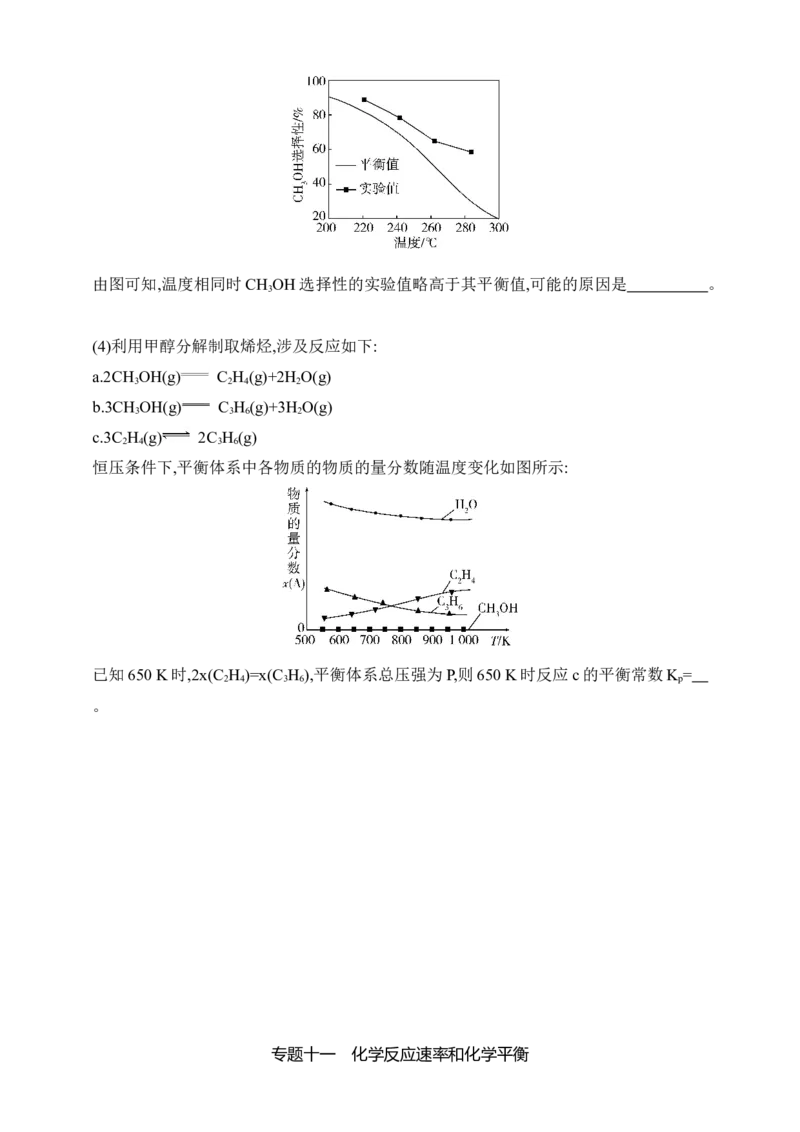
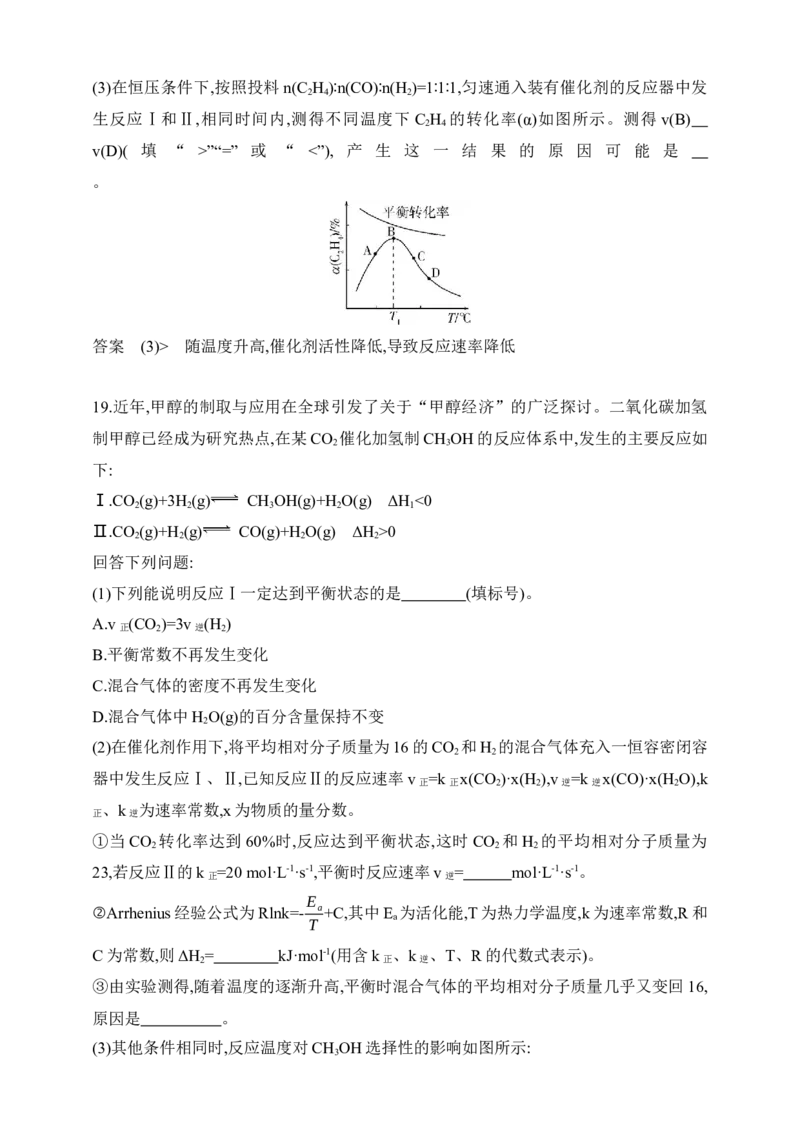
(3)在恒压条件下,按照投料n(C H )∶n(CO)∶n(H )=1∶1∶1,匀速通入装有催化剂的反应器中发
2 4 2
生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 C H 的转化率(α)如图所示。测得 v(B)
2 4
v(D)( 填 “ >”“=” 或 “ <”), 产 生 这 一 结 果 的 原 因 可 能 是
。19.近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。二氧化碳加氢
制甲醇已经成为研究热点,在某CO 催化加氢制CH OH的反应体系中,发生的主要反应如
2 3
下:
Ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH <0
2 2 3 2 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 2
回答下列问题:
(1)下列能说明反应Ⅰ一定达到平衡状态的是 (填标号)。
A.v (CO )=3v (H )
正 2 逆 2
B.平衡常数不再发生变化
C.混合气体的密度不再发生变化
D.混合气体中H O(g)的百分含量保持不变
2
(2)在催化剂作用下,将平均相对分子质量为16的CO 和H 的混合气体充入一恒容密闭容
2 2
器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v =k x(CO )·x(H ),v =k x(CO)·x(H O),k
正 正 2 2 逆 逆 2
、k 为速率常数,x为物质的量分数。
正 逆
①当CO 转化率达到60%时,反应达到平衡状态,这时CO 和H 的平均相对分子质量为
2 2 2
23,若反应Ⅱ的k =20 mol·L-1·s-1,平衡时反应速率v = mol·L-1·s-1。
正 逆
E
②Arrhenius经验公式为Rlnk=- a+C,其中E 为活化能,T为热力学温度,k为速率常数,R和
a
T
C为常数,则ΔH = kJ·mol-1(用含k 、k 、T、R的代数式表示)。
2 正 逆
③由实验测得,随着温度的逐渐升高,平衡时混合气体的平均相对分子质量几乎又变回16,
原因是 。
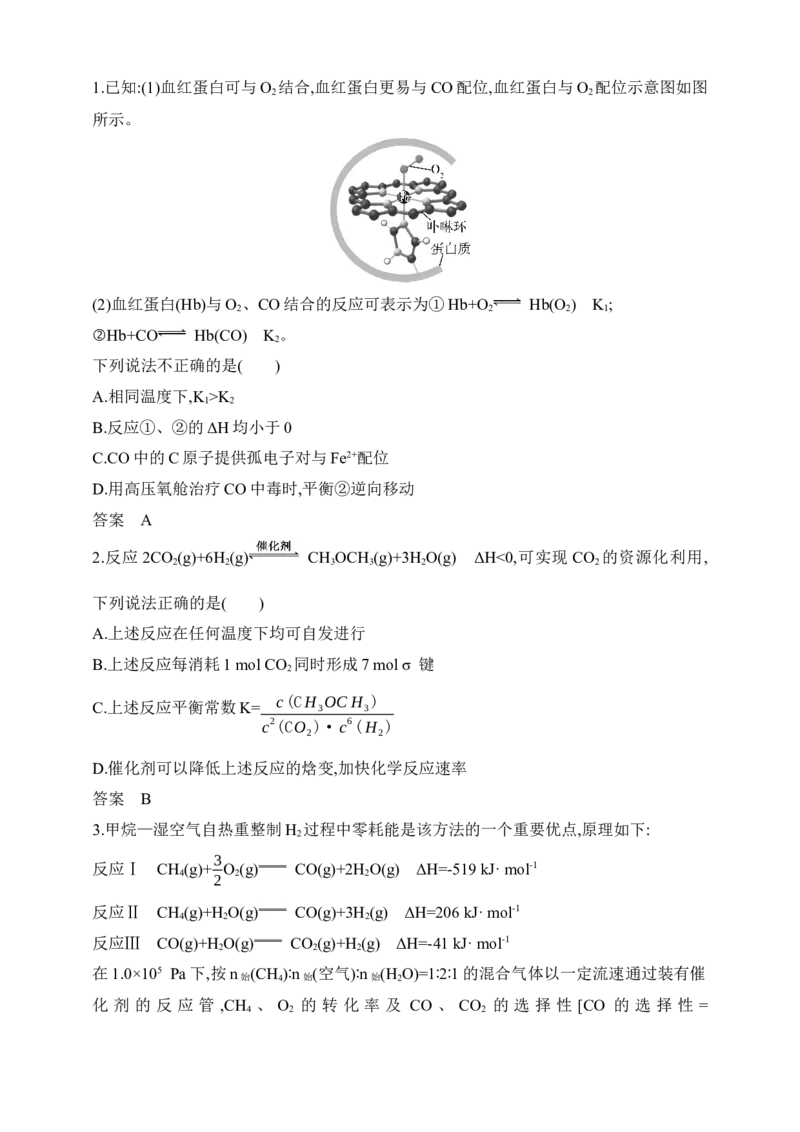
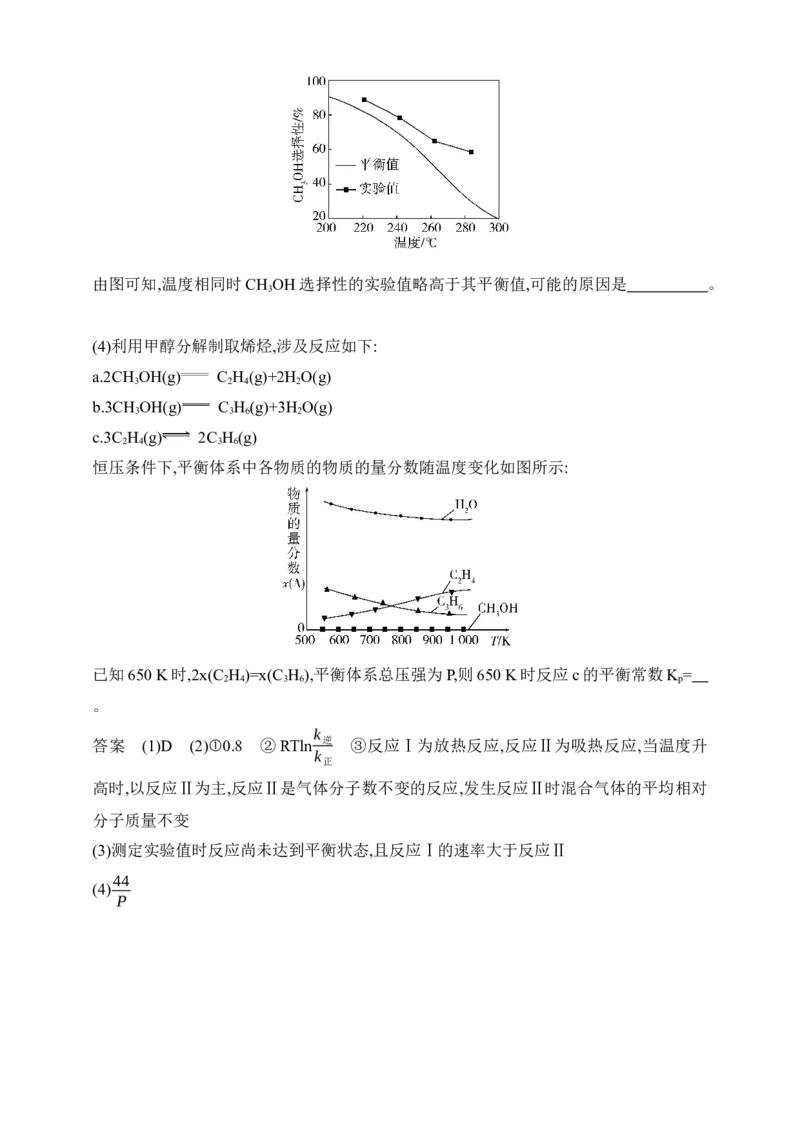
(3)其他条件相同时,反应温度对CH OH选择性的影响如图所示:
3由图可知,温度相同时CH OH选择性的实验值略高于其平衡值,可能的原因是 。
3
(4)利用甲醇分解制取烯烃,涉及反应如下:
a.2CH OH(g) C H (g)+2H O(g)
3 2 4 2
b.3CH OH(g) C H (g)+3H O(g)
3 3 6 2
c.3C H (g) 2C H (g)
2 4 3 6
恒压条件下,平衡体系中各物质的物质的量分数随温度变化如图所示:
已知650 K时,2x(C H )=x(C H ),平衡体系总压强为P,则650 K时反应c的平衡常数K =
2 4 3 6 p
。
专题十一 化学反应速率和化学平衡1.已知:(1)血红蛋白可与O 结合,血红蛋白更易与CO配位,血红蛋白与O 配位示意图如图
2 2
所示。
(2)血红蛋白(Hb)与O 、CO结合的反应可表示为①Hb+O Hb(O ) K ;
2 2 2 1
②Hb+CO Hb(CO) K 。
2
下列说法不正确的是( )
A.相同温度下,K >K
1 2
B.反应①、②的ΔH均小于0
C.CO中的C原子提供孤电子对与Fe2+配位
D.用高压氧舱治疗CO中毒时,平衡②逆向移动
答案 A
2.反应 2CO (g)+6H (g) CH OCH (g)+3H O(g) ΔH<0,可实现 CO 的资源化利用,
2 2 3 3 2 2
下列说法正确的是( )
A.上述反应在任何温度下均可自发进行
B.上述反应每消耗1 mol CO 同时形成7 mol σ 键
2
c(CH OCH )
C.上述反应平衡常数K=
3 3
c2(CO )·c6(H )
2 2
D.催化剂可以降低上述反应的焓变,加快化学反应速率
答案 B
3.甲烷—湿空气自热重整制H 过程中零耗能是该方法的一个重要优点,原理如下:
2
3
反应Ⅰ CH (g)+ O (g) CO(g)+2H O(g) ΔH=-519 kJ· mol-1
4 2 2
2
反应Ⅱ CH (g)+H O(g) CO(g)+3H (g) ΔH=206 kJ· mol-1
4 2 2
反应Ⅲ CO(g)+H O(g) CO (g)+H (g) ΔH=-41 kJ· mol-1
2 2 2
在1.0×105 Pa下,按n (CH )∶n (空气)∶n (H O)=1∶2∶1的混合气体以一定流速通过装有催
始 4 始 始 2
化 剂 的 反 应 管 ,CH 、 O 的 转 化 率 及 CO 、 CO 的 选 择 性 [CO 的 选 择 性 =
4 2 2n (CO) ×100%]与温度的关系如图所示。下列说法错误的是( )
生成
n (CO)+n (CO )
生成 生成 2
A.图中曲线②表示O 的转化率随温度的变化关系
2
B.由图可知,温度升高,CO选择性增大
C.975 K时,改用高效催化剂能提高平衡时CO 的选择性
2
D.其他条件不变,增大n(H O)的值可提高CH 的转化率
2 4
n(CH )
4
答案 C
4. CO -H 催化重整可获得CH OH。其主要反应如下。
2 2 3
反应Ⅰ:CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-53.7 kJ· mol-1
2 2 3 2 1
反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH =+41 kJ· mol-1
2 2 2 2
若仅考虑上述反应,在5.0 MPa、n (CO )∶n (H )=1∶3时,原料按一定流速通过反应器,达到
始 2 始 2
平衡时,CO 的转化率和 CH OH 的选择性随温度变化如图所示。CH OH 的选择性=
2 3 3
n (CH OH)×100%,下列说法正确的是( )
生成 3
n (CO )
消耗 2
A.其他条件不变,升高温度,CO 的平衡转化率增大
2
B.其他条件不变,T>236 ℃时,曲线下降的可能原因是反应Ⅰ正向进行的程度减弱
C.一定温度下,增大n (CO )∶n (H )可提高CO 的平衡转化率
始 2 始 2 2
D.研发高温高效催化剂可提高平衡时CH OH的选择性
3
答案 B5.在恒温恒容的密闭容器中发生反应 2NH (g)+CO (g) CO(NH ) (s)+H O(g) ΔH<0,T
3 2 2 2 2
℃时平衡常数为K,下列说法正确的是( )
A.该反应在任何温度下都可自发进行
B.T ℃时,若
c(H
2
O)
8后,总反应的速率常数k基本不变
答案 A
8. (2023湘潭二模,13)T ℃时,含等浓度的AgNO 与Fe(NO ) 的混合溶液中发生反应Fe2+
3 3 2
(aq)+Ag+(aq) Fe3+(aq)+Ag(s) ΔH<0,t s时,改变某一外界条件继续反应至t s(t =4t )
1 2 2 1
时,溶液中c(Ag+)和c(Fe3+)随时间的变化关系如图所示。下列说法正确的是( )
已知:T ℃时,该反应的化学平衡常数K=1。
A.若t s时未改变外界条件,则此时反应未平衡
1
B.若t s时反应达到平衡,则t 时刻改变的条件可能为升温
2 1
C.若始终保持温度不变,则平均反应速率 > ( 表示0~t s内Fe2+的平均反应速率, 表
v v v 1 v
t t t t
1 2 1 2
示0~t s内Fe2+的平均反应速率)
2
0.04
D.0~t s内Ag+的平均反应速率为 mol·L-1·s-1
2 t
2
答案 C
13. (2024届雅礼中学第一次月考,14)在催化剂作用下,CO 氧化C H 可获得C H 。其主
2 2 6 2 4
要化学方程式如下:
反应Ⅰ.CO (g)+C H (g) C H (g)+CO(g)+H O(g) ΔH =+177 kJ·mol-1
2 2 6 2 4 2 1
反应Ⅱ.2CO (g)+C H (g) 4CO(g)+3H (g) ΔH =+430 kJ·mol-1
2 2 6 2 2
压强分别为p 、p 时,将2 mol C H 和2 mol CO 的混合气体置于密闭容器中反应,不同温
1 2 2 6 2
度下体系中乙烷的平衡转化率、乙烯的选择性[C H 的选择性= n (C H ) ×100%]如
2 4 生成 2 4
n (C H )
总转化 2 6
图所示。下列说法正确的是( )A.p >p
1 2
B.压强为p 、温度为210 ℃时,反应达平衡时,n (CO)=n (C H )
1 生成 生成 2 4
C.C H 的选择性下降的原因可能是随着温度的升高,反应Ⅱ中生成的CO抑制了反应Ⅰ的
2 4
进行
D.研发低温下C H 转化率高和C H 选择性高的催化剂,可以提高平衡时C H 的产率
2 6 2 4 2 4
答案 C
9.利用反应2CO(g)+SO (g) 2CO (g)+S(l) ΔH<0可实现从燃煤烟气中回收硫。向三
2 2
个体积相同的恒容密闭容器中各通入2 mol CO(g)和1 mol SO (g)发生反应,反应体系的总
2
压强随时间的变化如图所示。下列说法错误的是( )
A.实验b中,40 min内CO的平均反应速率为2.0 kPa·min-1
B.与实验a相比,实验b改变的条件是加入催化剂
C.实验b中SO 的平衡转化率是75%
2
D.实验a、b、c相应条件下平衡常数:K =K N
3
n(HCl)
C. 的值越大,SiHCl 平衡产率越高
n(Si) 3
D.M、N点的逆反应速率:v >v
M N
答案 C
12.恒容密闭容器中,n mol CO 与3n mol H 在不同温度下发生反应:2CO (g)+6H (g)
2 2 2 2
C H (g)+4H O(g),达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:
2 4 2下列说法正确的是( )
A.该反应的平衡常数随温度升高而增大
B.曲线Y表示c(C H )随温度的变化关系
2 4
C.提高投料比[n(CO )∶n(H )],可提高H 的平衡转化率
2 2 2
D.其他条件不变,2n mol CO 与6n mol H 在T ℃下反应,达到平衡时c(H )0
答案 B
14.一定温度下,在2 L的密闭容器中,A、B、C三种气体的物质的量浓度随时间变化的曲
线如图所示。下列描述正确的是( )A.X点的v >Y点的v
正 正
B.Z点时反应达到平衡状态
C.B的平衡转化率为30%
D.保持温度、容器容积不变,5 min时充入1 mol He,正、逆反应速率均增大
答案 A
15.向1 L刚性容器中投入a mol A(g)与M(s)(足量)发生反应:M(s)+5A(g) 5B(g)+N(s)
(相对分子质量:M大于N)。测得不同温度下B(g)的体积分数φ(B)随时间t的变化曲线如
图所示。下列说法正确的是( )
0.14a
A.0~t min内,v(N)= mol·L-1·min-1
1 t
1
B.温度升高,容器内气体的密度减小
C.T ℃,再投入a mol A(g),平衡时n(A)=0.7a mol
1
D.由图上信息可知:T >T
2 1
答案 D
16.CH 和CO 重整制取合成气CO和H ,在减少温室气体排放的同时,可充分利用碳资源。
4 2 2
该重整工艺主要涉及以下反应:
反应a:CH (g)+CO (g) 2CO(g)+2H (g) ΔH >0
4 2 2 1
反应b:CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 2
反应c:CH (g) C(s)+2H (g) ΔH >0
4 2 3
反应d:2CO(g) C(s)+CO (g) ΔH <0
2 4
(1)重整时往反应体系中通入一定量的水蒸气,可在消除积碳的同时生成水煤气,反应为
C(s)+H O(g) CO(g)+H (g),该反应的ΔH= (写出一个代数式)。
2 2
(2)关于CH 和CO 重整,下列说法正确的是 (填编号)。
4 2A.CH 的物质的量保持不变时,反应体系达到平衡状态
4
B.恒容时通入N 增大压强,CO 的平衡转化率减小
2 2
C.加入反应c的催化剂,该反应的平衡常数K增大
D.降低反应温度,反应d的v >v
正 逆
(3)一定压强下,按照n(CH )∶n(CO )=2∶1 投料,CH 和CO 重整反应达到平衡时各组分的物
4 2 4 2
质的量分数随温度的变化如图所示:
①图中曲线m、n分别表示物质 、 的变化(填“H ”“CO”或“CO ”)。
2 2
②700 ℃后,C(s)的物质的量分数随温度升高而增大的原因是 。
③某温度下体系中不存在积碳,CH 和H O的物质的量分数分别是0.50、0.04,该温度下甲
4 2
烷的平衡转化率为 ,反应b的平衡常数K= (列出计算式)。
答案 (1)ΔH -ΔH -ΔH (或-ΔH -ΔH 、-ΔH -ΔH +ΔH -2ΔH )
1 2 3 2 4 1 2 3 4
(2)AD
(3)①CO H ②反应c为吸热反应,反应d为放热反应。700 ℃后,随着温度升高,反应c
2 2
右移对 C(s)的物质的量分数的影响比反应 d 左移对 C(s)的物质的量分数的影响大
0.64×0.14
③12.5%
0.61×0.36
17.我国在应对气候变化工作中取得显著成效,并向国际社会承诺 2030 年实现“碳达
峰”,2060年实现“碳中和”。因此将CO 转化为高附加值化学品成为科学家研究的重
2
要课题。工业上在Cu-ZnO催化下利用CO 发生如下反应Ⅰ生产甲醇,同时伴有反应Ⅱ发
2
生。
Ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH
2 2 3 2 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH =+41.2 kJ· mol-1
2 2 2 2
回答下列问题:
(1)已知:CO(g)+2H (g) CH OH(g) ΔH=-90.6 kJ· mol-1,则ΔH = 。
2 3 1
(2)向密闭容器中加入CO (g)和H (g),合成CH OH(g)。已知反应Ⅰ的正反应速率可表示
2 2 3
为v =k ·c(CO )·c3(H ),逆反应速率可表示为v =k c(CH OH)·c(H O),其中k 、k 为
正 正 2 2 逆 逆 3 2 正 逆速率常数。
①上图中能够代表k 的曲线为 (填“L ”“L ”“L ”或“L ”)。
逆 1 2 3 4
②温度为T K时,反应Ⅰ的化学平衡常数K= 。
1
③对于上述反应体系,下列说法正确的是 。
A.增大CO 的浓度,反应Ⅰ、Ⅱ的正反应速率均增大
2
B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,H 的平衡转化率不变
2
(3)不同条件下,按照n(CO )∶n(H )=1∶3投料,CO 的平衡转化率如下图所示。
2 2 2
①压强p 、p 、p 由大到小的顺序是 。压强为p 时,温度高于570 ℃之后,
1 2 3 1
随着温度升高CO 平衡转化率增大的原因: 。
2
2
②图中点M(500,60),此时压强p 为0.1 MPa,CH OH的选择性为 (选择性:转化的CO 中
1 3 2
3
生成CH OH和CO的百分比),CO 的平衡转化率为60%。则该温度时反应Ⅰ的平衡常数
3 2
K = MPa-2(分压=总压×物质的量分数)。
p
答案 (1)-49.4 kJ·mol-1 (2)①L ②1 ③AC
4
(3)①p >p >p 反应Ⅰ是放热反应,反应Ⅱ是吸热反应,温度高于570 ℃之后,温度对反应
3 2 1
Ⅱ的影响大于对反应Ⅰ的影响,CO 的平衡转化率主要由反应Ⅱ决定 ②150
2
18.丙醛是一种重要的有机原料,在许多领域都有广泛的应用。在铑催化剂作用下,用乙烯
合成丙醛涉及的反应如下:
主反应Ⅰ.C H (g)+H (g)+CO(g) CH CH CHO(g) ΔH
2 4 2 3 2 1
副反应Ⅱ.C H (g)+H (g) C H (g) ΔH
2 4 2 2 6 2(3)在恒压条件下,按照投料n(C H )∶n(CO)∶n(H )=1∶1∶1,匀速通入装有催化剂的反应器中发
2 4 2
生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 C H 的转化率(α)如图所示。测得 v(B)
2 4
v(D)( 填 “ >”“=” 或 “ <”), 产 生 这 一 结 果 的 原 因 可 能 是
。
答案 (3)> 随温度升高,催化剂活性降低,导致反应速率降低
19.近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。二氧化碳加氢
制甲醇已经成为研究热点,在某CO 催化加氢制CH OH的反应体系中,发生的主要反应如
2 3
下:
Ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH <0
2 2 3 2 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 2
回答下列问题:
(1)下列能说明反应Ⅰ一定达到平衡状态的是 (填标号)。
A.v (CO )=3v (H )
正 2 逆 2
B.平衡常数不再发生变化
C.混合气体的密度不再发生变化
D.混合气体中H O(g)的百分含量保持不变
2
(2)在催化剂作用下,将平均相对分子质量为16的CO 和H 的混合气体充入一恒容密闭容
2 2
器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v =k x(CO )·x(H ),v =k x(CO)·x(H O),k
正 正 2 2 逆 逆 2
、k 为速率常数,x为物质的量分数。
正 逆
①当CO 转化率达到60%时,反应达到平衡状态,这时CO 和H 的平均相对分子质量为
2 2 2
23,若反应Ⅱ的k =20 mol·L-1·s-1,平衡时反应速率v = mol·L-1·s-1。
正 逆
E
②Arrhenius经验公式为Rlnk=- a+C,其中E 为活化能,T为热力学温度,k为速率常数,R和
a
T
C为常数,则ΔH = kJ·mol-1(用含k 、k 、T、R的代数式表示)。
2 正 逆
③由实验测得,随着温度的逐渐升高,平衡时混合气体的平均相对分子质量几乎又变回16,
原因是 。
(3)其他条件相同时,反应温度对CH OH选择性的影响如图所示:
3由图可知,温度相同时CH OH选择性的实验值略高于其平衡值,可能的原因是 。
3
(4)利用甲醇分解制取烯烃,涉及反应如下:
a.2CH OH(g) C H (g)+2H O(g)
3 2 4 2
b.3CH OH(g) C H (g)+3H O(g)
3 3 6 2
c.3C H (g) 2C H (g)
2 4 3 6
恒压条件下,平衡体系中各物质的物质的量分数随温度变化如图所示:
已知650 K时,2x(C H )=x(C H ),平衡体系总压强为P,则650 K时反应c的平衡常数K =
2 4 3 6 p
。
k
答案 (1)D (2)①0.8 ②RTln 逆 ③反应Ⅰ为放热反应,反应Ⅱ为吸热反应,当温度升
k
正
高时,以反应Ⅱ为主,反应Ⅱ是气体分子数不变的反应,发生反应Ⅱ时混合气体的平均相对
分子质量不变
(3)测定实验值时反应尚未达到平衡状态,且反应Ⅰ的速率大于反应Ⅱ
44
(4)
P