文档内容
专题十六 沉淀溶解平衡
一、基础知识总结
1.固体溶质的溶解性
不同物质在水中的溶解度不同,有的很大,有的很小,但无论大小,都有一定的溶解度。在 20 ℃时,
物质的溶解度与溶解性的关系如下:
2.沉淀溶解平衡
(1)含义
在一定温度下的水溶液中,当沉淀溶解和生成的速率相等时,即建立了溶解平衡状态。
(2)建立过程
固体溶质溶液中的溶质
(3)特征
(4)影响因素
3.沉淀溶解平衡的应用
(1)沉淀的生成
①调节pH法
如除去CuCl 溶液中的杂质FeCl ,可以向溶液中加入CuO,调节溶液的pH,使Fe3+形成Fe(OH) 沉淀
2 3 3
而除去。离子方程式为Fe3++3HOFe(OH) +3H+,CuO+2H+===Cu2++HO。
2 3 2
②沉淀剂法
如用HS沉淀Hg2+的离子方程式为HS+Hg2+===HgS↓+2H+。
2 2(2)沉淀的溶解
①酸溶解法
如CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++CO↑+HO。
3 3 2 2
Cu(OH) 溶于稀硫酸,离子方程式为Cu(OH) +2H+===Cu2++2HO。
2 2 2
②盐溶液溶解法
如Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
(3)沉淀的转化
①实质:沉淀溶解平衡的移动。
②规律:一般来说,溶解度小的沉淀容易转化成溶解度更小的沉淀。沉淀的溶解度差别越大,越容易
转化。
③应用
a.锅炉除垢:将CaSO 转化为CaCO ,离子方程式为
4 3
CaSO(s)+CO(aq)===CaCO (s)+SO(aq)。
4 3
b.矿物转化
CuSO 溶液遇PbS转化为CuS,离子方程式为PbS(s)+Cu2+(aq)===CuS(s)+Pb2+(aq)。
4
【归纳总结】(1)沉淀溶解平衡移动过程是固体溶解和析出的相互转化过程,属于物理变化,但遵循
勒·夏特列原理。
(2)沉淀溶解达到平衡时,再加入该难溶物对平衡无影响。
(3)用沉淀法除杂不可能将杂质离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于 1.0×10
-5 mol·L-1时,沉淀已经完全。
(4)对于化学式中阴、阳离子个数比不同的难溶物,不能直接根据 K 的大小来确定其溶解能力的大小,
sp
需通过计算转化为溶解度。
二、四种曲线
1、溶解度曲线图
溶解度随温度变化曲线 曲线可知信息
** 错误的表达式 **曲线上各点的意义:曲线上任一点都表示饱和溶液,曲
线上方的任一点均表示过饱和溶液,此时有沉淀析出,曲线下方的任一点
均表示不饱和溶液
** 错误的表达式 **曲线的变化趋势:A曲线表示溶解度随温度升高而增
大;B曲线表示溶解度随温度升高而减小;C曲线表示溶解度随温度升高
变化不大
** 错误的表达式 **分离提纯:A(C):蒸发浓缩、冷却结晶、过滤、洗涤、
干燥
C(A):蒸发结晶、趁热过滤
** 错误的表达式 **计算K :对于难溶电解质来说,若知道溶解度的值S
spg,可求出难溶电解质饱和溶液时的浓度c= mol·L-1,进而求出K
sp
2、双曲线
(1)阳离子~阴离子单曲线图:横、纵坐标分别为阳离子或阴离子
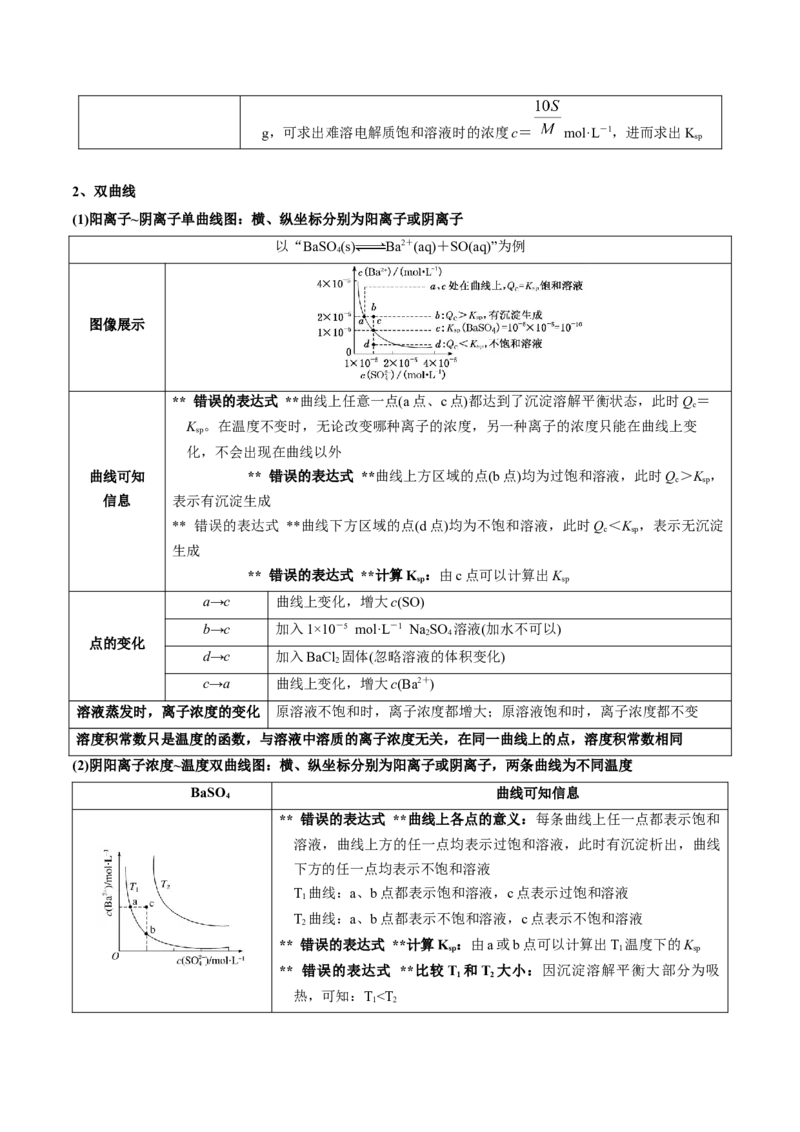
以“BaSO(s) Ba2+(aq)+SO(aq)”为例
4
图像展示
** 错误的表达式 **曲线上任意一点(a点、c点)都达到了沉淀溶解平衡状态,此时Q=
c
K 。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变
sp
化,不会出现在曲线以外
曲线可知 ** 错误的表达式 **曲线上方区域的点(b点)均为过饱和溶液,此时Q>K ,
c sp
信息 表示有沉淀生成
** 错误的表达式 **曲线下方区域的点(d点)均为不饱和溶液,此时Q<K ,表示无沉淀
c sp
生成
** 错误的表达式 **计算K :由c点可以计算出K
sp sp
a→c 曲线上变化,增大c(SO)
b→c 加入1×10-5 mol·L-1 Na SO 溶液(加水不可以)
2 4
点的变化
d→c 加入BaCl 固体(忽略溶液的体积变化)
2
c→a 曲线上变化,增大c(Ba2+)
溶液蒸发时,离子浓度的变化 原溶液不饱和时,离子浓度都增大;原溶液饱和时,离子浓度都不变
溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的点,溶度积常数相同
(2)阴阳离子浓度~温度双曲线图:横、纵坐标分别为阳离子或阴离子,两条曲线为不同温度
BaSO 曲线可知信息
4
** 错误的表达式 **曲线上各点的意义:每条曲线上任一点都表示饱和
溶液,曲线上方的任一点均表示过饱和溶液,此时有沉淀析出,曲线
下方的任一点均表示不饱和溶液
T 曲线:a、b点都表示饱和溶液,c点表示过饱和溶液
1
T 曲线:a、b点都表示不饱和溶液,c点表示不饱和溶液
2
** 错误的表达式 **计算K :由a或b点可以计算出T 温度下的K
sp 1 sp
** 错误的表达式 **比较T 和T 大小:因沉淀溶解平衡大部分为吸
1 2
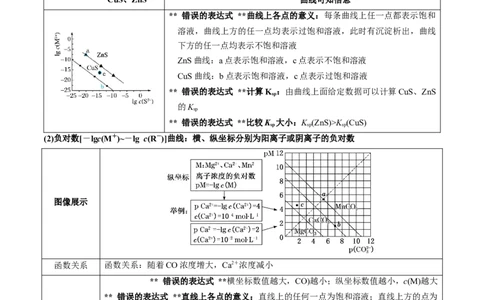
热,可知:TK (CuS)
sp sp sp
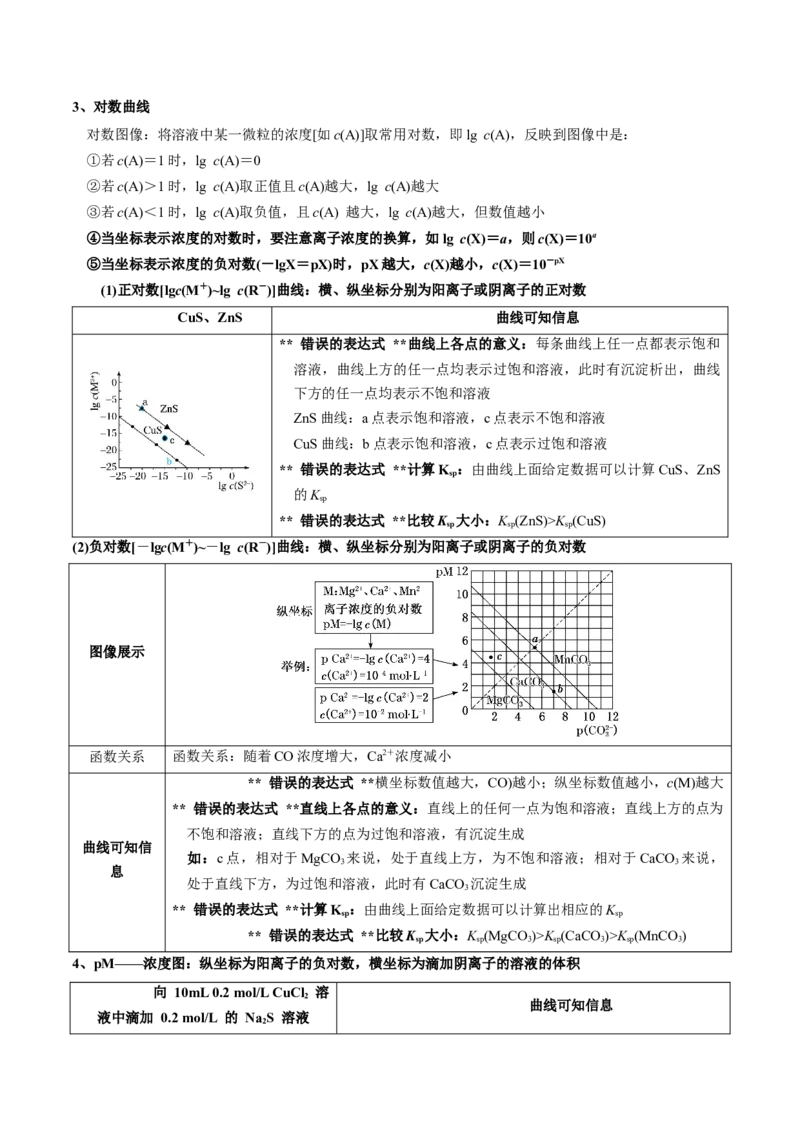
(2)负对数[-lgc(M+)~-lg c(R-)]曲线:横、纵坐标分别为阳离子或阴离子的负对数
图像展示
函数关系 函数关系:随着CO浓度增大,Ca2+浓度减小
** 错误的表达式 **横坐标数值越大,CO)越小;纵坐标数值越小,c(M)越大
** 错误的表达式 **直线上各点的意义:直线上的任何一点为饱和溶液;直线上方的点为
不饱和溶液;直线下方的点为过饱和溶液,有沉淀生成
曲线可知信
如:c点,相对于MgCO 来说,处于直线上方,为不饱和溶液;相对于CaCO 来说,
3 3
息
处于直线下方,为过饱和溶液,此时有CaCO 沉淀生成
3
** 错误的表达式 **计算K :由曲线上面给定数据可以计算出相应的K
sp sp
** 错误的表达式 **比较K 大小:K (MgCO )>K (CaCO )>K (MnCO )
sp sp 3 sp 3 sp 3
4、pM——浓度图:纵坐标为阳离子的负对数,横坐标为滴加阴离子的溶液的体积
向 10mL 0.2 mol/L CuCl 溶
2
曲线可知信息
液中滴加 0.2 mol/L 的 Na S 溶液
2** 错误的表达式 **曲线上各点的意义:曲线上任一点(a、
b、c点)都表示饱和溶液
** 错误的表达式 **计算K :由b点恰好完全反应可知的
sp
c(Cu2+)=10-17.7,进而求出K =10-17.7×10-17.7=10-35.4
sp
** 错误的表达式 **比较a、b、c三点水的电离程度大小
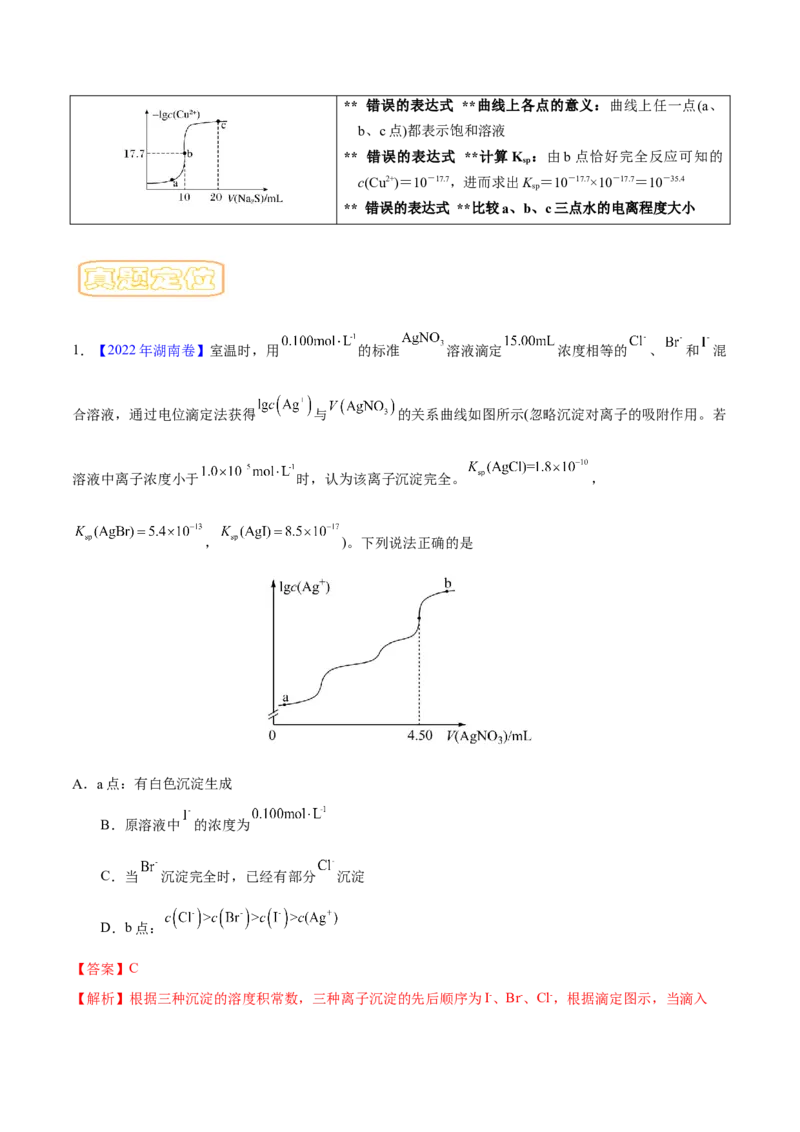
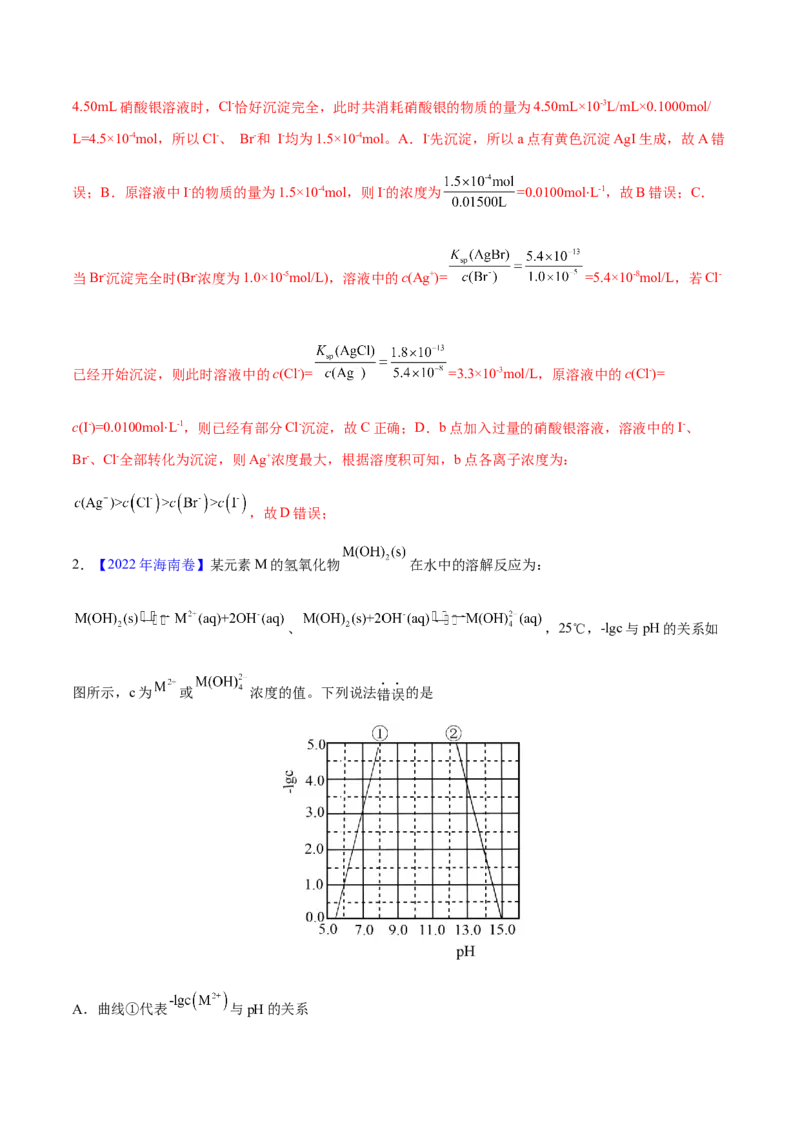
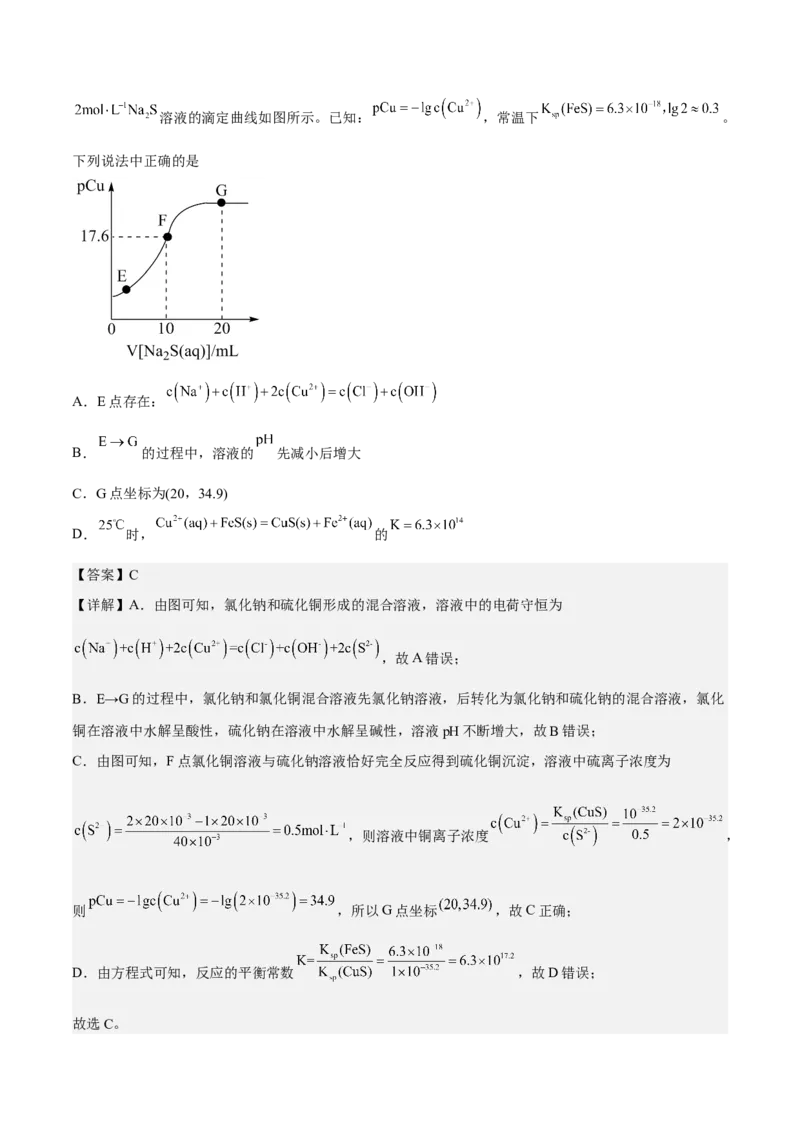
1.【2022年湖南卷】室温时,用 的标准 溶液滴定 浓度相等的 、 和 混
合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。若
溶液中离子浓度小于 时,认为该离子沉淀完全。 ,
, )。下列说法正确的是
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
【答案】C
【解析】根据三种沉淀的溶度积常数,三种离子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,此时共消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/
L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-4mol。A.I-先沉淀,所以a点有黄色沉淀AgI生成,故A错
误;B.原溶液中I-的物质的量为1.5×10-4mol,则I-的浓度为 =0.0100molL-1,故B错误;C.
⋅
当Br-沉淀完全时(Br-浓度为1.0×10-5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若Cl-
已经开始沉淀,则此时溶液中的c(Cl-)= =3.3×10-3mol/L,原溶液中的c(Cl-)=
c(I-)=0.0100molL-1,则已经有部分Cl-沉淀,故C正确;D.b点加入过量的硝酸银溶液,溶液中的I-、
Br-、Cl-全部转化⋅ 为沉淀,则Ag+浓度最大,根据溶度积可知,b点各离子浓度为:
,故D错误;
2.【2022年海南卷】某元素M的氢氧化物 在水中的溶解反应为:
、 ,25℃,-lgc与pH的关系如
图所示,c为 或 浓度的值。下列说法错误的是
A.曲线①代表 与pH的关系B. 的 约为
C.向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 存在
D.向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存
在
【答案】BD
【解析】M(OH) (s) M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) (aq),随着pH增大,c(OH-)
2 2
增大,则c(M2+)减小,c[M(OH) ]增大,即-lg c(M2+)增大,-lg c[M(OH) ]减小,因此曲线①代表-lg c(M2+)
与pH的关系,曲线②代表-lg c[M(OH) ]与pH的关系。A.曲线①代表-lg c(M2+)与pH的关系,A正确;
B.由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,B错误;C.根据图像,
2 sp
pH=9.0时,c(M2+)、c[M(OH) ]均极小,则体系中元素M主要以M(OH) (s)存在,C正确;D.c[M(OH)
2
]=0.1mol/L的溶液中,由于溶解平衡是少量的,因此加入等体积的0.4mol/L的HCl后,体系中元素M仍主
要以M(OH) 存在,D错误。
3.【2022年山东卷】工业上以 为原料生产 ,对其工艺条件进行研究。现有含
的 、 溶液,含 的 、 溶液。在一定pH范围
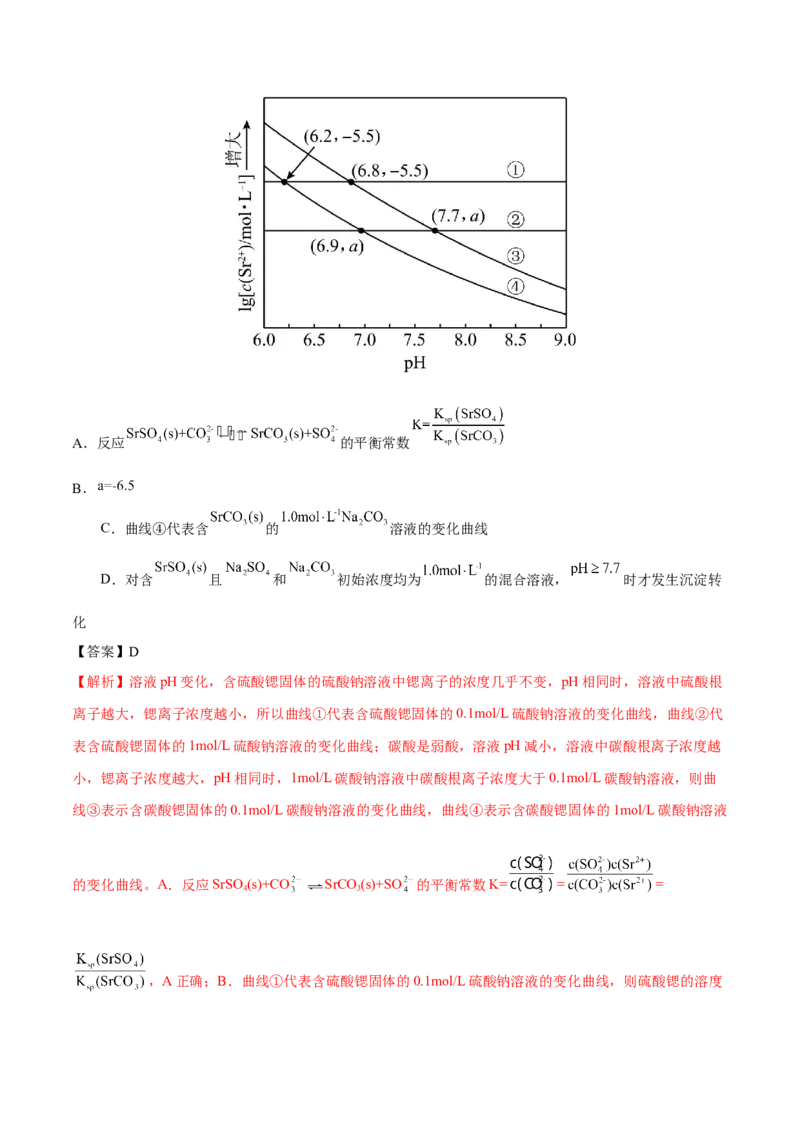
内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是A.反应 的平衡常数
B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀转
化
【答案】D
【解析】溶液pH变化,含硫酸锶固体的硫酸钠溶液中锶离子的浓度几乎不变,pH相同时,溶液中硫酸根
离子越大,锶离子浓度越小,所以曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,曲线②代
表含硫酸锶固体的1mol/L硫酸钠溶液的变化曲线;碳酸是弱酸,溶液pH减小,溶液中碳酸根离子浓度越
小,锶离子浓度越大,pH相同时,1mol/L碳酸钠溶液中碳酸根离子浓度大于0.1mol/L碳酸钠溶液,则曲
线③表示含碳酸锶固体的0.1mol/L碳酸钠溶液的变化曲线,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液
的变化曲线。A.反应SrSO (s)+CO SrCO (s)+SO 的平衡常数K= = =
4 3
,A正确;B.曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶的溶度积K (SrSO )=10—5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度为 =10
sp 4
—6.5,则a为-6.5,B正确;C.曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变化曲线,C正确;D.对
含SrSO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液中锶离子的浓度为10-6, 5,根据图示,
4 2 4 2 3
锶离子的降低,所以 发生沉淀转化,D错误。
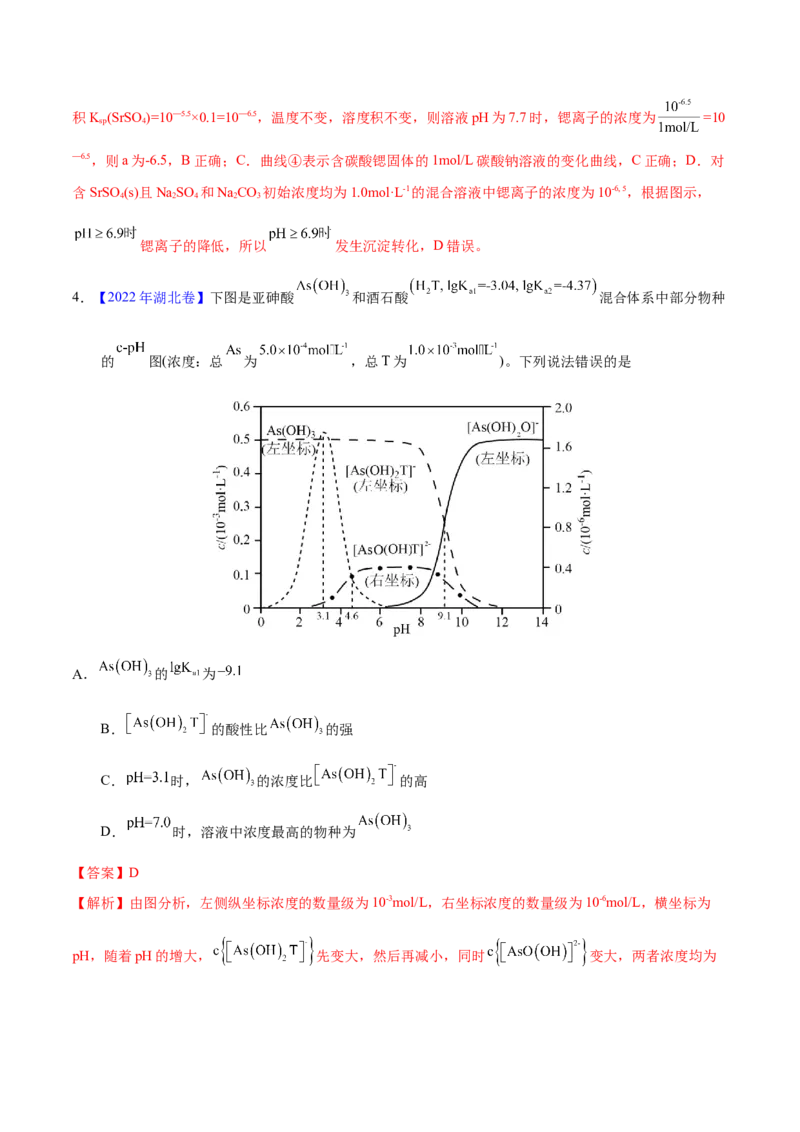
4.【2022年湖北卷】下图是亚砷酸 和酒石酸 混合体系中部分物种
的 图(浓度:总 为 ,总T为 )。下列说法错误的是
A. 的 为
B. 的酸性比 的强
C. 时, 的浓度比 的高
D. 时,溶液中浓度最高的物种为
【答案】D
【解析】由图分析,左侧纵坐标浓度的数量级为10-3mol/L,右坐标浓度的数量级为10-6mol/L,横坐标为
pH,随着pH的增大, 先变大,然后再减小,同时 变大,两者浓度均为右坐标,说明变化的程度很小,当pH=4.6时, = ,Ka=10-4.6。pH继续增
大,则 减小,同时 增大,当pH=9.1时, = ,
,二者用左坐标表示,浓度比较大,说明变化的幅度比较大,但混合溶液中存在着酒石
酸,电离常数远大于亚砷酸,且总T浓度也大于总As。A. ,
,当pH=9.1时, = , ,
为 ,A正确;B. ,当
pH=4.6时, = ,Ka=10-4.6,而由A选项计算得HAsO 的
3 3
,即Ka > Ka1,所以 的酸性比 的强,B正确;C.由图可知
的浓度为左坐标,浓度的数量级为10-3mol/L, 的浓度为右坐标,浓度的数量级为
10-6mol/L,所以 时, 的浓度比 的高,C正确;D.由可知条件,酒石酸
, 的 为 ,即酒石酸的第一部电离常数远大于亚砷酸的第
一步电离常数,所以酒石酸的酸性远强于 ,另外总As的浓度也小于总T的浓度,所以当
时,溶液中浓度最高的物种不是 ,D错误。5.(2021·全国乙卷真题)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化, 不发生
水解。实验发现, 时 为线性关系,如下图中实线所示。
下列叙述错误的是
A.溶液 时,
B.MA的溶度积度积
C.溶液 时,
D.HA的电离常数
【答案】C
【解析】A.由图可知pH=4,即c(H+)=10×10-5mol/L时,c2(M+)=7.5×10-8mol2/L2,c(M+)=
mol/L<3.0×10-4mol/L,A正确;B.由图可知,c(H+)=0时,可看作溶液中有较
大浓度的OH-,此时A-的水解极大地被抑制,溶液中c(M+)=c(A-),则
,B正确;C.设调pH所用的酸为HX,则结合电荷守恒可知
n
,题给等式右边缺阴离子部分nc(Xn-),C错误;D.当 时,由物料守恒知 ,则 ,
,则 ,对应图得此时溶液中
, ,D正确;故选C。
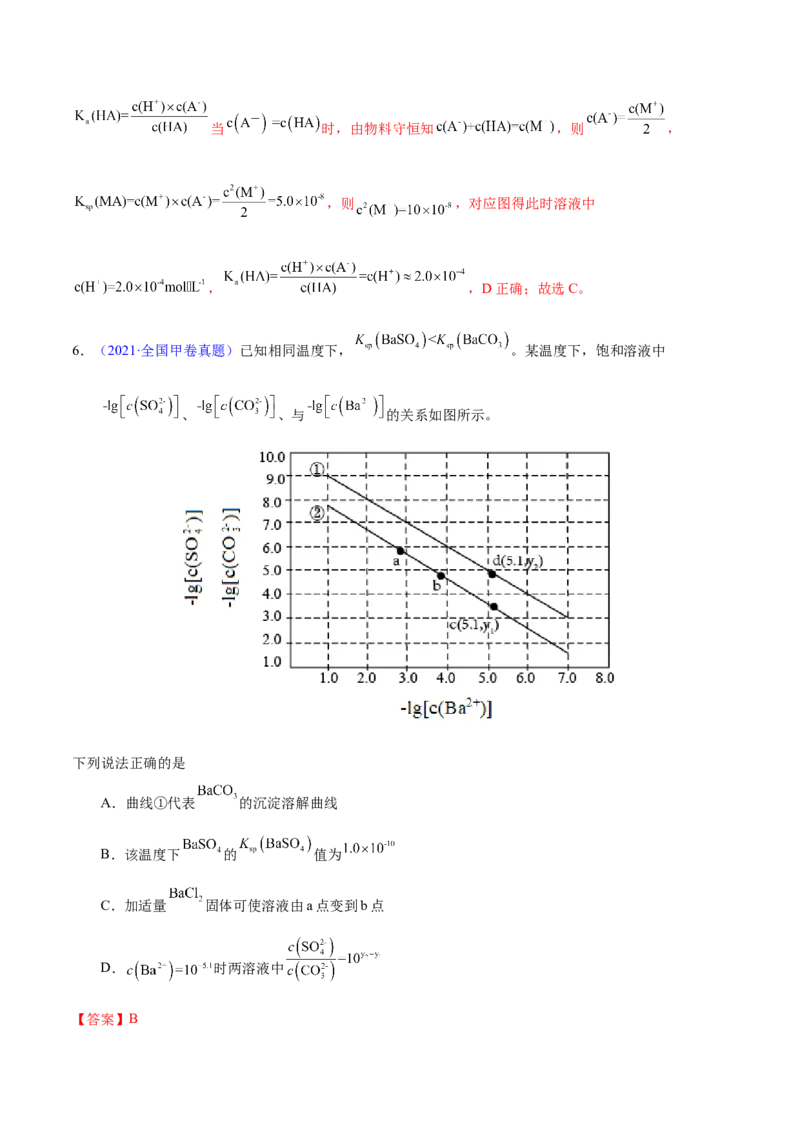
6.(2021·全国甲卷真题)已知相同温度下, 。某温度下,饱和溶液中
、 、与 的关系如图所示。
下列说法正确的是
A.曲线①代表 的沉淀溶解曲线
B.该温度下 的 值为
C.加适量 固体可使溶液由a点变到b点
D. 时两溶液中
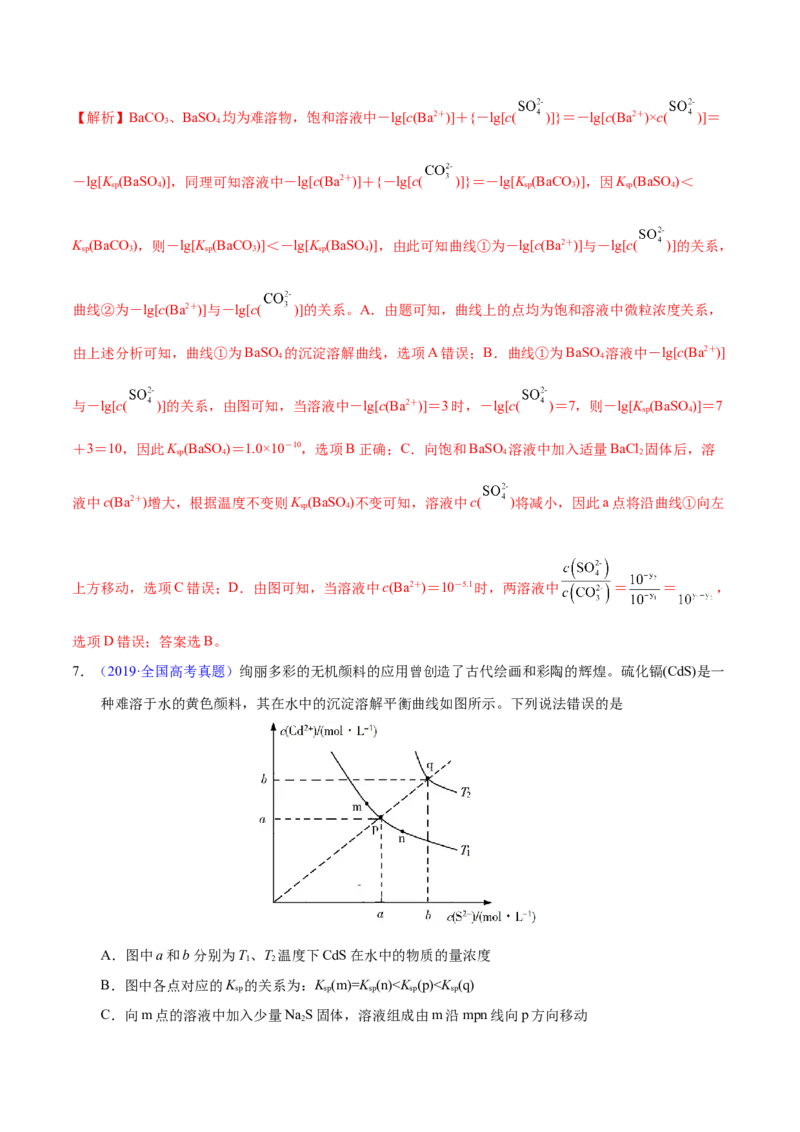
【答案】B【解析】BaCO 、BaSO 均为难溶物,饱和溶液中-lg[c(Ba2+)]+{-lg[c( )]}=-lg[c(Ba2+)×c( )]=
3 4
-lg[K (BaSO)],同理可知溶液中-lg[c(Ba2+)]+{-lg[c( )]}=-lg[K (BaCO)],因K (BaSO)<
sp 4 sp 3 sp 4
K (BaCO),则-lg[K (BaCO)]<-lg[K (BaSO)],由此可知曲线①为-lg[c(Ba2+)]与-lg[c( )]的关系,
sp 3 sp 3 sp 4
曲线②为-lg[c(Ba2+)]与-lg[c( )]的关系。A.由题可知,曲线上的点均为饱和溶液中微粒浓度关系,
由上述分析可知,曲线①为BaSO 的沉淀溶解曲线,选项A错误;B.曲线①为BaSO 溶液中-lg[c(Ba2+)]
4 4
与-lg[c( )]的关系,由图可知,当溶液中-lg[c(Ba2+)]=3时,-lg[c( )=7,则-lg[K (BaSO)]=7
sp 4
+3=10,因此K (BaSO)=1.0×10-10,选项B正确;C.向饱和BaSO 溶液中加入适量BaCl 固体后,溶
sp 4 4 2
液中c(Ba2+)增大,根据温度不变则K (BaSO)不变可知,溶液中c( )将减小,因此a点将沿曲线①向左
sp 4
上方移动,选项C错误;D.由图可知,当溶液中c(Ba2+)=10-5.1时,两溶液中 = = ,
选项D错误;答案选B。
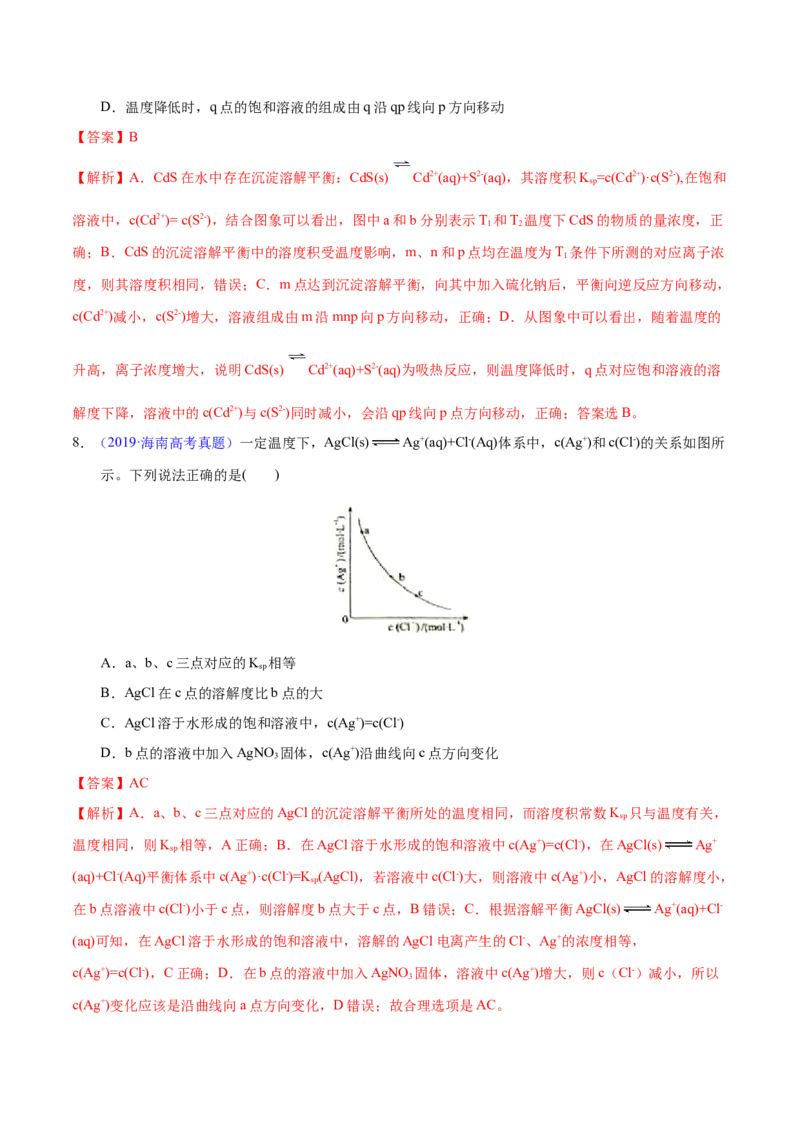
7.(2019·全国高考真题)绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一
种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
A.图中a和b分别为T、T 温度下CdS在水中的物质的量浓度
1 2
B.图中各点对应的K 的关系为:K (m)=K (n)