文档内容
专题十 实验基础
核心考点1.实验安全 化学实验基本操作
1.化学实验安全常识
(1)常见实验事故的处理
意外事故 处理方法
先用干抹布擦净,再用大量水冲洗,然
少量浓硫酸溅到皮肤上
后涂上3%~5%的碳酸氢钠溶液
浓NaOH溶液溅到皮肤上 立即用大量水冲洗,再涂上5%的稀硼酸
酒精等有机物在实验台上着 用湿抹布、石棉或沙子盖灭,不能用水
火 灭火
酸液溅入眼睛 用大量水冲洗,边洗边眨眼睛
苯酚沾到皮肤上 用酒精擦洗
误食重金属盐 服用大量牛奶或蛋清,并及时送往医院
水银洒到桌面或地面上 撒上硫粉并进行处理
(2)认识常用危险化学药品的标志
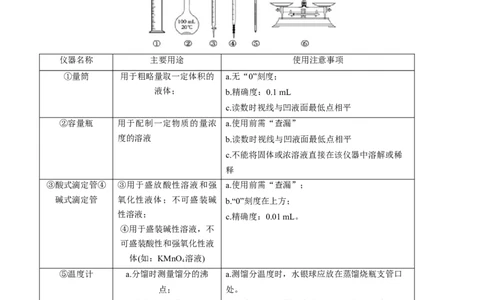
2.常见仪器的识别与使用
(1)可加热的仪器
①试管:加热液体时,体积不能超过其容积的1/3;加热固体时,一般情况下,试管口应略向下倾斜。
②蒸发皿:用于蒸发或浓缩溶液,加热时液体体积不超过其容积的,蒸发浓缩时要用玻璃棒不断搅拌,快
蒸干时(出现大量固体)停止加热。
③坩埚:用于灼烧固体物质,把坩埚放在三脚架上的泥三角上加热,取放坩埚时必须使用坩埚钳,加热完的坩埚应放在石棉网上冷却。
④A的名称为圆底烧瓶,B的名称为蒸馏烧瓶。A常用于组装有液体参与反应的反应器,B主要用于混合
液体的蒸馏和分馏;所盛液体体积约为烧瓶容积的 。
⑤锥形瓶:a.可用于组装气体发生器;b.用于滴定操作;c.作蒸馏装置的接收器等。
⑥烧杯:a.可用于物质的溶解与稀释;b.用于称量具有腐蚀性的固体药品;c.组装水浴加热装置。
(2)常用的计量仪器
仪器名称 主要用途 使用注意事项
①量筒 用于粗略量取一定体积的 a.无“0”刻度;
液体; b.精确度:0.1 mL
c.读数时视线与凹液面最低点相平
②容量瓶 用于配制一定物质的量浓 a.使用前需“查漏”
度的溶液 b.读数时视线与凹液面最低点相平
c.不能将固体或浓溶液直接在该仪器中溶解或稀
释
③酸式滴定管④ ③用于盛放酸性溶液和强 a.使用前需“查漏”;
碱式滴定管 氧化性液体;不可盛装碱 b.“0”刻度在上方;
性溶液; c.精确度:0.01 mL。
④用于盛装碱性溶液,不
可盛装酸性和强氧化性液
体(如:KMnO 溶液)
4
⑤温度计 a.分馏时测量馏分的沸 a.测馏分温度时,水银球应放在蒸馏烧瓶支管口
点; 处。
b.测量反应液的温度; b.测反应混合液的温度时,温度计的水银球应插
c.测量水浴温度 入混合液中但不能接触容器内壁;
c.测蒸气的温度时,水银球应在液面以上;
d.不可用于搅拌
⑥托盘天平 称量固体物质的质量 a.称量前先调零点;
b.腐蚀性药品应放于烧杯内称量;
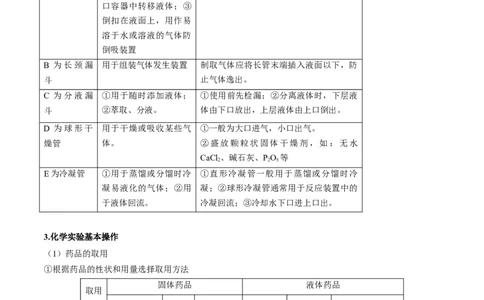
③“左物右码,先大后小”;④精确度:0.1 g(3)常用的分离提纯仪器
仪器名称 主要用途 使用方法和注意事项
A为漏斗 ①组装过滤器;②向小 过滤时,要做到“一贴、二低、三靠”
口容器中转移液体;③
倒扣在液面上,用作易
溶于水或溶液的气体防
倒吸装置
B 为长颈漏 用于组装气体发生装置 制取气体应将长管末端插入液面以下,防
斗 止气体逸出。
C 为分液漏 ①用于随时添加液体; ①使用前先检漏;②分离液体时,下层液
斗 ②萃取、分液。 体由下口放出,上层液体由上口倒出。
D 为球形干 用于干燥或吸收某些气 ①一般为大口进气,小口出气。
燥管 体。 ②盛放颗粒状固体干燥剂,如:无水
CaCl 、碱石灰、PO 等
2 2 5
E为冷凝管 ①用于蒸馏或分馏时冷 ①直形冷凝管一般用于蒸馏或分馏时冷
凝易液化的气体;②用 凝;②球形冷凝管通常用于反应装置中的
于液体回流。 冷凝回流;③冷却水下口进上口出。
3.化学实验基本操作
(1)药品的取用
①根据药品的性状和用量选择取用方法
固体药品 液体药品
取用
药品 粉末 块状 一定量 少量 多量 一定量
使用 药匙(或纸 用托盘天 用试剂瓶 用量筒、滴定管
镊子 胶头滴管
仪器 槽) 平称量 倾倒 (或移液管)量取
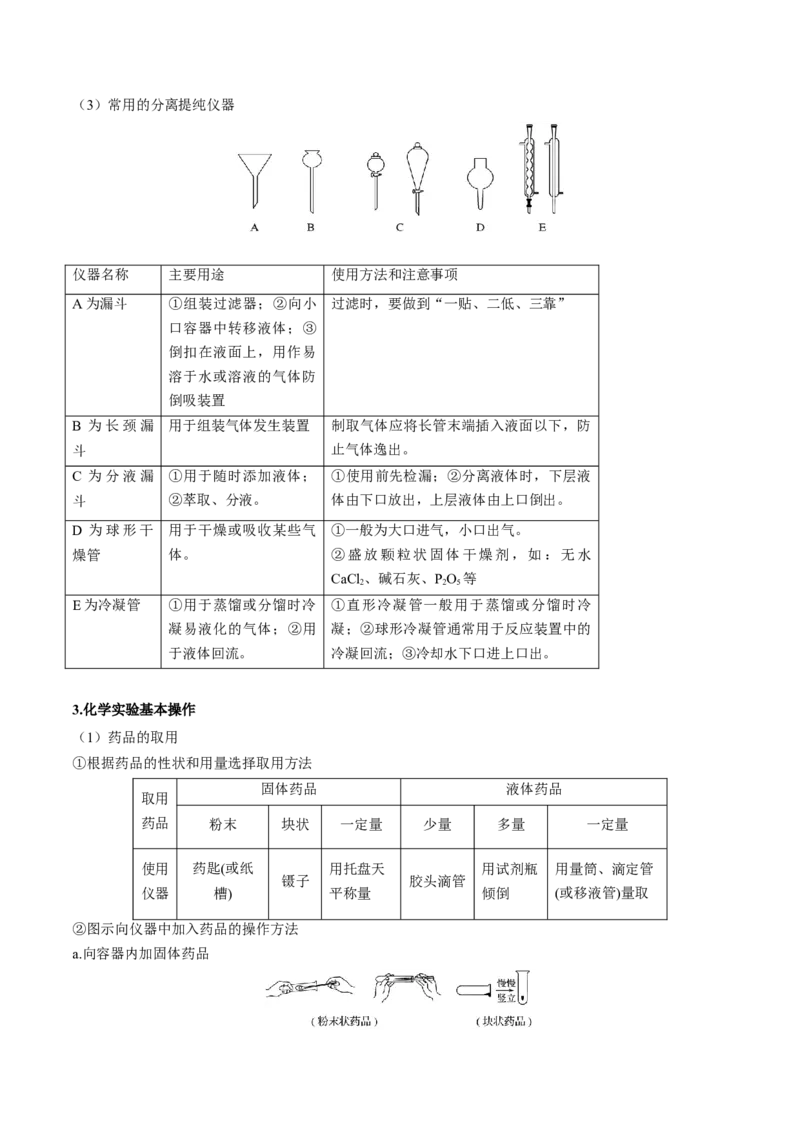
②图示向仪器中加入药品的操作方法
a.向容器内加固体药品b.向容器内加液体药品
(2)试纸的使用
①试纸的类型及用途
②使用方法
a.检验溶液:取一片试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液,点在试纸中部,观察试纸
的颜色变化。等pH试纸变色后,与标准比色卡对照。
b.检验气体:先用蒸馏水把试纸润湿,再用镊子夹取或粘在玻璃棒的一端,然后放在集气瓶口或导管口处,
观察试纸的颜色变化。
(3)物质的溶解
①固体的溶解
②液体的溶解(稀释)
一般把密度较大的液体沿着器壁慢慢注入到密度较小的液体中,并用玻璃棒轻轻搅动,如浓硫酸的稀释、
浓硫酸与浓硝酸的混合等。
③气体的溶解或吸收a.溶解度不大的气体,如CO 、Cl 、HS等,为了增大气体分子与水分子的接触机会,可将导管插入水中,
2 2 2
用如图a所示装置。
b.极易溶于水的气体,如NH 、HCl等,导管口只能靠近液面,也可在导管口连接一倒置的漏斗,并使漏
3
斗边缘刚好与液面接触,或者使用球形干燥器,小口放入水中,这样可以增大气体的吸收率,减少气体的
逸出,同时避免倒吸现象,用如图b所示装置。
(4)玻璃仪器的洗涤
①洗净的标准:玻璃仪器内壁附着均匀的水膜,既不聚成滴,也不成股流下。
②常见残留物的洗涤
残留物 洗涤剂
可溶性物质 水
容器里附有的油污 NaOH溶液或热的纯碱溶液
容器壁上附着的硫磺 CS 或热的NaOH溶液
2
试管壁上附着的银镜 稀HNO
3
难溶性碳酸盐 稀盐酸
AgCl 氨水
容器内残留的MnO 热的浓盐酸
2
1.(2020·天津高考真题)下列实验仪器或装置的选择正确的是
配制50.00mL0.1000mol.L-1
盛装NaSiO 溶液的试
除去Cl 中的HCl 蒸馏用冷凝管 2 3
2 剂瓶
NaCO 溶液
2 3
A B C D
【答案】B
【解析】A.配制50.00mL0.1000mol.L-1NaCO 溶液需要用容量瓶,不能使用量筒配置溶液,错误;B.除
2 3去氯气中的氯化氢气体使用饱和氯化钠溶液,可以吸收氯化氢气体,根据氯气在水中的反应:
Cl
2
+H
2
O⇌H++Cl-+HClO,饱和氯化钠溶液中的氯离子使氯气溶于水的平衡逆向移动,降低氯气在水中的溶
解度,洗气瓶长进短出,利于除杂,正确;C.蒸馏要使用直形冷凝管,接水口下口进上口出,球形冷凝
管一般作反应装置,错误;D.硅酸钠溶液呈碱性,硅酸钠溶液是一种矿物胶,能将玻璃塞与试剂瓶的瓶
口粘在一起,盛装NaSiO 溶液的试剂瓶不能使用玻璃塞,应使用橡胶塞,错误。答案选B。
2 3
2.(2020·山东高考真题)实验室中下列做法错误的是
A.用冷水贮存白磷 B.用浓硫酸干燥二氧化硫
C.用酒精灯直接加热蒸发皿 D.用二氧化碳灭火器扑灭金属钾的燃烧
【答案】D
【解析】A.白磷着火点低,易自然,且密度比水大,常保存在冷水中,A正确;B.浓硫酸有吸水性且不
与SO 反应,可用浓硫酸干燥SO ,B正确;C.蒸发皿可直接加热,蒸发操作时,用酒精灯直接加热蒸发
2 2
皿,C正确;D.K燃烧有KO、KO 生成,KO、KO 和CO 反应产生O 助燃,所以不能用CO 灭火器
2 2 2 2 2 2 2 2 2
扑灭金属钾的燃烧,D错误。答案选D。
3.(2020·浙江高考真题)固液分离操作中,需要用到的仪器是( )
A. B. C. D.
【答案】C
【解析】A.该仪器是干燥管,不能用于固液分离,A不符合题意;B.该仪器为蒸馏烧瓶,不能用于固液
分离,B不符合题意;C.该仪器为普通漏斗,常用于过滤以分离固液混合物,C符合题意;D.该仪器为
牛角管,又叫接液管,连接在冷凝管的末端以收集蒸馏产生的蒸气所冷凝成的液体,不能用于固液分离,
D不符合题意。综上所述,本题答案为C。
4.(2020·浙江高考真题)萃取碘水中的碘并分液,需要用到的仪器是()
A. B. C. D.
【答案】A
【解析】萃取碘水中的碘并分液,需要用到的仪器是分液漏斗;A.该仪器为分液漏斗,正确;B.该仪器为容量瓶,错误;C.该仪器为直形冷凝管,错误;D.该仪器为漏斗,错误;故答案为A。
5.(2019·天津高考真题)下列实验操作或装置能达到目的的是()
A B C D
配制一定浓度的 证明乙炔可使溴水褪
混合浓硫酸和乙醇 收集 气体
溶液 色
【答案】B
【解析】A、乙醇的密度小于浓硫酸,混合时应将浓硫酸沿烧杯壁倒入乙醇中,边倒边搅拌,若顺序相反
则容易引起液体飞溅,不能达到目的;B、容量瓶上的刻度与凹液面的最低处相切,胶头滴管垂直位于容
量瓶的正上方,能达到目的;C、二氧化氮的密度大于空气,集气瓶中的导气管应长进短出,不能达到目
的;D、乙炔中的HS等杂质也能使溴水褪色,应先通过一个盛碱液的洗气瓶将杂质除去,不能达到目的;
2
故选B。
6.(2019·浙江高考真题)下列图示表示过滤的是
A. B. C. D.
【答案】C
【解析】A.该操作是分液,A不合题意;B.该操作是配制一定物质的量浓度溶液中定容步骤,B不合题
意;C.该操作是过滤,C符合题意;D.该操作是配制一定物质的量浓度溶液中转移溶液步骤,D不合题
意。故答案选C。
7.(2019·上海高考真题)用镁带和稀硫酸反应产生氢气来测定氢气的气体摩尔体积,所用的步骤有①冷
却至室温,②调节使水准管和量气管液面持平,③读数。正确的顺序是()A.①②③ B.①③②
C.③①② D.③②①
【答案】A
【解析】因为排出的气体是需要用排出的水的体积来衡量的,镁和硫酸反应过程中放热,需要将装置冷却
到室温,并调节水准管和量气管液面相平,气体的大气压和外界大气压相同时再读数,故选A。
1.(2022秋·河南驻马店·高三统考期末)下列关于仪器使用的说法错误的是
A.①可直接加热,可用作反应容器
B.②可用于蒸馏操作,冷凝水应“上进下出”
C.为球形干燥管,也可用作防倒吸装置
D.④用作洗气瓶时,气体应“长进短出”
【答案】B
【详解】A. ①为坩埚、是陶瓷制品,可直接加热,灼烧固体时的反应容器,A正确;
B. ②可用于蒸馏操作,冷凝水应“下进上出” 以充满整个套管、达到充分冷却的目的 ,B不正确;
C. 为球形干燥管、能装固体干燥剂,球形部分能容纳较多液体、故也可用作防倒吸装置,C正确;
D. ④用作洗气瓶时,气体应“长进短出”,使进入瓶内的气体与液体充分接触、不被吸收的气体则可从
短管逸出 ,D正确;
答案选B。2.(2023秋·海南·高三统考期末)下列实验操作方法正确的是
A.向试管中添加液体 B.称取21.6gNaOH C.检验装置气密性 D.分液放出下层液体
A.A B.B C.C D.D
【答案】C
【详解】A.向试管中添加液体,标签应对着手心,A错误;
B.用托盘天平称量物体质量时,应该左边托盘放物体,右边托盘放砝码,B错误;
C.可以用手握住试管,导管口产生气泡,松开手,导管口形成一段稳定的水柱,检验装置的气密性,C
正确;
D.分液放出下层液体时,分液漏斗的尖端应紧靠烧杯内壁,D错误;
故选C。
3.(2023秋·浙江衢州·高二校联考期末)下列说法不正确的是
A.pH计、酚酞和甲基橙均能用于 NaOH 溶液滴定盐酸终点的判断
B.受溴腐蚀致伤时,先用甘油清洗伤口,再用大量的水洗
C.萃取前,向分液漏斗中加少量水,检查旋塞芯处不漏水,即可使用
D.不可用溴水溶液检验丙烯醛中的碳碳双键
【答案】C
【详解】A.NaOH溶液滴定盐酸,终点时溶液显中性,可用pH计、酚酞和甲基橙判断滴定终点,故A正
确;
B.溴易溶于甘油,则受溴腐蚀致伤时,先用甘油洗伤口,再用大量的水洗,故B正确;
C.萃取前向分液漏斗中加少量水,检查旋塞处,不漏水,再将旋塞旋转180°,不漏水,还需检验上口塞
子是否漏水,故C错误;
D.醛基和碳碳双键均能使溴水褪色,不可用溴水溶液检验丙烯醛中的碳碳双键,故D正确;
故选C。
4.(2022·福建福州·福建省福州第八中学校考模拟预测)下列实验能达到实验目的且符合实验要求的是A.煅烧石灰石 B.检查装置气密性 C.收集并检验 D.用该装置制取少量
A.A B.B C.C D.D
【答案】B
【详解】A.煅烧石灰石用坩埚,A错误;
B.关闭止水夹,从长颈漏斗中加水,当水的液面高于长颈漏斗下端时,继续加水,漏斗中液面高于烧瓶
内液面,一段时间内液面差保持不变,证明装置不漏气,B正确;
C.氨气密度比空气小,应采用向下排空气法,导气管应该插入试管底部,C错误;
D.纯碱为粉末状会从带孔隔板漏下,不能控制反应停止,无法满足制取少量二氧化碳的要求,D错误;
故选B。
5.(2023秋·山东青岛·高一山东省青岛第五十八中学校考期末) 具有热胀冷缩的特性,精密测量仪器
中掺杂 来抵消仪器的热胀冷缩。 通入酸化的 溶液,过滤,得到 沉淀,已知 在有水
存在时能被氧气等氧化剂所氧化,生成 。装置如图所示:下列对实验的分析正确的是
A.装置A中的反应为
B.装置B中盛放饱和硫氢化钠溶液用于除去
C.装置C恒压滴液漏斗中的稀硫酸可以用稀硝酸代替
D.洗涤生成的 沉淀的洗涤液应用煮沸过的蒸馏水
【答案】BD
【详解】A.CuS溶解度过低,不能与HCl及稀HSO 反应,可用FeS与浓盐酸制取HS气体,A错误;
2 4 2
B.除去HS中的HCl,需使用饱和NaHS溶液,NaHS与HS不反应,HCl极易溶于水,从而达到除杂的
2 2
目的,B正确;
C.稀硝酸具有强氧化性,会氧化HS,C错误;
2
D.煮沸蒸馏水可以除去水中溶解的氧气,避免NiS被氧化,D正确;
故选BD。
核心考点2、物质的检验、分离与提纯
1.物质分离与提纯的基本原理
(1)“四原则”
①不增,不得引入新杂质;②不减,尽量不减少被提纯的物质;③易分,使被提纯或分离的物质跟其他物
质易分离;④复原,被提纯的物质要易被还原。
(2)“三必须”
①除杂试剂必须过量;②过量试剂必须除尽(除去过量试剂带入的新杂质,同时注意加入试剂的顺序);③选择最佳的除杂途径。
2.物质分离与提纯的常用方法
3.物质分离与提纯的常见类型
(1)“固+固”混合物的分离(提纯)
(2)“固+液”混合物的分离(提纯)
(3)“液+液”混合物的分离(提纯)
(4)“气+气”混合物的分离(提纯)
4.常见混合物的除杂举例
(1)常见固体混合物的除杂
固体混合物(括号内为
除杂试剂 分离方法
杂质)
NaCO(NaHCO ) 加热或加适量NaOH
2 3 3NaHCO (Na CO) CO 和HO
3 2 3 2 2
NaCl(NH Cl) 加热分解
4
FeCl (FeCl ) 过量铁粉 过滤
2 3
FeCl (FeCl ) Cl
3 2 2
I(SiO) 加热 升华
2 2
Fe O(AlO) 过量NaOH溶液 过滤
2 3 2 3
NH Cl(FeCl ) 适量氨水 过滤
4 3
KNO(NaCl) 水 结晶、重结晶
3
炭粉(CuO) 稀盐酸 过滤
镁粉(铝粉) 过量NaOH溶液 过滤
铁粉(铝粉) 过量NaOH溶液 过滤
(2)常见混合气体的除杂
混合气体(括号内为杂质) 除杂试剂 分离方法
H(NH ) 浓硫酸 洗气
2 3
Cl(HCl) 饱和NaCl溶液 洗气
2
CO(HCl) 饱和NaHCO 溶液 洗气
2 3
CO(SO ) 饱和NaHCO 溶液 洗气
2 2 3
CO(CO) 灼热CuO
2
CO(CO ) 石灰乳或NaOH溶液 洗气
2
NO(NO ) 水 洗气
2
N(O ) 灼热铜网
2 2
溴水
CH(C H) 洗气
4 2 4
酸性高锰酸钾和石灰乳
1.(2020·全国高考真题)下列气体去除杂质的方法中,不能实现目的的是
气体(杂质) 方法
A SO (H S) 通过酸性高锰酸钾溶液
2 2B Cl(HCl) 通过饱和的食盐水
2
C N(O ) 通过灼热的铜丝网
2 2
D NO(NO ) 通过氢氧化钠溶液
2
【答案】A
【解析】A.SO 和HS都具有较强的还原性,都可以被酸性高锰酸钾溶液氧化;因此在用酸性高锰酸钾溶
2 2
液除杂质HS时,SO 也会被吸收,不能实现除杂目的;B.氯气中混有少量的氯化氢气体,可以用饱和食
2 2
盐水除去;饱和食盐水在吸收氯化氢气体的同时,也会抑制氯气在水中的溶解,能实现除杂目的;C.氮
气中混有少量氧气,在通过灼热的铜丝网时,氧气可以与之发生反应: ,而铜与氮气
无法反应,因此可以采取这种方式除去杂质氧气,能实现除杂目的;D.NO 可以与NaOH发生反应:
2
,NO与NaOH溶液不能发生反应;尽管NO可以与NO 一同
2
跟NaOH发生反应: ,但由于杂质的含量一般较少,所以也不会对
NO的量产生较大的影响,能实现除杂的目的;答案选A。
2.(2019·上海高考真题)下列物质分离(括号内的物质为杂质)的方法错误的是()
A.硝基苯(苯)--蒸馏
B.乙烯(SO )--氢氧化钠溶液
2
C.己烷(己烯)--溴水,分液
D.乙酸乙酯(乙醇)--碳酸钠溶液,分液
【答案】C
【解析】A.苯和硝基苯是互溶的液体混合物,利用沸点不同进行蒸馏分离,正确;B.二氧化硫和氢氧化
钠反应,而乙烯不反应,能分离除去,正确;C.己烯和溴水反应二溴己烷,能溶于己烷,不能分离,错
误;D.乙醇能溶于碳酸钠溶液,而乙酸乙酯不溶于碳酸钠溶液,可利用分液分离,正确;答案选C。
3.(2019·北京高考真题)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4D NO(NO ) HO、无水CaCl
2 2 2
【答案】B
【解析】A.FeCl 与Fe反应生成FeCl ,2FeCl +Fe=3FeCl ,此过程中Fe的化合价发生变化,涉及到了氧
3 2 3 2
化还原反应,不符合题意;B.MgCl 与NaOH溶液发生复分解反应MgCl +2NaOH=Mg(OH) +2NaCl,
2 2 2
过量的NaOH溶液可用HCl除去HCl+NaOH=NaCl+H O ,此过程中没有元素化合价发生变化,未涉及氧
2
化还原反应,符合题意;C.部分氯气与HO 发生反应生成氯化氢和次氯酸,应该用饱和食盐水除去
2
HCl,除杂方法不正确,不符合题意;D.NO 与水反应生成硝酸和NO。反应过程中氮元素化合价发生变
2
化,涉及到了氧化还原反应,不符合题意;综上所述,本题应选B。
4.(2019·上海高考真题)下列物质分离(括号内的物质为杂质)的方法错误的是()
A.硝基苯(苯)--蒸馏
B.乙烯(SO )--氢氧化钠溶液
2
C.己烷(己烯)--溴水,分液
D.乙酸乙酯(乙醇)--碳酸钠溶液,分液
【答案】C
【解析】A.苯和硝基苯是互溶的液体混合物,利用沸点不同进行蒸馏分离,正确;B.二氧化硫和氢氧化
钠反应,而乙烯不反应,能分离除去,正确;C.己烯和溴水反应二溴己烷,能溶于己烷,不能分离,错
误;D.乙醇能溶于碳酸钠溶液,而乙酸乙酯不溶于碳酸钠溶液,可利用分液分离,正确;答案选C。
5.(2019·全国高考真题)实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中的碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
【答案】D【解析】在溴化铁作催化剂作用下,苯和液溴反应生成无色的溴苯和溴化氢,装置b中四氯化碳的作用是
吸收挥发出的苯和溴蒸汽,装置c中碳酸钠溶液呈碱性,能够吸收反应生成的溴化氢气体,倒置漏斗的作
用是防止倒吸。A.若关闭K时向烧瓶中加注液体,会使烧瓶中气体压强增大,苯和溴混合液不能顺利流
下。打开K,可以平衡气压,便于苯和溴混合液流下,正确;B.装置b中四氯化碳的作用是吸收挥发出
的苯和溴蒸汽,溴溶于四氯化碳使液体逐渐变为浅红色,正确;C.装置c中碳酸钠溶液呈碱性,能够吸
收反应生成的溴化氢气体,正确;D.反应后得到粗溴苯,向粗溴苯中加入稀氢氧化钠溶液洗涤,除去其
中溶解的溴,振荡、静置,分层后分液,向有机层中加入适当的干燥剂,然后蒸馏分离出沸点较低的苯,
可以得到溴苯,不能用结晶法提纯溴苯,错误。故选D。
6.(2014·大纲全国卷,10)下列除杂方案错误的是( )
选项 被提纯的物质 杂质 除杂试剂 除杂方法
A CO(g) CO(g) NaOH溶液、浓HSO 洗气
2 2 4
B NH Cl(aq) Fe3+(aq) NaOH溶液 过滤
4
C Cl(g) HCl(g) 饱和食盐水、浓HSO 洗气
2 2 4
D NaCO(s) NaHCO (s) — 灼烧
2 3 3
【答案】B
【解析】A项,CO 与NaOH溶液反应生成NaCO ,而CO与NaOH溶液不反应,正确;B项,NaOH溶
2 2 3
液不仅与Fe3+反应,也会与NH发生反应,还引入了Na+,错误;C项,HCl极易溶于水,而Cl 在饱和食
2
盐水中溶解度较小,正确;D项,灼烧可以使NaHCO 固体分解,且生成NaCO,正确。
3 2 3
1.(2023秋·山东潍坊·高三统考期末)茶叶中铁元素的检验可经过“灼烧→溶解→过滤→检验”等步骤。
下列操作方法错误的是
B.用浓硝酸溶解茶叶灰并加蒸馏水 D.检验滤液中的
A.将茶叶灼烧灰化 C.过滤得到滤液
稀释 Fe3+
A.A B.B C.C D.D
【答案】A【详解】A.将茶叶灰化应在坩埚中灼烧,A错误;
B.茶叶灰在烧杯中溶解,并且用玻璃棒不断搅拌,B正确;
C.过滤时,烧杯紧靠玻璃棒,玻璃棒紧贴三层滤纸,漏斗下端紧靠烧杯内壁,C正确;
D.用 溶液检验滤液中的 ,D正确;
故选A。
2.(2023秋·江西吉安·高三江西省宜丰中学统考期末)下列实验室中做法错误的是
A.用冷水贮存白磷
B.实验室中将多余的金属钠放回原试剂瓶
C.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二
D.用标准HCl溶液滴定 溶液来测定其浓度,选择酚酞为指示剂
【答案】D
【详解】A.白磷着火点低,易自然,且密度比水大,常保存在冷水中,A正确;
B.钠非常活泼,做实验时,多余的钠要放回原试剂瓶中,防止发生危险,B正确;
C.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二,确保实验安全,C正确;
D.用标准HCl溶液滴定 溶液来测定其浓度,达到终点生成氯化钠和碳酸,碳酸显酸性,所以需
用甲基橙作指示剂,D错误;
故选D。
3.(2022秋·广东汕尾·高三统考期末)陈述I和II均正确,但不具有因果关系的是
选项 陈述 I 陈述 II
A 金刚砂的熔沸点高 金刚砂(SiC)可用作切割钢板的砂轮
B 碘单质和 CCl 都是非极性分子 碘单质易溶于 CCl
4 4
C 盐卤中氯化镁、硫酸钾属于电解质 盐卤可使豆浆中的蛋白质聚沉
D 活性炭具有吸附性 活性炭可用作制糖业的脱色剂
A.A B.B C.C D.D
【答案】A
【详解】A.金刚砂(SiC)可用作切割钢板的砂轮是利用其硬度大,耐磨性好,与熔沸点高无关,选项A错
误;
B.碘和四氯化碳都属于非极性分子,根据相似相溶原理,所以碘易溶于四氯化碳,选项B正确;C.盐卤中氯化镁、硫酸钾属于电解质,可以中和胶体微粒表面吸附的离子的电荷,使蛋白质分子凝聚起
来得到豆腐豆腐,选项C正确;
D.活性炭具有吸附性,可用作制糖业脱色剂,选项D正确;
答案选A。
4.(2023秋·上海普陀·高三校考期末)我国海带产量居世界第一位,除供食用外,主要用于制碘。实验室
提取碘的途径如下:
下列有关叙述错误的是
A.实验室可在表面皿中焙烧干海带
B.“氧化”时,可选用的试剂有O、HO 等
2 2 2
C.海带灰中含有难溶于水的无机物
D.“系列操作”有过滤、萃取、分液、蒸馏等
【答案】A
【分析】海带干焙烧成海带灰,加水溶解,悬浊液中含有KI,过滤、加氧化剂,将I-氧化成I,加CCl4或
2
者苯萃取碘,分液,蒸馏得到碘单质。
【详解】A.实验室焙烧干海带应该在坩埚中灼烧,故A错误;
B.“氧化”KI时,可选用的试剂有O、HO 等,故B正确;
2 2 2
C.海带灰溶于水呈悬浊液,含有难溶于水的无机物,故C正确;
D.根据分析可知“系列操作”有过滤、萃取、分液、蒸馏等,故D正确;
故答案为A。
5.(2023秋·上海浦东新·高三统考期末)用如下装置制备并收集乙烯,下列说法正确的是
A.为防止暴沸,烧瓶中应放入几片碎瓷片
B.为控制反应温度,温度计的量程为0~150℃
C.为除去杂质 ,试剂X可选择酸性 溶液D.可用排气法或排水法收集乙烯
【答案】A
【详解】A.为防止暴沸,烧瓶中应放入几片碎瓷片,故A正确;
B.该反应为乙醇在浓硫酸的作用下发生消去反应生成乙烯,温度为170℃,故B错误;
C.产生 说明浓硫酸表现了氧化性,故还应有 生成,同时乙醇易挥发,故乙烯中混有乙醇蒸气、
、 ,酸性 溶液不能除去 ,因此应选择NaOH溶液,故C错误;
D.乙烯的相对分子质量为28,空气的相对分子质量为29,乙烯与空气的密度接近,故不可用排空气法收
集乙烯,故D错误;
故选A。
6.(2023·湖南衡阳·统考一模)为完成下列各组实验,所选玻璃仪器和试剂均准确完整的是(不考虑存放
试剂的容器)
实验目的 玻璃仪器 试剂
A 组装实验室制乙烯的发生装置 圆底烧瓶、温度计、酒精灯、导管 浓硫酸、无水乙醇、碎瓷片
粗盐提纯中将最后所得的滤液
B 表面皿、玻璃棒、酒精灯 粗盐提纯中最后所得的滤液
蒸发结晶
除去新制乙酸乙酯中的少量乙 混有乙酸的乙酸乙酯、饱和
C 分液漏斗、烧杯
酸 NaOH溶液
配制100mL一定物质的量浓 100mL容量瓶、胶头滴管、烧杯、量
D 蒸馏水
度的稀硫酸 筒、玻璃棒
【答案】A
【详解】A.实验室制备乙烯时,在圆底烧瓶中放入浓硫酸、无水乙醇和碎瓷片,将温度计的水银球伸入
液面以下,用酒精灯进行加热,烧瓶口连接导管,A项正确;
B.蒸发结晶要用到蒸发皿而不是表面皿,B错误;
C.乙酸乙酯在碱性溶液中会发生水解,不能用饱和NaOH溶液进行乙酸的除杂,C错误;
D.配置稀硫酸要用到蒸馏水和一定浓度的浓硫酸,D项试剂缺少给定浓度的浓硫酸,D错误。
本题选A。
7.(2023秋·湖南长沙·高三统考期末)实验室可在硝酸铁晶体的催化下,用液氨与钠制备氨基钠
(NaNH )。如图装置(夹持、搅拌、尾气处理装置已省略)。已知: 几乎不溶于液氨,易与水、氧气
2等反应。下列说法正确的是
A.加入钠之前向装置A中通入氨气的目的是增大液氨的量,提高钠的转化率
B.装置B的可以防止外界氧气和水蒸气进入装置
C.钠与液氨的反应方程式为
D.从反应后A的混合液中提纯氨基钠的操作方法是蒸发结晶
【答案】BC
【详解】在硝酸铁催化下钠与液氨的反应来生成 和氢气,其化学方程式为:
,该反应是放热反应,为保证液氨处于微沸状态,需要用冷却液控制一定的
温度。
A. 易与水和氧气发生反应,加入钠之前处先通入氨气的目的是排尽密闭体系中空气,选项 错误;
B.装置 中 可防止氧气、水进入密闭体系,选项B正确;
C.钠与液氨反应生成NaNH 和氢气,反应的化学方程式为 ,选项C正确;
2
D.反应后 难溶于液氨中,可过滤除去液氨,得到产品 ,选项D错误;
答案选BC。