文档内容
专题十 能力提升检测卷
一、选择题
1.荣昌陶器为中国四大名陶,其主要成分为O、Si、Al、Fe,还含有少量Ca、Ti等元素。对于上述有关
元素,下列说法正确的是
A.基态Fe原子的价层电子轨道表示式为
B.基态Ca原子最高能级的轨道形状为哑铃形
C.Ti最稳定的化合价为 价
D.第一电离能:O>Si>Al
【答案】D
【解析】A.Fe是26号元素,Fe原子的价层电子排布式为3d64s2,价层电子轨道表示式为
,故A错误;
B.基态Ca原子最高能级为4s,轨道形状为球形,故B错误;
C.钛元素的原子序数为22,基态原子的电子排布式为1s22s22p63s23p63d24s2,Ti原子失去4个电子后得到
Ti4+,电子排布式为1s22s22p63s23p6,p轨道是全充满较稳定,则Ti最稳定的化合价为+4价,故C错误;
D.同周期自左而右,元素的第一电离能成增大的趋势,故第一电离能:Al<Si,O难失去电子,第一电
离能大于Si,则第一电离能:O>Si>Al,故D正确;
故选D。
2.黑火药爆炸时发生反应 。下列说法正确的是
A.半径大小: B.熔点:
C.电离能大小: D.电负性大小:
【答案】D
【解析】A.硫离子和钾离子具有相同的电子层数,层数相同,原子序数越大半径越小,即半径大小:
,A错误;B. 是离子晶体, 为分子晶体,一般情况下,离子晶体的熔点大于分子晶体的熔点,即熔点:
,B错误;
C. 原子电子排布式为 达半充满,能量较低,失去第一个电子所需的能量较大, 原子电子排
布式为 ,即电离能大小: ,C错误;
D.同一主族元素的电负性从上到下逐渐减少,即电负性大小: ,D正确;
故选D。
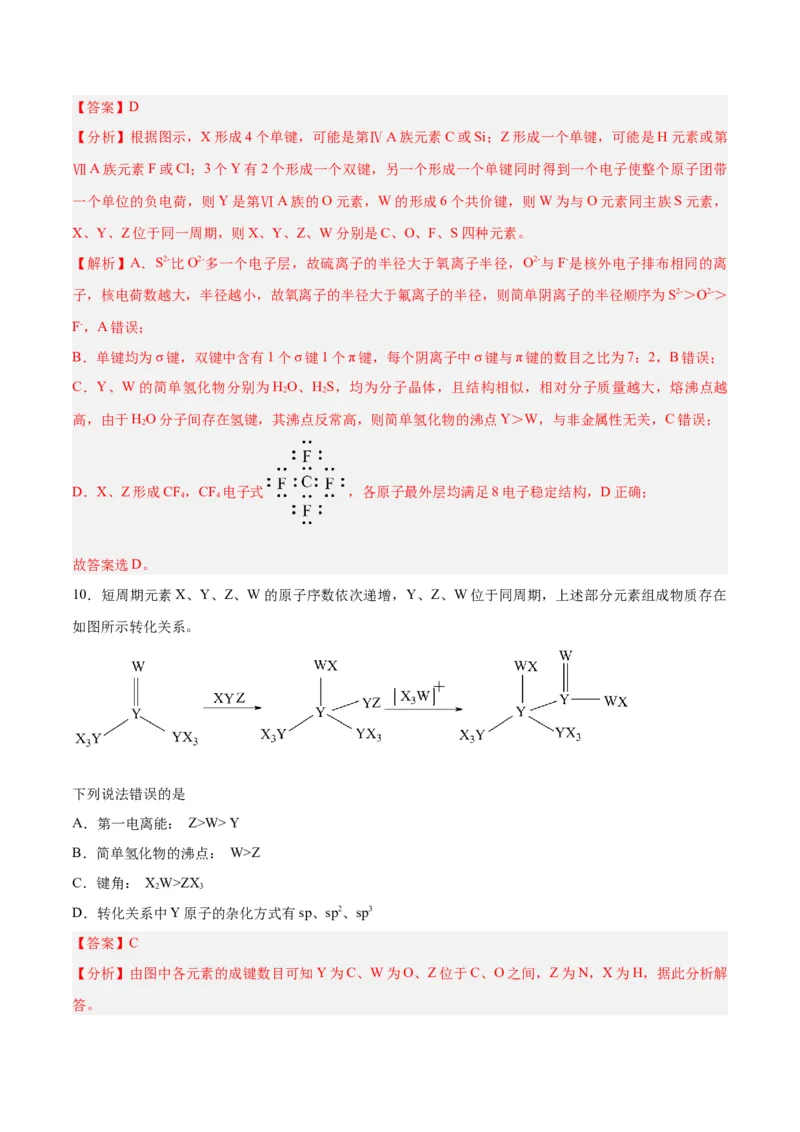
3.R、X、Y、Z四种短周期主族元素,其原子半径与原子序数关系如图所示。已知:它们的原子序数之和
等于51,R的原子序数与Z的最外层电子数相等。下列叙述错误的是
A.最简单氢化物的稳定性:Y<Z
B.第一电离能:R<Y
C.化合物XY 中含两种化学键
2 2
D.等浓度的X、Z最高价氧化物对应的水化物的稀溶液中,水的电离程度相同
【答案】B
【分析】由图中信息可知,X、Y、Z在第三周期,Y与Z相邻,R的原子序数与Z的最外层电子数相等,
若Z的最外层电子数为7,则R、X、Y、Z分别为N、Na、S、Cl;若Z的最外层电子数为6,则R、X、
Y、Z分别为C、Si、P、S,X与Y也相邻,不符合题干;若Z的最外层电子数为5,则R、X、Y、Z分别
为B、Cl、Si、P,X半径小于Y了,不符合题意;其他也不满足要求。
【解析】A.非金属性越强,其简单氢化物稳定性越强,因此最简单氢化物的稳定性:Y(H S)<Z(HCl),
2
故A正确;
B.根据同周期从左到右第一电离能呈增大趋势,但第IIA族、第VA族反常,同主族从上到下第一电离能逐渐减小,则第一电离能:Y(S)<R(N),故B错误;
C.化合物XY(Na S)中含离子键和非极性键两种化学键,故C正确;
2 2 2 2
D.X、Z最高价氧化物对应的水化物分别为NaOH、HClO,等浓度的两种稀溶液中,酸中氢离子浓度等
4
于碱中氢氧根浓度,则两者抑制水的电离程度相等,则水的电离程度相等,故D正确;
综上所述,答案为B。
4.X、Y、Z、J、Q是原子序数依次增大,且分布在三个短周期的主族元素,Y元素原子的核外未成对电
子数在同周期中最多,Y、Z同周期,Z、J同主族.下列说法错误的是
A.电负性:Q>J;第一电离能:Y>Z B.最高价含氧酸的酸性:Q>J
C. 、 的中心原子杂化方式相同 D.简单离子半径:Y>Z、J>Q
【答案】C
【分析】由X、Y、Z、J、Q是原子序数依次增大,分布在三个短周期的主族元素,可知X为第一周期元
素,为H,由Z、J同主族可知,Y、Z为第二周期元素,J、Q为第三周期元素,Y元素原子的核外未成对
电子数在同周期中最多,则可知为N,可推出,Z为O,J为S,Q为Cl。
【解析】A.同周期原子从左到右电负性逐渐增大,则电负性Q>J(Cl>S),N最外层电子为半充满状态,第
一电离能Y>Z(N>O),A正确;
B.非金属性越强,最高价含氧酸的酸性越强,酸性 ,B正确;
C. 中N原子价层电子对数 ,为 杂化, 中Cl原子价层电子对数
,为 杂化,C错误;
D.简单离子半径 , ,D正确。
故选C。
5.短周期元素X、Y、Z、W的原子序数依次递增,Y、Z、W位于同周期,上述部分元素组成物质存在如
图所示转化关系。下列说法错误的是
A.第一电离能: Z>W> Y
B.简单氢化物的沸点: W>Z
C.键角: XW>ZX
2 3
D.转化关系中Y原子的杂化方式有sp、sp2、sp3
【答案】C
【分析】由图中各元素的成键数目可知Y为C、W为O、Z位于C、O之间,Z为N,X为H,据此分析解
答。
【解析】A.同周期元素第一电离能呈增大趋势,但N最外层为半满稳定结构,其第一电离能大于O,因
此第一电离能:N>O>C,故A正确;
B.HO常温下为液态,NH 常温下为气态,沸点:HO>NH ,故B正确;
2 3 2 3
C.HO、NH 中心原子的价层电子对数均为4,HO含两对孤电子对,NH 中只有1对孤电子对,孤对电
2 3 2 3
子越多,对成键电子对的排斥作用越大,键角越小,因此键角:HOY
C.物质M的晶体中存在的微粒间作用力只有共价键和范德华力
D.等物质的量的M和N中σ键数目和π键数目均相等
【答案】D
【分析】W、X、Y、Z为原子序数依次增大的短周期元素,X和Z的最外层电子数分别为其电子层数的2
倍,则X为C元素、Z为S元素;由M和N的结构可知,W、Y形成共价键的数目分别为1、3,X和Y
位于同一周期,则W为H元素、Y为N元素。
【解析】A.硫化氢分子中含有18个电子,不是10电子分子,故A错误;
B.同周期元素,从左到右第一电离能呈增大趋势,则氮元素的第一电离能大于碳元素,故B错误;
C.由M的结构可知,M分子中含有氨基,能形成分子间氢键,则晶体中存在的微粒间作用力有共价键、
氢键和范德华力,故C错误;
D.有机化合物中配位键、单键为σ键,双键中含有1个σ键和1个π键,由物质M和N的结构式分析可
知, M、N中所含的σ键数目均为9,π键数目均为2,故D正确;
故选D。
9.我国科学家用如图所示的阴离子的盐作水系锌离子电池的电解质溶液,显示了优良的循环性能。X、
Y、Z、W均为短周期元素且原子序数依次增大,其中X、Y、Z位于同一周期,Y、W核外最外层电子数
相等。下列叙述正确的是
A.简单离子半径大小顺序为W>Z>Y
B.每个阴离子中σ键与π键的数目之比为5:2
C.Y的简单氢化物的沸点高于W的简单氢化物,是因为Y的非金属性强于W
D.X和Z形成的简单化合物各原子最外层均满足8电子稳定结构【答案】D
【分析】根据图示,X形成4个单键,可能是第ⅣA族元素C或Si;Z形成一个单键,可能是H元素或第
ⅦA族元素F或Cl;3个Y有2个形成一个双键,另一个形成一个单键同时得到一个电子使整个原子团带
一个单位的负电荷,则Y是第ⅥA族的O元素,W的形成6个共价键,则W为与O元素同主族S元素,
X、Y、Z位于同一周期,则X、Y、Z、W分别是C、O、F、S四种元素。
【解析】A.S2-比O2-多一个电子层,故硫离子的半径大于氧离子半径,O2-与F-是核外电子排布相同的离
子,核电荷数越大,半径越小,故氧离子的半径大于氟离子的半径,则简单阴离子的半径顺序为S2->O2->
F-,A错误;
B.单键均为σ键,双键中含有1个σ键1个π键,每个阴离子中σ键与π键的数目之比为7:2,B错误;
C.Y、W的简单氢化物分别为HO、HS,均为分子晶体,且结构相似,相对分子质量越大,熔沸点越
2 2
高,由于HO分子间存在氢键,其沸点反常高,则简单氢化物的沸点Y>W,与非金属性无关,C错误;
2
D.X、Z形成CF,CF 电子式 ,各原子最外层均满足8电子稳定结构,D正确;
4 4
故答案选D。
10.短周期元素X、Y、Z、W的原子序数依次递增,Y、Z、W位于同周期,上述部分元素组成物质存在
如图所示转化关系。
下列说法错误的是
A.第一电离能: Z>W> Y
B.简单氢化物的沸点: W>Z
C.键角: XW>ZX
2 3
D.转化关系中Y原子的杂化方式有sp、sp2、sp3
【答案】C
【分析】由图中各元素的成键数目可知Y为C、W为O、Z位于C、O之间,Z为N,X为H,据此分析解
答。【解析】A.同周期元素第一电离能呈增大趋势,但N最外层为半满稳定结构,其第一电离能大于O,因
此第一电离能:N>O>C,故A正确;
B.HO常温下为液态,NH 常温下为气态,沸点:HO>NH ,故B正确;
2 3 2 3
C.HO、NH 中心原子的价层电子对数均为4,HO含两对孤电子对,NH 中只有1对孤电子对,孤对电
2 3 2 3
子越多,对成键电子对的排斥作用越大,键角越小,因此键角:HO NH >H O,故键角按由大到小的
2 3 3 2
顺序排列为b>a>c;
(3)Na+与[Cu(OH) ]2-之间形成离子键,[Cu(OH) ]2-内的O与H之间形成极性共价键,氢键不是化学键,
4 4
故答案选AC;
(4)顺磁性物质即含有未成对电子的物质。A中的铜离子价电子排布式为3d10,无未成对电子,B中的铜
离子价电子排布式为3d9,含有1个未成对电子,C中的铁离子价电子排布式为3d5,含有5个未成对电
子,D中锌离子价电子排布式为3d10,无未成对电子,故答案选BC;
(5)A.钠和锌属于金属晶体,碘单质属于分子晶体,金刚石属于原子晶体,只涉及3种晶体类型,故A
错误;
B.碘升华时破坏了分子间作用力,没有破坏非极性键,故B错误;
C.一般而言,熔点:原子晶体>金属晶体>分子晶体,金刚石是原子晶体,则四种晶体中熔点最高的是金刚
石,故C正确;
D. 晶胞中原子数目:①Zn晶胞顶点有8个Zn原子,体心有1个Zn原子,8× +1=2,则一个Zn晶胞中含
2个Zn原子;②Cu晶胞顶点有8个Cu原子,面心有6个Cu原子,8× +6× =4,则一个Cu晶胞中含4
个Cu原子;③碘单质在顶点和面心,I 数目为6× +8× =4,含碘原子数目为2×4=8;④金刚石顶点有8
2
个C原子,面心有6个C原子、晶胞内部有4个C原子,8× +6× +4=8,则一个金刚石晶胞中含8个C原子;故1个晶胞含8个原子有③④,D正确;答案选CD。
(6)由(5)中铜的晶胞图可知,每个晶胞中铜原子个数为8× +6× =4,假设铜原子半径为r,晶胞参数
为a,铜晶胞中面对角线上的3个铜原子相切,故面对角线长度为4r,由 可得 ,所
以该晶胞中原子的空间利用率为 。
3.镍是一种亲铁元素,地核主要由铁、镍元素组成。
(1)基态镍原子的价电子排布式为 。
(2)配合物 常温为液体,其晶体类型是 ,配位原子是 。 与 互为等电子体,
的熔沸点更高,其原因是 。
(3) 溶液与丁二酮肟的反应如下图,该反应可以用来鉴别 。
①丁二酮肟中四种元素电负性由大到小的顺序为 ,碳原子的杂化轨道类型为 。
②二(丁二酮肟)合镍(Ⅱ)中不存在的作用力有 (填选项字母)。
A.氢键 B.π键 C.范德华力 D. 键 E.配位键
(4)某种镁、镍和碳三种元素形成的晶体具有超导性。该晶体可看作是镁原子做顶点,镍原子作面心的面心
立方堆积(晶胞结构如图,未标出碳原子位置),碳原子只填充在由镍构成的八面体空隙。
①图中碳原子的位置位于晶胞的 。
②已知晶胞中相邻且最近的镁、碳原子间核间距为 为阿伏加德罗常数的值,其密度为(列出算式即可)。
【答案】(1)
(2) 分子晶体 C 均为分子晶体,相对分子质量相同,极性越大,范德华力越强,熔点较高
(3) C
(4) 体心
【解析】(1)Ni为28号元素,基态原子核外电子排布式为[Ar]3d84s2,价电子排布式为3d84s2;
(2)Ni(CO) 常温为液体,熔沸点较低,应为分子晶体;CO分子中C、O原子都有孤电子对,但C的电负
4
性较小,更容易给出电子,所以配位原子为C;CO和N 均为分子晶体,相对分子质量相同,但CO为极
2
性分子,极性越大,范德华力越大,熔沸点越高;
(3)①非金属性越强,电负性越大,所以丁二酮肟中四种元素电负性由大到小的顺序为O>N>C>H;
丁二酮肟中甲基中的C原子为sp3杂化,C=N键中的C原子为sp2杂化;
②C=N键中有一个σ键,一个π键,N原子共形成四个共价键,则N原子与Ni原子之间为配位键,分子内
存在氢键,故选C;
(4)①碳原子只填充在由镍构成的八面体空隙中,碳原子应位于体心;
②相邻且最近的镁、碳原子间核间距为apm,则晶胞的体对角线为2apm,所以晶胞的棱长
,体积为 ,由均摊法可知,晶胞中C原子数目为1,Ni原子数目为
,Mg原子数目为 ,所以一个晶胞是质量为 ,即密度为
。
4.近日,中国科学院深圳先进技术研究院某研究团队发现,二维铜铟磷硫( )能作纳米药物,用于
未来安全有效的抗SARS-CoV-2治疗,以降低SARS-CoV-2的传染性。(1)已知铟( )与铝同主族,则基态In原子的价电子的轨道表示式为 ;焰火中铜的焰色是绿
色,该光谱属于 (填“发射”或“吸收”)光谱。
(2)第一电离能:P S(填“>”或“<”,下同);键角: 。
(3) 常作消毒剂,其合成途径之一为 , ( )中硫原子的杂化类型为
; 分子的VSEPR模型是 。
(4) 可用于制造火柴及火柴盒摩擦面,已知 分子中各原子最外层均满足8电子结构,且该分子中只
含有9个 键,则 的结构式可能为 (写一种即可)。
(5) 呈黑色或灰黑色,其晶胞结构如图所示,若晶胞的参数为 ,晶体的密度为 ,则阿伏加
德罗常数的值为 (用含a和d的代数式表示)。
【答案】(1)5s25p1 发射
(2) > >
(3) sp3 四面体形
(4)
【解析】(1)已知铟( In)与铝同主族,54>49>36,故In在周期表第5周期第ⅢA族,则基态In原子的
49
价电子的轨道表示式为5s25p1,焰火中的绿色是铜的焰色,基态铜原子在灼烧时价电子发生了跃迁而变为
激发态,该光谱是发射光谱;
(2)由于P的价电子排布为:3s23p3处于半充满的稳定状态,而S的价电子排布为:3s23p4处于不稳定状态,故第一电离能:P>S,已知PH 中心原子P周围的价层电子对数为:3+ =4,HS中心原子S
3 2
周围的价层电子对数为:2+ =4,二者价层电子对互斥模型均为四面体形,由于HS中存在2对孤
2
电子对,而PH 中只有1对孤电子对,且知孤电子对对成键电子对的排斥作用大于成键电子对对成键电子
3
对的排斥作用,故键角:PH >HS;
3 2
(3)已知S为16号元素,其价电子排布式为:3s23p4,结合 ( )结构式可知,其中硫原子周围
形成2个S-S单键和2个孤电子对,故其杂化类型为sp3,SCl 分子中心原子S周围的价层电子对数为:2+
2
=4,根据价层电子对互斥理论可知,其VSEPR模型是四面体形,故答案为:sp3;四面体形;
(4)已知P是15号元素,S为16号元素,则P周围需形成3个共价键,S周围需形成2个共价键才能满
足PS 分子中各原子最外层均满足8电子结构,且该分子中只含有9个 键,则PS 的结构式可能为
4 3 4 3
。