文档内容
专题突破(七) 化学反应速率和化学平衡图像的分析
化学反应速率和平衡的图像及分析是高考考查的重点,此类试题将抽象的理论知识图
像化,既能考查考生化学反应速率和平衡的相关知识,又能考查学生读图、识图,并应用知识
解决综合问题的能力,要求考生获取有关信息、识别有效证据、推测反应结果、归纳总结规律,
体现《中国高考评价体系》对于“学习掌握”“思维方法”等化学科核心素养的要求。
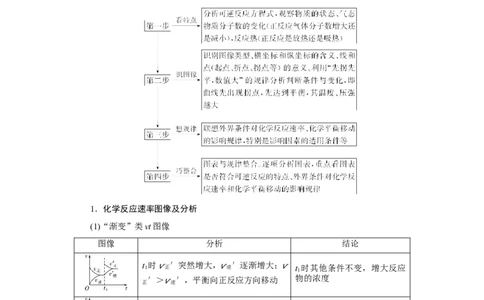
分析、解答化学反应速率和化学平衡图像题的思维流程如下:
1.化学反应速率图像及分析
(1)“渐变”类vt图像
图像 分析 结论
t 1 时 v正 ′突然增大, v逆 ′逐渐增大; v t 时其他条件不变,增大反应
1
′> ′,平衡向正反应方向移动 物的浓度
正 v逆
t 1 时 v正 ′突然减小, v逆 ′逐渐减小; v t 时其他条件不变,减小反应
1
′> ′,平衡向逆反应方向移动 物的浓度
逆 v正
t 1 时 v逆 ′突然增大, v正 ′逐渐增大; v t 时其他条件不变,增大生成
1
′> ′,平衡向逆反应方向移动 物的浓度
逆 v正
t 1 时 v逆 ′突然减小, v正 ′逐渐减小; v t 时其他条件不变,减小生成
1
′> ′,平衡向正反应方向移动 物的浓度
正 v逆(2)“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体系的压强
t 1 时 v正 ′、 v逆 ′均突然增 且 1 m+n>p+q(正反应为体积减小的反应)
大,且 ′> ′;平衡
v正 v逆
向正反应方向移动
t 时其他条件不变,升高温度且ΔH>0(正
1
反应为吸热反应)
t 时其他条件不变,增大反应体系的压强
1
t 1 时 v正 ′、 v逆 ′均突然增 且m+n<p+q(正反应为体积增大的反应)
大,且 ′> ′;平衡
v逆 v正 t 时其他条件不变,升高温度且ΔH<0(正
1
向逆反应方向移动
反应为放热反应)
t 时其他条件不变,减小反应体系的压强
t 1 时 v正 ′、 v逆 ′均突然减 且 1 m+n<p+q(正反应为体积增大的反应)
小,且 ′> ′;平衡
v正 v逆 t 时其他条件不变,降低温度且ΔH<0(正
1
向正反应方向移动
反应为放热反应)
t 时其他条件不变,减小反应体系的压强
t 1 时 v逆 ′、 v正 ′均突然减 且 1 m+n>p+q(正反应为体积减小的反应)
小,且 ′> ′;平衡
v逆 v正 t 时其他条件不变,降低温度且ΔH>0(正
1
向逆反应方向移动
反应为吸热反应)
(3)“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 1 时 v正 ′、 v逆 ′均突然增大且 v t 时其他条件不变增大反应体系的
1
正
′=
v逆
′,平衡不移动 压强且m+n=p+q(反应前后气体
体积无变化)
t 1 时 v正 ′、 v逆 ′均突然减小且 v t 1 时其他条件不变,减小反应体系的
压强且m+n=p+q(反应前后气体
′= ′,平衡不移动
正 v逆 体积无变化)
2.化学平衡图像及分析
(1)浓度时间图像
例如,反应A(g)+B(g)⇌AB(g),充入一定量A(g)和B(g),达到平衡过程如图所示:
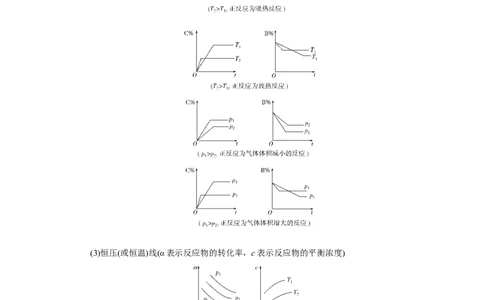
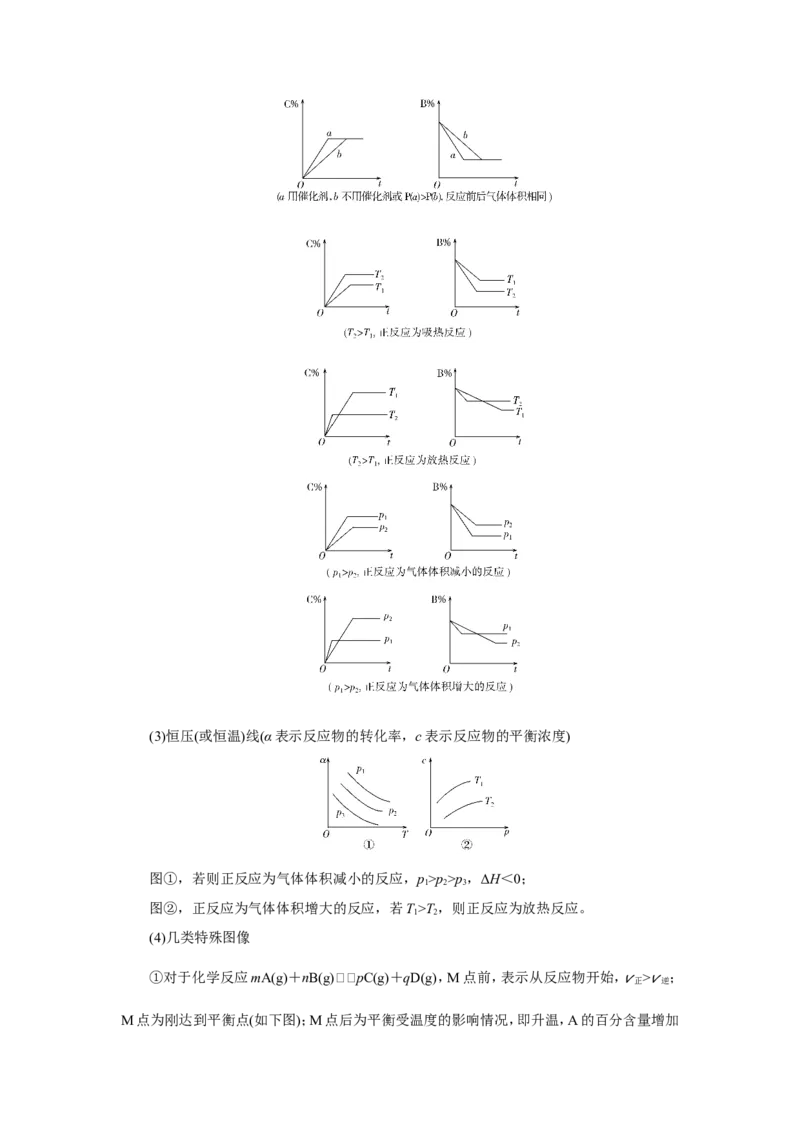
(2)含量时间温度(压强)(C%指产物的质量分数,B%指某反应物的质量分数)(3)恒压(或恒温)线(α表示反应物的转化率,c表示反应物的平衡浓度)
图①,若则正反应为气体体积减小的反应,p>p>p,ΔH<0;
1 2 3
图②,正反应为气体体积增大的反应,若T>T,则正反应为放热反应。
1 2
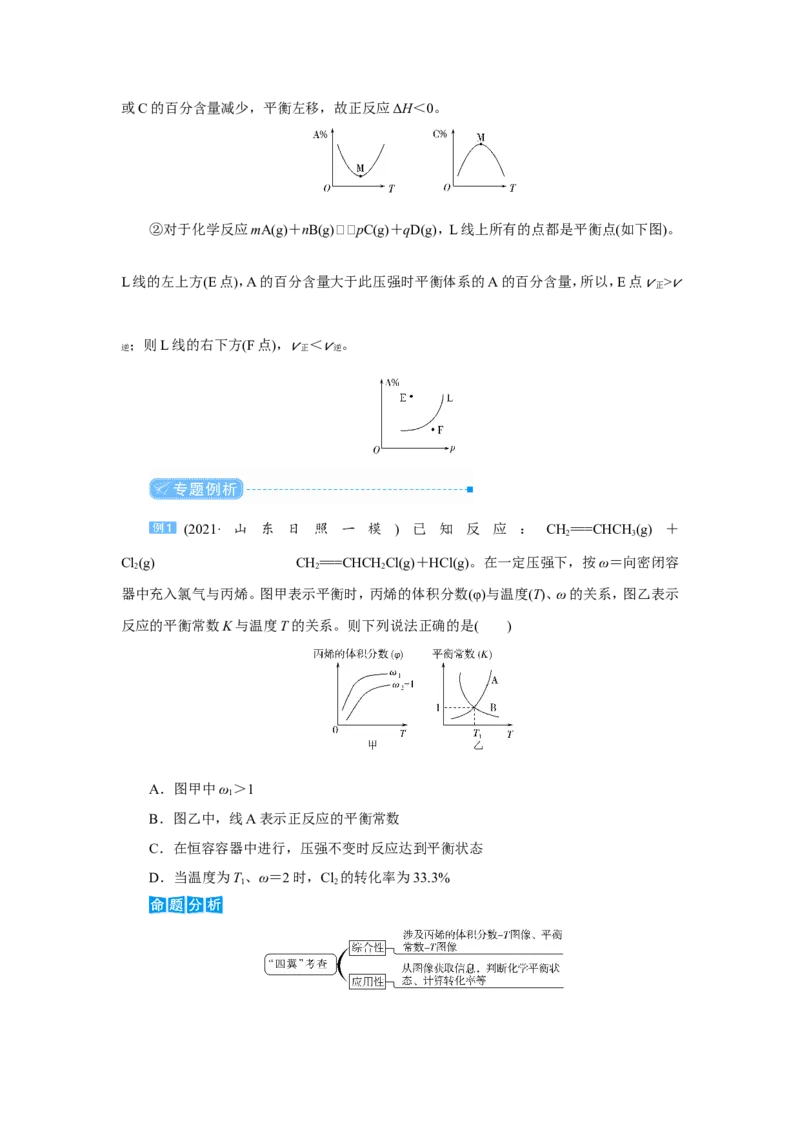
(4)几类特殊图像
①对于化学反应mA(g)+nB(g)pC(g)+qD(g),M点前,表示从反应物开始, v正 >v逆 ;
M点为刚达到平衡点(如下图);M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平衡左移,故正反应ΔH<0。
②对于化学反应mA(g)+nB(g)pC(g)+qD(g),L线上所有的点都是平衡点(如下图)。
L线的左上方(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以,E点 v正 >v
逆
;则L线的右下方(F点),
v正
<
v逆
。
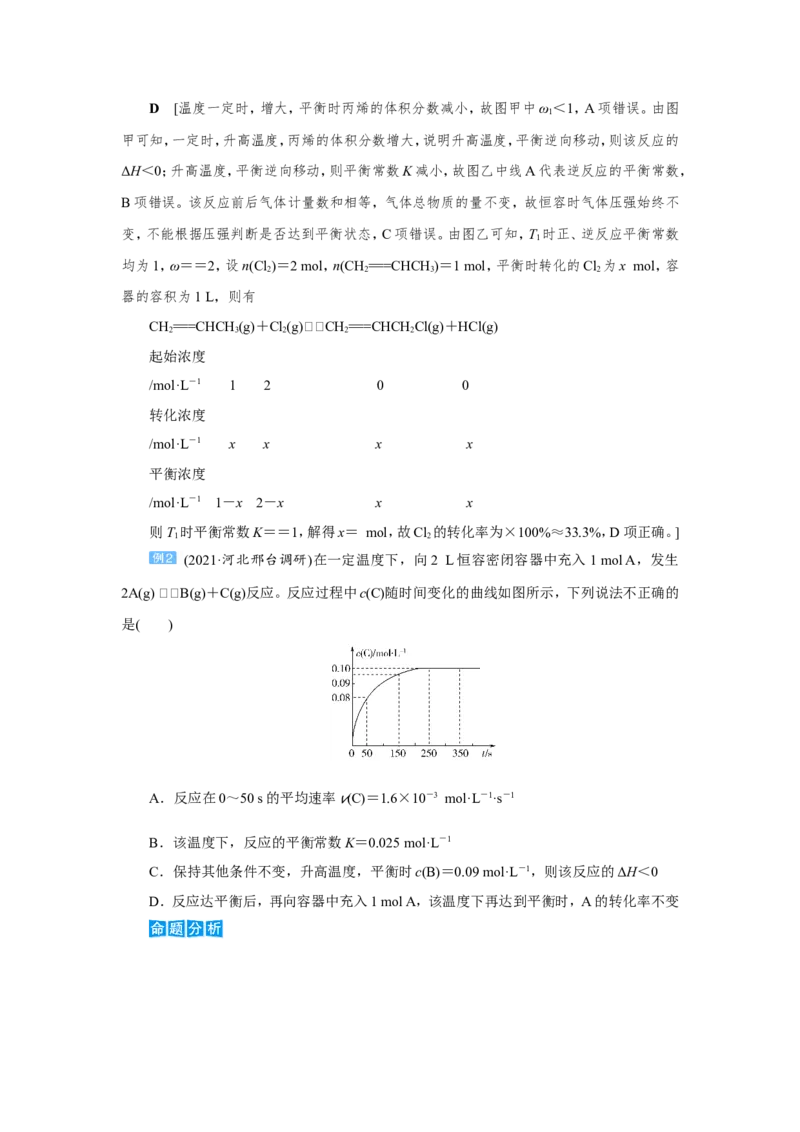
(2021· 山 东 日 照 一 模 ) 已 知 反 应 : CH===CHCH(g) +
2 3
Cl(g)CH===CHCHCl(g)+HCl(g)。在一定压强下,按ω=向密闭容
2 2 2
器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、ω的关系,图乙表示
反应的平衡常数K与温度T的关系。则下列说法正确的是( )
A.图甲中ω>1
1
B.图乙中,线A表示正反应的平衡常数
C.在恒容容器中进行,压强不变时反应达到平衡状态
D.当温度为T、ω=2时,Cl 的转化率为33.3%
1 2D [温度一定时,增大,平衡时丙烯的体积分数减小,故图甲中ω<1,A项错误。由图
1
甲可知,一定时,升高温度,丙烯的体积分数增大,说明升高温度,平衡逆向移动,则该反应的
ΔH<0;升高温度,平衡逆向移动,则平衡常数K减小,故图乙中线A代表逆反应的平衡常数,
B项错误。该反应前后气体计量数和相等,气体总物质的量不变,故恒容时气体压强始终不
变,不能根据压强判断是否达到平衡状态,C项错误。由图乙可知,T 时正、逆反应平衡常数
1
均为1,ω==2,设n(Cl )=2 mol,n(CH===CHCH)=1 mol,平衡时转化的Cl 为x mol,容
2 2 3 2
器的容积为1 L,则有
CH===CHCH(g)+Cl(g)CH===CHCHCl(g)+HCl(g)
2 3 2 2 2
起始浓度
/mol·L-1 1 2 0 0
转化浓度
/mol·L-1 x x x x
平衡浓度
/mol·L-1 1-x 2-x x x
则T 时平衡常数K==1,解得x= mol,故Cl 的转化率为×100%≈33.3%,D项正确。]
1 2
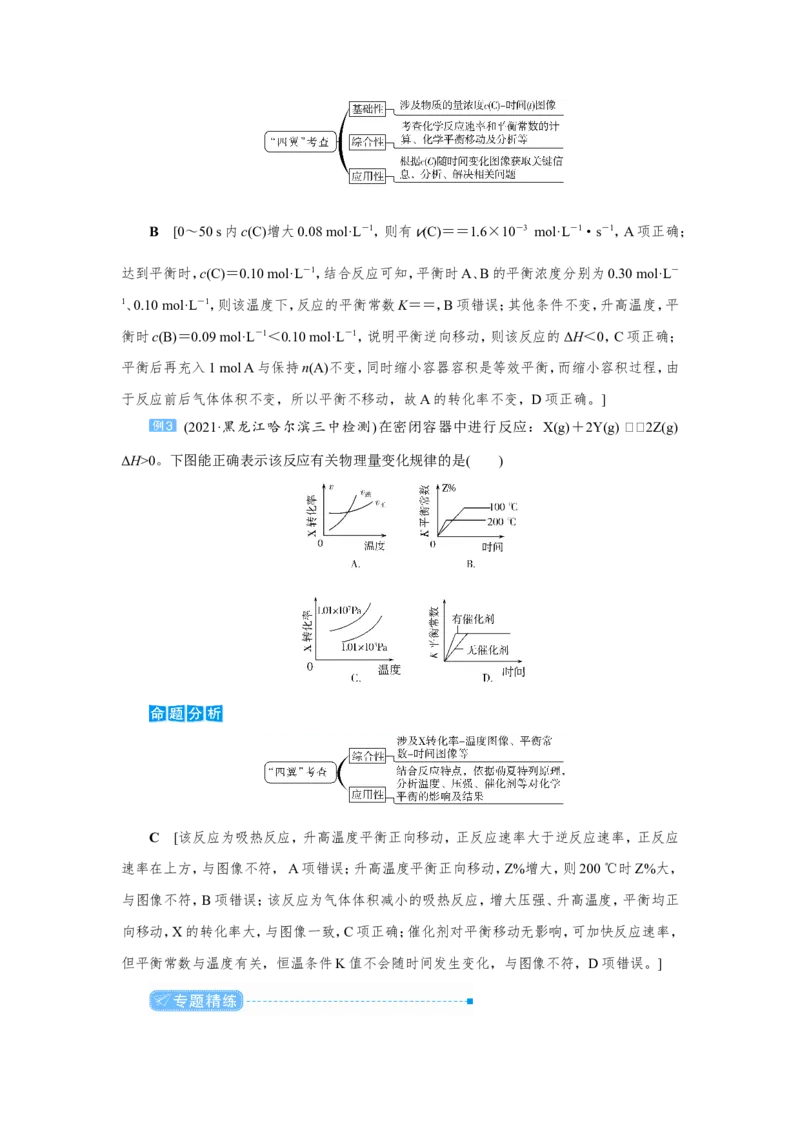
(2021·河北邢台调研)在一定温度下,向2 L恒容密闭容器中充入1 mol A,发生
2A(g) B(g)+C(g)反应。反应过程中c(C)随时间变化的曲线如图所示,下列说法不正确的
是( )
A.反应在0~50 s的平均速率 v(C)=1.6×10-3 mol·L-1·s-1
B.该温度下,反应的平衡常数K=0.025 mol·L-1
C.保持其他条件不变,升高温度,平衡时c(B)=0.09 mol·L-1,则该反应的ΔH<0
D.反应达平衡后,再向容器中充入1 mol A,该温度下再达到平衡时,A的转化率不变B [0~50 s内c(C)增大0.08 mol·L-1,则有 v(C)==1.6×10-3 mol·L-1·s-1,A项正确;
达到平衡时,c(C)=0.10 mol·L-1,结合反应可知,平衡时A、B的平衡浓度分别为0.30 mol·L-
1、0.10 mol·L-1,则该温度下,反应的平衡常数K==,B项错误;其他条件不变,升高温度,平
衡时c(B)=0.09 mol·L-1<0.10 mol·L-1,说明平衡逆向移动,则该反应的ΔH<0,C项正确;
平衡后再充入1 mol A与保持n(A)不变,同时缩小容器容积是等效平衡,而缩小容积过程,由
于反应前后气体体积不变,所以平衡不移动,故A的转化率不变,D项正确。]
(2021·黑龙江哈尔滨三中检测)在密闭容器中进行反应:X(g)+2Y(g) 2Z(g)
ΔH>0。下图能正确表示该反应有关物理量变化规律的是( )
C [该反应为吸热反应,升高温度平衡正向移动,正反应速率大于逆反应速率,正反应
速率在上方,与图像不符, A项错误;升高温度平衡正向移动,Z%增大,则200 ℃时Z%大,
与图像不符,B项错误;该反应为气体体积减小的吸热反应,增大压强、升高温度,平衡均正
向移动,X的转化率大,与图像一致,C项正确;催化剂对平衡移动无影响,可加快反应速率,
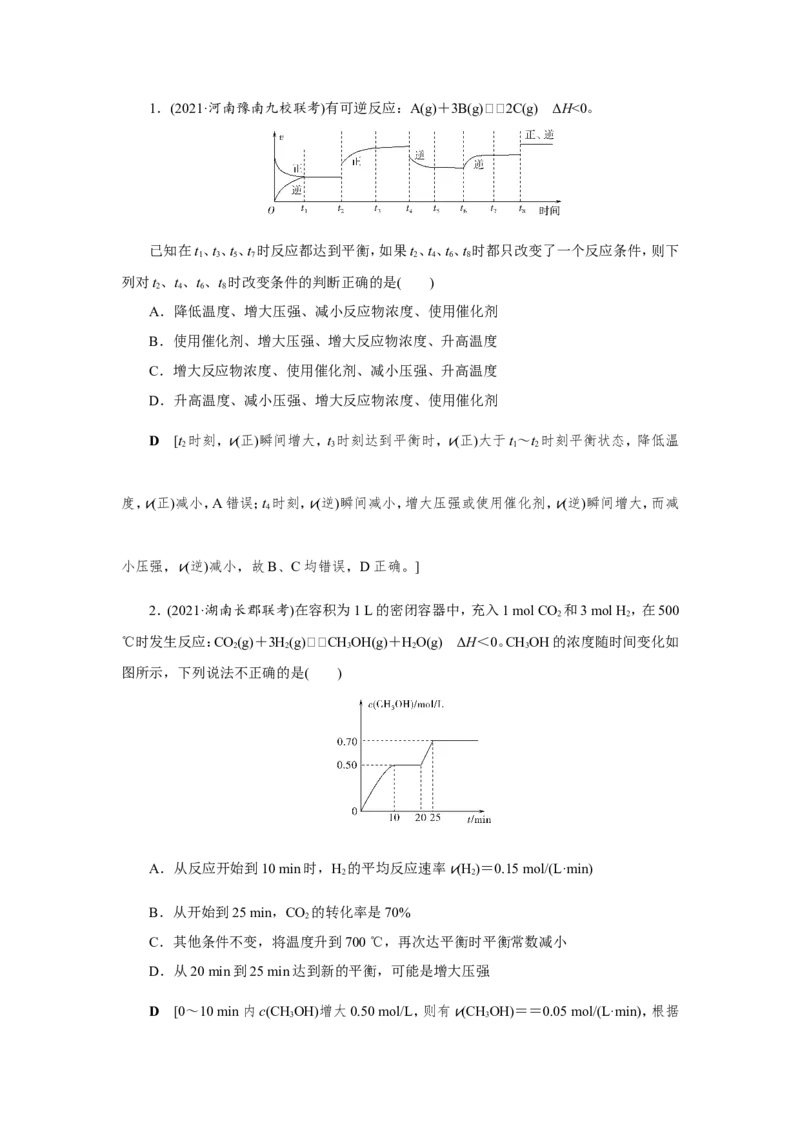
但平衡常数与温度有关,恒温条件K值不会随时间发生变化,与图像不符,D项错误。]1.(2021·河南豫南九校联考)有可逆反应:A(g)+3B(g)2C(g) ΔH<0。
已知在t、t、t、t 时反应都达到平衡,如果t、t、t、t 时都只改变了一个反应条件,则下
1 3 5 7 2 4 6 8
列对t、t、t、t 时改变条件的判断正确的是( )
2 4 6 8
A.降低温度、增大压强、减小反应物浓度、使用催化剂
B.使用催化剂、增大压强、增大反应物浓度、升高温度
C.增大反应物浓度、使用催化剂、减小压强、升高温度
D.升高温度、减小压强、增大反应物浓度、使用催化剂
D [t
2
时刻, v(正)瞬间增大,t
3
时刻达到平衡时, v(正)大于t
1
~t
2
时刻平衡状态,降低温
度, v(正)减小,A错误;t
4
时刻, v(逆)瞬间减小,增大压强或使用催化剂, v(逆)瞬间增大,而减
小压强, v(逆)减小,故B、C均错误,D正确。]
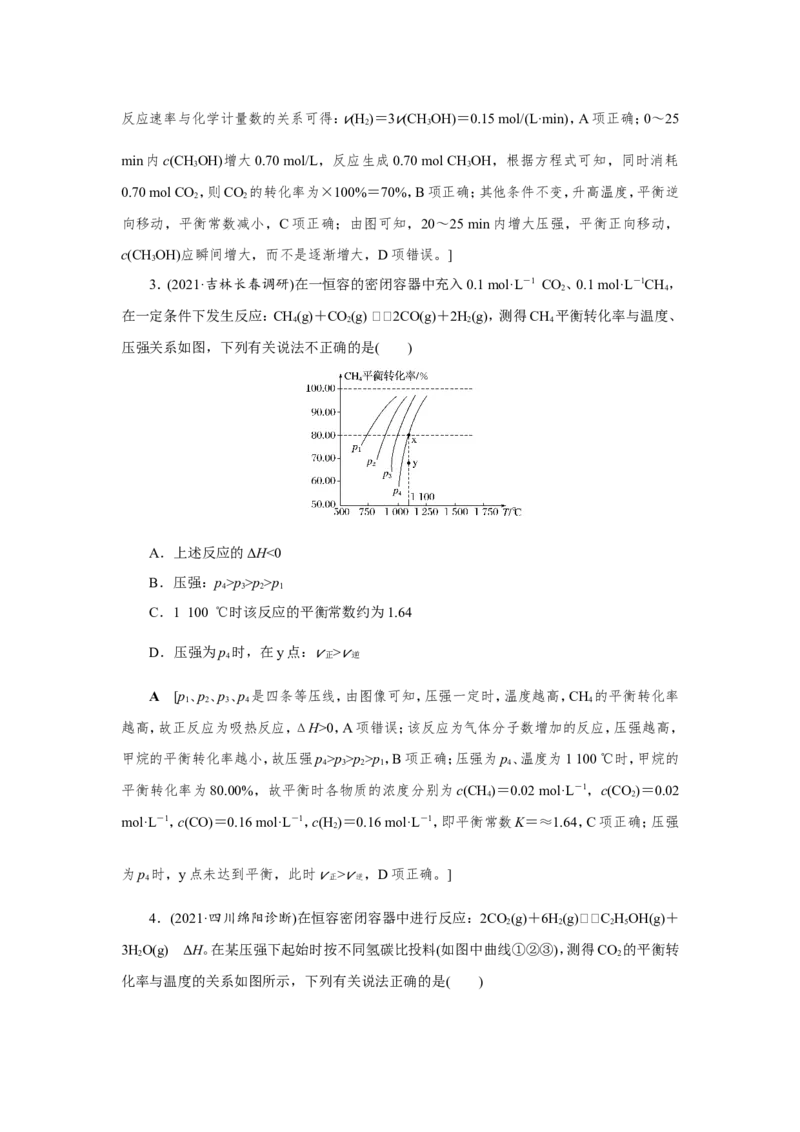
2.(2021·湖南长郡联考)在容积为1 L的密闭容器中,充入1 mol CO 和3 mol H ,在500
2 2
℃时发生反应:CO(g)+3H(g)CHOH(g)+HO(g) ΔH<0。CHOH的浓度随时间变化如
2 2 3 2 3
图所示,下列说法不正确的是( )
A.从反应开始到10 min时,H
2
的平均反应速率 v(H
2
)=0.15 mol/(L·min)
B.从开始到25 min,CO 的转化率是70%
2
C.其他条件不变,将温度升到700 ℃,再次达平衡时平衡常数减小
D.从20 min到25 min达到新的平衡,可能是增大压强
D [0~10 min 内c(CH
3
OH)增大0.50 mol/L,则有 v(CH
3
OH)==0.05 mol/(L·min),根据反应速率与化学计量数的关系可得: v(H
2
)=3v(CH
3
OH)=0.15 mol/(L·min),A项正确;0~25
min内c(CHOH)增大0.70 mol/L,反应生成0.70 mol CH OH,根据方程式可知,同时消耗
3 3
0.70 mol CO ,则CO 的转化率为×100%=70%,B项正确;其他条件不变,升高温度,平衡逆
2 2
向移动,平衡常数减小,C项正确;由图可知,20~25 min内增大压强,平衡正向移动,
c(CHOH)应瞬间增大,而不是逐渐增大,D项错误。]
3
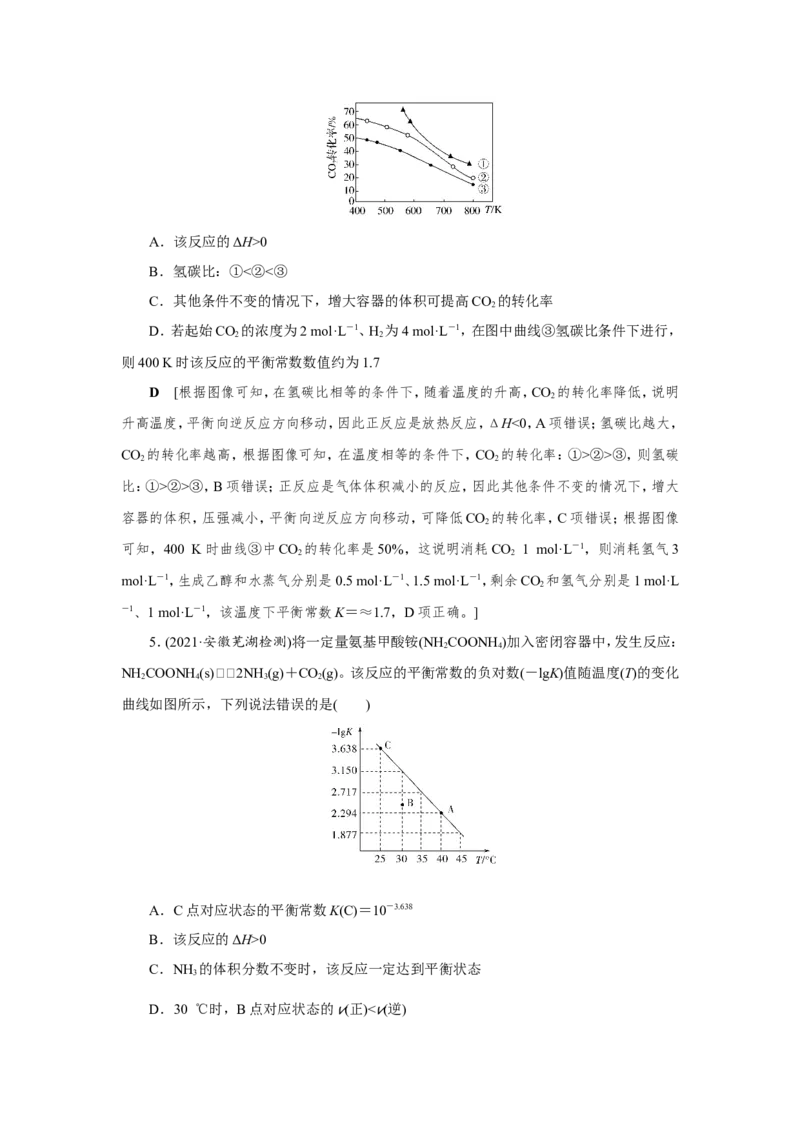
3.(2021·吉林长春调研)在一恒容的密闭容器中充入0.1 mol·L-1 CO、0.1 mol·L-1CH,
2 4
在一定条件下发生反应:CH(g)+CO(g) 2CO(g)+2H(g),测得CH 平衡转化率与温度、
4 2 2 4
压强关系如图,下列有关说法不正确的是( )
A.上述反应的ΔH<0
B.压强:p>p>p>p
4 3 2 1
C.1 100 ℃时该反应的平衡常数约为1.64
D.压强为p 4 时,在y点: v正 >v逆
A [p、p、p、p 是四条等压线,由图像可知,压强一定时,温度越高,CH 的平衡转化率
1 2 3 4 4
越高,故正反应为吸热反应,ΔH>0,A项错误;该反应为气体分子数增加的反应,压强越高,
甲烷的平衡转化率越小,故压强p>p>p>p,B项正确;压强为p、温度为1 100 ℃时,甲烷的
4 3 2 1 4
平衡转化率为80.00%,故平衡时各物质的浓度分别为c(CH)=0.02 mol·L-1,c(CO)=0.02
4 2
mol·L-1,c(CO)=0.16 mol·L-1,c(H )=0.16 mol·L-1,即平衡常数K=≈1.64,C项正确;压强
2
为p 4 时,y点未达到平衡,此时 v正 >v逆 ,D项正确。]
4.(2021·四川绵阳诊断)在恒容密闭容器中进行反应:2CO(g)+6H(g)C HOH(g)+
2 2 2 5
3HO(g) ΔH。在某压强下起始时按不同氢碳比投料(如图中曲线①②③),测得CO 的平衡转
2 2
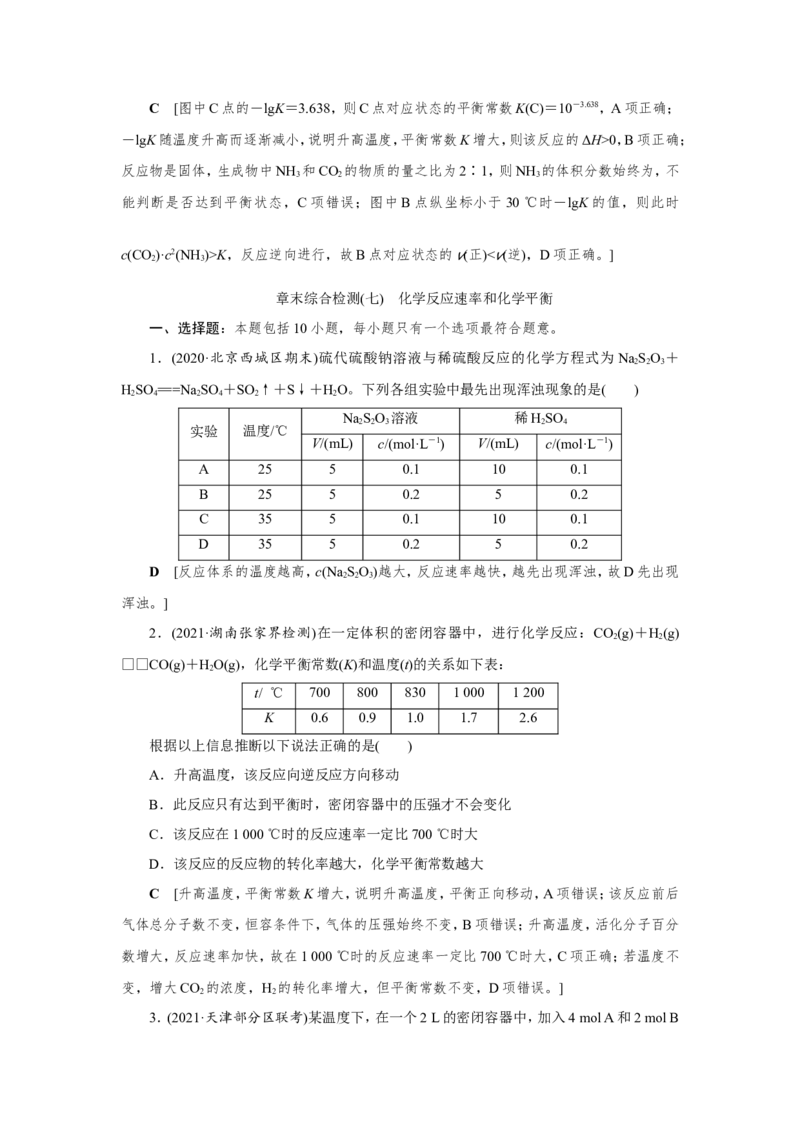
化率与温度的关系如图所示,下列有关说法正确的是( )A.该反应的ΔH>0
B.氢碳比:①<②<③
C.其他条件不变的情况下,增大容器的体积可提高CO 的转化率
2
D.若起始CO 的浓度为2 mol·L-1、H 为4 mol·L-1,在图中曲线③氢碳比条件下进行,
2 2
则400 K时该反应的平衡常数数值约为1.7
D [根据图像可知,在氢碳比相等的条件下,随着温度的升高,CO 的转化率降低,说明
2
升高温度,平衡向逆反应方向移动,因此正反应是放热反应,ΔH<0,A项错误;氢碳比越大,
CO 的转化率越高,根据图像可知,在温度相等的条件下,CO 的转化率:①>②>③,则氢碳
2 2
比:①>②>③,B项错误;正反应是气体体积减小的反应,因此其他条件不变的情况下,增大
容器的体积,压强减小,平衡向逆反应方向移动,可降低CO 的转化率,C项错误;根据图像
2
可知,400 K时曲线③中CO 的转化率是50%,这说明消耗CO 1 mol·L-1,则消耗氢气3
2 2
mol·L-1,生成乙醇和水蒸气分别是0.5 mol·L-1、1.5 mol·L-1,剩余CO 和氢气分别是1 mol·L
2
-1、1 mol·L-1,该温度下平衡常数K=≈1.7,D项正确。]
5.(2021·安徽芜湖检测)将一定量氨基甲酸铵(NH COONH)加入密闭容器中,发生反应:
2 4
NH COONH(s)2NH (g)+CO(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化
2 4 3 2
曲线如图所示,下列说法错误的是( )
A.C点对应状态的平衡常数K(C)=10-3.638
B.该反应的ΔH>0
C.NH 的体积分数不变时,该反应一定达到平衡状态
3
D.30 ℃时,B点对应状态的 v(正)0,B项正确;
反应物是固体,生成物中NH 和CO 的物质的量之比为2∶1,则NH 的体积分数始终为,不
3 2 3
能判断是否达到平衡状态,C项错误;图中B点纵坐标小于30 ℃时-lgK的值,则此时
c(CO
2
)·c2(NH
3
)>K,反应逆向进行,故B点对应状态的 v(正)K,A项错误;
b c
T 温度下,a点NO 体积分数大于平衡值,若由a点达到平衡,应减小压强,使平衡逆向移动,
1 2 4
B项正确;T 温度下,d点处于平衡曲线下方,NO 体积分数小于平衡值,此时反应正向进行,
2 2 4
则有 v(正)>v(逆),C项错误;从b点变为c点,体系的温度升高,只要增加N
2
O
4
的物质的量不
能达到要求,D项错误。]
5.(2020·天津滨海七校联考)可逆反应:mA(s)+nB(g) eC(g)+fD(g),反应过程中,其
他条件不变时,C的百分含量(C%)与温度(T)、压强(P)的关系如图所示。下列叙述中正确的是( )
A.达平衡后,升高温度,则平衡常数K减小
B.达到平衡后,加入催化剂,C%增大
C.化学方程式中:n>e+f
D.达到平衡后,增加A的量,B的转化率增大
A [根据“先拐先平,速率大”的规律,温度为T 时先达到平衡,则温度:TP;压强为P 时C%小于压强为P 时C%,说明压强增大,平衡逆向移动,则
2 1 2 1
有n