文档内容
章末综合检测(三) 金属及其化合物
一、选择题:本题包括8小题,每小题只有一个选项最符合题意。
1.(2021·山西运城高三调研《) 新修本草》中关于“青矾”的描述:“本来绿色,新出窟未
见风者,正如琉璃,烧之赤色”。据此推测,“青矾”的主要成分为( )
A.CuSO ·5H O B.FeSO ·7H O
4 2 4 2
C.ZnSO·7H O D.KAl(SO )·12H O
4 2 4 2 2
B [“青矾”本来绿色,……,烧之赤色,说明“青矾”灼烧过程由绿色变成红色,据此
推知“青矾”可能是FeSO ·7HO。]
4 2
2.(2020·北京顺义区期末)下列关于钠、铝、铁、铜和氧气的反应,不正确的是( )
A.铁在氧气中燃烧,产物为Fe O
2 3
B.钠在空气中易被氧化,所以应该保存在煤油中
C.铝表面很容易被氧气氧化,生成致密的氧化物保护膜
D.铜可以在加热的条件下和氧气反应,生成氧化铜
A [铁在氧气中燃烧生成Fe O,A项错误。]
3 4
3.(2021·河南鹤壁一中检测)下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末
B.二氧化碳通过NaO 粉末
2 2
C.铝与Fe O 发生铝热反应
2 3
D.将锌粒投入Cu(NO ) 溶液
3 2
B [氢气通过灼热的CuO粉末发生的反应为CuO+H=====Cu+HO,固体由CuO变
2 2
为Cu,反应后固体质量减小,A项错误;二氧化碳通过NaO 粉末发生的反应为2NaO +
2 2 2 2
2CO===2Na CO +O ,固体由NaO 变为NaCO ,反应后固体质量增加,B项正确;铝与
2 2 3 2 2 2 2 3
Fe O 发生铝热反应,化学方程式为2Al+Fe O=====Al O+2Fe,反应前后各物质均为固体,
2 3 2 3 2 3
根据质量守恒定律知,反应后固体质量不变,C项错误;将锌粒投入Cu(NO ) 溶液发生的反
3 2
应为Zn+Cu(NO )===Zn(NO)+Cu,固体由Zn变为Cu,反应后固体质量减小,D项错误。]
3 2 3 2
4.(2021·河南洛阳一中检测)用如图所示实验装置进行相关实验探究,其中装置不合理
的是( )
A.鉴别纯碱与小苏打
B.证明NaO 与水反应放热
2 2
C.证明Cl 能与烧碱溶液反应
2
D.探究钠与Cl 反应
2
A [鉴别纯碱与小苏打,试管口略向下倾斜,且铁架台的铁夹要夹在离试管口的三分之一处,故此实验装置错误,A项错误;过氧化钠与水反应放出大量热,则脱脂棉燃烧,B项正
确;氯气与烧碱溶液反应时,锥形瓶中氯气被消耗,压强减小,气球会变大,C项正确;氯气与
钠反应时,尾气端一定要加上蘸有碱液的棉花除去尾气中残留的氯气,避免氯气污染环境,D
项正确。]
5.(2021·安徽六校教育研究会联考)已知A、B、D、E均为中学化学
中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列
有关物质的推断不正确的是( )
A.若A是铁,则E可能为稀硝酸
B.若A是AlCl 溶液,E可能是氨水
3
C.若A是CuO,E是碳,则B为CO
D.若A是NaOH溶液,E是CO,则B为NaHCO
2 3
B [铁与过量稀硝酸反应生成Fe(NO ),与少量稀硝酸反应生成Fe(NO ),Fe(NO ) 与
3 3 3 2 3 3
铁生成Fe(NO ),Fe(NO ) 与稀硝酸生成Fe(NO ),A项正确;AlCl 溶液与氨水反应,无论氨
3 2 3 2 3 3 3
水是否过量均生成Al(OH) 沉淀,B项错误;CuO与过量碳反应生成Cu和CO,与少量碳反
3
应生成Cu和CO,CO和CO 之间可相互转化,C项正确;NaOH溶液与过量CO 反应生成
2 2 2
NaHCO ,与少量CO 反应生成NaCO,NaHCO 和NaCO 之间可相互转化,D项正确。]
3 2 2 3 3 2 3
6.(2021·山西应县检测)新版人民币的硬币采用镍合金,工业上利用镍矿提取镍的一种
流程如下:
已知:镍的金属活动性介于铁和铜之间。下列说法不正确的是( )
A.将镍矿粉碎可以加快“酸浸”速率
B.NaClO的作用是氧化Fe2+
C.NaFe(SO ) (OH) 中,x+2y=n+2m
x y 4 m n
D.工业上可以用热还原法炼镍
C [将镍矿粉碎,可以增大与硫酸接触面积,加快“酸浸”速率,A项正确;NaClO具有
强氧化性,可将酸浸液中Fe2+氧化成Fe3+,B项正确;Na、Fe的化合价分别为+1价、+3价,
根据NaFe(SO ) (OH) 中各元素化合价代数和为0推知,x+3y=n+2m,C项错误;镍的金
x y 4 m n
属活动性介于铁和铜之间,而工业上常采用热还原法冶炼铁和铜,据此推知,可用热还原法
冶炼镍,D项正确。]
7.(2021·山东师大附中一模)实验室可利用硫酸厂废渣(主要成分为铁的氧化物及少量
FeS、SiO 等)制备聚铁和绿矾(FeSO ·7H O),聚铁的化学式可表示为[Fe (OH) (SO ) ] ,主
2 4 2 2 n 4 3-0.5n m
要工艺流程如下:下列说法错误的是( )
A.炉渣中FeS与稀硫酸和氧气反应的离子方程式为:4FeS+3O +12H+===4Fe3++
2
4S↓+6HO
2
B.气体M的成分是SO ,通入HO 溶液得到硫酸,可循环使用
2 2 2
C.向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸干即得绿矾
D.溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数
偏小
C [炉渣中FeS与稀硫酸和氧气反应生成硫单质、硫酸铁和水,反应的离子方程式为
4FeS+3O+12H+===4Fe3++4S↓+6HO,A项正确;气体M的成分是SO ,通入HO 溶液
2 2 2 2 2
得到硫酸,可循环使用,B项正确;溶液X中加入过量铁粉,铁和硫酸铁溶液反应生成硫酸亚
铁,通过蒸发浓缩,冷却结晶,过滤得到绿矾,C项错误;若溶液Z的pH偏小,则聚铁中生成
的氢氧根离子的含量减少,硫酸根离子的含量偏大,将导致聚铁中铁的质量分数偏小,D项
正确。]
8.(2021·北京门头沟区一模)某小组在Fe2+检验实验中观察到异常现象,为探究“红色
褪去”的原因,进行如下实验:
编号 实验步骤 现象
溶液先变红,片刻后红
实验Ⅰ 色褪去,有气体生成(经
检验为O)
2
将实验Ⅰ褪色后的溶液分三份分别进行实验
①无明显现象
实验Ⅱ ②溶液变红
③产生白色沉淀
①溶液变红,一段时间
为进一步探究“红色褪去”的原因,又进行以
实验Ⅲ 后不褪色
下实验
②无白色沉淀产生①
②取反应后的溶液,滴加盐酸和BaCl 溶液
2
分析上述三个实验,下列叙述不正确的是( )
A.在此实验条件下HO 氧化Fe2+的速率比氧化SCN-的速率快
2 2
B.通过实验Ⅱ推出实验Ⅰ中红色褪去的原因是由于SCN-被氧化
C.通过实验Ⅰ和实验Ⅲ对比推出红色褪去只与HO 的氧化性有关
2 2
D.综上所述,实验Ⅰ中红色褪去的原因与化学平衡移动原理无关
D [对比实验Ⅰ和Ⅱ可知,HO 可将Fe2+、SCN-氧化,由于实验Ⅰ中溶液先变红,片刻
2 2
后红色褪去,说明HO 氧化Fe2+的速率比氧化SCN-的速率快,A项正确;实验Ⅱ中滴加盐
2 2
酸和BaCl 溶液,产生白色沉淀,该沉淀应为BaSO,说明SCN-被氧化生成了SO,B项正确;
2 4
对比实验Ⅰ和Ⅲ,说明O 不能将SCN-氧化为SO,溶液红色褪去是由于SCN-被HO 氧化
2 2 2
生成了SO,C项正确;实验Ⅰ中存在平衡:Fe3++3SCN- ⇌Fe(SCN)
3
,SCN-被H
2
O
2
氧化生成
SO,平衡逆向移动,溶液的红色逐渐褪去,D项错误。]
二、非选择题:本题包括3个小题。
9.(2021·安徽蚌埠质检)实验室由铁泥(主要成分为铁的氧化物)制备软磁性材料αFe O。
2 3
其主要实验流程如下:
→→→→……→αFe O
2 3
(1)酸浸。用一定浓度的HSO 溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取
2 4
下列措施能提高铁元素浸出率的有________(填序号)。
A.适当升高酸浸温度
B.适当缩短酸浸时间
C.适当加快搅拌速度
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程
中除生成Fe2+外,还会生成________(填化学式);检测Fe3+是否还原完全的实验操作是
________________________________________________________________________。
(3)除杂。向“还原”后的滤液中加入NH F溶液,使Ca2+转化为CaF 沉淀除去。若溶液
4 2
的pH偏低,将会导致CaF 沉淀不完全,其原因是______________________________。
2
[K (CaF )=5.3×10-9、K(HF)=6.3×10-4]
sp 2 a
(4)沉铁。将提纯后的FeSO 溶液与NH ·H O-NH HCO 混合溶液反应,生成FeCO 沉淀。
4 3 2 4 3 3
生成FeCO 沉淀的离子方程式为_____________________________________。
3答案 (1)AC
(2)H 取少量清液,向其中滴加几滴KSCN溶液,观察溶液颜色是否呈红色
2
(3)pH偏低形成HF,导致溶液中F-浓度减小,CaF 沉淀不完全
2
(4)Fe2++HCO+NH ·H O===FeCO ↓+NH+HO或Fe2++HCO+NH ===FeCO ↓+
3 2 3 2 3 3
NH
10.(2021·河南部分重点校联考)草酸铅(PbC O)是某医药的中间体,以废旧铅酸电池的
2 4
铅膏(PbO、PbO 、PbSO )为原料,制备草酸铅的工艺流程如下:
2 4
――→ComComCom
binbinbin
已知:①PbO 具有强氧化性,稀硝酸不能氧化HO。
2 2
②PbO可溶于稀硝酸。
回答下列问题:
(1)步骤①的目的是“脱硫”,即将PbSO 转化为PbCO ,“脱硫”
4 3
过程可在如图所示的装置中进行。仪器 X的名称是________,“脱
硫”时适宜温度为35 ℃,则可采用的加热方式是______________。
(2)步骤③中HO 的作用是_________________________,
2 2
该反应的离子方程式为_________________________________;
溶解PbO的离子方程式为______________________________。
(3)已知:得到的PbC O 样品中不可能含有碱式碳酸铅[2PbCO ·Pb(OH) ],二者受热都易
2 4 3 2
分解生成PbO。请完成如下实验,证明该样品中不存在碱式碳酸铅。
实验步骤 实验现象
取一定量干燥的样品,
__________________________________
______________________________________
(4)测定制得的草酸铅固体的纯度:称取5.90 g PbC O 固体,酸溶后配制成250 mL溶液,
2 4
然后量取25.00 mL该溶液,用0.05 mol·L-1的EDTA(Na HY)标准溶液滴定(Pb2++HY2-
2 2 2
===PbY2-+2H+,杂质不反应),至滴定终点时消耗EDTA标准溶液28.00 mL。则草酸铅的纯
度为________;若滴定完成时,发现滴定管内有气泡,测定结果将________(填“偏高”“偏
低”或“不变”)。
解析 (1)仪器X的名称为三颈烧瓶;根据“脱硫”时适宜温度为35 ℃,所以采用温水
浴加热。
(2)PbO 具有强氧化性,能够将双氧水氧化,加双氧水的目的是将PbO 还原为Pb2+,反
2 2
应的离子方程式为PbO +2H++HO===Pb2++2HO+O↑;根据已知信息②可知PbO溶
2 2 2 2 2
解的离子方程式为PbO+2H+===Pb2++HO。
2
(3)二者受热都易分解生成PbO,根据元素守恒可知,碱式碳酸铅分解可以生成水,利用
无水硫酸铜不变蓝色,证明样品中没有碱式碳酸铅。
(4)根据Pb2++HY2-===PbY2-+2H+,消耗EDTA标准溶液28.00 mL,则n(PbC O)=
2 2 4
n(Pb2+)=n(H Y2-)=0.028 L×0.05 mol·L-1,则250 mL溶液中n(PbC O)=0.028 L×0.05
2 2 4
mol·L-1×,因此草酸铅的纯度=×100%=70%;若滴定完成时发现滴定管内有气泡,则滴定过程中实际消耗的EDTA标准液体积大于滴定管测得的体积,导致测定结果偏低。
答案 (1)三颈烧瓶 温水浴(或水浴加热)
(2)将PbO 还原为Pb2+ PbO +2H++HO===Pb2++2HO+O↑ PbO+2H+===Pb2+
2 2 2 2 2 2
+HO
2
(3)加热样品使其分解,将产生的气体通过装有无水硫酸铜的干燥管 无水硫酸铜不变
蓝色
(4)70% 偏低
11.(2020·北京房山区二模)某小组用实验Ⅰ验证Fe (SO ) 与Cu的反应,观察到了异常
2 4 3
现象,决定对其进行深入探究。
实验Ⅰ:
(1)Fe (SO ) 溶液常温下呈酸性的原因是____________________________________。
2 4 3
(2)Fe (SO ) 与KSCN溶液反应的离子方程式为_______________________________。
2 4 3
(3)实验前,小组同学预测经过步骤2后溶液不应该呈现红色,依据是_______________。
(4)实验小组对白色沉淀的产生进行了深入探究
查阅资料:ⅰ.CuSCN为难溶于水的白色固体。
ⅱ.SCN-被称为拟卤素离子,性质与卤素离子相似
经过实验测定白色固体为CuSCN,查阅资料后小组同学猜测CuSCN的生成有如下两种
可能
猜测1:Cu2+与KSCN发生了氧化还原反应
猜测2:亚铁离子将其还原Cu2++Fe2+===Cu++Fe3+ Cu++SCN-===CuSCN↓
为证实猜想小组同学做了实验Ⅱ和Ⅲ。
(FeSO 和CuSO 溶液浓度为0.1 mol/L,KSCN溶液浓度为0.4 mol/L)
4 4
实验序号 对比实验及试剂 实验步骤 实验现象
加入1 mL 开始时溶液的上方变为红
KSCN溶 色,一段时间后红色向下蔓
液 延,最后充满整支试管
Ⅱ
加入1 mL
KSCN溶 溶液变成绿色
液
①猜测1的离子方程式___________________________________________;
②实验Ⅱ中试管________(填字母)中的现象可以证实猜测1不成立。
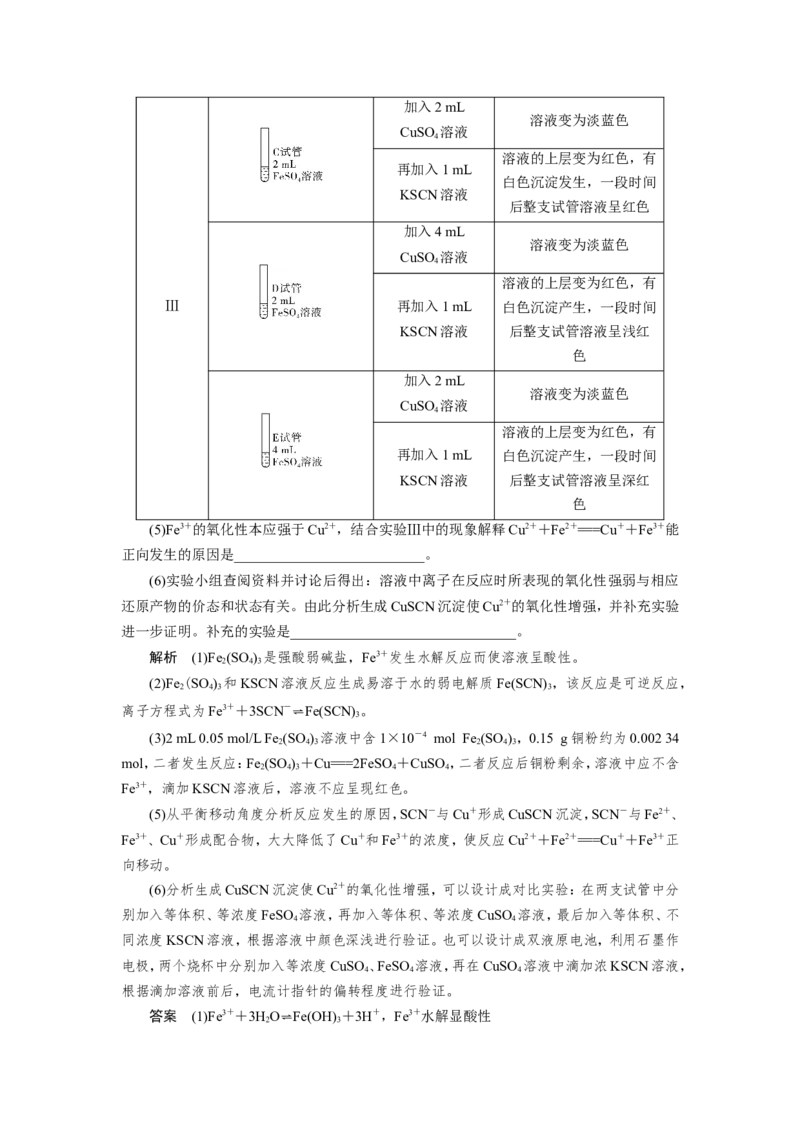
实验序号 对比实验及试剂 实验步骤 实验现象加入2 mL
溶液变为淡蓝色
CuSO 溶液
4
溶液的上层变为红色,有
再加入1 mL
白色沉淀发生,一段时间
KSCN溶液
后整支试管溶液呈红色
加入4 mL
溶液变为淡蓝色
CuSO 溶液
4
溶液的上层变为红色,有
Ⅲ 再加入1 mL 白色沉淀产生,一段时间
KSCN溶液 后整支试管溶液呈浅红
色
加入2 mL
溶液变为淡蓝色
CuSO 溶液
4
溶液的上层变为红色,有
再加入1 mL 白色沉淀产生,一段时间
KSCN溶液 后整支试管溶液呈深红
色
(5)Fe3+的氧化性本应强于Cu2+,结合实验Ⅲ中的现象解释Cu2++Fe2+===Cu++Fe3+能
正向发生的原因是___________________________。
(6)实验小组查阅资料并讨论后得出:溶液中离子在反应时所表现的氧化性强弱与相应
还原产物的价态和状态有关。由此分析生成CuSCN沉淀使Cu2+的氧化性增强,并补充实验
进一步证明。补充的实验是________________________________。
解析 (1)Fe (SO ) 是强酸弱碱盐,Fe3+发生水解反应而使溶液呈酸性。
2 4 3
(2)Fe (SO ) 和KSCN溶液反应生成易溶于水的弱电解质Fe(SCN) ,该反应是可逆反应,
2 4 3 3
离子方程式为Fe3++3SCN- ⇌Fe(SCN)
3
。
(3)2 mL 0.05 mol/L Fe (SO ) 溶液中含1×10-4 mol Fe (SO ),0.15 g铜粉约为0.002 34
2 4 3 2 4 3
mol,二者发生反应:Fe (SO )+Cu===2FeSO+CuSO ,二者反应后铜粉剩余,溶液中应不含
2 4 3 4 4
Fe3+,滴加KSCN溶液后,溶液不应呈现红色。
(5)从平衡移动角度分析反应发生的原因,SCN-与Cu+形成CuSCN沉淀,SCN-与Fe2+、
Fe3+、Cu+形成配合物,大大降低了Cu+和Fe3+的浓度,使反应Cu2++Fe2+===Cu++Fe3+正
向移动。
(6)分析生成CuSCN沉淀使Cu2+的氧化性增强,可以设计成对比实验:在两支试管中分
别加入等体积、等浓度FeSO 溶液,再加入等体积、等浓度CuSO 溶液,最后加入等体积、不
4 4
同浓度KSCN溶液,根据溶液中颜色深浅进行验证。也可以设计成双液原电池,利用石墨作
电极,两个烧杯中分别加入等浓度CuSO 、FeSO 溶液,再在CuSO 溶液中滴加浓KSCN溶液,
4 4 4
根据滴加溶液前后,电流计指针的偏转程度进行验证。
答案 (1)Fe3++3H
2
O⇌Fe(OH)
3
+3H+,Fe3+水解显酸性(2)Fe3++3SCN- ⇌Fe(SCN)
3
(3)依据反应Cu+2Fe3+===Cu2++2Fe2+,Cu粉过量不应有Fe3+存在
(4)①2Cu2++4SCN-===2CuSCN↓+(SCN) ↑
2
②B
(5)由于SCN-与Cu+形成沉淀以及SCN-与Fe2+、Fe3+、Cu+形成配合物,大大降低了产
物中Cu+和Fe3+的浓度,使得该反应平衡得以正向移动
(6)答案不唯一,合理即可得分,可设计对比实验
对比实验及试剂 实验步骤 实验现象
加入4 mL 0.1 mol/L CuSO 溶液 一段时间后整支试
4
再加入1 mL 0.4 mol/L KSCN溶液 管溶液呈红色
一段时间后整支试
加入4 mL 0.1 mol/L CuSO 溶液
4
管溶液比F试管颜
再加入1 mL 1 mol/L KSCN溶液
色更深
也可设计成原电池装置
在左侧烧杯中滴入1滴浓度较大的硫氰化钾溶液,在滴入前与滴入后记录电压表(或电
流计)示数的变化