文档内容
专题讲座(三) 热重分析中的物质成分的判断
目录
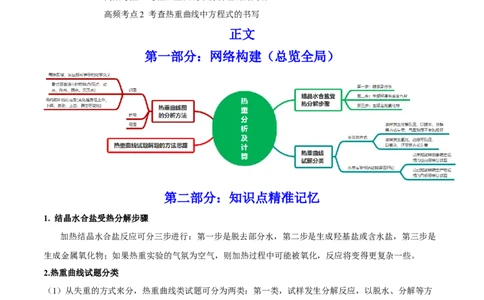
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查热重曲线中物质组成的判断
高频考点2 考查热重曲线中方程式的书写
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
1. 结晶水合盐受热分解步骤
加热结晶水合盐反应可分三步进行:第一步是脱去部分水,第二步是生成羟基盐或含水盐,第三步是
生成金属氧化物;如果热重实验的气氛为空气,则加热过程中可能被氧化,反应将变得更复杂一些。
2.热重曲线试题分类
(1)从失重的方式来分,热重曲线类试题可分为两类:第一类,试样发生分解反应,以脱水、分解等方
式失重,气氛物质不参加反应;第二类,试样发生氧化、还原等反应,以氧化、还原等方式失重。当然也
有试题形式上是两者的结合,但本质上可以分步处理,故仍属于上述类型。
(2)根据热重实验所选试样是否已知,热重曲线类试题可分为两类:第一类以已知试样确定产物组成的
目标思维法试题;第二类以未知试样需要确定组成的逆向思维法试题。
3.热重曲线图的分析方法
坐标曲线题解题时可以拆分为识图、析图、用图三个步骤。其中识图是基础,析图是关键,用图是目的。
(1)识图。识图的关键是三看:一看轴即横、纵坐标所表示的化学含义(自变量X轴和函数Y轴表示的意义),寻找X、Y轴之间的关系,因为这是理解题意和进行正确思维的前提;二看点即曲线中的特殊点(顶点、始
点、终点、拐点、交叉点);三看线即曲线的走势(变化趋势是上升、下降、波动、正态、偏态等变化)。
(2)析图。分析图中为什么会出现这些特殊点,曲线为什么有这样的变化趋势和走向,分析曲线变化的因果
关系;通过联想,把课本内的有关化学概念、原理、规律等与图中的曲线和相关点建立联系。
(3)用图。将相关的化学知识与图中曲线紧密结合,在头脑中构建新的曲线——知识体系,然后运用新的曲
线——知识体系揭示问题的实质,解决实际问题。
4.解题的方法思路
(1)设晶体为1 mol,其质量为m。
(2)失重一般是先失水,再失非金属氧化物。
(3)计算每步固体剩余的质量(m )
余
m
余×100%=固体残留率。
m
(4)晶体中金属质量不再减少,仍在m 中。
余
(5)失重最后一般为金属氧化物,由质量守恒得m ,由n ∶n ,即可求出失重后物质的化学式。
氧 金属 氧
(6)根据失重后物质的化学式,写出相应的化学方程式。
第三部分:典型例题剖析
高频考点1 考查热重曲线中物质组成的判断
例1.正极材料为LiCoO 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
2
Co(OH) 在空气中加热时,固体残留率随温度的变化曲线如图所示。已知钴的氢氧化物加热至290 ℃时已
2
完全脱水,则1 000 ℃时,剩余固体成分为________(填化学式,下同);在350~400 ℃范围内,剩余固体
成分为________。
Co(OH) 的热重曲线
2
【解析】Co(OH) 的摩尔质量为93 g/mol,设Co(OH) 的物质的量为1 mol,则C点1 000 ℃时失重的质量
2 2
为1 mol×93 g/mol×(1-80.65%)=18 g,即1 mol H O,根据质量守恒定律,化学反应方程式为Co(OH)
2 2
CoO+HO。1 000 ℃时剩余固体的成分为CoO。B点500 ℃时失重的质量为1 mol×93 g/mol×(1-86.38%)
2
=12.7 g。已知290 ℃时Co(OH) 已完全脱水,1 mol Co(OH) 脱水成CoO时应失重的质量为18 g,因为
2 2
500 ℃时失重的质量不到18 g,所以一定有氧气进入,使钴元素的化合价发生了变化。进入氧元素的物质
的量为n(O)== mol,即可表述为CoO·O O。
,整理得化学式为Co3 4同理,A点290 ℃时失重的质量为1 mol×93 g/mol×(1-89.25%)=10 g,进入氧元素的物质的量为n(O)==
0.5 mol,即可表述为CoO·O ,整理得化学式为Co O。
0.5 2 3
所以在350~400 ℃范围剩余固体是Co O 和Co O 的混合物。
3 4 2 3
【答案】CoO Co O 和Co O
3 4 2 3
【名师点睛】本题是固体试样以氧化、还原等方式失重的热重曲线试题考查某温度时物质组成的判断,分
析时要注意空气中的氧气参与反应,不完全是分解反应的结果。
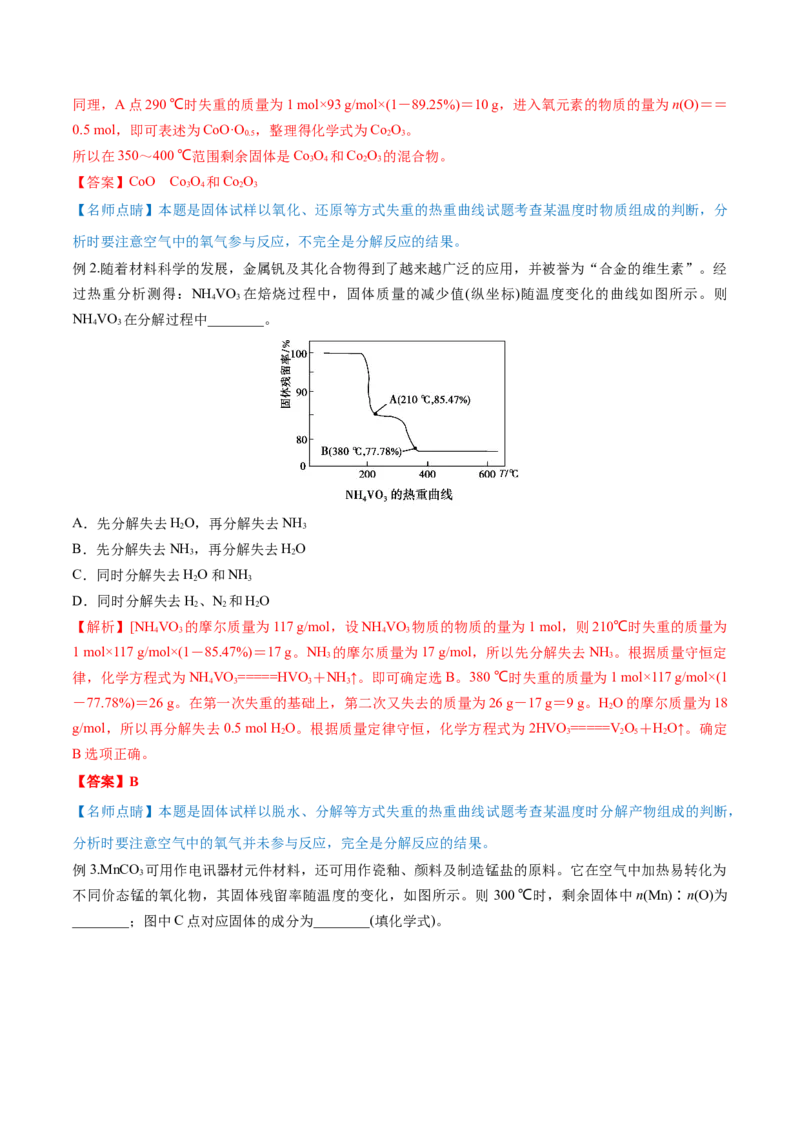
例2.随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”。经
过热重分析测得:NH VO 在焙烧过程中,固体质量的减少值(纵坐标)随温度变化的曲线如图所示。则
4 3
NH VO 在分解过程中________。
4 3
A.先分解失去HO,再分解失去NH
2 3
B.先分解失去NH ,再分解失去HO
3 2
C.同时分解失去HO和NH
2 3
D.同时分解失去H、N 和HO
2 2 2
【解析】[NH VO 的摩尔质量为117 g/mol,设NH VO 物质的物质的量为1 mol,则210℃时失重的质量为
4 3 4 3
1 mol×117 g/mol×(1-85.47%)=17 g。NH 的摩尔质量为17 g/mol,所以先分解失去NH 。根据质量守恒定
3 3
律,化学方程式为NH VO =====HVO +NH ↑。即可确定选B。380 ℃时失重的质量为1 mol×117 g/mol×(1
4 3 3 3
-77.78%)=26 g。在第一次失重的基础上,第二次又失去的质量为26 g-17 g=9 g。HO的摩尔质量为18
2
g/mol,所以再分解失去0.5 mol HO。根据质量定律守恒,化学方程式为2HVO=====VO +HO↑。确定
2 3 2 5 2
B选项正确。
【答案】B
【名师点睛】本题是固体试样以脱水、分解等方式失重的热重曲线试题考查某温度时分解产物组成的判断,
分析时要注意空气中的氧气并未参与反应,完全是分解反应的结果。
例3.MnCO 可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为
3
不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。则 300 ℃时,剩余固体中n(Mn)∶n(O)为
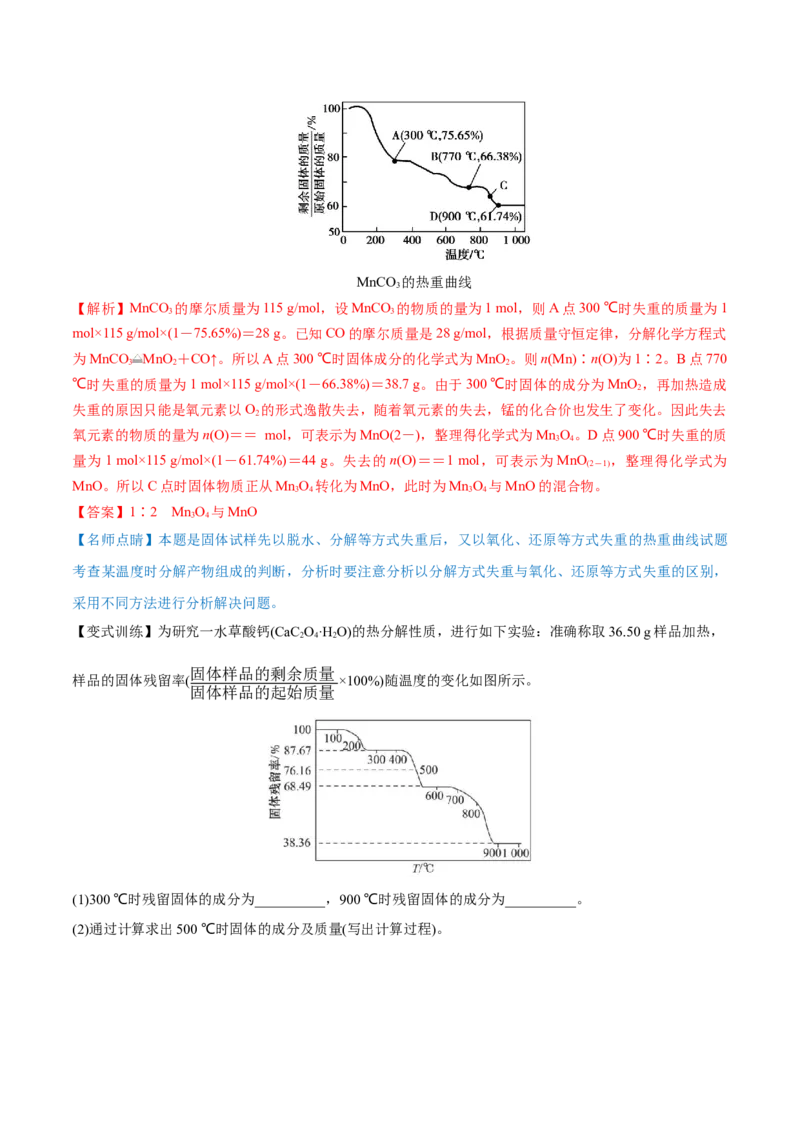
________;图中C点对应固体的成分为________(填化学式)。MnCO 的热重曲线
3
【解析】MnCO 的摩尔质量为115 g/mol,设MnCO 的物质的量为1 mol,则A点300 ℃时失重的质量为1
3 3
mol×115 g/mol×(1-75.65%)=28 g。已知CO的摩尔质量是28 g/mol,根据质量守恒定律,分解化学方程式
为MnCO MnO +CO↑。所以A点300 ℃时固体成分的化学式为MnO 。则n(Mn)∶n(O)为1∶2。B点770
3 2 2
℃时失重的质量为1 mol×115 g/mol×(1-66.38%)=38.7 g。由于300 ℃时固体的成分为MnO ,再加热造成
2
失重的原因只能是氧元素以O 的形式逸散失去,随着氧元素的失去,锰的化合价也发生了变化。因此失去
2
氧元素的物质的量为n(O)== mol,可表示为MnO(2-),整理得化学式为MnO。D点900 ℃时失重的质
3 4
量为1 mol×115 g/mol×(1-61.74%)=44 g。失去的n(O)==1 mol,可表示为MnO ,整理得化学式为
(2-1)
MnO。所以C点时固体物质正从MnO 转化为MnO,此时为MnO 与MnO的混合物。
3 4 3 4
【答案】1∶2 MnO 与MnO
3 4
【名师点睛】本题是固体试样先以脱水、分解等方式失重后,又以氧化、还原等方式失重的热重曲线试题
考查某温度时分解产物组成的判断,分析时要注意分析以分解方式失重与氧化、还原等方式失重的区别,
采用不同方法进行分析解决问题。
【变式训练】为研究一水草酸钙(CaC O·H O)的热分解性质,进行如下实验:准确称取36.50 g样品加热,
2 4 2
固体样品的剩余质量
样品的固体残留率( ×100%)随温度的变化如图所示。
固体样品的起始质量
(1)300 ℃时残留固体的成分为__________,900 ℃时残留固体的成分为__________。
(2)通过计算求出500 ℃时固体的成分及质量(写出计算过程)。36.50 g
【解析】(1)n(CaC O·H O)= =0.25 mol,含有m(HO)=0.25 mol×18 g·mol-1=4.50 g,在300 ℃
2 4 2 146 g·mol-1 2
m(剩余)
时, ×100%=87.67%,m(剩余)=36.50 g×87.67%≈32 g,减少的质量为36.50 g-32 g=4.50 g,故此
m(起始)
m(剩余)
时失去全部的结晶水,残留固体为CaC O;在900 ℃时, ×100%=38.36%,m(剩余) =36.50
2 4 m(起始)
g×38.36%≈14 g,其中Ca的质量没有损失,含m(Ca)=0.25 mol×40 g·mol-1=10 g,另外还含有m(O)=14 g-10
4 g
g=4 g,n(O)= =0.25 mol,则n(Ca)∶n(O)=1∶1,化学式为CaO。
16 g·mol-1
m(剩余)
(2)在600 ℃时, ×100%=68.49%,m(剩余)=36.50 g×68.49%≈25 g,从300 ℃至600 ℃时,失去的
m(起始)
总质量为32 g-25 g=7 g,失去物质的摩尔质量为7 g÷0.25 mol=28 g·mol-1,所以600 ℃时残留固体成分为
CaCO ,则500 ℃时残留固体的成分为CaC O 和CaCO 的混合物,样品中CaC O·H O的物质的量
3 2 4 3 2 4 2
36.50 g
n(CaC O·H O)= =0.25 mol,设混合物中CaC O 和CaCO 的物质的量分别为x mol和y mol,
2 4 2 146 g·mol-1 2 4 3
根据500 ℃时固体总质量可得128x+100y=36.50 g×76.16%,根据钙元素守恒可得x+y=0.25,解得x≈0.10,
y≈0.15,m(CaC O)=0.10 mol ×128 g·mol-1=12.80 g,m(CaCO )=0.15 mol×100 g·mol-1=15.0 g,500 ℃时固体
2 4 3
的成分为12.8 g CaC O 和15.0 g CaCO 。
2 4 3
答案:(1)CaC O CaO(2)12.8 g CaC O 和15.0 g CaCO 。
2 4 2 4 3
高频考点2 考查热重曲线中方程式的书写
例4.在空气中加热10.98 g草酸钴晶体(CoC O·2H O)样品,受热过程中不同温度范围内分别得到一种固体
2 4 2
物质,其质量如表。
温度范围/℃ 固体质量/g
150~210 8.82
290~320 4.82
890~920 4.50
(1)加热到210 ℃时,固体物质的化学式为__________。
(2)经测定,加热到210~320℃过程中的生成物只有CO 和钴的氧化物,此过程发生反应的化学方程式为
2
____ _______________________。147
【解析】(1)CoC O·2H O失去全部结晶水的质量为10.98× g=8.82 g,即加热到210 ℃时,固体物质是
2 4 2
183
8.82
CoC O。(2)根据元素守恒,n(CO)=( ×2) mol=0.12 mol,质量为0.12 mol×44 g·mol-1=5.28 g,固体质量
2 4 2
147
减少(8.82-4.82) g =4.00 g,说明有气体参加反应,即氧气参加,氧气的质量为(5.28-4.00) g=1.28 g,其物质
1.28 8.82
的量为 mol=0.04 mol,n(CoC O)∶n(O )∶n(CO)= ∶0.04∶0.12=0.06∶0.04∶0.12=3∶2∶6,依
2 4 2 2
32 147
据原子守恒,3CoC O+2O Co O+6CO 。
2 4 2 3 4 2
【答案】(1)CoC O (2)3CoC O+2O Co O+6CO
2 4 2 4 2 3 4 2
【名师点睛】本题是固体试样先以脱水、分解等方式失重后,又以氧化、还原等方式失重的热重曲线试题
考查某温度时分解产物组成的判断,分析时要注意分析以分解方式失重与氧化方式失重的区别,采用不同
方法进行分析解决问题。150~210℃为脱水失重,得到的固体产物为CoC O;290~320℃为氧化、分解失
2 4
重,得到的固体产物为Co O;890~920℃为分解失重,得到的固体产物为CoO。
3 4
MgC O ⋅nH O
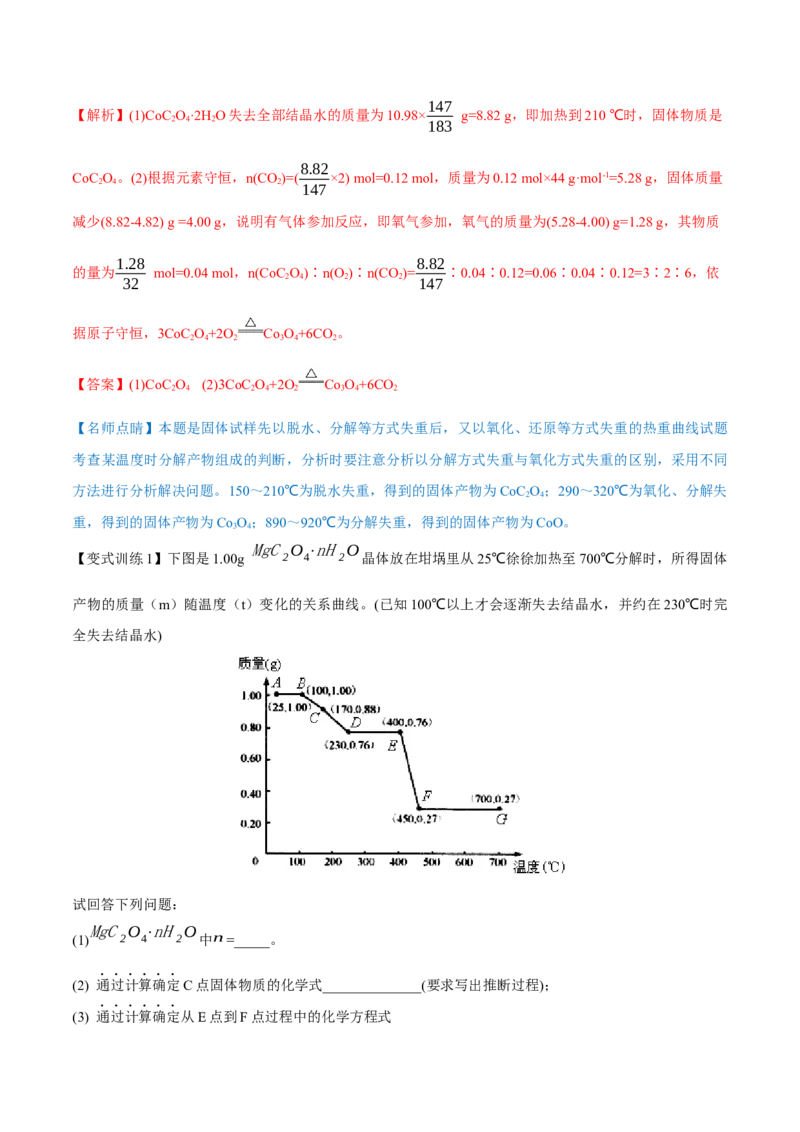
【变式训练1】下图是1.00g 2 4 2 晶体放在坩埚里从25℃徐徐加热至700℃分解时,所得固体
产物的质量(m)随温度(t)变化的关系曲线。(已知100℃以上才会逐渐失去结晶水,并约在230℃时完
全失去结晶水)
试回答下列问题:
MgC O ⋅nH O
(1) 2 4 2 中n=_____。
(2) 通过计算确定C点固体物质的化学式______________(要求写出推断过程);
(3) 通过计算确定从E点到F点过程中的化学方程式(要求写出推断过程)。
MgC O ⋅nH O MgC O nH O
解析:(1) 2 4 2 2 4+ 2
18ng
144+18ng
1.00g (1.00-0.76) g
144+18n 1.00g
18n (1.00−0.76)g
= n=2
MgC O ⋅2H O MgC O ⋅xH O (2−x)H O
(2) 解法一: 2 4 2 2 4 2 + 2
(2−x)18g
148g
1.00g (1.00-0.88) g
148 1.00g
(2−x)18
=
(1.00−0.88)g x=1
B点固体的化学式为
MgC
2
O
4
⋅H
2
O
(没有推断过程,答案正确
也不给分)
MgC O ⋅xH O MgC O xH O
解法二: 2 4 2 2 4+ 2
18x
112
0.76g (0.88-0.76) g
112 0.76g
18x
=
(0.88−0.76)g x=1
B点固体的化学式为
MgC
2
O
4
⋅H
2
O
(没有推断过程,答案正确也
不给分)
MgC O
(3) 2 4 X(s)+Y↑+ Z↑
X(s)
应为Mg之元素的或其他元素组成化合物,利用Mg的原子守恒。
0.76g 0.27g
:
n(MgC O ):n(X) 112g⋅mol−1 M(X) 1:1 M(X)
2 4 = = =40
MgC O
可推测出X即为MgO,而完整的化学方程式为 2 4 MgO+CO↑+ CO ↑(没有推断过程,答
2
案正确也不给分)【答案】(1)2
MgC O ⋅H O
(2) 2 4 2
MgC O
(3) 2 4 MgO+CO↑+ CO ↑
2
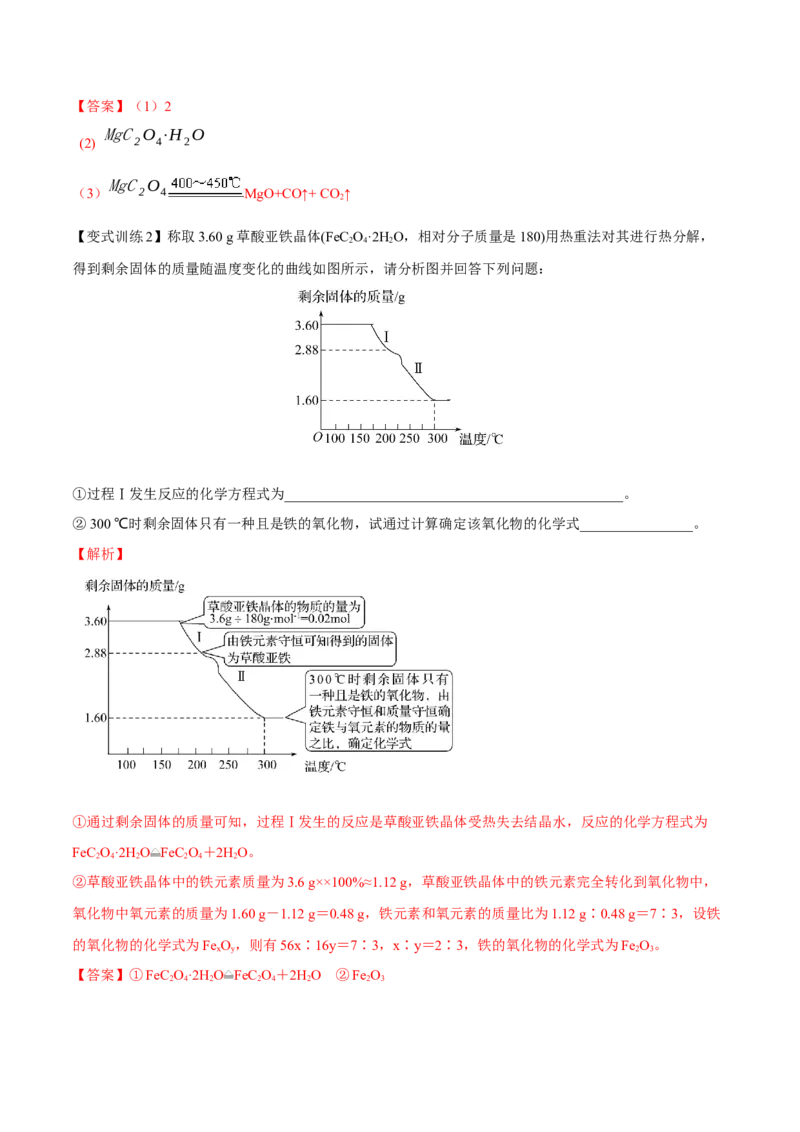
【变式训练2】称取3.60 g草酸亚铁晶体(FeC O·2H O,相对分子质量是180)用热重法对其进行热分解,
2 4 2
得到剩余固体的质量随温度变化的曲线如图所示,请分析图并回答下列问题:
①过程Ⅰ发生反应的化学方程式为________________________________________________。
②300 ℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式________________。
【解析】
①通过剩余固体的质量可知,过程Ⅰ发生的反应是草酸亚铁晶体受热失去结晶水,反应的化学方程式为
FeC O·2H O FeC O+2HO。
2 4 2 2 4 2
②草酸亚铁晶体中的铁元素质量为3.6 g××100%≈1.12 g,草酸亚铁晶体中的铁元素完全转化到氧化物中,
氧化物中氧元素的质量为1.60 g-1.12 g=0.48 g,铁元素和氧元素的质量比为1.12 g∶0.48 g=7∶3,设铁
的氧化物的化学式为Fe O,则有56x∶16y=7∶3,x∶y=2∶3,铁的氧化物的化学式为Fe O。
x y 2 3
【答案】①FeC O·2H O FeC O+2HO ②Fe O
2 4 2 2 4 2 2 3