文档内容
主题三 化学反应原理测试(一)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1.下列有关化学概念或原理的论述中,正确的是 ( )
A.Cl、SO 、NH 的水溶液都能够导电,因此Cl、SO 、NH 都属于电解质
2 2 3 2 2 3
B.用醋酸溶液做导电性实验,灯泡很暗说明醋酸为弱酸
C.将纯水加热到较高温度,水的离子积变大、pH变小、呈中性
D.任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大
【答案】C
【解析】A项,电解质是在水溶液里或熔融状态下能导电的化合物,Cl 是单质,既不是电解质也不是
2
非电解质,SO 、NH 的水溶液虽然可以导电,但是溶液中的离子是由亚硫酸、一水合氨电离产生的,并非
2 3
SO 、NH 自身电离产生的,因此SO 、NH 属于非电解质,A项错误;B项,溶液的导电性与溶液中离子
2 3 2 3
的浓度有关,与酸的强弱无关,B项错误;C项,水的电离是吸热过程,且存在电离平衡HO H+
2
+OH-,将纯水加热到较高温度,水的电离程度增大,c(H+)、c(OH-)均增大,pH变小,但始终
c(H+)=c(OH-),则扔呈中性,水的离子积K =c(H+)c(OH-)变大,C项正确;D项,对于放热反应,降低温度
w
平衡向正反应方向移动,平衡常数变大,但反应速率减小,反应物的转化率增大,D项错误;故选C。
2.下列关于化学平衡常数(K),电离常数(K 或K ),水解常数(K ),溶度积常数(K ),水的离子积常数
a b h sp
(K )的叙述中错误的是( )
W
A.K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行就基本完全
B.比较K 与离子积Q 的相对大小,可判断难溶电解质在给定条件下沉淀能否生成或溶解
sp c
C.K、K 或K 、K 、K 、K 都与温度有关,温度越高,常数值越大
a b h sp W
D.弱酸HA的K 与NaA的K 、水的离子积常数K 三者间的关系可表示为K =K·K
a h W W a h
【答案】C
【解析】K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行就基本完全,A正确;
若K 大于Q,则沉淀溶解,若K 小于Q,则沉淀生成,B正确;放热反应的化学平衡常数K随温度升高
sp c sp c
而减小,C不正确;由表达式可知,三者间的关系可表示为K =K·K ,D正确。
W a h
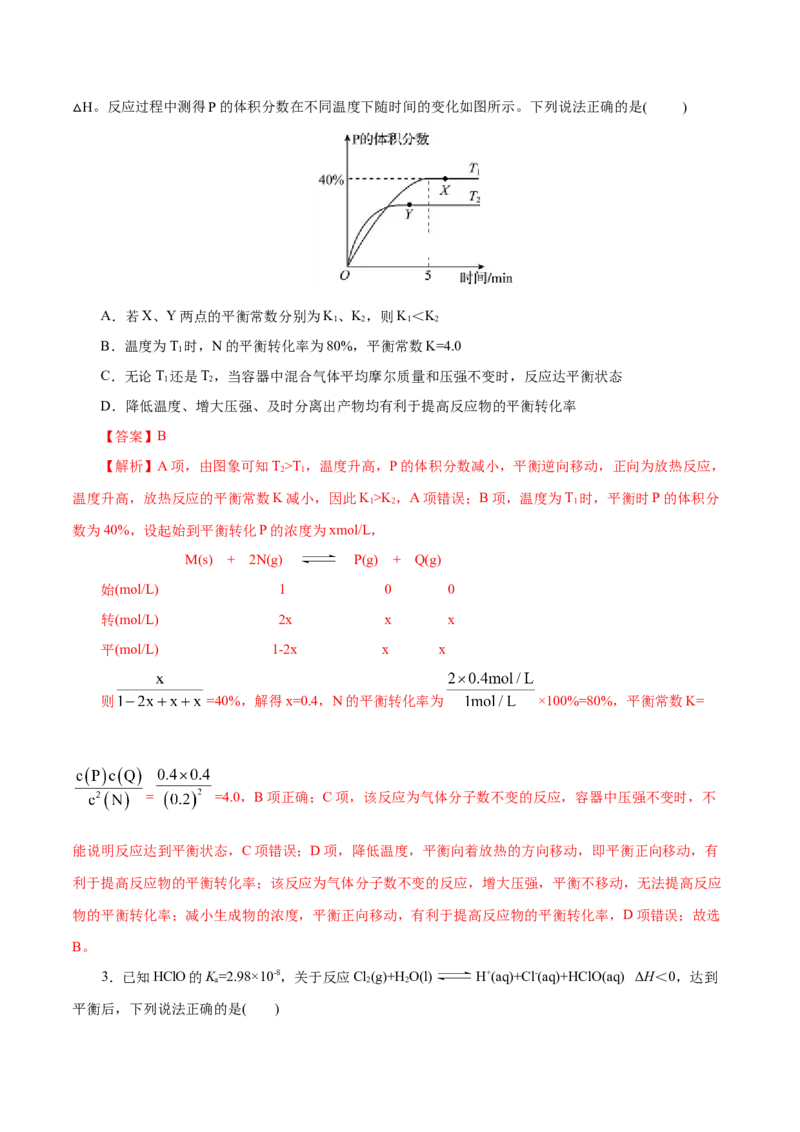
7.将1molM和2 molN置于体积为2L的恒容密闭容器中,发生反应:M(s)+2N(g) P(g)+Q(g)H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
△
A.若X、Y两点的平衡常数分别为K、K,则K<K
1 2 1 2
B.温度为T 时,N的平衡转化率为80%,平衡常数K=4.0
1
C.无论T 还是T,当容器中混合气体平均摩尔质量和压强不变时,反应达平衡状态
1 2
D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率
【答案】B
【解析】A项,由图象可知T>T,温度升高,P的体积分数减小,平衡逆向移动,正向为放热反应,
2 1
温度升高,放热反应的平衡常数K减小,因此K>K ,A项错误;B项,温度为T 时,平衡时P的体积分
1 2 1
数为40%,设起始到平衡转化P的浓度为xmol/L,
M(s) + 2N(g) P(g) + Q(g)
始(mol/L) 1 0 0
转(mol/L) 2x x x
平(mol/L) 1-2x x x
则 =40%,解得x=0.4,N的平衡转化率为 ×100%=80%,平衡常数K=
= =4.0,B项正确;C项,该反应为气体分子数不变的反应,容器中压强不变时,不
能说明反应达到平衡状态,C项错误;D项,降低温度,平衡向着放热的方向移动,即平衡正向移动,有
利于提高反应物的平衡转化率;该反应为气体分子数不变的反应,增大压强,平衡不移动,无法提高反应
物的平衡转化率;减小生成物的浓度,平衡正向移动,有利于提高反应物的平衡转化率,D项错误;故选
B。
3.已知HClO的K=2.98×10-8,关于反应Cl(g)+H O(l) H+(aq)+Cl-(aq)+HClO(aq) ΔH<0,达到
a 2 2
平衡后,下列说法正确的是( )A.取氯水稀释,c(HClO)/c(Cl-)增大
B.100 mL pH=2的新制氯水中:n(OH-)+n(ClO-)+n(HClO)= 0.001mol
C.已知CHCOOH的K=1.75×10-5,CHCOOH溶液的pH一定比HClO溶液的pH小
3 a 3
D.饱和氯水中加入碳酸氢钠固体,上述平衡正向移动,有CO 气体逸出\
2
【答案】D
【解析】氯水中存在平衡Cl+H O H++Cl-+HClO,电离平衡HClO H++ClO-。A项,氯水
2 2
中存在平衡Cl+H O H++Cl-+HClO,HClO H++ClO-,加水稀释,Cl-、ClO-浓度均减小,但平衡
2 2
HClO H++ClO-正向移动,Cl-浓度减小幅度比ClO-浓度减小幅度小,故c(HClO)/c(Cl-)的比值会减小,
A错误;B项,100 mL pH=2的新制氯水中,氢离子的物质的量为n(H+)= =0.001mol,根据
溶液中电荷守恒式可知,n(OH-)+n(ClO-)+n(Cl-)= n(H+)= 0.001mol,但n(H+)>n(HClO),故n(OH-)+n(ClO-)
+n(HClO)<0.001mol,B错误;C项,虽然醋酸的电离平衡常数比次氯酸的大,但起始浓度未知,所以
CHCOOH溶液的pH不一定比HClO溶液的pH小,C错误;D项,碳酸氢钠固体会消耗氢离子,产生二
3
氧化碳气体,从而使Cl(g)+H O(l) H+(aq)+Cl-(aq)+HClO(aq) 平衡向正向移动,D正确;故选D。
2 2
4.一定温度下,H (g)+ Br(g) 2HBr(g) ΔH,该反应历程与能量变化如图所示。已知H-H、
2 2 1
Br-Br、H-Br键能(kJ/mol)分别为a、b、c。下列说法正确的是( )
A.ΔH=E-E ,当加入催化剂时E、E 及两者的差值均减小
1 1 2 1 2
B.平衡后降温,正、逆反应速率均减小,v 比v 减小程度更大
逆 正
C.已知a>c,若反应H (g)+ Br(g) 2HBr(g) ΔH<0,则b>a
2 2
D.H (g)+I(g) 2HI (g) ΔH,则ΔH>ΔH
2 2 2 2 1
【答案】D
【解析】A项,生成物能量大于反应物能量,反应为吸热反应,焓变ΔH=E-E ;催化剂改变反应历
1 1 2
程,降低反应的活化能,但不改变反应焓变,故当加入催化剂时E-E 减小,但是两者的差值不变,A错误;
1 2
B项,反应为吸热反应,平衡后降温,正、逆反应速率均减小,平衡逆向移动,故v 比v 减小程度更小,
逆 正
B错误;C项,若反应H (g)+ Br(g) 2HBr(g) ΔH<0,反应焓变等于反应物键能和减去生成物键
2 2能和,则a+b-2c<0,已知a>c,则a+ba,所需要的时间:a>b,D项正确;故选B。
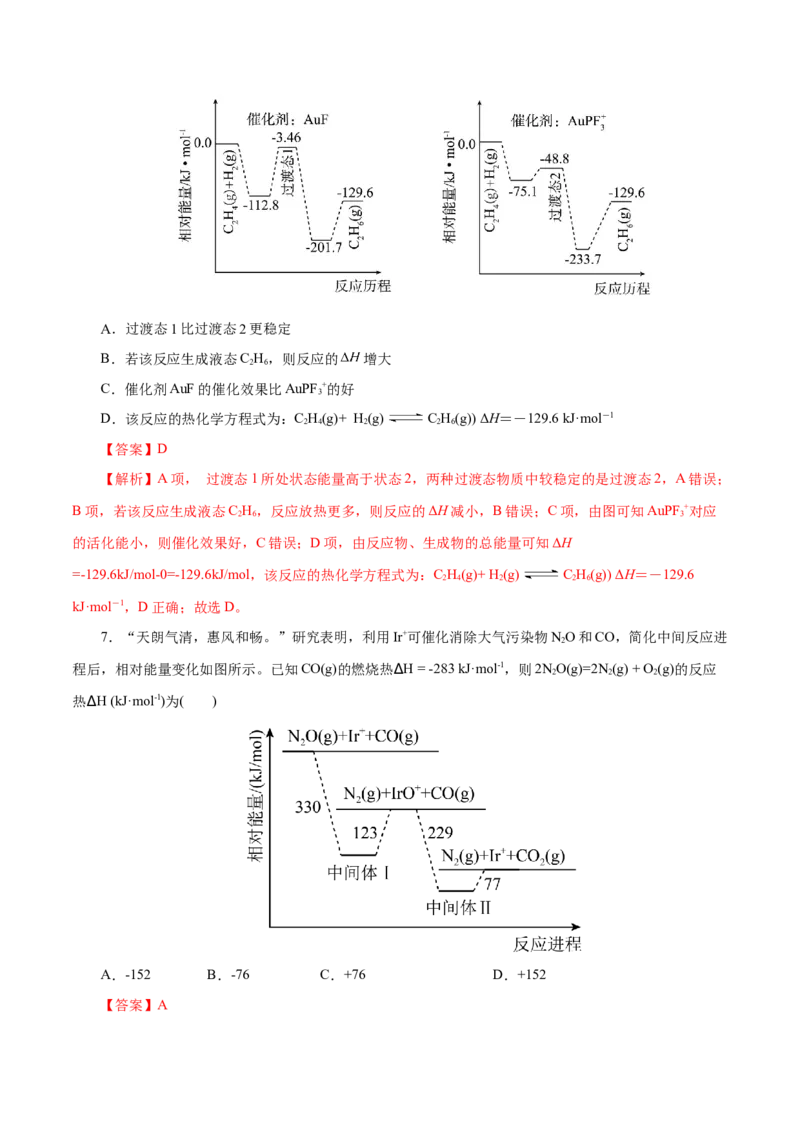
6.我国科学家研究了不同含金化合物催化乙烯加氢的反应历程如图所示,下列说法正确的是( )A.过渡态1比过渡态2更稳定
B.若该反应生成液态C H,则反应的 增大
2 6
C.催化剂AuF的催化效果比AuPF +的好
3
D.该反应的热化学方程式为:C H(g)+ H(g) C H(g)) ΔH=-129.6 kJ·mol-1
2 4 2 2 6
【答案】D
【解析】A项, 过渡态1所处状态能量高于状态2,两种过渡态物质中较稳定的是过渡态2,A错误;
B项,若该反应生成液态C H,反应放热更多,则反应的ΔH减小,B错误;C项,由图可知AuPF +对应
2 6 3
的活化能小,则催化效果好,C错误;D项,由反应物、生成物的总能量可知ΔH
=-129.6kJ/mol-0=-129.6kJ/mol,该反应的热化学方程式为:C H(g)+ H (g) C H(g)) ΔH=-129.6
2 4 2 2 6
kJ·mol-1,D正确;故选D。
7.“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物NO和CO,简化中间反应进
2
程后,相对能量变化如图所示。已知CO(g)的燃烧热∆H = -283 kJ·mol-1,则2NO(g)=2N (g) + O(g)的反应
2 2 2
热∆H (kJ·mol-1)为( )
A.-152 B.-76 C.+76 D.+152
【答案】A【解析】已知CO(g)的燃烧热∆H = -283 kJ·mol-1,可得 ①,由
图可得NO(g)+CO(g)=N (g)+CO (g) ∆H=-330+123-229+77=-359kJ/mol②,由盖斯定律,(反应②-①)×2可
2 2 2
得反应2NO(g)=2N (g) + O(g),反应热∆H =( -359+283)×2 =-152kJ·mol-1,故选A。
2 2 2
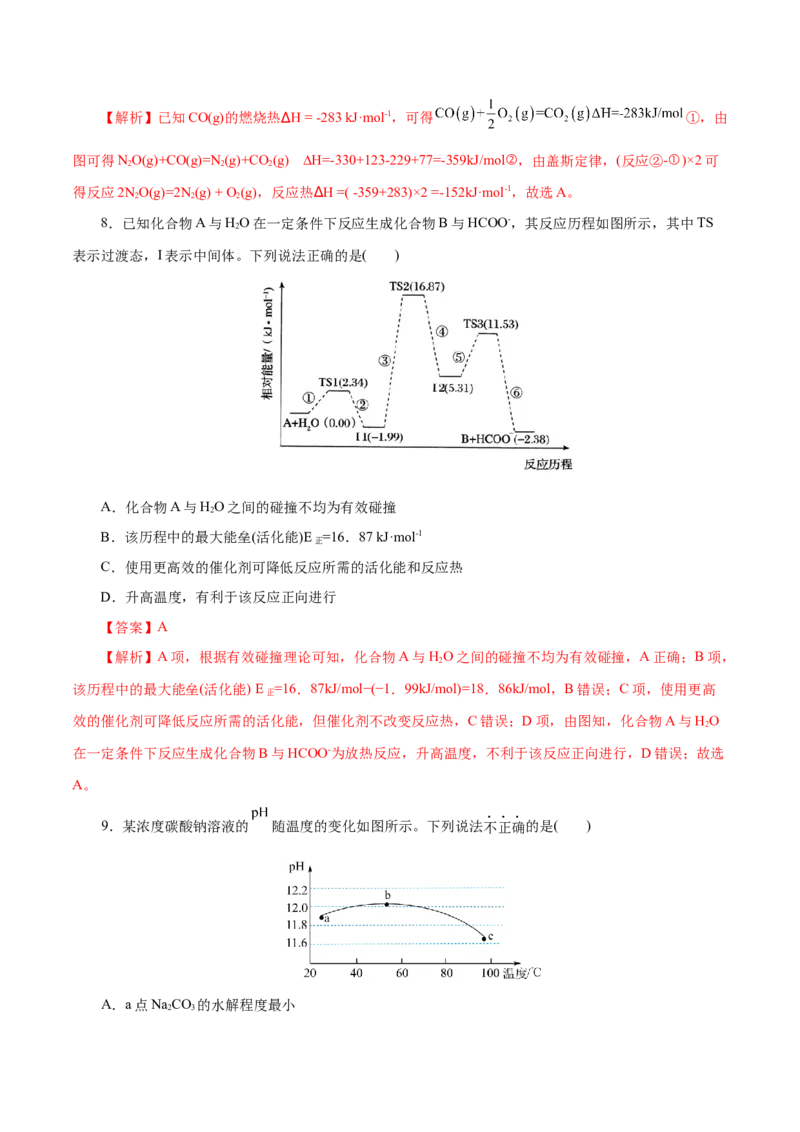
8.已知化合物A与HO在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,其中TS
2
表示过渡态,I表示中间体。下列说法正确的是( )
A.化合物A与HO之间的碰撞不均为有效碰撞
2
B.该历程中的最大能垒(活化能)E =16.87 kJ·mol-1
正
C.使用更高效的催化剂可降低反应所需的活化能和反应热
D.升高温度,有利于该反应正向进行
【答案】A
【解析】A项,根据有效碰撞理论可知,化合物A与HO之间的碰撞不均为有效碰撞,A正确;B项,
2
该历程中的最大能垒(活化能) E =16.87kJ/mol−(−1.99kJ/mol)=18.86kJ/mol,B错误;C项,使用更高
正
效的催化剂可降低反应所需的活化能,但催化剂不改变反应热,C错误;D项,由图知,化合物A与HO
2
在一定条件下反应生成化合物B与HCOO-为放热反应,升高温度,不利于该反应正向进行,D错误;故选
A。
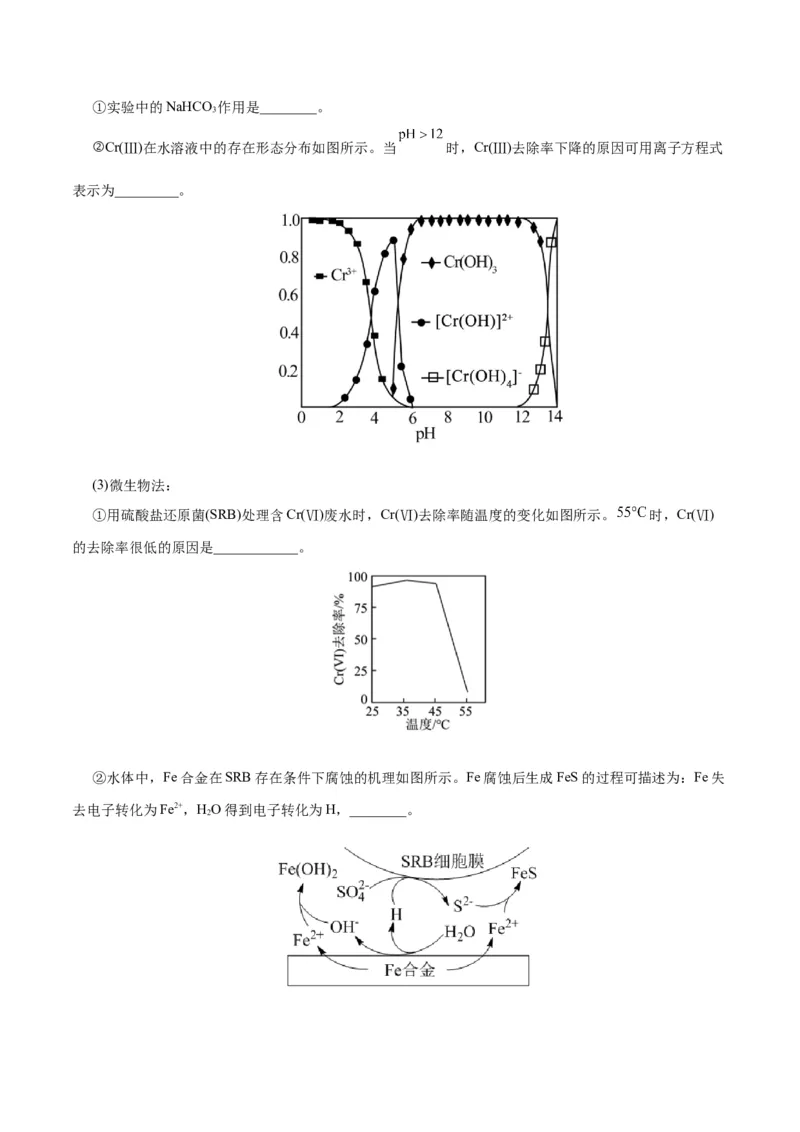
9.某浓度碳酸钠溶液的 随温度的变化如图所示。下列说法不正确的是( )
A.a点NaCO 的水解程度最小
2 3B.b点水的电离程度最大
C.向上述溶液中通入NH , 减小
3
D.c点溶液中存在cNa+=2cCO2-+2cHCO -+2cHCO
3 3 2 3
【答案】B
【解析】加热碳酸钠溶液,存在碳酸根离子的水解平衡和水的电离平衡,温度升高平衡均正向移动,
pH先上升说明,碳酸根离子水解平衡占主导,碱性增强,随后pH下降,说明水的电离平衡占主导,由于
K 变大,c(OH-)、c(H+)浓度均变大,pH变小。A项,升高温度促进NaCO 水解平衡正向移动,故a点
w 2 3
NaCO 的水解程度最小,A正确;B项,升高温度促进水的电离,故c点水的电离程度最大,B不正确;C
2 3
项,向上述溶液中通入NH ,NH 与水反应生成一水合氨,电离出氢氧根离子,抑制CO2-离子水解,CO2-
3 3 3 3
浓度变大,Na+浓度不变,故 减小,C正确;D项,根据物料守恒,c点溶液中存在cNa+=
2cCO2-+2cHCO -+2cHCO,D正确;故选B。
3 3 2 3
10.恒温恒容密闭容器中,在某催化剂表面上发生氨分解反应2NH (g) N(g)+3H(g) ,测得不
3 2 2
同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法正确的是( )
0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.相同条件下,增加氨气浓度,反应速率增大
B.实验①,0至20min时,v(N )=1.00×10-2mol/(L∙min)
2
C.实验②,60min时处于平衡状态,且x<0.20
D.实验③,达到平衡时,H 的体积分数约为22.7%
2
【答案】C
【解析】A项,实验①和实验②催化剂表面积相同,但氨气初始浓度实验①中是实验②中的两倍,结
合数据,可知0~20min、20~40min时间段内实验①和②氨气浓度变化量都是0.40×10-3mol/L,故相同条件下,增加氨气的浓度,反应速率并未加快,A项错误;B项,实验①中,0~20min时间段内,NH 浓度变化
3
量为0.40×10-3mol/L,v(NH ) =2.00×10-5mol/(L∙min),由于反应速率之比等于化学计量数之比,
3
故v(N )= v(NH )=1.00×10-5mol/(L∙min),B项错误;C项,催化剂表面积大小只影响反应速率,不影响平
2 3
衡,实验③中NH 初始浓度与实验①中一样,实验③达到平衡时NH 浓度为0.40×10-3mol/L,则实验①达
3 3
平衡时NH 浓度也为0.40×10-3mol/L,而恒温恒容条件下,实验②相对于实验①为减小压强,平衡正向移
3
动,结合A项,实验②60min时处于平衡状态,x<0.20,C项正确;D项,由实验③中数据可知,达平衡
时NH 反应了2.40×10-3mol/L-0.40mol/L=2×10-3mol/L,则生成的N、H 分别为1.00×10-3mol/L、3.00×10-
3 2 2
3mol/L,平衡时体积分数等于物质的量浓度分数,故H 的体积分数为
2
×100%≈68.2%,D项错误;故选C。
11.将xmolH S气体平均分成两份,分别通入容器A、容器B(容积均为1L),其中一容器为绝热环境,
2
另一容器为25℃恒温环境,在容器内均发生:2HS(g) 2H(g) +S (g) ΔH>0 (25℃),相关数据
2 2 2
如下表:
时间/min 0 10 20 30 40 50 60
容器A 0 0.8 1.5 2 2.3 2.4 2.4
容器B 0 1 1.8 2.5 3 3 3
下列说法正确的是( )
A.根据上表信息,可推算出x=3
B.容器A为25℃恒温环境,容器B为绝热环境
C.1~60min内,25℃恒温环境反应速率可表示为v(H S生成)=0.1mol·L-1·min-1
2
D.可通过降低容器的温度,从而加快逆反应的速率,达到抑制HS气体分解的目的
2
【答案】C
【解析】该反应是吸热反应,反应过程中绝热环境容器的反应温度低于25℃恒温环境容器的反应温度,
反应速率慢于25℃恒温环境容器的反应速率,由表格数据可知,容器A中反应达到平衡的时间多于容器B
中反应达到平衡的时间,则容器A为绝热环境,容器B为25℃恒温环境,由40s反应达到平衡时,B容器
中S 的物质的量为3mol可知,平衡时容积为1L的容器中硫化氢、氢气、S 的浓度为 mol/L、
2 26mol/L、3mol/L,由平衡常数为12可得: =12,解得x=18。A项,x为18,故A错误;B项,容
器A为绝热环境,容器B为25℃恒温环境,故B错误;C项,容器B为25℃恒温环境,60min时S 的物
2
质的量为3mol,则1~60min内,则容积为1L的容器中硫化氢的反应速率为 =0.1 mol/(L·min),故C
正确;D项,降低容器的温度,正、逆反应速率均减慢,故D错误;故选C。
12.乙醛酸(OHC-COOH)是一种重要的化工中间体。工业上以乙二醛为原料制备乙醛酸的装置如图所
示,通电后,阳极产物将乙二醛氧化为乙醛酸。下列说法错误的是( )
A.a极电势高于b极
B.离子交换膜为阴离子交换膜
C.当有0.5mol离子通过离子交换膜时,理论上最多可生成乙醛酸的质量为18.5g
D.乙二醛被氧化的化学方程式: +H O+Cl → +2HCl
2 2
【答案】B
【解析】由题中信息:通电后,阳极产物将乙二醛氧化为乙醛酸,结合题中装置图,可知阳极生成
的Cl 通入盛放盐酸和乙二醛混合液一侧,Cl 与乙二醛发生氧化还原反应,生成Cl-移向与a电极相连的电
2 2
极,与b电极相连的电极发生还原反应,生成H,a为电源正极,b为电源负极。根据电解原理,可知阳
2
极发生的电极反应式为2Cl-―2e-=Cl↑,阴极发生还原反应,电极反应方程式为2H++2e-=H ↑。A项,a电
2 2
极为正极,b电极为负极,因此a极电势高于b极,故A正确;B项,根据题意氢离子由左侧经离子交换膜
进入右侧,则离子交换膜为阳离子交换膜,故B错误;C项,根据得失电子守恒有1molOHC—
COOH~1molCl ~2mole-,则当有0.5mol离子通过离子交换膜时,理论上最多可生成乙醛酸的质量为
2,故C正确;D项,氯气将乙二醛氧化为乙醛酸,自身被还原为氯离子,化学
方程式为: +H O+Cl → +2HCl,故D正确;故选B。
2 2
13.在化学实践中,科研工作者会使用许多缓冲溶液。在缓冲溶液中发挥作用的物质称为缓冲对,一
个缓冲对包含2个相差1个H+的分子或离子。在人体的血液(pH约7.35-7.45)中也有HCO/HCO-,
2 3 3
HPO -/HPO 2-/等缓冲对。下图为参考数据。关于缓冲溶液相关实验,下列说法正确的是( )
2 4 4
物质 HCO HCO - CHCOOH NH HC O HC O-
2 3 3 3 3 2 2 4 2 4
pKa/pK 6.4 10.3 4.7 4.7 1.3 4.3
b
A.为构建pH=3的缓冲溶液,可采用HCO/HCO-缓冲对
2 3 3
B.某缓冲溶液仅由HC O/NaHC O 配制而成,且该溶液pH=1,则配制时可将0.2mol/L的HC O 溶
2 2 4 2 4 2 2 4
液与0.1mol/L的NaHC O 溶液等体积混合
2 4
C.将浓度均为2mol/L的CHCOONH/ Na C O 溶液混合,则c(OH-)>c(HC O-)
3 4 2 2 4 2 4
D.将浓度均为0.2mol/L的1L MgCl 溶液与2L Na CO 溶液混合,此时Mg2+可视为完全沉淀,且沉淀
2 2 3
质量为14.2g,则此时溶液pH约为10
【答案】D
【解析】A项,由表可知,HCO/HCO-缓冲对形成的溶液的pH大于3,A错误;B项,0.2mol/L的
2 3 3
HC O 溶液与0.1mol/L的NaHC O 溶液等体积混合,则得到0.1mol/L的HC O 与0.05mol/L的NaHC O 的
2 2 4 2 4 2 2 4 2 4
混合溶液,则 , c(H+)=20×10-2.3mol·L-1 mol/L,pH≠1,B错误;
C项,由表知,铵根离子、乙酸根离子水解程度相等,而铵根离子水解程度大于草酸根离子,铵根离子水
解的氢离子结合了草酸根离子水解的氢氧根离子生成水,使得草酸氢根离子浓度大于氢氧根离子浓度,C
错误;D项,设生成氢氧化镁、碳酸镁分别为amol、(0.2-a)mol,则58a+84×(0.2-a)=14.2,a=0.1mol,CO2-
3
+H O HCO -+OH-,0.2mol碳酸根离子水解生成0.2mol碳酸氢根离子、0.2mol氢氧根离子,氢氧根离
2 3
子转化为氢氧化镁沉淀,结合碳质量守恒,反应后碳酸根离子为0.2mol、碳酸氢根离子为0.2mol,则
, c(OH-)=10-3.7mol·L-1,pOH≈4,pH≈10,D正确;故选D。14.已知:常温下,氢硫酸HS的电离常数K =1.1×10-7,K =1.3×10-13,K (FeS)= 6.3×10-18,
2 a1 a2 sp
K (HgS)= 1.6×10-52。往10mL0.1mol/LH S(pH约为4.1)溶液中加入10mL0.1mol/LNaOH溶液,然后再滴加
sp 2
入0.1mol/LFeSO 溶液。溶液混合后体积变化忽略不计,下列说法不正确的是( )
4
A.0.1mol/LH S溶液中存在c(H+)>c(HS-)>c(OH―)>c(S2-)
2
B.HS与NaOH溶液反应至溶液呈中性时,cNa++cHS- c(S2-)=0.1mol·L-1
2 2
C.滴加入0.1mol/LFeSO 溶液时,会产生FeS沉淀
4
D.FeS固体能用于去除工业废水中的Hg2+
【答案】B
【解析】A项,0.1mol/LH S溶液中存在电离平衡HS SH-+H+ (H S以第一步电离为主)、H -
2 2 2 S
S2-+H+、HO OH-+H+,0.1mol/LH S溶液的pH约为4.1,则c(OH-)=1.0×10-9.9mol·L-1,
2 2
, ,则
,故c(H+)>c(HS-)>
c(OH―)>c(S2-),故A正确;
B项,溶液中存在电荷守恒cNa++cH+=cOH-+cHS-+2cS2-,HS与NaOH溶液反应至溶液呈中性
2
时,c(OH―)=c(H+),则 cNa+=cHS-+2c(S2-),则 cNa++ cHS=cHS-+2cS2-+ cHS,cNa++
2 2
cHS- cS2-=cHS-+cS2-+ cHS= cS溶液体积变大,故,c(S2-)<0.1mol·L-1,cNa++cHS- c(S2-)
2 2 2
<0.1mol·L-1,故B错误;C项,往10mL0.1mol/LH S溶液中加入10mL0.1mol/LNaOH溶液,恰好发生反应
2
生成 NaHS,滴加入 0.1mol/LFeSO 溶液时,发生反应 HS-+Fe2+=FeS+H+,该反应的平衡常数为
4
,会产生FeS沉淀,故 C正确;D
项,FeS的溶度积比HgS的溶度积大,难溶电解质易转化为更难溶的电解质,则 FeS固体能用于去除工业
废水中的Hg2+,故 D正确;故选B。
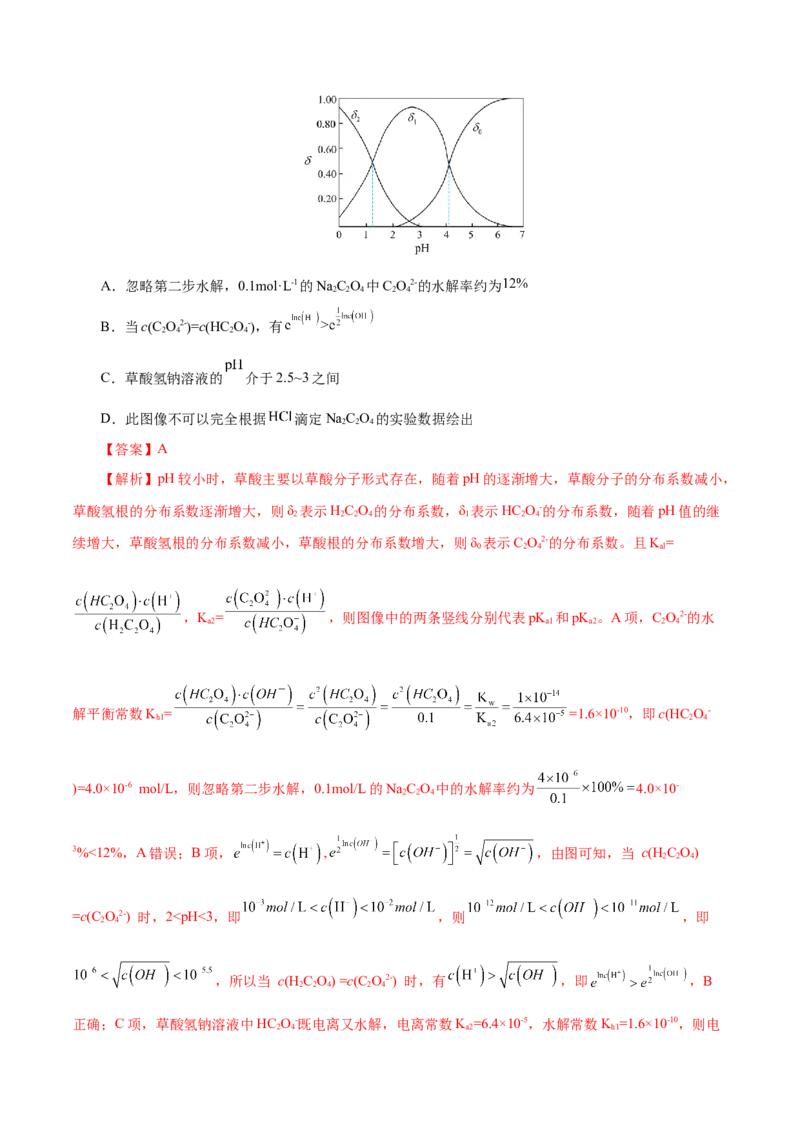
15.分布系数 在处理平衡浓度时,应用广泛。图为草酸的分布系数与pH的关系图。其中,草酸
K =5.9×10-2,K =6.4×10-5下列说法不正确的是( )
a1 a2A.忽略第二步水解,0.1mol·L-1的NaC O 中C O2-的水解率约为
2 2 4 2 4
B.当cC O2-=cHC O-,有
2 4 2 4
C.草酸氢钠溶液的 介于2.5~3之间
D.此图像不可以完全根据 滴定NaC O 的实验数据绘出
2 2 4
【答案】A
【解析】pH较小时,草酸主要以草酸分子形式存在,随着pH的逐渐增大,草酸分子的分布系数减小,
草酸氢根的分布系数逐渐增大,则δ 表示HC O 的分布系数,δ 表示HC O-的分布系数,随着pH值的继
2 2 2 4 1 2 4
续增大,草酸氢根的分布系数减小,草酸根的分布系数增大,则δ 表示C O2-的分布系数。且K =
0 2 4 al
,K = ,则图像中的两条竖线分别代表pK 和pK 。A项,C O2-的水
a2 a1 a2 2 4
解平衡常数K = =1.6×10-10,即cHC O-
h1 2 4
=4.0×10-6 mol/L,则忽略第二步水解,0.1mol/L的NaC O 中的水解率约为 4.0×10-
2 2 4
3%<12%,A错误;B项, , ,由图可知,当 c(H C O)
2 2 4
=c(C O2-) 时,2K,
平衡逆向,同时没有改变温度,K值不变,A项错误;B项,A点Cr O2-为0.25mol/L,由原子守恒得溶液
2 7
中的CrO2-为1.0-0.25×2=0.5mol/L,则v(CrO 2-)= ,B项正确;C项,升温CrO2-
4 4 4
转化率减小即平衡逆向移动,说明逆向为吸热反应,该反应为放热反应,ΔH<0,C项错误;故选AC。(2)
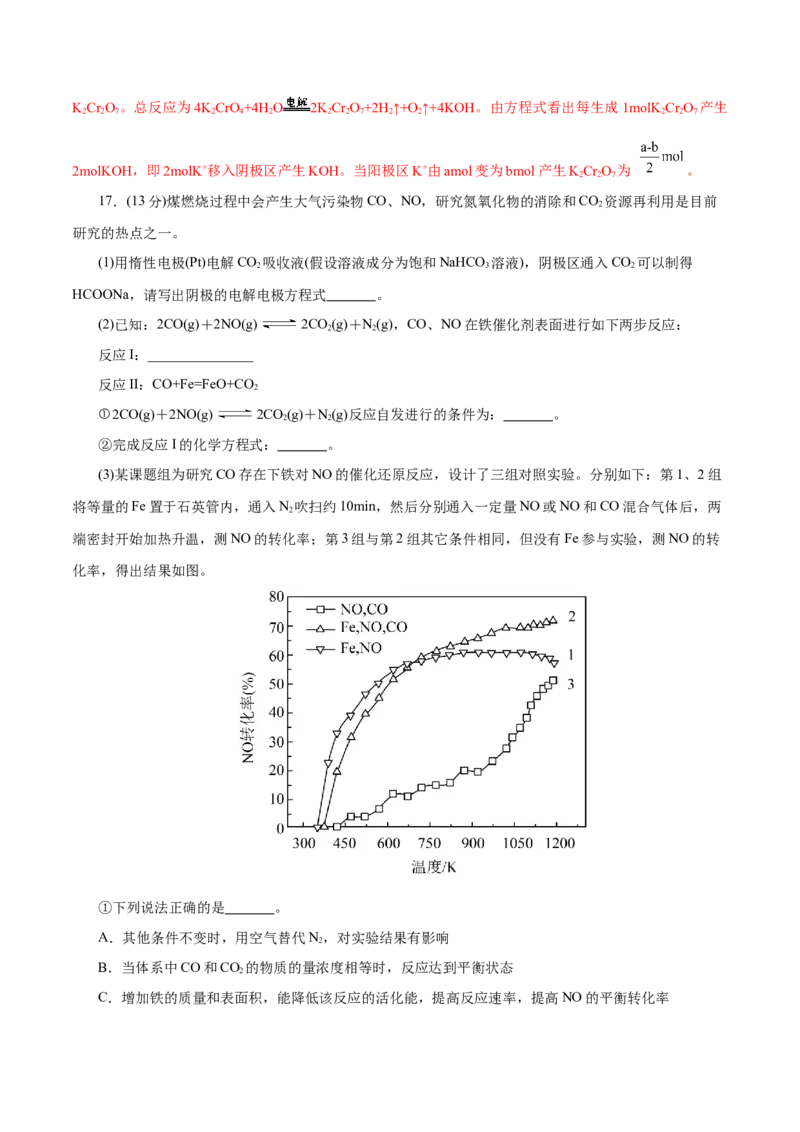
实验中将除Cr(OH) 沉淀除去,则NaHSO 将Cr(Ⅵ)还原为Cr(III) ,便于沉淀除去。从图分析 pH>12时
3 3
[Cr(OH) ]-增大而Cr(OH) 降低,则反应为Cr(OH) +OH-=[Cr(OH) ]-;(3)温度过高,硫酸盐还原菌失活导致
4 3 3 4
去除率降低。从图看H和SO 2-经SRB细胞膜之后转变为S2-和HO,S2-再与Fe2+结合为FeS;(4)阴极区为
4 2
H+放电产生H 。阳极区OH-放电产生H+和O ,H+促使2CrO2-+2H+ CrO2-+H O 平衡正向从而制备
2 2 4 4 2KCr O 。总反应为4KCrO+4H O 2KCr O+2H ↑+O ↑+4KOH。由方程式看出每生成1molK Cr O 产生
2 2 7 2 4 2 2 2 7 2 2 2 2 7
2molKOH,即2molK+移入阴极区产生KOH。当阳极区K+由amol变为bmol产生KCr O 为 。
2 2 7
17.(13分)煤燃烧过程中会产生大气污染物CO、NO,研究氮氧化物的消除和CO 资源再利用是目前
2
研究的热点之一。
(1)用惰性电极(Pt)电解CO 吸收液(假设溶液成分为饱和NaHCO 溶液),阴极区通入CO 可以制得
2 3 2
HCOONa,请写出阴极的电解电极方程式 。
(2)已知:2CO(g)+2NO(g) 2CO(g)+N(g),CO、NO在铁催化剂表面进行如下两步反应:
2 2
反应I:_______________
反应II:CO+Fe=FeO+CO
2
①2CO(g)+2NO(g) 2CO(g)+N(g)反应自发进行的条件为: 。
2 2
②完成反应I的化学方程式: 。
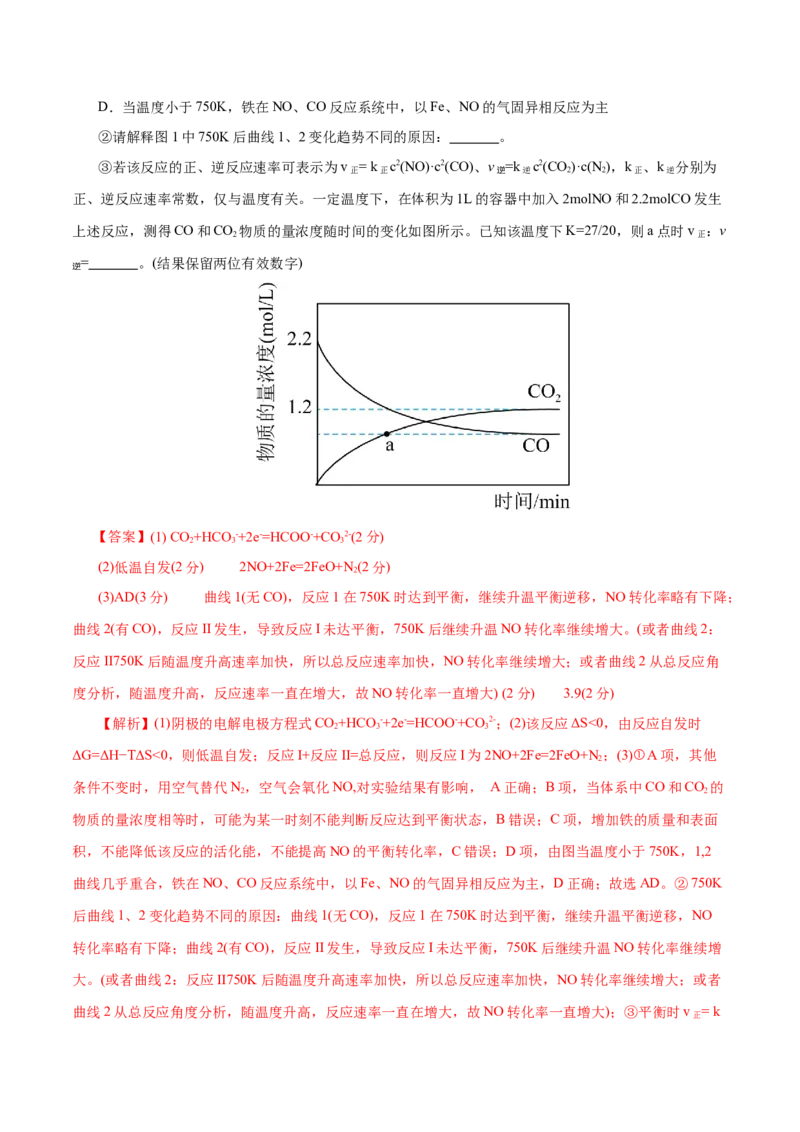
(3)某课题组为研究CO存在下铁对NO的催化还原反应,设计了三组对照实验。分别如下:第1、2组
将等量的Fe置于石英管内,通入N 吹扫约10min,然后分别通入一定量NO或NO和CO混合气体后,两
2
端密封开始加热升温,测NO的转化率;第3组与第2组其它条件相同,但没有Fe参与实验,测NO的转
化率,得出结果如图。
①下列说法正确的是 。
A.其他条件不变时,用空气替代N,对实验结果有影响
2
B.当体系中CO和CO 的物质的量浓度相等时,反应达到平衡状态
2
C.增加铁的质量和表面积,能降低该反应的活化能,提高反应速率,提高NO的平衡转化率D.当温度小于750K,铁在NO、CO反应系统中,以Fe、NO的气固异相反应为主
②请解释图1中750K后曲线1、2变化趋势不同的原因: 。
③若该反应的正、逆反应速率可表示为v = k c2(NO)·c2(CO)、v =k c2(CO)·c(N),k 、k 分别为
正 正 逆 逆 2 2 正 逆
正、逆反应速率常数,仅与温度有关。一定温度下,在体积为1L的容器中加入2molNO和2.2molCO发生
上述反应,测得CO和CO 物质的量浓度随时间的变化如图所示。已知该温度下K=27/20,则a点时v :v
2 正
= 。(结果保留两位有效数字)
逆
【答案】(1) CO +HCO-+2e-=HCOO-+CO 2-(2分)
2 3 3
(2)低温自发(2分) 2NO+2Fe=2FeO+N (2分)
2
(3)AD(3分) 曲线1(无CO),反应1在750K时达到平衡,继续升温平衡逆移,NO转化率略有下降;
曲线2(有CO),反应II发生,导致反应I未达平衡,750K后继续升温NO转化率继续增大。(或者曲线2:
反应II750K后随温度升高速率加快,所以总反应速率加快,NO转化率继续增大;或者曲线2从总反应角
度分析,随温度升高,反应速率一直在增大,故NO转化率一直增大) (2分) 3.9(2分)
【解析】(1)阴极的电解电极方程式CO+HCO-+2e-=HCOO-+CO 2-;(2)该反应ΔS<0,由反应自发时
2 3 3
ΔG=ΔH−TΔS<0,则低温自发;反应I+反应II=总反应,则反应I为2NO+2Fe=2FeO+N ;(3)①A项,其他
2
条件不变时,用空气替代N,空气会氧化NO,对实验结果有影响, A正确;B项,当体系中CO和CO 的
2 2
物质的量浓度相等时,可能为某一时刻不能判断反应达到平衡状态,B错误;C项,增加铁的质量和表面
积,不能降低该反应的活化能,不能提高NO的平衡转化率,C错误;D项,由图当温度小于750K,1,2
曲线几乎重合,铁在NO、CO反应系统中,以Fe、NO的气固异相反应为主,D正确;故选AD。②750K
后曲线1、2变化趋势不同的原因:曲线1(无CO),反应1在750K时达到平衡,继续升温平衡逆移,NO
转化率略有下降;曲线2(有CO),反应II发生,导致反应I未达平衡,750K后继续升温NO转化率继续增
大。(或者曲线2:反应II750K后随温度升高速率加快,所以总反应速率加快,NO转化率继续增大;或者
曲线2从总反应角度分析,随温度升高,反应速率一直在增大,故NO转化率一直增大);③平衡时v = k
正c2(NO)·c2(CO)= v =k c2(CO)·c(N),则
正 逆 逆 2 2
,a点时列三段式为
。
18.(14分)CO 甲烷化是实现“双碳”目标的重要途径。已知合成塔内发生的反应有:
2
Ⅰ. 4H (g)+ CO (g) CH(g)+ 2H O(g) ΔH
2 2 4 2 1
Ⅱ. H (g)+ CO (g) CO (g)+ H O(g) ΔH>0
2 2 2 2
Ⅲ. 3H (g)+ CO (g) CH (g)+ H O(g) ΔH<0
2 2 4 2 3
回答下列问题:
(1)催化剂的选择是CO 甲烷化技术的核心,图1为催化剂M催化反应Ⅰ的历程。根据图1中能量变化
2
情况,求算ΔH=_______ kJ·mol-1 (列式表示);反应_______(填“ⅰ”或“ⅱ”)决定了反应Ⅰ正反应速率
1
的快慢。
(2)反应Ⅱ的正、逆反应速率可分别表示为v =k c(CO)c(H),v =k c(CO)c(H O),k 、k 分别为
正 正 2 2 逆 逆 2 正 逆正、逆反应速率常数。T℃,在一恒容密闭容器中加入等物质的量的CO(g)和H (g)只发生反应Ⅱ,测得
2 2
HO(g)和H (g)的物质的量随时间变化如图2,则M点时, _______。
2 2
(3)保持CO 和H 体积比1:4向合成塔内投料,发生反应Ⅰ、Ⅱ、Ⅲ。
2 2
①若塔内气体的总流量控制在 ,300℃测得CO 的转化率为80%,则CO 反应速率为
2 2
_______
②关于合成塔内反应体系,说法错误的是_______(填序号)。
A.降低反应温度,Ⅰ、Ⅱ、Ⅲ的反应速率都减小
B.平衡后增大体系压强,Ⅰ和Ⅲ平衡正向移动,Ⅱ平衡不移动
C.选用合适的催化剂能提高甲烷的选择性
D.其他条件不变时,增大CO 和H 的投料比,可提高CO 的平衡转化率
2 2 2
E.及时分离出水蒸气、循环使用CO 和H,可提高原料的利用率
2 2
③不同压强时,反应塔内CO 的平衡转化率随温度变化曲线如图所示。压强p、p、p 由大到小的顺
2 1 2 3
序为_______;温度为T℃时,三条曲线几乎交于一点的原因是_______。
【答案】(1) ∆H+∆H(1分) ⅱ(1分)
2 3
(2)9(2分)
(3)9.6(2分) D(3分) p >p >p(2分) T℃时以反应Ⅱ为主,反应Ⅱ前后气体分子数相等,压
1 2 3强改变对平衡没有影响(2分)
【解析】(1)由热化学方程式可知,反应Ⅱ+反应Ⅲ可以得到反应Ⅰ,根据盖斯定律,∆H=∆H+∆H ;
1 2 3
由图1可知,反应ⅱ的活化能较大,活化能大的反应较慢,慢反应决定反应速率,因此反应ⅱ决定了反应
Ⅰ正反应速率的快慢;(2)根据图2可知,平衡时n(H O)=1.5mol,n(H )=0.5mol,列出三段式:
2 2
设体积为V,平衡常数K= = =9,此时v =v ,k c(CO)c(H)=k c(CO)c(H O),
正 逆 正 2 2 逆 2
故 = =K=9,M点时n(H O)= n(H ),设反应的CO 的物质的量为x,列出三段式:
2 2 2
2-x=x,解得 x=1mol,
;(3)① 取初始的1min为研究对象,1min内总气体量为60mL,CO 与H 体积比为1:4,CO 的体积为
2 2 2
60mL× =12mL,转化率为 80%,因此反应的 CO 的体积为 12mL×80%=9.6mL,反应速率为
2
=9.6mL/min;②A项,反应温度降低,反应速率减小,因此Ⅰ、Ⅱ、Ⅲ的反应速率都减小,A正确;B项,
Ⅰ和Ⅲ反应物中气体系数之和较大,增大体系压强,根据勒夏特列原理,Ⅰ和Ⅲ平衡正向移动,Ⅱ反应前
后气体系数之和相等,因此增大体系压强,Ⅱ平衡不移动,B正确;C项,选用合适的催化剂能提高甲烷
的选择性,更大程度地进行反应Ⅰ和Ⅲ,C正确;D项,其他条件不变时,增大CO 和H 的投料比,可提
2 2
高CO 的平衡转化率D项,其他条件不变时,增大CO 和H 的投料比,可提高H 的平衡转化率,D错误;
2 2 2 2
E.及时分离出水蒸气,可使反应正向移动,提高产率,循环使用 CO 和H ,可提高原料的利用率,E正
2 2
确;故选D;③对反应Ⅰ和Ⅲ,压强增大,平衡正向移动,CO 平衡转化率增大,即p>p>p;当图乙中
2 1 2 3
温度到了T℃时,主要进行反应Ⅱ,此时反应前后系数和不变,压强的变化不会引起平衡的移动,故三条
曲线几乎交于一点。
19.(14分)I.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一
种重要的化工原料。(1) 工业上可利用甲烷水蒸气重整制备氢气,体系中发生反应:
ⅰ. CH(g)+HO(g) CO(g)+3H(g) ∆H=+206.2kJ∙mol-1
4 2 2 1
ⅱ. CO(g)+H O(g) CO(g)+H(g) ∆H
2 2 2 2
(1)① 在_______(填“高温”、“低温”或“任意温度”)条件下有利于反应ⅰ自发进行。
②已知:25℃、101kPa时,部分化学键的键能数据如下表:
化学键 C≡O (CO) C=O H-O H-H
键能/( kJ∙mol-1) 1072 803 464 436
请根据提供的键能数据,计算 H=_______ kJ∙mol-1。
2
II.氮的固定一直是科学家研究的∆ 重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N
2
(g)
+3H (g) 2NH (g)。
2 3
(2)在不同温度、压强和相同催化剂条件下,初始N、H 分别为0.1mol、0.3mol时,平衡后混合物中
2 2
氮的体积分数(φ)如图所示。
①其中,p、p 和p 由大到小的顺序是____,其原因是____。
1 2 3
②若分别用V(N )和V (N )表示从反应开始至达平衡状态A、B时的化学反应速率,则
A 2 B 2
V(N )____V (N )(填“>”“<”或“=”)。
A 2 B 2
③若在250℃、p 为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N 的分压p(N )
1 2 2
为_____Pa(分压=总压×物质的量分效,保留一位小数)。
III.以连二硫酸根(S O2-)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
2 4(3)① 阴极区的电极反应式为____。
②NO吸收转化后的主要产物为NH +,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的
4
NO在标况下的体积为____mL。
【答案】(1) 高温(1分) +247.1(2分)
(2) p >p>p (2分) 该反应为气体分子数减小的反应,温度相同时,增大压强化学平衡向正反应方向
1 2 3
移动,故平衡混合物中氨的体积分数越大压强越大(2分) <(1分) 8.3×103(2分)
(3) 2SO2-+4H++2e-=S O2-+2H O(2分) 1344(2分)
3 2 4 2
【解析】(1)(1)① 因为反应ⅰ为吸热反应,所以在高温条件下有利于反应ⅰ自发进行;②根据表中提
供的键能数据,计算∆H=(1072+2×464-2×803-436) kJ∙mol-1=-42kJ∙mol-1。(2)① 由N+3H 2NH 可知,
2 2 2 3
反应为气体分子数减小的反应,增大压强,平衡正向移动,由图象可知在相同温度下,平衡后混合物中氨
的体积分数(φ)为φ>φ>φ,因此压强关系是p>p>p;②温度越大,压强越大,反应速率越大,p>
1 2 3 1 2 3 1
p,由图可知,B对应的温度、压强大,则反应速率大; ③由三段式可知:
2
,x=0.08mol,则B点N 的分压p(N )为 ×105Pa=8.3×103 Pa;
2 2
(3)① 由图可知,阴极区通入液体主要含SO 2-,流出主要含SO2-,所以阴极区发生还原反应生成SO2-,
3 2 4 2 4
电极反应式为2SO 2-+4H++2e-=S O2-+2H O;②由于NO吸收转化后的主要产物为NH +,根据电子转移可知,
3 2 4 2 4
NO~NH +~5e-,若电路中转移转移0.3mol e-,需要消耗NO 0.06mol,标准状况下体积为0.06mol×22.4L/
4
mol =1344mL。