文档内容
主题三 化学反应原理测试(二)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1.下列说法不正确的是( )
A.铅蓄电池在放电过程中,正极得到电子,电极质量增加
B.0.1mol/L CH COOH溶液加水稀释后,溶液中 减小
3
C.SiO(s)+2C(s)=Si(s)+2CO(g)必须在高温下反应才能发生,则ΔH>0
2
D.合成氨生产中将NH 液化分离,可加快正反应速率,提高H 的转化率
3 2
2.下列依据热化学方程式得出的结论正确的是( )
A.己知:正丁烷(g)=异丁烷(g) H<0,则正丁烷比异丁烷稳定
B.己知:C H(g)+3O(g)=2CO (g)△+2HO(g) H=-1478.8k·mol-1,则C H 的燃烧热△H=-1478.8kJ·mol-1
2 4 2 2 2 2 4
C. 己知:H+(aq)+OH-(aq)==H O(1) H=-5△7.3kJ· mol-1,但稀Ba(OH) (aq)和稀HSO (aq)完全反应
2 2 2 4
△
的
生成1molH O(1)时,放出 热量大于57.3kJ
2
D.已知:S(g)+O(g)==SO (g) H;S(s)+O (g)==SO (g) H,则△H> H
2 2 1 2 2 2 1 2
3.化学平衡常数(K)、电离常数 △(K a 、K b )、水的离子积常数 △(K W )、溶度积 △ 常数(K sp )等常数是表示判断物
质性质的重要常数,下列关于这些常数的说法中,正确的是( )
A.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
B.K(HCN)<K(CHCOOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
a a 3
C.当温度升高时,弱酸、弱碱的电离常数(K、K )和水的离子积常数(K )均变大
a b W
D.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生 BaSO 沉淀,则K (BaSO)>
4 sp 4
K (BaCO)
sp 3
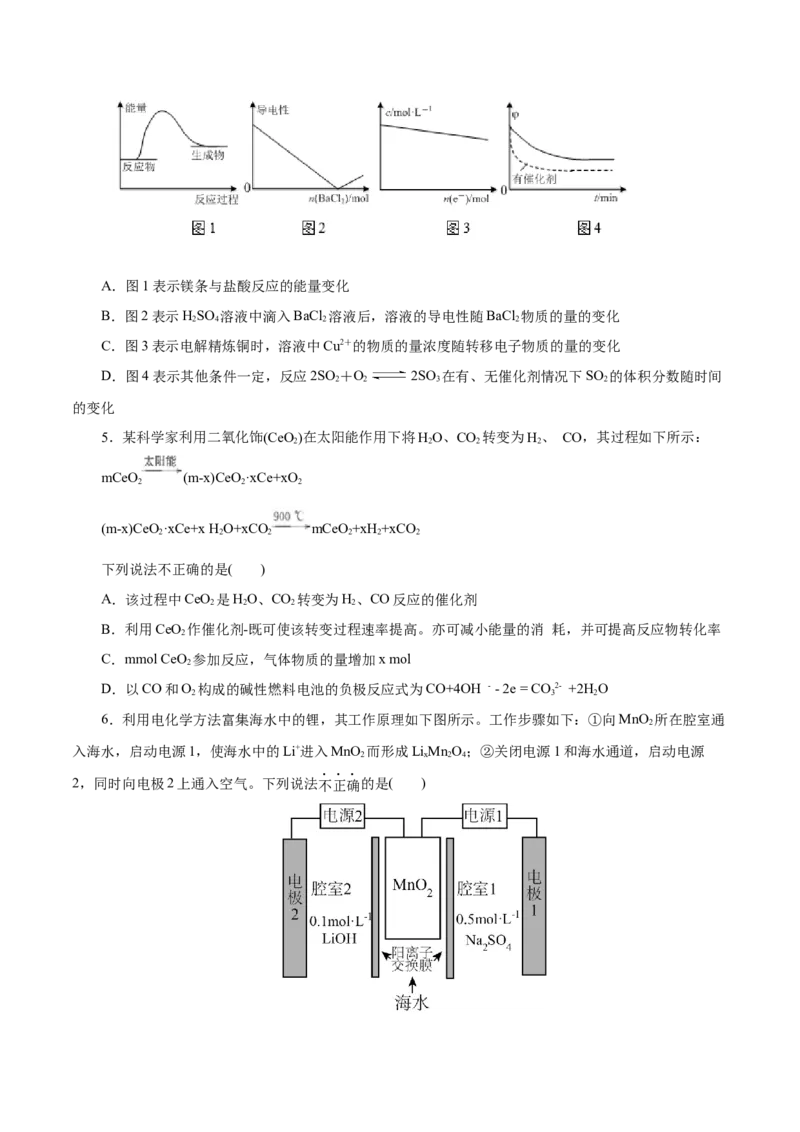
4.下列图示与对应的叙述相符的是( )A.图1表示镁条与盐酸反应的能量变化
B.图2表示HSO 溶液中滴入BaCl 溶液后,溶液的导电性随BaCl 物质的量的变化
2 4 2 2
C.图3表示电解精炼铜时,溶液中Cu2+的物质的量浓度随转移电子物质的量的变化
D.图4表示其他条件一定,反应2SO +O 2SO 在有、无催化剂情况下SO 的体积分数随时间
2 2 3 2
的变化
5.某科学家利用二氧化饰(CeO)在太阳能作用下将HO、CO 转变为H、 CO,其过程如下所示:
2 2 2 2
mCeO (m-x)CeO ·xCe+xO
2 2 2
(m-x)CeO ·xCe+x HO+xCO mCeO +xH +xCO
2 2 2 2 2 2
下列说法不正确的是( )
A.该过程中CeO 是HO、CO 转变为H、CO反应的催化剂
2 2 2 2
B.利用CeO 作催化剂-既可使该转变过程速率提高。亦可减小能量的消 耗,并可提高反应物转化率
2
C.mmol CeO 参加反应,气体物质的量增加x mol
2
D.以CO和O 构成的碱性燃料电池的负极反应式为CO+4OH - - 2e = CO 2- +2H O
2 3 2
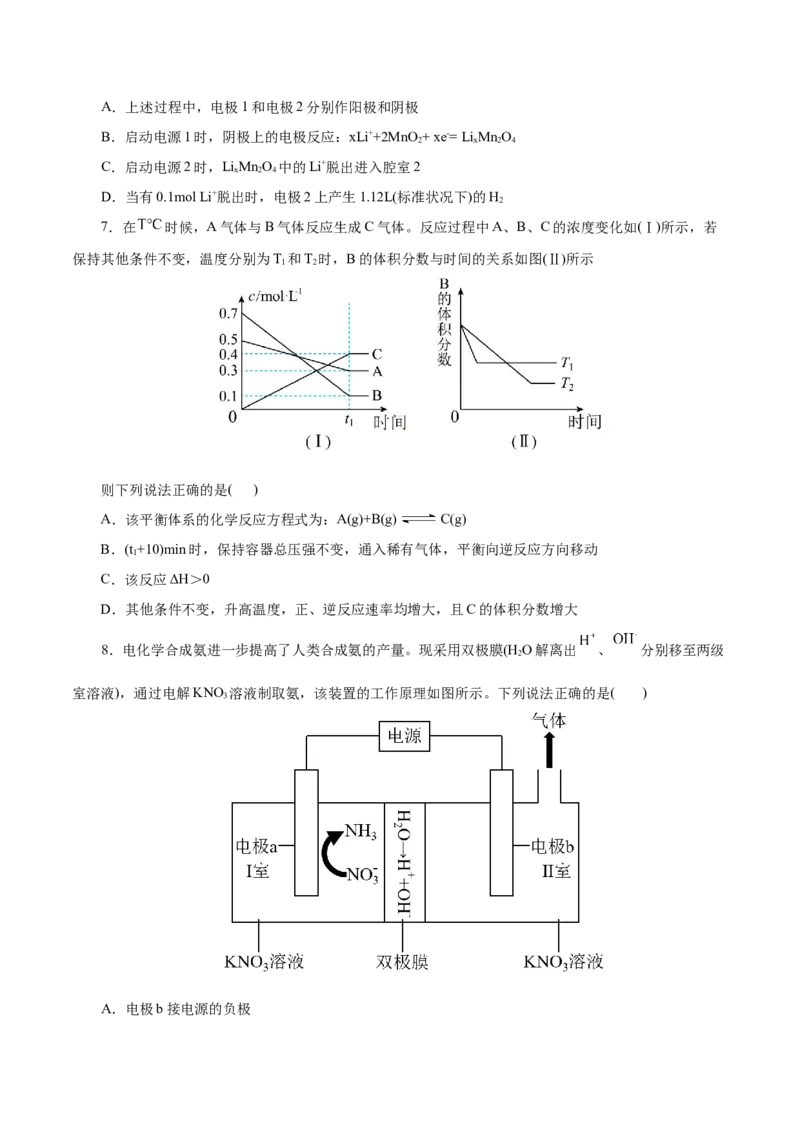
6.利用电化学方法富集海水中的锂,其工作原理如下图所示。工作步骤如下:①向MnO 所在腔室通
2
入海水,启动电源1,使海水中的Li+进入MnO 而形成LiMnO;②关闭电源1和海水通道,启动电源
2 x 2 4
2,同时向电极2上通入空气。下列说法不正确的是( )A.上述过程中,电极1和电极2分别作阳极和阴极
B.启动电源1时,阴极上的电极反应:xLi++2MnO+ xe-=LiMnO
2 x 2 4
C.启动电源2时,LiMnO 中的Li+脱出进入腔室2
x 2 4
D.当有0.1mol Li+脱出时,电极2上产生1.12L(标准状况下)的H
2
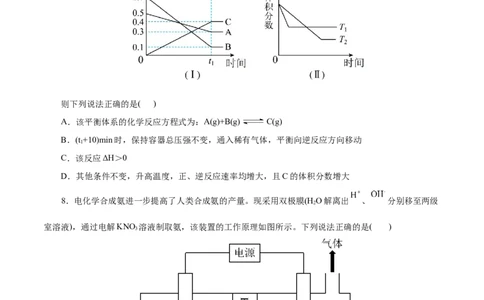
7.在 时候,A气体与B气体反应生成C气体。反应过程中A、B、C的浓度变化如(Ⅰ)所示,若
保持其他条件不变,温度分别为T 和T 时,B的体积分数与时间的关系如图(Ⅱ)所示
1 2
则下列说法正确的是( )
A.该平衡体系的化学反应方程式为:A(g)+B(g) C(g)
B.(t +10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
1
C.该反应ΔH>0
D.其他条件不变,升高温度,正、逆反应速率均增大,且C的体积分数增大
8.电化学合成氨进一步提高了人类合成氨的产量。现采用双极膜(H O解离出 、 分别移至两级
2
室溶液),通过电解KNO 溶液制取氨,该装置的工作原理如图所示。下列说法正确的是( )
3
A.电极b接电源的负极B.电解一段时间后I室的pH值增大
C.双极膜中HO解离出的H+向电极b极移动
2
D.理论上电极a与电极b上产生的气体的物质的量之比为2:1
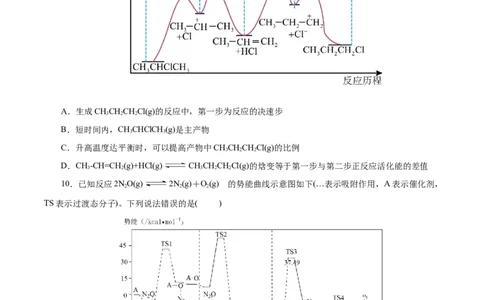
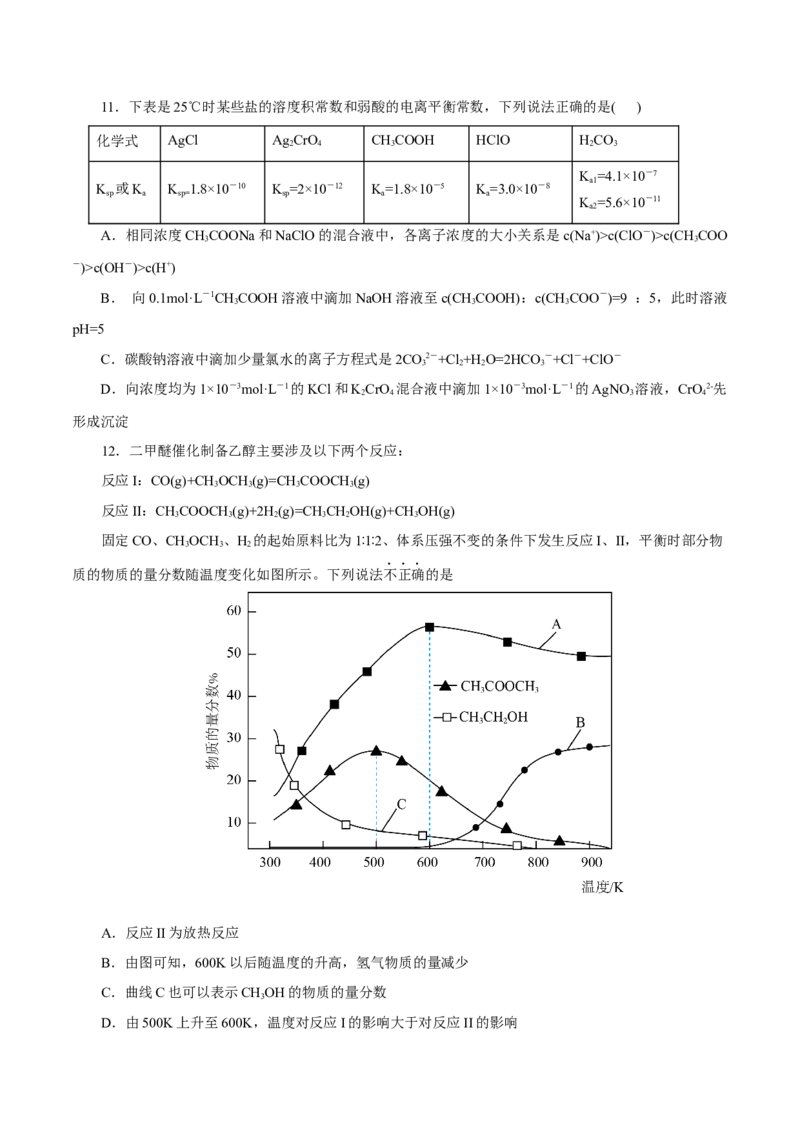
9.一定温度圧强下,CH-CH=CH(g)与HCl(g)反应可以生成CHCHClCH (g)和CHCHCHCl(g),反
3 2 3 3 3 2 2
应中的能量变化如图所示。下列说法不正确的是( )
A.生成CHCHCHCl(g)的反应中,第一步为反应的决速步
3 2 2
B.短时间内,CHCHClCH (g)是主产物
3 3
C.升高温度达平衡时,可以提高产物中CHCHCHCl(g)的比例
3 2 2
D.CH-CH=CH(g)+HCl(g) CHCHCHCl(g)的焓变等于第一步与第二步正反应活化能的差值
3 2 3 2 2
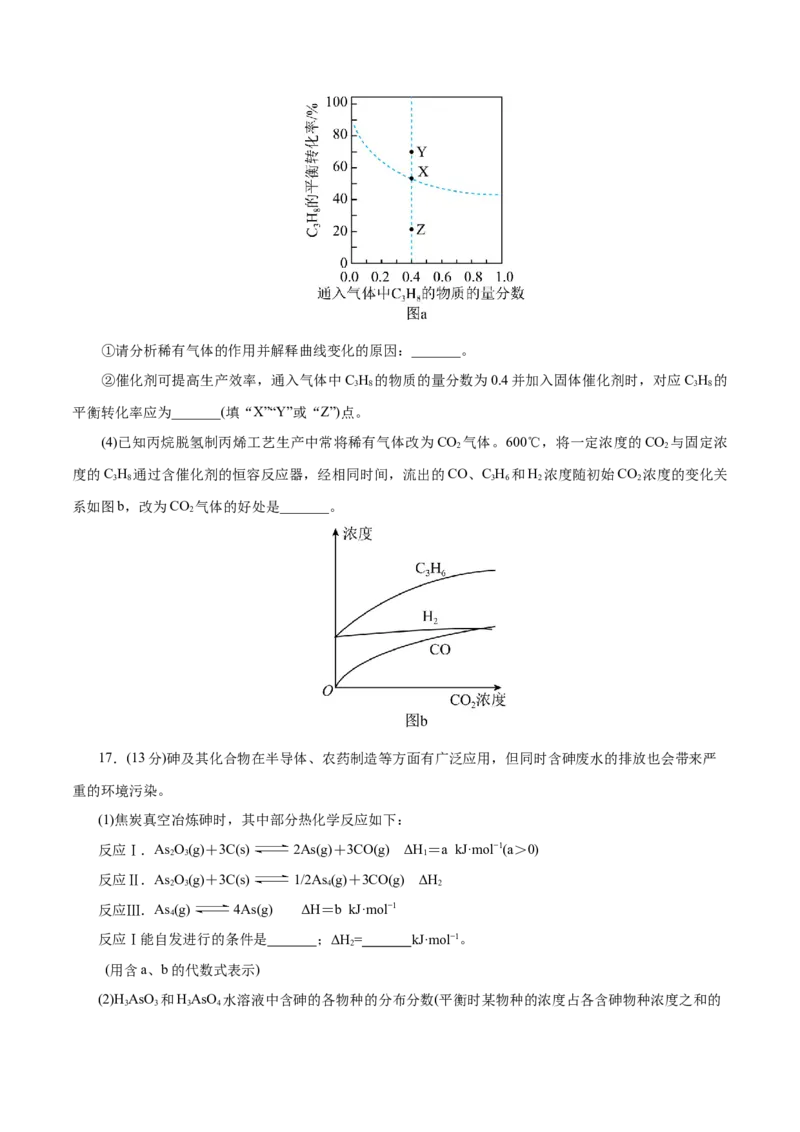
10.已知反应2NO(g) 2N(g)+O(g) 的势能曲线示意图如下(…表示吸附作用,A表示催化剂,
2 2 2
TS表示过渡态分子)。下列说法错误的是( )
A.该反应中只有两种物质能够吸附NO分子
2
B.过程I、Ⅱ、Ⅲ中都有N 生成
2
C.中间体A-O 可释放O,也可吸附NO分子
2 2 2
D.过程Ⅲ中最大能垒为82.17kcal·mol-111.下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是( )
化学式 AgCl Ag CrO CHCOOH HClO HCO
2 4 3 2 3
K =4.1×10-7
a1
K 或K K 1.8×10-10 K =2×10-12 K=1.8×10-5 K=3.0×10-8
sp a sp= sp a a
K =5.6×10-11
a2
A.相同浓度CHCOONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH COO
3 3
-)>c(OH-)>c(H+)
B. 向0.1mol·L-1CHCOOH溶液中滴加NaOH溶液至c(CHCOOH):c(CHCOO-)=9 :5,此时溶液
3 3 3
pH=5
C.碳酸钠溶液中滴加少量氯水的离子方程式是2CO2-+Cl+H O=2HCO -+Cl-+ClO-
3 2 2 3
D.向浓度均为1×10-3mol·L-1的KCl和KCrO 混合液中滴加1×10-3mol·L-1的AgNO 溶液,CrO2-先
2 4 3 4
形成沉淀
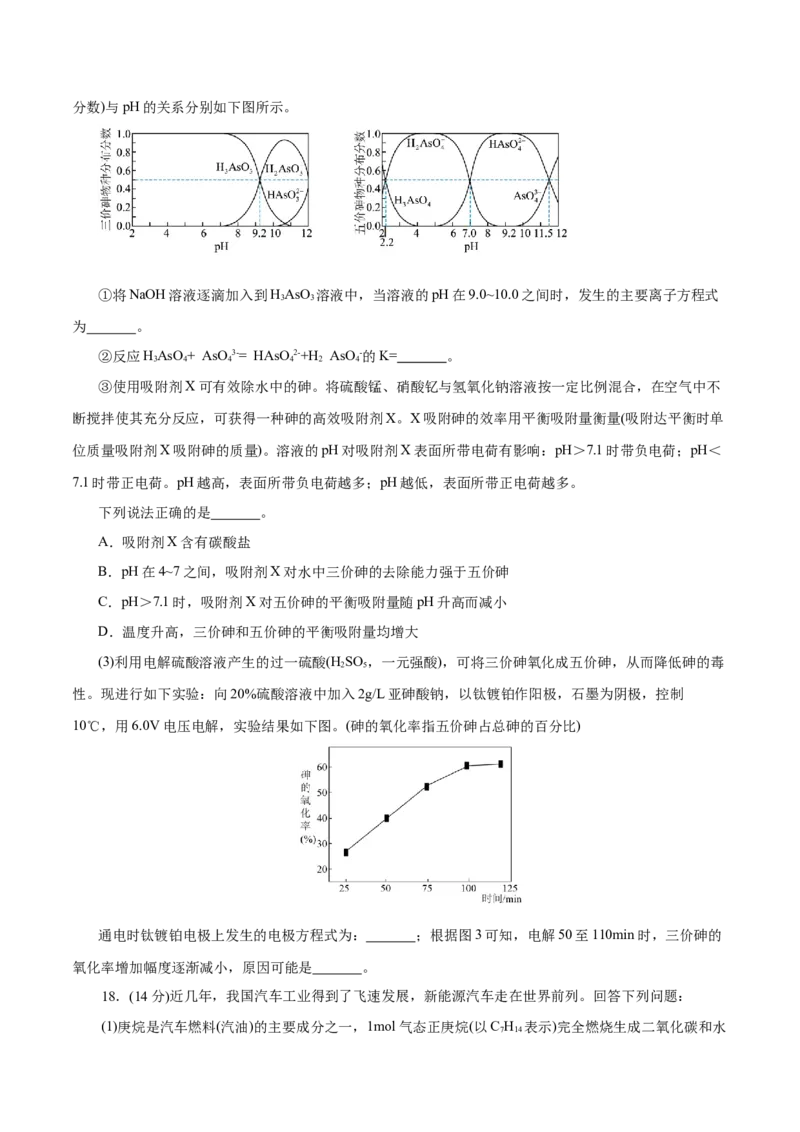
12.二甲醚催化制备乙醇主要涉及以下两个反应:
反应I:CO(g)+CHOCH (g)=CH COOCH (g)
3 3 3 3
反应II:CHCOOCH (g)+2H(g)=CH CHOH(g)+CH OH(g)
3 3 2 3 2 3
固定CO、CHOCH 、H 的起始原料比为1∶1∶2、体系压强不变的条件下发生反应I、II,平衡时部分物
3 3 2
质的物质的量分数随温度变化如图所示。下列说法不正确的是
A.反应II为放热反应
B.由图可知,600K以后随温度的升高,氢气物质的量减少
C.曲线C也可以表示CHOH的物质的量分数
3
D.由500K上升至600K,温度对反应I的影响大于对反应II的影响13.某小组做如下两组实验:
实验Ⅰ:往10mL0.1mol/L氨水中滴加0.1mol/L的草酸溶液。
实验Ⅱ:往10mL0.1mo/L氨水中滴加0.1mol/L的氢氟酸。
已知:溶液混合后体积变化忽略不计。溶液中某离子的浓度小于1.0×10-5mol·L-1时,可认为该离子已
沉淀完全。25℃时,相关常数如下表。
NH ·H O HF HC O CaF CaC O
3 2 2 2 4 2 2 4
电
离
1.8×10-5 6.3×10-4 K =5.6×10-2,K =1.5×10-4 溶度积K 4.0×10-11 2.5×10-9
a1 a2 sp
常
数
下列说法正确的是( )
A.实验Ⅰ,滴加过程中始终满足cC O2-+cHC O-+cHC O=0.1mol·L-1
2 4 2 4 2 2 4
B.实验Ⅱ中 时,因NH +和F-水解相互促进,导致所得溶液中含氟微粒的主要形式
4
为HF分子
C.相同温度下,CaC O 在NH Cl溶液中的溶解度比水中要小
2 4 4
D.用Ca(NO ) 溶液,无法将混合液中相同浓度的C O2-和F-先后沉淀而分离
3 2 2 4
14.室温下,通过下列实验探究0.0100mol·L-1NaC O 溶液的性质。
2 2 4
实验1:实验测得0.0100mol·L-1NaC O 溶液pH为8.6。
2 2 4
实验2:向溶液中滴加等体积0.0100mol·L-1HCl溶液,pH由8.6降为4.8。
实验3:向溶液中加入等体积0.0200mol·L-1CaCl 溶液,出现白色沉淀。
2
实验4:向稀硫酸酸化的 溶液中滴加NaC O 溶液至溶液褪色。
2 2 4
已知室温时K (CaC O)= 2.5×10-9,下列说法正确的是( )
sp 2 4
A.0.0100mol·L-1NaC O 溶液中满足:
2 2 4
B.实验2滴加盐酸过程中不可能满足:cNa+=2c(C O2-)+c(HC O-)+ c(Cl-)
2 4 2 4
C.实验3所得上层清液中c(C O2-)=5.0×10-7mol·L-1
2 4
D.实验4发生反应离子方程式为:C O2-+4MnO-+12H+=2CO ↑+4Mn2++6H O
2 4 4 2 2
15.下列实验能达到预期目的的是( )
编号 实验内容 实验目的向含有酚酞的 NaCO 溶液中加入少量 BaC1 固
A 2 3 2 证明NaCO 溶液中存在水解平衡
体,溶液红色变浅 2 3
室温下,用 pH 试纸分别测定浓度为 18mol/L 和
B 比较不同浓度HSO 的酸性强弱
0.1 mol/L H SO 溶液的pH 2 4
2 4
配制 FeCl 溶液时,先将 FeCl 溶于适量浓盐酸
2 2
C 中,再用蒸馏水稀释到所需浓度,最后在试剂瓶 抑制Fe2+水解,并防止Fe2+被氧化
中加入少量铜粉
向 10mL 0.2 mol/L NaOH 溶液中滴入 2 滴 0.1
证明在相同温度下的
D mol/L MgCl 溶液,产生白色沉淀后,再滴加2滴
2
Ksp[Mg(OH) ]>Ksp[Fe(OH) ]
0.1 mol/L FeCl 溶液,又生成红褐色沉淀 2 3
3
第II卷(非选择题 共55分)
二、填空题(本题共4小题,共55分)
16.(14分)丙烯是重要的有机化工原料,工业上丙烷脱氢可制丙烯:C H(g) C H(g)+H(g)。回
3 8 3 6 2
答下列问题:
(1)已知部分共价键键能见下表:
共价键 H-H C-C C=C C-H
键能(kJ•mol-1) 436 347 614 413
请写出丙烷脱氢制丙烯的热化学方程式_______,该反应自发进行的条件是_______(填“高温”“低
温”或“任意温度”)。
(2)T K时,总压恒定为0.1MPa,起始时向恒温密闭容器中充入0.75 mol C H(g)发生反应。
1 3 8
①下列情况能说明上述反应达到平衡状态的是_______(填字母)。
A.n(C H)= n(H ) B.体系温度不变 C.体系压强不变 D.气体密度不变
3 8 2
②达到平衡时,混合气体中 C H 的物质的量分数为 50%,则对应温度下该反应的压强平衡常数
3 8
K =_______MPa(用平衡分压代替平衡浓度计算,某气体分压=总压×某气体物质的量分数)。
P
(3)温度为T 时,总压恒定为100kPa,在密闭容器中充入C H 和稀有气体(稀有气体不参与反应)的混
1 3 8
合气体,C H 的平衡转化率与充入气体中C H 的物质的量分数的关系如图a虚线所示。
3 8 3 8①请分析稀有气体的作用并解释曲线变化的原因:_______。
②催化剂可提高生产效率,通入气体中C H 的物质的量分数为0.4并加入固体催化剂时,对应C H 的
3 8 3 8
平衡转化率应为_______(填“X”“Y”或“Z”)点。
(4)已知丙烷脱氢制丙烯工艺生产中常将稀有气体改为CO 气体。600℃,将一定浓度的CO 与固定浓
2 2
度的C H 通过含催化剂的恒容反应器,经相同时间,流出的CO、C H 和H 浓度随初始CO 浓度的变化关
3 8 3 6 2 2
系如图b,改为CO 气体的好处是_______。
2
17.(13分)砷及其化合物在半导体、农药制造等方面有广泛应用,但同时含砷废水的排放也会带来严
重的环境污染。
(1)焦炭真空冶炼砷时,其中部分热化学反应如下:
反应Ⅰ.As O(g)+3C(s) 2As(g)+3CO(g) ΔH =a kJ·mol−1(a>0)
2 3 1
反应Ⅱ.As O(g)+3C(s) 1/2As(g)+3CO(g) ΔH
2 3 4 2
反应Ⅲ.As (g) 4As(g) ΔH=b kJ·mol−1
4
反应Ⅰ能自发进行的条件是 ;ΔH= kJ·mol−1。
2
(用含a、b的代数式表示)
(2)H AsO 和HAsO 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各含砷物种浓度之和的
3 3 3 4分数)与pH的关系分别如下图所示。
①将NaOH溶液逐滴加入到HAsO 溶液中,当溶液的pH在9.0~10.0之间时,发生的主要离子方程式
3 3
为 。
②反应HAsO + AsO 3-= HAsO 2-+H AsO -的K= 。
3 4 4 4 2 4
③使用吸附剂X可有效除水中的砷。将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,在空气中不
断搅拌使其充分反应,可获得一种砷的高效吸附剂X。X吸附砷的效率用平衡吸附量衡量(吸附达平衡时单
位质量吸附剂X吸附砷的质量)。溶液的pH对吸附剂X表面所带电荷有影响:pH>7.1时带负电荷;pH<
7.1时带正电荷。pH越高,表面所带负电荷越多;pH越低,表面所带正电荷越多。
下列说法正确的是 。
A.吸附剂X含有碳酸盐
B.pH在4~7之间,吸附剂X对水中三价砷的去除能力强于五价砷
C.pH>7.1时,吸附剂X对五价砷的平衡吸附量随pH升高而减小
D.温度升高,三价砷和五价砷的平衡吸附量均增大
(3)利用电解硫酸溶液产生的过一硫酸(H SO ,一元强酸),可将三价砷氧化成五价砷,从而降低砷的毒
2 5
性。现进行如下实验:向20%硫酸溶液中加入2g/L亚砷酸钠,以钛镀铂作阳极,石墨为阴极,控制
10℃,用6.0V电压电解,实验结果如下图。(砷的氧化率指五价砷占总砷的百分比)
通电时钛镀铂电极上发生的电极方程式为: ;根据图3可知,电解50至110min时,三价砷的
氧化率增加幅度逐渐减小,原因可能是 。
18.(14分)近几年,我国汽车工业得到了飞速发展,新能源汽车走在世界前列。回答下列问题:
(1)庚烷是汽车燃料(汽油)的主要成分之一,1mol气态正庚烷(以C H 表示)完全燃烧生成二氧化碳和水
7 14蒸气放出4817kJ热量,该反应的热化学议程式为_______。
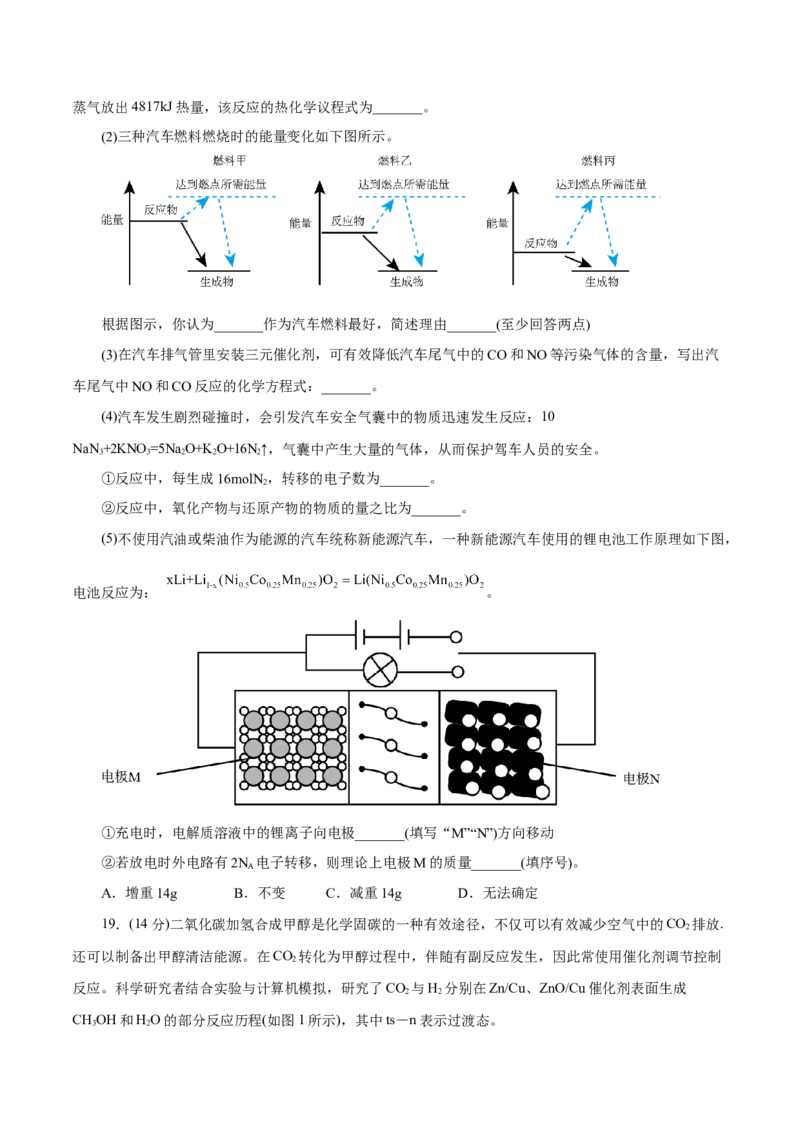
(2)三种汽车燃料燃烧时的能量变化如下图所示。
根据图示,你认为_______作为汽车燃料最好,简述理由_______(至少回答两点)
(3)在汽车排气管里安装三元催化剂,可有效降低汽车尾气中的CO和NO等污染气体的含量,写出汽
车尾气中NO和CO反应的化学方程式:_______。
(4)汽车发生剧烈碰撞时,会引发汽车安全气囊中的物质迅速发生反应:10
NaN+2KNO =5NaO+KO+16N↑,气囊中产生大量的气体,从而保护驾车人员的安全。
3 3 2 2 2
①反应中,每生成16molN ,转移的电子数为_______。
2
②反应中,氧化产物与还原产物的物质的量之比为_______。
(5)不使用汽油或柴油作为能源的汽车统称新能源汽车,一种新能源汽车使用的锂电池工作原理如下图,
电池反应为: 。
①充电时,电解质溶液中的锂离子向电极_______(填写“M”“N”)方向移动
②若放电时外电路有2N 电子转移,则理论上电极M的质量_______(填序号)。
A
A.增重14g B.不变 C.减重14g D.无法确定
19.(14分)二氧化碳加氢合成甲醇是化学固碳的一种有效途径,不仅可以有效减少空气中的CO 排放.
2
还可以制备出甲醇清洁能源。在CO 转化为甲醇过程中,伴随有副反应发生,因此常使用催化剂调节控制
2
反应。科学研究者结合实验与计算机模拟,研究了CO 与H 分别在Zn/Cu、ZnO/Cu催化剂表面生成
2 2
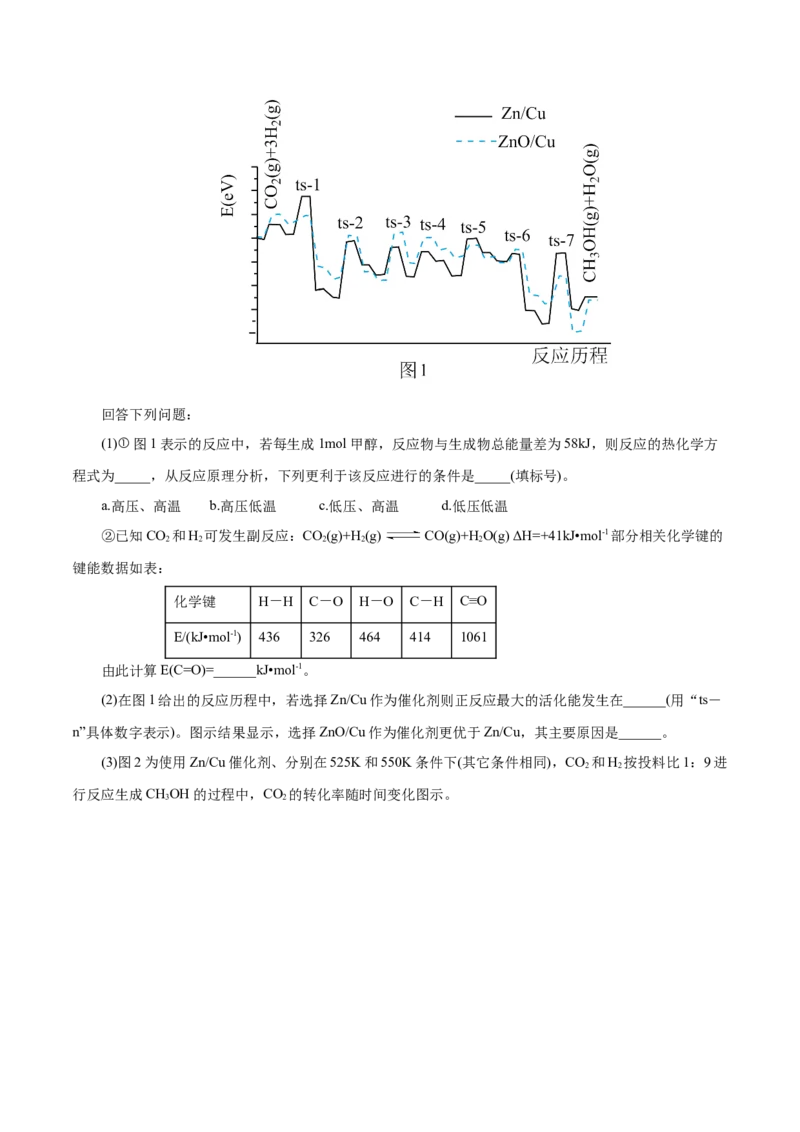
CHOH和HO的部分反应历程(如图1所示),其中ts-n表示过渡态。
3 2回答下列问题:
(1)①图1表示的反应中,若每生成1mol甲醇,反应物与生成物总能量差为58kJ,则反应的热化学方
程式为_____,从反应原理分析,下列更利于该反应进行的条件是_____(填标号)。
a.高压、高温 b.高压低温 c.低压、高温 d.低压低温
②已知CO 和H 可发生副反应:CO(g)+H(g) CO(g)+HO(g) ΔH=+41kJ•mol-1部分相关化学键的
2 2 2 2 2
键能数据如表:
化学键 H-H C-O H-O C-H C≡O
E/(kJ•mol-1) 436 326 464 414 1061
由此计算E(C=O)=______kJ•mol-1。
(2)在图1给出的反应历程中,若选择Zn/Cu作为催化剂则正反应最大的活化能发生在______(用“ts-
n”具体数字表示)。图示结果显示,选择ZnO/Cu作为催化剂更优于Zn/Cu,其主要原因是______。
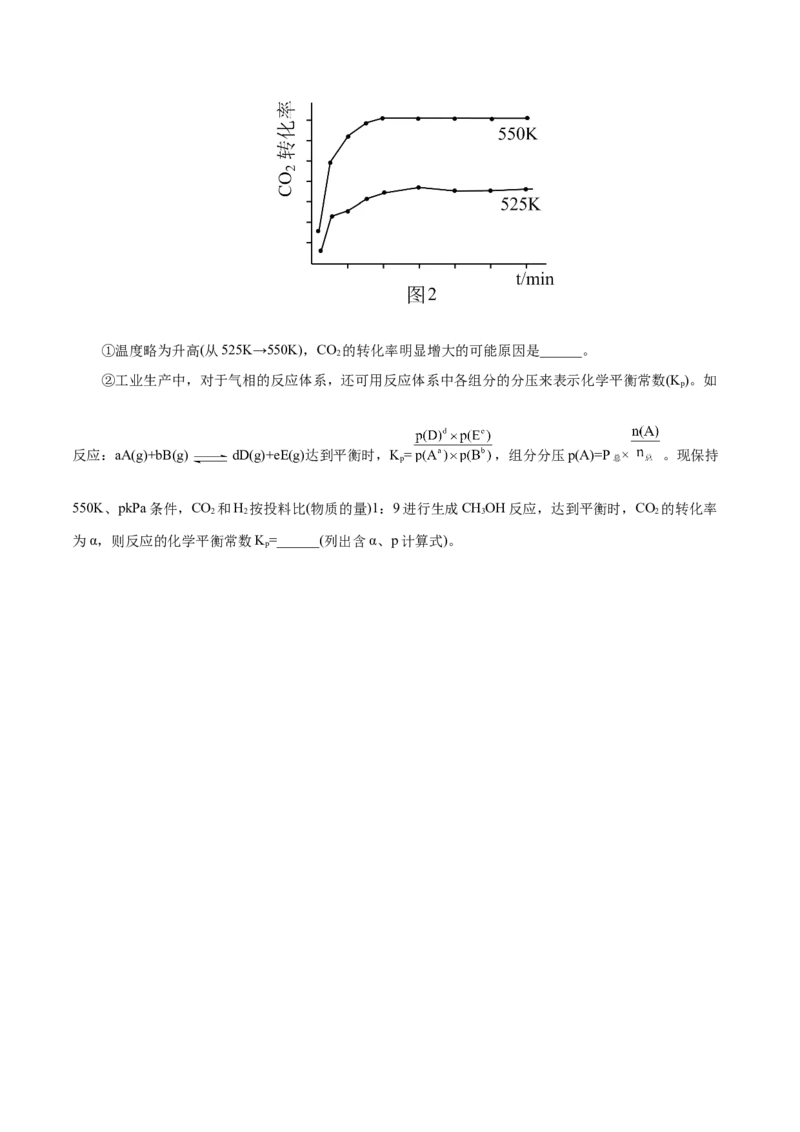
(3)图2为使用Zn/Cu催化剂、分别在525K和550K条件下(其它条件相同),CO 和H 按投料比1:9进
2 2
行反应生成CHOH的过程中,CO 的转化率随时间变化图示。
3 2①温度略为升高(从525K→550K),CO 的转化率明显增大的可能原因是______。
2
②工业生产中,对于气相的反应体系,还可用反应体系中各组分的分压来表示化学平衡常数(K )。如
p
反应:aA(g)+bB(g) dD(g)+eE(g)达到平衡时,K= ,组分分压p(A)=P × 。现保持
p 总
550K、pkPa条件,CO 和H 按投料比(物质的量)1:9进行生成CHOH反应,达到平衡时,CO 的转化率
2 2 3 2
为α,则反应的化学平衡常数K=______(列出含α、p计算式)。
p