文档内容
专题 13 速率常数、平衡常数的分析应用
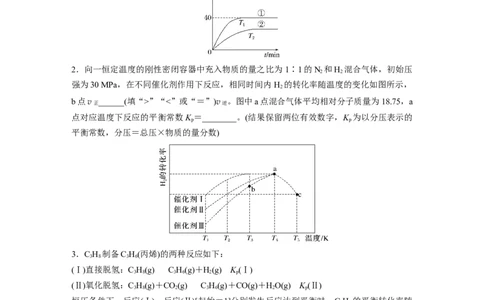
1.恒容密闭容器中,在 Ni 作催化剂条件下,NH 分解反应如下:2NH (g)N(g)+
3 3 2
3H
2
(g),不同温度下,NH
3
分解率随时间变化如图所示,v
正
=k
正
·c2(NH
3
),v
逆
=k
·c(N )·c3(H );NH 的初始浓度为c ,T 时NH 分解反应达到平衡时=____________;曲线
逆 2 2 3 1 1 3
①②中,k -k 值较小的曲线为__________。
正 逆
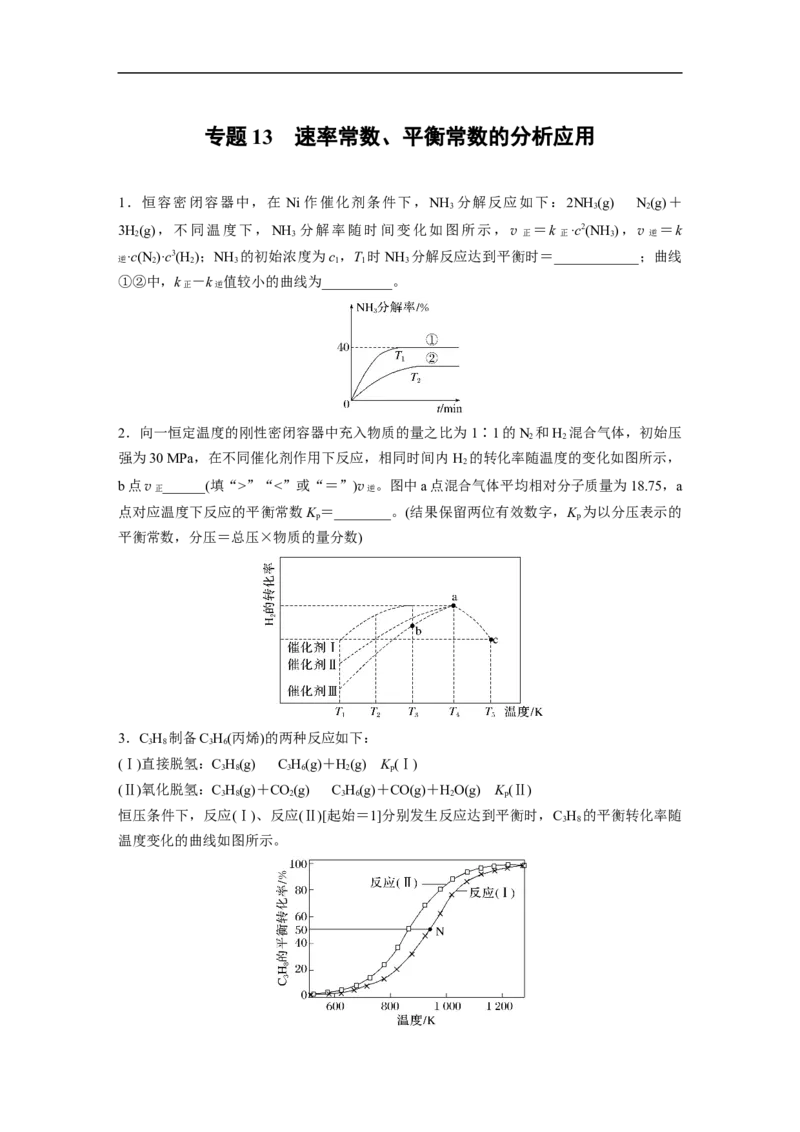
2.向一恒定温度的刚性密闭容器中充入物质的量之比为 1∶1的N 和H 混合气体,初始压
2 2
强为30 MPa,在不同催化剂作用下反应,相同时间内 H 的转化率随温度的变化如图所示,
2
b点v正 ______(填“>”“<”或“=”)v逆 。图中a点混合气体平均相对分子质量为18.75,a
点对应温度下反应的平衡常数K =________。(结果保留两位有效数字,K 为以分压表示的
p p
平衡常数,分压=总压×物质的量分数)
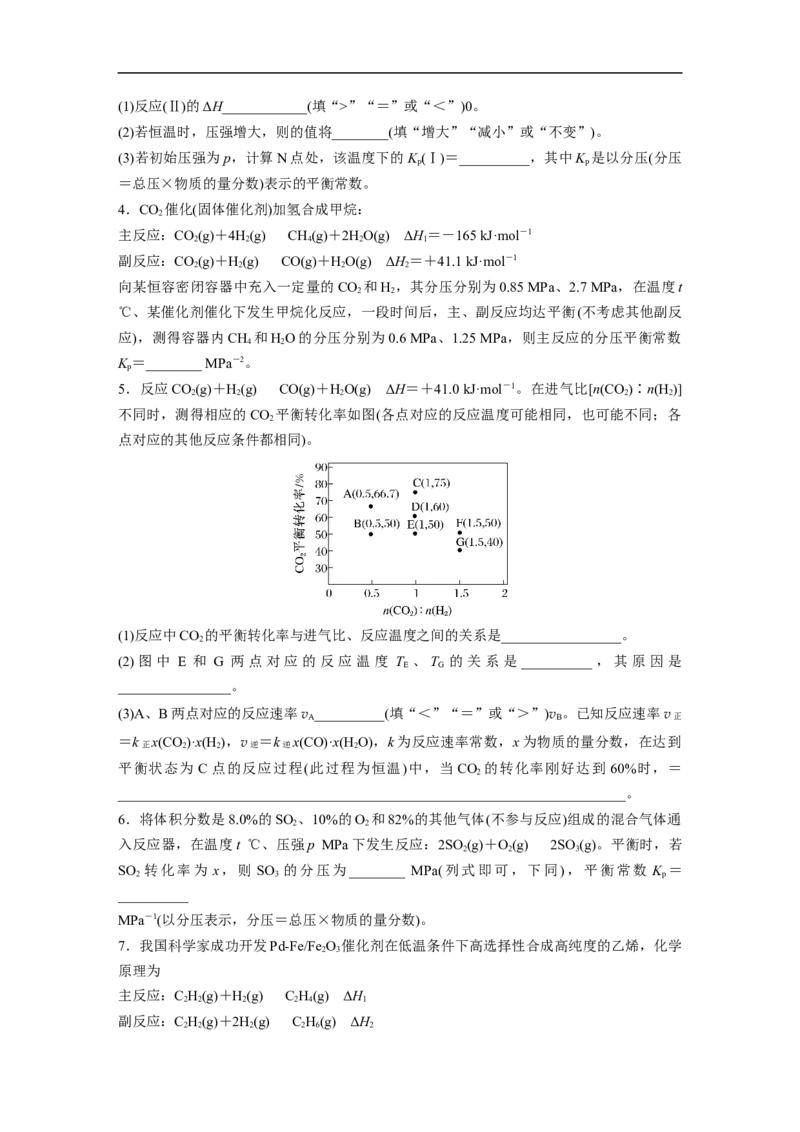
3.C H 制备C H(丙烯)的两种反应如下:
3 8 3 6
(Ⅰ)直接脱氢:C H(g)C H(g)+H(g) K (Ⅰ)
3 8 3 6 2 p
(Ⅱ)氧化脱氢:C H(g)+CO(g)C H(g)+CO(g)+HO(g) K (Ⅱ)
3 8 2 3 6 2 p
恒压条件下,反应(Ⅰ)、反应(Ⅱ)[起始=1]分别发生反应达到平衡时,C H 的平衡转化率随
3 8
温度变化的曲线如图所示。(1)反应(Ⅱ)的ΔH____________(填“>”“=”或“<”)0。
(2)若恒温时,压强增大,则的值将________(填“增大”“减小”或“不变”)。
(3)若初始压强为p,计算N点处,该温度下的K (Ⅰ)=__________,其中K 是以分压(分压
p p
=总压×物质的量分数)表示的平衡常数。
4.CO 催化(固体催化剂)加氢合成甲烷:
2
主反应:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-165 kJ·mol-1
2 2 4 2 1
副反应:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.1 kJ·mol-1
2 2 2 2
向某恒容密闭容器中充入一定量的CO 和H ,其分压分别为0.85 MPa、2.7 MPa,在温度t
2 2
℃、某催化剂催化下发生甲烷化反应,一段时间后,主、副反应均达平衡(不考虑其他副反
应),测得容器内CH 和HO的分压分别为0.6 MPa、1.25 MPa,则主反应的分压平衡常数
4 2
K =________ MPa-2。
p
5.反应CO(g)+H(g)CO(g)+HO(g) ΔH=+41.0 kJ·mol-1。在进气比[n(CO)∶n(H )]
2 2 2 2 2
不同时,测得相应的CO 平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各
2
点对应的其他反应条件都相同)。
(1)反应中CO 的平衡转化率与进气比、反应温度之间的关系是_________________。
2
(2)图中 E 和 G 两点对应的反应温度 T 、T 的关系是 __________,其原因是
E G
________________。
(3)A、B两点对应的反应速率v
A
__________(填“<”“=”或“>”)v
B
。已知反应速率v正
=k
正
x(CO
2
)·x(H
2
),v逆 =k
逆
x(CO)·x(H
2
O),k为反应速率常数,x为物质的量分数,在达到
平衡状态为 C 点的反应过程(此过程为恒温)中,当 CO 的转化率刚好达到 60%时,=
2
________________________________________________________________________。
6.将体积分数是8.0%的SO 、10%的O 和82%的其他气体(不参与反应)组成的混合气体通
2 2
入反应器,在温度t ℃、压强p MPa下发生反应:2SO (g)+O(g)2SO (g)。平衡时,若
2 2 3
SO 转化率为 x,则 SO 的分压为________ MPa(列式即可,下同),平衡常数 K =
2 3 p
__________
MPa-1(以分压表示,分压=总压×物质的量分数)。
7.我国科学家成功开发Pd-Fe/Fe O 催化剂在低温条件下高选择性合成高纯度的乙烯,化学
2 3
原理为
主反应:C H(g)+H(g)C H(g) ΔH
2 2 2 2 4 1
副反应:C H(g)+2H(g)C H(g) ΔH
2 2 2 2 6 2在密闭容器中充入1 mol C H 和2 mol H ,发生上述两个反应,测得C H 平衡转化率与温度、
2 2 2 2 2
压强的关系如图所示。在T K、20 kPa下C H 的选择性等于[C H 选择性=]。p_______(填
0 2 4 2 4 0
“>”“<”或“=”)20 kPa。T K下,主反应的平衡常数K =________ kPa-1(K 为用气
0 p p
体分压计算的平衡常数,气体分压等于气体总压×物质的量分数)。
8.反应CHOH(g)CO(g)+2H(g) ΔH=+90.7 kJ·mol-1,若在一定温度下、恒压容器中
3 2
进行,总压为p,CHOH的平衡转化率为α,平衡时,CO的分压为__________;该反应的
3
平衡常数K =__________________(用含p、α的代数式表示,K 为以分压代替浓度表示的平
p p
衡常数,分压=总压×物质的量分数)。