文档内容
专题 12 化学反应速率与化学平衡归因分析
1.研究碳及其化合物的资源化利用具有重要的意义。已知下列热化学方程式:
反应Ⅰ:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-164.9 kJ·mol-1
2 2 4 2 1
反应Ⅱ:CO(g)+H(g)CO(g)+HO(g)
2 2 2
ΔH=+41.2 kJ·mol-1
2
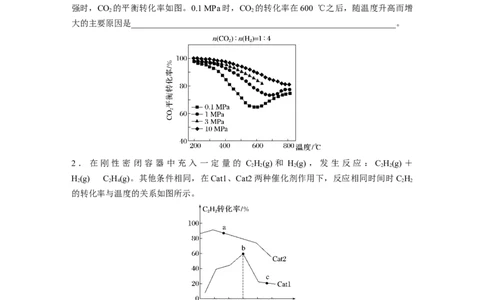
将n(CO)∶n(H )=1∶4的混合气体充入密闭容器中发生上述反应Ⅰ、Ⅱ,在不同温度和压
2 2
强时,CO 的平衡转化率如图。0.1 MPa时,CO 的转化率在600 ℃之后,随温度升高而增
2 2
大的主要原因是______________________________________________________________。
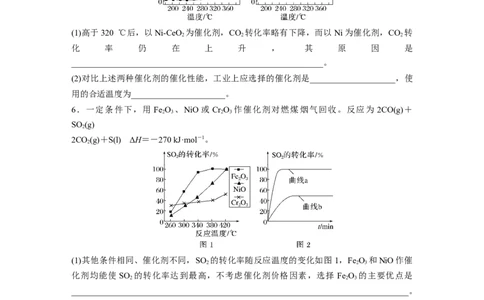
2 . 在 刚 性 密 闭 容 器 中 充 入 一 定 量 的 C H(g) 和 H(g) , 发 生 反 应 : C H(g) +
2 2 2 2 2
H(g)C H(g)。其他条件相同,在Cat1、Cat2两种催化剂作用下,反应相同时间时C H
2 2 4 2 2
的转化率与温度的关系如图所示。
(1)催化效率较高的是__________(填“Cat1”或“Cat2”);b点____________(填“达到”或
“未达到”)平衡。
(2)温度高于300 ℃,升高温度,b→c的原因可能是_______________________(答1条即可)。
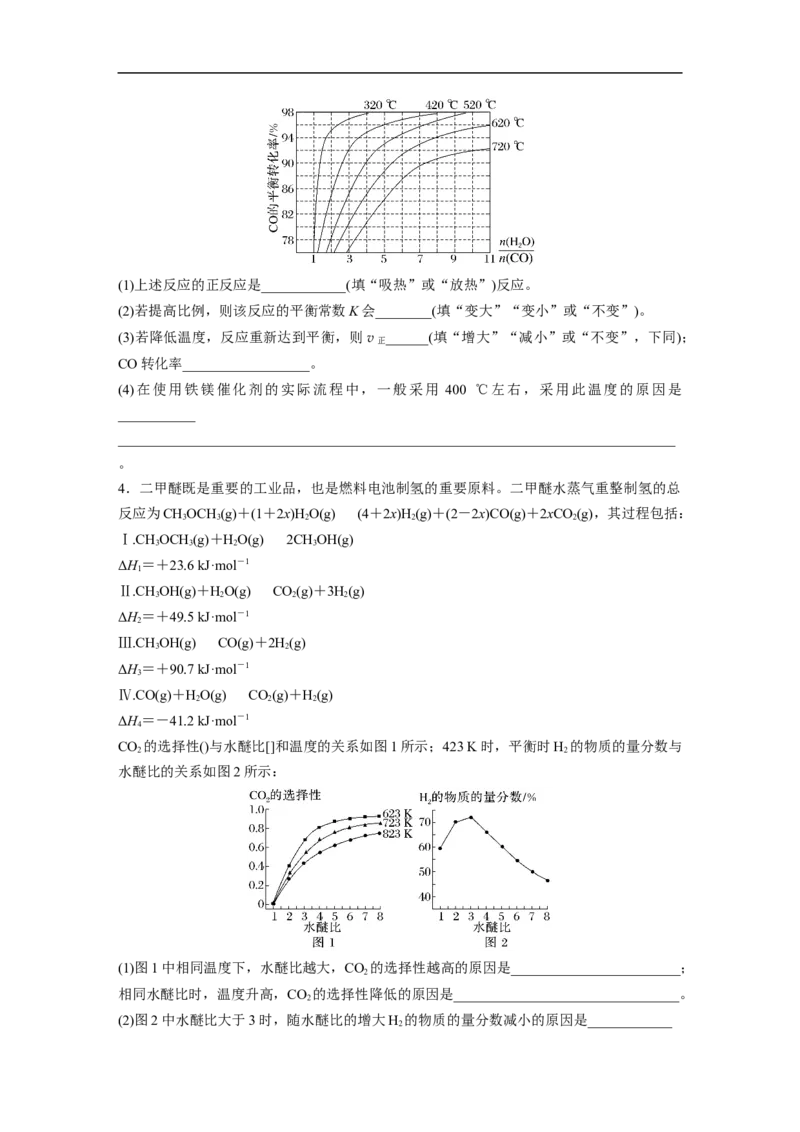
3.煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:
CO(g)+HO(g)H(g)+CO(g)中CO的平衡转化率随比例及温度变化关系如图所示:
2 2 2(1)上述反应的正反应是____________(填“吸热”或“放热”)反应。
(2)若提高比例,则该反应的平衡常数K会________(填“变大”“变小”或“不变”)。
(3)若降低温度,反应重新达到平衡,则 v正 ______(填“增大”“减小”或“不变”,下同);
CO转化率__________________。
(4)在使用铁镁催化剂的实际流程中,一般采用 400 ℃左右,采用此温度的原因是
___________
_______________________________________________________________________________
。
4.二甲醚既是重要的工业品,也是燃料电池制氢的重要原料。二甲醚水蒸气重整制氢的总
反应为CHOCH (g)+(1+2x)H O(g)(4+2x)H (g)+(2-2x)CO(g)+2xCO(g),其过程包括:
3 3 2 2 2
Ⅰ.CH OCH (g)+HO(g)2CHOH(g)
3 3 2 3
ΔH=+23.6 kJ·mol-1
1
Ⅱ.CH OH(g)+HO(g)CO(g)+3H(g)
3 2 2 2
ΔH=+49.5 kJ·mol-1
2
Ⅲ.CH OH(g)CO(g)+2H(g)
3 2
ΔH=+90.7 kJ·mol-1
3
Ⅳ.CO(g)+HO(g)CO(g)+H(g)
2 2 2
ΔH=-41.2 kJ·mol-1
4
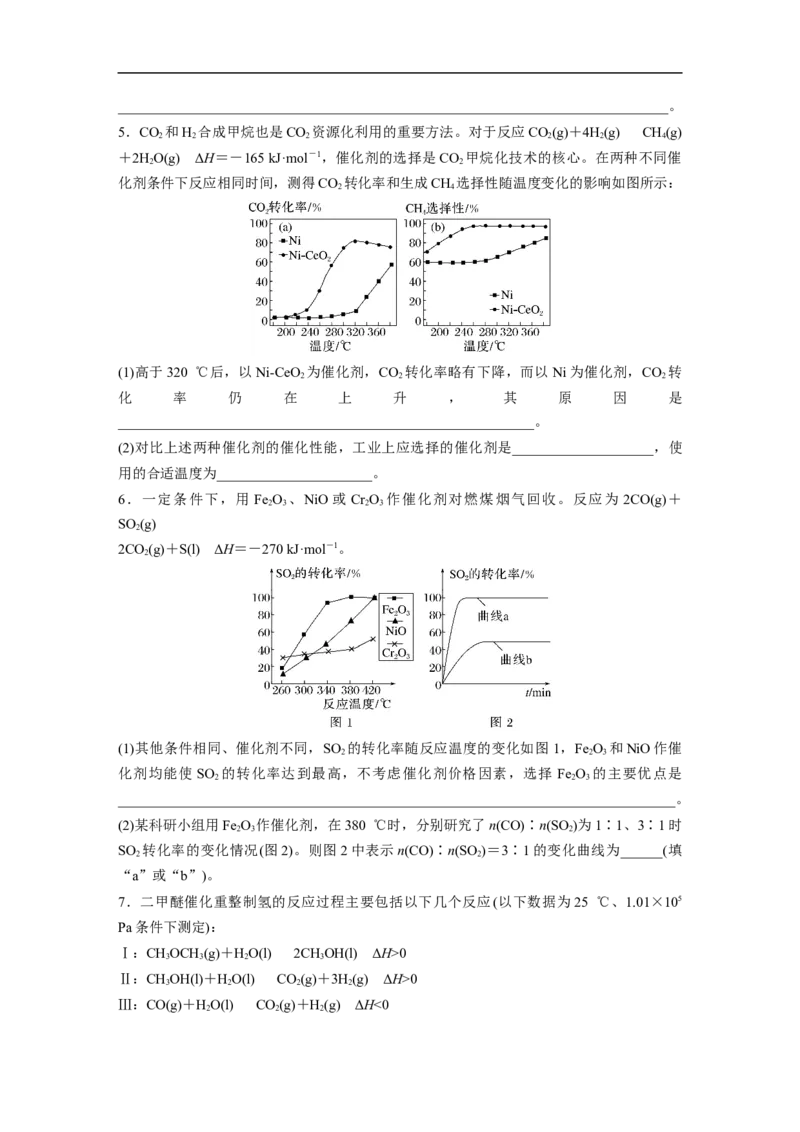
CO 的选择性()与水醚比[]和温度的关系如图1所示;423 K时,平衡时H 的物质的量分数与
2 2
水醚比的关系如图2所示:
(1)图1中相同温度下,水醚比越大,CO 的选择性越高的原因是________________________;
2
相同水醚比时,温度升高,CO 的选择性降低的原因是________________________________。
2
(2)图2中水醚比大于3时,随水醚比的增大H 的物质的量分数减小的原因是____________
2______________________________________________________________________________。
5.CO 和H 合成甲烷也是CO 资源化利用的重要方法。对于反应CO(g)+4H(g)CH(g)
2 2 2 2 2 4
+2HO(g) ΔH=-165 kJ·mol-1,催化剂的选择是CO 甲烷化技术的核心。在两种不同催
2 2
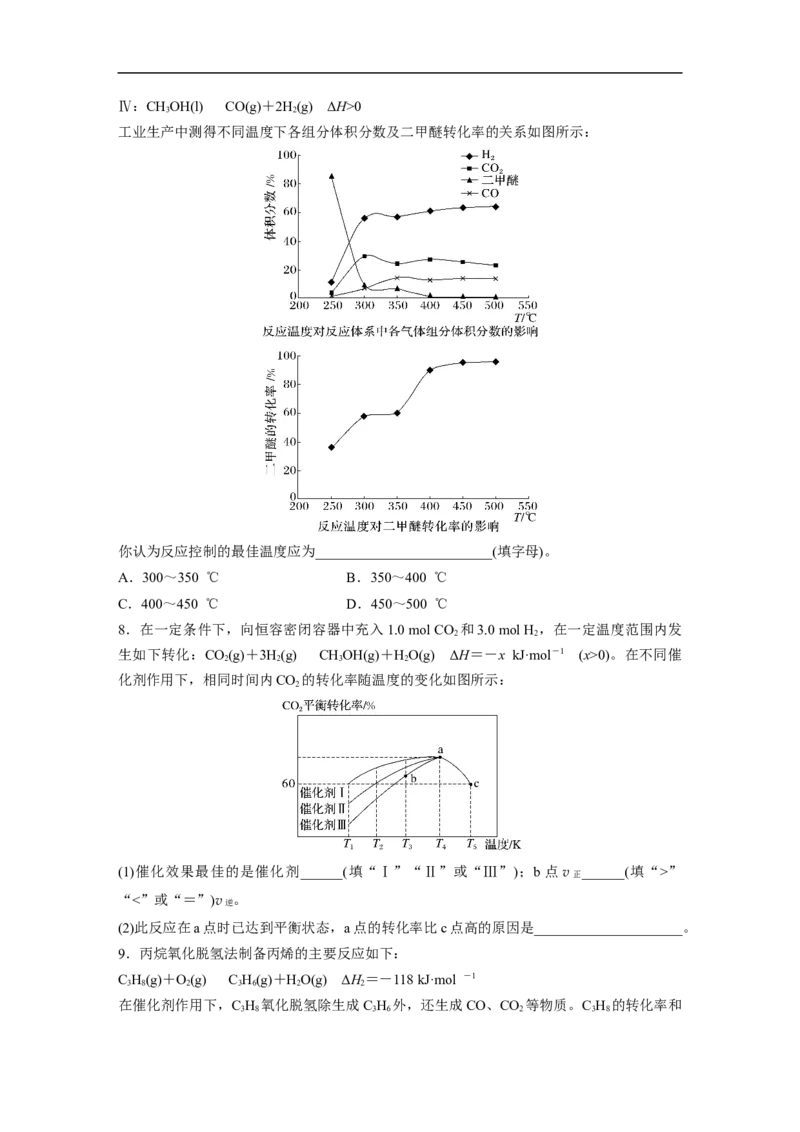
化剂条件下反应相同时间,测得CO 转化率和生成CH 选择性随温度变化的影响如图所示:
2 4
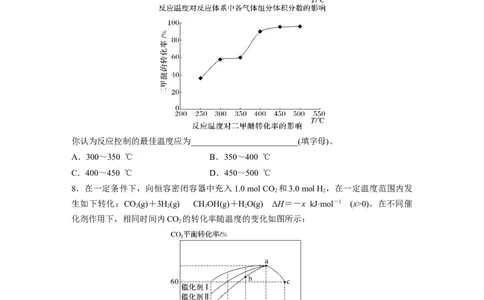
(1)高于320 ℃后,以Ni-CeO 为催化剂,CO 转化率略有下降,而以Ni为催化剂,CO 转
2 2 2
化 率 仍 在 上 升 , 其 原 因 是
___________________________________________________________。
(2)对比上述两种催化剂的催化性能,工业上应选择的催化剂是____________________,使
用的合适温度为______________________。
6.一定条件下,用 Fe O 、NiO 或 Cr O 作催化剂对燃煤烟气回收。反应为 2CO(g)+
2 3 2 3
SO (g)
2
2CO(g)+S(l) ΔH=-270 kJ·mol-1。
2
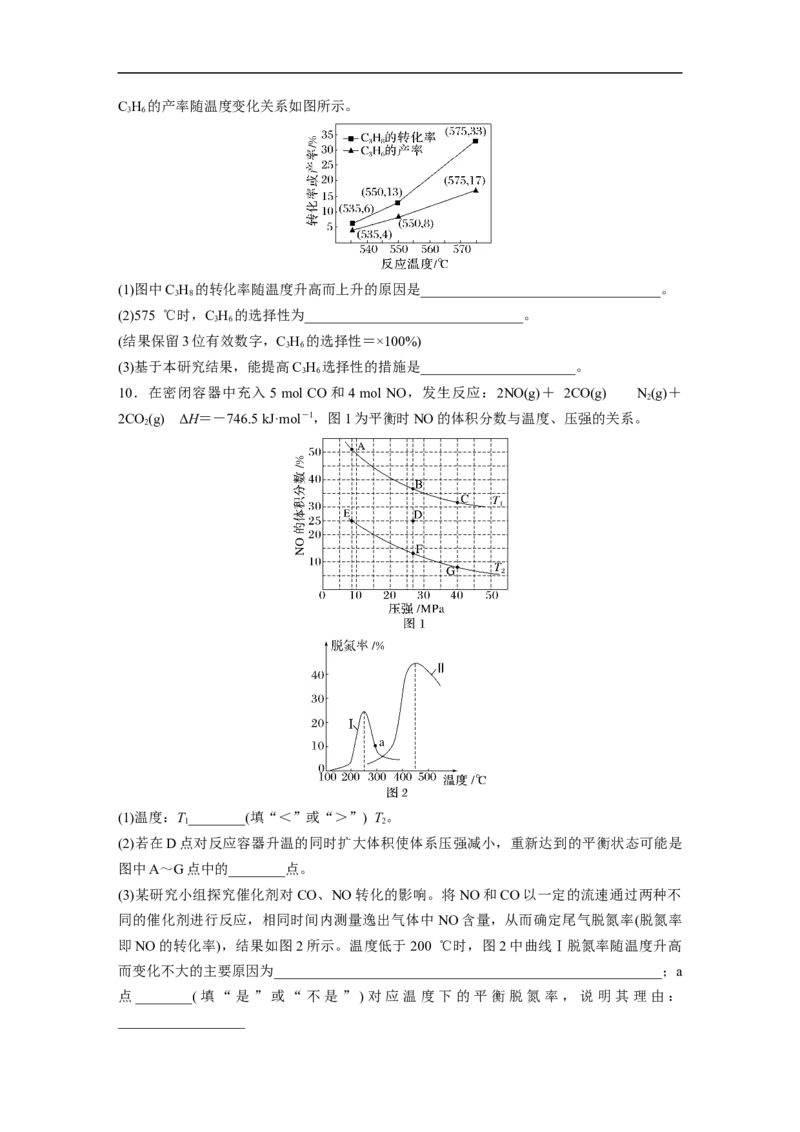
(1)其他条件相同、催化剂不同,SO 的转化率随反应温度的变化如图1,Fe O 和NiO作催
2 2 3
化剂均能使 SO 的转化率达到最高,不考虑催化剂价格因素,选择 Fe O 的主要优点是
2 2 3
_______________________________________________________________________________。
(2)某科研小组用Fe O 作催化剂,在380 ℃时,分别研究了n(CO)∶n(SO )为1∶1、3∶1时
2 3 2
SO 转化率的变化情况(图2)。则图2中表示n(CO)∶n(SO )=3∶1的变化曲线为______(填
2 2
“a”或“b”)。
7.二甲醚催化重整制氢的反应过程主要包括以下几个反应(以下数据为25 ℃、1.01×105
Pa条件下测定):
Ⅰ:CHOCH (g)+HO(l)2CHOH(l) ΔH>0
3 3 2 3
Ⅱ:CHOH(l)+HO(l)CO(g)+3H(g) ΔH>0
3 2 2 2
Ⅲ:CO(g)+HO(l)CO(g)+H(g) ΔH<0
2 2 2Ⅳ:CHOH(l)CO(g)+2H(g) ΔH>0
3 2
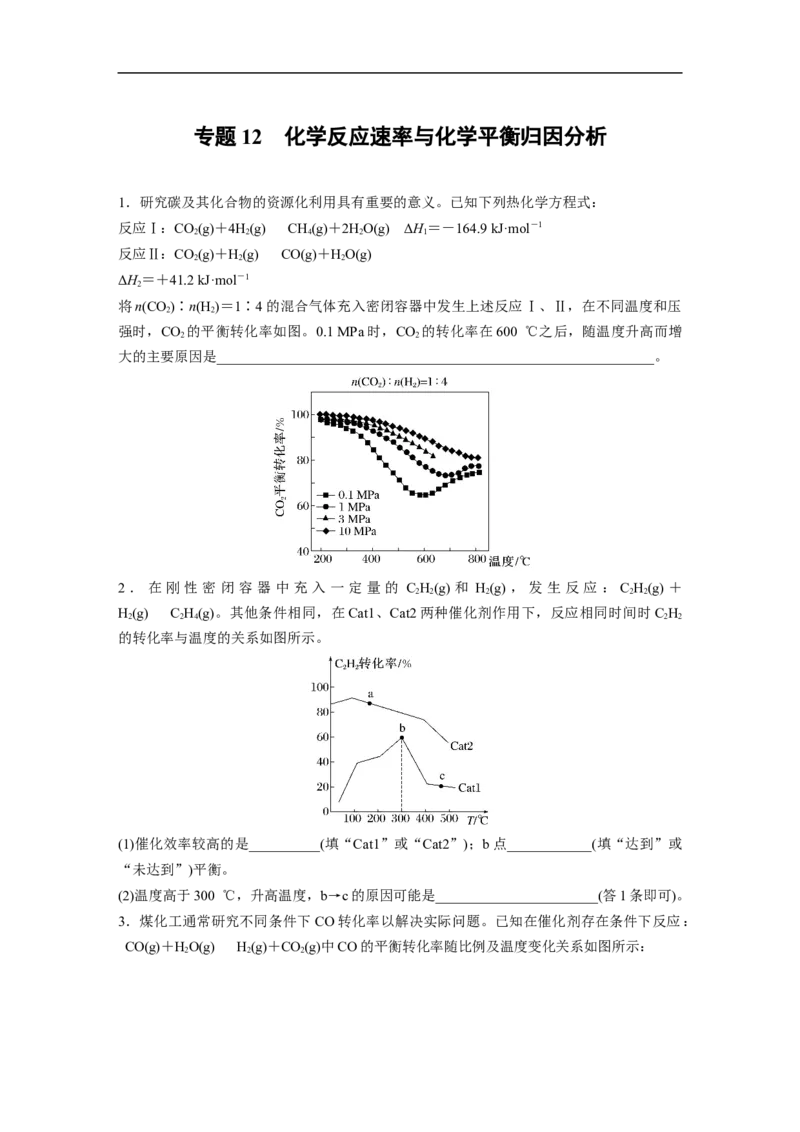
工业生产中测得不同温度下各组分体积分数及二甲醚转化率的关系如图所示:
你认为反应控制的最佳温度应为_________________________(填字母)。
A.300~350 ℃ B.350~400 ℃
C.400~450 ℃ D.450~500 ℃
8.在一定条件下,向恒容密闭容器中充入1.0 mol CO 和3.0 mol H ,在一定温度范围内发
2 2
生如下转化:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-x kJ·mol-1 (x>0)。在不同催
2 2 3 2
化剂作用下,相同时间内CO 的转化率随温度的变化如图所示:
2
(1)催化效果最佳的是催化剂______(填“Ⅰ”“Ⅱ”或“Ⅲ”);b点v正 ______(填“>”
“<”或“=”)v逆 。
(2)此反应在a点时已达到平衡状态,a点的转化率比c点高的原因是_____________________。
9.丙烷氧化脱氢法制备丙烯的主要反应如下:
C H(g)+O(g)C H(g)+HO(g) ΔH=-118 kJ·mol -1
3 8 2 3 6 2 2
在催化剂作用下,C H 氧化脱氢除生成C H 外,还生成CO、CO 等物质。C H 的转化率和
3 8 3 6 2 3 8C H 的产率随温度变化关系如图所示。
3 6
(1)图中C H 的转化率随温度升高而上升的原因是__________________________________。
3 8
(2)575 ℃时,C H 的选择性为_______________________________。
3 6
(结果保留3位有效数字,C H 的选择性=×100%)
3 6
(3)基于本研究结果,能提高C H 选择性的措施是______________________。
3 6
10.在密闭容器中充入 5 mol CO和4 mol NO,发生反应:2NO(g)+ 2CO(g) N(g)+
2
2CO(g) ΔH=-746.5 kJ·mol-1,图1为平衡时NO的体积分数与温度、压强的关系。
2
(1)温度:T________(填“<”或“>”) T。
1 2
(2)若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是
图中A~G点中的________点。
(3)某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不
同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率
即NO的转化率),结果如图2所示。温度低于200 ℃时,图2中曲线Ⅰ脱氮率随温度升高
而变化不大的主要原因为_______________________________________________________;a
点________(填“是”或“不是”)对应温度下的平衡脱氮率,说明其理由:
_________________________________________________________________________________________________
。
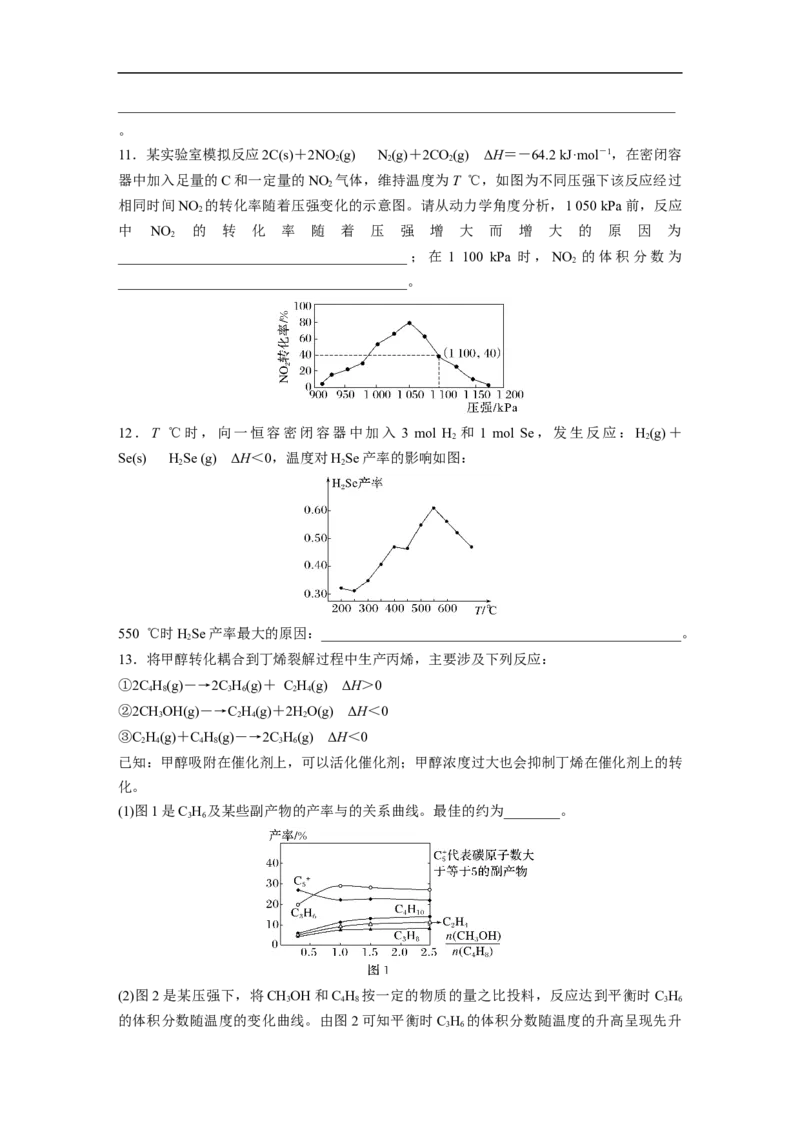
11.某实验室模拟反应2C(s)+2NO (g)N(g)+2CO(g) ΔH=-64.2 kJ·mol-1,在密闭容
2 2 2
器中加入足量的C和一定量的NO 气体,维持温度为T ℃,如图为不同压强下该反应经过
2
相同时间NO 的转化率随着压强变化的示意图。请从动力学角度分析,1 050 kPa前,反应
2
中 NO 的 转 化 率 随 着 压 强 增 大 而 增 大 的 原 因 为
2
_________________________________________;在 1 100 kPa 时,NO 的体积分数为
2
_________________________________________。
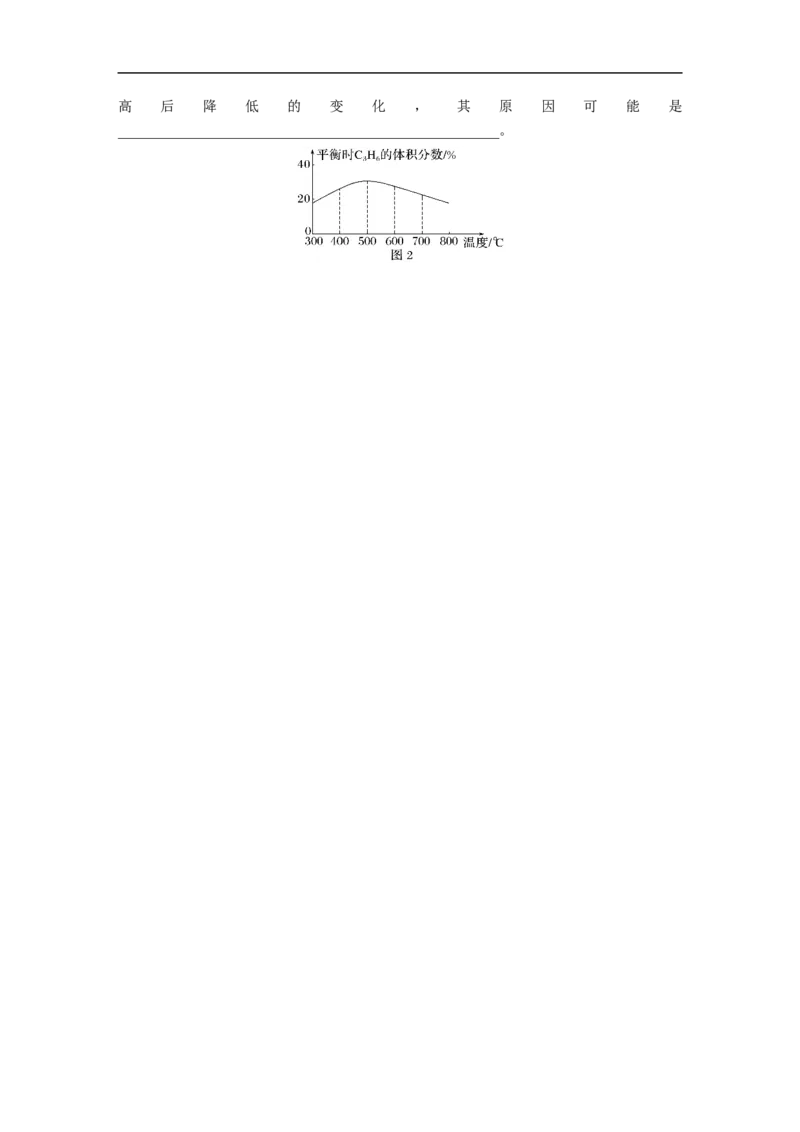
12.T ℃时,向一恒容密闭容器中加入 3 mol H 和 1 mol Se,发生反应:H(g)+
2 2
Se(s)HSe (g) ΔH<0,温度对HSe产率的影响如图:
2 2
550 ℃时HSe产率最大的原因:___________________________________________________。
2
13.将甲醇转化耦合到丁烯裂解过程中生产丙烯,主要涉及下列反应:
①2C H(g)―→2C H(g)+ C H(g) ΔH>0
4 8 3 6 2 4
②2CHOH(g)―→C H(g)+2HO(g) ΔH<0
3 2 4 2
③C H(g)+C H(g)―→2C H(g) ΔH<0
2 4 4 8 3 6
已知:甲醇吸附在催化剂上,可以活化催化剂;甲醇浓度过大也会抑制丁烯在催化剂上的转
化。
(1)图1是C H 及某些副产物的产率与的关系曲线。最佳的约为________。
3 6
(2)图2是某压强下,将CHOH和C H 按一定的物质的量之比投料,反应达到平衡时C H
3 4 8 3 6
的体积分数随温度的变化曲线。由图2可知平衡时C H 的体积分数随温度的升高呈现先升
3 6高 后 降 低 的 变 化 , 其 原 因 可 能 是
______________________________________________________。