文档内容
绝密★启用前
2025 年高考考前信息必刷卷 02
(陕西、山西、宁夏、青海专用)
化 学
考情速递
高考·新动向:2025年的高考命题将更加注重基础性知识的考查,避免出现偏题怪题。这意味着,未来
的高考将不再是一场对特殊技巧的记忆比拼,而是对基本概念、原理和方法的深刻理解。对于基础较
为薄弱的学生而言,这无疑是一个好消息,他们可以通过集中精力攻克核心考点,实现成绩上的突
破。形如此试卷第1、2、3、4、9题
高考·新考法:近年来,高考命题愈发重视对学生综合素质的评估。开放性问题、探究性问题成为新的
命题趋势,旨在鼓励学生深入思考,培养批判性思维能力和创新能力。这样的转变要求考生不仅仅停
留在知识的积累层面,更要学会运用知识去解决实际问题,展现出更高的思维品质,形如此试卷第
10、11、13题
高考·新情境:在科学与科技领域,题目设计将更加贴近当前科研动态和技术应用前沿,信息维度更加
丰富多元。题干中不仅直接呈现核心知识点,还巧妙隐藏间接信息、数据及深层结论,要求考生不仅
掌握课本知识,还需具备从复杂信息中提取关键要素,运用综合知识进行分析推理的能力,形如此试
卷第17、18题
命题·大预测:基于本卷的题目中可以看出绝大多数题目源于课本高于课本(比如此试卷离子方程式、
离子共存、化学用语、氧化还原、元素周期表及结构、基础实验、有机基础)同时紧跟时代脉搏聚焦
热点领域注重科学与科技领域级热形式进行考查(比如电化学、工业流程、有机推断等),新高考命
题的核心理念在于,通过设计新颖独特的情境,引导学生在运用关键能力和学科素养的基础上,通过
积极的思维活动而非单纯的知识回忆,来解决具有挑战性的学科问题。这不仅是当前高考改革的方
向,也是培养未来社会所需高素质人才的关键路径。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.化学与生活息息相关。下列有关“剂”的解读错误的是
A.选择“催化剂”加快对人类有益的化学反应速率B.月饼袋中“脱氧剂”去除 ,延长月饼保鲜时间
C.用 试剂检验“补血剂”中的
D.“泡沫灭火剂”可以减慢可燃物的燃烧速率(或灭火)
【答案】C
【详解】A.选择合适的催化剂可以加快有益的化学反应速率,也可以抑制不益人类的反应的发生,A正
确;
B.月饼袋中“脱氧剂”去除 ,从而减缓月饼变质的速率,能延长月饼的保鲜时间,B正确;
C.不能用 试剂检验补血剂中的 ,可用铁氰化钾检验 ,C错误,
D.“泡沫灭火剂”使用过程中喷出的氢氧化铝覆盖在可燃物表面,生成的二氧化碳可赶走可燃物附近的
氧气,从而减慢可燃物的燃烧速率,达到灭火的效果,D正确;
故选:C。
2.化学用语是化学学科知识的专业语言符号,下列有关表述正确的是
A. 是一种绿色氧化剂,其电子式为
B. 的化学名称是 甲基 戊烯
C.核废水中含 、 、 互为同素异形体
D. 的原子结构示意图为
【答案】B
【详解】
A. 是共价化合物,其电子式为 ,故A错误;
B.根据烯烃的系统命名法, 的化学名称是 甲基 戊烯,故B正确;
2 / 22C.同素异形体是同种元素组成的不同单质, 、 是化合物,不是同素异形体,故C错误;
D. 的原子结构示意图为 ,故D错误;
选B。
3.下列实验操作或事故处理方法正确的是
A.金属钠着火时,可用泡沫灭火器灭火
B.容量瓶用蒸馏水洗净,烘干后才能用于溶液的配制
C.水银温度计破碎后,应立即开窗通风并用硫磺粉末覆盖
D.氯气泄漏时,可用蘸NaOH溶液的湿毛巾捂住口鼻撤离
【答案】C
【详解】A.钠等活泼金属可以与水反应得到H,而H 也是易燃气体,所以当钠等活泼金属着火时,不能
2 2
使用任何含有水的灭火剂进行灭火,A错误;
B.配制过程中需要向容量瓶中加入水,所以经洗涤干净的容量瓶不必烘干,B错误;
C.水银温度计破碎后应立即开窗通风并用硫磺粉末覆盖,使Hg和S反应生成HgS,避免Hg蒸发为Hg
蒸气使人中毒,C正确;
D.NaOH具有较强的腐蚀性,因此氯气泄漏时,不可用蘸NaOH溶液的湿毛巾捂住口鼻,D错误;
答案选C。
4.下列反应的方程式书写错误的是
A.用过量氨水吸收工业尾气中的
B.向饱和纯碱溶液中通入过量
C.将硫酸铬溶液滴入含NaClO的强碱性溶液中:
D.用氢氟酸刻蚀玻璃:
【答案】C
【详解】A.用过量氨水吸收工业尾气中的 ,即 不足,则得到亚硫酸铵,离子方程式:
,A正确;B.因为碳酸氢钠的溶解度小于碳酸钠,则向饱和纯碱溶液中通入过量 得到碳酸氢钠沉淀,离子方程
式: ,B正确;
C.将硫酸铬溶液滴入含NaClO的强碱性溶液中,碱性条件应该生成铬酸根离子,根据得失电子守恒以及
电荷、原子守恒可得: ,C错误;
D.用氢氟酸刻蚀玻璃得到氟化硅与水: ,D正确;
故选C。
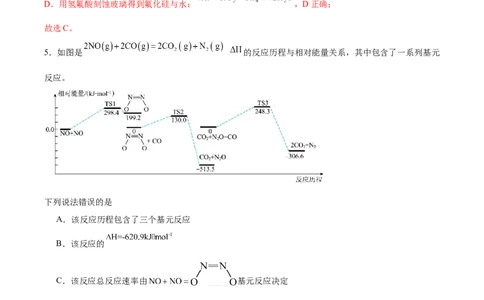
5.如图是 的反应历程与相对能量关系,其中包含了一系列基元
反应。
下列说法错误的是
A.该反应历程包含了三个基元反应
B.该反应的
C.该反应总反应速率由 基元反应决定
D. 与 具有相似的结构, 中 键和 键的数目不相等
【答案】D
【详解】A.根据分析可知,该反应历程包含了三个基元反应,故A正确;
B.利用盖斯定律,将反应①+②+③得, ,故B
正确;
4 / 22C.由于第一个基元反应活化能最大,所以该反应总反应速率由 基元反应决定,
故C正确;
D. 与 结构相似,所以 的结构式为N=N=O,所以 中 键和 键的数目也相等,故D错
误;
答案选D。
6.X、Y、Z、M和Q是五种前四周期元素,原子序数依次增大,基态X原子核外电子有3种空间运动状
态,基态Z原子的2p能级上所有电子自旋方向平行且不存在空轨道,M的原子序数是其上一周期同族元
素的2倍,基态Q原子的内层全满,最外层只有一个电子。下列说法正确的是
A.原子半径:
B.同周期元素中,第一电离能介于X和Z之间的元素有2种
C.Q的单质与M的单质在加热条件下反应生成QM
D. 、 均为非极性分子
【答案】D
【详解】A.原子半径S>B>C>N,即M>X>Y>Z,故A错误;
B.第一电离能介于B、N之间的元素包括Be、C、O,有3种,故B错误;
C.Q为Cu,M为S,S的氧化性较弱,故Cu和S加热生成Cu S,故C错误;
2
D.CO 分子中C原子价层电子对数为2+ 2+0=2,无孤电子对,空间构型为直线形,为非极
2
性分子,SO 分子中S原子价层电子对数为3+ 3+0=3,无孤电子对,空间构型为平面正三角
3
形,为非极性分子,故D正确;
故答案为D。
7.用下列实验装置进行相应的实验,能达到实验目的的是A.图①装置注射器活塞自动右移,说明 与 反应放热
B.图②装置可制备并收集
C.图③装置可制备少量干燥的 气体
D.图④装置验证氧化性:
【答案】C
【详解】A.Na和水产生氢气,也能使注射器活塞自动右移,不能证明反应放热,A错误;
B.NO 能够和水发生反应生成硝酸和NO,不能用排水法收集,B错误;
2
C.浓盐酸具有挥发性,浓硫酸具有吸水性,而且吸水相当于稀释,该过程会放热,可以用图③装置制备
少量干燥的HCl气体,C正确;
D.氯气也能使碘化钾反应生成碘单质使淀粉变蓝色,不能证明氧化性Br >Ⅰ,D错误;
2 2
故答案选C。
8.X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X基态原子中电子只有一种自旋方向;Y
核外电子有5种空间运动状态, 与 左右相邻; 与 的基态原子核外电子排布中的 能级和 能级电
子数相等; 在地壳中含量居第二位。下列说法不正确的是
A.第一电离能:
B.电负性:
C.气态氢化物的还原性:
D. 与 形成的晶体具有手性
【答案】A
【详解】A.同周期元素从左到右,第一电离能呈增大趋势,第一电离能 ,故A错误;
B.元素非金属性越强,电负性越大,电负性: ,故B正确;
C.元素非金属性越强,气态氢化物的还原性越弱,气态氢化物的还原性: ,故C正确;
D.Si与O形成SiO 晶体,在SiO 晶体中,由于其四面体结构的不对称性,使得晶体在某些条件下表现出
2 2
手性特性,故D正确;
选A。
6 / 229.常温常压下,下列指定条件的各组离子一定能大量共存的是
A.透明的溶液中: 、 、 、
B.在酒精中: 、 、 、
C.溶有 的水溶液中: 、 、 、
D.由水电离出 为 的溶液中: 、 、 、
【答案】C
【详解】A. 、 、 能发生氧化还原反应,不能大量共存,故A错误;
B.酒精具有还原性,能被 氧化,不能大量共存,故B错误;
C.该组离子均不与 反应,可以大量共存,故C正确;
D.水电离出 为 ,水的电离被抑制,溶液可能为酸溶液,也可能为碱溶液,若为碱
溶液则 不能大量共存,故D错误;
故选:C。
10.汽车尾气通过三元催化剂高效处理废气,发生反应为 。一定温度
下,在恒容密闭容器中充入 发生上述反应,测得 的浓度随时间的变化如图所示。
下列叙述错误的是
A. 时正反应速率大于逆反应速率B. 内 的转化率
C.当 消耗速率等于 消耗速率一半时到达 对应状态
D. 内 平均速率
【答案】C
【详解】A.由图可知, 时反应没有达到平衡,向正方向进行,故正反应速率大于逆反应速率,A正
确;
B.由图可知, 内 的转化率为 ,根据转化率定义, 、 起始投料相等、
化学计量数相同,则它们转化率相等,B正确;
C. 达到平衡状态,此时 消耗速率等于 消耗速率的2倍,C错误;
D.由图可知, 内 平均速率 ,在相同时间内, 的平均速率是
的一半, ,D正确;
答案选C。
11. 是一种优良的锂离子电池负极材料。在充电过程中,负极材料晶胞的组成变化如下图所示。
下列说法正确的是
A.基态 的价电子排布式为
B. 的 为
8 / 22C.图示的 晶胞中
D. 晶胞中 的配位数为4
【答案】C
【详解】A. 是30号元素,基态 的价电子排布式为 ,则基态 的价电子排布式为 ,A
错误;
B. 晶体中 的个数为4, 的个数为 , 的 为
,B错误;
C.图示黑球为7个,设图示的 晶胞中Li+、Zn2+的个数分别为x、y,则x+y=7、又由电荷守恒可
知,两者所带正电荷为8,即x+2y=8,解得x=6、y=1,则 ,C正确;
D.由 晶胞结构可知,以底面面心硫离子为例,距离 最近且相等的 上下层各有4个,共有8个,
则 的配位数为8,D错误;
故选C。
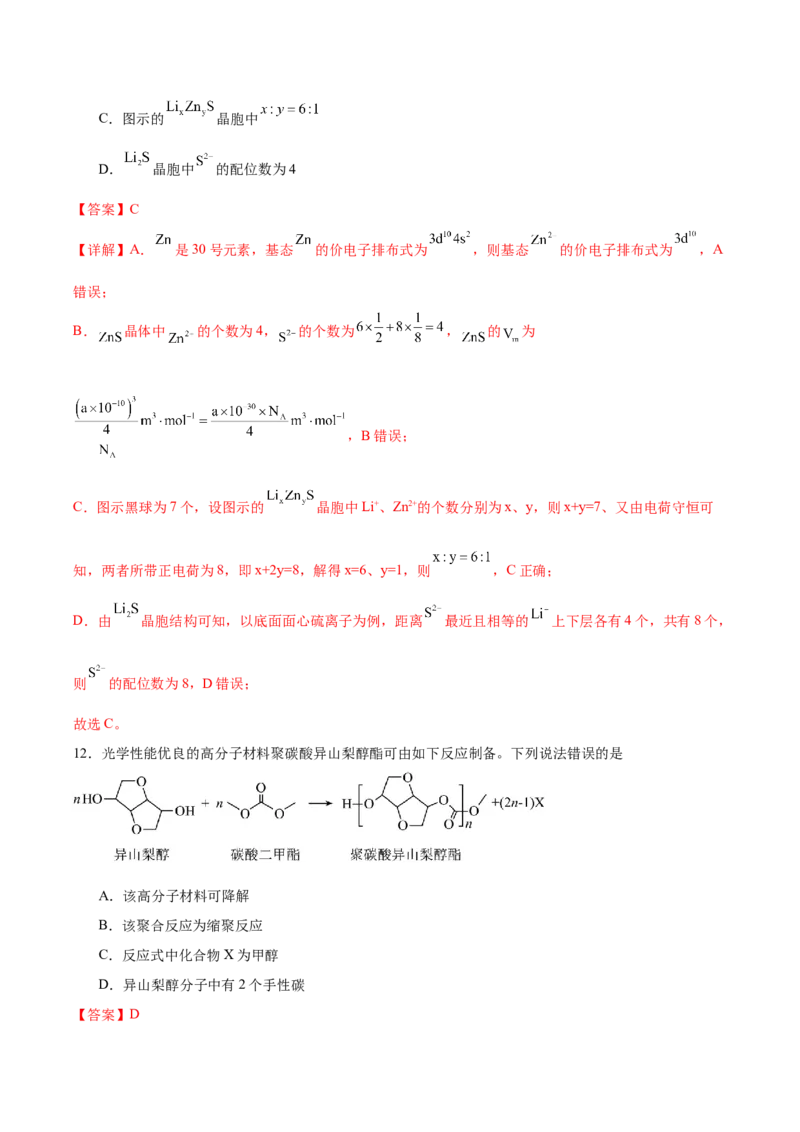
12.光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。下列说法错误的是
A.该高分子材料可降解
B.该聚合反应为缩聚反应
C.反应式中化合物X为甲醇
D.异山梨醇分子中有2个手性碳
【答案】D【详解】A.根据高分子结构可知,含酯基可以降解,A正确;
B.该反应在生产高聚物的同时还有小分子的物质生成,属于缩聚反应,B正确;
C.反应式中异山梨醇释放出一个氢原子与碳酸二甲酯释放出的甲氧基结合生成甲醇,故反应式中X为甲
醇,C正确;
D.连接4个不同原子或原子团的碳原子为手性碳原子,异山梨醇中有四个碳原子为手性碳原子(
),D错误;
答案选D。
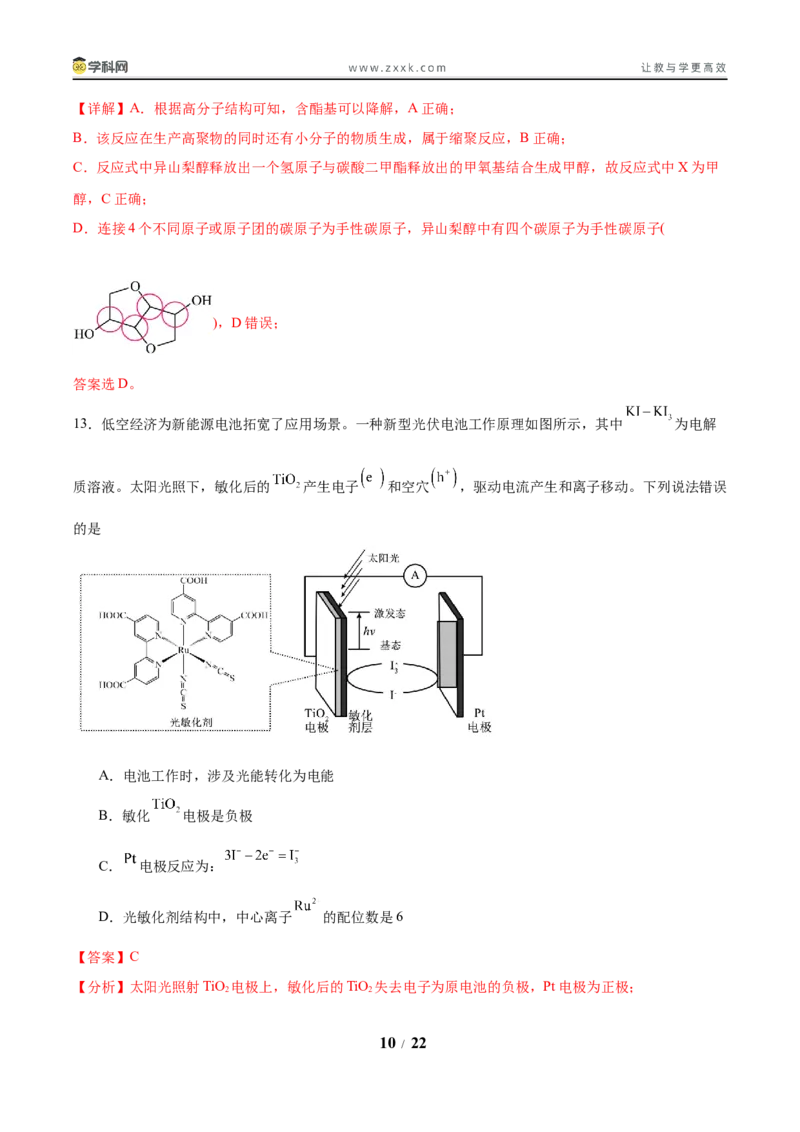
13.低空经济为新能源电池拓宽了应用场景。一种新型光伏电池工作原理如图所示,其中 为电解
质溶液。太阳光照下,敏化后的 产生电子 和空穴 ,驱动电流产生和离子移动。下列说法错误
的是
A.电池工作时,涉及光能转化为电能
B.敏化 电极是负极
C. 电极反应为:
D.光敏化剂结构中,中心离子 的配位数是6
【答案】C
【分析】太阳光照射TiO 电极上,敏化后的TiO 失去电子为原电池的负极,Pt电极为正极;
2 2
10 / 22【详解】A.该装置是光伏电池,太阳光照下敏化后的 产生电子 和空穴 ,驱动电流产生和离
子移动,所以电池工作时,涉及光能转化为电能,A正确;
B.太阳光照下,敏化后的 产生电子 和空穴 ,即敏化 电极失电子为负极,B正确;
C. 电极为正极,发生得电子还原反应, 电极电极反应为: ,C错误;
D.由图可知,光敏化剂结构中,中心离子 与6个N原子成键,配位数是6,D正确;
答案选C。
14.室温下,用含少量 的 溶液制备 的过程如图所示。已知 ,
。下列说法正确的是
A. 的 溶液中:
B.“除钙”得到的上层清液中:
C. 的 溶液中:
D.“沉镍”后的滤液中一定存在:
【答案】B
【详解】A. 的 溶液中电荷守恒: ,物料守恒:
,根据以上两式可得: ,A错误;
B.“除钙”得到的上层清液为氟化钙饱和溶液,存在沉淀溶解平衡,因此有: ,B
正确;C. 的 溶液中有电荷守恒: ,整理得:
,C错误;
D.“沉镍”时生成碳酸镍、二氧化碳和氯化钠,“沉镍”后的滤液中含有碳酸、多余的碳酸氢钠和氯化
钠,根据物料守恒一定存在: ,D错误;
故选B。
二、非选择题:本题共4小题,共58分。
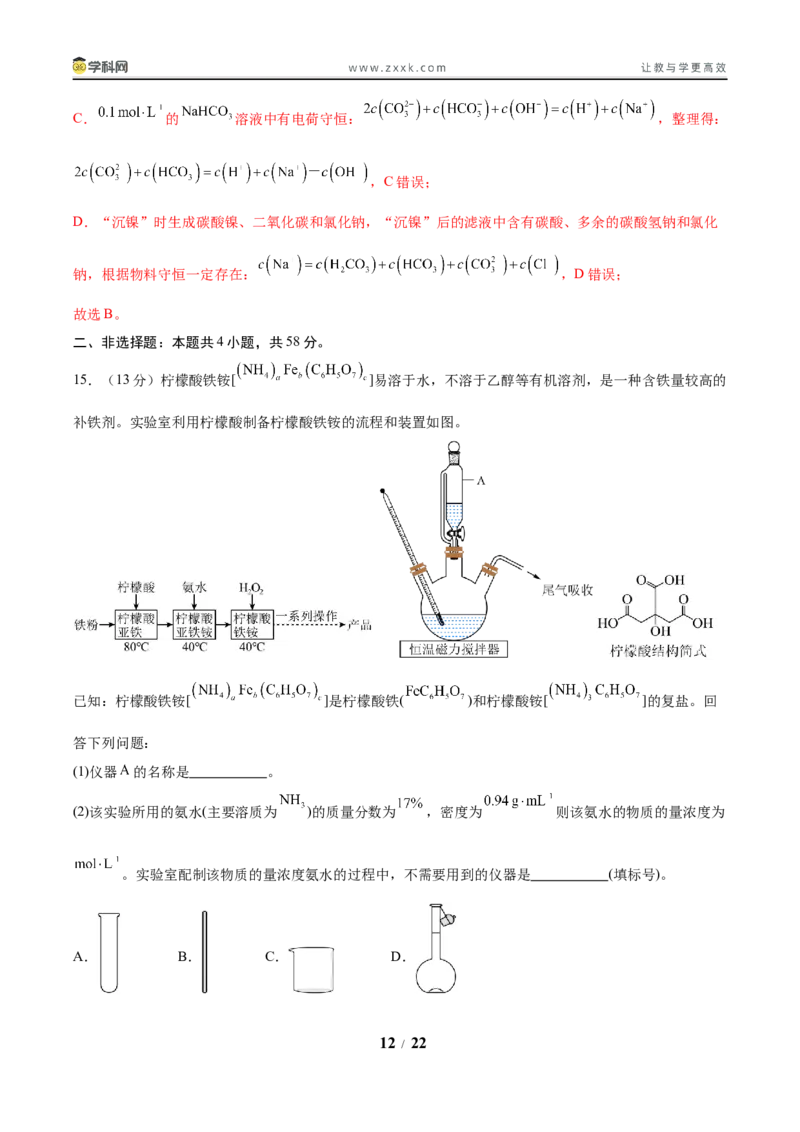
15.(13分)柠檬酸铁铵[ ]易溶于水,不溶于乙醇等有机溶剂,是一种含铁量较高的
补铁剂。实验室利用柠檬酸制备柠檬酸铁铵的流程和装置如图。
已知:柠檬酸铁铵[ ]是柠檬酸铁( )和柠檬酸铵[ ]的复盐。回
答下列问题:
(1)仪器 的名称是 。
(2)该实验所用的氨水(主要溶质为 )的质量分数为 ,密度为 则该氨水的物质的量浓度为
。实验室配制该物质的量浓度氨水的过程中,不需要用到的仪器是 (填标号)。
A. B. C. D.
12 / 22(3)写出反应生成柠檬酸亚铁( )的化学方程式: (柠檬酸写分子式即可)。
(4)制备柠檬酸亚铁铵和柠檬酸铁铵时均需控温40℃,其原因是 。
(5)“一系列操作”包括 、 ,过滤,洗涤,干燥。
(6)测定柠檬酸铁铵组成的实验方案如下:取适量样品溶于蒸馏水,配成 溶液。取 溶液,
加入足量 溶液充分反应,过滤、洗涤,灼烧至恒重,测得 固体。另取 溶液于锥
形瓶中,依次加入足量 、 溶液充分反应,滴入2滴酚酞试液,用 标准溶
液滴定至终点,消耗标准溶液 ,滴定过程中反应如:
, ,柠檬酸铁
铵化学式为 。
【答案】(1)恒压滴液漏斗
(2) 9.4 A
(3)Fe+C HO=FeC HO+H ↑
6 8 7 6 6 7 2
(4)温度低于40℃时,化学反应速率慢,温度高于40℃时,双氧水和氨水发生分解反应而损耗
(5) 蒸发浓缩 冷却结晶
(6)(NH )Fe(C HO)
4 3 6 5 7 2
【详解】(1)由仪器的外形可知,A为恒压滴液漏斗;
(2)根据公式c= =9.4mol/L;配制溶液时需要用烧杯稀释,用玻璃棒引
流,用容量瓶配制溶液,不需要试管,故选A;
(3)铁和柠檬酸发生置换反应生成柠檬酸亚铁和氢气,化学方程式为Fe+C HO=FeC HO+H ↑;
6 8 7 6 6 7 2
(4)温度低于40℃时,化学反应速率慢,温度高于40℃时,双氧水和氨水发生分解反应而损耗,故需要
控制温度40℃;
(5)柠檬酸铁铵易溶于水,不溶于乙醇等有机溶剂,从溶液得到晶体的方法为蒸发浓缩、冷却结晶、过
滤、洗涤(用乙醇)、干燥;
(6)灼烧后得到0.002mol固体为Fe O,则20.00mL溶液中n(Fe3+)=0.002×2=4×10-3mol,根据反应方程式,
2 3
建立关系式为4 ~4OH-,20.00mL溶液中n( )=n(OH-)=12.00×10-3L×1.00mol/L=12×10-3mol,根据化合价代数和为0,12×10-3mol×1+4×10-3mol×3=n( )×3,解得n( )=8×10-3mol,因此a∶b∶c=12×10-
3mol∶4×10-3mol∶8×10-3mol=3∶1∶2,化学式为(NH )Fe(C HO)。
4 3 6 5 7 2
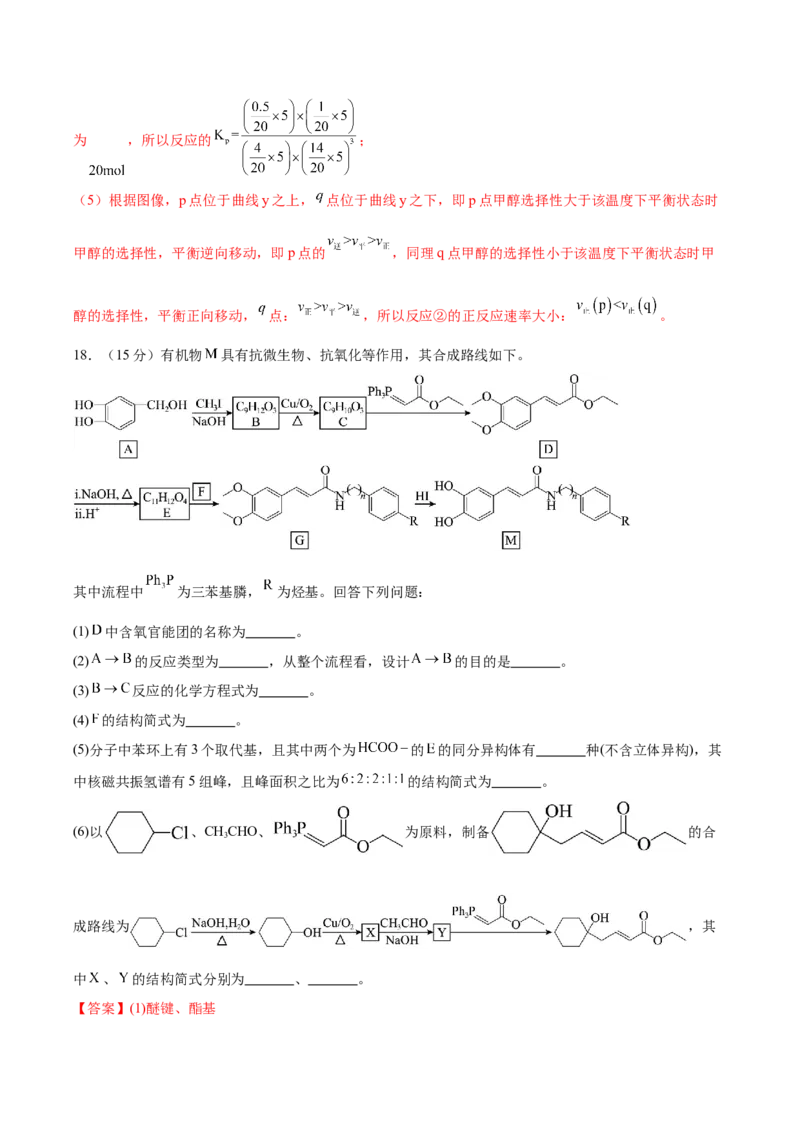
16.(15分)氧化钴 粉体材料在工业、电子、电讯等领域都有着广阔的应用前景。某工厂用废旧
钴基合金(主要成分为 ,还含有 、 、 、 、 )制备 ,工艺流程如图所示:
已知:①该工艺条件下, 、 不能氧化 。
②常温下, , , 。
③ 。
回答下列问题:
(1)钴元素在元素周期表中的位置是 。
(2)“碱浸”时要将“废旧钴基合金”粉碎,其目的是 。
(3)“酸浸”所得“浸渣”的成分为 (填化学式)。
(4)“除铁”时需要控制反应温度低于50℃的目的是 。
(5)“沉钙”时反应的离子方程式为 。若“沉钙”后的溶液中 ,则
此时溶液的 为 。
(6)为测定“转化”时获得草酸钴( )的纯度,现称取 草酸钴样品,将其用适当试剂转化为草酸
铵 溶液,再用过量稀硫酸酸化,并用 高锰酸钾标准溶液滴定,平行实验三次,
达到滴定终点时,消耗高锰酸钾标准溶液的体积如下表所示:
实验序号 1 2 3
高锰酸钾标准溶液的体积/mL 39.97 41.86 40.03
①达到滴定终点时的标志为 。
14 / 22②草酸钴样品的纯度为 。
【答案】(1)第四周期Ⅷ族
(2)增大接触面积,提高反应速率与碱浸效率(合理即可)
(3) 、
(4)防止双氧水分解及氨水的挥发与分解(合理即可)
(5) 5.7
(6) 当滴加最后半滴高锰酸钾标准溶液时,溶液颜色由无色变为浅紫红色且 内不变色(合理即可)
73.5%
【详解】(1)钴元素的原子序数为27,原子核外有27个电子,核外电子排布为1s22s22p63s23p63d74s2,则
位于第四周期Ⅷ族,故答案为:第四周期Ⅷ族。
(2)粉碎可以增大接触面积,“碱浸”时要将“废旧钴基合金”粉碎的原因为增大接触面积,提高反应
速率与碱浸效率,故答案为:增大接触面积,提高反应速率与碱浸效率。
(3)根据分析,“酸浸”时和硫酸反应生成硫酸铅沉淀、硫酸钙沉淀,所得“浸渣”的成分为 、
,故答案为: 、 。
(4)双氧水受热易分解,氨水易挥发,“除铁”时需要控制反应温度不能高于的原因是防止双氧水分解,
及浓氨水的挥发与分解,故答案为:防止双氧水分解及氨水的挥发与分解。
(5)“沉钙”是钙离子和HF反应,生成CaF 和H+的过程,反应的离子方程式为
2
;若“沉钙”后的溶液中 ,根据
、 ,则
,
,则此时溶液的 为,故答案为:5.7。
(6)①酸性KMnO 溶液为紫红色,滴定终点时无色变为紫红色,则滴定终点的现象是当滴加最后半滴高
4
锰酸钾标准溶液时,溶液颜色由无色变为浅紫红色且 内不变色,故答案为:当滴加最后半滴高锰酸钾
标准溶液时,溶液颜色由无色变为浅紫红色且 内不变色。
②第2次实验误差较大,舍弃,消耗高锰酸钾标准溶液的体积为 mL=40.00mL,根据反应的离
子方程式 可知,
,则样品中含有的草酸钴的质量为=
,则样品的纯度为 ,故答案为:73.5%。
17.(15分)在催化剂作用下可将温室气体 加氢制甲醇,再通过甲醇制备燃料和化工原料等,是解决
能源问题与实现双碳目标的主要技术之一、
Ⅰ.通过以下反应可获得新型能源二甲醚。
①
②
③
(1)反应 的 。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
A.增大 浓度,反应①、②的正反应速率都增加
B.移去部分 ,反应②、③的平衡均向右移动
C.加入反应①的催化剂,可提高 的平衡转化率
D.降低反应温度,反应①②③的正、逆反应速率都减小
16 / 22Ⅱ.在 下,将 和 在催化剂作用下仅发生上述反应①和②,平衡时 为
选择性 [ ]及 的转化率 随温度的变化如图所示。
(3)表示平衡时 的转化率的曲线是 (填“ ”“ ”或“ ”), 转化率随温度改变呈现
该曲线变化的原因: 。
(4)250℃时,平衡体系共有 ,则 的平衡转化率 ,反应②的
( 为用分压表示的平衡常数,气体的分压 总压 该气体的物质的量分数,列计算式)。
(5) 、 两点反应②的正反应速率大小: 。(填“ ”“ ”或“ ”)
【答案】(1)
(2)AD
(3) z 反应①为吸热反应,反应②为放热反应,温度低于250℃时,以反应②为主,随温度升高,
平衡逆向移动, 的转化率降低;温度高于250℃时,以反应①为主,随温度升高,平衡正向移动,
的转化率升高
(4)
(5)【详解】(1)根据盖斯定律,反应 的 ,可由
;
(2)A.增大 的浓度,反应①和②反应物浓度增大,平衡正向移动,所以①、②的正反应速率都增加,
A 正确;
B.移去部分 ,反应②的平衡向右移动,反应③的平衡向左移动,B错误;
C.加入反应①的催化剂,平衡不移动,C错误;
D.降低反应温度,平衡会移动,同时会导致反应①②③的正、逆反应速率都减小,D正确;
答案选AD;
(3)反应①为吸热反应,反应②为放热反应。随着温度升高,反应②平衡逆移,甲醇含量降低,则x是
甲醇选择性变化曲线,甲醇选择性与CO的选择性之和为1,且升温反应①平衡正向移动,导致CO的量增
大,故y曲线代表CO的选择性,则曲线z表示的是二氧化碳的转化率。温度低于 时,以反应②为主,
随温度升高,平衡逆向移动, 的转化率降低;温度高于 时,以反应①为主,随温度升高,平衡
正向移动, 的转化率升高,因此二氧化碳的转化率随温度改变呈现该曲线的变化;
(4) 时,平衡体系共有 甲醇,结合图像可知,选择性 。说明此时 ,
则其平衡转化率为: 。反应②的方程式为: ,
根据分析列出: ,
,反应平衡以后,平衡体系中含有5-0.5-0.5=
、16-1.5-0.5= 、0.5+0.5= 、 。即气体的总物质的量
18 / 22为 ,所以反应的 ;
(5)根据图像,p点位于曲线y之上, 点位于曲线y之下,即p点甲醇选择性大于该温度下平衡状态时
甲醇的选择性,平衡逆向移动,即p点的 ,同理q点甲醇的选择性小于该温度下平衡状态时甲
醇的选择性,平衡正向移动, 点: ,所以反应②的正反应速率大小: 。
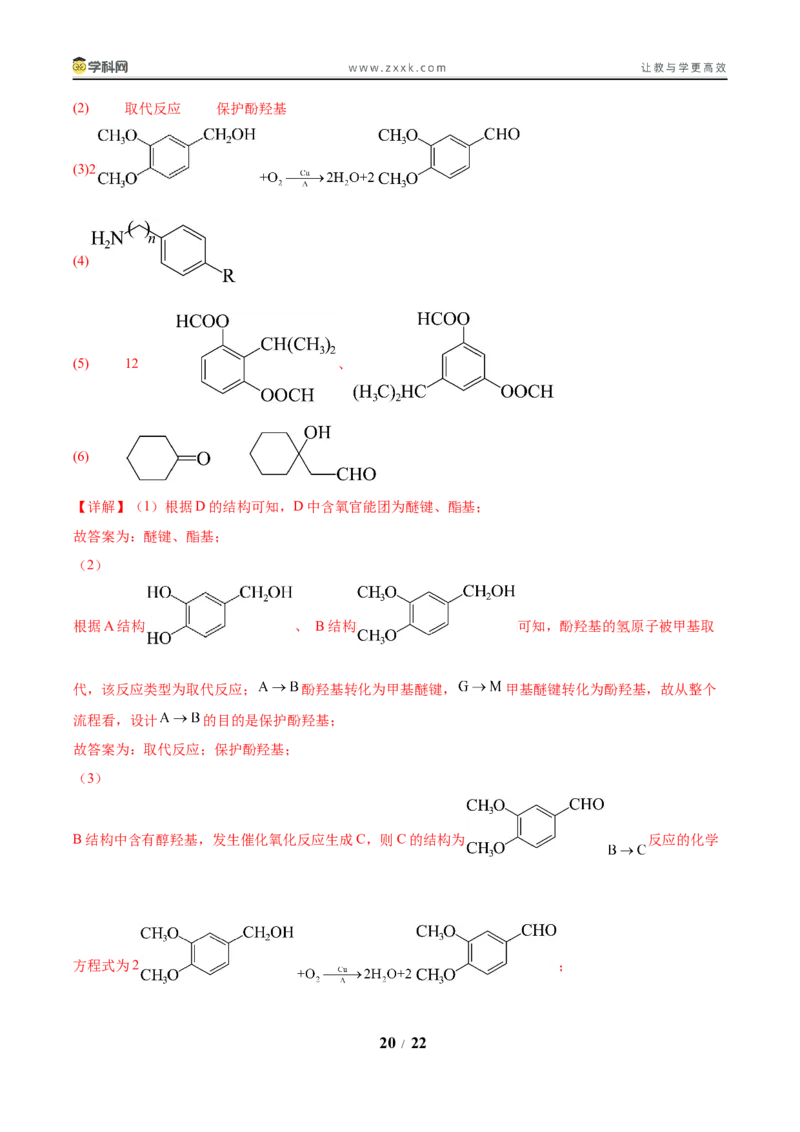
18.(15分)有机物 具有抗微生物、抗氧化等作用,其合成路线如下。
其中流程中 为三苯基膦, 为烃基。回答下列问题:
(1) 中含氧官能团的名称为 。
(2) 的反应类型为 ,从整个流程看,设计 的目的是 。
(3) 反应的化学方程式为 。
(4) 的结构简式为 。
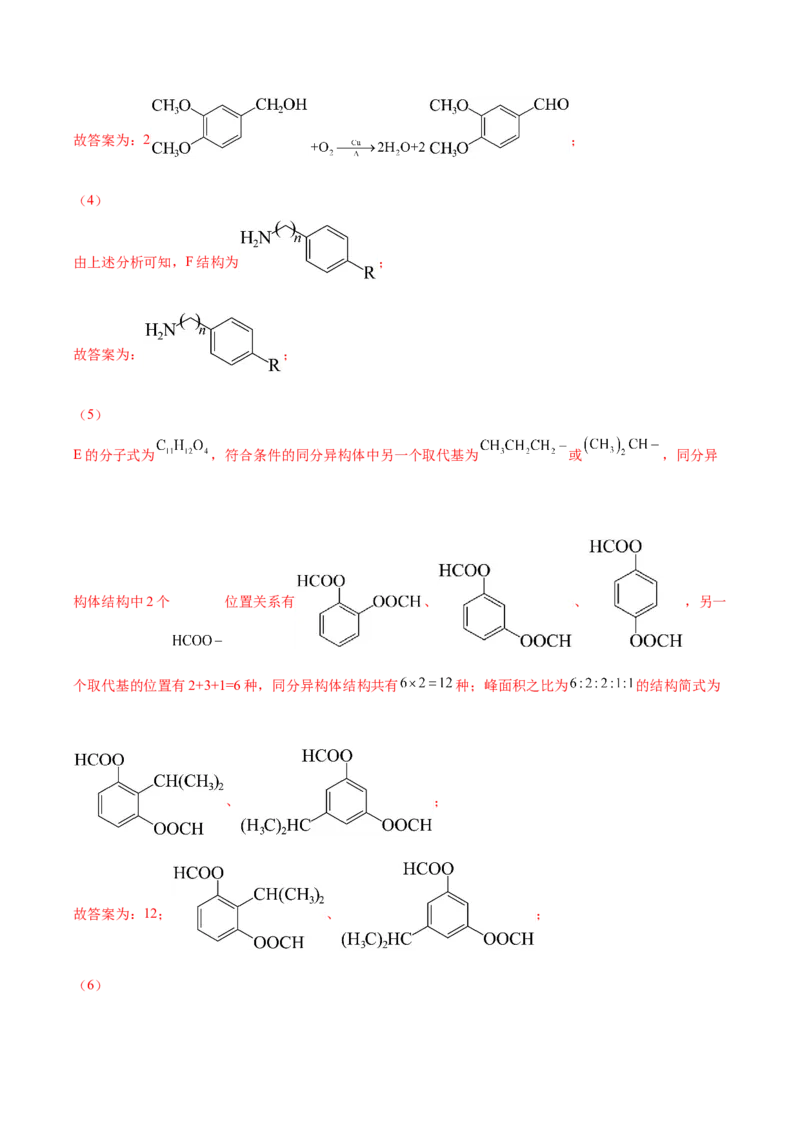
(5)分子中苯环上有3个取代基,且其中两个为 的 的同分异构体有 种(不含立体异构),其
中核磁共振氢谱有5组峰,且峰面积之比为 的结构简式为 。
(6)以 、CHCHO、 为原料,制备 的合
3
成路线为 ,其
中 、 的结构简式分别为 、 。
【答案】(1)醚键、酯基(2) 取代反应 保护酚羟基
(3)2
(4)
(5) 12 、
(6)
【详解】(1)根据D的结构可知,D中含氧官能团为醚键、酯基;
故答案为:醚键、酯基;
(2)
根据A结构 、 B结构 可知,酚羟基的氢原子被甲基取
代,该反应类型为取代反应; 酚羟基转化为甲基醚键, 甲基醚键转化为酚羟基,故从整个
流程看,设计 的目的是保护酚羟基;
故答案为:取代反应;保护酚羟基;
(3)
B结构中含有醇羟基,发生催化氧化反应生成C,则C的结构为 反应的化学
方程式为2 ;
20 / 22故答案为:2 ;
(4)
由上述分析可知,F结构为 ;
故答案为: ;
(5)
E的分子式为 ,符合条件的同分异构体中另一个取代基为 或 ,同分异
构体结构中2个 位置关系有 、 、 ,另一
个取代基的位置有2+3+1=6种,同分异构体结构共有 种;峰面积之比为 的结构简式为
、 ;
故答案为:12; 、 ;
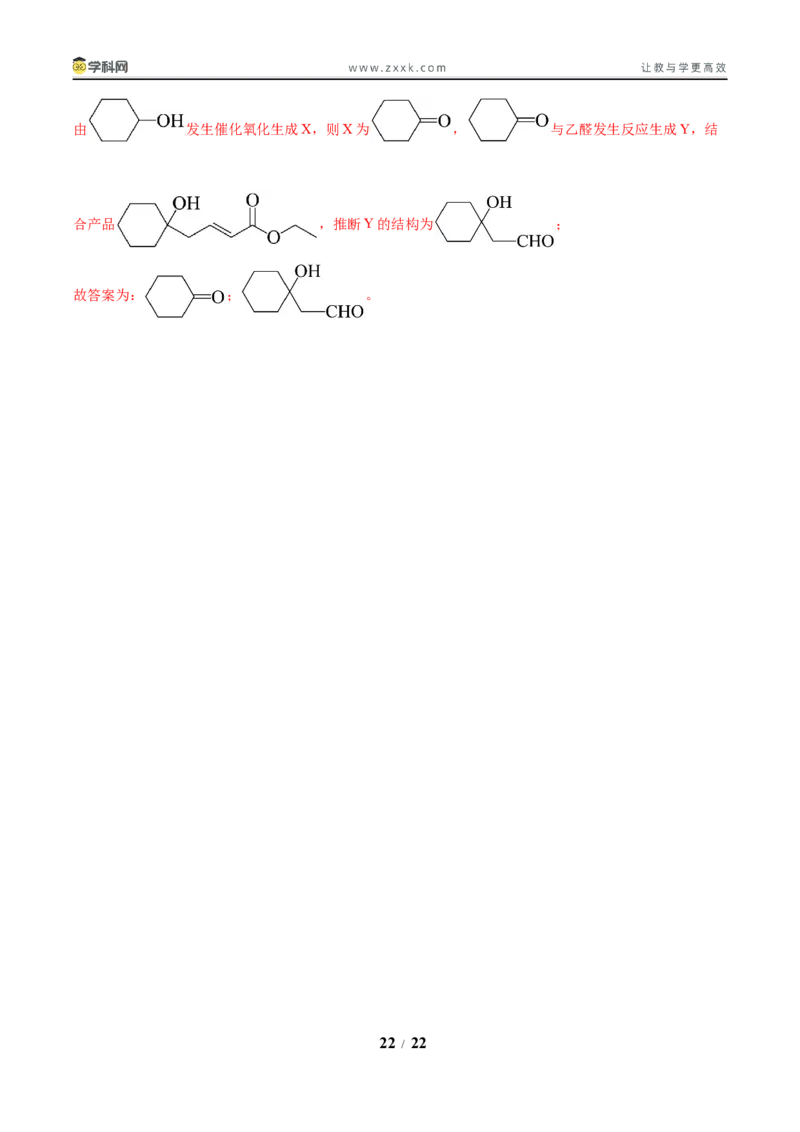
(6)由 发生催化氧化生成X,则X为 , 与乙醛发生反应生成Y,结
合产品 ,推断Y的结构为 ;
故答案为: ; 。
22 / 22