文档内容
高三年级调研考试
化 学
题号
1 2 3 4 5 6 7 8 9 10 11 12 13
答案
C B B C D D C C D A AB C BD
解析: 消毒液中含有 水解显碱性 且有强氧化性的 生成 其主要通过 的强氧化
1.C “84” NaClO, , HClO , HClO
性杀菌消毒 项错误 乙醇没有强氧化性 消毒原理与 消毒液不同 项错误 消毒液显碱
,A ;75% , “84” ,B ;“84”
性 滴到红色石蕊试纸上 先变蓝后褪色变为白色 故试纸由内到外会的颜色分别为白 蓝 红的 项正
, , , 、 、 ,C
确 消毒液中有效成分为 漂白粉的有效成分是 项错误
;“84” NaClO, Ca(ClO)2,D 。
解析:合金熔点通常低于其组成金属的熔点 项错误 碳纤维 石墨烯均为碳单质 与金刚石 石墨互
2.B ,A ; 、 , 、
为同素异形体 项正确 树脂基复合材料是由以有机聚合物为基体的纤维增强材料 其属于有机高分子
,B ; ,
材料 项错误 陶瓷基复合材料具有耐温高 密度低的优势 其属于新型陶瓷材料 项错误
,C ; 、 , ,D 。
解析:制备氢氧化铁胶体是将饱和氯化铁溶液滴入沸水中 而不是氢氧化钠溶液 项错误 制备硝基
3.B , ,A ;
苯 原料为苯 浓硫酸与浓硝酸的混酸 选用水浴加热 项正确 中和滴定不选用石蕊作指示剂 且未使用
, 、 , ,B ; ,
滴定管夹 项错误 氯化铵和氢氧化钙加热制氨气 但不能无水氯化钙干燥氨气 需用碱石灰干燥 项
,C ; , , ,D
错误
。
解析:光导纤维是信息高速公路的骨架 其成分是 项正确 氮氧化物与硫氧化物均是酸雨的主
4.C , SiO2,A ;
要成因 项正确 与 均可于碱反应 但 与碱反应歧化为亚硝酸盐和硝酸盐 所以 不是酸性
,B ;NO2 SO2 , NO2 , NO2
氧化物 项错误 具有漂白作用 但有毒 不能用于食品的增白 项正确
,C ;SO2 , , ,D 。
解析: 原子的质子数为 中子数为 则质量数为 故含中子数为 的 原子为49 项正
5.D Ti 22, 27, 49, 27 Ti 22Ti,A
确 原子的最外层电子数为 得到一个电子后最外层电子数变为 项正确 含有两个 键
;Cl 7, 8,B ;H2O O—H ,
两个孤电子对 孤电子对不体现在结构式中 故 结构式为 项正确 属于共价化合物
, , H2O H—O—H,C ;HCl ,
其电子式 ·· 项错误
· ·
H·Cl·,D 。
··
解析: 和 反应为可逆反应 故 溶于水中 转移的电子数小于 N 项错误 标准状况
6.D Cl2 H2O , 1 mol Cl2 , 1 A,A ;
下 是固体 项错误 -1的 溶液 并未指出体积 项错误 表示c +
,SO3 ,B ;1 mol·L NaCl , ,C ;pH=1 (H )= 0.1 mol·
-1 的 的 溶液中 n + 项正确
L ,1 L pH=1 CH3COOH , (H )= 0.1 mol,D 。
解析:烟气主要含 故不可直接排放于空气中 项正确 加入 的目的是将 2+完全转化为
7.C SO2, ,A ; H2O2 Fe
3+ 为方便后续完全除去铁元素 项正确 进一步净化过程主要除去 2+ 为不引入杂质阳离子 应用
Fe , ,B ; Cu , ,
除去 2+ 项错误 电解 溶液时 2+向在阴极移动 并在阴极发生还原反应 在阴极析出
Zn Cu ,C ; ZnSO4 ,Zn , ,Zn ,D
项正确
。
解析: 二羟基萘的分子式为 项错误 苯环无法与 加成 二羟基萘与足量
8.C 2,6- C10H8O2,A ; Br2 ,1 mol 2,6-
反应 可产生 项错误 二羟基萘分子中最多有 个原子共面 项正确 二羟基萘
Na , 1 mol H2,B ;2,6- 20 ,C ;2,6-
虽存在羟基 但萘环无法进行消去反应 项错误
, ,D 。
解析:放电时 电极为负极 发生氧化反应 项正确 该电池有由金属钾参与反应 不能为水溶液
9.D Al , ,A ; , ,B
项正确 放电时 电极为正极 +向正极移动 项正确 放电时 每转移 - +向 电极区
; ,Cu ,K ,C ; , 1 mol e ,1 mol K Cu
移动 即 电极区质量增重 项错误
, Cu 39 g,D 。
解析:根据化合物的结构和三种元素原子序数之和为 可推断出 为 为 为 化合物
10.A 19, X Na、Y H、Z N。
在自然界中一般不存在单质 项正确 与 形成的化合物 中 为 价 项错误 的简
Na ,A ;Na H NaH ,H -1 ,B ;N
答案 第 页(共 页)
1 5H
单氢化物为氨气 氨气电子式为 ·· 项错误 三种元素中 原子半径最大 原子半径最小
· ·
, H·N·H,C ; ,Na ,H ,D
··
项错误
。
解析:邻苯二甲酸二甲酯水解可得到甲醇和邻苯二甲酸两种有机物 项错误 邻苯二甲酸二甲酯中
11.AB ,A ;
含有 个苯环和 个酯基 酯基无法和氢气加成 故 邻苯二甲酸二甲酯最多可与 加成
1 2 , , 1 mol 3 mol H2 ,B
项错误 邻苯二甲酸二甲酯所有碳原子均可共面 故邻苯二甲酸二甲酯中最多有 个碳原子共面 项
; , 10 ,C
正确 邻苯二甲酸二甲酯中苯环可发生加成反应和取代反应 酯基可发生取代反应 项正确
; , ,D 。
解析:依据题意 浸锰过程中 与 会发生反应 离子方程式为 + 2+
12.C , Fe2O3 SO2 , Fe2O3+SO2+2H 2Fe +
2- 项正确 在浸锰过程中发生不反应 故滤渣 中主要成分为 项正确 氧化过程的
SO4 +H2O,A ;SiO2 , Ⅰ SiO2,B ;
目的是将过量的 消耗 并将 2+氧化 以便后续过滤除去 项错误 加入 溶液后 发生的
SO2 , Fe , ,C ; NH4HCO3 ,
反应为 2+ - 项正确
Mn +2HCO3 MnCO3↓+CO2↑+ H2O,D 。
解析: -1的 溶液的 约为 由此计算平衡常数K -7.3 数量级为 -8
13.BD 0.1 mol·L HX pH 4.3, =10 , 10 ,0.1 mol·
-1的 溶液的 约为 由此计算平衡常数 K -3 数量级为 -3 项错误 点溶质为
L HY pH 2, =1.11×10 , 10 ,A ;B NaY
和 的混合物 且物质的量浓度之比为 电荷守恒为c + c + c - c - 物料守
HY , 1 ∶ 1, (H )+ (Na ) (OH )+ (Y ),
恒为 c + c c - 两式合并可得 c + c c - c - 项正确
2 (Na ) (HY)+ (Y ), 2 (H )+ (HY) 2 (OH )+ (Y ),B ;HX
曲线上的 与 点混合后 形成 和 的混合物 且物质的量浓度之比为 根据物料守恒可得c
A C , NaX HX , 3 ∶ 1,
- c c + 项错误 两点均显酸性 均抑制水的电离 点的酸性强 水的电离程
(X )+ (HX) 4 (Na ),C ;A、B , ,b ,
度小 而 点为盐促进水的电离 故 三点中由水电离出的c + 顺序为 项正确
, C , A、B、C (H ) C>A>B,D 。
分
14.(14 )
答案: 分液漏斗 分 分
(1) (1 ) 2NaClO3+H2O2+H2SO4 2ClO2↑+O2↑+Na2SO4+2H2O(2 )
可以起到搅拌作用 将产生的 排至 中充分反应 稀释二氧化氯 防止因二氧化氯的
(2)① ,② ClO2 C ,③ ,
浓度过高而发生爆炸 分 答任意两点即满分 表述合理即可
(2 , , )
防止倒吸 或作安全瓶 分 吸收尾气 防止污染环境 分
(3) ( )(1 ) ClO2, (1 )
+ - 分 防止温度过高 分解 防
(4)2ClO2+H2O2+2Na +2OH 2NaClO2↓+O2+2H2O(2 ) ① ,H2O2 ;②
止 分解爆炸 防止 挥发 降温析出更多晶体 分 答 点即满分 表述合理即可
ClO2 , ClO2 ,③ (1 , 1 , )
最后一滴硫代硫酸钠溶液加入后 溶液由蓝色变为无色 且 不恢复原色 分
(5)① , , 30s (2 )
分
②90.5%(2 )
解析: 盛放硫酸的仪器名称为分液漏斗 装置 中反应的化学方程式为
(1) ; A 2NaClO3+H2O2+H2SO4
2ClO2↑+O2↑+Na2SO4+2H2O。
氮气可以起到搅拌作用 氮气将产生的 排至 中充分反应 由于二氧化氯 浓
(2)① ;② ClO2 C ;③ (ClO2)
度过高时易分解爆炸 还能稀释二氧化氯 防止因二氧化氯的浓度过高而发生爆炸
, , 。
气体易溶于水 故 的作用是防止倒吸 或作安全瓶 气体会污染空气 因此用氢氧
(3)ClO2 , B ( );ClO2 ,
化钠溶液吸收 以防止污染
, 。
一段时间后 装置中有 晶体析出 则 装置中发生的离子反应方程式为
(4) ,C NaClO2 , C 2ClO2+H2O2+
+ - 冰水浴冷却的目的是防止温度过高 分解
2Na +2OH 2NaClO2↓+O2+2H2O, ,H2O2 。
此时淀粉变蓝 用硫代硫酸钠标准溶液滴定 滴定终点的现象为最后一滴硫代硫酸钠溶液加入
(5)① , ,
后 溶液由蓝色变为无色 且 不恢复原色
, , 30 s 。
含有 的溶液中加入足量酸化的 溶液反应 被还原为 - 离子反应方程式为
② NaClO2 KI ,NaClO2 Cl , :
- - + - 根据 2- 2- - 可得关系式 - 2- 则
ClO2+4I +4H 2I2+Cl +2H2O, I2+2S2O3 S4O6 +2I , :ClO2 ~2I2~4S2O3 ,
样品的溶液中n n 2- -1 则
500 mL (NaClO2)= 1/4× (S2O3 )×500/10=1/4×0.20 mol·L ×0.02 L×50=0.05 mol,
样品的纯度 故答案为
NaClO2 = (0.05×90.5)/5=90.5%。 :90.5%。
分
15.(14 )
答案: 增大接触面积 加快反应速率 使反应更充分 分
(1) , , (2 )
分 分
(2)+3(2 ) 2CuS2+16NH3·H2O+7O2 2[Cu(NH3)4](OH)2+4(NH4)2SO4+10H2O(2 )
答案 第 页(共 页)
2 5将 3+还原成 2+ 以免在生成 的同时生成 沉淀 分
(3) Fe Fe , BiOCl Fe(OH)3 (2 )
温度升高 挥发加快 且 3+水解程度增大 分
(4) HCl , Bi (2 )
3+ - 2- 分
(5)Bi +Cl +CO3 BiOCl↓+CO2↑(2 )
bV
130.25 分
(6) a (2 )
解析: 粉碎铋精矿可以增大接触面积 加快反应速率 使反应更充分
(1) , , ;
根据 中 元素的变化 可知 在此过程中也会被氧化得到硫酸根 元素转化为
(2) FeS2 S , CuS2 ,Cu [Cu
根据电子守恒可知 和 的系数比为 再结合元素守恒可得化学方程式为
(NH3)4](OH)2, CuS2 O2 2 ∶ 7,
2CuS2+16NH3·H2O+7O2 2[Cu(NH3)4](OH)2+4(NH4)2SO4+10H2O;
盐酸羟胺在 酸浸还原 过程中使用 在 值为 时开始沉淀 而后续流程为了得到
(3) “ ” ,Fe(OH)3 pH 2.7 ,
需要将 调制约为 若 元素为 价 则该过程中会产生 沉淀 而稀盐酸 稀硫酸都
BiOCl, pH 3, Fe +3 , Fe(OH)3 , 、
不能还原 3+ 所以盐酸羟胺在反应中的作用为将 3+还原成 2+ 以免在生成 的同时生成
Fe , Fe Fe , BiOCl
沉淀
Fe(OH)3 ;
酸浸还原 过程中浸出铋 根据图示可知 在温度接近 时 的浸出率最高 此后温度升高
(4)“ ” , : 40 ℃ Bi , ,
浸出率反而降低 主要是由于温度升高 挥发加快 且温度升高使 3+水解程度也增大 最终导致铋的
, ,HCl , Bi ,
浸出率随温度的升高而降低
;
沉铋 过程中 有气体放出 沉铋 的主要化学反应的方程式为
(5)“ ” , 。 “ ” BiCl3+Na2CO3 BiOCl↓+
离子方程式为 3+ - - -
2NaCl+CO2↑, Bi +Cl +CO3 BiOCl↓+2Cl +CO2↑;
由 原 子 守 恒 可 知 存 在 则 产 品 中 的 质 量 分 数 为
(6) BiOCl ~ AgCl ~ AgNO3, BiOCl
b V -3 100.0 mL
mol/L× ×10 L× ×260.5 g/mol b
20.0 mL 130.25 V
a ×100%= a %。
g
分
16.(14 )
答案: 分
(1)-75(2 )
-1 -1 分 分 c 分
(2)①0.125 mol·L ·min (2 ) ②57.6(2 ) ③ (2 )
为放热反应 而 为吸热反应 温度升高 反应逆向移动 而 正向移动 时 为主
(3)Ⅰ , Ⅱ , Ⅰ , Ⅱ ,300~500 ℃ Ⅰ
要变化因素 而 时 为主要变化因素 分 甲醇选择性先升高是由于催化剂随温度升高
, 500~100 ℃ ,Ⅱ (2 )
活性提高 催化剂选择性提高 后下降说明随温度继续升高 催化剂失活 选择性降低 分
, , , , ,(2 )
- - 分
(4)3CO2+2e + H2O CO+ 2HCO3 (2 )
解析: 依据图像可知 H -1
(1) ,CO2(g)+2H2(g) CH3OH(g) Δ 1=-116 kJ·mol ;CO2(g)+H2(g) CO(g)+
的 H -1 故 的 H -1
H2O(g) Δ 2=+41 kJ·mol , CO2(g)+3H2(g) CH3OH(g)+H2O(g) Δ =-75 kJ·mol
根据原子守恒 所有 均在甲醇和水中 前 中甲醇中含 原子共 水中含 原子
(2)① , H , 10 min H 1.6 mol, H
共消耗 故反应速率为 -1 -1 已达到平衡 根据原子守恒可
0.9 mol, H21.25 mol, 0.125 mol·L ·min ;②60 min ,
知 平衡时 和 故该反应的平衡常数K 是
, 0.1 mol CO2、0.5 mol H2、0.8 mol CH3OH 0.9 mol H2O, =57.6;③Ⅰ
气体分子数减小的反应 而 是气体分子数不变的反应 故将容器的容积压缩到原来的一半 反应正向
, Ⅱ , ,Ⅰ
移动 而 平衡不移动 故n 减小 根据勒夏特列原理 c 增大 a错误 反应正逆反应速率均加
, Ⅱ , (H2) , , (H2) , ;Ⅰ
c
快 b错误 的物质的量增加 正确 原平衡时 (H2O) 重新平衡时 甲醇和水等物质
, ;CH3OH ,c ; ,c = 1.125, ,
(CH3OH)
c
的量增加 且甲醇和水处于同一容器中 体积相等 故 (H2O) 比值减少 错误 故答案选
, , , c ,d , c。
(CH3OH)
由表可知 平衡转化率先降低后升高 为放热反应 而 为吸热反应 温度升高 反应逆向移
(3) ,CO2 ,Ⅰ , Ⅱ , Ⅰ
动 而 正向移动 时 为主要变化因素 而 时 为主要变化因素 甲醇选择性
, Ⅱ ,300~500 ℃ Ⅰ , 500~100 ℃ ,Ⅱ ;
先升高是由于催化剂随温度升高活性提高 催化剂选择性提高 后下降说明随温度继续升高 催化剂失
, , ,
活 选择性降低 根据电池示意图可知 为负极 为正极 故正极反应为
-
, 。 (4) ,Zn ,Au , 3CO +2e + H2O
答案 第 页(共 页)
3 5。
分
17.(15 )
3d
答案: 分 分
(1)4s(1 ) ↑ ↑ ↑ ↑ ↑(1 )
3 分 小 分 中含有 对孤电子对 而 + 中孤电子对为 孤电子对排斥力大于成
(2)sp (1 ) (1 ) NH3 1 , NH4 0,
键电子对 故 中键角比 + 中键角小 分
, NH3 NH4 。 (2 )
分
(3)CD(2 )
分 或碳 原子 分
(4)5(1 ) C ( )(1 )
分
(5)O>N>C>H>Fe(2 )
3
分 238 7 分
(6)(1/2,0,1/2)(1 ) N ×10 (2 )
A×d
解析: 的核外电子排布式为 6 2 失去两个电子成为 2+时是失去 轨道电子 3+价层电
(1)Fe [Ar]3d 4s , Fe 4s ,Fe
3d
子排布图为
↑ ↑ ↑ ↑ ↑。
中 的杂化类型是 3 杂化 和 + 中 均为 3 杂化 其夹角的大小与孤电子对数有关
(2)NH3 N sp ,NH3 NH4 N sp , ,
孤电子对数越多成键夹角就越小
。
+ 中含有共价键与配位键 中含有共价键与配位键
(3)NH4 ,CO 。
羰基铁粉 中铁元素的配位数是 配位原子为 原子
(4) [Fe(CO)5] 5, C 。
根据电负性大小顺序可以判断
(5) O>N>C>H>Fe。
根据晶胞结构 点的原子坐标为 可以判断 点的原子的坐标为 根据晶
(6) ,Fe1 (0,0,0), Fe2 (1/2,0,1/2);
3
胞结构 可以判断晶胞中含有 个 和 个 原子 根据密度 56×4+14 计算出 238 7
, 4 Fe 1 N , d= 3 N -21 , a= N ×10
a × A×10 A×d
nm。
分
18.(15 )
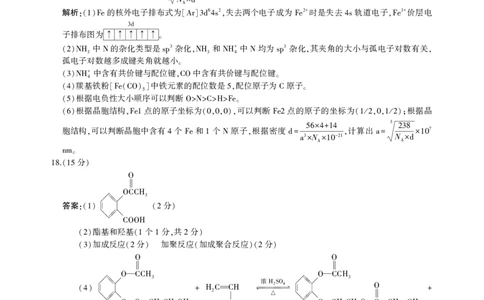
答案:
(1)
答案 第 页(共 页)
4 5
O
OCCH3
分
(2 )
COOH
酯基和羟基 个 分 共 分
(2) (1 1 , 2 )
加成反应 分 加聚反应 加成聚合反应 分
(3) (2 ) ( )(2 )
(4)
O
O CCH3
C
O
浓
H2SO4
+ H2CCH
△
O—CH2CH2OH COOH
O
O CCH3
C
O
O
CH2CH2O C
+
CHCH2
分
H2O(2 )
(5)
O CH
O
O
CH2OCH
-
CO+ 2HCO3
分
(2 )(6)
+
HCN H2O/H
CH2CH2 →CH3CH2CN →CH3CH2COOH O
浓
H2SO4
→CH3CH2 C
△
答案 第 页(共 页)
5 5
O
O—CH2CH2O O
O O CH2CH3
CH3CH2COOH
H2C CH2 一定条件 → CH3CH2C
O—CH2CH2OH
分
(3 )
解析: 根据 的结构和反应条件可推出 为
(1) A B
O
OCCH3
;
COOH
的结构简式为
(2)C
O
O CCH3
C
O
含氧官能团分别为酯基和羟基
, ;
O—CH2CH2OH
为加成反应 的反应属于加聚反应
(3)D→E ,G→H ;
是由 含有羟基 和 含有羧基 进行酯化反应得到 反应方程式见答案
(4)G C( ) F( ) , ;
有机物 是阿司匹林的同分异构体 核磁共振氢谱为五组峰 峰面积比为 说明
(5) M , , 2 ∶ 2 ∶ 2 ∶ 1 ∶ 1,
含有两个取代基 且处于对位 取代基含有亚甲基 另外有机物 只含 中官能团 能够发生银镜反应
, ,1 ; M 1 ,
和水解反应 且水解产物只有两种 说明两个取代基末端均为甲酸酯型 故答案为
, , , :
O CH
O
O
CH2OCH
设计合成路线 根据题目已知和上述合成路线 可利用逆推法分析得到上一步原料为
(6) , , ;
O
和
CH3CH2COOH CH3CH2 C
O
O CH2CH2O C
进一步可推知上一步物质为
CH2CH3 , CH3CH2CN
O
和 进而可完成全部合成路线
H2C CH2 , 。