文档内容
万州二中 2023 年高 2023 届 1 月质量检测
化学试题
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选
项中,只有一项是符合题目要求的。
1.用N 表示阿伏加德罗常数,下列说法正确的是
A
A.摩尔是一个基本物理量 B.含有2N 个氢原子的水,其物质的量为1 mol
A
C.0.5 mol氧气所含氧元素为N D.2 mol NaCl中含离子数2N
A A
2.下列实验合理的是
A.用新制氢氧化铜悬浊液(必要时可加热)鉴别甲酸与乙酸
B.用澄清石灰水鉴别SO 与CO
2 2
C.用淀粉-KI试纸鉴别碘水与FeCl 溶液
3
D.用湿润的pH试纸测定CHCOONa的pH
3
3.下列关于有机化合物的叙述正确的是
A.有机物 和氢气加成后的产物的一氯取代物有3种
B. 表示苯的分子结构,其中含有碳碳双键,因此苯的性质跟乙烯相同
C.乙烯使溴水褪色和苯与溴水混合振荡后水层变为无色的原理相同
D. 只有一种结构,说明甲烷是正四面体结构而不是平面正方形结构
4.下图是合成高分子材料Ⅰ和部分物质转化的过程示意。已知:G、H和I均含有酯基,
下列说法正确的是
A.HC=CHCOOH存在顺反异构 B.G合成高分子材料I是缩聚反应
2
C.F是CHCHCOOH D.G发生氧化反应生成H
3 2
5.下列说法不正确的是
A. 和 是氧元素的同素异形体
B.干燥的 固体不导电,所以 不是电解质
C. 是碱性氧化物,能与酸反应生成盐和水
D. 在水溶液中的电离方程式为
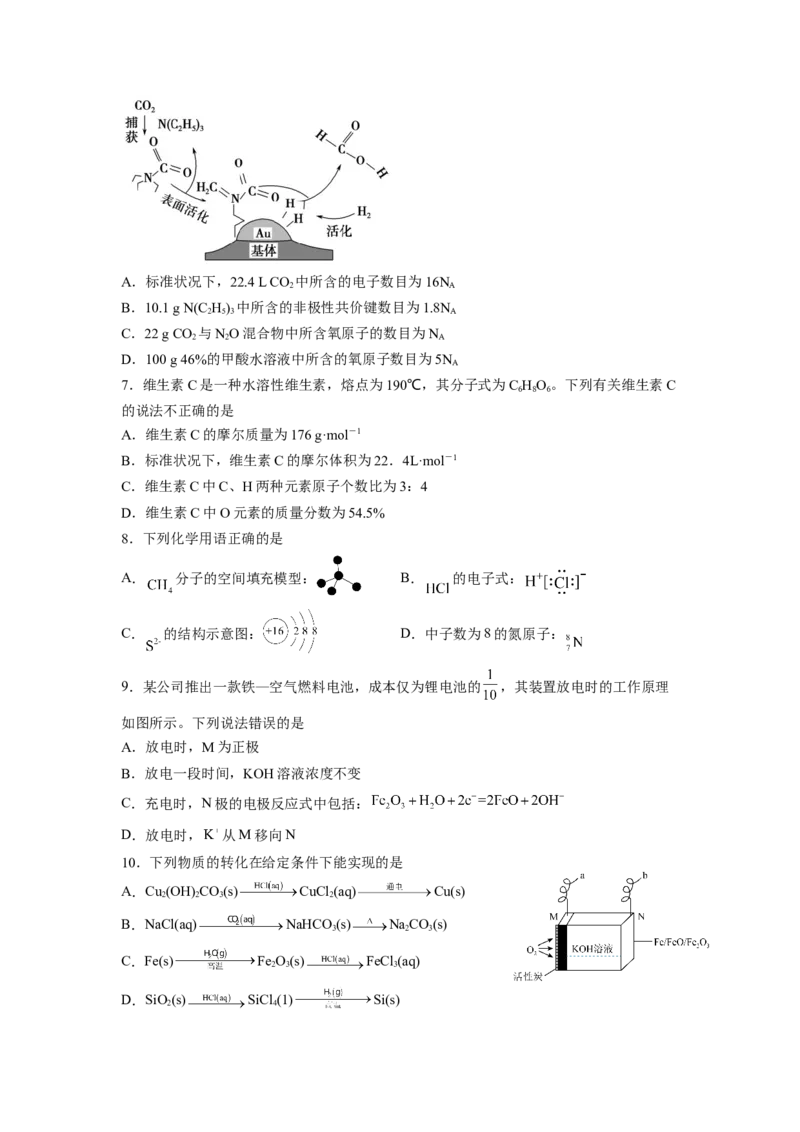
6.为实现“双碳”目标,某科研小组设计捕获二氧化碳生成甲酸的过程如图所示。下列说
法正确的是(N 为阿伏加德罗常数的值)
AA.标准状况下,22.4 L CO 中所含的电子数目为16N
2 A
B.10.1 g N(C H) 中所含的非极性共价键数目为1.8N
2 5 3 A
C.22 g CO 与NO混合物中所含氧原子的数目为N
2 2 A
D.100 g 46%的甲酸水溶液中所含的氧原子数目为5N
A
7.维生素C是一种水溶性维生素,熔点为190℃,其分子式为C HO。下列有关维生素C
6 8 6
的说法不正确的是
A.维生素C的摩尔质量为176 g·mol-1
B.标准状况下,维生素C的摩尔体积为22.4L·mol-1
C.维生素C中C、H两种元素原子个数比为3:4
D.维生素C中O元素的质量分数为54.5%
8.下列化学用语正确的是
A. 分子的空间填充模型: B. 的电子式:
C. 的结构示意图: D.中子数为8的氮原子:
9.某公司推出一款铁—空气燃料电池,成本仅为锂电池的 ,其装置放电时的工作原理
如图所示。下列说法错误的是
A.放电时,M为正极
B.放电一段时间,KOH溶液浓度不变
C.充电时,N极的电极反应式中包括:
D.放电时, 从M移向N
10.下列物质的转化在给定条件下能实现的是
A.Cu (OH) CO(s) CuCl (aq) Cu(s)
2 2 3 2
B.NaCl(aq) NaHCO (s) NaCO(s)
3 2 3
C.Fe(s) Fe O(s) FeCl (aq)
2 3 3
D.SiO(s) SiCl (1) Si(s)
2 411. 在水溶液中与HCHO发生如下反应:
。下列说法正确的是
A.HCHO的分子构型是是三角锥形
B.基态 的电子排布式为
C. 中与 形成配位键的原子是H
D.1mol 中所含 键的数目是6mol
12.有机物分子中原子(或原子团)间的相互影响会导致物质化学性质的不同。下列各项事
实不能说明上述观点的是
A.苯不能和溴水反应,苯酚能和溴水反应
B.苯不能使酸性高锰酸钾溶液褪色,甲苯能使酸性高锰酸钾溶液褪色
C.乙醇不能和氢氧化钠溶液反应,苯酚能和氢氧化钠溶液反应
D.苯不能使溴的四氯化碳溶液褪色,苯乙烯能使溴的四氯化碳溶液褪色
13.下列实验对应的离子方程式书写正确的是
A.将 溶液滴入酸性 溶液:
B.向 溶液中滴加少量 溶液:
C.向 溶液滴入过量 溶液:
D.向明矾溶液中加入 溶液至生成沉淀的物质的量最多:
14. 由于核外有空的d轨道,可与一些配体形成配位数为6的配离子。某同学将淡紫
色的 晶体溶于水后再依次加KSCN和NaF,发现溶液出现下列变化:
已知: 为浅紫色, 为红色, 为无色。
下列说法错误的是
A. 晶体溶于水后溶液不是浅紫色而是黄色,是因为 水解生成
所致B. 与 形成配位键时,S原子提供孤电子对
C.溶液Ⅱ加NaF后溶液由红色变为无色,说明 与 配位键强度不及 与 配
位键强度
D.焰色试验中可用无锈铁丝替代铂丝,说明铁灼烧时无焰色且不会产生发射光谱
二、非选择题:共58分。
15.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化
合物相关的问题:
(1)下列有关NH 的说法中,不正确的是___________(双选,填标号)。
3
A.工业合成NH 需要在高温高压催化剂下进行
3
B.NH 可用来生产碳铵和尿素等化肥
3
C.NH 可用浓硫酸或无水氯化钙干燥
3
D.NH 受热易分解,须置于冷暗处保存
3
(2)NH 易溶于水,标准状况下,用充满NH 的烧瓶做喷泉实验,水充满整个烧瓶后所形成
3 3
溶液的物质的量浓度为___________mol·L-1。
(3)氨气燃烧的化学方程式为___________。
(4)HNO 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常
3
温下能使铝、铁钝化,说明浓硝酸具有很强的___________性。
(5)“吸收塔” 尾部会有含NO、NO 等氮氧化物的尾气排出,为消除它们对环境的破坏作
2
用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO 的反应原理为NaCO+2NO =NaNO +___________+
2 2 3 2 3
CO(请填写完成化学方程式)。
2
②氨转化法。已知7 mol氨恰好能将含NO和NO 共6 mol 的混合气体完全转化为N 则混
2 2
合气体中NO和NO 的物质的量之比为___________,若用通式NO 表示氮氧化物,则每摩
2 x
尔氨可将___________mol的NO 转化为N
x 2。
16.I.为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是_______,过一会儿,
溶液的颜色褪去,起作用的微粒是_______。
II.某研究小组为了制备84消毒液(主要成分为NaClO)设计了如图装置。并查阅到下列资料:
“氯气与水的反应是放热反应,在加热条件下氯气与碱液发生如下反应:3Cl+6NaOH
2
5NaCl+NaClO +3H O”。回答下列问题:
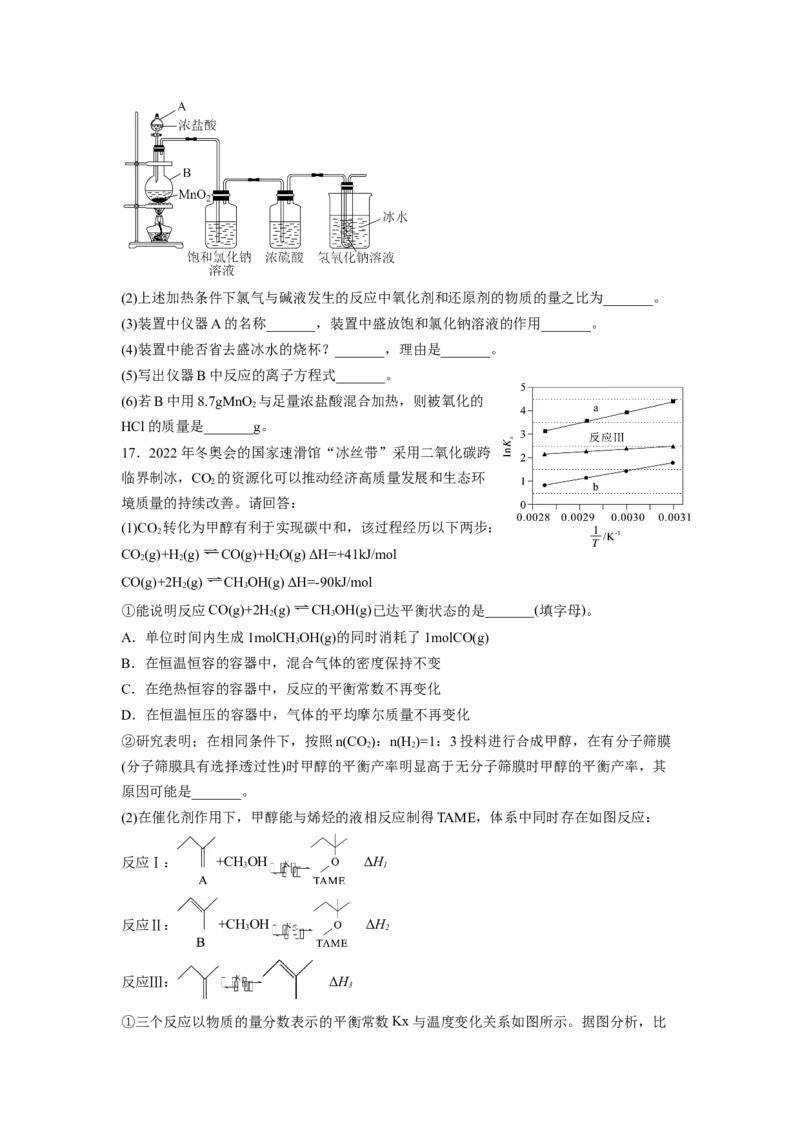
3 2(2)上述加热条件下氯气与碱液发生的反应中氧化剂和还原剂的物质的量之比为_______。
(3)装置中仪器A的名称_______,装置中盛放饱和氯化钠溶液的作用_______。
(4)装置中能否省去盛冰水的烧杯?_______,理由是_______。
(5)写出仪器B中反应的离子方程式_______。
(6)若B中用8.7gMnO 与足量浓盐酸混合加热,则被氧化的
2
HCl的质量是_______g。
17.2022年冬奥会的国家速滑馆“冰丝带”采用二氧化碳跨
临界制冰,CO 的资源化可以推动经济高质量发展和生态环
2
境质量的持续改善。请回答:
(1)CO 转化为甲醇有利于实现碳中和,该过程经历以下两步:
2
CO(g)+H(g) CO(g)+HO(g) ΔH=+41kJ/mol
2 2 2
CO(g)+2H(g) CHOH(g) ΔH=-90kJ/mol
2 3
①能说明反应CO(g)+2H(g) CHOH(g)已达平衡状态的是_______(填字母)。
2 3
A.单位时间内生成1molCH OH(g)的同时消耗了1molCO(g)
3
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,气体的平均摩尔质量不再变化
②研究表明;在相同条件下,按照n(CO):n(H )=1:3投料进行合成甲醇,在有分子筛膜
2 2
(分子筛膜具有选择透过性)时甲醇的平衡产率明显高于无分子筛膜时甲醇的平衡产率,其
原因可能是_______。
(2)在催化剂作用下,甲醇能与烯烃的液相反应制得TAME,体系中同时存在如图反应:
反应Ⅰ: +CH OH ΔH
3 1
反应Ⅱ: +CH OH ΔH
3 2
反应Ⅲ: ΔH
3
①三个反应以物质的量分数表示的平衡常数Kx与温度变化关系如图所示。据图分析,比较A、B稳定性:_______, 的数值范围是_______。
A.<-1 B.-1~0 C.0~1 D.>1
②向某反应容器中加入1.0molTAME,控制温度为353K,测得TAME的平衡转化率为。
已知反应Ⅲ的平衡常数Kx(Ⅲ)=9.0,则反应I的平衡常数Kx(I)=_______。同温同压下,再
向该容器中注入惰性溶剂四氢呋喃稀释,达到平衡时,A与CHOH物质的量浓度之比
3
c(A):c(CHOH)=_______。
3
(3)工业上还可采用CHOH CO+2H 的原理来制取高纯度的CO和H。有科学家研究在钯
3 2 2
基催化剂表面上利用甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下
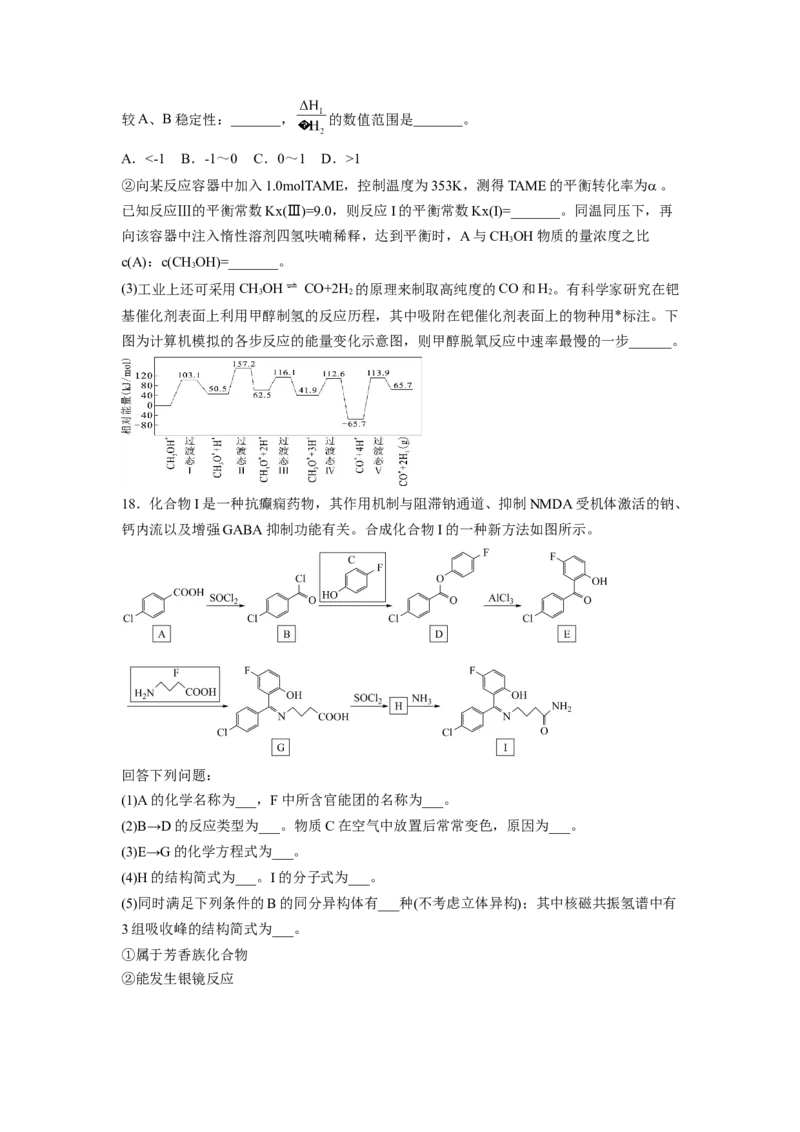
图为计算机模拟的各步反应的能量变化示意图,则甲醇脱氧反应中速率最慢的一步______。
18.化合物I是一种抗癫痫药物,其作用机制与阻滞钠通道、抑制NMDA受机体激活的钠、
钙内流以及增强GABA抑制功能有关。合成化合物I的一种新方法如图所示。
回答下列问题:
(1)A的化学名称为___,F中所含官能团的名称为___。
(2)B→D的反应类型为___。物质C在空气中放置后常常变色,原因为___。
(3)E→G的化学方程式为___。
(4)H的结构简式为___。I的分子式为___。
(5)同时满足下列条件的B的同分异构体有___种(不考虑立体异构);其中核磁共振氢谱中有
3组吸收峰的结构简式为___。
①属于芳香族化合物
②能发生银镜反应(6)结合题给信息,以 为原料(无机试剂任选),设计制备 的合成路线:___。