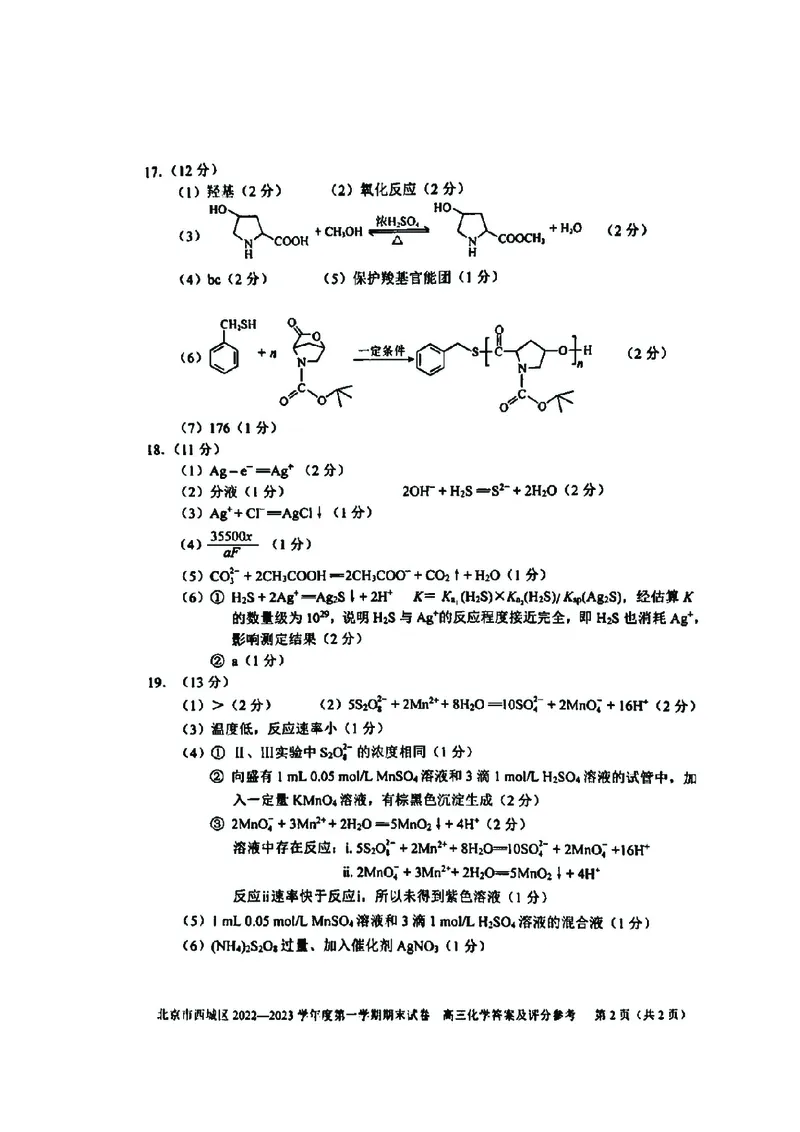
文档内容
北京市西城区 2022—2023 学年度第一学期期末试卷
高三化学
2023.1
本试卷共10页,100分。考试时长90分钟。考生务必将答案答在答题卡上,在试卷上作
答无效。考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Cl 35.5
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的
一项。
1.2022年10月“和合共生——故宫•国博藏文物联展”中的展品《御制月令七十二候诗》
彩色墨展现了中国古代文化的魅力。下列关于制墨材料主要成分性质的说法不正确的是
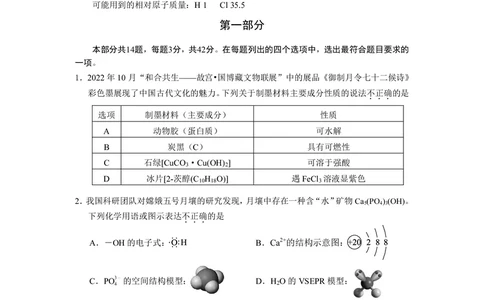
...
选项 制墨材料(主要成分) 性质
A 动物胶(蛋白质) 可水解
B 炭黑(C) 具有可燃性
C 石绿[CuCO ·Cu(OH) ] 可溶于强酸
3 2
D 冰片[2-茨醇(C H O)] 遇FeCl 溶液显紫色
10 18 3
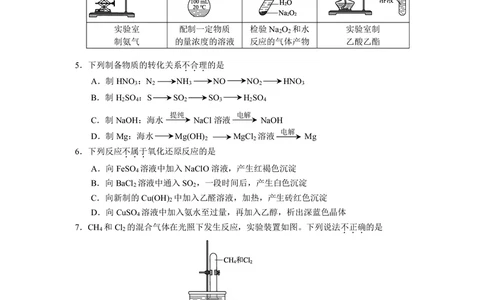
2.我国科研团队对嫦娥五号月壤的研究发现,月壤中存在一种含“水”矿物Ca (PO ) (OH)。
5 4 3
下列化学用语或图示表达不正确的是
...
A.―OH的电子式: B.Ca2+的结构示意图:
C.PO3― 的空间结构模型: D.H O的VSEPR模型:
4 2
3.解释下列事实所用的化学用语不正确的是
...
A.酚酞滴入Na CO 溶液中,溶液变红:CO2― + H O HCO― + OH−
2 3 3 2 3
B.铜片放入浓硝酸中,产生红棕色气体:3Cu + 8H+ + 2NO―==3Cu2+ + 2NO↑+ 4H O
3 2
C.钢铁发生吸氧腐蚀,负极反应:Fe – 2e− == Fe2+
D.SO 通入溴水中,溶液褪色:SO + Br + 2H O == H SO + 2HBr
2 2 2 2 2 4
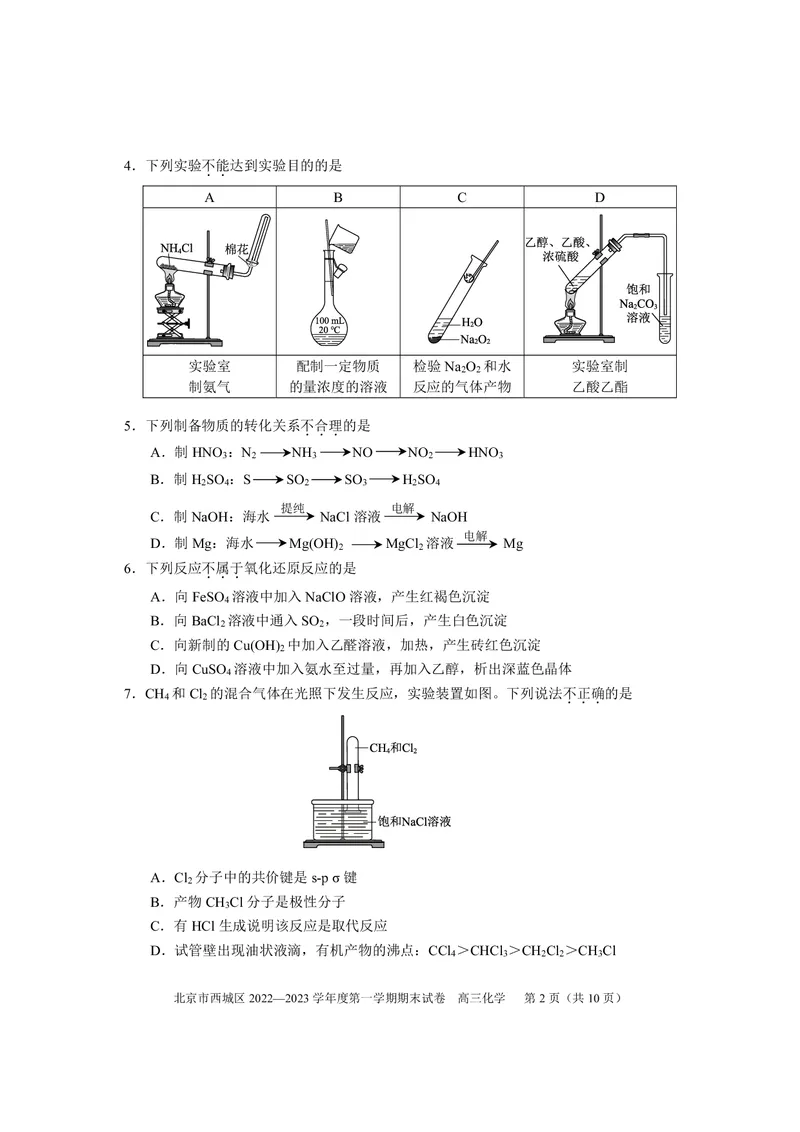
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第1页(共10页)4.下列实验不能达到实验目的的是
..
A B C D
实验室 配制一定物质 检验Na O 和水 实验室制
2 2
制氨气 的量浓度的溶液 反应的气体产物 乙酸乙酯
5.下列制备物质的转化关系不合理的是
...
A.制HNO :N NH NO NO HNO
3 2 3 2 3
B.制H SO :S SO SO H SO
2 4 2 3 2 4
提纯 电解
C.制NaOH:海水 NaCl溶液 NaOH
电解
D.制Mg:海水 Mg(OH) MgCl 溶液 Mg
2 2
6.下列反应不属于氧化还原反应的是
...
A.向FeSO 溶液中加入NaClO溶液,产生红褐色沉淀
4
B.向BaCl 溶液中通入SO ,一段时间后,产生白色沉淀
2 2
C.向新制的Cu(OH) 中加入乙醛溶液,加热,产生砖红色沉淀
2
D.向CuSO 溶液中加入氨水至过量,再加入乙醇,析出深蓝色晶体
4
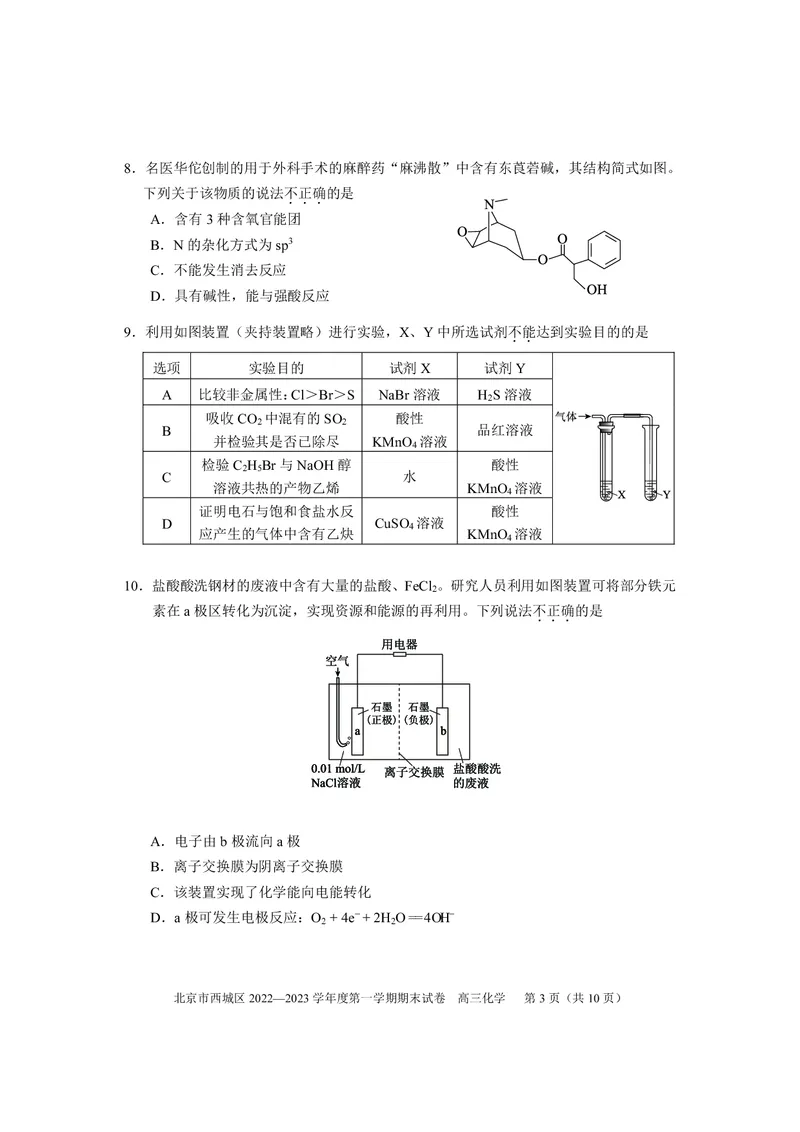
7.CH 和Cl 的混合气体在光照下发生反应,实验装置如图。下列说法不正确的是
4 2 ...
A.Cl 分子中的共价键是s-p σ键
2
B.产物CH Cl分子是极性分子
3
C.有HCl生成说明该反应是取代反应
D.试管壁出现油状液滴,有机产物的沸点:CCl >CHCl >CH Cl >CH Cl
4 3 2 2 3
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第2页(共10页)8.名医华佗创制的用于外科手术的麻醉药“麻沸散”中含有东莨菪碱,其结构简式如图。
下列关于该物质的说法不正确的是
...
A.含有3种含氧官能团
B.N的杂化方式为sp3
C.不能发生消去反应
D.具有碱性,能与强酸反应
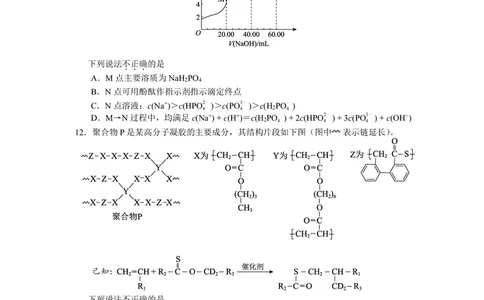
9.利用如图装置(夹持装置略)进行实验,X、Y中所选试剂不能达到实验目的的是
..
选项 实验目的 试剂X 试剂Y
A 比较非金属性:Cl>Br>S NaBr溶液 H S溶液
2
吸收CO 中混有的SO 酸性
2 2
B 品红溶液
并检验其是否已除尽 KMnO 溶液
4
检验C H Br与NaOH醇 酸性
2 5
C 水
溶液共热的产物乙烯 KMnO 溶液
4
证明电石与饱和食盐水反 酸性
D CuSO 溶液
4
应产生的气体中含有乙炔 KMnO 溶液
4
10.盐酸酸洗钢材的废液中含有大量的盐酸、FeCl 。研究人员利用如图装置可将部分铁元
2
素在a极区转化为沉淀,实现资源和能源的再利用。下列说法不正确的是
...
A.电子由b极流向a极
B.离子交换膜为阴离子交换膜
C.该装置实现了化学能向电能转化
D.a极可发生电极反应:O + 4e− + 2H O == 4 OH−
2 2
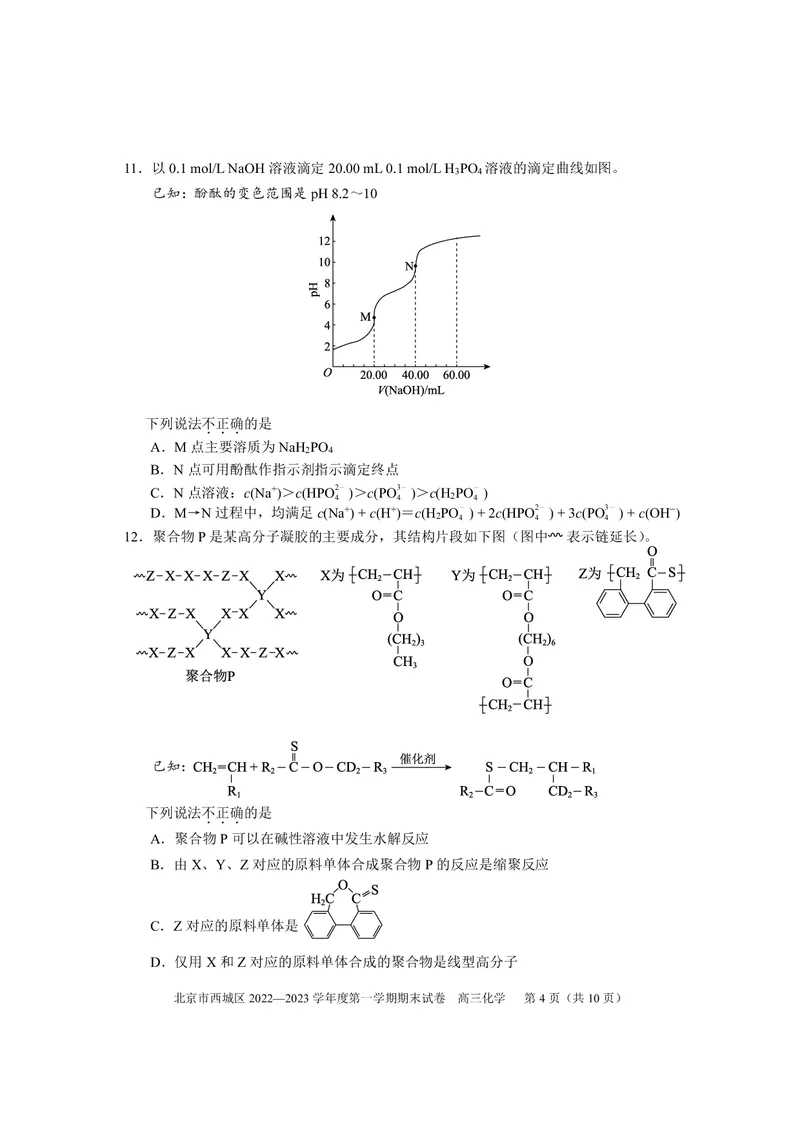
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第3页(共10页)11.以0.1 mol/L NaOH溶液滴定20.00 mL 0.1 mol/L H PO 溶液的滴定曲线如图。
3 4
已知:酚酞的变色范围是pH 8.2~10
下列说法不正确的是
...
A.M点主要溶质为NaH PO
2 4
B.N点可用酚酞作指示剂指示滴定终点
C.N点溶液:c(Na+)>c(HPO2― )>c(PO3― )>c(H PO― )
4 4 2 4
D.M→N过程中,均满足c(Na+) + c(H+)=c(H PO― ) + 2c(HPO2― ) + 3c(PO3― ) + c(OH−)
2 4 4 4
12.聚合物P是某高分子凝胶的主要成分,其结构片段如下图(图中 表示链延长)。
已知:
下列说法不正确的是
...
A.聚合物P可以在碱性溶液中发生水解反应
B.由X、Y、Z对应的原料单体合成聚合物P的反应是缩聚反应
C.Z对应的原料单体是
D.仅用X和Z对应的原料单体合成的聚合物是线型高分子
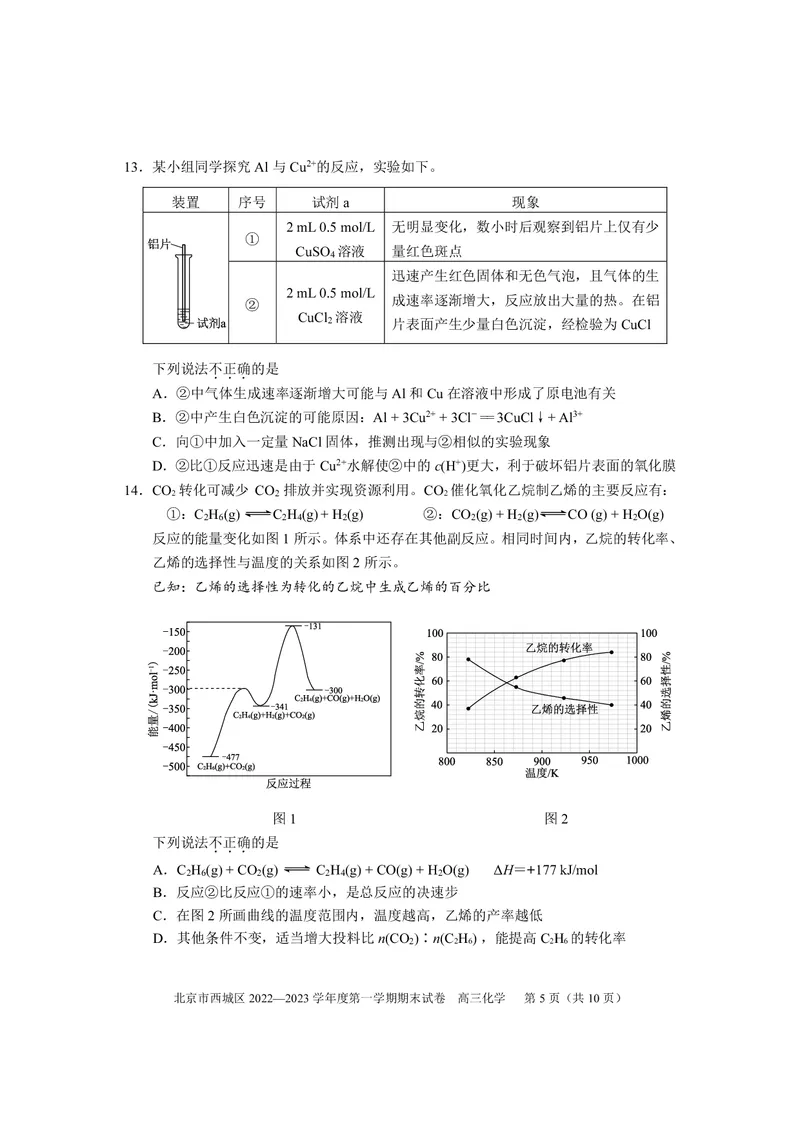
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第4页(共10页)13.某小组同学探究Al与Cu2+的反应,实验如下。
装置 序号 试剂a 现象
2 mL 0.5 mol/L 无明显变化,数小时后观察到铝片上仅有少
①
CuSO 溶液 量红色斑点
4
迅速产生红色固体和无色气泡,且气体的生
2 mL 0.5 mol/L
成速率逐渐增大,反应放出大量的热。在铝
②
CuCl 溶液
2 片表面产生少量白色沉淀,经检验为CuCl
下列说法不正确的是
...
A.②中气体生成速率逐渐增大可能与Al和Cu在溶液中形成了原电池有关
B.②中产生白色沉淀的可能原因:Al + 3Cu2+ + 3Cl− == 3CuCl↓+ Al3+
C.向①中加入一定量NaCl固体,推测出现与②相似的实验现象
D.②比①反应迅速是由于Cu2+水解使②中的c(H+)更大,利于破坏铝片表面的氧化膜
14.CO 转化可减少 CO 排放并实现资源利用。CO 催化氧化乙烷制乙烯的主要反应有:
2 2 2
①:C H (g) C H (g)+ H (g) ②:CO (g) + H (g) CO (g) + H O(g)
2 6 2 4 2 2 2 2
反应的能量变化如图1所示。体系中还存在其他副反应。相同时间内,乙烷的转化率、
乙烯的选择性与温度的关系如图2所示。
已知:乙烯的选择性为转化的乙烷中生成乙烯的百分比
图1 图2
下列说法不正确的是
...
A.C H (g) + CO (g) C H (g) + CO(g) + H O(g) ΔH=+177 kJ/mol
2 6 2 2 4 2
B.反应②比反应①的速率小,是总反应的决速步
C.在图2所画曲线的温度范围内,温度越高,乙烯的产率越低
D.其他条件不变,适当增大投料比n(CO )∶n(CH) ,能提高C H 的转化率
2 2 6 2 6
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第5页(共10页)第二部分
本部分共5题,共58分。
15.(9分)向CoCl 溶液中滴加过量的氨水得到含有[Co(NH ) ]Cl 的溶液。
2 3 6 2
(1)基态Co2+的价层电子排布式为______。
(2)基态Cl−占据的最高能级的电子云轮廓图的形状是______。
(3)O、N、H的电负性由大到小的顺序是______。
(4)下列状态的氮中,电离最外层一个电子所需能量最小的是______(填序号)。
a. b. c.
(5) [Co(NH ) ]Cl 的晶胞结构示意图如下。
3 6 2
① 在下图虚线框内画出[Co(NH ) ]2+中一个NH 的结构式。
3 6 3
② 比较H―N―H键角:NH ______ [Co(NH ) ]2+(填“>”“<”或“=”),
3 3 6
原因是______。
③ 该立方晶胞的边长为a cm,阿伏加德罗常数为N ,[Co(NH ) ]Cl 的摩尔质
A 3 6 2
量为M g/mol,则该晶体的密度为______ g/cm3。
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第6页(共10页)16.(13分)黏土钒矿中,钒以+3价、+4价、+5价的化合物存在,还包括SiO 、Fe O 和
2 2 3
铝硅酸盐(Al O ·SiO )等。采用以下流程可由黏土钒矿制备V O 、Fe O 和硫酸铝
2 3 2 2 5 2 3
铵。
已知:ⅰ. 有机酸性萃取剂HR的萃取原理为:
Mn+(aq) + nHR(org) MR (org) + nH+(aq) org表示有机溶液
n
ⅱ. 酸性溶液中,HR对+4价钒萃取能力强,而对+5价钒的萃取能力较弱
ⅲ. HR能萃取Fe3+而不能萃取Fe2+
(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施有______。
(2)滤渣的主要成分是______。
(3)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因:______。
(4)从平衡移动原理解释加入20% H SO 溶液的作用:______。
2 4
(5)KClO 和VO2+反应生成VO+ 和Cl−的离子方程式是______。
3 2
(6)测定V O 产品的纯度
2 5
称取 V O 产品 a g,先加入硫酸将 V O 转化为 VO+ ,加入指示剂后,用 c mol/L
2 5 2 5 2
(NH ) Fe(SO ) 溶液滴定将 VO+ 转化为VO2+至终点,消耗(NH ) Fe(SO ) 溶液的
4 2 4 2 2 4 2 4 2
体积为V mL。假设杂质不参与反应,则V O 产品中V O 的质量分数是______
2 5 2 5
(V O 的摩尔质量为M g/mol)。
2 5
(7)从无机层获得Fe(OH) 的离子方程式是______。
3
(8)硫酸铝铵固体中含有少量硫酸铵杂质,根据下图的溶解度曲线,进一步提纯硫酸
铝铵的操作是加热溶解、______、洗涤、干燥。
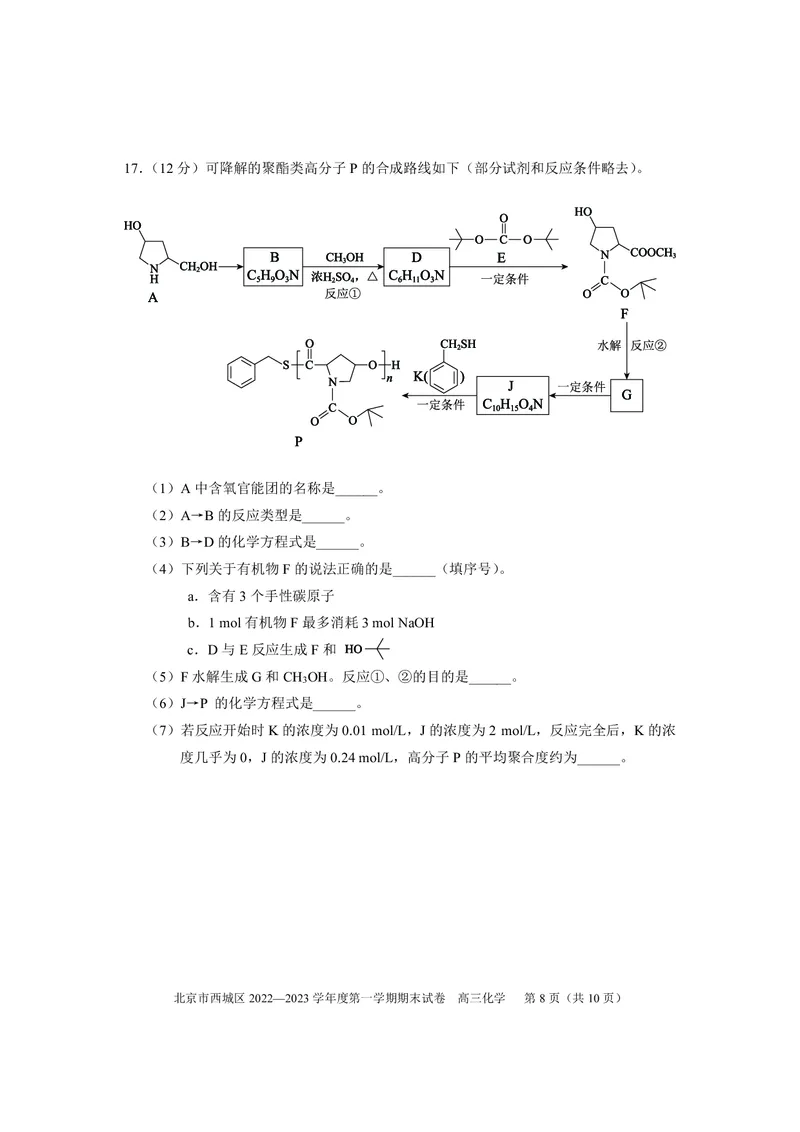
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第7页(共10页)17.(12分)可降解的聚酯类高分子P的合成路线如下(部分试剂和反应条件略去)。
(1)A中含氧官能团的名称是______。
(2)A→B的反应类型是______。
(3)B→D的化学方程式是______。
(4)下列关于有机物F的说法正确的是______(填序号)。
a.含有3个手性碳原子
b.1 mol有机物F最多消耗3 mol NaOH
c.D与E反应生成F和
(5)F水解生成G和CH OH。反应①、②的目的是______。
3
(6)J→P 的化学方程式是______。
(7)若反应开始时K的浓度为0.01 mol/L,J的浓度为2 mol/L,反应完全后,K的浓
度几乎为0,J的浓度为0.24 mol/L,高分子P的平均聚合度约为______。
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第8页(共10页)18.(11分)石油中含有有机氯和无机氯(主要以Cl−的形式存在),还含有少量的硫化氢、
硫酸盐和碳酸盐等。微库仑滴定法可快速测定石油中的有机氯和无机氯的含量。
已知:库仑测氯仪中电解原理示意图如下。检测前,电解质溶液中的c(Ag+)保持定值
时,电解池不工作。待测物质进入电解池后与Ag+反应,测氯仪便立即自动进
行电解到c(Ag+)又回到原定值,测定结束。通过测定电解消耗的电量可以求出
石油中氯的含量。
(1)库仑测氯仪电解池中的阳极反应是______。
Ⅰ.石油中有机氯含量的测定
(2)用过量 KOH 溶液和水除去石油样品中的 H S 和无机盐,再通过______操作
2
分离得到处理后的石油样品。KOH溶液除去H S的离子方程式是______。
2
(3)经处理后的石油样品在高温、富氧条件下燃烧,有机氯转化为 HCl。在库仑
测氯仪中,待测气体通入电解池后与Ag+反应的离子方程式是______。
(4)石油样品为a g,电解消耗的电量为x库仑,样品中有机氯的含量(按含氯元
素计)为______mg/g。
已知:电解中转移1 mol 电子所消耗的电量为F库仑
Ⅱ.石油中无机氯含量的测定
在极性溶剂存在下加热石油样品,再用水提取其中的无机盐。含盐的待测液体注
入库仑测氯仪进行测定。
已知:ⅰ. 样品中存在的CO2― 和SO2― 不影响测定结果
3 4
ⅱ. K (H S)=1.1×10−7 K (H S)=1.3×10−13 K (Ag S)=6.3×10−50
a 2 a 2 sp 2
1 2
(5)用离子方程式解释CO2― 不影响测定结果的原因:______。
3
(6)石油样品中存在的H S会影响测定结果。
2
① 通过估算说明H S的存在会影响测定结果:______。
2
② 待测液体注入库仑测氯仪前,可加入______(填序号)以消除H S的影响。
2
a.H O 溶液 b.NaOH溶液 c.碘水
2 2
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第9页(共10页)19.(13分)资料显示,酸性介质中,S O2― 和Mn2+可反应转化为MnO― 和SO2― 。小组探
2 8 4 4
究利用该反应测定Mn2+含量的条件。
实验 序号 物质a 实验现象
0.002 mol/L
Ⅰ 无明显变化
MnSO 溶液
4
0.002 mol/L
Ⅱ 加热至沸腾,5 min后溶液变为紫色
MnSO 溶液
4
0.05 mol/L 加热至沸腾,生成大量棕黑色沉淀,
Ⅲ
MnSO 溶液 静置,上层溶液未变紫色
4
(1)根据实验Ⅱ的现象,氧化性:S O2― ______ MnO― (填“>”或“<”)。
2 8 4
(2)实验Ⅱ中反应的离子方程式是______。
(3)实验Ⅰ的条件下S O2― 能将Mn2+氧化为MnO― ,推测实验Ⅰ未出现紫色的原因:
2 8 4
______。
(4)经检验,棕黑色沉淀为MnO ,针对实验Ⅲ中的现象,提出以下假设:
2
假设1:S O2― 的浓度较低,不足以将Mn2+氧化为MnO―
2 8 4
假设2:溶液中存在还原剂Mn2+,将生成的MnO― 还原为MnO
4 2
① 甲同学分析上述实验设计,认为假设1不成立,理由是______。
② 针对假设2,乙同学设计实验Ⅳ证实了推测合理。
请写出实验操作和现象:______。
③ 实验Ⅲ中生成MnO 的离子方程式是______,从化学反应速率的角度分析实验
2
Ⅲ未得到紫色溶液的原因:______。
(5)资料表明Ag+可作为Mn2+和S O2― 反应转化为MnO― 的催化剂。丙同学设计实验
2 8 4
Ⅲ的对比实验进行了证实。向______中滴加2 滴 0.1 mol/L AgNO 溶液,再加入
3
0.0005 mol (NH ) S O 固体,加热至沸腾,观察到溶液变为紫色。
4 2 2 8
(6)根据上述实验,要利用(NH ) S O 将 Mn2+转化为 MnO― 的反应来快速测定 Mn2+
4 2 2 8 4
的含量,应控制的反应条件有:加热至沸腾、______。
北京市西城区2022—2023学年度第一学期期末试卷 高三化学 第10页(共10页)