文档内容
微专题21 二氧化硫性质四重性探究
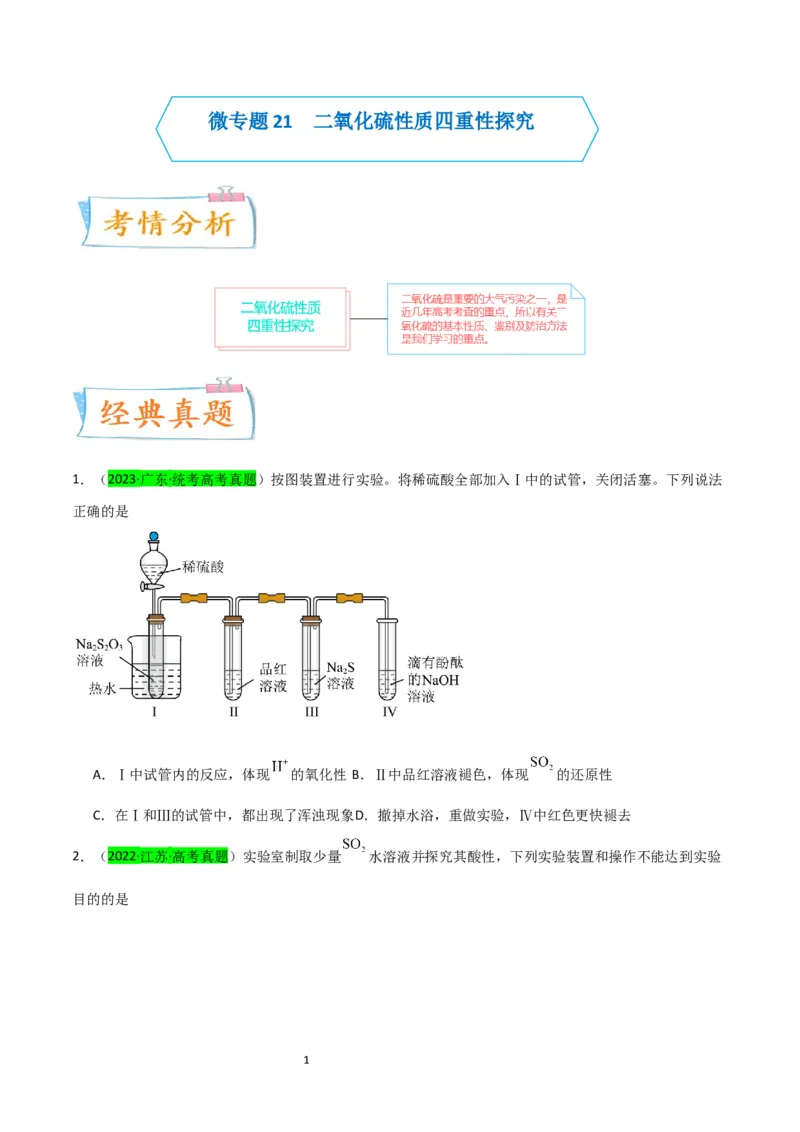
1.(2023·广东·统考高考真题)按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法
正确的是
A.Ⅰ中试管内的反应,体现 的氧化性 B.Ⅱ中品红溶液褪色,体现 的还原性
C.在Ⅰ和Ⅲ的试管中,都出现了浑浊现象D.撤掉水浴,重做实验,Ⅳ中红色更快褪去
2.(2022·江苏·高考真题)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验
目的的是
1A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
1. SO 和CO 的鉴别方法
2 2
2.检验SO 和CO 同时存在的一般流程
2 2
SO 和CO 都可使澄清的石灰水变浑浊,检验二者同时存在的一般流程为,
2 2
流程
设计
选用 品红 酸性KMnO 品红 澄清的
4
试剂 溶液 溶液 溶液 石灰水
预期现象 褪色 褪色 不褪色 变浑浊
[注意] 有时为了简化装置,可将除去SO 和检验SO 是否除尽合并为一个装置,用较浓的酸性 KMnO 溶
2 2 4
液,现象是酸性KMnO 溶液颜色变浅但不褪成无色。
4
3.除去CO 中的SO 气体
2 2
将混合气体通入酸性KMnO 溶液或溴水中,也可通入饱和NaHCO 溶液(H SO 的酸性大于H CO )。
4 3 2 3 2 3
4.四种常见的SO 尾气处理方法
2
方法一:钙基固硫法
2为防治酸雨,工业上常用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、O 共同反应生成硫酸钙,从
2
而使硫转移到煤渣中,反应原理为CaO+SO =====CaSO ,2CaSO +O =====2CaSO ,总反应的化学方程式
2 3 3 2 4
为 2CaO+2SO +O =====2CaSO 。
2 2 4
方法二:氨水脱硫法
该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO 直接接触吸收SO ,其反应的化学方程式为2NH +
2 2 3
SO +H O===(NH ) SO ,2(NH ) SO +O ===2(NH ) SO (或生成NH HSO ,然后进一步氧化)。
2 2 4 2 3 4 2 3 2 4 2 4 4 3
方法三:钠、碱脱硫法
钠、碱脱硫法是用 NaOH/Na CO 吸收烟气中的 SO ,得到Na SO 和NaHSO ,发生反应的化学方程式为
2 3 2 2 3 3
2NaOH+SO ===Na SO +H O,Na CO +SO ===Na SO +CO ,Na SO +SO +H O===2NaHSO 。
2 2 3 2 2 3 2 2 3 2 2 3 2 2 3
方法四:双碱脱硫法
先利用烧碱吸收SO ,再利用熟石灰浆液进行再生,再生后的NaOH可循环使用,化学反应原理为
2
①吸收反应:2NaOH+SO ===Na SO +H O,2Na SO +O ===2Na SO 。
2 2 3 2 2 3 2 2 4
②再生反应:Na SO +Ca(OH) ===CaSO ↓+2NaOH,Na SO +Ca(OH) ===CaSO ↓+2NaOH。
2 3 2 3 2 4 2 4
二氧化硫的基本性质有以下四个方面:
1.酸性氧化物的通性 2.氧化性 3.还原性 4.漂白性
二氧化硫(SO )
2
(1)物理性质
颜色 气味 状态 水溶性 毒性
易溶,1体积水溶解约
色 气味 气体 毒
体积SO
2
(2)化学性质
3②氧化性(如与H S溶液反应):(生成淡黄色沉淀)
2
④漂白性:SO 可使品红溶液,加热后,溶液由色变为色。
2
SO 与HClO、H O 、Na O 、O 、活性炭漂白原理的比较
2 2 2 2 2 3
HClO、H O 、
SO 2 2
物质 活性炭
2 Na O 、O
2 2 3
漂白 与有色物质结合生成无色 将有色物质氧化为
吸附有色物质
原理 物质 无色物质
变化
化学变化 化学变化 物理变化
类型
是否 可逆,加热或久置后恢复 不可逆,加热或久
置后不恢复原来颜 —
可逆 原来颜色 色
漂白 有色的有机物,不能漂白 有色的有机物和指
有机色质
对象 指示剂 示剂
41.(2023·北京·统考高考真题)回收利用工业废气中的 和 ,实验原理示意图如下。
下列说法不正确的是
A.废气中 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
C.装置a中溶液的作用是吸收废气中的 和
D.装置 中的总反应为
2.(2023·浙江·统考高考真题)下列反应的离子方程式正确的是
A.碘化亚铁溶液与等物质的量的氯气:
B.向次氯酸钙溶液通入足量二氧化碳:
C.铜与稀硝酸:
D.向硫化钠溶液通入足量二氧化硫:
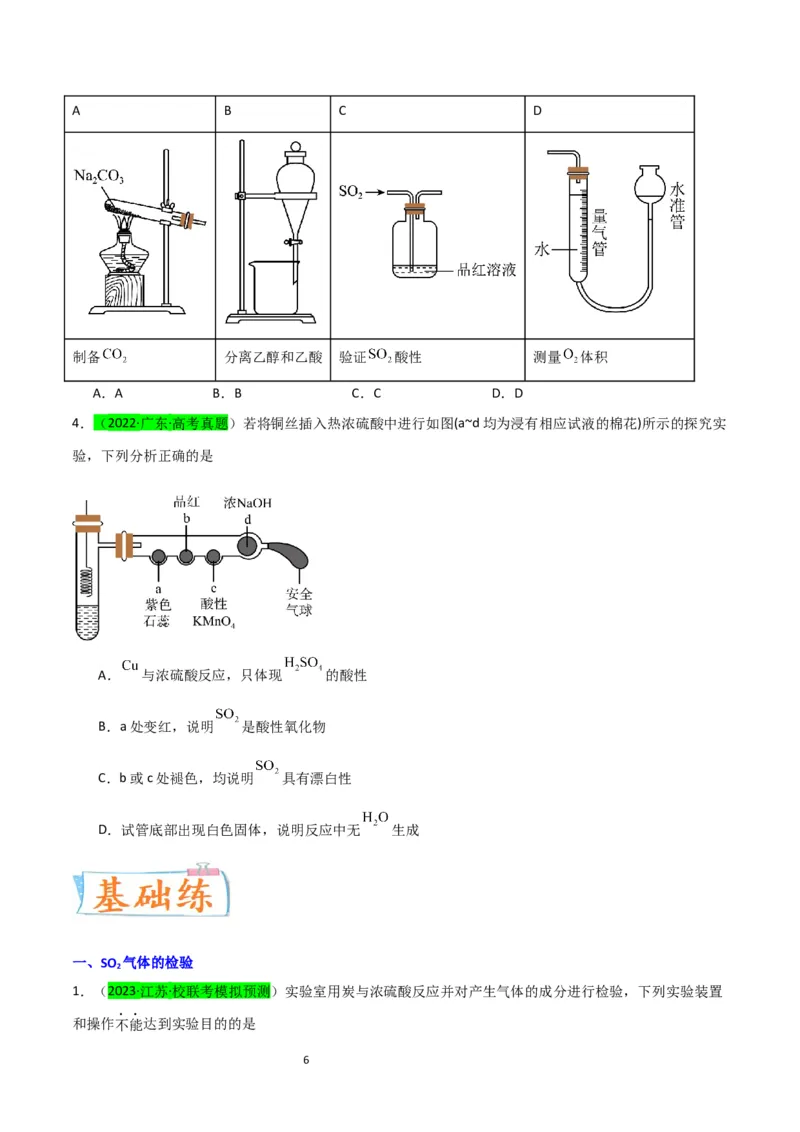
3.(2023·全国·统考高考真题)下列装置可以用于相应实验的是
5A B C D
制备 分离乙醇和乙酸 验证 酸性 测量 体积
A.A B.B C.C D.D
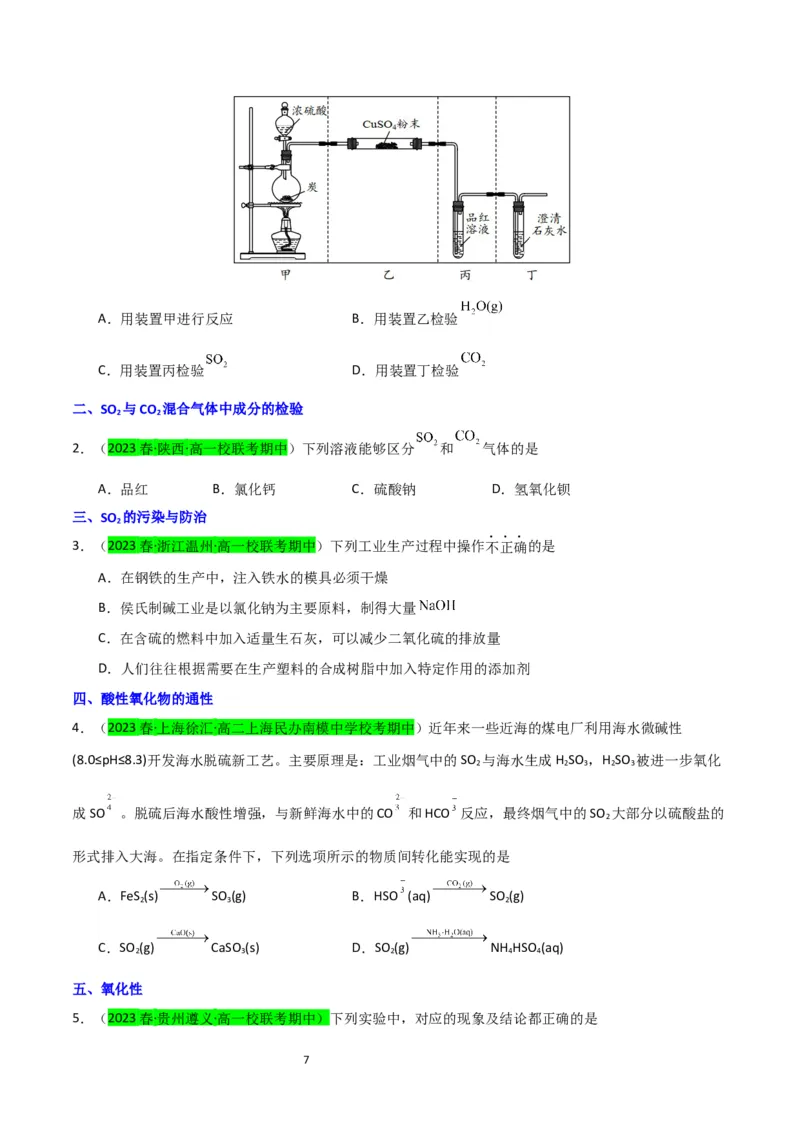
4.(2022·广东·高考真题)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实
验,下列分析正确的是
A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
一、SO 气体的检验
2
1.(2023·江苏·校联考模拟预测)实验室用炭与浓硫酸反应并对产生气体的成分进行检验,下列实验装置
和操作不能达到实验目的的是
6A.用装置甲进行反应 B.用装置乙检验
C.用装置丙检验 D.用装置丁检验
二、SO 与CO 混合气体中成分的检验
2 2
2.(2023春·陕西·高一校联考期中)下列溶液能够区分 和 气体的是
A.品红 B.氯化钙 C.硫酸钠 D.氢氧化钡
三、SO 的污染与防治
2
3.(2023春·浙江温州·高一校联考期中)下列工业生产过程中操作不正确的是
A.在钢铁的生产中,注入铁水的模具必须干燥
B.侯氏制碱工业是以氯化钠为主要原料,制得大量
C.在含硫的燃料中加入适量生石灰,可以减少二氧化硫的排放量
D.人们往往根据需要在生产塑料的合成树脂中加入特定作用的添加剂
四、酸性氧化物的通性
4.(2023春·上海徐汇·高二上海民办南模中学校考期中)近年来一些近海的煤电厂利用海水微碱性
(8.0≤pH≤8.3)开发海水脱硫新工艺。主要原理是:工业烟气中的SO 与海水生成H SO ,H SO 被进一步氧化
2 2 3 2 3
成SO 。脱硫后海水酸性增强,与新鲜海水中的CO 和HCO 反应,最终烟气中的SO 大部分以硫酸盐的
2
形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
A.FeS (s) SO (g) B.HSO (aq) SO (g)
2 3 2
C.SO (g) CaSO (s) D.SO (g) NH HSO (aq)
2 3 2 4 4
五、氧化性
5.(2023春·贵州遵义·高一校联考期中)下列实验中,对应的现象及结论都正确的是
7选
实验步骤 现象 结论
项
向 和 的混合溶液中通入过 溶液变为浅绿色且有白色沉淀
A 沉淀为
量 生成
碘易溶于 ,难溶于
B 向 溶液中加入 ,振荡后静置 液体分层,下层呈紫红色
水
C 向溴水中通入过量 溶液变为无色 具有漂白性
D 将 通入氢硫酸( )溶液中 有黄色沉淀产生 具有还原性
A.A B.B C.C D.D
六、还原性
6.(2023春·湖南长沙·高一统考学业考试)已知 能使酸性 褪色,此反应中体现了 的性质是
A.氧化性 B.还原性 C.酸性氧化物 D.漂白性
七、漂白性
7.(2023春·辽宁鞍山·高一校联考期中) 通入下列溶液中,溶液褪色或变浅,说明 具有漂白作用
的组合是
① ( ,aq) ②溴水 ③碘水 ④氯水 ⑤品红
A.①⑤ B.②③ C.全部 D.⑤
八、二氧化硫的毒性
8.(2022春·湖北·高一统考期末)SO 是一种可添加在葡萄酒、果酒、干菜、果脯、白砂糖等食品中的添
2
加剂,食品中添加适量SO 的作用不正确的是
2
A.增酸味 B.杀菌 C.抗氧化 D.去色
九、SO 与CO 混合气体中成分的检验
2 2
9.(2023春·广东深圳·高一校考阶段练习)下列溶液中:①澄清的石灰水、②H S溶液、③KMnO 溶液、
2 4
④溴水、⑤酸化的Ba(NO ) 溶液、⑥品红溶液,不能用于区别SO 和CO 气体的是
3 2 2 2
A.只有① B.①③ C.①②③⑤ D.②③④⑤
十、二氧化硫性质综合考查
10.(2023春·江西赣州·高一江西省石城中学校考阶段练习)探究 的性质,进行如下实验。
8编号 实验装置 试剂a 实验现象
① 品红溶液 溶液褪色
② 溶液 溶液变浑浊
③ 溶液 白色沉淀
④ 溶液 有气泡
由上述实验所得 的性质及对应的解释不正确的是
A.实验①表明 具有漂白性,实验②表明 具有氧化性
B. 通入紫色石蕊试液先变红后褪色
C.实验③产生的白色沉淀难溶于盐酸
D.实验④通入足量 发生反应的离子方程式为:
1.(2023·湖南株洲·高一炎陵县第一中学校考学业考试)下列对 的性质描述不正确的是
A.无色、有刺激性气味的气体 B.和水反应生成亚硫酸
C.能使溴水褪色,体现漂白性 D.具有还原性,能被氧气氧化
2.(2022·全国·高三校联考阶段练习)某同学在实验室中对 的制备和性质进行探究,下列说法正确的
是
A.实验室中可用装置a制备
9B.装置b可用于检验 的漂白性
C.装置c可用于收集 ,此时应从f口进气
D.装置d可用于吸收 ,其中倒置的漏斗可以防倒吸
3.(2022春·上海黄浦·高三上海市敬业中学校考阶段练习)室温下,1体积的水能溶解约40体积的SO 。
2
用试管收集SO 后进行如下图实验。对实验现象分析与推测正确的是
2
A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C.取出试管中溶液,在空气中放置一段时间后溶液pH减小
D.取出试管中的溶液,滴加盐酸酸化的BaCl 溶液产生大量白色沉淀
2
4.(2023春·陕西西安·高一统考阶段练习)食品添加剂是指为改善食品的色、香、味,以及对食品进行防
腐和加工而加入食品中的化学合成或天然物质。下列关于SO 的说法正确的是
2
A.SO 具有还原性,不能用浓硫酸干燥
2
B.SO 是一种无色无味的有毒气体
2
C.SO 可以使酸性KMnO 溶液褪色,体现了它的漂白性
2 4
D.SO 具有还原性,少量的SO 可防止葡萄酒氧化变质
2 2
5.(2023春·陕西西安·高一西安市第八十五中学校考阶段练习)设N 为阿伏加德罗常数的值,下列说法
A
正确的是
A.lmol SO 与足量的O 反应,产生的SO 数目为 N
2 2 3 A
B.某浓硝酸中n(HNO )= 2mol,该浓硝酸与足量的铜完全反应可生成1molNO
3 2
C.lmolFe 与S完全反应,转移电子数为2N
A
D.标准状况下,11.2L 的SO 中含有的分子数为0.5N
3 A
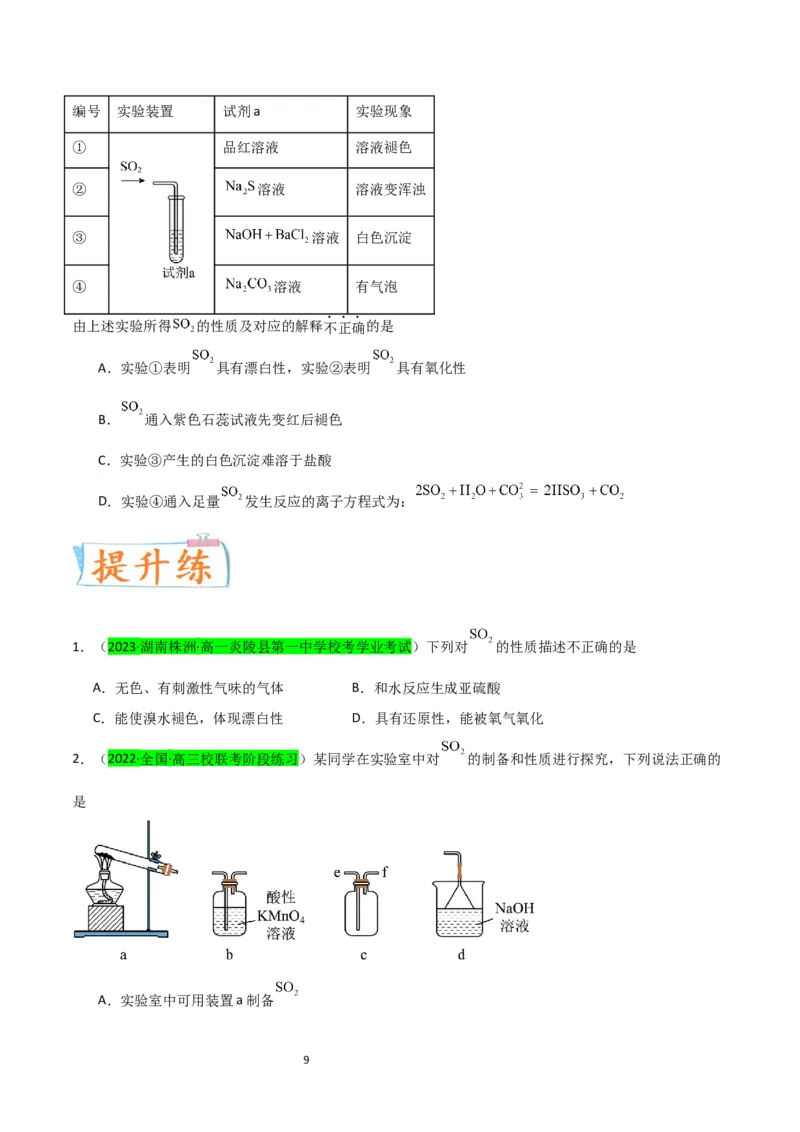
6.(2023春·河南洛阳·高一统考期中)一种以黄铁矿(主要成分是 ,设杂质均不参与反应)为原料生产
硫酸的简要流程图如图:
10下列说法不正确的是
A.黄铁矿“煅烧”时反应的化学方程式为
B.依据上述流程,当最终生成0.1 mol 时,理论上共转移0.75 mol电子
C.标准状况下,22.4 L 中含有的原子总数为
D.“吸收”时若用水吸收三氧化硫会有酸雾产生
7.(2023春·上海浦东新·高一上海市进才中学校考阶段练习)将SO 通入BaCl 溶液中至饱和,未见沉淀生
2 2
成,继续通入或加入适量某一物质后,仍无沉淀,则该物质可能是
A.CO B.Cl C.NaOH D.H S
2 2 2
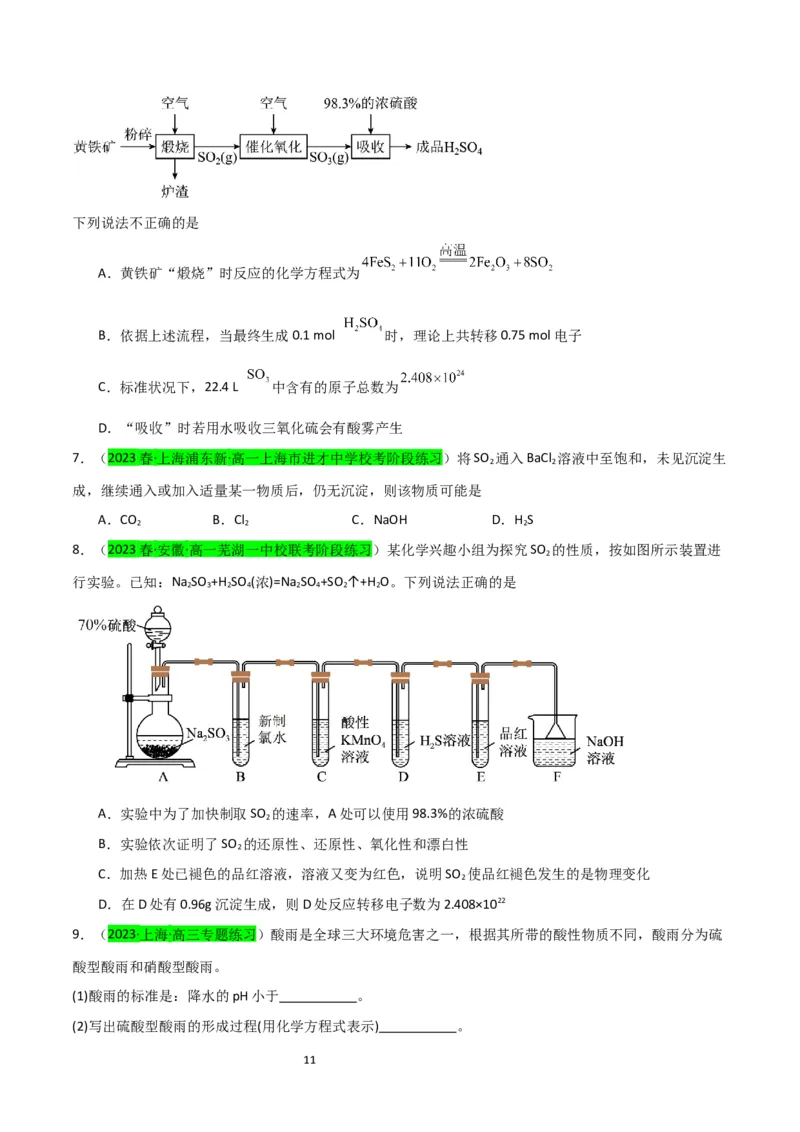
8.(2023春·安徽·高一芜湖一中校联考阶段练习)某化学兴趣小组为探究SO 的性质,按如图所示装置进
2
行实验。已知:Na SO +H SO (浓)=Na SO +SO ↑+H O。下列说法正确的是
2 3 2 4 2 4 2 2
A.实验中为了加快制取SO 的速率,A处可以使用98.3%的浓硫酸
2
B.实验依次证明了SO 的还原性、还原性、氧化性和漂白性
2
C.加热E处已褪色的品红溶液,溶液又变为红色,说明SO 使品红褪色发生的是物理变化
2
D.在D处有0.96g沉淀生成,则D处反应转移电子数为2.408×1022
9.(2023·上海·高三专题练习)酸雨是全球三大环境危害之一,根据其所带的酸性物质不同,酸雨分为硫
酸型酸雨和硝酸型酸雨。
(1)酸雨的标准是:降水的pH小于 。
(2)写出硫酸型酸雨的形成过程(用化学方程式表示) 。
11(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:
①写出装置C中反应的离子方程式 。
②该流程中可以循环利用的物质是 (填写化学式)。
(4)还有学者提出利用 、 等离子的催化作用,常温下将 氧化成 而实现 的回收利用。某
研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成 的转化率。
①该小组采用下图装置在实验室测定模拟烟气中 的体积分数,X溶液可以是 (选填字母)。
a.碘的淀粉溶液 b.酸性高锰酸钾溶液 c.氢氧化钠溶液 d.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中 氧化成 的转化率。已知气体流速,还需测
定的数据有 、 。
10.(2023·河南开封·统考二模)某小组根据硫元素的化合价,预测SO 既有还原性又有氧化性,并设计实
2
验进行探究。
I.探究SO 的还原性:向试管中通入足量SO (尾气处理装置已略) ,记录如下。
2 2
装置 编号 试剂 实验现象
12a 碘水 溶液的棕黄色褪去
b Fe (SO ) 溶液
2 4 3
(1)a中反应的离子方程式为 。
(2)b中的实验现象为 。将b所得溶液分成三份,进行如下实验。
实验①向第一份溶液中加入K [Fe(CN) ]溶液,产生蓝色沉淀。
3 6
实验②向第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
实验③向第三份溶液中先加入稀盐酸酸化,再加入BaCl 溶液,产生白色沉淀。
2
上述实验不能证明SO 与Fe3+发生了氧化还原反应的是 ,原因是 。
2
II.探究SO 的氧化性:向试管中通入足量SO (尾气处理装置已略) ,记录如下。
2 2
装置 编号 试剂 实验现象
c 3mol·L-1稀硫酸 始终无明显变化
d 3 mol·L-1稀盐酸 铜片表面变黑,溶液变为棕色
已知:i.水合Cu+既易被氧化也易被还原,因此水溶液中无法生成水合Cu+。
ii.CuCl为白色固体,难溶于水,可溶于c(Cl-)较大的溶液生成[CuCl ]2-。
3
(3)证明d所得棕色溶液含有[CuCl ]2- :用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡
3
移动原理解释产生该现象的原因是 。
(4)与c对比,d能发生反应的原因是 。
(5)由实验II可推知,该条件下SO 、CuCl、Cu2+的氧化性由强到弱的顺序为 。
2
13