文档内容
大题优练 8 以电解质溶液为主线串联反应原理
优 选 例 题
例:2020年六盘水市荣获第六届全国文明城市称号,保护生态环境、建设生态文明是文明城市重要的评价指
标。工业三废的处理与利用对环境保护意义重大。
Ⅰ.燃煤烟气中含有大量的SO ,工业上常用NaSO 溶液脱除烟气中的SO 。
2 2 3 2
(1)Na SO 溶液显碱性的原因_______________________________。(用离子方程式表示)
2 3
(2)0.1mol/L Na SO 溶液中离子浓度关系正确的是_______。(选填序号)
2 3
a.c(Na+)=c(SO)+c(HSO)+c(H SO ) b.c(Na+)>c(SO)>c(OH−)>c(H+)
2 3
c.c(Na+)+c(H+)=2c(SO)+c(HSO)+c(OH−) d.c(OH−)=c(HSO)+c(H SO )+c(H+)
2 3
(3)Na SO 溶液脱除烟气中SO 的离子方程式为___________________________。
2 3 2
Ⅱ.硫酸工业废气中的SO 常用于处理酸性含铬废水中的Cr O。
2 2
(1)SO 将Cr O还原为Cr3+,还原剂与氧化剂物质的量之比为_______。
2 2
(2)当Cr O转化为Cr3+后,调节pH可使Cr3+转化为Cr(OH) 沉淀除去,常温下调节 pH为8时,废水中
2 3
Cr3+浓度为_______mol/L。(K [Cr(OH) ]=6.3×10−31)
sp 3
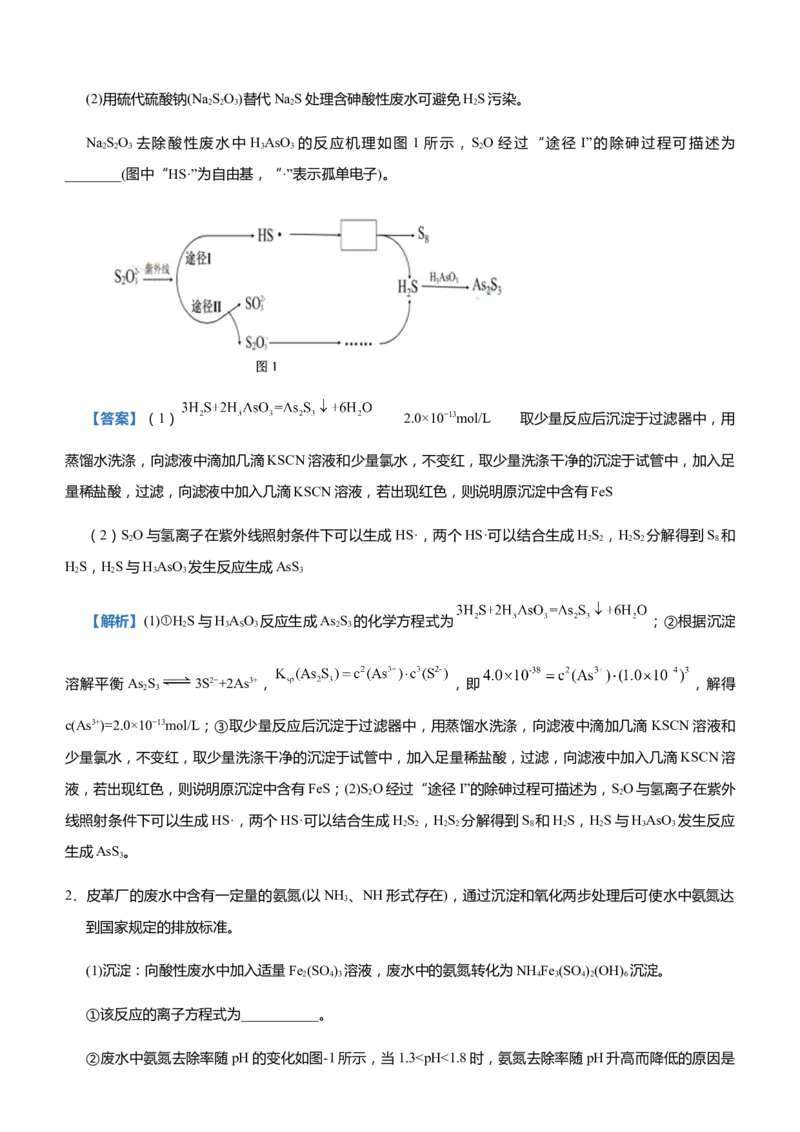
Ⅲ.SO 在一定条件下与氧气构成原电池,利用该电池在铁制品表面镀铜,装置如图所示。
2(1)铁制品为_______极。(填“c”或“d”)
(2)a极电极反应式为_____________________。
【答案】Ⅰ.(1)SO+H O=HSO+OH−
2
(2)bc
(3)SO+SO +H O=2HSO
2 2
Ⅱ.(1)3∶1
(2)6.3×10−13
Ⅲ.(1)c
(2)O+4e−+4H+=H O
2 2
【解析】(1)Na SO 中SO水解生成HSO和OH−,导致溶液显碱性,离子方程式为SO+H O=HSO+OH−;
2 3 2
(2)a.根据物料守恒,则c(Na+)=2c(SO)+2c(HSO)+2c(H SO ),a关系错误;b.NaSO 溶液则c(Na+)>c(SO),
2 3 2 3
少量的SO水解,溶液呈碱性,则c(OH−)>c(H+),c(Na+)>c(SO)>c(OH−)>c(H+),b关系正确;c.根据溶液
呈电中性,c(Na+)+c(H+)=2c(SO)+c(HSO)+c(OH−),c 关系正确;d.根据质子守恒,则 c(OH−)= c(HSO)
+2c(H SO )+c(H+),d 关系错误;答案为 bc;(3)Na SO 溶液与 SO 反应生成亚硫酸氢钠,离子方程式为
2 3 2 3 2
SO+SO +H O=2HSO;Ⅱ.(1)SO 将Cr O还原为Cr3+,S的化合价由+4价变为+6价,SO 为还原剂,而Cr由
2 2 2 2 2
+6价变为+3价,则还原剂与氧化剂物质的量之比为3∶1;(2)K [Cr(OH) ]=c(Cr3+)×c3(OH−),pH为8时,
sp 3
c(OH−)=10−6,则c(Cr3+)=6.3×10−31÷c3(OH−)=6.3×10−13mol/L;Ⅲ.(1)左池为原电池,b极失电子,作负极,目
的为在铁制品表面镀铜,则铜作阳极,与a极相连,铁制品做阴极,与b极相连,为c极;(2)a极作正极,氧
气得电子,与氢离子反应生成水,电极反应式为O+4e−+4H+=H O。
2 2模 拟 优 练
1.酸性废水中的砷元素主要以亚砷酸(H AsO )形式存在。已知As S 难溶于水,也不溶于稀硫酸、稀盐酸等
3 3 2 3
无机酸。
(1)工业上采用硫化法(通常用NaS)去除废水中的砷。
2
①向酸性废水中加入NaS,产生的HS与HA O 反应生成As S 的化学方程式为_______。
2 2 3 S 3 2 3
②沉淀后,若废水中c(S2−)=1.0×10−4mol·L−1,则c(As3+)=_______。[K (As S)=4.0×10−38]
sp 2 3
③为了防止As S 与过量的S2−形成络合离子而溶解,通常需添加适量的 FeSO 溶液,形成FeS,与As S
2 3 4 2 3
共沉淀。验证沉淀中含有FeS的实验方法是_______。(2)用硫代硫酸钠(Na SO)替代NaS处理含砷酸性废水可避免HS污染。
2 2 3 2 2
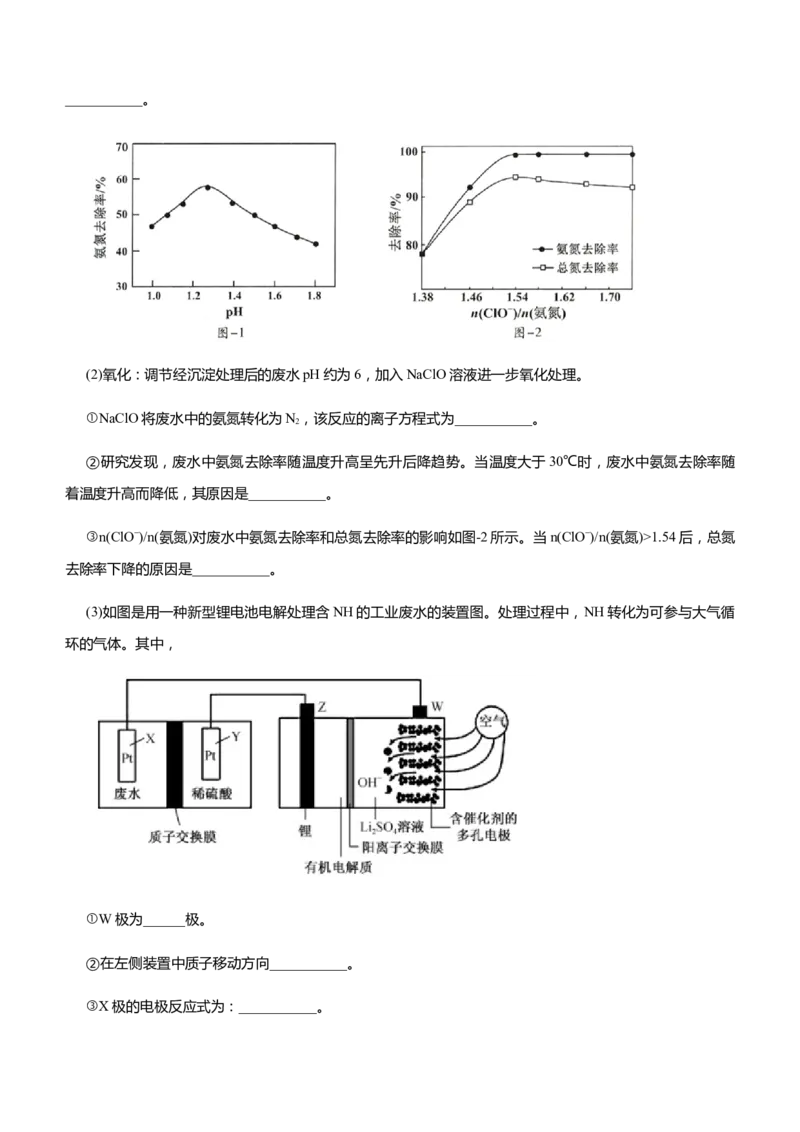
NaSO 去除酸性废水中 HAsO 的反应机理如图 1 所示,SO 经过“途径 I”的除砷过程可描述为
2 2 3 3 3 2
________(图中“HS·”为自由基,“·”表示孤单电子)。
【答案】(1) 2.0×10−13mol/L 取少量反应后沉淀于过滤器中,用
蒸馏水洗涤,向滤液中滴加几滴KSCN溶液和少量氯水,不变红,取少量洗涤干净的沉淀于试管中,加入足
量稀盐酸,过滤,向滤液中加入几滴KSCN溶液,若出现红色,则说明原沉淀中含有FeS
(2)SO与氢离子在紫外线照射条件下可以生成HS·,两个HS·可以结合生成HS ,HS 分解得到S 和
2 2 2 2 2 8
HS,HS与HAsO 发生反应生成AsS
2 2 3 3 3
【解析】(1)①HS与HA O 反应生成As S 的化学方程式为 ;②根据沉淀
2 3 S 3 2 3
溶解平衡As S 3S2−+2As3+, ,即 ,解得
2 3
c(As3+)=2.0×10−13mol/L;③取少量反应后沉淀于过滤器中,用蒸馏水洗涤,向滤液中滴加几滴 KSCN溶液和
少量氯水,不变红,取少量洗涤干净的沉淀于试管中,加入足量稀盐酸,过滤,向滤液中加入几滴KSCN溶
液,若出现红色,则说明原沉淀中含有FeS;(2)S O经过“途径I”的除砷过程可描述为,SO与氢离子在紫外
2 2
线照射条件下可以生成HS·,两个HS·可以结合生成HS ,HS 分解得到S 和HS,HS与HAsO 发生反应
2 2 2 2 8 2 2 3 3
生成AsS 。
3
2.皮革厂的废水中含有一定量的氨氮(以NH 、NH形式存在),通过沉淀和氧化两步处理后可使水中氨氮达
3
到国家规定的排放标准。
(1)沉淀:向酸性废水中加入适量Fe (SO ) 溶液,废水中的氨氮转化为NH Fe (SO )(OH) 沉淀。
2 4 3 4 3 4 2 6
①该反应的离子方程式为___________。
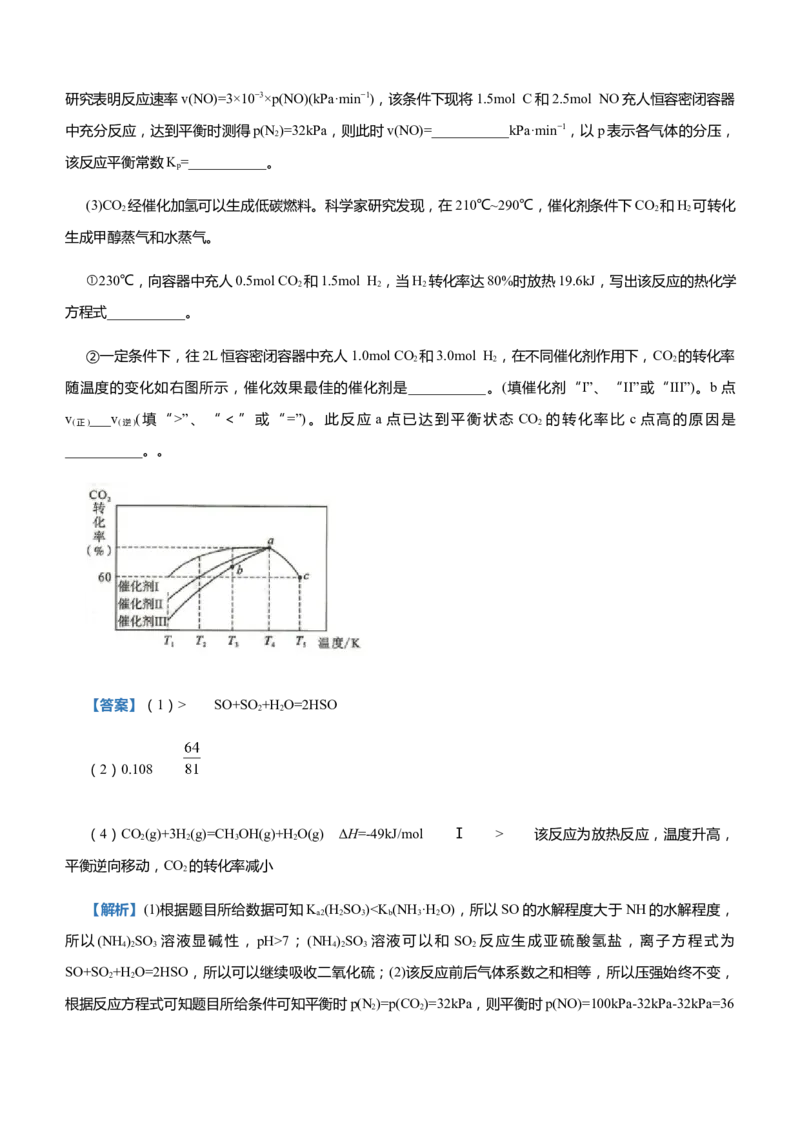
②废水中氨氮去除率随pH的变化如图-1所示,当1.31.54后,总氮
去除率下降的原因是___________。
(3)如图是用一种新型锂电池电解处理含NH的工业废水的装置图。处理过程中,NH转化为可参与大气循
环的气体。其中,
①W极为______极。
②在左侧装置中质子移动方向___________。
③X极的电极反应式为:___________。【答案】(1)3Fe3++2SO+NH+6H O=NH Fe (SO )(OH) +6H+ Fe3+发生水解造成溶液中该离子浓度降
2 4 3 4 2 6
低,生成的沉淀量减小,所以氨氮去除率下降
(2)3ClO−+2NH=N↑+3Cl−+2H++3H O 由于水解反应为吸热反应,所以当温度升高时,溶液中的铵根
2 2
离子和铁离子均倾向于水解,无法形成沉淀,氨氮去除率降低 污水中部分氨氮氧化为其它价态例如硝酸根
离子,则总氮去除率下降
(3)正 从X到Y 2NH-6e−=N ↑+8H+
2
【解析】由已知信息和装置图可知,右边为锂电池,为原电池,左边为电解池,Z为负极,电极反应式为
Li-e−=Li+,W为正极,电极反应式为O+4e−+2H O=4OH−,Y为阴极,电极反应式为2HO+2e−=H ↑+2OH−,X
2 2 2 2
为阳极,电极反应式2NH-6e−=N ↑+8H+。(1)①铁离子与硫酸根、铵根、水分子反应生成沉淀,离子方程式
2
为3Fe3++2SO+NH+6H O=NH Fe (SO )(OH) +6H+;②pH升高时,Fe3+发生水解造成溶液中该离子浓度降低,
2 4 3 4 2 6
生成的沉淀量减小,所以氨氮去除率下降;(2)①次氯酸跟离子与铵根离子发生氧化还原反应生成氮气和氯离
子,Cl元素由+1价下降到-1价,N元素由-3价上升到0价,根据得失电子守恒和原子守恒配平反应的离子方
程式为3ClO−+2NH=N↑+3Cl−+2H++3H O;②水解反应为吸热反应,当温度升高时,有利于溶液中各离子的水
2 2
解,所以溶液中的铵根离子和铁离子均倾向于水解,无法形成沉淀,氨氮去除率降低;③当 后,
次氯酸钠投加量过大,导致污水中部分氨氮氧化为其它价态例如硝酸根离子,则总氮去除率下降;(3)①由分
析可知,右边为锂电池,为原电池,左边为电解池,Z为负极,电极反应式为Li-e−=Li+,W为正极,故答案
为:正;②左边为电解池,Y为阴极,X为阳极,阳离子从阳极移向阴极,则左侧装置中质子移动方向为从
X到Y,故答案为:从X到Y;③右边为锂电池,为原电池,左边为电解池,Y为阴极,电极反应式为
2HO+2e−=H ↑+2OH−,X为阳极,电极反应式2NH-6e−=N ↑+8H+,故答案为:2NH-6e−=N ↑+8H+。
2 2 2 2
3.燃煤废气中的氮氧化物(NO )、CO、SO 等气体常用下列方法处理,以实现节能减排、废物利用。
x 2 2
(1)处理烟气中的SO 常用液吸法。室温下,将烟气通人浓氨水中得到(NH )SO 溶液,0.1mol/L (NH )SO
2 4 2 3 4 2 3
溶液的pH_____(填“>”、“<”或“=”)7。将烟气通人(NH )SO 溶液可以继续吸收SO ,用离子方程式表示
4 2 3 2
出能继续吸收二氧化硫的原因___________。(已知:25℃时,K(NH ·H O)=1.8×10−5;HSO :K =1.5×10−2,
b 3 2 2 3 a1
K =1.0×10−7)
a2
(2)处理烟气中氮氧化物常用活性炭还原法,反应为:C(s)+2NO(g)→N (g)+CO (g)。在T℃、100kPa时,
2 2研究表明反应速率v(NO)=3×10−3×p(NO)(kPa·min−1),该条件下现将1.5mol C和2.5mol NO充人恒容密闭容器
中充分反应,达到平衡时测得p(N )=32kPa,则此时v(NO)=___________kPa·min−1,以p表示各气体的分压,
2
该反应平衡常数K=___________。
p
(3)CO 经催化加氢可以生成低碳燃料。科学家研究发现,在210℃~290℃,催化剂条件下CO 和H 可转化
2 2 2
生成甲醇蒸气和水蒸气。
①230℃,向容器中充人0.5mol CO 和1.5mol H,当H 转化率达80%时放热19.6kJ,写出该反应的热化学
2 2 2
方程式___________。
②一定条件下,往2L恒容密闭容器中充人1.0mol CO 和3.0mol H,在不同催化剂作用下,CO 的转化率
2 2 2
随温度的变化如右图所示,催化效果最佳的催化剂是___________。(填催化剂“I”、“II”或“III”)。b点
v ___v (填“>”、“<”或“=”)。此反应 a 点已达到平衡状态 CO 的转化率比 c 点高的原因是
(正) (逆) 2
___________。。
【答案】(1)> SO+SO +HO=2HSO
2 2
(2)0.108
(4)CO(g)+3H(g)=CH OH(g)+HO(g) ΔH=-49kJ/mol Ⅰ > 该反应为放热反应,温度升高,
2 2 3 2
平衡逆向移动,CO 的转化率减小
2
【解析】(1)根据题目所给数据可知K (H SO )7;(NH )SO 溶液可以和 SO 反应生成亚硫酸氢盐,离子方程式为
4 2 3 4 2 3 2
SO+SO +HO=2HSO,所以可以继续吸收二氧化硫;(2)该反应前后气体系数之和相等,所以压强始终不变,
2 2
根据反应方程式可知题目所给条件可知平衡时p(N )=p(CO )=32kPa,则平衡时p(NO)=100kPa-32kPa-32kPa=36
2 2kPa,则v(NO)=3×10−3×36kPa=0.108;K = = ;(3)①CO 与H 反应的化学方程式为
p 2 2
CO+3H=CH OH+HO,当 H 转化率达 80%时放热 19.6kJ,即 1.5mol×80%=1.2mol 氢气完全反应时放出
2 2 3 2 2
19.6kJ热量,则3mol氢气完全反应放出 kJ=49kJ热量,热化学方程式为 CO(g)+3H(g)=CH OH(g)
2 2 3
+HO(g) ΔH=-49kJ/mol;②据图可知,温度较低时催化剂Ⅰ条件下CO 的转化率最大,即反应速率最快,催
2 2
化效果最好;a点前随温度升高CO 转化率增大,a点后随温度升高转化率减小,说明a点前由于温度较低,
2
反应速率较慢,在测定转化率时反应还未达到平衡,即 b点时反应正向移动,正反应速率大于逆反应速率;
该反应为放热反应,温度升高,平衡逆向移动,CO 的转化率减小,所以a点CO 的转化率比c点高。
2 2
4.硒(Se)元素位于元素周期表第四周期第VIA族。请回答下列问题:
I.工业上用精炼铜的阳极泥(硒主要以CuSe形式存在,还含有少量Ag、Au)为原料与浓硫酸混合焙烧,
将产生的SO 、SeO 混合气体用水吸收即可得Se固体。
2 2
(1)写出“混合气体用水吸收”时发生反应的化学方程式______________________。
(2)下列说法正确的是_______(填字母)。
A.SeO 可以氧化HS,但遇到强氧化剂时可能表现还原性
2 2
B.热稳定性:HSe>H S
2 2
C.“焙烧”时的主要反应为:CuSe+4H SO (浓)=====CuSO +SeO ↑+3SO↑+4H O
2 4 4 2 2 2
II.硒及其氢化物HSe在新型光伏太阳能电池和金属硒化物方面有重要应用。
2
(3)已知:①HSe(g)+1/2O (g) Se(s)+H O(l) ΔH=m kJ·mol−1
2 2 2 1
②2H (g)+O(g)=2HO(g) ΔH=n kJ·mol−1
2 2 2 2
③HO(g)=H O(l) ΔH=p kJ·mol−1
2 2 3
反应H(g)+Se(s) HSe(g)的反应热ΔH=_______kJ·mol−1(用含m、n、p的代数式表示)。
2 2
(4)已知常温HSe的电离平衡常数K=1.3×10−4,K=5.0×10−11,则NaHSe溶液的离子浓度由大到小的顺
2 1 2
序为_________________。Ag SO 在一定条件下可以制备 Ag SeO 已知该条件下 Ag SeO 的K =5.7×10−8,
2 4 2 4 2 4 sp
Ag SO 的的K =1.4×10−5,则反应Ag SO (s)+SeO(aq) Ag SeO(s)+SO(aq)的化学平衡常数K=_______(保留
2 4 sp 2 4 2 4两位有效数字)。
III.研究含硒工业废水的处理工艺,对控制水体中硒超标具有重要意义。
(5)用惰性电极电解弱电解质亚硒酸(H SeO)溶液可制得强酸HSeO ,电解过程中阳极生成2mol产物时,
2 3 2 4
阴极析出标准状态下的气体_______L。
(6)木炭包覆纳米零价铁除硒法是一种改良的含硒废水处理方法。制备纳米零价铁时,以木炭和
FeCl ·6H O为原料,在N 氛围中迅速升温至600℃,保持2小时,该过程中木炭的作用有吸附和_______。木
3 2 2
炭包覆纳米零价铁在碱性含硒废水中形成许多微电池,加速SeO的还原过程。已知SeO转化为单质Se,写出
其对应的电极反应式_____________________。
【答案】(1)SeO+2SO+2H O=Se↓+2H SO
2 2 2 2 4
(2)AC
(3)p-m+
(4)c(Na+)>c(HSe−)>c(OH−)>c(H+)>c(Se2−) 2.5×102
(5)44.8L
(6)将三价铁还原为零价铁/作还原剂 SeO+4e−+3H O=Se+6OH−
2
【解析】(1)混合气体为SO 、SeO 和水反应生成Se固体,Se元素由+4价下降到0价,S元素由+4价
2 2
要上升到+6价,根据得失电子守恒和原子守恒配平方程式为:SeO+2SO+2H O=Se↓+2H SO ;A.硒(Se)元
2 2 2 2 4
素位于元素周期表第四周期第VIA族,Se的性质与S相似,因SO 遇强氧化剂时可能表现还原性,所以SeO
2 2
可以氧化HS,但遇到强氧化剂时可能表现还原性,故A正确;B.硒(Se)元素位于元素周期表第四周期第
2
VIA族,非金属性S>Se,则热稳定性:HSec(HSe−)>c(OH−)>
c(H+)>c(Se2−);已知Ag SeO(s) 2Ag+(aq)+SeO(aq) K =c2(Ag+)×c(SeO)=5.7×10−8,Ag SO (s) 2
2 4 sp1 2 4
Ag+(aq)+SO(aq) K =c2(Ag+)×c(SO)=1.4×10−5,则反应Ag SO (s)+SeO(aq) Ag SeO(s)+SO(aq)的化学平衡
sp2 2 4 2 4
常数K= = = =2.5×102;故答案为:c(Na+)>c(HSe−)>c(OH−)>c(H+)>c(Se2−);2.5×102;(5)
用惰性电极电解弱电解质亚硒酸(H SeO)溶液可制得强酸HSeO,该电解方程式为:HSeO+H O=HSeO+
2 3 2 4 2 3 2 2 4
H↑,电解过程中阳极生成2mol HSeO 时转移2 2mol=4mol电子,则阴极产生2mol氢气,标准状态下的体
2 2 4
积为44.8L,故答案为:44.8L;(6)由题干信息可知,该过程中木炭的作用有吸附和还原剂,将三价铁还原为
零价铁;已知SeO转化为单质Se,Se元素由+4价下降到0价,得到4个电子,结合电荷守恒和原子守恒配
平电极方程式为:SeO+4e−+3H O=Se+6OH−,故答案为:将三价铁还原为零价铁/作还原剂;SeO+4e−+3H O
2 2
=Se+6OH−。
5.国家规定,排放的废水中氟的含量不得超过 ,砷的含量不得超过 。硫酸工厂废水
中除含有稀硫酸外,还含有HAsO 、HSiF 等物质。工业上常通过化学沉淀和氧化、吸附沉降处理废水,
3 3 2 6
实现水体达标排放。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH) 为主]、过滤。滤渣中主要含有CaSO 、CaF 、SiO 和少量
2 4 2 2
Ca (AsO)。
3 3 2
①Ca (AsO) 中阴离子的空间构型为_______。
3 3 2
②写出该过程中HSiF 和石灰乳反应生成CaF 、SiO 的化学方程式:_______。
2 6 2 2③充分沉淀后测得废水中 的含量为 ,此时 SO 的浓度为_______mol·L−1。[已知:
、 ]
(2)氧化、吸附沉降:利用NaClO和FeSO 进一步处理废水中残余的As(III)。
4
已知:i.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH) 胶体吸附废水中的As(V)
3
物种而沉降。
ii.溶液的pH对Fe(OH) 胶体表面所带电荷有影响。pH>7时,Fe(OH) 胶体表面带负电荷,pH越高,表
3 3
面所带负电荷越多。
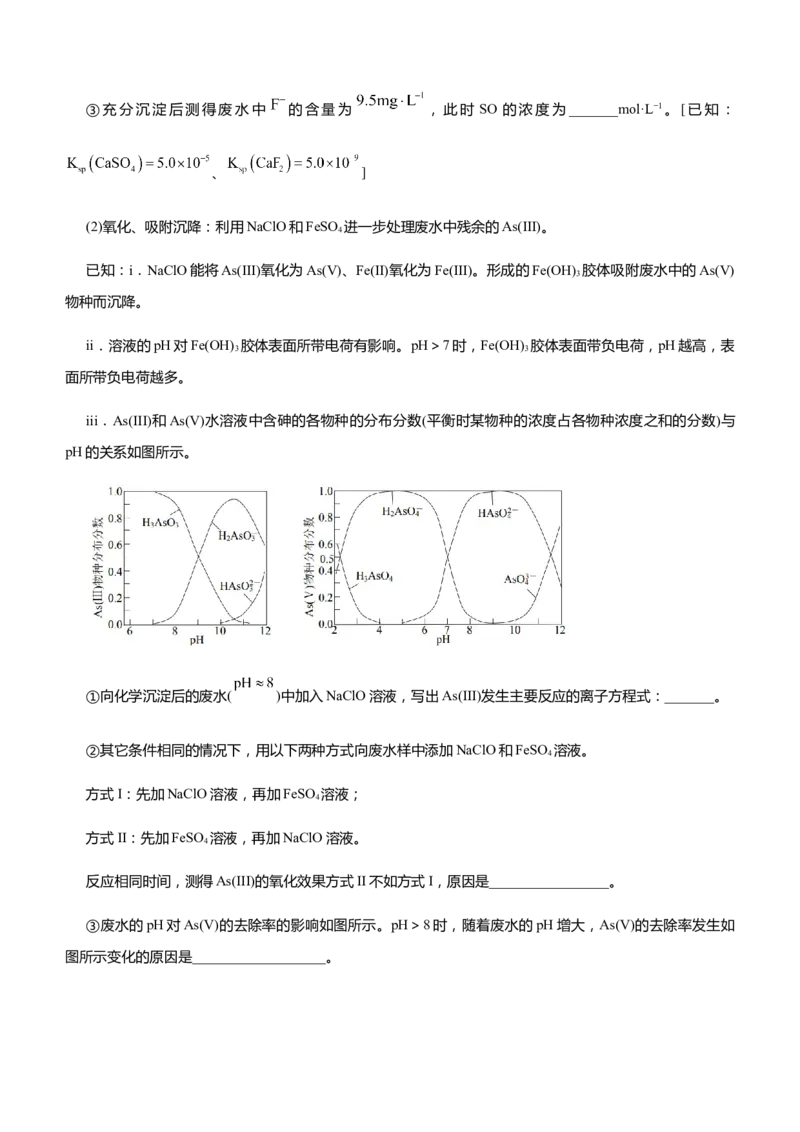
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与
pH的关系如图所示。
①向化学沉淀后的废水( )中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:_______。
②其它条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO 溶液。
4
方式I:先加NaClO溶液,再加FeSO 溶液;
4
方式II:先加FeSO 溶液,再加NaClO溶液。
4
反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是_________________。
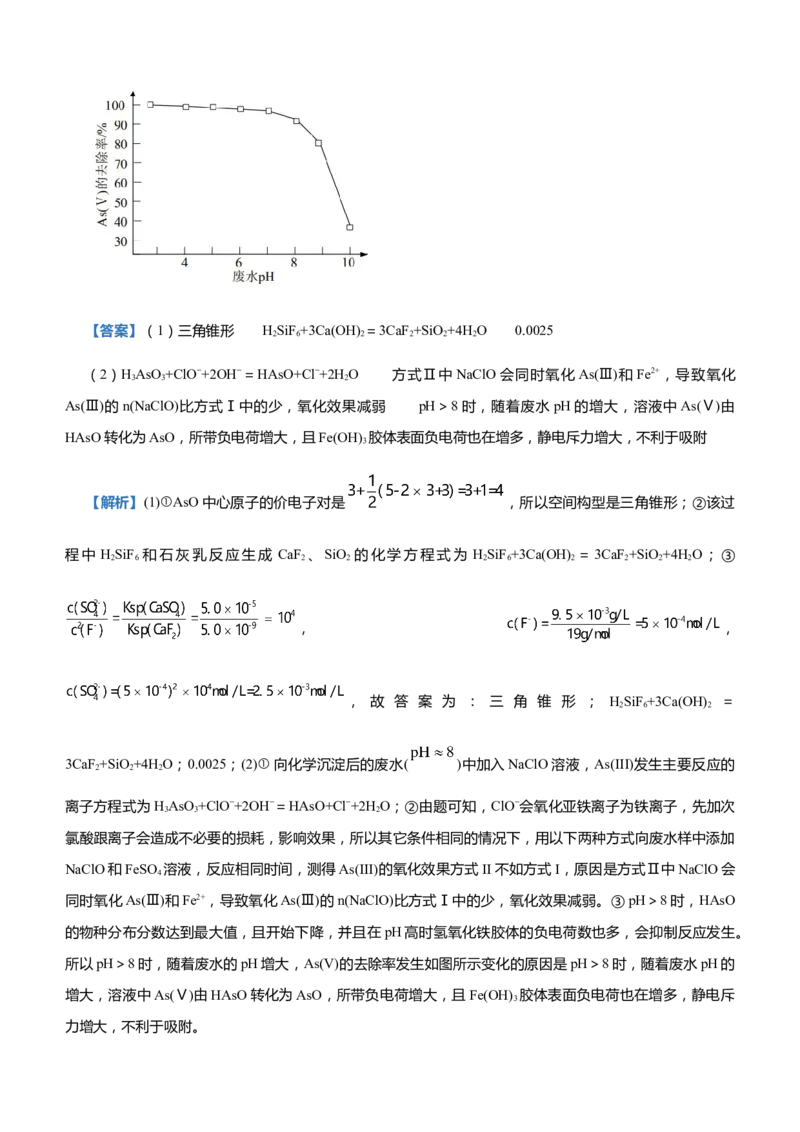
③废水的pH对As(V)的去除率的影响如图所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如
图所示变化的原因是___________________。【答案】(1)三角锥形 HSiF+3Ca(OH) =3CaF +SiO +4H O 0.0025
2 6 2 2 2 2
(2)HAsO +ClO−+2OH−=HAsO+Cl−+2HO 方式Ⅱ中NaClO会同时氧化As(Ⅲ)和Fe2+,导致氧化
3 3 2
As(Ⅲ)的n(NaClO)比方式Ⅰ中的少,氧化效果减弱 pH>8时,随着废水pH的增大,溶液中As(Ⅴ)由
HAsO转化为AsO,所带负电荷增大,且Fe(OH) 胶体表面负电荷也在增多,静电斥力增大,不利于吸附
3
【解析】(1)①AsO中心原子的价电子对是 ,所以空间构型是三角锥形;②该过
程中 HSiF 和石灰乳反应生成 CaF 、SiO 的化学方程式为 HSiF+3Ca(OH) =3CaF +SiO +4H O;③
2 6 2 2 2 6 2 2 2 2
, ,
, 故 答 案 为 : 三 角 锥 形 ; HSiF+3Ca(OH) =
2 6 2
3CaF +SiO +4H O;0.0025;(2)①向化学沉淀后的废水( )中加入NaClO溶液,As(III)发生主要反应的
2 2 2
离子方程式为HAsO +ClO−+2OH−=HAsO+Cl−+2HO;②由题可知,ClO−会氧化亚铁离子为铁离子,先加次
3 3 2
氯酸跟离子会造成不必要的损耗,影响效果,所以其它条件相同的情况下,用以下两种方式向废水样中添加
NaClO和FeSO 溶液,反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是方式Ⅱ中NaClO会
4
同时氧化As(Ⅲ)和Fe2+,导致氧化As(Ⅲ)的n(NaClO)比方式Ⅰ中的少,氧化效果减弱。③pH>8时,HAsO
的物种分布分数达到最大值,且开始下降,并且在pH高时氢氧化铁胶体的负电荷数也多,会抑制反应发生。
所以pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是pH>8时,随着废水pH的
增大,溶液中As(Ⅴ)由HAsO转化为AsO,所带负电荷增大,且Fe(OH) 胶体表面负电荷也在增多,静电斥
3
力增大,不利于吸附。